Лекарство от столбняка как средство от рака
Обновлено: 23.04.2024
Экстренная профилактика столбняка
Экстренная профилактика столбняка начинается с первичной хирургической обработки раны и одновременной специфической иммунопрофилактики. Экстренную иммунопрофилактику столбняка нужно провести как можно раньше и аж до 20 дня с момента получения травмы, учитывая длительность инкубационного периода при заболевании столбняком.
Экстренную профилактику столбняка проводят при:
-
и ожогах (химических, термических, радиационных) 2-й, третьей и четвертой степени;
- травмах, при которых было нарушение целостности кожных покровов и слизистых оболочек; , сделанных вне больничных учреждений;
- проникающих повреждениях ЖКТ;
- гангрене или некрозе тканей любого типа, длительно текущих карбункулах, абсцессах;
- родах вне медицинских учреждений (например, в домашних условиях);
- укусах животными.
Примечание
Вместо 0,5 мл адсорбированного столбнячного анатоксина можно применять АДС-М, если необходима вакцинация против дифтерии этим средством. Если локализация раны позволяет, АС предпочтительно вводить в область ее расположения путем подкожного обкалывания.
Применять один из указанных препаратов: ПСЧИ или ПСС (предпочтительнее вводить ПСЧИ).
При "инфицированных" ранах вводят 0,5 мл АС, если после последней ревакцинации прошло 5 и более лет.
Полный курс иммунизации АС для взрослых состоит из двух прививок по 0,5 мл каждая с интервалом 30-40 дней и ревакцинации через 6-12 мес. той же дозой. По сокращенной схеме полный курс иммунизации включает однократную вакцинацию АС в удвоенной дозе (1 мл) и ревакцинацию через 1-2 года дозой 0,5 мл АС.
Две прививки по обычной схеме иммунизации (для взрослых и детей) или одна прививка по сокращенной схеме иммунизации для взрослых.
При "инфицированных" ранах вводят ПСЧИ или ПСС.
Все люди, которым сделали активно-пассивную профилактику, для завершения курса иммунизации через 6 мес. - 2 года должны быть еще раз вакцинированы АС в объеме 0,5 мл.
После нормализации посттравматического состояния детей нужно привить АКДС-вакциной.
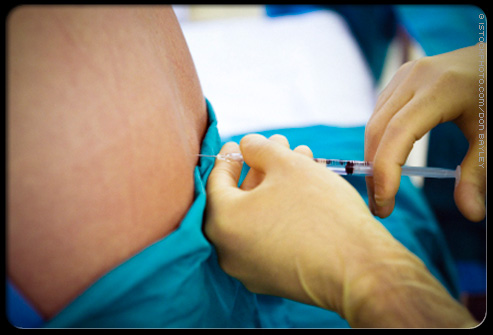
Препараты для экстренной иммунопрофилактики столбняка
- Адсорбированный дифтерийно-столбнячный анатоксин с уменьшенным содержанием антигенов (АДС-М); (АС);
- Сыворотка противостолбнячная лошади.
Иммунологический контроль при экстренной профилактике столбняка
При отсутствии достоверных сведений о прививках состояние противостолбнячного иммунитета оценивается непосредственно в момент обращения больного по поводу травмы. Схема выбора экстренной профилактики основывается на результатах определения уровня специфического антитоксина в сыворотке крови пациента с травмой либо – на косвенных критериях факта проведения прививки против столбняка (возраст, пол, отсутствие противопоказаний, служба в армии и пр.)
Достаточный для исследования объем крови 0,2 мл – может быть получен из раны или одновременно со взятием крови из пальца для проведения любого клинического анализа. Забор крови осуществляется в капилляр или пробирку, которую оставляют при комнатной температуре или в бытовом холодильнике на 15-20 минут, после чего надосадочную над эритроцитами жидкость (сыворотку) используют для проведения серологических исследований.
При взятии крови из вены используют стандартный способ отделения сыворотки крови. Определение столбнячного антитоксина в сыворотке крови больного осуществляется в РПГА в соответствии с инструкциями по применению диагностикумов. Минимальный титр столбнячного антитоксина, свидетельствующий о проведенной иммунизации, равен 1:20.
Назначение препаратов
Назначение препаратов для экстренной иммунопрофилактики столбняка проводится дифференцированно в зависимости от наличия документального подтверждения о проведении профилактической прививки или данных иммунологического контроля напряженности противостолбнячного иммунитета, а также с учетом характера травмы.
Введение препаратов не проводится
- детям и подросткам, которые имеют документальное подтверждение о проведении плановых профилактических прививок, которые положены им по возрасту, независимо от времени, которое прошло после очередной прививки;
- взрослым людям, имеющим документальное подтверждение о проведенном полном курсе иммунизации не более пяти лет назад;
- людям, имеющим титр столбнячного антитоксина в сыворотке крови выше 1:160 по данным РПГА (согласно данным экстренного иммунологического контроля), что соответствует титру выше 0,1 МЕ/мл по данным биологической peaкции нейтрализации – РН (защитный титр).
Вводят только 0,5 мл АС-анатоксина
- взрослым людям, имеющим документальное подтверждение о проведенном полном курсе иммунизации более 5 лет назад;
- детям и подросткам, имеющим документальное подтверждение о проведении курca плановых профилактических прививок без последней возрастной ревакцинации, независимо от срока последней прививки;
- лицам, имеющим, по данным экстренного иммунологического контроля, титр столбнячного анатоксина в пределах 1:20-1:80 по данным РПГА или в пределах 0,01-0,1 МЕ/мл по данным РН;
- лицам всех возрастов, получившим две прививки не более 5 лет назад, либо одну прививку не более 2 лет назад; детям с 5-месячного возраста, подросткам, военнослужащим срочной службы и отслужившим в армии установленный срок, прививочный анамнез которых не известен, а противопоказаний к проведению прививок не было.
Вместо 0,5 мл АС можно вводить 0,5 мл АДС-М, если необходима иммунизация этим препаратом.
Экстренную профилактику столбняка осуществляют с соблюдением следующих правил:
- перед введением ампулу с препаратом тщательно просматривают. Препарат не подлежит применению в следующих случаях:
- – при отсутствии на этикетке полных сведений о препарате;
– при отсутствии на ампуле этикетки;
– при наличии неразбивающихся хлопьев, осадка или посторонних включений (волокна, пригар и др.);
– при наличии трещин на ампуле;
– в случае неправильного хранения препарата;
– в случае истекшего срока годности лекарственного средства;
- непосредственно перед введением АС ампулу встряхивают до получения гомогенной взвеси;
- при вскрытии ампулу до и после надреза напильником протирают стерильной ватой, смоченной спиртом. Вскрытую ампулу с АС или ПСС можно хранить, накрыв стерильной салфеткой, в течение не более 30 минут;
- препараты набирают в шприц из ампулы длинной иглой с широким просветом. Для инъекции используют обязательно другую иглу;
- кожу на месте укола дезинфицируют 70%-ным спиртом;
- после введения препарата место укола смазывают йодом или спиртом.
Экстренная профилактика путем ревакцинации
АС вводят в количестве 0,5 мл в соответствии с инструкцией к препарату. Если позволяет локализация раны, предпочтительно вводить АС-анатоксин в регион ее расположения путем подкожного обкалывания.
Активно-пассивная профилактика столбняка
АС нужно ввести в объеме 1 мл, перед этим ознакомившись с инструкцией к препарату. Вместе с этим в другой участок тела нужно ввести ПСЧИ 250 ME в/м, при отсутствии ПСЧИ вводят 3000 ME ПСС. Перед введением ПСС обязательно ставят внутрикожную пробу с лошадиной сывороткой, разведенной в пропорции 1:100, для определения чувствительности к белкам сыворотки лошади (ампула маркирована красным цветом). Внутрикожную пробу нельзя ставить, если пострадавшему на протяжении 1-3 суток перед введением ПСС проба была проведена с разведенным 1:100 антирабическим гаммаглобулином из сыворотки лошади в связи с необходимостью введения антирабического гаммаглобулина.
Для постановки пробы нужно применить индивидуальную ампулу, а также стерильные шприцы с делениями на 0,1 мл и тонкую иглу. Разведенную 1:100 сыворотку вводят под кожу в сгибательную поверхность предплечья в колиестве 0,1 мл. Реакцию контролируют спусатя 20 минут. Пробу считают отрицательной, если диаметр отека или покраснения на месте введения менее 1,0 сантиметра.
Проба считается положительной, если отек или покраснение в диаметре равняются 1,0 см и более. При отрицательной кожной пробе ПСС (из ампулы, маркированной синим цветом) вводят подкожно в объеме 0,1 мл. При отсутствии реакции спустя пол часа, нужно ввести стерильным шприцем остальную дозу сыворотки. На протяжении этого срока вскрытая ампула с ПСС должна быть закрыта стерильной салфеткой.
Примечание. Людям с аллергическими болезнями и реакциями на различные аллергены, а также получавшим ранее препараты, содержащие лошадиную сыворотку (ПСС и другие) или гетерологичные гаммаглобулины (антирабический, противоэнцефалитный и др.), перед введением основной дозы ПСС лучше всего прибегнуть к введению антигистаминных лекарственных средств.
Лицам с положительной реакцией на внутрикожное введение 0,1 мл разведенной 1:100 лошадиной сыворотки или имевшим реакцию на подкожное введение 0,1 мл ПСС, дальнейшее введение ПСС проводить нельзя.
Учитывая, что после введения ПСС и препаратов, в составе которых есть столбнячный анатоксин, у особо чувствительных лиц может развиться шок, за каждым привитым необходимо организовать медицинское наблюдение на протяжении 60 минут после прививания. А учреждение, в котором людям делают прививки, должно быть обеспечено средствами противошоковой терапии на случай необходимости.
Противопоказания к применению специфическиз средств экстренной профилактики столбняка
Основными противопоказаниями к применению средств специфической профилактики столбняка являются:
-
(в первой половине противопоказано введение АС (АДС-М) и ПСС, во второй половине – ПСС);
- повышенная чувствительность к соответствующему средству профилактики;
- у лиц, имевших противопоказания к введению АС (АДС-М) и ПСС, возможность проведения экстренной профилактики с помощью ПСЧИ определяется лечащим врачом.
Состояние алкогольного опьянения не является противопоказанием к экстренной профилактике.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Столбняк: причины появления, симптомы, диагностика и способы лечения.
Определение
Столбняк представляет собой опасное инфекционное заболевание, вызванное столбнячной палочкой Clostridium tetani. Эта бактерия отличается крайней устойчивостью в окружающей среде: ее споры сохраняют жизнеспособность годами, а при температуре 90°С – около двух часов. Вегетативные формы клостридий погибают через несколько минут в кипящей воде и в течение 3-6 часов после обработки антисептическими и дезинфицирующими средствами. Попадая в рану, бактерии начинают вырабатывать токсин, который оказывает влияние нервную систему, приводя к тяжелым мышечным спазмам и судорогам.
По мере развития болезни спазм мышц вызывает серьезные проблемы с дыханием и в конечном итоге может привести к летальному исходу.
Столбняком можно заразиться в любом уголке земного шара, однако больше всего случаев заражения отмечается в жарких странах с плохой санитарно-гигиенической обстановкой. В странах с умеренным климатом пик заболеваемости приходится на летне-осенний период.
Причины появления столбняка
Огромную роль в распространении инфекции играет отсутствие профилактической вакцинации населения.
Столбнячные палочки живут в почве. Путь заражения – контактный. Бактерии попадают в организм через раны, ссадины, при ожогах, обморожениях и т.д.
После попадания в рану бактерии начинают вырабатывать токсин, который проникает в отростки нервных клеток, вызывая спастические сокращения мышц и судороги.
В связи со способностью продолжительно существовать в виде спор в почве, водоемах, на предметах возбудитель столбняка может попасть с пылью и грязью в любые помещения и инфицировать любые поверхности, включая медицинские.
- раневой,
- послеоперационный,
- послеродовой,
- послеожоговый,
- после обморожения,
- постинъекционный,
- столбняк новорожденных.
- локальный (поражаются только близлежащие к ране мышцы),
- генерализованный (поражаются все мышцы организма).
По степени тяжести: легкая форма (от момента заражения до первых симптомов проходит около 3 недель), средняя форма (симптомы появляются спустя 2 недели с момента заражения), тяжелая (симптомы возникают через 9–15 дней с момента заражения), крайне тяжелая (инкубационный период длится всего 3-5 дней).
Симптомы столбняка
Первые симптомы появляются в среднем через 7–10 дней от момента заражения, в редких случаях заболевание может развиться и раньше.
Различают три классических симптома столбняка:
- боль в области раны и иногда подергивание близлежащих мышц;
- скованность мышц живота;
- болезненные спазмы тела, продолжающиеся в течение нескольких минут, как правило, вызванные незначительными явлениями - сквозняком, громким шумом, прикосновением, светом;
- головная боль;
- боль в спине и затылке;
- повышенная потливость.
При прогрессировании заболевания судороги распространяются на мышцы всего тела (опистотонус), больной для облегчения состояния принимает различные вынужденные позы - выгибается дугой, сгибается в сторону или застывает как столб (отсюда и произошло название болезни).
В тяжелых случаях судороги настолько сильны, что могут приводить к разрывам мышц и перелому костей.
Тяжелое течение заболевания сопровождается повышением температуры тела, снижением артериального давления, увеличением частоты сердечных сокращений.
Диагностика столбняка
Как правило, поставить точный диагноз удается на фоне клинической картины при наличии раны, указывающей на возможное заражение.
Лабораторная диагностика не проводится, поскольку присутствие антител в крови может указывать на вакцинацию в детстве. При столбняке нарастания титров антител не происходит, так как даже летальные дозы экзотоксина не вызывают иммунного ответа. Ликвор (спинномозговая жидкость) также остается неизмененным, несмотря на поражение нервной системы.
В отдельных случаях применяют бактериологические методы (микроскопию мазков-отпечатков, гистологическое исследование тканей, иссекаемых при хирургической обработке ран, посевы раневого отделяемого на питательные среды в анаэробных условиях), позволяющие обнаружить возбудитель в месте расположения раны. Однако выделить культуру возбудителя из раны удается лишь у 30% больных.
К каким врачам обращаться
При травме с нарушением целостности кожных покровов, обморожении или ожоге следует обратиться к врачу-травматологу или врачу-хирургу, который после осмотра, сбора анамнеза и жалоб направит больного к узким специалистам: врачу-инфекционисту, врачу-неврологу.
Лечение столбняка
Лечение больных столбняком проводится только в стационаре. При тяжелом течении заболевания больного госпитализируют в реанимационное отделение.
Для купирования судорог применяют миорелаксанты, нейролептики. В связи с нарушением глотания введение препаратов зачастую осуществляется внутримышечно или внутривенно.
При поражении дыхательных мышц может потребоваться искусственная вентиляция легких.
Обязательным является введение антистолбнячной сыворотки. Причем чем скорее она будет введена, тем больше вероятность нейтрализации токсина.
Хирургическое лечение заключается в обработке раны, удалении инородных тел, назначении антибактериальной терапии при подозрении на присоединение бактериальной инфекции и в целях предупреждения развития гнойного процесса. Зашивать рану нельзя, чтобы не допустить размножения противостолбнячной палочки, поскольку закрытая рана без доступа кислорода является благотворной средой для данной бактерии.
Особое внимание уделяется восполнению жидкости, обеспечению питания с достаточным количеством калорий, насыщенного витаминами и микроэлементами. При выраженном нарушении глотания питание осуществляется жидкими питательными смесями с помощью зонда - специальной тонкой трубки, которую вводят через нос в полость желудка.
Осложнения
Осложнения делятся на ранние, возникающие в самый разгар болезни, и поздние, которые могут оставаться после выздоровления.
К ранним осложнениям относятся:
- Инфекции органов дыхания (бронхит, пневмония) - возникают в результате нарушения вентиляции легких, связанного с мышечным спазмом и длительным постельным режимом.
- Инфаркт миокарда – отмечается при тяжелом и крайне тяжелом течении столбняка, поскольку сердечная мышца, как и остальные мышцы организма, может подвергаться воздействию столбнячного токсина. Токсин особенно опасен для пожилых людей и пациентов с заболеваниями сердечно-сосудистой системы.
- Сепсис представляет собой системную воспалительную реакцию в ответ на попадание микроорганизмов в кровоток. Опасность сепсиса состоит в том, что воспалительный процесс затрагивает все органы и системы организма, нарушая их правильную работу, и в ряде случаев может привести к летальному исходу. Лечение сепсиса требует одновременного назначения нескольких внутривенных антибиотиков, постоянного контроля лабораторных показателей крови, пульса, артериального давления, температуры тела, мочеиспускания.
- Переломы костей, вывихи, разрывы мышц характерны для крайне тяжелого течения столбняка.
- Деформация позвоночника.
- Контрактуры мышц и суставов - состояние, при котором мышца или сустав сохраняют ограничение, скованность в движении даже после излечения от основного заболевания.
- Нарушение ритма сердца.
- Временный паралич черепных нервов, самым частым проявлением которого является нарушение функции глотания, двоение в глазах, птоз (опущение) века.
Плановая профилактики включает вакцинацию, которая проводится с рождения ребенка.
В России курс вакцинации против столбняка состоит из 3 прививок АКДС (в возрасте 3, 4,5 и 6 месяцев) и однократной ревакцинации в возрасте 18 месяцев. Далее ревакцинация проводится в 6–7 лет и в 14 лет вакциной АДС-М анатоксином. Последующие ревакцинации проводятся через каждые 10 лет.
Все прививки должны быть внесены в прививочные сертификаты. Полный курс прививок обеспечивает защиту у 95–100% привитого населения.
Экстренную профилактику необходимо проводить у непривитых или неправильно привитых людей при получении любых механических повреждений кожных покровов. Для этого как можно раньше (допустимо до 20 дня с момента травмы) вводят противостолбнячную сыворотку. Перед ее введением проводят пробу с разведенной сывороткой: если диаметр покраснения менее 1 см — проба отрицательная, если 1 см и более — положительная. При отрицательной пробе вводят сыворотку подкожно в наружную поверхность плеча или подлопаточную область. При положительной пробе введение сыворотки противопоказано. В этом случае вводят иммуноглобулин человека.
- Инфекционные болезни: национальное руководство / Под ред. Н.Д. Ющука, Ю.Я. Венгерова. - М.: ГЭОТАР-Медиа, 2009. С. 521–529.
- Рюмин А.М., Соболевская О.Л., Корочкина О.В., Волский Н.Е., Михайлова Е.А., Отмахова И.А., Собчак Д.М., Хряева О.Л. Случай столбняка легкого течения: тактические особенности ведения // Нижегородская государственная медицинская академия. 2017. С. 98–100.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.

Новость
Автор
Редактор
Более полувека назад двое ученых — Льюис Томас и Фрэнк Макфарлейн Бёрнет — выдвинули гипотезу о роли иммунной системы в контроле развития новообразований [1–3]. Ее суть Бёрнет сформулировал следующим образом:
У гипотезы было немало противников, но в последние десятилетия она получила многочисленные подтверждения. Иммунитет защищает человека от рака, и в этих защитных механизмах принимают участие T- и B-лимфоциты, макрофаги и натуральные киллеры (NK-клетки).
В процессе развития иммунологической толерантности по отношению к опухолевым клеткам участвуют разные механизмы [4], [5]. Они не до конца изучены, и все же в последние десятилетия, во многом благодаря достижениям молекулярной биологии и молекулярной генетики, многое стало известно. Полученные знания легли в основу относительного нового направления в лечении онкологических заболеваний — иммунотерапии. Сегодня многие ученые и врачи-онкологи возлагают на нее большие надежды [6].
Существует несколько направлений современной иммунотерапии [7–9]. Для борьбы с раком используют моноклональные антитела [10], цитокины (интерфероны, интерлейкины), противораковые вакцины, онколитические вирусы, перепрограммированные T-клетки (здесь большие перспективы открывает технология редактирования генов CRISPR-Cas9 [11–14]) и даже микобактерии туберкулеза [15–17].
Контрольные точки и их ингибиторы
Важную роль в противоопухолевом иммунитете играет клеточно-опосредованный иммунный ответ. Опухолевые клетки производят антигены, которые могут быть переработаны и представлены примитивным (наивным) T-лимфоцитам антигенпредставляющими клетками (APC) в виде соединений с молекулами главного комплекса гистосовместимости (MHC). В результате наивный T-лимфоцит превращается в эффекторный и запускает цепочку событий, которая в конечном счете приводит к уничтожению опухолевой клетки (рис. 1) [6], [18].

Рисунок 1. Активация T-лимфоцита с участием MHC-I. Наибольшее значение в качестве антигенпрезентирующих клеток имеют специализированные именно на этом дендритные клетки (но также эту функцию могут выполнять и макрофаги и B-клетки). После представления опухолевого антигена наивный T-лимфоцит трансформируется в цитотоксический CD8+ и вызывает гибель опухолевой клетки за счет продукции перфоринов, фрагментинов и индукции апоптоза через Fas-лиганды.
Некоторые опухолевые клетки защищаются от иммунной агрессии еще на стадии этого первичного иммунного ответа. Так, мутационные изменения структуры человеческих лейкоцитарных антигенов (молекул на поверхности клеток, которые извлекают из цитоплазмы куски неправильных или чужеродных, например, вирусных, белков и привлекают ими к себе Т-киллеров) приводят к нарушению их функций и мешает процессу активации иммунных клеток [6], [19].
Помимо механизма распознавания и представления антигенов с участием MHC, в противоопухолевом клеточно-опосредованном иммунном ответе важную роль играют дополнительные мембранные корецепторы. Они обеспечивают положительную и отрицательную модуляции иммунного ответа. В онкологических процессах особое значение имеют два таких корецептора: цитотоксический T-лимфоцитарный антиген-4 (CTLA-4, также известный как CD152) и мембранный белок PD-1 (а также его лиганд PD-L1, или CD274). [6]
CTLA-4 — белок, который в основном экспрессируют CD4+ и CD8+ T-лимфоциты (но также его экспрессия обнаружена и в B-лимфоцитах). В экспериментах in vitro и in vivo доказано его ингибирующее воздействие на первичный иммунный ответ [20]. Для начала пролиферации T-лимфоцитов необходимо, чтобы молекула B7-1 (CD80) или B7-2 (CD86) на поверхности APC связалась с CD28 на Т-клетке. При этом происходит передача сигнала. CTLA-4 — гомолог CD28, обладающий более высокой афинностью по отношению к B7. Однако при связывании CTLA-4 с B7 передачи сигнала не происходит. От соотношения количества связей CD28:B7 и CTLA-4:B7 зависит, будет ли T-клетка находиться в состоянии активации или анергии (рис. 2). Кроме того, CTLA-4, по-видимому, оказывает прямое ингибирующее влияние на иммунный синапс TCR, ингибирует CD28 и его сигнальный путь, а также повышает подвижность T-клеток, что снижает их способность к взаимодействию с APC [21].

Рисунок 2. CTLA-4-опосредованное ингибирование T-клеток. а — Благодаря связыванию MHC:TCR и CD28:B7 T-лимфоциты продуцируют интерлейкин-2 (ИЛ-2), активируется их пролиферация, повышается выживаемость. б — CTLA-4 конкурирует с CD28 за связывание с B7. Клетка получает негативный сигнал, снижается продукция ИЛ-2, ингибируется пролиферация Т-лимфоцитов и их выживаемость.
В норме в иммунной системе работает обратная связь. Поначалу молекулы CTLA-4 находятся в везикулах внутри клетки в неактивном состоянии. Сигналом к выходу на поверхность служит возникновение связей MHC:TCR и CD28:B7. Кроме того, CTLA-4 содержатся на поверхности регуляторных Т-клеток (Tregs) (рис. 3) [21].

Рисунок 3. CTLA-4-опосредованное ингибирование T-клеток с участием Tregs. Согласно гипотезе, CTLA-4 на поверхности Tregs вступают в связь с B7 на поверхности APC. В итоге CD28 на поверхности T-лимфоцитов не могут вступить в связь с B7, что нарушает активацию клеток.
CTLA-4, PD-1 и подобные им корецепторы, эффекты которых имеют большое значение при онкологических заболеваниях, были названы контрольными точками . Так как они мешают активации T-лимфоцитов и тем самым подавляют противоопухолевый иммунитет, однажды появилась идея создать препараты, которые могли бы ингибировать их. И в настоящее время такие иммунопрепараты созданы, прошли испытания и даже применяются в клинической практике. Называются они ингибиторами контрольных точек [22]. Механизмы действия этих препаратов показаны на рисунках 4 и 5.

Рисунок 4. Механизм действия ингибиторов CTLA-4 и B7-1/B7-2.

Рисунок 5. Механизм действия ингибиторов PD-1 и PD-L1.
По природе ингибиторы контрольных точек являются человеческими моноклональными антителами. Одновременно их можно отнести к группе таргетных препаратов, так как они прицельно связываются с определенными молекулами-мишенями.
Ингибиторы контрольных точек показали высокую эффективность у многих онкологических пациентов, но не обошлось и без проблем. Главная из них состоит в том, что не все пациенты одинаково хорошо отвечают на лечение.
Полезные бактерии, вредные бактерии
Считается, что резистентность к иммунотерапии при онкологических заболеваниях возникает главным образом из-за слабой инфильтрации опухолевой ткани иммунными клетками и иммуносупрессивных эффектов микроокружения опухоли [23], [24]. На иммунный ответ оказывают влияние в том числе и микроорганизмы, населяющие кишечник [25].
Накоплено немало данных, подтверждающих влияние кишечной микрофлоры на обменные процессы и иммунные реакции. Так, известно, что нарушение взаимодействия между хозяином и микробиотой связано с такими патологиями, как сахарный диабет, цирроз печени, воспалительные заболевания кишечника, колоректальный рак [25], [26].
У животных, которые получают антибиотики или искусственно лишены кишечной микробиоты, развивается резистентность к препаратам платины: снижается цитотоксичность, образование активных форм кислорода [29]. Состав кишечной микрофлоры оказывает влияние на фармакологические эффекты таких препаратов, как 5-фторурацил, иринотекан, оксалиплатин, гемцитабин, метотрексат [30].
Модуляция ответа на химиопрепараты и иммунопрепараты микробиотой кишечника сводится к одному из трех клинических эффектов:
- повышение эффективности препарата;
- ослабление противоопухолевого эффекта;
- повышение токсичности.
Представители микрофлоры используют разные механизмы ответа на препараты. Известные на данный момент объединяет аббревиатура TIMER (табл. 1) [30].
| Механизм ответа | Препараты, активирующие механизм | Бактерии, изпользующие механизм | Эффект взаимодействия бактерий с препаратом |
|---|---|---|---|
| Транслокация (Translocation) | Циклофосфамид Доксорубицин | Грамположительные микроорганизмы (Lactobacillus johnsonii, L. murinus, Enterococcus hirae) | Бактерии пересекают кишечный барьер и мигрируют во вторичные лимфоидные органы. |
| Иммуномодуляция (Immunomodulation) | Циклофосфамид | Lactobacillus | Грамположительные бактерии стимулируют иммунный ответ с участием клеток Th17 и Th1. |
| Метотрексат | Неизвестно | Бактерии регулируют повреждение кишечника химиопрепаратом через сигнализацию TLR2 и белок множественной лекарственной устойчивости. | |
| Блокаторы CTLA-4 | Bacteroidales | Подавление активации селезеночных эффекторных CD4+ Т-клеток и опухоль-инфильтрирующих лимфоцитов. | |
| Блокаторы PD-L1 | Bifidobacterium | Стимуляция опухолеспецифических Т-клеток и увеличение количества Т-лимфоцитов в микроокружении опухоли. | |
| Метаболизм (Metabolism) | Иринотекан | Неизвестно | Точная роль бактерий не известна, но лечение стрептомицином ингибирует поглощение иринотекана и снижает активность эпителиальной карбоксилэстеразы. |
| Ипилимумаб | Bacteroidetes | Бактериально опосредованная продукция витамина B и дефицит транспорта полиамина, связанные с повышенным рискоминдуцированного блоком CTLA-4 колита. | |
| Ферментная деградация (Enzymatic degradation) | Гемцитабин | Mycoplasma | Микоплазменные нуклеозидные фосфорилазы ограничивают цитостатическую активность. |
| Иринотекан | β-глюкуронидаза-экспрессирующая кишечная бактерия | Бактериальная β-глюкуронидаза расщепляет глюкуронид неактивного иринотекана (SN-38G), высвобождая активный метаболит (SN-38) в кишечнике. | |
| Сокращение разнообразия и функций экологической сети (Reduced diversity and ecological network function) | Комбинации кармустина, этопозида, цитарабина и мелфалана | Firmicutes Actinobacteria Proteobacteria | Уменьшается количество бактерий, которые подавляют воспаление, и увеличивается число бактерий, которые приводят к колиту. |
| Метотрексат | Анаэробы Стрептококки Bacteroides | Уменьшается разнообразие микроорганизмов, и сдвиги в составе кишечной микробиоты приводят к диарее. |
Свежие данные
Начало 2018 года ознаменовалось сразу тремя научными работами, посвященными влиянию микрофлоры кишечника на эффективность ингибиторов контрольных точек.
Работа Виары Мэтсон с соавторами посвящена метастатической меланоме. Ученые отобрали 42 пациента, страдавших этим заболеванием, и провели анализ их стула тремя различными методами. В дальнейшем бóльшая часть пациентов (38 человек) получала блокаторы PD-1 (ниволумаб, пембролизумаб), а четверо — блокатор CTLA-4 (ипилимумаб) [31].
Оказалось, что в составе кишечной микрофлоры пациентов, которые хорошо отвечали на терапию ингибиторами контрольных точек, было повышено количество восьми видов бактерий: Enterococcus faecium, Collinsella aerofaciens, Bifidobacterium adolescentis, Klebsiella pneumoniae, Veillonella parvula, Parabacteroides merdae, Lactobacillus sp. и Bifidobacterium longum. В кишечной микробиоте испытуемых, не ответивших на терапию, были многочисленны два микроорганизма: Ruminococcus obeum и Roseburia intestinalis.
Затем представителей кишечной микрофлоры пациентов с помощью метода трансплантации фекальной микробиоты (fecal microbiota transplantation, FMT) пересадили в кишечник стерильных (безмикробных) мышей [32]. Спустя некоторое время животным имплантировали клетки меланомы. Опухоли в теле мышей, которым пересадили бактерий от людей, ответивших на иммунотерапию, в целом росли медленнее. У них оказались более эффективны блокаторы PD-1 [31], [33].
Ванчесваран Гопалакришнан с коллегами также изучил микрофлору пациентов, страдающих распространенной меланомой, причем, не только в кишечнике, но и в полости рта [34]. Участники исследования получали лечение ингибиторами PD-1. Наилучший ответ наблюдался среди людей, у которых в стуле преобладали микроорганизмы рода Faecalibacterium. Преобладание группы Bacteroidales, напротив, оказалось связано с более низкой активностью препаратов. Ученые не обнаружили корреляции между составом микрофлоры полости рта и ответом пациентов на иммунотерапию.
Затем провели фекотрансплантацию микрофлоры пациентов стерильным мышам, после чего животным имплантировали опухолевые клетки и начали вводить блокаторы PD-1 (рис. 6). У мышей, получивших микробиоту людей, хорошо ответивших на терапию, отмечалось более существенное сокращение роста опухолей. В их стуле также преобладали бактерии рода Faecalibacterium [33], [34].

Рисунок 6. Эксперимент с трансплантацией фекальной микробиоты мышам от пациентов, по-разному ответивших на лечение блокаторами PD-1.
Работа Бертрана Роути с соавторами посвящена взаимосвязи состава кишечной микрофлоры и эффективности блокаторов PD-1 при немелкоклеточном раке легких, карциноме почек и уротелиальной карциноме [35]. Исследователи отметили, что прием антибактериальных препаратов для лечения инфекции во время онкологического заболевания ухудшает ответ на введение ингибиторов контрольных точек. Причем, в стуле у людей, хорошо отвечавших на терапию, авторы обнаружили повышенное количество микроорганизмов Akkermansia muciniphila.

Рисунок 7. FMT и имплантация опухолевых клеток в тело лабораторных мышей. Слева — пациент, не ответивший на лечение блокаторами PD-1. Справа — пациент, хорошо ответивший на иммунотерапию.
Проблемы
Авторы всех трех исследований сходятся на том, что кишечная микрофлора — важный фактор, влияющий на эффективность ингибиторов контрольных точек, и с ним однозначно нужно считаться. Тем не менее результаты расходятся: в качестве предикторов названы разные группы микроорганизмов. Возможно, это зависит от типа злокачественной опухоли или индивидуальных особенностей пациентов. Вероятно, в этом загадочном треугольнике — микрофлора—хозяин—иммунопрепарат — существуют общие механизмы и закономерности, но ученым они пока неизвестны. Главная проблема состоит в том, что знания в этой сфере пока немногочисленны и фрагментарны [33].
Перспективы
Есть надежда, что дальнейшее изучение влияния микрофлоры на эффективность противоопухолевых препаратов поможет решить две проблемы:
Эти подходы могут открыть новые возможности для персонализированной терапии онкологических заболеваний.

Рисунок 8. Схема FMT-терапии при рецидивирующей инфекции Clostridium difficile.
Инфицирование столбняком происходит при контакте с грамположительной столбнячной палочкой. Выделяемые ею споры проникают в открытые раны, после чего бактерия начинает выделять в организме носителя сильнейший токсин. Действие токсина провоцирует судороги и паралич, вызывая тяжелейшие поражения нервной системы. Это заболевание крайне опасно, поэтому любой человек должен знать, что за болезнь – столбняк, как она проявляется и что нужно делать в случае подозрений на заражение.
Говоря о столбняке, стоит упомянуть о дифтерии – родственной патологии. Обе носят бактериальный характер и имеют схожие симптомы, но возбудители у них разные. Тем не менее, от них делается одна и та же комбинированная прививка, направленная на формирование титра антител.
Столбняк: разновидности и стадии
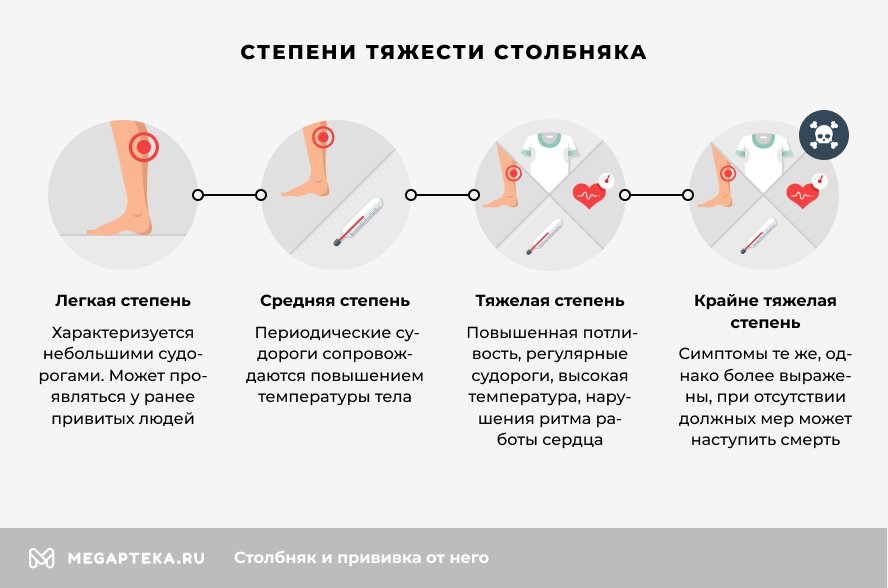
Столбняк провоцируется единственным патогеном – бактерией Clostridium tetani, поэтому болезнь классифицируют только по степени тяжести. Всего их насчитывается четыре:
- Легкая – длится менее одной недели и характеризуется незначительными судорогами. Может поражать ранее вакцинированных людей.
- Средняя – периодические судороги сопровождаются фебрильной температурой или жаром, и могут сохраняться на протяжении 3-4 дней.
- Тяжелая – отличается симптомокомплексом: повышенная потливость, регулярные судороги до 5-7 раз в час, высокая температура, озноб, нарушения сердечного ритма (тахикардия).
- Крайне тяжелая – симптомы те же, что у тяжелой, однако выражены интенсивнее. При неоказании медицинской помощи возможен летальный исход.
Возбудитель и симптомы столбняка
Лучше всего фекальные бактерии и споры чувствуют себя в соответствующей среде. В связи с этим повышенный риск заражения присутствует в местах скопления фекалий – на удобренных навозом полях, в деревенских туалетах и т.д. Контакты травмированной кожи с фекальными массами грозят обернуться большими неприятностями, хотя люди слабо представляют себе подобные события и не видят серьезной угрозы. Еще одна благоприятная среда для возбудителей столбняка – поверхности наподобие ржавого металла и грязного стекла. Инфицирование путем пореза кожи железом регистрируется в медицинской практике чаще всего. Иногда даже порез домашним кухонным ножом требует экстренных мер вакцинопрофилактики.
Важно знать, что столбняк не передается от одного человека к другому! Зараженный не опасен для окружающих. Болезнь возникает исключительно перечисленными выше путями.
Когда в больницу поступает пациент с повреждениями кожи, который потенциально мог заразиться столбняком, медики предпочитают проводить неотложную вакцинопрофилактику. Клинические же признаки столбняка – поздние. Инкубационный период длится около 2 недель, и лишь после этого пациент чувствует симптоматику столбняка.
Симптоматика столбняка имеет свойство нарастать. И если сначала человек может не придать значения легкому недомоганию, буквально через несколько часов или дней состояние вынуждает его обратиться за срочной медицинской помощью.
Читайте также:

