Лимбический энцефалит что это такое
Обновлено: 19.04.2024
В настоящее время среди врачей-психиатров и в специальной научной и медицинской литературе отсутствует единое мнение на этиологию и патогенез развития шизофрении. В клинике профессора В.Л. Минутко в г. Москва при лечении этого заболевания придерживаются мнения, что в генезе шизофрении принимают участие вирусы герпеса. При их активации, причиной которой является снижение иммунитета, на фоне сопутствующих инфекционных заболеваний возникает аутоиммунный лимбический энцефалит. При этом заболевании обнаруживается слабое воспаление в некоторых областях головного мозга – медиальной части височной доли, орбитофронтальной и фронтобазальной областях головного мозга.
Лечение шизофрении, с точки зрения наличия воспалительных изменений в головном мозге, является прерогативой именно нашей клиники и нигде больше не практикуется в г. Москва.
Стандартно воспалительные процессы в вышеуказанных областях мозга относятся к паранеопластическим. И на данный момент времени неизвестен механизм патогенеза аутоиммунного энцефалита, но вероятнее всего в нем участвуют антитела, направленные против внутриклеточных и мембранных антигенов нейронов. Это антитела к NMDA-рецепторам нейронов и к кальциевым каналам мембраны нейронов. Возможно, в патогенезе участвуют антитела к AMPA- и ГАМК-рецепторам второго типа.
Наши исследования и эффективность лечения с учетом аутоиммунной теории возникновения шизофрении подтверждаются и зарубежными учеными. В российской науке существует традиционный подход к причинам и лечению данного заболевания, что тормозит поиск новых методов лечения шизофрении.
Если сравнить клинические проявления аутоиммунного энцефалита и шизофрении, то можно найти много совпадений в динамике этих двух заболеваний. А именно фазности процесса: продромальная фаза, фаза психоза, фаза развития негативных синдромов, гиперкинетическая фаза.
В продромальной фазе мы наблюдаем такие симптомы как:
· психотические синдромы (апатия, тревога, фобии, колебания настроения, галлюцинации, бред преследования, нарушение сна, навязчивые состояния).
При классическом аутоиммунном лимбическом энцефалите можно видеть более выраженные органические повреждения при психозе:
Но при шизофрении аутоиммунный лимбический энцефалит имеет атипичное течение, поэтому использование аутоиммунотерапии и противовоспалительных средств позволяет проводить в нашей клинике более сбалансированное лечение.
Назначение противовоспалительных средств актуально при лечении шизофрении. Так, при исследовании наблюдается изменение С-реактивного белка, возникновение антител к стрептолизину, G-глиадину и глютаматтрансферазе.
Поэтому использование таких препаратов как целекоксиб или небольших доз кортикостероидов вполне обоснованно.
Если шизофрения протекает с наличием аутоиммунных процессов, спровоцированных вирусной инфекцией и патоморфологическими изменениями в нейроглии (пролиферация микроглии и астроглии), то их можно обнаружить на электроэнцефалографии.
При этом на ЭЭГ видны нечетко выраженные локальные изменения – билатеральные синхронные разряды тета-волн, с повышенной амплитудой в левом полушарии.
Общий анализ крови у пациентов с шизофренией позволяет выявить лейкоцитоз – увеличенное количество лейкоцитов. Ряд исследователей при аутоиммунном лимбическом энцефалите обнаруживали повышенный титр энтеровирусов, криптококков, цитомегаловируса, токсоплазмы, вируса Эпштейн-Барр.
В клинике доктора В.Л. Минутко, где обследовалось и проходило лечение много больных с шизофренией, динамика нейротеста отображала изменения в глютаматэргических рецепторах (NMDA-рецепторах).
Эти показатели плюс данные биоэлектрической активности мозга могут использоваться в качестве маркеров шизофрении, в генезе которой участвует аутоиммунный лимбический энцефалит.
Таким образом, лечение шизофрении лучше проводить, исследуя аутоиммунные повреждения лимбической системы головного мозга, тогда эффективность терапии возрастает многократно.
Facebook Если у вас не работает этот способ авторизации, сконвертируйте свой аккаунт по ссылке ВКонтакте Google RAMBLER&Co ID
Авторизуясь в LiveJournal с помощью стороннего сервиса вы принимаете условия Пользовательского соглашения LiveJournal
Лимбический энцефалит

[читать] (или скачать)
статью в формате PDF

Лимбический энцефалит (ЛЭ) является редким неврологическим синдромом, при котором аутоиммунный воспалительный процесс локализуется в лимбических структурах - гиппокампе, миндалевидном теле, опоясывающей извилине, гипоталамусе и переднем ядре таламуса (участвующих в осуществлении высших корковых функций - памяти, обучения, эмоций). Согласно общепринятой концепции, в основе ЛЭ лежит аутоиммунная реакция, вызванная раковым, инфекционным или системным заболеванием. Иногда причину ЛЭ идентифицировать не удается и тогда ЛЭ называют также идиопатическим.
Клиническая картина ЛЭ. Как непаранеопластический, так и паранеопластический лимбический энцефалит характеризуется сходными клиническими проявлениями. Клиническая картина ЛЭ обычно развивается подостро, в течение нескольких недель, иногда дней (остро), реже нескольких месяцев. Кардинальными симптомами являются нарушения памяти и других когнитивных функций, аффективные и поведенческие расстройства, у большинства больных ассоциированные с комплексными парциальными (фокальными) и генерализованными эпилептическими припадками. Нарушения памяти, как правило, значительные, касаются преимущественно краткосрочной памяти и обусловлены прежде всего дисфункцией гиппокампа. Характерны невропсихиатрические нарушения в виде тревожных и депрессивных расстройств, апатии, ажитации, обсессивно-компульсивного поведения, возможны галлюцинации, спутанность и помрачение сознания, описаны также психогенные припадки. Эпилептические приступы часто носят характер мезотемпоральных. Из других симптомов могут наблюдаться дискинезии, афазия, апраксия, гиперсомния или инсомния, гипертермия, а также иные автономные расстройства и эндокринные нарушения. Нередко клиническая картина соответствует синдрому быстро прогрессирующей деменции и может напоминать болезнь Крейцфельдта - Якоба.
Дифференциальная диагностика ЛЭ проводится с паранеопластическим ЛЭ, с герпес-вирусным энцефалитом, нейросифилисом, первичным церебральным васкулитом, энцефалитом, ассоциированным с вирусом герпеса человека 6-го типа, опухолями головного мозга (глиоматозом, лимфомой, метастазами опухолей и др.), непаранеопластическим (аутоиммунным) лимбическим энцефалитом, токсико-метаболической энцефалопатией, поражением головного мозга на фоне аутоиммунных заболеваний (системной красной волчанки, тиреоидита Хашимото, синдрома Сьёгрена, антифосфолипидного синдрома), нарушением обмена витаминов (энцефалопатией Вернке-Корсакова, дефицитом витамина В12 – цианокобаламина), рассеянным склерозом, нейродегенеративными заболеваниями (болезнью Альцгеймера, фронто-темпоральной деменцией) и др.

Распространенная точка зрения о плохом прогнозе ЛЭ в настоящее время пересмотрена. Существенный процент больных, особенно с аутоиммунным идиопатическим ЛЭ, может отвечать на лечение. Прогноз во многом зависит от вовремя начатого лечения, что делает важным раннюю диагностику заболевания.
Этиология и патогенез. Первоначально ЛЭ был описан как паранеопластический синдром. На сегодняшний день известно около 30 антигенов, антитела к которым разделяют на 2 основные группы: [ 1 ] антитела к внутриклеточным антигенам, являющимся классическими онконевральными или паранеопластическими (к ним, в частности, относятся такие ассоциированные с ЛЭ анти- тела, как анти-Hu, анти-Ма2 и анти-CV2/CRMP5); [ 2 ] антитела к антигенам нейрональной мембраны, или поверхностные нейрональные антитела, которые включают антитела к белкам вольтаж-зависимых калиевых каналов (voltage-gated potassium channels - VGPC) и NMDA (N-methyl-D-aspartate) рецепторов, а также другие, выделенные в нейропиле гиппокам- па и мозжечка, в том числе пока еще не получившие названия.
Считается, что ЛЭ может быть ассоциирован с раком любой локализации, но наиболее часто - с раком легкого (40 - 50%), семиномой (20 - 25%) и раком молочных желез (8%). Описаны также единичные случаи ЛЭ при лимфоме Ходжкина, злокачественной тимоме, аденокарциноме толстой кишки, раке яичников и хронической миелоидной лейкемии. Неврологические симптомы предшествуют диагнозу карциномы у 60 - 75% больных в среднем на 3,5 месяца, иногда на 2 - 3 года. После обнаружения ракового заболевания ЛЭ может развиться в течение 1 - 48 месяца. Среди паранеопластических синдромов ЛЭ встречается реже, чем поражение периферической нервной системы, его частота сопоставима с такими расстройствами, как мозжечковая дегенерация и стволовая энцефалопатия той же природы.
Хотя в подавляющем большинстве случаев ЛЭ считают редким и неизлечимым заболеванием, которое почти всегда ассоциировано с раком, тем не менее, описаны клинические случаи ЛЭ (ПЛЭ) у пациентов с выявленными антителами к VGPC, у которых в дальнейшем не было диагностировано рака, но он (ЛЭ) хорошо поддавался иммуномодулирующему лечению, а титры антител отражали тяжесть клинических проявлений. Это указывает на то, что ПЛЭ чаще, чем ранее предполагалось часто выступает как самостоятельное заболевание.
ЛЭ и анти-VGPC-антитела . ЛЭ, ассоциированный с антителами к VGPC, описан недавно и в 80% случаев не является пара- неопластическим. Тем не менее такие антитела не считают патогномоничными для идиопатического ЛЭ, поскольку они могут быть обнаружены и у пациентов с неопластическими процессами, например, злокачественной тимомой или мелкоклеточным раком легкого. Известно, что анти-VGPC-антитела играют ведущую роль в патогенезе синдромов Исаакса (нейромиотонии) и Морвана. При первом наблюдается повышенная возбудимость периферических нервов, при втором - сочетание периферической и центральной гипервозбудимости. Если нет вовлечения периферической нервной системы, заболевание развивается как ЛЭ и эпилепсия. У таких пациентов часто обнаруживают гипонатриемию, которая может быть преходящей. Для клинической картины характерны рано возникающие нарушения памяти без выраженного снижения интеллекта, а также генерализованные и парциальные эпилептические припадки. В перечень реже встречающихся нарушений, ассоциированных с антителами к VGPC, входят также автономные расстройства, миоклонус, диссомния, экстрапирамидные и стволовые симптомы (перечисленные в порядке убывания частоты наблюдений). Не характерны головная боль, головокружение и нарушения сознания вне эпилептических припадков.
Верификация диагноза ЛЭ может вызывать большие трудности, поскольку дополнительные методы исследования и даже аутопсия нередко не дают ожидаемого результата и мало специфичны. Магнитно-резонансная томография (МРТ) в зависимости от этиологии ЛЭ обнаруживает патологию, по данным разных авторов, в 30 - 90% случаев ЛЭ. Характерно одностороннее или двустороннее повышение сигнала в мезотемпоральных отделах в режиме Т2 и FLAIR, иногда только во FLAIR, которое варьирует от значительного до слабого, может быть преходящим и не всегда коррелирует с клинической картиной. Изменения могут распространяться на ствол мозга, средний мозг, лобную долю и базальные ганглии. В части случаев в гиппокампе и гипоталамусе отмечают накопление контраста. Единичные исследования МР-спектроскопии описывают снижение N-ацетил-аспартата и повышение холина и ацетата в наиболее вовлеченных зонах. Позитронная эмиссионная томография (ПЭТ) с флюоро-2-дезоксиглюкозой может быть нормальной или выявляет гиперметаболизм в височных областях, описаны также единичные случаи гипоперфузии. При NMDA-энцефалите наблюдается лобно-височно-затылочный градиент метаболизма глюкозы, который коррелирует с активностью заболевания. В восстановительной стадии и отдаленном периоде более характерны гипоперфузия и гипометаболизм в лобно-височных отделах мозга. Исследование МРТ в динамике может выявлять исход первоначальных изменений в атрофию гиппокампа и височных долей.

В диагностике ЛЭ первостепенное значение имеет клиническая картина заболевания. Важным условием являются негативные результаты инфектологического, в том числе и вирусологического обследования. Большое значение имеют данные нейровизуализации и/или других перечисленных выше методов исследования, указывающие на воспалительный аутоиммунный процесс типичной локализации. Во всех случаях предполагаемого ЛЭ необходимо проводить поиск онкологического заболевания.
Алгоритм обследования и ведения пациентов с подозрением на ЛЭ (адаптированная схема T. Wingfi eld и соавт., 2011):

Лечение ЛЭ во многом зависит от его этиологии. При паранеопластическом ЛЭ наиболее эффективно радикальное удаление первичной раковой опухоли. Если такое возможно, то более чем в 2/3 случаев может наблюдаться улучшение неврологической симптоматики или выздоровление. Дополнительно используется иммуномодулирующая терапия, которая при идиопатическом ЛЭ является основным способом лечения. Применяются кортикостероиды (преднизолон в дозе 60 - 100 мг/ сут или пульс-терапия метилпреднизолоном), цитостатики (ритуксимаб, циклофосфамид, азатио- прин), IgG (0,4 мг/кг/сут) и плазмаферез. В целом сочетание различных методов лечения позволяет добиться неврологического улучшения в среднем у 1/3 больных с паранеопластическим ЛЭ. При этом лечение основного онкологического заболевания более эффективно, чем иммуносупрессивная терапия. Идиопатический, или аутоиммунный ЛЭ, по сравнению с паранеопластическим ЛЭ гораздо лучше отвечает на иммуномодулирующую терапию. Частичное или полное выздоровление коррелирует со снижением уровня поверхностных мембранных антител. Чем раньше начато лечение, тем лучше прогноз и меньше резидуальный дефект.
Паранеопластические синдромы на КТ, МРТ головного мозга
а) Терминология:
1. Синонимы:
• Паранеопластические синдромы (ПС), паранеопластическая болезнь
2. Определение:
• Отдаленные неврологические эффекты рака, связанные с неопластическим процессом экстра-ЦНС локализации:
о Наиболее частая опухоль: мелкоклеточный рак легкого
• Лимбический энцефалит (ЛЭ) является наиболее частым клиническим паранеопластическим синдромом:
о Единственный ПС с четкими томографическими признаками
б) Визуализация:
1. Общие характеристики паранеопластических синдромов:
• Лучший диагностический критерий:
о Лимбический энцефалит: повышение интенсивности сигнала от медиальных отделов височных долей, структур лимбической системы:
- Визуализационная картина такая же, как и при герпетическом энцефалите, однако характерно иное клиническое течение (подострая/хроническая стадия)
о При первичном исследовании в 20-40% изменения не наблюдаются
• Локализация изменений при ЛЭ: гиппокамп, миндалина мозжечка, поясная извилина, пириформная кора, субфронтальная кора, островок
2. КТ при паранеопластическом синдроме:
• Бесконтрастная КТ: при первичной КТ в > 95% случаев изменения не наблюдаются:
о Снижение плотности медиальных отделов височных долей (редко)
• КТ с контрастированием: обычно контрастирование не наблюдается
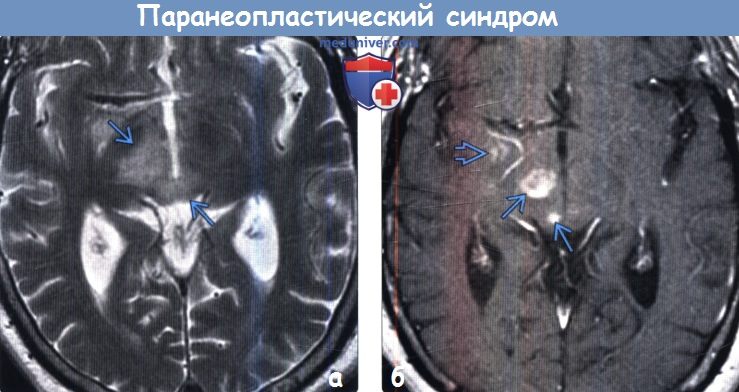
(а) МРТ, Т2-ВИ, аксиальный срез: в среднем мозге определяется гиперинтенсивная зона, отражающая стволовой энцефалит, который характеризуется появлением гиперинтенсивных зон в среднем мозге, мосте, ножках мозжечка и базальных ганглиях.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у того же пациента определяется фрагментарное контрастирование зон поражения в среднем мозге и медиальных отделах височной доли. Данному пациенту с новыми стволовыми симптомами был поставлен диагноз лимбический энцефалит. У одного и того же пациента возможно развитие нескольких паранеопластических синдромов.
4. Радионуклидная диагностика:
• ПЭТ с ФДГ: гиперметаболизм глюкозы в медиальных отделах височных долей у пациентов с ЛЭ
5. Рекомендации по визуализации:
• Советы по протоколу исследования:
о МРТ с получением постконтрастных Т1-ВИ, корональных Т2-ВИ или FLAIR-изображений
о Рассмотрите возможность повторной МРТ, если на фоне отсутствия изменений при первичном исследовании сохраняется высокое клиническое подозрение
в) Дифференциальная диагностика паранеопластического синдрома:
1. Герпетический энцефалит:
• Повышение интенсивности сигнала на Т2-ВИ от медиальных отделов височных долей, структур лимбической системы
• Часто наблюдается масс-эффект, ограничение диффузии
• Быстрое начало, лихорадочное состояние
• Титры ВПГ (вСМЖ, сыворотке) на ранних этапах заболевания могут быть отрицательными
• Возможные кровоизлияния на поздней острой/подострой стадии
• Может быть неотличим от лимбического энцефалита
2. Диффузная астроцитома низкой степени злокачественности (grade II):
• Одностороннее гиперинтенсивное объемное образование
• Могут поржаться медиальные отделы височной доли
• Характерно отсутствие контрастного усиления
3. Эпилептический статус:
• Судороги могут обусловливать аномальное изменения сигнальных характеристик на Т2-ВИ/FLAIR медиальных отделов височных долей
• Характерно контрастирование коры, ограничение диффузии в ее области
• Судорожный синдром в анамнезе
4. Глиоматоз головного мозга:
• Диффузный процесс, склонность к поражению лимбической системы отсутствует
• Гиперинтенсивные на Т2-ВИ зоны в нескольких смежных долях
• Увеличение объема пораженных структур
5. Паренхимальные метастазы:
• Обычно мультифокальное поражение, характерно накопление контраста
• Часто известна первичная опухоль
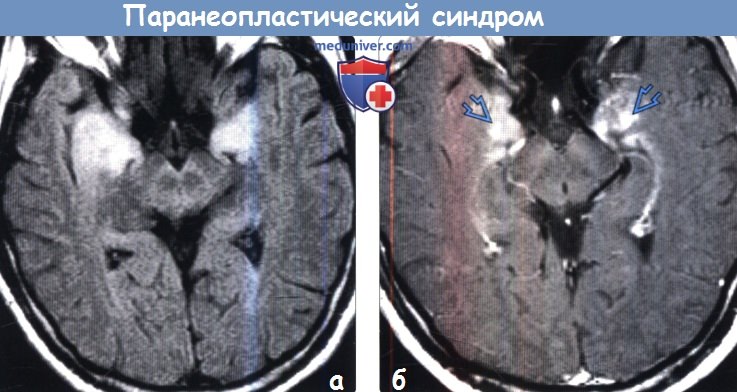
(а) MPT, FLAIR, аксиальный срез: аномальное двустороннее повышение интенсивности сигнала от медиальных отделов височных долей, что обусловлено лимбическим энцефалитом. Поскольку визуализационные признаки в этом случае имитируют герпетический энцефалит, большинству пациентов первоначально проводят противовирусную терапию до тех пор, пока титры ВПГ не окажутся отрицательными. Пара неопластический синдром развивается у менее 7 % пациентов с раковыми заболеваниями.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у этого же пациента определяется фрагментарное контрастирование медиальных отделов височных долей. Лимбический энцефалит является единственным паранеопластическим синдромом с четкими визуализационными признаками.
г) Патология:
3. Макроскопические и хирургические особенности:
• ЛЭ: плохо отграниченное от окружающих структур размягчение и изменение цвета серого вещества (СВ):
о Гиппокамп, поясная извилина, пириформная кора, лобная орбитальная поверхность височной доли, островок, миндалевидное тело; типично двустороннее поражение
• ПМД: атрофия мозжечка, истончение извилин
• Стволовой энцефалит: размягчение ствола мозга
4. Микроскопия:
• Лимбической энцефалит:
о Потеря нейронов, реактивный глиоз, периваскулярная лимфоцитарная инфильтрация, микроглиальные узелки
о Отсутствие новообразований и вирусных включений
• ПМД: потеря клеток Пуркинье, микроглиальная пролиферация, гиперплазия глии Бергмана, уменьшение числа зернистых клеток
• Стволовой энцефалит: периваскулярные воспалительные инфильтраты, глиальные узелки, нейронофагия
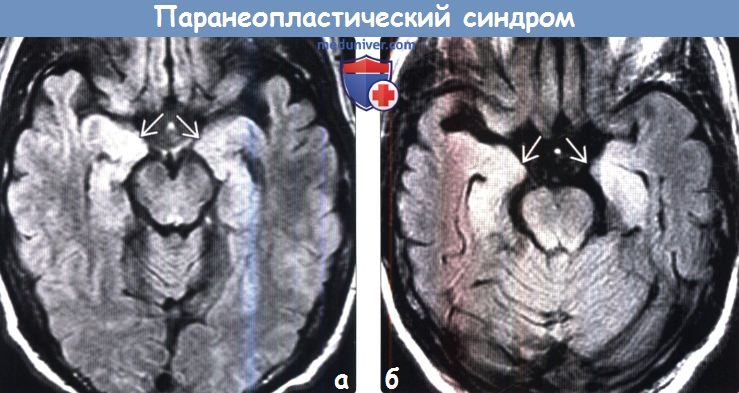
(а) МРТ, FAIR, аксиальный срез: у молодого пациента с меланомой и подострой деменцией определяется легкое асимметричное повышение интенсивности сигнала от гиппокампов.
(б) МРТ, FAIR, аксиальный срез: у пациента с подострой деменцией и аутоиммунной реакцией против потенциалзависимых калиевых каналов (VGKC) определяется повышение интенсивности сигнала от медиальных отделов обеих височных долей. Аутоиммунная реакция против VGKC может возникать при отсутствии первичной опухоли или может представлять собой паранеопластический синдром, имитируя лимбический энцефалит. Данное состояние характеризуется хорошим ответом на иммунотерапию.
д) Клиническая картина:
1. Проявления паранеопластического синдрома:
• Наиболее частые признаки/симптомы:
о ЛЭ: потеря памяти, когнитивная дисфункции, деменция, психологические изменения (тревога, депрессия, галлюцинации), судороги; подострый характер проявлений
о ПМД: атаксия, дискоординация, дизартрия, нистагм:
- У пациентов возрастом > 50 лет мозжечковая дегенерация имеет паранеопластический генез в 50% случаев, часто предшествует развитию отдаленного злокачественного поражения
о Стволовой энцефалит: дисфункция стволовых структур, включая параличи черепных нервов, нарушения зрения
о У пациентов с известной первичной опухолью необходимо исключать другие осложнения:
- Метастазы, инфекция, нарушение обмена веществ, эффект химиотерапии
• Клинический профиль:
о У 60% пациентов с ПС при поступлении в лечебное учреждение в анамнезе может отсутствовать известная первичная опухоль, у многих из них опухоль при обследовании не выявляется
о Обнаружение антинейрональных антител в сыворотке или СМЖ облегчает диагностику паранеопластического синдрома (ПС) и первичной раковой опухоли
о Первичные новообразования:
- Лимбический энцефалит:
Наиболее часто: мелкоклеточный рак легкого
Другие = желудочно-кишечный тракт, мочеполовая система (яичники > почки > матка), лимфома, молочные железы, семенники, тимус, нейробластома (у детей)
У 90% пациентов имеет место положительные тесты СМЖ (плеоцитоз, ↑ белка, олигоклональные полосы)
Вовлечение височных долей по данным ЭЭГ
- Паранеопластическая мозжечковая дегенерация:
Мочеполовая система (яичники), молочные железы, легкие, лимфома
- Опсоклонус-миоклонус синдром:
Нейробластома, рак легкого
- Миастенический синдром Ламберта-Итона:
Мелкоклеточный рак легкого
2. Демография:
• Возраст: встречается в любом возрасте, чаще всего у взрослых
• Эпидемиология: у < 1% пациентов с метастатическим раком развивается паранеопластический синдром
3. Течение и прогноз:
• Зависят от первичной опухоли
• По некоторым данным у пациентов с паранеопластическим синдромом (ПС) по сравнению с пациентами без его развития опухоли более вялотекущий темп роста
• Зависят от типа паранеопластического синдрома:
о Медленное долгосрочное снижение когнитивных функций (ЛЭ)
о Прогрессирующая атаксия, мышечная слабость (ПМД, дегенерация спинного мозга)
4. Лечение:
• Лечение первичной опухоли может позволить купировать неврологические симптомы паранеопластического синдрома (ПС) (25-45%)
• Резекция первичной опухоли ± химиорадиотерапия
• Тактика лечения паранеопластических синдромов вариабельна:
о Лечение первичной опухоли является лучшим методом
о ± стероиды, иммуноглобулины, плазмаферез
е) Диагностическая памятка:
1. Обратите внимание:
• ЛЭ-единственный ПС с явно выраженными томографическими признаками
• Клиническое проявление паранеопластических синдромов часто предшествует диагностике первичной опухоли
• Повторите МРТ, если на фоне отсутствия изменений при первичном исследовании сохраняется высокое клиническое подозрение, поскольку при ЛЕ поданным первичной МРТ характерных изменений обычно не выявляется
2. Советы по интерпретации изображений:
• Герпетический энцефалит при визуализации имитирует ЛЭ, но характеризуется острыми проявлениями:
о Пациенты часто изначально подвергаются противовирусной терапии до окончательного исчезновения титров ВПГ
• Кровотечение характерно для герпетического, а не лимбического энцефалита.
Герпетический энцефалит у ребенка - причины, клиника, диагностика, лечение
Первичные энцефалиты характеризуются наличием вирусов и их репликацией в клетках-мишенях в ЦНС. Хотя большое число вирусов может индуцировать первичный энцефалит, в Западной Европе одним из наиболее распространенных возбудителей является вирус простого герпеса. Энтеровирусы также могут стать причиной первичного энцефалита. Однако в других странах, включая Северную Америку, важнейшим этиологическим фактором являются арбовирусы.
Не менее 90% случаев связаны с вирусом простого герпеса 1 типа, хотя и ВПГ-2 является широко распространенным возбудителем диссеминированной инфекции и энцефалитов новорожденных (Kennedy и Chaudhuri, 2002). До появления ацикловира смертность от герпетического энцефалита составляла более 70% и менее 3% пациентов выживали без тяжелых последствий. В западных странах заболевание среди всех возрастных групп встречается от 1 на 200000 до 1 на 400000 населения в год, что составляет около 10% всех тяжелых вирусных инфекций ЦНС.
31% случаев относятся к возрасту до 20 лет, из них 12% среди детей от 6 месяцев до 10 лет (Whitley et al., 1982b; Whitley и Kimberlin, 2005).
Первоначально большинство случаев герпетического энцефалита приписывали реактивации латентной вирусной инфекции, но геномный анализ вирусных штаммов от пациентов показал, что случаи энцефалита вызываются путем первичной инфекции, реактивации латентной инфекции и реинфекции новыми штаммами (Whitley и Alford, 1982). Первичное инфицирование у новорожденных и детей раннего возраста встречается в норме.
Герпетический энцефалит крайне цитопатический, патоморфологически характеризующийся некротическими поражениями, которые чаще всего имеют геморрагический характер с обширными участками размягчения и, в тяжелых случаях, с полной утратой нейрональных и глиальных элементов. Повреждение преобладает в орбитальной, средней височной, поясной и островковой коре и в некоторых случаях может распространяться на ствол мозга (Duarte et al., 1994). У перинатально инфицированных новорожденных повреждение обычно распространяется по всему мозгу. Внутриядерные эозинофильные включения (тельца Каудри типа А) можно обнаружить в нейронах, олигодендроцитах и астроцитах, а вирус может быть выделен из ткани и СМЖ.
Клиническим симптомам энцефалита в 60% случаев предшествуют продромальные явления, которые могут быть чисто системными, такими как лихорадка и недомогание, но встречаются и более специфичные при наличии очевидных расстройств памяти и поведения. Продромальная фаза обычно длится несколько дней с усилением симптомов угнетения сознания, патологического поведения и высокой лихорадки. Наиболее полная картина включает симптомы, обычные для всех случаев энцефалита, т.е. вялость, оглушенность или кома и судорожные припадки.
Судороги особенно часто встречаются и повторяются в случаях герпетической инфекции и почти всегда бывают очаговыми, особенно поражая лицо и верхнюю конечность, отражая грубую асимметрию повреждений, что несомненно является патологическим. Может также встречаться эпилептический статус фокальных судорог. ВЧД зачастую повышено, и отек зрительного сосочка представлен у 15% пациентов. Часто становятся заметны гемиплегия и афазия, нередко они являются первой находкой у более старших детей и подростков. Могут проявляться изменения, указывающие на очаговый некроз височнобазальных структур, такие как аносмия, обонятельные галлюцинации и расстройства поведения (Whitley et al., 1981).
С момента появления более чувствительного метода ПЦР для диагностики герпесных энцефалитов спектр заболеваний ЦНС, вызываемых этим вирусом у взрослых и детей, расширился за счет включения более легких и атипичных форм (Dennett et al., 1996). Общепризнано, что заболевание у пациентов с иммуносупрессией протекает длительнее (Kleinschmidt-DeMasters и Gilden, 2001).
В отличие от диффузных медленных волн на ЭЭГ при других менингитах, запись при ВПГ обычно очень асимметрична, и часто выявляется четкий очаг спайков при патологически замещенной фоновой активности. Низкая амплитуда в одной или многих областях, особенно над височной долей, не является необычной. В этих же областях часто имеются периодические комплексы через 1-3 секунды, но обычно они имеют транзиторный характер (Mizrahi и Tharp, 1982). Периодические комплексы возникают чаще всего между 2-15 сутками болезни и реже выявляются в более поздние сроки (Schauseil-Zipf et al., 1982). Они не специфичны, но могут встречаться при энцефалите, вызванном М. pneumoniae (Hulihan et al., 1992) или вирусом Эпштейна-Барр.
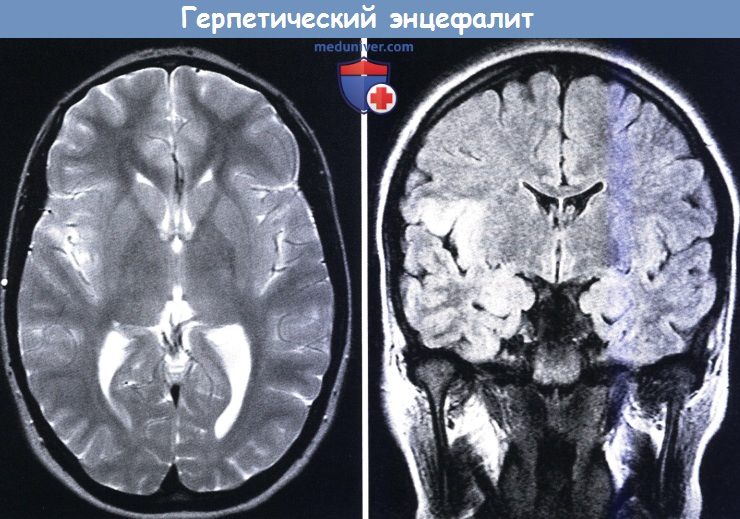
FLAIR (слева) и Т2-взвешенное (справа) МРТ:
гиперинтенсивные зоны в правой островковой коре и задне-базальной части лобной доли как вторичные проявления герпетического энцефалита.
Сканирование мозга может дать нормальные показатели в первые 24-48 часов после начала заболевания, а изменения на МРТ визуализируются до изменений на КТ (Kapur et al., 1994). На МРТ можно увидеть очаговый отек в средних отделах височной и орбитальной поверхности лобных долей, коры островка и угловой извилины. Патологическая КТ обычно показывает сниженное затухание в одной или обеих лобных или височных долях и иногда участки гиперэхогенности, представляющие небольшие кровоизлияния, в более чем 50% случаев также может быть смещение срединных структур (Greenberg et al., 1981; Dutt и Johnston, 1982).
В ходе течения болезни может наблюдаться начальное распространение поражения (Koskiniemi и Ketonen, 1981). Позже постепенно появляется и остается атрофия паренхимы с отчетливым преобладанием в перисильвиевой и височной области, иногда развивается кальцификация. Полное исчезновение патологических изменений на КТ у детей отмечается редко, но бывает у взрослых.
Ликвор может быть нормальным у 20-25% пациентов. В большинстве случаев он находится под повышенным давлением и содержит избыточное количество клеток, обычно лимфоцитов, и менее, чем 50 мононуклеаров/мм 3 приблизительно в четверти случаев (Whitley et al., 1982b). СМЖ часто геморрагическая или ксантохромная из-за некротического и геморрагического характера поражений.
Диагностика герпетического энцефалита основана на ПЦР амплификации ДНК вируса простого герпеса из ликвора. Этот метод высоко чувствительный (>95%) и специфичный (>95%), но могут встречаться ложноотрицательные результаты ПЦР в образцах, взятых рано, в течение первых 24-48 часов или позднее, через 10-14 дней и у пациентов, получавших лечение ацикловиром (Lakeman и Whitley, 1995; Koskiniemi et al., 1996; Davis, 2000). Количественное соотношение ДНК-копий вируса в миллилитре ликворной жидкости и степени повреждения ЦНС до сих пор не изучалось (Tyler, 2004). При отрицательном результате ПЦР наличие четырехкратного увеличения титра антител против ВПГ-1 инфекции в СМЖ является значимым, но требуется не менее 10-14 дней для их появления (Koskiniemi et al., 1984).
Изначально антитела принадлежат к классу IgM, позднее сменяющимся типом IgG. Они связаны с наличием олигоклонального белка в СМЖ (Mathiesen et al., 1988). Антитела и олигоклональные структуры могут персистировать годами, после приступа герпетического энцефалита (Tardieu и Lapresle, 1980), отражая сохранение ВПГ в ЦНС.
При наличии анамнестических, клинических и/или полученных при визуализации признаков герпетического энцефалита лечение должно быть начато немедленно. Биопсия мозга показана только в исключительных случаях детям, у которых после сканирования мозга предполагается другой диагноз, требующий иного лечения, а не для подтверждения диагноза ВПГ. Такие диагнозы могут включать абсцессы мозга, опухоли или гранулематозный менингит (Whitley et al, 1989). Другие состояния, имитирующие герпетический энцефалит, такие как паранеопластический лимбический энцефалит или митохондриальная энцефаломиопатия с лактоцизом и инсультоподобные эпизоды (MELAS) (Johns et al., 1993), у детей встречаются редко.
Лечение герпетического энцефалита проводится аналогом нуклеозидов — ацикловиром, который ингибирует ДНК-полимеразу ВПГ и таким образом, вирусную репликацию (Skoldenberg et al., 1984; Whitley et al, 1986). Ацикловир фосфорилируется в активную форму с помощью вирусной тимидин-киназы в ВПГ инфицированных клетках и поэтому нетоксичен для здоровых клеток хозяина. В оригинальном рандомизированном контролируемом исследовании Skoldenberg et al., смертность среди взрослых с лечением ацикловиром составила 19% в отличие от 70% смертельных исходов без лечения, существенные последствия встречались в 14%, а 56% пациентов были выписаны с полным выздоровлением.
Даже при начале лечения вскоре после начала заболевания почти у двух третей выживших сохраняются остаточные неврологические расстройства, а у детей в возрасте менее 12-18 месяцев наблюдались наиболее неблагоприятные прогнозы по показателям заболеваемости и смертности (Whitley и Kimberlin, 2005). Среди последствий выделяют гемиплегию (Rautonen et al., 1991), билатеральный оперкулярный синдром (van der Poel et al., 1995) и тяжелую эпилепсию, которая у новорожденных может проявляться в виде инфантильных спазмов. Часто наблюдаются изменения в поведении. Обычно имеется афазия из-за частых поражений височной локализации, которая может быть глобальной или более специализированной.
Резистентные штаммы ВПГ у детей встречаются редко; они более распространены у пациентов с ослабленным иммунитетом, которых часто лечили ацикловиром и в таких случаях может потребоваться использование других противовирусных средств, таких как фоскарнет или цидофовир (Whitley, 2002). Применение кортикостероидов совместно с противовирусными препаратами оправдано для устранения отека, но в связи с сопутствующим риском снижения реакции хозяина их использование не рекомендуется (Wood et al., 1994).
Как и у взрослых, лечебная дозировка ацикловира у детей составляет 10 мг/кг (или 500 мг/м 2 ) внутривенно каждые 8 часов (доза в мг/м 2 несколько превышает общую суточную дозу при дозировании в мг/кг). Внутривенное введение препарата рекомендовано для поддержания адекватной дозы, проникающей в ЦНС. В целом дети очень хорошо переносят ацикловир, хотя при высоких дозах при отсутствии достаточной дегидратации возможна нефротоксичность. В подтвержденных случаях курс терапии проводится 21 день; более короткие курсы лечения были связаны с повышенным риском рецидивов. Дети раннего возраста и новорожденные, по всей видимости, более подвержены риску или рецидиву (Davis, 2000; Ito et al„ 2000; Love et al., 2004; Valencia et al., 2004).
Хотя в некоторых случаях рецидив обусловлен возвратом вируса в ЦНС, другим этиологическим фактором может быть иммуноопосредованный механизм, связанный со вторичной демиелинизацией (Barthez et al., 1987; Pike et al, 1991; Rautonen et al., 1991; De Tiege et al., 2003, 2005). Рецидив у детей может быть связан с хореоатетоидным синдромом, который имеет плохой прогноз (Barthez et al, 1987; Shanks et al., 1991; Wang et al., 1994; Valencia et al., 2004). Рецидив также может быть связан с отсутствием выработки антител против ВПГ в ликворе (De Tiege et al., 2006).
У новорожденных более высокая доза ацикловира (20 мг/кг внутривенно каждые 8 часов до 21 дня) увеличила эффективность по показателям смертности и заболеваемости (Kimberlin et al., 2001). Увеличение дозы сопровождалось легкой нейтропенией у большинства пациентов, но при более тяжелой форме проводили поддержку колониестимулирующим фактором гранулоцитов. В связи с более обширным и диффузным поражением ЦНС и незрелым иммунным ответом у новорожденных, рекомендуется повторить исследование СМЖ методом ПЦР после лечения для подтверждения очистки от вирусов (Kimberlin, 2004). Кроме того, постоянная профилактика высокими дозами перорального ацикловира в первые 1-2 года жизни рекомендуется для снижения риска реактивации вируса и дальнейшего поражения ЦНС (Tiffany et al., 2005). Спорным остается вопрос о необходимости профилактики младенцам и детям после неонатального периода.
Обычная клиническая дилемма возникает при отрицательном результате ПЦР ликвора в случае начатого лечения пациента с фебрильным энцефалитом. Можно ли остановить начатое лечение ацикловиром, особенно с учетом того, что трехнедельное внутривенное введение препарата весьма обременительно для маленьких детей? Если не было выявлено иного диагноза, наш прагматичный подход при таких обстоятельствах допускает раннее прекращение лечения ацикловиром только в тех случаях, если клинически состояние ребенка возвращается к нормальному, данные ЭЭГ в пределах нормы, и УЗ-сканирование мозга хотя бы 5-7 дней не выявляет патологии. Но при выявлении очаговых патологических изменений при УЗ-сканировании или ЭЭГ необходимо провести полный курс (21 день).
Другие герпесвирусные энцефалиты. Они менее распространены и чаще всего связаны с иными механизмами, чем прямое внедрение.
• Вирус ветряной оспы. Первичное инфицирование ВОГ (ветряной оспы) может вызвать как постинфекционный энцефалит, обычно мозжечковый энцефалит, так и первичный энцефалит, чаще с более размытым проявлением, возникающим в первые пять дней вместе с высыпанием новых везикулярных элементов. Сообщалось о нескольких случаях раннего преэруп-тивного начала энцефалита (Maguire и Meissner, 1985). Манифестация патологии ЦНС, вызванной ВОГ, также встречается при повторной инфекции ветряной оспы или даже без каких-либо кожных поражений, что более характерно для взрослых или для пациентов с ослабленным иммунитетом (Koskiniemi et al., 2002). Количественный анализ ДНК ВОГ в ликворе показывает повышенные уровни у пациентов с более тяжелым течением заболевания (Aberle et al., 2005). Ветряная оспа может вызывать и синдром Рейе.
Ветряночный церебеллит обычно имеет легкое течение, проявляясь острой атаксией у детей с недавней перенесенной инфекцией в анамнезе и в большинстве случаев с полным выздоровлением через несколько недель. В одном из небольших исследований у некоторых детей с таким постинфекционным состоянием были выявлены высокие титры аутотоантител, реагирующих на ткань мозга или мозжечка (Adams et al., 2000). Лечение ацикловиром (500 мг/м 2 /дозу через каждые 8 часов) может быть эффективным против острого энцефалита, но не требуется при постинфекционном церебеллите.
Диагноз энцефалита, вызванного ВГЧ-6/7, основывается на выделении вируса из ликвора и/или сероконверсии в крови. Эти вирусы имеют отношение также к энцефалитам у у детей с ослабленным иммунитетом.
• Вирус Эпштейна-Барр. Большинство случаев инфицирования ВЭБ на раннем этапе жизни бессимптомно; позднее могут развиваться симптомы инфекционного мононуклеоза. Неврологические проявления инфекции В-клеточным лимфотропным вирусом герпеса встречаются редко, но первичное инфицирование может быть связано с энцефалитическими поражениями (Domachowske et al., 1996; Hung et al., 2000). Другие неврологические проявления включают острый паркинсонизм с последующим полным выздоровлением (Hsieh et al., 2002); энцефалит ствола мозга, имитирующий опухоль (Angelini et al., 2000); и постинфекционные энцефалитные синдромы (Weinberg et al., 2002). Реактивация латентной инфекции ВЭБ также может проявляться в виде неврологического заболевания, и в одном из исследований наблюдалась связь с продолжительными последствиями, включающими гиппокампальный склероз (Hausler et al., 2002).
ДНК вируса может быть амплифицирована из СМЖ в течение острого энцефалита, хотя более высокие уровни ДНК ВЭБ обнаруживаются у пациентов с иммунодефицитом с вызываемой ВЭБ лимфомой ЦНС (Weinberg et al., 2002).
• Цитомегаловирус. Инфицирование плода ЦМВ может привести к тяжелому повреждению ЦНС, тогда как первичная инфекция в детском возрасте обычно имеет бессимптомное течение, хотя в редких случаях возможно заболевание, подобное инфекционному мононуклеозу. Как и при всех других герпесвирусах, первичная инфекция может быть представлена в виде латентной с последующей реактивацией. Она также обычно бессимптомная, исключая хозяев с ослабленным иммунитетом, у которых могут развиваться симптомы сочетанных заболеваний.
Читайте также:

