Лимфогенный путь передачи инфекции это
Обновлено: 23.04.2024
Острые нейроинфекции и их последствия. Инфекционные поражения нервной системы – одна из часто встречающихся форм неврологической патологии, которая составляет не менее 42% всех заболеваний этой сферы.
Нейроинфекция головного мозга классифицируется в зависимости от локализации патологического процесса, исходя из чего, различают:
энцефалит (воспаление ткани головного мозга, обусловленное инфекцией); миелит (воспалительный процесс спинного мозга, вызванный болезнетворными микроорганизмами); арахноидит (инфекционное воспаление затрагивает паутинную мозговую оболочку); менингит (инфекционное воспаление распространяется на оболочки мозга).
Кроме перечисленных видов нейроинфекции, развиваются и комбинированные патологии, например, энцефаломиелит, менингоэнцефалит.
Сочетанные формы инфекции нервной системы диагностировать намного сложней, несмотря даже на то, что в последние годы возможности диагностики нейроинфекций значительно улучшились.
В зависимости от длительности патогенного процесса, различают острое (менингит, энцефалит), подострое и хроническое (арахноидиты, арахноэнцефалиты) течение инфекционного поражения центральной нервной системы.
Основной путь передачи – воздушно — капельный: инфицирование чаще всего происходит при контакте с вирусоносителем, больным человеком, во время его кашля или чихания. Передается инфекция, в том числе, посредством поцелуя, если слюна попала на слизистую оболочку здоровых людей.
Предрасполагающим фактором является наличие эрозий на деснах или их воспаление, а также микроскопические травмы слизистого эпителия полости рта – при актуальности перечисленных обстоятельств, болезнетворному возбудителю будет проще проникнуть в организм и начать циркулировать в нем, развивая инфекцию.
Гематогенный путь инфицирования – не менее распространенный. Патологический процесс переходит на головной и спинной мозг в том случае, когда в организме имеется очаг хронической инфекции, в том числе, поражение сосудов, снабжающих эти важные центры. Такими предрасполагающими патологиями являются отит, абсцесс мозга, тромбоз синусов мозга.
Нейроинфекция развивается, в том числе из-за лимфогенного пути передачи, когда в организме пациента присутствуют скрытые осложнения перенесенных черепно-мозговых и спинномозговых травм. Особенно, если это отягощено ликвореей.
Инфекция не передается контактно-бытовым путем, поэтому, если использовать личные средства и вещи вирусоносителя, заражение не произойдет. Сезонность патологии – жаркое лето – такое условие является наиболее благоприятным для распространения инфекции, поэтому поражению нейроинфекцией больше подвержены населенные места с засушливым, знойным климатом.
Обобщая, следует отметить, что инфекция, поражающая нервную систему, может быть вызвана как вирусной, бактериальной, так и грибковой этиологией.
Причинами нейроинфекции головного мозга являются:
Перенесенные черепно-мозговые травмы (особенно, сопровождающиеся длительной компрессией); переохлаждение (пребывание на воздухе низкой температуры без головного убора); если во время проведения оперативных вмешательств на головном или спинном мозге, использовались медицинские инструменты или расходный материал, некачественного уровня стерилизации; если хирургическое или терапевтическое вмешательство осложнилось нарушением целостности перчаток врача или осуществлялось без их применения; перенесенные вирусные заболевания (чаще – грипп).
Нейроинфекция нередко возникает как внутрибольничное заболевание и может стать следствием посещения стоматолога, который во время работы использовал недостаточно продезинфицированные инструменты.К предрасполагающим факторам относится:
низкий иммунитет (особенно, если у пациента ВИЧ, туберкулез, сифилис или другие заболевания, подрывающие защитные свойства организма); наличие очагов гнойной инфекции (тонзиллит, отит), их скрытое течение или стремительный переход из острой стадии в хроническую форму; игнорирование контрольного обследования после перенесенных заболеваний, а также черепно — или спинномозговых травм.
В неврологической практике встречаются следующие виды инфекции нервной системы.
Менингит — воспаление оболочек головного и/или спинного мозга. Инфицирование происходит гематогенным, лимфогенным или воздушно-капельным путем.
Болезнетворные возбудители – вирусы, бактерии, грибы; предрасполагающими факторами являются наличие (в том числе скрытых) гнойных или воспалительных хронических процессов в пазухах носоглотки или слуховом канале, а также переохлаждение организма.
Симптомы менингита – достаточно специфические: визуализируя их, можно максимально быстро диагностировать этот вид нейроинфекции, приступив к ее лечению.
Наиболее выраженные проявления:
ригидность мышц затылка (пациент не может наклонить голову вперед); интенсивная головная боль, которая всегда сопровождается рвотой (этот симптом вызывает сомнение специалистов относительно того, менингит ли у пациента или же сотрясение мозга – определяющим фактором является анамнез); повышение температуры тела до высокой отметки.
Лечение предполагает постельный режим и антибиотикотерапию лекарственными препаратами антимикробного широкого спектра действия. Прогноз – благоприятный.
Арахноидит — воспалительный процесс, локализация которого – в паутинной оболочке головного мозга. Развитие арахноидита обусловливают перенесенные травмы головы, наличие ревматизма, своевременно не вылеченной ЛОР-инфекции.
Симптомами этого вида нейроинфекции являются:
сильная, устойчивая головная боль, лишающая возможности выполнять даже элементарные действия; ухудшение зрения; слабость; тошнота, приступ которой завершается рвотой; повышение температуры тела; возможно развитие носового кровотечения из-за нарушения мозгового кровообращения; бессонница; в тяжелых случаях – нарушение сознания или его отсутствие.
Прогноз для пациента благоприятный лишь в том случае, когда своевременно установлен диагноз и выполняется лечение. Терапия этой болезни направлена на устранение воспалительного процесса, стабилизацию мозгового кровообращения и общее укрепление организма пациента.
Энцефалит — воспаление ткани головного мозга является следствием клещевого поражения, а также проникновения и воздействия бактерий и вирусов. Если пациент пренебрегает обращением за медицинской помощью – прогноз неблагоприятный и даже летальный. Симптомы этого вида нейроинфекции ярко выражены:
головная боль усиливается в положении лежа, устойчива (плохо и кратковременно купируется анальгетиками); происходит повышение температуры тела; нарастает слабость и чувство разбитости, как проявления общей интоксикации организма.
лазодвигательные расстройства – часть симптомокомплекса, характерного для этого вида нейроинфекции: у пациента формируется птоз (опущение века), ощущение двоения в глазах, общее нарушение зрения.
Диспепсия проявляется тошнотой, которая особенно часто возникает после передвижения транспортом; возникает рвота.
Госпитализация предполагает дальнейшую терапию антибиотиками, гормональными препаратами и общеукрепляющими средствами.
Наиболее информативным видом исследования является МРТ, КТ, а также энцефалограмма. Лабораторная часть диагностики предполагает исследование крови и мочи.
Также проводится анализ спинномозговой жидкости – ликвора, в котором определяется повышенный уровень белка. Каждая из этих диагностических процедур позволяет визуализировать состояние головного и спинного мозга, определить локализацию патогенного процесса, степень инфицирования и вовлечения в воспалительный процесс тканей.
Лечение нейроинфекции сводится к следующему:
Установив диагноз, больного госпитализируют. Выполняется катетеризация вены (устанавливается постоянный внутривенный катетер). Назначается антибиотикотерапия. Антимикробный препарат выбирается врачом с учетом того, какой возбудитель спровоцировал развитие нейроинфекции: только придерживаясь этого, можно рассчитывать на успешность лечения. Антибиотики вводят внутривенно или капельно (посредством инфузий), поскольку это обеспечивает мгновенно попадание лекарственного вещества в кровь, в отличие от выполнения внутримышечных инъекций. Среди часто используемых препаратов – Цефепим, Медаксон, Цефтазидим. Пациенту назначают гормональные препараты – в основном, Преднизолон и Дексаметазон, дозировку которых определяется степенью тяжести пациента и формой патологии. Если нейроинфекция сочетанная, то дозировка гормонального вещества должна быть выше, чем при отдельном инфекционном заболевании нервной системы. Иммунитет пациента поддерживают введением витаминных комплексов. Коррекция уровня артериального давления проводится посредством введения сернокислой магнезии. Для того чтобы снизить степень отека мозга, больному вводят мочегонные средства: Фуросемид, Лазикс. На протяжении всего пребывания пациента в больнице, проводится мониторинг жизненных показателей его организма. Поддержание их на нормальном уровне обеспечивает постоянная инфузионная терапия пациента солевыми растворами и глюкозой. Проводят контроль диуреза больного. В целях профилактики истощения, выполняется парентеральное питание больного; осуществляют гигиенический уход. К наиболее тяжелым последствиям нейроинфекции относится летальный исход; инвалидность; слабоумие. Эти последствия являются веским основанием не откладывать обращение за медицинской помощью, пройти обследование и выполнять все назначения врача.Предупредить развитие нейроинфекции возможно: для этого следует своевременно лечить ЛОР и стоматологические патологии, избегать контакта с инфицированными людьми, надевать голвной убор при низкой температуре воздуха и укреплять иммунитет.Нейроинфекции — что это такое? Каковы причины развития таких заболеваний, эффективные пути лечения? С такими вопросами сталкиваются люди, которые впервые услышали от врача, что у них развивается нейроинфекция.В медицинских справочниках это заболевание трактуется как инфекционное, вызванное грибками, вирусами или бактериями, которое поражает нервную систему, при этом имеет тяжелое течение с высоким процентом смертности.Нейроинфекция включает в себя достаточно большой список заболеваний, многие из которых губительны для головного мозга. Все они могут иметь острую форму течения или переходить в хроническую и протекать достаточно вяло. Как показывает медицинская практика, эти заболевания могут пройти в острой форме один раз и больше не беспокоить больного или иметь частые и яркие рецидивы до конца его дней.Среди всех заболеваний этой группы к острым формам относятся:
Энцефалит — воспаляется вещество головного мозга. Самой частой причиной становится вирус клещевого энцефалита. Менингит — воспаляется оболочка мозга. Здесь может поражаться как головной, так и спинной мозг. Столбняк. Бешенство. Миелит — воспаляется спинной мозг из-за запущенной в нем инфекции. Арахноидит — воспаляется арахноидальная оболочка головного мозга.
К хроническим формам относят:
нейросифилис; нейроСПИД; проказа; поражение нервной системы туберкулезом; нейробруцеллез; бруцеллез.
Независимо от вида и места поражения, нейроинфекция головного и спинного мозга проявляется тремя яркими симптомами:
Общая интоксикация организма. У больного резко поднимается температура тела, очень часто до критических отметок, появляется общая слабость в организме, снижается трудоспособность. Ликворный синдром. В клетках ликворы значительно увеличивается количество белка и клеток, которые превалируют над белками. Симптомы ликворной гипертензии. Больные указывают, что в положении лежа у них значительно усиливается головная боль, особенно в утренние часы, может отмечаться спутанность или рассеянность сознания, бывают случаи тахикардии и пониженного артериального давления.
Миелит. Этот вид нейроинфекций считается одним из самых тяжелых и опасных для человека. При поражении спинного мозга практически всегда остаются серьезные осложнения: гибнут нервные клетки, что приводит к параличу, нарушениям функций кишечника, мочевого пузыря.В качестве лечения будут использоваться препараты группы глюкокортикостероидов и антибиотики широкого спектра действия. Очень важно проходить своевременное лечение в стационаре, чтобы сразу останавливать развитие сопутствующих заболеваний, которые будут активироваться на фоне миелита.Так как практически во всех случаях при миелите наступает паралич, то крайне важно организовать правильный уход за больным и его кожей, использовать средства, которые предотвращают появление пролежней.
У взрослого человека после перенесенных заболеваний остается головная боль, постоянные болевые ощущения в спине, которые усиливаются при изменении погоды. Многие медики также констатируют, что у таких больных после выздоровления ухудшается память, отмечаются проблемы с запоминанием, может нарушаться слух, зрение. Встречаются единичные случаи, когда нейроинфекционное заболевание приводит к полной инвалидизации, человек теряет зрение или слух.
Однако для уточнения диагноза и определения места поражения используют лабораторные и инструментальные методы:
Методы нейровизуализации: компьютерная и магнитно-резонансная томография, позволяют оценить состояние ткани ЦНС, мозговых оболочек. Электроэнцефалография используется для оценки функционирования клеток головного мозга и позволяет выявить распространенность и тяжесть поражения нервной ткани. Электронейромиография применяется для выявления степени тяжести поражения проводящих нервных путей при наличии у пациента парезов или параличей. Люмбальная пункция с последующим анализом спинномозговой жидкости позволяет выявить воспалительный процесс в ЦНС, определить его возбудителей (вирусы или бактерии). Клинический и биохимический анализ крови способствуют выявлению воспалительного процесса в организме. Правильное использование описанных методов совместно со сбором жалоб и проведением неврологического осмотра позволяет ставить верный диагноз и назначить рациональное лечение.
Источники инфекций. Распространение инфекционных болезней
Источники инфекции. Инфекционный процесс может быть вызван как представителями нормальной микрофлоры организма хозяина (эндогенные инфекции), так и микроорганизмами извне (экзогенные инфекции).
Условно-патогенные бактерии нормальной микрофлоры кишечника становятся источниками инфекции только при определённых условиях (например, при перфорации кишечника). Энтеробактерии и неспорообразующие анаэробы (например, Bacteroides fragilis) вызывают внутрибрюшинные абсцессы. При попадании в лёгкие содержимого желудочного и ротоглотки, в котором присутствуют представители нормальной микрофлоры (факультативные и облигатные анаэробы), развивается пневмония или абсцесс лёгкого.
Обитающий на слизистой оболочке передних отделов носовых ходов Staphylococcus aureus может вызвать раневую инфекцию после хирургического вмешательства. Нейтропенический сепсис (бактериемия) возникает, когда бактериям удаётся преодолеть внутренние защитные механизмы слизистой оболочки кишечника или при снижении функции нейтрофилов во время химиотерапевтического лечения лейкемии. Различные изменения в организме хозяина повышают риск развития заболеваний: хирургическое вмешательство и катетеризация сосудов способствуют развитию инфекций, вызываемых представителями нормальной микрофлоры; применение иммунодепрессантов увеличивает риск возникновения оппортунистических инфекций, вызываемых возбудителями с низкой вирулентностью.
Источником экзогенных инфекций могут стать различные животные (зоонозныс инфекции). В этом случае заражение происходит контактно-бытовым и пищевым путями. Кроме того, инфекции могут быть вызваны микроорганизмами, обитающими в окружающей среде (например, Legionella или Clostridium).
Изменение условий окружающей среды ведёт к выраженному повышению риска заражения. Так, распространению зоонозных инфекций способствовало активное развитие сельского хозяйства и земледелия. Например, скармливание крупному рогатому скоту белков животного происхождения привело к возникновению эпидемии губчатой энцефалопатии, которая затем распространилась среди людей (вариантная болезнь Крейцфельдта—Якоба).
Развитие птицеводства способствовало распространению сальмонеллёза (факторы передачи — пух и перо домашней птицы), а механизация пищевой промышленности — повышению риска перекрёстной контаминации. Избежать подобных проблем позволяет совершенствование методов ведения сельского хозяйства и соблюдение санитарно-гигиенических норм.
Недостаточный контроль систем вентиляции в зданиях приводит к возникновению заболеваний, вызываемых Legionella pneumophila.
Сложный жизненный цикл некоторых микроорганизмов помогает им выжить в неблагоприятных условиях и способствует их распространению. Например, возбудители, выделяющиеся из организма хозяина с экскрементами, как правило, передаются посредством фекально-орального механизма. Многие возбудители часть своего жизненного цикла проводят в организме переносчика, и в этом случае заражение происходит во время укуса. Иногда в качестве промежуточного хозяина паразиты могут использовать не животных, а человека (например, при эхинококкозе).

Выживание и распространение возбудителей инфекций
Каждый микроорганизм по-своему приспосабливается к условиям окружающей среды. Так, бактерии способны долгое время выживать в неблагоприятных условиях в виде спор — покоящихся клеток со сниженным метаболизмом, снабжённых твёрдой многослойной оболочкой. Яйца гельминтов также снабжены твёрдой оболочкой, помогающей им выживать в окружающей среде. Распространению возбудителей способствует их длительное персистирование в организме хозяина, который в этом случае становится резервуаром инфекции.
Микроорганизмы, выделяющиеся в окружающую среду при чихании, могут долгое время находиться в воздухе в составе микроскопических капель (5 мкм). Инфекционный процесс возникает при их попадании в лёгкие здорового человека (воздушно-капельный путь передачи). Этим способом происходит распространение как возбудителей респираторных заболеваний (вирусы гриппа и др.), так и микроорганизмов, поражающих другие органы (например, Neisseria meningitides).
Возбудителей желудочно-кишечных расстройств (Salmonella) можно обнаружить в воде и пище (алиментарный путь передачи). Такое распространение инфекции наблюдают при токсоплазмозе и цистицеркозе, поражающих различные органы.
Через неповреждённый кожный покров проникают Leptospira, Treponema и Schistosoma. Передача ВИЧ происходит во время инъекций и переливаний крови (при нарушении кожного барьера). Представители нормальной микрофлоры кожного покрова (Staphylococcus epidermidis) могут проникать в организм через венозный катетер. Переносчиками некоторых инфекций служат насекомые, питающиеся кровью (например, малярию переносят самки комара рода Anopheles).
При половом контакте происходит передача микроорганизмов, не способных к жизни вне организма человека (например, Neisseria gonorrhoeae или Treponema pallidum). При этом заражению способствуют изъязвления слизистой оболочки половых органов.
Факторы распространения инфекций
Улучшение социальной обстановки и условий окружающей среды способствует снижению риска заражения и распространения инфекционных болезней. Например, соблюдение санитарно-гигиенических норм ведёт к уменьшению риска возникновения диареи, а улучшение жилищных условий препятствует распространению туберкулёза. Кроме того, полноценное питание уменьшает восприимчивость человека к инфекционным заболеваниям.
Однако как ни парадоксально, с увеличением уровня жизни возрастает и смертность от некоторых инфекционных заболеваний. Тяжесть осложнений инфекционного процесса прямо пропорциональна возрасту пациента, например при паралитическом полиомиелите или ветряной оспе.
Просвещение населения и распространение инфекций. Существует большое количество программ медицинского просвещения населения, охватывающих такие проблемы, как половое воспитание, рекомендации для беременных, соблюдение правил личной гигиены (гигиенические нормы при приёме пищи, рекомендации для путешественников и др.), использование одноразовых игл и шприцев.
Безопасность пищевых продуктов и распространение инфекций. В Европейском союзе существуют общепринятые стандарты безопасности пищевых продуктов. Контроль за их соблюдением осуществляют специалисты по вопросам гигиены окружающей среды, а также представители Министерства окружающей среды, продовольствия и сельского хозяйства. Пастеризация молока помогает снизить риск возникновения заболеваний, вызываемых Mycobacterium bovis и бактериями рода Campylobacter.
Борьба с переносчиками инфекций. Борьбе с переносчиками инфекций придают огромное значение в регионах, где промежуточными хозяевами возбудителей могут быть насекомые. Лица, посещающие тропические страны, могут существенно снизить риск развития заболевания, приняв меры, предотвращающие нападение и укусы насекомых. Попытки контролировать популяции насекомых с помощью инсектицидов могут быть неудачными вследствие наличия резистентности к этим препаратам.
Профилактика инфекционных заболеваний
Для профилактики некоторых заболеваний (например, дифтерия, менингококковая инфекция) применяют лекарственные препараты. Цель — уничтожение возбудителей заболевания в организме носителя для предупреждения развития острого состояния или распространения инфекции.
Например, для профилактики менингококковой инфекции применяют рифампицин или ципрофлоксацин, приём изониазида рекомендован пациентам с риском обострения туберкулёза при снижении иммунитета.
Значение эпидемиологии в распространении инфекций
Значение организации здравоохранения в распространении инфекционных заболеваний
В большинстве стран существует департамент здравоохранения, занимающийся изучением, профилактикой и лечением инфекционных заболеваний. Обязанности департамента:
• контроль за инфекционной заболеваемостью;
• эпидемиологическое обследование в очаге инфекционного заболевания;
• контроль за вакцинопрофилактикой;
• научные эпидемиологические исследования и обучение медицинского персонала.
Для предотвращения вспышек зоонозных инфекционных заболеваний необходимо тесное сотрудничество между учреждениями (министерствами) пищевой и сельскохозяйственной промышленности и органами санитарно-эпидемиологического надзора. В некоторых странах функции всех этих организаций выполняет одна из них, например Департамент здравоохранения в Великобритании и СДС — Центр по контролю и предупреждению распространения заболеваний — в США. Кроме того, в ведении этих организаций находится решение проблемы биологического терроризма. При этом особую важность приобретает быстрое определение вида возбудителя и своевременное оповещение населения о применении биологического оружия.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
- Вернуться в раздел "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Пути инфицирования позвоночника. Классификация инфекций позвоночника
а) Вопросы лучевой диагностики с позиций анатомии. Возбудители инфекционных заболеваний могут проникать в органы и ткани человека различными путями, в т.ч. путем прямого контакта, лимфогенным путем, гематогенным путем или с током спинномозговой жидкости Контактный путь, как говорит само его название, предполагает прямое соприкосновение кости или мягких тканей с источником инфекции с развитием абсцесса мягких тканей или остеомиелита.
Если вести речь о позвоночнике, то такой путь инфицирования можно видеть, например, при развитии спондилита в области глубокого пролежня. Инфекционное поражение межпозвонкового диска может распространяться на окружающие паравертебральные мягкие ткани и приводить к формированию абсцессов поясничных мышц. Контактный путь также является механизмом развития эпидуральных абсцессов, расположенных краниальней или каудальней уровня поражения межпозвонкового диска. Этот путь инфицирования имеет место и при развитии интрамедуллярных абсцессов спинного мозга, при которых возбудитель проникает в спинной мозг через эпителиальный ход и дефект в задних элементах позвонка.
Лимфогенный путь имеет ограниченное значение, поскольку при инфекционных поражениях позвоночника намного чаще мы видим контактный или гематогенный пути инфицирования. Лимфогенный путь может быть актуален, например, при поражении забрюшинных лимфоузлов при первичных злокачественных новообразованиях брюшной полости и таза.
б) Гематогенный путь инфицирования. Гематогенный путь является одним из самых главных механизмов развития инфекционных поражений костей аксиального скелета. При этом вопрос о том, какой именно гематогенный путь (артериальный или венозный) имеет большее значение, остается спорным. Артериальный путь распространения инфекции в отношении позвоночника традиционно считается более актуальным. В телах позвонков существуют области, с физиологической точки зрения очень похожие на метафизы длинных трубчатых костей. Области эти расположены вблизи передней продольной связки и характеризуются наличием разветвленной сети конечных артериол, которая делает их восприимчивыми к развитию инфекционного процесса.
Дистальные сосуды в этих областях характеризуются отсутствием сети анастомозов и медленным кровотоком, тромбоз их ведет к аваскулярному некрозу кости. Сегментарные артерии обычно кровоснабжают тела двух смежных позвонков и расположенный между ними диск, в связи с чем и картина инфекционного поражения позвоночника бывает достаточно типична. Венозный путь инфицирования традиционно реализуется через сплетение Батсона, представляющее собой продольно ориентированную сеть бесклапанных вен, расположенных параллельно позвоночному столбу. Вены эти располагаются за пределами брюшной или плевральных полостей. Сплетение Батсона сообщается с различными другими венозными системами, в т. ч. с полой веной, системой воротной вены, системой непарной вены, межреберными венами, легочными и почечными венами.
Направление тока крови в сплетении меняется в зависимости от градиента давления в грудной и брюшной полостях. Аналогичную функцию на уровне шейного отдела позвоночника выполняет глоточно-позвоночное сплетение. Непрерывность ликворных пространств полости черепа и дурального мешка обеспечивает возможность прямого распространения возбудителей инфекций или метастазов опухолей стоком ликвора. Внутричерепные новообразования таким образом могут давать отсевы с развитием метастазов в шейном, грудном или поясничном отделах дурального мешка. Точно также новообразования, расположенные в самых дистальных отделах дурального мешка, могут метастазировать с током ликвора в полость черепа.
(Слева) На схеме сагиттального среза показаны признаки инфекционного поражения поясничного межпозвонкового диска с распространением процесса на тела позвонков с развитием спондилита, деструкцией замыкательных пластинок и отеком костного мозга. Отражено формирование дорзального и вентрального абсцессов.
(Справа) Сагиттальный срез, Т1-ВИ FS с КУ, пациент со спондилодисцитом: контрастное усиление сигнала тел L5 и S1 позвонков и межпозвонкового диска, флегмонозные изменения превертебральных и эпидуральных тканей. (Слева) Аксиальный срез, Т1-ВИ с КУ, пациент со спондилодисцитом: распространение инфекционного процесса в превертебральные ткани, поясничные мышцы и дорзальные мышцы позвоночника. Флегмона проникает в вентральный отдел эпидурального пространства и вызывает сдавление дурального мешка.
(Справа) Аксиальный срез, Т2-ВИ FS: распространение воспалительного процесса в превертебральное пространство, на поясничные мышцы и дорзальные мышцы позвоночника. (Слева) Аксиальный срез, Т1-ВИ с КУ: случай диссеминированного кокцидиомикоза с диффузным поражением костной и мягких тканей, распространением процесса в паравертебральные ткани и легкое.
(Справа) Сагиттальный срез, Т2-ВИ: пациенте кокцидиомикозом: массивные паравертебральные абсцессы. Дуральный мешок в спинномозговом канале деформирован за счет пора -жения межпозвонкового диска и тел позвонков.
в) Патологическая лучевая анатомия. Варианты инфекционного поражения позвоночника можно разделить на инфекцию межтелового пространства/остеомиелит позвонков, субдуральную эмпиему, менингит, интрамедуллярный абсцесс спинного мозга и септический артрит/поражение дугоотростчатых суставов. Инфекция межтелового пространства характеризуется типичной картиной снижения интенсивности сигнала в Т1 -режиме в области соответствующего межпозвонкового диска, распространяющейся на смежные замыкательные пластинки. Типичной характеристикой является неровность контура замыкательных пластинок. В Т2-режиме характерна гиперинтенсивность сигнала межпозвонкового диска, не повторяющая анатомию диска и распространяющаяся на смежные тела позвонков. При контрастировании наблюдается неравномерное усиление сигнала межпозвонкового диска и диффузное усиление, распространяющееся на пораженные тела позвонков.
Важным аспектом инфекционного поражения позвоночника является распространение процесса на паравертебральные ткани, признаки чего будут видны в режимах подавления сигнала жировой ткани, постконтрастныхЛ -ВИ, на которых мы ищем признаки контрастного усиления сигнала паравертебральных тканей и поясничных мышц, или Т2-ВИ, характеризующихся усилением Т2-сигнала соответствующих анатомических образований. В протоколе исследования важно описать не только уровень поражения, но также признаки нестабильности или изменения анатомии позвоночника, если таковые имеют место, признаки распространения инфекционного процесса на паравертебральные ткани, эпидуральное пространство и поясничные мышцы.
г) Эпидуральный абсцесс и менингит. Изолированные эпидуральные абсцессы могут возникать и в отсутствии сопутствующей инфекции межпозвонкового диска, а также могут быть связаны с постоянной катетеризацией эпидурального пространства или перенесенным стабилизирующим вмешательством на позвоночнике. Изредка эпидуральный абсцесс может быть следствием гематогенного заноса инфекции. Менингит обычно проявляется на постконтрастных Т1 -ВИ как линейное усиление сигнала вдоль мягкой мозговой оболочки спинного мозга или корешков конского хвоста. При грибковых инфекциях наблюдается узелковый характер усиления сигнала, что напоминает картину метастатического поражения. Субдуральная эмпиема позвоночника встречается редко и может развиваться при тяжелом течении инфекционного процесса межпозвонкового диска с его распространением на эпидуральное пространство. Эмпиема является результатом в первую очередь прямого распространения процесса через твердую мозговую оболочку в субдуральное пространство.
Интрамедуллярные абсцессы спинного мозга встречаются редко и могут возникать как вследствие гематогенного, так и прямого распространения инфекции. У взрослых более типичным механизмом является контактный путь, у детей-также контактный путь через функционирующий эпителиальный ход. Септический артрит/поражение дугоотростчатых суставов может развиваться как вследствие гематогенного, так и контактного распространения инфекции. Ранние стадии инфекционного поражения могут характеризоваться лишь некоторым усилением интенсивности Т2-сигнала субхондральных участков суставных отростков в сочетании с выпотом в полость суставов.
д) Особенности течения инфекционного процесса у взрослых и детей. В силу анатомических особенностей пути распространения инфекции у взрослых и детей отличаются друг от друга. У взрослых в первую очередь поражаются замыкательные пластинки, затем процесс распространяется на межпозвонковый диск, смежные участки тел позвонков, паравертебральные ткани и эпидуральное пространство. У детей через толщу ростковой зоны проходят сосуды, за счет которых первичный очаг инфекционного поражения развивается в межпозвонковом диске с последующим вторичным распространением в тело позвонка. Наиболее частой локализацией инфекции межпозвонкового диска является поясничный отдел позвоночника, за которым следует грудной и шейный отделы. Факторы риска развития инфекции многочисленны и включают возраст старше 50 лет, сахарный диабет, ревматоидный артрит, СПИД, прием глюкокортикоидов, инородные тела мочевыводящих путей, перенесенную травму позвоночника и параплегию. Наиболее распространенной этиологической причиной инфекции является Staphylococcus aureus.
У лиц, употребляющих внутривенные наркотики, возбудителем могут бактерии рода Pseudomonas. Для пациентов с серповидноклеточной анемией классикой считаются поражения, вызванные бактериями рода Salmonella, однако и у них наиболее распространенными остаются стафилококковые поражения.
е) Классификация. Классификация инфекционных поражений костей подразделяет эти поражения на четыре анатомических типа заболевания и три вида ответа организма-хозяина и включает, таким образом, 12 клинических стадий заболевания. Четыре анатомических типа: (1) ранний гематогенный или медуллярный остеомиелит, (2) поверхностный остеомиелит (контактное инфицирование), (3) локальная или полнослойная секвестрация и (4) диффузный остеомиелит. Классификация ответа организма: (А) нормальный физиологический ответ, (В) локальный или системный патологический ответ и (С) лечение остеомиелита будет более тяжелым, чем лечение собственно инфекции.
Классификация туберкулеза позвоночника Mehta (2001) подразделяет заболевания на четыре группы: (1) стабильное поражение передней колонны без кифотической деформации, при котором показан передний дебридмент и костная пластика опорным трансплантатом, (2) тотальное поражение с кифотической деформацией и нестабильностью, показана задняя стабилизация и передняя костная пластика опорным костным трансплантатом, (3) пациенты высокого риска трансторакальных вмешательств, которым показана задняя декомпрессия и стабилизация, (4) изолированные задние поражения, при которых показана задняя декомпрессия.
ж) Клинические вопросы. Инфекционные поражения позвоночника составляют 2-5% всех остеомиелитов. Наиболее распространенным симптомом является боль в спине. Болевой синдром прогрессирует, развиваясь постепенно, он становится постоянным, не уменьшаясь даже в состоянии покоя. Температурная реакция вариабельна и присутствует в
Интрамедуллярные абсцессы оканчиваются фатально в 8% случаев, более, чем у 70% этих пациентов остается стойкий неврологический дефицит. Более, чем у 90% пациентов отмечается повышение СОЭ. Также повышается и уровень С-реактивного белка. Бактериологическое исследование крови оказывается положительным у 25-60% пациентов с остеомиелитом позвоночника.
Показания к хирургической санации очага и спондилодезу при инфекционном поражении позвоночника включают необходимость забора материала для бактериологического исследования, дренирование абсцесса, сохраняющийся неврологический дефицит, деформацию и нестабильность позвоночника, и неэффективность консервативного лечения. Первой линий терапии при условии отсутствия острого или прогрессирующего неврологического дефицита остается продленная внутривенная антибактериальная терапия. Курс внутривенной терапии антибиотиками обычно продолжается 6 недель, по завершении антибактериальная терапия может быть продолжена перорально. Может быть показана наружная иммобилизация позвоночника. Рецидивы инфекции проявляются рецидивирующими эпизодами бактериемии, формированием паравертебральных абсцессов и хронических функционирующих свищей. Наиболее распространенным и благоприятным исходом консервативного лечения является формирование спонтанного костного блока пораженных позвонков.
(Слева) На схеме сагиттального среза показаны эпителиальный ход, соединяющий поверхность кожи с конусом спинного мозга, абсцесс конуса спинного мозга и распространенный отек спинного мозга.
(Справа) Сагиттальный срез, Т2-ВИ: пациент с абсцессом шейного отдела спинного мозга и стрептококковым эндокардитом отмечается диффузное расширение спинного мозга с формированием на уровне С4-С6 в его толще кольцевидной зоны низкоинтенсивного сигнала (капсула абсцесса). (Слева) Сагиттальный срез, Т1-ВИ с КУ и подавлением сигнала жировой ткани: распространенная субдуральная эмпиема с периферическим контрастным усилением сигнала на протяжении всего шейного отдела позвоночника и распространением вдоль поверхности ската.
(Справа) Случай септического артрита дугоотростчатого сустава. Аксиальный срез, Т1-ВИ с КУ на уровне L4-L5: распространение инфекционного процесса на правый дугоотростчатый сустав с диффузным усилением сигнала суставных отростков и поражением околосуставных мягких тканей. (Слева) Аксиальный срез Т1-ВИ с КУ: признаки прямого распространения инфекционного процесса (аневризма аорты на фоне грибкового поражения) от аорты в тело позвонка с формированием зоны деструкции и развитием спондилита. Инфекция также напрямую распространяется на поясничную мышцу.
(Справа) Аксиальный срез с КУ: признаки прямого распространения инфекционного процесса (аневризма аорты на фоне грибкового поражения) от аорты в тело позвонка и на левую поясничную мышцу.
з) Дифференциальный диагноз. Первичным методом диагностики эпидуральных абсцессов является МРТ, чувствительность которой в отношении диагностики инфекционного поражения эпидурального пространства аналогична КТ-миелографии, однако она в то же время позволяет исключить другую патологию, например, грыжу диска, кисту, опухоль и инфаркт спинного мозга. МР-картина эпидурального абсцесса включает мягкотканное образование эпидурального пространства с конусовидными краями, оттесняющее дуральный мешок и спинной мозг. В Т1 -режиме абсцесс характеризуется изоинтенсивностью сигнала, в Т2-режиме — усилением сигнала.
Для полноценного трактования наблюдаемых изменений как признаков эпидурального абсцесса необходимо исследование с контрастированием. Картина контрастного усиления при эпидуральном абсцессе включает: (1) диффузное и гомогенное усиление, (2) неоднородное усиление и (3) тонкий ободок периферического усиления сигнала. Контрастирование является очень полезным дополнительным инструментом исследования, позволяющим оценить протяженность поражения в случаях, когда стандартные режимы МР-томографии оказываются недостаточно информативными. Контрастное усиление сигнала свидетельствует об активности инфекционного процесса и позволяет рационально ограничить зону интереса для последующей игольной биопсии или хирургического вмешательства. Эффективное медикаментозное лечение должно приводить к прогрессирующему снижению выраженности контрастного усиления сигнала паравертебральных мягких тканей, дисков и тел позвонков. На ранних стадиях развития инфекционного процесса, когда межпозвонковые диски еще интактны, только с использованием МРТ инфекционный процесс сложно дифференцировать с опухолевым поражением, дегенеративными изменениями замыкательных пластинок I типа или компрессионным переломом.
Для окончательного определения природы наблюдаемых изменений необходимо исследование в динамике.
Boden et al. предположили, что признаком инфекции позвоночника в послеоперационном периоде будеттриада из контрастного усиления сигнала межпозвонкового диска, контрастного усиления сигнала фиброзного кольца и контрастного усиления сигнала костного мозга позвонков в сочетании с соответствующими лабораторными изменениями, например, увеличением СОЭ. Однако бывают пациенты с неосложненным течением послеоперационного периода и признаками контрастного усиления сигнала фиброзного кольца (в зоне вмешательства), межпозвонкового диска и замыкательных пластинок и без признаков инфекционного поражения. В послеоперационном периоде в норме контрастное усиление сигнала межпозвонкового диска обычно определяется в виде тонких полос, параллельных смежным замыкательным пластинкам, а усиление сигнала костного мозга тел позвонков связано с дегенеративными изменениями замыкательных пластинок I типа.
Подобную МР-картину следует отличать от аморфного усиления сигнала межпозвонкового диска при инфекционном поражении.
и) Список использованной литературы:
1. Duarte RM et al: Spinal infection: state of the art and management algorithm. Eur Spine J. 22(12):2787-99, 2013
2. Malghem J et al: Necrotizing fasciitis: Contribution and limitations of diagnostic imaging. Joint Bone Spine. 80(2): 146-54, 2013
3. Go JL et al: Spine infections. Neuroimaging Clin N Am. 22(4):755-72, 2012
4. DeSanto J et al: Spine infection/inflammation. Radiol Clin North Am. 49(1):105-27,2011
5. Celik AD et al: Spondylodiscitis due to an emergent fungal pathogen: Blastoschizomyces capitatus, a case report and review of the literature. Rheumatol Int. 29(10):1237-41,2009
6. Hong SH et al: MR imaging assessment of the spine: infection or an imitation? Radiographics. 29(2):599-612, 2009
7. Karikari IO et al: Management of a spontaneous spinal epidural abscess: a single-center 10-year experience. Neurosurgery. 65(5):919-23; discussion 923-4, 2009
8. Mylona E et al: Pyogenic vertebral osteomyelitis: a systematic review of clinical characteristics. Semin Arthritis Rheum. 39(1): 10-7, 2009
9. Petruzzi N et al: Recent trends in soft-tissue infection imaging. Semin Nucl Med. 39(2): 115-23, 2009
10. Posacioglu H et al: Rupture of a nonaneurysmal abdominal aorta due to spondylitis. Tex Heart Inst J. 36(1):65-8, 2009
11. Sobottke R et al: Treatment of spondylodiscitis in human immunodeficiency virus-infected patients: a comparison of conservative and operative therapy. Spine (Phila Pa 1976). 34(13):E452-8, 2009
12. Thwaites G et al: British Infection Society guidelines for the diagnosis and treatment of tuberculosis of the central nervous system in adults and children. J Infect. 59(3):167-87, 2009
13. Dai LY et al: Anterior instrumentation for the treatment of pyogenic vertebral osteomyelitis of thoracic and lumbar spine. EurSpineJ. 17(8):1027-34, 2008
14. Mehta JS et al: Tuberculosis of the thoracic spine. A classification based on the selection of surgical strategies. J Bone Joint Surg Br. 83(6):859-63, 2001
15. Mader JT et al: Staging and staging application in osteomyelitis. Clin Infect Dis. 25(6):1303-9, 1997
16. Boden SD et al: Postoperative diskitis: distinguishing early MR imaging findings from normal postoperative disk space changes. Radiology. 184(3):765-71, 1992
Лимфогенные патогенетические процессы легких. Участие лимфатических сосудов в воспалении
При распространении живых патогенных факторов мы различаем главным образом 3 типа лимфогенных патогенетических процессов. Чаще всего они распространяются без ответной реакции лимфатических сосудов на перемещение, сплавливание изолированных микробов, скоплений или эмболов из патогенных факторов с последующим метастазом.
Такие состояния и процессы встречаются при начальных бактериемиях или виремиях многих инфекционных болезней или при заразных заболеваниях. Сравнительно хорошо изученным представителем этого способа распространения является туберкулез.
При другой форме распространения происходит одновременная или самостоятельная воспалительная реакция в лимфатических сосудах, как, например, лимфангит и тромболимфангит. Легочным представителем этого способа распространения является упомянутый туберкулез. Он встречается при стрептококковых процессах туляремии и при других болезнях.
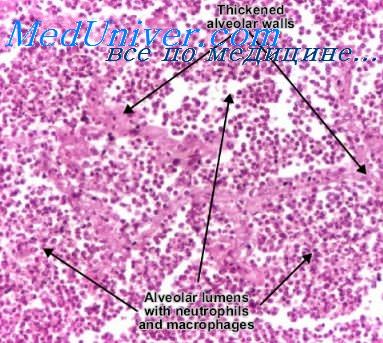
У третьей формы инфильтративный рост протекает в лимфатическом сосуде без первичного участия его эндотелия, это так называемый лимфангиоз (Bingold 1953, Огнев 1953).
Лимфатические сосуды играют важную роль в патогенетических и гигиогенетических процессах при воспалениях легких. Воспалительный отек возникает также вследствие закрытия лимфатических сосудов, сначала в виде спазма. Это до определенной степени целесообразная оборонительная реакция для того, чтобы патогенные микробы и другие токсические вещества останавливались в месте воспаления и не попадали в круг кровообращения. Кроме спазма оттоку препятствуют также фибринозные тромбы в лимфатических капиллярах и сосудах (Менкин 1929, 1931, Foldi 1950, Rusznyak 1955).
При бактериальных, главным образом пневмококковых и очаговых пневмониях можно вначале, благодаря оживленным всасывающим процессам, наблюдать значительное увеличение лимфатических узлов, которое исчезает во время гепатизации. Во время резорбции узлы снова увеличиваются, о чем снова напоминаю в связи со значительностью этого факта.
Эти реакции в лимфатических узлах являются последствиями, а не причиной развития и прогрессирования пневмонических процессов. Некоторое развитие лимфатита и перилимфатита наблюдается и при пневмониях. Иногда это ведет к закрытию лимфатических сосудов. Бесперебойные и безостаточные гигиогенетические процессы возможны также только при совершенной дренажной способности лимфатической системы легких. Приостанавливающие изменения (ретикулоэндотелиальная система), возникающие вследствие первого заражения и вследствие хотя и небольших воспалительных процессов, ограничивают дренажные способности лимфатических сосудов в легких и облегчают укрепление синергических или других патогенных факторов.
В воспаленной области останавливаются не только корпускулярные образования, но и кристаллоиды, и другие вещества (Janeso).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

