Медсестринство в инфекционных болезнях
Обновлено: 16.04.2024
Резюме
Актуальность Эпштейна - Барр вирусной инфекции объясняется широкой циркуляцией вируса Эпштейна - Барр среди детского и взрослого населения, его тропностью к иммунокомпетентным клеткам с пожизненной персистенцией после первичного инфицирования и полиморфизмом клинических проявлений от субклинических форм, инфекционного мононуклеоза до формирования онкологических, аутоиммунных гематологических заболеваний. Персистенция Эпштейна -Барр вируса приводит к подавлению клеточного звена иммунитета, снижению продукции интерферонов и факторов неспецифической защиты, что способствует реактивации персистирующей инфекции, чаще всего без мононуклеозоподобного синдрома, и появлению атипичных мононуклеаров в крови с формированием лимфопролиферативного, интоксикационного, астеновегетативного синдромов, длительного субфебрилитета, что диктует необходимость применения иммунокоррегирующей терапии. В статье приведен клинический случай, в котором изложены описание и анализ течения хронической Эпштейна - Барр вирусной инфекции у ребенка дошкольного возраста (5 лет 8 мес.) с отягощенным преморбидным фоном. Эпизоды реактивации хронической персистирующей инфекции протекали под маской острой респираторной инфекции с лимфопролиферативным синдромом, гнойного тонзиллита, гнойного аденоидита. Терапия, включавшая антибиотики, препараты с противовирусной активностью коротким курсом, бактериальные лизаты, физиотерапию, имела временный и непродолжительный эффект. В силу отсутствия полного мононуклеозоподобного синдрома в клинике и атипичных мононуклеаров в гемограмме обследование на Эпштейна - Барр вирусную инфекцию не проводилось до пятилетнего возраста, в связи с чем она не была верифицирована, и, соответственно, ребенок не получал адекватной иммунотропной терапии. Только в 5 лет 8 мес. при очередном эпизоде активации хронической Эпштейна - Барр вирусной инфекции в состав комплексной терапии был включен меглюмина акридонацетат, на фоне которого была достигнута хорошая клинико-лабораторная динамика. Описанный клинический случай демонстрирует эффективность включения в состав комплексного лечения Эпштейна - Барр вирусной инфекции меглюмина акридонацетата, обладающего противовирусным, иммуномодулирующим и противовоспалительным действиями, что позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем - и астеновегетативного синдрома и достигнуть перехода активной хронической Эпштейна - Барр вирусной инфекции в латентную форму.
Ключевые слова: острая респираторная инфекция, гнойный тонзиллит, гнойный аденоидит, лимфопролиферативный синдром, меглюмина акридонацетат, иммунотропная терапия.
Chronic Epstein-Barr viral infection in children: a clinical case
Svetlana P. Kokoreva, Veronika B. Kotlova®, Oleg A. Razuvaev
Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia
Abstract
The urgency of Epstein-Barr virus infection is explained by wide circulation of Epstein-Barr virus among children and adults, its tropism to immunocompetent cells with lifelong persistence after primary infection and polymorphism of clinical manifestations from subclinical forms, infectious mononucleosis to formation of oncological, autoimmune hematological diseases. Persistence of Epstein - Barr virus leads to suppression of cellular immunity, decreased production of interferons and nonspecific protection factors, which contributes to reactivation of persistent infection, most often without mononucleosis-like syndrome, and the appearance of atypical mononuclears in blood with the formation of lymphoproliferative, intoxication, astheno-vegetative syndrome, long-term subfebrile condition, which dictates the need for immunocorrective therapy. This article presents a clinical case describing and analyzing the course of a chronic Epstein-Barr virus infection in a preschool child (5 years 8 months) with a pre-morbid background. Episodes of reactivation of chronic persistent infection occurred under the mask of acute respiratory infection with lymphoproliferative syndrome, purulent tonsillitis, purulent adenoiditis. Therapy, including antibiotics, short-course antiviral agents, bacterial lysates, and physiotherapy, had a temporary and short-lived effect. meglumine acridonacetate. The described clinical case demonstrates the effectiveness of the inclusion of meglumine acridonacetate, which has antiviral, immunomodulatory and anti-inflammatory effects, in the complex treatment of Epstein-Barr virus infection, This allowed to obtain fairly rapid positive clinical dynamics of relieving intoxication and febrile and lymphoproliferative syndromes in the acute period, and subsequently - astheno-vegetative syndrome and achieve the transition of active chronic Epstein - Barr virus infection into a latent form.
Keywords: acute respiratory infection, purulent tonsillitis, purulent adenoiditis, lymphoproliferative syndrome, meglumine acridonacetate, immunotropic therapy.
Введение
Сегодня Эпштейна - Барр вирусная инфекция (ЭБВИ) представляет собой междисциплинарную проблему и активно изучается не только инфекционистами, но и врачами других специальностей: педиатрами, оториноларингологами, ревматологами, гематологами, онкологами, неврологами, иммунологами. Это объясняется тем, что вирус Эпштейна - Барр (ВЭБ) является одним из наиболее распространенных возбудителей, выявляемых как в детском возрасте, так и среди взрослого населения. По данным различных исследователей, инфицированность ВЭБ составляет 17,7% в периоде новорожденности и возрастает до 90% и выше у лиц старших возрастных групп 1. Являясь оппортунистической инфекцией, она в большинстве случаев протекает бессимптомно. Особенностью манифестных форм ЭБВИ является полиморфизм клинических симптомов, начиная от инфекционного мононуклеоза до фульминантных тяжелейших форм, аутоиммунных и онкологических заболеваний, реализующихся спустя годы после диагностированной ЭБВИ. Доказано, что манифестация клинических проявлений развивается при первичном инфицировании и реактивации персистирующей инфекции 4.
В случае адекватного иммунологического ответа первичное инфицирование приводит к формированию латентной формы инфекции - персистирующей неактивной ЭВБИ. Приравниваясь к здоровому носительству, она является естественным завершением иммунологических изменений. При снижении иммунитета происходит реактивация инфекции с манифестными проявлениями -активация персистирующей инфекции. При тяжелом течении могут формироваться органные поражения: менингоэнцефалит, миокардит, гепатит, гломерулонефрит и другие с возможным летальным исходом 9.
Но чаще в клинической практике встречаются варианты повторной реактивации ЭБВИ с неспецифической симптоматикой, когда при отсутствии остро развившегося полного мононуклеозоподобного синдрома и появления атипичных мононуклеаров в периферической крови, характерных для инфекционного мононуклеоза, возникают утомляемость, слабость, артралгии, головная боль, снижение памяти и внимания, депрессия, субфебрилитет. При этом принято говорить о хронической инфекции, если симптоматика сохраняется в течение полугода. Дети с хронической ЭБВИ имеют, как правило, отягощенный преморбидный фон, страдают хроническим тонзиллитом, хроническим аденоидитом; у них формируются различные варианты лимфопролиферативного синдрома, умеренно выраженный интоксикационный синдром, астенизация, может быть субфебрилитет; у этой категории больных отмечаются частые рекуррентные заболевания, что объясняется иммуносупрессивным воздействием ВЭБ 14.
Изучение форм ЭБВИ стало быстро развиваться благодаря возможностям современной лабораторной диагностики, которая позволяет оценить время инфицирования и активность инфекционного процесса [15, 16]. Для острой первичной инфекции типично появление ДНК вируса в крови и иммуноглобулинов М к капсидному антигену (аVCAJgM) и (или) иммуноглобулинов к раннему ЕА-антигену (аЕАIgG), которые циркулируют с третьей недели инфицирования, а также низкоавидных иммуноглобулинов к капсидному антигену (аVCAIgG). Со временем низкоавидные аVCAIgG трансформируются в высокоавидные, сохраняясь пожизненно. Начиная со второго месяца с момента заражения появляются антитела к ядерному антигену (аEBNAIgG). У части пациентов они сохраняются всю жизнь, у части -элиминируются. Положительный результат исследования полимеразной цепной реакции (ПЦР) крови не позволяет судить о форме инфекции, так как может регистрироваться как при первичном инфицировании, так и при реактивации персистирующей инфекции. На фоне высокоавидных аVCAIgG и (или) аEBNAIgG при реактивации персистирующей инфекции появляются капсидные антитела класса М и (или) ранние антитела. Давность инфицирования вне обострения инфекционного процесса подтверждается обнаружением высокоавидных аVCAIgG и аEBNAIgG. Положительные результаты ПЦР слюны могут быть у 15-25% здоровых серопозитивных людей. Это происходит в силу пожизненной персистенции вируса в В-лимфоцитах, которые, находясь в лимфоидной ткани миндалин при латентной инфекции или ее активации, дают положительный результат исследования [17].
Иммунокорригирующая терапия Эпштейна - Барр вирусной инфекции
На сегодняшний день общепринятых принципов этиотропного лечения ЭБВИ не разработано, так как препараты с противовирусной активностью не позволяют элиминировать возбудитель из организма, и основой лечения является симптоматическая и патогенетическая терапия. Однако длительная персистенция ВЭБ, приводящая к угнетению клеточного иммунитета, факторов неспецифической защиты, интерферон-продуцирующей функции лейкоцитов, свидетельствует о необходимости использования иммунокорригирующих препаратов [18, 23-26].
В педиатрической практике хорошо зарекомендовали себя индукторы эндогенного интерферона, в частности меглюмина акридонацетат (Циклоферон®), которые имеют ряд преимуществ по сравнению с экзогенными интерферонами. При их назначении не вырабатываются аутоантитела на собственный интерферон, время выработки стимулированных эндогенных интерферонов контролируется макроорганизмом, что не приводит к его передозировке. Кроме того, индукторы эндогенного интерферона имеют высокую биодоступность 30. Циклоферон® является низкомолекулярным индуктором интерферона и, соответственно, оказывает противовирусное, иммуномодулирующее, противовоспалительное действия, стимулируя синтез а- и у-интерферона, что способствует усилению Т-клеточного иммунитета - нормализации субпопуляций СD3-лимфоцитов, СD4-лимфо-цитов, NK-клеток и иммунорегуляторного индекса. Прямое действие меглюмина акридонацетата реализуется через нарушение репликации вируса, блокирование вирусной ДНК или РНК, увеличение дефектных вирусных частиц и снижение вирус-индуцированного синтеза белка [32, 33]. Его клиническая эффективность доказана у детей при острой респираторной вирусной инфекции (ОРВИ) и гриппе, так как на ранней стадии инфицирования он подавляет репликацию вируса, стимулирует и поддерживает уровень всех видов интерферона. Из всех индукторов интерферона Циклоферон является самым быстрым, вызывая продукцию интерферона через 2-72 ч после введения, реализуя таким образом противовирусный и иммуномодулирующий эффекты уже через 2-3 ч после приема 34. Наибольшую эффективность у детей препарат имеет при низком интерфероновом статусе 37. Доказано прямое противовирусное действие Циклоферона с подавлением размножения вируса на стадии репликации и вирусного потомства, его способность индуцировать синтез эндогенного интерферона в отношении герпетических вирусов, и показана его клиническая эффективность у детей при различных герпесвирусных инфекциях, в том числе и ЭБВИ 41. В качестве примера успешного использования иммуно-тропной терапии при герпесвирусной инфекции приводим клинической случай течения и исхода хронической ЭБВИ у ребенка дошкольного возраста.
Anamnesis vitae: ребенок от третьей беременности (в семье есть двое детей 8 и 10 лет), протекавшей с угрозой прерывания (терапия дюфастоном) на фоне хронической фетоплацентарной недостаточности, третьих срочных родов путем кесарева сечения. Вес при рождении -3260 г, оценка по Апгар - 7-8 баллов. По поводу конъюгационной гипербилирубинемии была переведена на второй этап выхаживания. С рождения находилась на искусственном вскармливании в связи с гипогалактией у матери. До года наблюдалась неврологом по поводу перинатального поражения нервной системы, профилактические прививки с 12 мес. Из перенесенных заболеваний мама отмечала нетяжелые ОРИ в 1,5 года и острую кишечную инфекцию в 2 года 4 мес.
Предварительный диагноз - острая респираторновирусная инфекция, осложненная аденоидитом. Синусит (?).
Динамика и исходы. В гемограмме лейкоцитоза нет -9,5 х 10 9 /л, абсолютный лимфомоноцитоз (п4%, с28%, л56%, м12%), СОЭ - 18 мм/час. Биохимические тесты без патологических изменений, СРБ - 3 мг (норма - 0-10). При рентгенологическом исследовании придаточных пазух носа данных по синуситу не выявлено. Получен отрицательный результат ПЦР-исследования мазков из носоглотки (респираторный скрин). Лор-врачом диагностирован гнойный аденоидит. По данным ультразвукового исследования органов брюшной полости выявлялись умеренная гепатомегалия, мезентериальная лимфаденопатия.
Терапия в отделении включала антибиотики (цефтриаксон парентерально), Виферон-1 per rectum 2 раза в сутки, симптоматические средства, физиолечение. На фоне проводимого лечения в течение трех суток состояние ребенка оставалось без убедительной клинической динамики: продолжала лихорадить, сохранялись интоксикационный и лимфопролиферативный синдромы. На четвертый день пребывания в стационаре результаты лабораторного обследования: ПЦР+ крови на ВЭБ, аVCAJgM+ и аVCAIgG+ авидность 100%, аEAIgG–, аEBNAIgG+, что позволило диагностировать реактивацию хронической ЭБВИ. К лечению добавлен Циклоферон в таблетках по схеме на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23-е сутки. На третий день у девочки нормализовалась температура, восстановился аппетит, улучшилось самочувствие. Стал менее выраженным лимфопролиферативный синдром: носовое дыхание более свободное, уменьшился насморк. На 10-й день лечения ребенок жалоб не предъявлял. При объективном осмотре меньше выражены гипертрофия небных миндалин 1-й степени, шейная лимфаденопатия (размеры лимфоузлов уменьшились до 0,5 см), гепатомегалия 1,5 см. Выписана с клиническим улучшением с рекомендацией продолжить прием Циклоферона по схеме.
Клинический диагноз - хроническая Эпштейна - Барр вирусная инфекция, реактивация: лимфопролиферативный синдром, обострение хронического аденоидита, астеновегетативный синдром.
При объективном осмотре сохранялась умеренная гипертрофия небных миндалин, пальпировались мелкие, 0,3-0,5 см, безболезненные подчелюстные, передне-и заднешейные лимфоузлы, гепатомегалия отсутствовала, клинических проявлений астеновегетативного синдрома не отмечалось. Гемограмма соответствовала возрастной норме. В лабораторных тестах отсутствовали маркеры активной ЭБВИ: ПЦР крови - ДНК ВЭБ не обнаружено, аVCAJgM отрицательные, аEAIgG отрицательные, обнаружены аVCAIgG с авидностью 100% и аEBNAIgG.
Рисунок. Этапы формирования у пациентки хронической Эпштейна - Барр вирусной инфекции
Figure. Stages of chronic Epstein - Barr virus infection development in a patient
Заключение
Описанный клинический пример демонстрирует течение хронической ЭБВИ у больной в возрасте 5 лет 8 мес. с развитием лимфопролиферативного и астено-вегетативного синдромов. При реактивации хронической ЭБВИ, протекавшей с клиническими проявлениями ОРИ, гнойного тонзиллита, применялись антибиотики, препараты интерферона, глюкокортикостероиды интраназально, физиотерапия с временным эффектом. Назначение Циклоферона в составе комплексного лечения позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем -и астеновегетативного синдрома и достигнуть перехода активной хронической ЭБВИ в латентную форму, что подтверждается отсутствием маркеров активности хронической инфекции в течение года после использования Циклоферона.
Информация об авторах:
Кокорева Светлана Петровна, д.м.н., доцент, заведующая кафедрой инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Котлова Вероника Борисовна, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Разуваев Олег Александрович, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Information about the authors:
Svetlana P. Kokoreva, Dr. Sci. (Med.), Associate Professor, Head of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Veronika B. Kotlova, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Oleg A. Razuvaev, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Особенности течения и терапии респираторного микоплазмоза у детей в эпидемический сезон 2020-2021 гг.
Список литературы
References
Инфекционные болезни характеризуются специфичностью, контагиозностью и цикличностью.
Специфичность инфекции
Каждую инфекционную болезнь вызывает конкретный возбудитель. Однако известны инфекции (например, гнойно-воспалительные процессы), вызываемые различными микробами. С другой стороны, один возбудитель (например, стрептококк) способен вызывать различные поражения.
Контагиозность инфекционного заболевания. Индекс контагиозности инфекции.
Контагиозность (заразительность) определяет способность возбудителя передаваться от одного лица к другому и скорость его распространения в восприимчивой популяции. Для количественной оценки контагиозности предложен индекс контагиозности — процент переболевших лиц в популяции за определённый период (например, заболеваемость гриппом в определённом городе за 1 год).
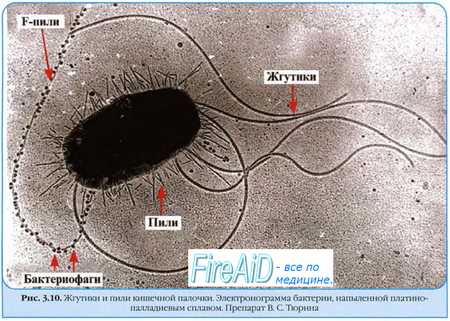
Цикличность инфекционного заболевания
Развитие конкретного инфекционного заболевания ограничено во времени, сопровождается цикличностью процесса и сменой клинических периодов.
Стадии инфекционной болезни. Периоды инфекционной болезни.
Инкубационный период [от лат. incubatio, лежать, спать где-либо]. Обычно между проникновением инфекционного агента в организм и проявлением клинических признаков существует определённый для каждой болезни промежуток времени — инкубационный период, характерный только для экзогенных инфекций. В этот период возбудитель размножается, происходит накопление как возбудителя, так и выделяемых им токсинов до определённой пороговой величины, за которой организм начинает отвечать клинически выраженными реакциями. Продолжительность инкубационного периода может варьировать от часов и суток до нескольких лет.
Период развития болезни. На этой фазе и проявляются черты индивидуальности болезни либо общие для многих инфекционных процессов признаки — лихорадка, воспалительные изменения и др. Б клинически выраженной фазе можно выделить стадии нарастания симптомов (stadium wcrementum), расцвета болезни (stadium acme) и угасания проявлений (stadium decrementum).
Реконвалесценция [от лат. re-, повторность действия, + convalescentia, выздоровление]. Период выздоровления, или реконвалесценции как конечный период инфекционной болезни может быть быстрым (кризис) или медленным (лизис), а также характеризоваться переходом в хроническое состояние. Б благоприятных случаях клинические проявления обычно исчезают быстрее, чем наступает нормализация морфологических нарушений органов и тканей и полное удаление возбудителя из организма. Выздоровление может быть полным либо сопровождаться развитием осложнений (например, со стороны ЦНС, костно-мышечного аппарата или сердечно-сосудистой системы). Период окончательного удаления инфекционного агента может затягиваться и для некоторых инфекций (например, брюшного тифа) может исчисляться неделями.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Огромный экономический ущерб, наносимый внутрибольничными инфекциями обществу, вызывает необходимость большего внимания к этой проблеме.
В нашей стране должности госпитальных эпидемиологов в некоторых многопрофильных стационарах начали вводить давно. Например, в нашей клинической больнице им. С.П. Боткина больничный эпидемиолог периодически работал с 1957 года, а постоянно эта должность введена с 1982 года. На больничных эпидемиологов в то время возлагались функции контроля за соблюдением санитарно-противоэпидемического режима и участие в расследовании специалистами санэпидстанций случаев возникновения внутрибольничных эпидочагов.
В условиях, когда основной планомерной противоэпидемической работой в больницах занимались эпидемиологи санэпидстанций, в функциональные обязанности больничных эпидемиологов входил контроль за работой среднего и младшего медицинского персонала по соблюдению ими санитарных норм, проведением стерилизации и дезинфекции и организация под контролем специалистов санэпидстанций карантинных мероприятий в эпидочагах.
В современных условиях в многопрофильных больницах, которые оснащены сложным и многообразным оборудованием и приборами и где проводятся различные оперативные вмешательства, возросли и требования к профессиональному уровню госпитальных эпидемиологов и их помощников. По нашему опыту и глубокому убеждению, современные госпитальные эпидемиологи должны быть высококвалифицированными врачами-эпидемиологами, а кроме того - иметь особую подготовку и знания клиницистов.
В ряде стран проблемами контроля и профилактики внутрибольничных инфекций занимаются специалисты специально созданных подразделений инфекционного контроля. Так, в США эта работа возложена на комиссию по внутрибольничным инфекциям и госпитальных эпидемиологов - специалистов со средним образованием. Их работа, в основном, ограничивается контролем за проведением медицинским персоналом инвазивных методов лечения, прежде всего в хирургических и урогинекологических отделениях.
В нашей стране ситуация по организации и проведению противоэпидемической работы в больницах изменилась в лучшую сторону после издания приказа Минздравмедпрома РФ № 220 от 17 сентября 1993 года "О мерах по развитию и совершенствованию инфекционной службы в Российской Федерации". В соответствии с этим приказом у руководителей лечебно-профилактических учреждений появилась возможность вводить должности врачей-эпидемиологов и их помощников. Здесь же были приведены основные нормативы для расчета количества должностей врачей и помощников эпидемиологов. Конечно, эти нормативы приблизительные и руководитель каждого учреждения должен исходить из числа больных, профилей отделений, конкретной эпидемиологической ситуации в регионе и др.
В нашей больнице эпидемиологическая служба работает уже третий год. В состав эпидемиологического отдела входит эпидемиологическое отделение (заведующий отделением, 2 врача эпидемиолога, 1 помощник эпидемиолога), дезинфекционное отделение и стерилизационное отделение (ЦСО). Дезинфекционным и стерилизационным отделениями руководят опытные старшие сестры. В целом эту работу возглавляет и направляет заместитель главного врача по санэпидвопросам и инфекционной заболеваемости.
В настоящее время в соответствии с положением об эпидотделе, утвержденным главным врачом больницы, специалисты проводят мероприятия по предупреждению и ликвидации инфекционных и паразитарных заболеваний. Они организовали в больнице полный учет инфекционных заболеваний, эпидемиологическое обследование возникающих в отделениях инфекционных очагов, эвакуацию инфекционных больных в инфекционные отделения или в соответствующие стационары, проведение и контроль за проведением медицинскими работниками отделений текущей и заключительной дезинфекции. Под их контролем находится бельевое хозяйство: организация стирки и дезинфекция нательного и постельного белья, своевременность смены белья. Большое внимание специалисты этого подразделения уделяют санитарно-техническому состоянию и санитарно-гигиеническому содержанию пищеблока. Они следят за сроками реализации готовой пищи, системой раздачи, за наличием в буфетных отделении холодной и горячей воды, оборудованием для подогрева пищи, шкафов для хранения посуды, соблюдением правил мытья столовой и кухонной посуды, за наличием и правильным использованием моющих и дезинфицирующих средств, контролируют и другие вопросы соблюдения противоэпидемического режима.
Самое пристальное внимание этими специалистами уделяется профилактике и предупреждению вспышек внутригоспитальных инфекций и инфекционных заболеваний. Эту проблему мы разделили условно на два раздела: предупреждение заноса и распространения инфекционных заболеваний среди сотрудников больницы и профилактика инфекционных болезней и гнойно-септических (или госпитальных) осложнений среди больных.
Эта работа ведется в соответствии с комплексным планом, в котором проблеме профилактики инфекционных заболеваний и внутрибольничных госпитальных осложнений отведен один из самых больших разделов.
В первую очередь, планируются мероприятия по недопущению заноса и распространения в больнице особо опасных инфекций: холеры, чумы, геморрагических лихорадок и др. Проводятся теоретические и практические занятия с медицинским персоналом по клинике, диагностике, лечению и профилактике этих нозологических форм инфекций с принятием зачетов в отделениях больницы. Вопросы эпидемиологической ситуации в районе, городе, стране и за рубежом обсуждаются на общебольничных и отделенческих врачебных конференциях.
Качество подготовки наших сотрудников и их умение работать в карантинных условиях прошли проверку в 1995 году, когда в больницу поступил тяжелобольной с диагнозом холера. В течение очень короткого времени медицинские работники развернули холерный госпиталь. В этих условиях особенно тяжело приходилось медицинским сестрам, ведь обычно больным с такими заболеваниями требуется тщательный уход и от профессионализма сестер зачастую зависит жизнь пациента.
В нашей больнице разработана и действует целая система профилактики гнойно-септических осложнений. Самое большое внимание в этом разделе уделено лабораторному контролю за проведением стерилизации и дезинфекции операционного и перевязочного материалов, инструментария и приборов для проведения инвазивных методов диагностики и лечения, воздуха и предметов ухода за больными и т.д. Этот контроль организован медицинским персоналом отделений и сотрудниками бактериологической лаборатории. Наших лаборантов-бактериологов хорошо знают во всех отделениях и операционных. Работают они в тесном контакте с эпидемиологическим отделом. Под постоянным контролем специалистов эпидемиологического отдела, главных медицинских сестер больницы, заведующих отделениями, заместителей главного врача находится работа всего медицинского персонала процедурных, перевязочных и операционных сестер, врачей всех специальностей. В процессе работы проводится постоянное обучение медицинского персонала, изучение действующих нормативных документов. Уже подготовлены некоторые адаптированные для нашей больницы инструктивно-методические документы.
Для сравнения, в американских больницах отделы контроля больничных инфекций осуществляют надзор только за осложнениями, связанными с проведением инъекций, оперативными вмешательствами или другими инвазивными методами диагностики или лечения. Проведением мероприятий по профилактике или ликвидации внутрибольничных инфекционных заболеваний, в том числе кишечных заболеваний, дифтерии и других, американцы не занимаются, хотя вспышки таких болезней бывают.
В этом году по инициативе главного врача нашей больницы был введен лабораторный контроль качества проведения генеральных уборок во всех отделениях, в том числе в палатах, буфетных и раздаточных.
Не скроем, что это начинание не сразу нашло отклик среди персонала. Однако результаты такого контроля убедили в необходимости его проведения даже тех, кто вначале категорически возражал. Например, в одном из отделений в 45 % случаев из взятых смывов в буфетной-раздаточной выросли культуры условно-патогенной флоры, что свидетельствует о плохой обработке столовой посуды. Для старшей сестры и заведующего отделением - это сигнал для срочного принятия мер. В другом отделении выросла культура условно-патогенной флоры на ручке вымытого горшка больного. Это говорит о том, что данный предмет не проходил обработку дезсредствами или же его замачивали не полностью, а только чуть-чуть окунули в дезинфицирующий раствор.
Вопросы профилактики внутрибольничных инфекций и гнойно-септических осложнений обсуждаются на больничном медицинском совете и на заседании лечебно-контрольной комиссии. Решения совета и ЛКК выполняются: оборудован кабинет УЗИ для инфекционных больных, приобретено оборудование для проведения гастроскопии и бронхоскопии для инфекционных больных и т.д.
Необходимо отметить особую роль в профилактике внутрибольничных инфекционных заболеваний и гнойно-септических осложнений главных медсестер больницы. Наши главные медицинские сестры прошли путь от рядовых до главных медсестер и знают все тонкости своей профессии. Вместе со специалистами эпидемиологического отдела главные медсестры не только проводят мероприятия по профилактике и недопущению распространения внутрибольничных заражений инфекционными болезнями и гнойно-септических осложнений, но и силами опытных старших медсестер отделений организуют контроль за работой в отделениях круглые сутки.
По инициативе главных медицинских сестер, вопросы профилактики ВБИ и ГСП постоянно выносятся для обсуждения и принятия мер на совещания заведующих и на совет медицинских сестер.
Хорошей литературы по профилактике гнойно-септических инфекций и инфекционных заболеваний пациентов и персонала не так уж много. Мы считаем также очень полезным обсуждение проблемы инфекционного контроля на страницах журнала и приглашаем к участию в нем медицинских сестер и врачей. Расскажите, как обстоит дело у вас.
А. СЕЛЬЦОВСКИЙ, главный врач Московской городской клинической больницы им. С.Л. Боткина,
Е. СЕЛЬКОВА, заместитель главного врача по санэпидвопросам и инфекционной заболеваемости Московской городской клинической больницы им. С.П. Боткина
В начале ХХ века И.И. Мечников высказал предположение о том, что соматические болезни и злокачественные опухоли имеют инфекционную природу. Он писал, что ". со временем, вероятно, удастся открыть паразитов не только при болезнях типично инфекционного характера, но и при болезнях совершенно другого рода" [2, 3] и предсказывал открытие паразитов злокачественных опухолей, а также микробов-возбудителей сахарной болезни. Гипотеза И.И. Мечникова получила серьезное подтверждение и в настоящее время список соматических и онкологических заболеваний, ассоциируемых с инфекционными возбудителями, достаточно велик. Для подтверждения гипотезы используют большой набор методов: эпидемиологические наблюдения, серологические исследования и обнаружение антигена бактерий или вирусов; выделение чистой культуры конкретного микроорганизма из органа-мишени, а также воспроизведение некоторых видов соматической патологии (миокардит, диабет) при заражении лабораторных животных.
Следует подчеркнуть, что до настоящего времени вывод об участии конкретного микроорганизма в развитии той или иной патологии базируется, как правило, на выявлении одного, реже двух признаков триады Кохаii, поэтому имеют в виду не этиологическую роль микроорганизма, а его ассоциацию с рассматриваемым заболеванием.
В табл.1 суммированы данные, свидетельствующие об ассоциации социально-значимых болезней сердечно-сосудистой и желудочно-кишечной систем человека, а также инсулинзависимого диабета с рядом широко распространенных инфекционных возбудителей.
Инфаркты, инсульты. На большом эпидемиологическом материале специалистами из разных стран продемонстрировано, что в период сезонного подъема гриппа увеличивается число госпитализированных с обострениями сердечно-сосудистых заболеваний и нарушениями мозгового кровообращения. Возрастает в этот период и летальность (см. ниже статью Б.Ф. Семенова и В.И. Покровского).
Миокардиты. В пораженной ткани сердца выявлен вирус Коксаки В и его антигены [9]. В экспериментах на мышах продемонстрирована способность вируса Коксаки В вызывать поражение мышцы сердца.
Атеросклероз. В атеросклеротических бляшках коронарных сосудов и аорты человека обнаружено присутствие бактерий Chlamydia pneumoniae [9].
Язва желудка, язва двенадцатиперстной кишки, гастрит. Чистые культуры Helicobacter pylori изолировали в 50% случаев при обследовании пациентов с гастритом, у 70-90% больных с язвой желудка и у 95% лиц, страдающих язвой двенадцатиперстной кишки [9].
Диабет I типа. Это заболевание связывают с инфекциями, вызываемыми представителями 6 семейств вирусов: Paramyxoviridae (вирус паротита), Picornaviridae (вирус Коксаки В), Retroviridae (ретровирус), Togaviridae (вирус краснухи), Reoviridae (ротавирус), Herpesviridae (цитомегаловирус, вирус Эпштейна-Барр) [5,6]. Наиболее интересные данные получены при изучении роли вирусов паротита, краснухи и Коксаки В.
Связь диабета с вирусом паротита была продемонстрирована более 20 лет тому назад с помощью эпидемиологических методов.
Развитие инсулинзависимого диабета при краснухе происходит после заражения плода в последнем триместре беременности. Установлено, что у 10-20% пациентов с синдромом врожденной краснухи в возрасте 5-20 лет развиваются нарушения углеводного обмена. Эти цифры существенно больше, чем показатели популяции в целом [8].
Ассоциацию инфекции вирусом Коксаки В с ранними этапами развития диабета доказывают результаты эпидемиологических наблюдений, находки вирусного антигена в поджелудочной железе и изоляции вируса из этой железы [5, 6, 10]. Описано выделение вируса из кала больной диабетом, у которой симптомы патологии обмена развились через 10 дней после Коксаки-вирусной инфекции [5]. После инокуляции этого штамма у лабораторных животных наблюдали развитие диабета. В многочисленных исследованиях продемонстрировано, что инфекция человека ретровирусами, ротавирусами, цитомегаловирусом и вирусом Эпштейна-Барр, как правило, сопровождается формированием аутоантител к клеткам поджелудочной железы [5]. Эти аутоантитела рассматривают в качестве одного из ведущих механизмов развития инсулинзависимого диабета [5, 6].
В табл. 2 суммированы современные данные, свидетельствующие о том, что в большом проценте случаев опухоли желудка, наружных половых органов и печени ассоциированы с бактериями или вирусами. H. pylori обнаруживают у 55% пациентов с аденокарциномой и лимфомой желудка. Вирус папилломы выделяют в новообразованиях половых органов у 65% пациентов из развитых и 87% больных из развивающихся стран. Развитие гепатокарциномы в 73% случаев связывают с инфекцией вирусом гепатита В, а в 27% - с заражением вирусом гепатита С. Патогенез соматических или онкологических заболеваний, ассоциированных с микроорганизмами, изучен недостаточно. Обсуждается несколько вариантов событий.
- Микроорганизм нарушает функцию органа-мишени, разрушая зараженные клетки. Эксперименты с культурами клеток in vitro позволяют думать о таком механизме действия вирусов паротита, краснухи и Коксаки В. Описано несколько случаев выделения последнего из поджелудочной железы пациентов с диабетом I типа [5, 6].
- Патоген запускает первые этапы патологического процесса, затем исчезает из организма. В дальнейшем процесс развивается самостоятельно. Такую гипотезу предложил Л.А. Зильбер при построении вирусной теории происхождения опухолей [1].
- Микроорганизм действует как кофактор, усиливая эффекты субпороговых доз других факторов. В качестве примера рассматривают развитие злокачественного процесса при взаимодействии вируса папилломы человека, никотина, оральных противозачаточных препаратов при дефиците витаминов А и С у людей с определенным генетическим статусом [5, 6, 9].
- Ассоциированный возбудитель запускает аутоиммунный процесс, направленный против клеток органа-мишени. Наиболее подробно описаны аутоиммунные события при инсулинзависимом диабете, ассоциированным с вирусами [5]. Практически во всех случаях у пациентов с такой патологией выявляют аутоантитела и аутореактивные Т-лимфоциты, направленные против b-клеток поджелудочной железы. При наличии симптомов диабета у пациентов с синдромом врожденной краснухи аутоантитела обнаруживают у 50-80% обследованных при 20% в контроле.
Очевидно, что при развитии соматического или злокачественного процесса, ассоциированного с микроорганизмом, действует несколько повреждающих механизмов, которые обусловлены этим патогеном. При этом большую роль играет генетическая предрасположенность организма, что хорошо продемонстрировано на примере диабета I типа и папилломатоза наружных половых органов [9]. Имеют значение и свойства микрорганизма. Изучение роли вируса Коксаки В показало, что лишь немногие штаммы этого возбудителя обладают диабетогенной активностью [5,6].
В настоящее время гипотеза об ассоциации соматических и злокачественных микроорганизмов является общепризнанной. Следует ожидать, что список таких ассоциаций будет увеличиваться.
Главным следствием рассмотренной гипотезы является предложение использовать существующие вакцины не только для профилактики конкретных заболеваний, но и для предупреждения ассоциируемой с этой инфекцией соматической или злокачественной патологии.
Читайте также:

