Менингит у новорожденных кишечная палочка
Обновлено: 24.04.2024
Эшерихиозный менингит - это вторичный гнойный менингит, развивается преимущественно у ново¬рожденных или детей первых месяцев жизни как осложнение генерализованной (септической) формы эшерихиоза. Характеризуется тяжелым течением, выраженной интоксикацией, общемозговой симптоматикой, менингеальным синдромом и высокой летальностью.
Что провоцирует / Причины Эшерихиозного менингита:
Возбудители заболевания - E. сoli, представляющие собой прямые палочковидные грамотрицательные бактерии размером 1,1–1,5 на 2,0–6,0 мкм, у большинства штаммов имеется капсула. Среди эшерихий есть подвижные и неподвижные штаммы, склонные к полиморфизму. Благодаря наличию ворсинок, содержащих фибрин и пили, эшерихии обладают способностью к адгезии и последующей колонизации. Растут на обычных питательных средах, являются факультативными анаэробами. Дифференцирование между патогенными и непатогенными штаммами эшерихий, имеющими сложную антигенную структуру, основано на различиях в структуре поверхностных антигенов: липополисахаридных (О), жгутиковых (Н) и капсульных (К). В настоящее время известно более 160 серотипов. Неоднородность эшерихий, разнообразие клинической симптоматики привели к делению патогенных эшерихий на 5 групп: энтеропатогенные (ЭПКП), энтеротоксигенные (ЭТКП), энтероинвазивные (ЭИКП), энтерогеморрагические (ЭГКП), энтероадгезивные (ЭАКП), из которых менингиты вызывают эшерихии первой группы - ЭПКП.
Механизм заражения эшерихиозом - фекально-оральный. Инфекция передается пищевым путем, а в закрытых коллективах большое значение может иметь контактный путь передачи. У новорожденных детей возможен эндогенный путь заражения с последующей гематогенной диссеминацией. Эшерихиозный менингит чаще вызывают серотипы патогенной кишечной палочки: 01, 06, 07, 016, 018, 083, К1. Предрасполагающими факторами являются: родовая черепно-мозговая травма, недоношенность, предшествующие инфекционные или соматические заболевания, пре- или интранатальная инфекция у матери. Основную группу риска по заболеванию эшерихиозным менингитом составляют новорожденные дети, чаще мальчики, с пониженной массой тела (ниже 2500 г). Однако не всегда удается установить путь инфицирования при развитии менингита. Чаще менингит развивается на фоне кишечной инфекции, но возможен и пупочный путь инфицирования с гематогенным распространением инфекции. В любом случае эшерихиозные менингиты являются осложнениями бактериемии и развиваются у 10–40 % новорожденных, больных эшерихиозом.
Патогенез (что происходит?) во время Эшерихиозного менингита:
Инфекция попадает в организм через рот. ЭПКП почти без потерь достигают тонкой кишки, где на поверхности энтероцитов происходит их колонизация и размножение. Наиболее цитотоксичные из них способны транспортироваться фагосомноподобными вакуолями через эпителиальную клетку в подлежащую ткань и далее в кровь, приводя к транзиторной бактериемии и сепсису (В.И. Покровский, 1989). Этому процессу способствует, помимо цитотоксичности эшерихий, анатомо-физиологическое несовершенство желудочно-кишечного тракта, повышенная проницаемость клеточных и сосудистых мембран и ГЭБ. Образующиеся при гибели эшерихий эндотоксины, продукты их метаболизма, биологически активные вещества усугубляют этот процесс и делают возможным проникновение ЭПКП через ГЭБ с поражением мозговых оболочек и вещества мозга.
Симптомы Эшерихиозного менингита:
Течение эшерихиозного менингита тяжелое, с высокой летальностью: у новорожденных, родившихся от физиологических родов, она достигает 12 %, у относящихся к группе риска - до 35 %. У 20–50 % больных, выживших после эшерихиозного менингита, сохранялись стойкие неврологические расстройства.
Диагностика Эшерихиозного менингита:
Основные диагностические критерии эшерихиозного менингита
1. Эпиданамнез: менингит развивается на фоне эшерихиозной инфекции, преимущественно болеют новорожденные и дети первых месяцев жизни с неблагоприятным преморбидным фоном, наличием пре- или интранатальной инфекции у матери.
2. Начало менингита острое, с развитием выраженного инфекционно-токсического синдрома и последующим присоединением менингеального синдрома.
3. Течение менингита может сопровождаться ликворной гипотензией.
4. Характерно наличие других гнойных очагов инфекции - отита, пневмонии, энтерита, пиелонефрита и др.
Бактериологическое выделение различных серотипов энтеропатогенной кишечной палочки из цереброспинальной жидкости изолированно или в ассоциации с другими возбудителями подтверждает этиологический диагноз.
Лабораторная диагностика
Общий анализ крови. В периферической крови обнаруживают лейкоцитоз, нейтрофилез со сдвигом влево, повышенную СОЭ.
Исследование ликвора. В цереброспинальной жидкости выявляются умеренный плеоцитоз нейтрофильного характера, высокое содержание белка, снижение концентрации глюкозы.
Бактериологическое исследование. Отличительной особенностью выделения возбудителя является то, что бактериологический анализ основан на определении антигенных свойств, а не на изучении биохимических признаков. Бактериологическому исследованию подвергают кровь, ликвор, кал, пупочное отделяемое. Посев производят на селективно-дифференцирующие среды (Плоскирева, Левина, Эндо, агар Аселя - Либермана).
При бактериологическом исследовании цереброспинальной жидкости выделяют патогенную кишечную палочку, устойчивую к большинству антибиотиков. Кроме того, в цереброспинальной жидкости часто обнаруживаются ассоциации кишечной палочки с другими возбудителями: стафилококком, микоплазмой, различными серотипами вируса гриппа.
Лечение Эшерихиозного менингита:
При подозрении на менингит необходима срочная госпитализация ребенка в специализированный стационар. При нарушениях сознания и дыхания транспортировку больного осуществляет реанимационная бригада. В стационаре проводят комплексное лечение, включающее охранительный режим, рациональное питание, этиотропную, патогенетическую и симптоматическую терапию. В остром периоде болезни необходимо соблюдение постельного режима. После проведения люмбальной пункции в течение 3 дней показан строгий постельный режим с укладкой на щите для профилактики постпункциональных осложнений.
Диета полноценная, высококалорийная, механически и химически щадящая. Детям первого года жизни проводят кормление сцеженным грудным молоком или адаптированными смесями с сохранением физиологического режима питания.
Выбор антибактериальных средств определяется этиологией менингита и проходимостью препарата через гемато-энцефалический барьер. Для стартовой антибактериальной терапии выбирают: левомицетина сукцинит в дозе 80 - 100 мг/кг/сутки внутримышечно или внутривенно с интервалом в 6 часов; бензилпенициллина натриевую соль в дозе 300 тыс. ЕД/кг/сутки внутримышечно или внутривенно с интервалом 4 ч. После бактериологического выделения, био- и серотипирования возбудителя проводят коррекцию антибактериальной терапии в соответствии с чувствительностью выделенного штамма. Препаратами резерва являются цефалоспорины III - IV поколений. Длительность антибактериальной терапии составляет не менее 10 - 14 дней. Показаниями к отмене антибиотиков являются: исчезновение симптомов интоксикации, стойкая нормализация температуры тела, восстановление формулы крови, санация ликвора (количество клеток не более 30 в 1 мкл, 70 % из них - лимфоциты).
С целью профилактики кандидоза при массивной и длительной антибактериальной терапии показано назначение нистатина, дифлюкана, амфитерицина Б (фунгизона).
Противовирусная терапия включает: препараты, нарушающие сборку нуклеиновых кислот вирусов; рекомбинантные интерфероны; индукторы эндогенного интерферона и иммуномодуляторы.
С иммуностимулирующей и заместительной целью применяют иммуноглобулины для внутривенного введения (эндобулин, сандоглобулин, пентаглобин) или специфические иммуноглобулины (против вируса клещевого энцефалита, противостафилококковый и др.).
Патогенетическая терапия направлена на борьбу с интоксикацией, на нормализацию внутричерепного давления и церебральной гемодинамики. При проведении дезинтоксикации необходимо обеспечить введение жидкости с учетом физиологической потребности и электролитного баланса. Введение жидкости осуществляется путем оральной регидратации (чай, 5 % раствор глюкозы, морс) или внутривенной инфузии. Для парентерального введения используют глюкозо-солевые (10 % глюкоза, 0,9 % NaCl, Рингера) и коллоидные (реополиглюкин, реомакродекс, гемодез) растворы в соотношении 3:1.
Одновременно назначают дегидратационную терапию (объем определяется степенью внутричерепного давления). В качестве стартового препарата в 1 - 2 сутки заболевания используют лазикс в дозе 1 - 2 мг/кг/сутки. Мочегонный эффект препарата начинается через 3 - 5 мин, достигает максимума через 30 мин и длится 1,5 - 3 часа.
Для улучшения кровоснабжения мозга и профилактики ишемии мозговой ткани используют сосудистые средства - трентал, кавинтон. Уменьшение энергодефицита нейронов и восстановление межнейрональных связей достигается применением препаратов ноотропного ряда (пирацетама, пантогама, перидитола) и вазоактивных нейрометаболитов (актовегина, инстенона). Длительность курса - до 6 мес. В тяжелых случаях ослабленным детям вводят лейковзвесь, свежезамороженную плазму; проводят сеансы УФО крови.
Основой комплексной интенсивной терапии отека-набухания головного мозга является адекватная респираторная поддержка (увлажненный кислород, эндотрахеальная интубация, ИВЛ), направленная на коррекцию кислотно-основного состояния и снижение выхода плазмы в периваскулярное пространство.
Широкое распространение получили осмодиуретики, действие которых основано на создании осмотического градиента между плазмой и мозговой тканью. С этой целью используют 15 % раствор манитола внутривенно (из расчета 0,5 - 1,0 г сухого вещества на 1 кг массы тела). Мочегонный эффект начинается через несколько минут и достигает максимума через 2 - 3 часа. Вследствие повреждения гематоэнцефалического барьера может возникнуть синдром "отдачи" - перемещение осмотически активного вещества из сосудистого русла в ткань мозга и усиление отёка. Для предупреждения данного состояния через 2 часа после начала введения манитола вводят лазикс.
К каким докторам следует обращаться если у Вас Эшерихиозный менингит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Эшерихиозного менингита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Менингит, вызванный кишечной палочкой. Лечение гнойных менингитов
Это одна из наиболее частых форм гнойных менингитов, наблюдаемых в последние годы у новорожденных детей. Менингит обычно носит вторичный характер. Развивается на фоне кишечной инфекции или сепсиса.
Заражение кишечной палочкой возможно во внутриутробный период. Заболевание почек и мочевыводящих путей у беременных в 60—70% случаев вызывается грамотрицательными возбудителями, в том числе кишечной палочкой. При восходящем распространении инфекции кишечная палочка попадает в амниотпческую жидкость, которая является хорошей питательной средой. Инфицирование околоплодных вод приводит к развитию хориоиамнионитов. В этом случае бактерии попадают к плоду через сосуды плаценты и пуповины. Возможны также заглатывание и аспирация околоплодных вод.
Состояние детей обычно тяжелое уже в первые дни после рождения. Они вялые, заторможенные, отказываются от груди. Наблюдаются срыгивания, рвота, частый, жидкий стул. Быстро нарастают признаки эксикоза. Кожные покровы бледные, с сероватым оттенком, сухие; большой родничок запавший. Дыхание стонущее, частое, поверхностное. Дети теряют в массе. Резко снижен тургор тканей. Развивается гипотрофия. Наблюдаются локальные или генерализованные клонико-тонические судороги. Специфические менингеальные симптомы отсутствуют.
Течение менингита тяжелое, часто с летальным исходом. Диагноз таких форм менингита у новорожденных представляет трудности, поскольку подобная клиническая симптоматика может быть расценена как проявление кишечной инфекции, сепсиса или внутричерепной родовой травмы. Тяжелое состояние новорожденных с указанием на возможность септического процесса является показанием для люмбальной пункции.
Спинномозговая жидкость вытекает редкими каплями, гнойная; иногда ее даже не удается получить из-за низкого давления. Содержание белка высокое (7—33 г/л), нейтрофильный цитоз. Возбудитель может быть выделен из крови и ликвора.
Течение гнойных менингитов. При своевременной и рациональной терапии на 3—4-й день болезни состояние больных значительно улучшается. Санация ликвора происходит на 8—15-й день болезни. При благоприятном течении через 2 нед после окончания курса лечения детей выписывают из стационара под наблюдение районного невропатолога. В этих случаях обычно отмечаются негрубо выраженные остаточные явления в виде повышенной истощаемости и возбудимости нервной системы, нарушения концентрации внимания, легких очаговых симптомов, гипертензионно-гидроцефального синдрома. При позднем диагнозе и неправильно проводимой терапии возможно затяжное течение.
Оно может быть связано и с характером возбудителя. При менингитах, вызванных стафилококком, кишечной палочкой, длительное течение заболевания обусловлено склонностью к абсцедированию и наличием гнойного очага в организме. При затяжном течении в оболочках преобладает продуктивный процесс, который приводит в дальнейшем к нарушению секреции, реабсорбции и циркуляции ликвора и развитию гидроцефалии. Гидроцефалия наиболее часто наблюдается после менингитов у новорожденных и грудных детей.
Одним из осложнений менингита является эпендиматит. Он чаще всего возникает при поздно начатой терапии. У больного на фоне улучшения состояния появляются тонические судороги, повышается мышечный тонус в экстензорных группах мышц, развивается поза децеребрационной ригидности. Дети теряют сознание. Прогрессирует гидроцефалия. Течение эпендиматитов неблагоприятное.
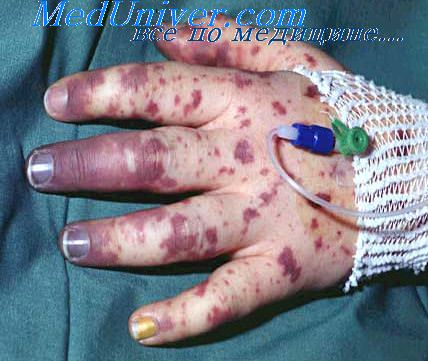
К другим осложнениям гнойного менингита, наблюдаемым у детей раннего возраста, относят абсцесс мозга, тромбоз латерального синуса, субдуральный выпот, локальные некрозы тканей в местах сливной геморрагической сыпи, вторичные инфекции дыхательных и мочевыводящих путей, образование множественных пристеночных бактериальных тромбов (рассеянная внутрисосудистая коагуляция). У 20% детей, перенесших гнойный менингит, в дальнейшем имеются признаки очагового поражения нервной системы: эпилептиформные судороги, поражение III, VI, VII, VIII пар черепномозговых нервов, пирамидная недостаточность, вегетативно-обменные расстройства и др.
Лечение гнойных менингитов должно быть начато как можно раньше. От этого зависят исход заболевания и характер остаточных явлений. Антибактериальную терапию следует назначать до получения результатов исследования ликвора, при малейшем подозрении на менингит. Ургентную антибактериальную терапию (до выделения возбудителя) начинают с назначения пенициллина, так как 90% гнойных менингитов вызывается кокками, высокочувствительными к пенициллину. Пенициллин назначают в больших дозах — 200 000—500 000 ЕД на 1 кг массы тела в сутки, в тяжелых случаях — 1 000 000 ЕД на 1 кг массы тела. Инъекции детям первых месяцев жизни делают каждые 2—3 ч, после 1 года — каждые 4 ч.
После установления характера возбудителя назначают антибиотики, к которым он наиболее чувствителен. При менингококковом менингите продолжают лечение пенициллином либо назначают полусинтетические пенициллины. Из них наиболее эффективен ампициллин. Детям до 2 мес его назначают в дозе 100—150 мг на 1 кг массы в сутки внутримышечно или внутривенно, старше 2 мес — 150—200 мг на 1 кг в сутки. Инъекции Делают с интервалом в 6 ч. Оксациллин и метициллин назначают из расчета 200—300 мг/кг в сутки внутримышечно каждые 4 ч. Полусинтетические пенициллины назначают больным с повышенной чувствительностью к пенициллину. Они эффективны также при стафилококковом менингите, особенно метициллин.
При стафилококковом менингите рекомендуется определить чувствительность возбудителя к антибиотикам. До получения этих данных целесообразно комбинировать 2 или 3 антибиотика (пенициллин — левомицетин, пенициллин — полусинтетические пенициллины). Если менингит вызван пневмококком, то назначают большие дозы пенициллина — до 1 000 000 ЕД/кг в сутки. Можно применить также сигмамицин — 50 000—100 000 ЕД/кг в сутки внутривенно через 12 ч или внутримышечно через 6 ч. Эффективно также применение гентамицина — 6—8 мг/кг в сутки внутримышечно через 8 ч.
При менингите, вызванном кишечной палочкой, назначают гентамицин или ампициллин в вышеуказанных дозах. Для профилактики кандидамикоза рекомендуется нистатин по 100 000 ЕД 3—4 раза в день.
Длительность лечения антибиотиками новорожденных и грудных детей составляет минимум 3 нед, более старших детей следует лечить до тех пор, пока не нормализовалась температура, и еще 5 дней. Контролем за лечением могут служить показатели спинномозговой жидкости: отсутствие возбудителя, цитоз — менее 30 клеток, нормализация концентрации глюкозы и уровня белка. Контрольную пункцию делают через 3—4 дня от начала лечения. Если тенденция к санации ликвора отсутствует, антибиотик следует заменить.
Курс лечения при менингококковом менингите в среднем составляет 6—8 дней, при менингитах другой этиологии — от 8 до 12 дней. Дозу антибиотиков в процессе лечения недопустимо снижать, так как по мере лечения проходимость гематоэнцефалического барьера для антибиотиков уменьшается.
В редких случаях, когда указанное выше лечение не дает желаемого эффекта, можно прибегнуть к введению антибиотиков под оболочки мозга или в желудочки. Чаще всего к этой мере приходится прибегать при менингите у новорожденных, вызванном грамотрицательными микроорганизмами.
Наряду с антибиотиками необходимо проводить симптоматическую и десенсибилизующую терапию, а также мероприятия, направленные на стабилизацию кровообращения и нормализацию электролитного баланса, борьбу с отеком мозга, лечение дыхательных нарушений, нормализацию кислотно-щелочного равновесия. При наличии судорог назначают противосудорожную терапию, при гипертермии — различные виды охлаждения (обтирание спиртом, клизма из холодной воды, литические смеси), жаропонижающие средства. При молниеносной форме менингита с развитием шокового состояния показано применение кортикостероидов: гидрокортизон (5—30 мг/кг), преднизолон (1—5 мг/кг) в зависимости от степени коллапса.
Большое значение при лечении менингитов имеют полноценное питание, введение витаминов, тщательное проветривание помещения и уход за больным ребенком.
Инфекционные осложнения (абсцесс мозга, субдуральный выпот) требуют специфической антибактериальной терапии и хирургического лечения. При рассеянной внутрисосудистой коагуляции проводят коррекцию коагулограммы путем возмещения расхода факторов свертываемости.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Острый бактериальный менингит у новорожденного и детей: причины, клиника, диагностика
Каждый год более 1,2 миллиона людей заболевают острым бактериальным менингитом, причем более чем 170 тысяч случаев имеют летальный исход, большинство из которых приходится на детский возраст (ВОЗ, 1998,2008). Несмотря на новые антибиотики и лечение, смертность за последние 20 лет по существу осталась неизменной. Среди выживших, примерно у половины имеются неврологические или другие осложнения после заболевания. Несколько факторов способствует этой неутешительной ситуации: отсроченная постановка диагноза из-за неспецифического характера симптомов, появление устойчивых штаммов болезнетворных микроорганизмов, слабость иммунологической защиты новорожденных детей, и отсутствие возможности предотвратить ущерб от воспалительного ответа хозяина посредством добавочных нейропротекторных или противовоспалительных механизмов.
а) Эпидемиология. Относительная заболеваемость острым бактериальным менингитом изменяется соответственно возрасту, социальным условиям жизни, географическому местоположению и политике иммунизации. В развитых странах за прошлое десятилетие эпидемиология острого бактериального менингита претерпела разительную перемену, и уровень заболеваемости снизился приблизительно до 4-5 случаев на 100000 населения, тогда как во многих развивающихся странах он остается высоким в пределах 40-50 случаев на 100000.
Вакцинация вызвала радикальное изменение в относительной частоте трех основных патогенных микроорганизмов — Haemophilus influenzae, Neisseria meningitidis и Streptococcus pneumoniae. H. influenzae тип В (HiB) был наиболее распространенным возбудителем детского бактериального менингита в Великобритании, с показателями заболеваемости в пределах 21-44 на 100000 среди детей до пяти лет, с пиковым возрастом 6-7 месяцев и коэффициентами смертности 2,4-4,3% (Вооу и Мохon, 1993; Вооу et al., 1993; Anderson et al., 1995; Heath и Me Vernon, 2002). После введения в начале 1990-х во многих странах комбинированной белково-полисахаридной вакцины против HiB, число случаев гемофильного менингита снизилось более чем на 90% (Schuchat et al., 1997), и S. pneumoniae и N. meningitides стали самыми обычными болезнетворными микроорганизмами.
В настоящее время в Европе уровень распространенности пневмококкового менингита составляет примерно 0,5 на 100000 населения; связанная с ним смертность 25%, но может достигать 45% среди очень молодых. Более чем у 30% выживших остаются постоянные неврологические осложнения (Lexau et al., 2005). Эта картина существенно хуже в развивающихся странах. Существует сезонное изменение с пиком в зимние месяцы. Дети младшего возраста наиболее подвержены риску, и 60% случаев приходится на возраст до двух лет. Комбинированная семивалентная белково-полисахаридная пневмококковая вакцина стала доступной в 2000 г. и была включена в британский национальный календарь прививок с 2006 г.
В тех странах, где эта вакцина включена в программу иммунизации, наблюдалось разительное снижение уровня инвазивной пневмококковой болезни, с сохранением N. meningitidis в качестве основного патогенного микроорганизма. Уровень заболеваемости N. meningitidis составляет около 1-3 на 100000 населения в Европе с самими обычными серотипами группы В и С. Вакцинация доступна, но пока еще только для групп А, С, Y и W135. C комбинированной полисахаридно-белковой вакциной против группы С. Она была включена в протокол иммунизации во многих развитых странах после введения в Великобритании в 1999 г. В Северной Америке недавно запущена 4-валентная вакцина для других групп (А, С, Y и W135) (Расе и Pollard, 2007).
Еще одной проблемой эпидемиологии стало появление резистентных к лекарственным средствам штаммов патогенных микроорганизмов, среди которых серьезную опасность представляет резистентный к пенициллину пневмококк (ПРП), встречающийся благодаря мутациям в одном или нескольких пенициллин-связывающих белках. Появление ПРП непосредственно связано распространением антибактериальных средств, и в определенных странах проблема больше, чем в других. В настоящее время в Великобритании менее 3% пневмококков являются ПРП, а в Испании, США и Южной Африке показатели выше. Резистентность пневмококков проверяется лабораторным анализом минимальной концентрации ингибитора (Minimum Inhibitory Concentration, MIC), и может быстро определяться с помощью специальных тестов с ПЦР для определения гена связывающего белка пенициллина 2b (ПРП2b). Устойчивость к пенициллину и хлорамфениколу при менингококковой инфекции также увеличивается, но к счастью, остается редкой.
б) Патофизиология и иммунология. Эффективная инвазия инфекции в ЦНС включает 4 стадии: в первой происходит, адгезия и колонизация патогенных микроорганизмов, часто из комменсалов носоглотки; вторая представляет собой инвазию в слизистую оболочку с последующим размножением и бактериемией; третья состоит в проникновении в подпаутинное пространство с преодолением ГЭБ, с пока еще не установленным механизмом; и наконец, размножение патогенов в подпаутинном пространстве, вызывающее воспалительный ответ хозяина.
• Адгезия и колонизация. Точные механизмы, посредством которых бактерии прикрепляются и проникают в слизистую оболочку, все еще неясны. Вовлекаются многочисленные поверхностные белки микроорганизмов (например, холиновые связывающие белки, сиаловая кислота и нейраминидаза на S. pneumoniae и К1-полисахарид на Е. coli) (Koedel et al„ 2002) и специфические рецепторы хозяина (например, pIgR). В случае менингококка пили прикрепляется к рецепторам CD46 и 66 клеток слизистой оболочки.
• Инвазия и размножение. Поверхностные белки (например, Psp А и С) и капсула пневмококков помогают сопротивляться фагоцитозу и разрушению комплиментом, для того, чтобы преодолеть защиту хозяина и выжить в пределах кровотока.
• Внедрение в ЦНС. Для проникновения патогенов в ЦНС должны быть нарушены ГЭБ и барьер между кровью и спинномозговой жидкостью (СМЖ). В этот процесс вовлечены различные гликоконъюгаты и рецепторы (например, фактор активации тромбоцитов). Было продемонстрировано, что количество бактерий в заражающем материале крови важно для возникновения менингита у экспериментальных животных, и это может также иметь место у людей (Moxon et al., 1974).
• Размножение. В СМЖ, в области ослабленной защиты хозяина, выживание и размножение патогенов наиболее вероятны. Тем не менее, их присутствие стимулирует перемещение лейкоцитов в СМЖ посредством многошагового процесса, включающего в себя различные адгезивные молекулы и лиганды (например, селектины и интегрины) с миграцией по градиенту хемотаксиса. При разрушении болезнетворных микроорганизмов запускается воспалительный каскад, который приводит к вторичному повреждению ткани. Стимуляция происходит через клеточую стенку (например, LPS у грамотрицательных микроорганизмов, таких как N. meningitidis и Н. influenzae и пептидогликаны у грамположительных микроорганизмов, таких как S. pneumoniae) (Tuomanen et al., 1985), прямо от пневмолизина (Friedland et al., 1995), и непосредственно через бактериальную ДНК (Deng et al., 2001). Через несколько часов запускаются провоспалительные цитокины, включая ФНО-α (TNFα) (Bazzoni и Beutler, 1996) и интерлейкины 1β, 6 и 8.
Они ускоряют каскад других цитокинов, хемокинов, протеолитических ферментов и реактивных кислородных радикалов и промежуточных форм азота из макрофагов, нейтрофилов и тромбоцитов. В экспериментах на крысах назначение дексаметазона и антиоксидантов показало частичное уменьшение эффекта (Auer et al, 2000). Гиперемия сосудов и повышение проницаемости кровеносных сосудов приводит к цитотоксическому и вазогенному отеку ткани мозга и увеличенному внутричерепному давлению (ВЧД), что в дальнейшем снижает церебральное перфузионное давление (ЦПД), увеличивая риск вклинения и необратимого повреждения головного мозга. Объем СМЖ увеличивается в течение первых двух или трех дней болезни (Ashwal et al., 1992), и уровни эндотоксинов (Mertsola, 1991) и других цитокинов (Arditi et al., 1989) коррелируют с тяжестью расстройств (Dulkerian et al., 1995). Частым осложнением является васкулит, приводящий к инфаркту в 2-19% случаев. Уровень мозгового кровообращения снижен на 30-70% у 30% пациентов (Ashwal et al., 1992), но авторегуляция кровообращения в основном сохранена (Ashwal et al., 1990).
Отек (цитотоксический, вазогенный и межуточный) встречается часто, как изолированно, так и с острой обструктивной гидроцефалией, обусловленной гнойным экссудатом в полостях, и может вызывать внутричерепную гипертензию и вторичное выбухание мозговой ткани. Это в свою очередь может еще больше препятствовать мозговому кровообращению (Minns et al., 1989), запуская порочный круг. Также происходит повреждение нейронов путем апоптоза, особенно в зубчатой извилине гиппокампа. Это имеет особое значение, поскольку есть доказательства, что это повреждение — причина связанных с менингитом трудностей в обучении (Loeffler et al., 2001). В экспериментах на животных гиппокампальное повреждение существенно уменьшалось в результате блокады активации каспазы-3 или управления специфическими каспаза-3-ингибиторами (Braun et al., 1999). Появление менингеального выпота может привести к хронической гидроцефалии, особенно у детей младшего возраста.
Гидроцефалия также может быть результатом стеноза сильвиева водопровода, который может возникнуть вследствие вентрикулита. Последний чрезвычайно распространен среди новорожденных и был выявлен в 92% патологоанатомических исследований (Berman и Banker, 1966), но также присутствует и у детей старшего возраста в более низкой пропорции (приблизительно 10%).

г) Клинические проявления и диагностика. Важность ранней постановки диагноза очевидна. Тем не менее, поздняя диагностика остается частой, потому что менингит относительно редко распознается в общей практике в сравнении с частыми, главным образом, вирусными, заболеваниями, сопровождающимися лихорадкой. Часто менингиту в течение нескольких дней предшествует лихорадка, поэтому невозможно определить его фактическое начало; в результате 33-40% пациентов до постановки диагноза получали антибиотики (Kaplan et al., 1986). Характер начала заболевания имеет важное прогностическое значение: прогрессирующее начало, сливающееся с предыдущими проявлениями болезни, часто прогнозирует благоприятный исход, в то время как молниеносное начало неблагоприятно (Radetsky, 1992, Kilpi et al., 1993). Лихорадка, тошнота, головная боль, сопровождающаяся рвотой, вялость и некоторое расстройство сознания (чаще умеренное оцепенение, чем кома) указывают на диагноз (Gururaj et al., 1973). Ригидность мышц шеи, а иногда также мышц спины, и симптом Кернига требуют выполнения люмбальной пункции.
На очень ранних стадиях единственными симптомами могут быть раздражительность и перемены настроения в сочетании с лихорадкой. Генерализованные припадки встречаются у 30-40% детей с острым бактериальным менингитом, особенно среди детей младше четырех лет. В одном исследовании 328 детей с первичными припадками на фоне лихорадки и без менингеальных знаков, менингит был диагностирован только у четырех детей по данным люмбальной пункции (1,2%), все они были в возрасте до 18 месяцев (Rutter и Smales, 1977). И хотя люмбальная пункция не должна быть рутинным методом исследования среди детей в возрасте до 18 месяцев, у которых могут отсутствовать менингеальные симптомы при лихорадочных припадках, она обязательна в случаях, когда ребенок не возвращается в абсолютно нормальное состояние вскоре после эпизодов припадков. Аналогично, люмбальная пункция проводится и детям до одного года при наличии малейших сомнений. Менингит у новорожденных может сопровождаться фебрилитетом или гипотермией и проявляться в виде затруднений при кормлении и дыхании. Ригидность мышц шеи и изменения родничка нетипичны. Люмбальная пункция обычно выполняется при любых септических проявлениях у нездоровых новорожденных.
Наличие пятнисто-папуллезной сыпи может служить ранним симптомом менингококкового сепсиса или проявлением вирусного заболевания. Петехии и пурпура говорят в пользу менингококковой инфекции, хотя также периодически встречаются при наличии вторичного сепсиса при гемофильной (тип В), пневмококковой инфекции или при некоторых вирусных заболеваниях (например, ECHO 9). Очаговая неврологическая симптоматика, такая как паралич черепных нервов или гемипарез обычно развивается поздно в ходе течения бактериального менингита, или раньше в качестве осложнения повышенного ВЧД (особенно параличи VI пары черепных нервов). Отек сосочка зрительного нерва редко заметен на ранних этапах; в сущности, наличие отека сосочка зрительного нерва должно вызывать подозрение о наличии очагового внутричерепного процесса, такого как абсцесс мозга или массивное повреждение, и является показанием к нейровизуализации до проведения люмбальной пункции.
При всех возможных рисках люмбальной пункции при менингитах на фоне повышенного ВЧД (Klein et al., 1986), отказ от выполнения пункции на раннем этапе заболевания значительно осложнит уход за больным ребенком. Диагноз на основе СМЖ, как было показано, изменил тактику ведения в 72% случаев с отсрочкой люмбальной пункции до тех пор, пока назначение антибиотиков повышало уровень стерильной СМЖ с 3% до 44%. Вероятность отека мозговой ткани, с предполагаемым риском смерти оценивается на уровне 4,3% (Rennick et al., 1993) и 6% (Wright et al., 1993; Lambert,1994). Люмбальная пункция, как предполагается, вызывает опущение мозгового конуса спинного мозга, хотя данных для определения явления как причины или следствия нет, а отеки мозговой ткани могут возникать и спонтанно.
Применение КТ для обнаружения отека или повышенного ВЧД чрезвычайно ограничено (Pike et al., 1990, Heyderman et al., 1992), и не способно предсказать риск опущения конуса. Данные полученные при компьютерной томографии заставили изменить тактику ведения пациентов в 5% случаев, при этом спинальная пункция откладывалась в среднем на 2,5 часа (Gopal et al., 1999). Кроме того, нормальные данные КТ не означают безопасное выполнение пункции, и в 36% случаев опущения, КТ было в пределах нормального. Используя строгий отбор пациентов, количество проведенных КТ можно значительно уменьшить (Hasbun et al., 2001). Mellor (1992) советовал откладывать спинномозговую пункцию по крайней мере на 30 минут после припадков, так как известно, что они вызывают транзиторное повышение ВЧД, и назначение маннитола перед проведением люмбальной пункции показано в сомнительных случаях, что обеспечивало эффективное снижение уровня ВЧД и повышение ЦПД и скорости кровотока (Goh и Minns, 1993). Другим противопоказанием к проведению спинальной пункции является необходимость срочного лечения шока (Lambert, 1994).
Это касаетс, прежде всего, менингококковой инфекции, диагностируемой по культуре крови. Таким образом, целесообразно отложить спинномозговую пункцию в случаях тяжелого угнетения сознания, когда ребенок находится в состоянии шока и когда имеется расширение зрачков, офтальмопарез или отек диска зрительного нерва.

е) Лабораторная диагностика:
Количество клеток в СМЖ при бактериальном менингите обычно колеблется между 1000 и 10000/мм 3 , и первоначально преобладают полиморфноядерные лейкоциты, но уровень более пяти одноядерных клеток считается ненормальным, а в 10% случаев отмечается преобладание лимфоцитов на ранних этапах. В норме нейтрофилы отсутствуют, но в цитоцентрифугированных образцах может быть обнаружен случайный единичный нейтрофил. После пункции возможно соотношение нейтрофилов и эритроцитов равное 1:700, если в периферической крови количество клеток красной крови и белых кровяных телец в пределах нормы.
Микроорганизмы можно обнаружить в мазках как внутриклеточно, так и внеклеточно. Окраска по Граму положительная в 25% случаев, в зависимости от концентрации патогенов в СМЖ (Onorato et al., 1980). Использование акридинового оранжевого, флюорохрома, окрашивающего нуклеиновые кислоты некоторых является исключение других возможно поддающихся лечению причин. Тщательные клинические, неврологические и лабораторные методы обследования определяются для каждого конкретного случая.

2. Другие лабораторные процедуры. Культура крови положительна в 80-90% случаев нелеченного менингита. Иногда культура крови может быть положительна, в то время как культура СМЖ отрицательная и, таким образом, информативна для терапии. Посевы из носа и зева не являются специфичными и чувствительными. Культура мочи и мазки из поражений кожи, окрашенные по Граму, дают возможность непосредственной идентификации патогенов.
Бактериологическое исследование жидкости из среднего уха, полученной при аспирации, в случаях сопутствующего среднего отита может выявить тот же микроорганизм, что и в ликворе, но это явление непостоянно, и даже при выявлении бактерии в обеих жидкостях нередко возможны разные штаммы.
Проводится подсчет форменных элементов крови с анализом воспалительного ответа. Обычно имеет место подъем лейкоцитов и повышенный уровень С-реактивного белка (Hansson et al., 1993).
3. Нейровизуализация. Визуализация на ранних этапах может быть нормальной, или показывать менингеальное повышение с контрастом, но его главным образом применяют для исключения другой патологии ЦНС и для диагностики осложнений (Klein et al., 1986) (см. ниже). Riordan et al., (1993) перечисляют следующие показания к КТ: длительное угнетение сознания, длительные частичные или поздние припадки, очаговые неврологические отклонения, увеличение окружности головы, подтверждение продолжающейся инфекции, и рецидивирующие симптомы и признаки. МРТ имеет дополнительные преимущества повышенной чувствительности, но не всегда доступно.
Бактериальный менингит новорожденных – это воспаление менингеальных оболочек, вызванное бактериальной инвазией. Признаки заболевания такие же, как и при сепсисе: раздражение центральной нервной системы (например, летаргия, судороги, рвота, раздражительность, ригидность затылочных мышц, набухший или выпуклый родничок) и аномалии черепных нервов. Диагноз ставится на основании результатов любмальной пункции. Лечение проводится с использованием антибиотиков.
Бактериальный менингит новорожденных возникает с частотой 2:10000 у доношенных детей и 2:1000 среди новорожденных с низкой массой тела при рождении, в основном заболевают мальчики. Данное заболевание выявляют примерно у 15% новорожденных с сепсисом, иногда развивается изолированно.
Этиология
Основные возбудители:

Стрептококки группы В Стрептококковые инфекции Стрептококки – грамположительные аэробные организмы, вызывающие множество заболеваний, включая фарингит, пневмонию, инфекции ран и кожи, сепсис и эндокардит. Симптомы изменяются в зависимости. Прочитайте дополнительные сведения (преимущественно типа III)
К другим известным патогенам относятся: энтерококк Энтерококковые инфекции Энтерококки являются грамположительными факультативными аэробными организмами. Enterococcus faecalis и E. faecium вызывают различные инфекции, включая эндокардит, инфекцию мочевых путей, простатит. Прочитайте дополнительные сведения , стрептококк группы D (неэнтерококк), альфа-гемолитический стрептококк Стрептококковые инфекции Стрептококки – грамположительные аэробные организмы, вызывающие множество заболеваний, включая фарингит, пневмонию, инфекции ран и кожи, сепсис и эндокардит. Симптомы изменяются в зависимости. Прочитайте дополнительные сведения , золотистый стафилококк (Staphylococcus aureus) Стафилококковые инфекции Стафилококки – грамположительные аэробные микроорганизмы. Staphylococcus aureus наиболее патогенный; как правило, он вызывает инфекции кожи, может вызывать пневмонию, эндокардит и остеомиелит. Прочитайте дополнительные сведения , коагулазонегативный стафилококк Стафилококковые инфекции Стафилококки – грамположительные аэробные микроорганизмы. Staphylococcus aureus наиболее патогенный; как правило, он вызывает инфекции кожи, может вызывать пневмонию, эндокардит и остеомиелит. Прочитайте дополнительные сведения и другие грамотрицательные кишечные микроорганизмы (например, виды Klebsiella Инфекции, вызываемые Klebsiella, Enterobacter, и Serratia Грамотрицательные бактерии Klebsiella, Enterobacter и Serratia – тесно связанная нормальная флора кишечника, которая редко вызывает заболевание у здоровых хозяев. Диагноз подтверждается посевом. Прочитайте дополнительные сведения , Enterobacter Инфекции, вызываемые Klebsiella, Enterobacter, и Serratia Грамотрицательные бактерии Klebsiella, Enterobacter и Serratia – тесно связанная нормальная флора кишечника, которая редко вызывает заболевание у здоровых хозяев. Диагноз подтверждается посевом. Прочитайте дополнительные сведения , Citrobacter diversus), Haemophilus influenzae Инфекции, вызываемые Haemophilus Грамотрицательные возбудители рода Haemophilus – причина многочисленных легких и тяжелых инфекций, включая бактериемию, менингит, пневмонию, синусит, средний отит, флегмону и эпиглоттит. Диагноз. Прочитайте дополнительные сведения , Neisseria meningitidis Менингококковая инфекция Менингококки (Neisseria meningitidis) – это грамотрицательные кокки, которые вызывают менингит и менингококкемию. Симптомы обычно тяжелые, включают головную боль, тошноту, рвоту, светобоязнь. Прочитайте дополнительные сведения , и Streptococcus pneumoniae Стрептококковые инфекции Стрептококки – грамположительные аэробные организмы, вызывающие множество заболеваний, включая фарингит, пневмонию, инфекции ран и кожи, сепсис и эндокардит. Симптомы изменяются в зависимости. Прочитайте дополнительные сведения .
Клинические проявления
Часто четко выражены только симптомы, типичные для неонатального сепсиса (например, нестабильная температура, расстройство дыхания, желтуха, апноэ). Проявления со стороны центральной нервной системы (например, летаргия, судороги (особенно фокальные), рвота, раздражительность) более точно указывают на наличие неонатального бактериального менингита. Так называемая парадоксальная раздражительность, при которой объятия и утешение родителей скорее раздражают (потому что движение воспаленных мозговых оболочек болезненно), а не утешают новорожденного, является более специфичной при диагностике. Набухший или выпуклый родничок выявляют примерно в 25% случаев, а ригидность в 15%. Чем младше пациент, тем реже встречаются эти признаки. Аномалии черепных нервов (особенно связанные с III, VI и VII нервами), также могут присутствовать.
Менингит, вызванный стрептококками группы В, может развиться в первые недели жизни, сопровождаясь раним сепсисом новорожденных, и часто первично проявляющийся в виде системного заболевания с выраженными признаками дыхательной недостаточности. Однако чаще менингит, вызванный стрептококками группы В, развивается по прошествии этого периода (наиболее часто в первые 3 месяца жизни) как изолированное заболевание, характеризующееся отсутствием предшествующих акушерских или перинатальных осложнений и наличием более четких признаков менингита (например, лихорадки, вялости, эпилептических припадков).
Вентрикулит часто сопровождает бактериальный менингит новорожденных, особенно когда вызван грамотрицательными кишечными бациллами. Возбудители, которые вызывают менингит с тяжелым васкулитом, особенно C. diversus и Cronobacter sakazakii (ранее Enterobacter sakazakii), могут вызвать кисты и абсцессы. Pseudomonas aeruginosa, E. coli К1, и виды Serratia также могут вызвать абсцессы мозга. Ранними клиническими признаками абсцесса головного мозга являются повышение внутричерепного давления, обычно проявляющееся рвотой, выпуклый родничок, а иногда и увеличение размера головы. Ухудшение ранее стабильных новорожденных с менингитом выражается прогрессирующим повышением внутричерепного давления, вызванным абсцессом, гидроцефалией или разрывом абсцесса в систему желудочков мозга.
Здравый смысл и предостережения
Классические признаки менингита являются редкостью у новорожденных; выпуклый родничок или его набухание возникает только у около 25% новорожденных, а ригидность затылочных мышц – только у 15% новорожденных.
Диагностика
Определение количества клеток цереброспинальной жидкости (ЦСЖ), уровня глюкозы и белка, окрашивание по Граму и культуральный посев
Анализ методом полимеразной цепной реакции (ПЦР)
Иногда ультрасонография или КТ, или МРТ головного мозга
Окончательный диагноз неонатальный бактериальный менингит устанавливают на основании исследования спинномозговой жидкости посредством спинномозговой пункции, которую нужно проводить всем новорожденным с подозрением на сепсис или менингит. Тем не менее, ЛП может быть тяжело провести у новорожденного, и есть некоторый риск возникновения гипоксии. Тяжелое клиническое состояние пациента (дыхательная недостаточность, шок, тромбоцитопения) делает проведение ЛП затруднительным. Если проведение ЛП откладывается, при наличии клинических признаков новорожденного следует рассматривать как имеющего менингит. Даже при улучшении клинического состояния наличие воспалительных клеток и аномальных уровней глюкозы и белка в СМЖ в течение нескольких дней после начала заболевания также дает нам право предположить наличие менингита. При проведении ЛП нужно использовать иглу с троакаром, чтобы избежать заноса частиц эпителия и последующего развития эпителиом.
СМЖ, даже если в ней отсутствуют кровь или клетки, следует исследовать культуральным методом. Примерно 15–35% новорожденных с отрицательными культуральными тестами с кровью имеют положительные результаты культуральных тестов со СМЖ. Если культуральное исследование СМЖ отрицательное, в случае подозрения на бактериальный менингит (например, если была возможность влияния на микроорганизмы предшествующим приемом антибиотиков) можно провести исследование СМЖ на наличие нескольких распространенных патогенных микроорганизмов с помощью мультиплексных ПЦР-панелей. ЛП повторяют через 24–48 часов при сомнительном клиническом ответе и через 72 часа при вовлечении грамотрицательных микроорганизмов (для подтверждения стерильности).
Повторные анализы СМЖ помогают определить продолжительность терапии и предсказать прогноз. Некоторые эксперты считают, что повторная ЛП в промежутке от 24 до 48 часов у новорожденных с менингитом, вызванным стрептококком группы В, имеет прогностическое значение. ЛП не нужно повторять в конце терапии, если отмечается положительная динамика в состоянии ребенка.
Нормальные показатели СМЖ противоречивы и частично зависят от возраста ребенка. В целом как у доношенных, так и у недоношенных новорожденных с менингитом в цереброспинальной жидкости (ЦСЖ) содержится ≤ 20 лейкоцитов/мкл (одна пятая из которых могут быть полиморфо-ядерными лейкоцитами). Содержание белка в спинномозговой жидкости при отсутствии менингита более изменчиво: доношенные дети содержат 100 мг/дл (1 г/л), в то время как у недоношенных детей этот показатель составляет до 150 мг/дл (1,5 г/л). Содержание глюкозы в СМЖ при отсутствии менингита составляет 75% от значений в сыворотке крови, измеренных в то же время. Этот показатель может снижаться до 20–30 мг/дл (1,1–1,7 ммоль/л). Бактериальный менингит был диагностирован с помощью культурального исследования у новорожденных с нормальными показателям СМЖ, демонстрируя, что нормальные значения СМЖ не исключают диагноз менингита.
Вентрикулит у детей возникает в том случае, если антибактериальная терапия неэффективна. Диагноз вентрикулита ставят при наличии больше лейкоцитов при вентрикулярной пункции, чем при спинномозговой, при положительном окрашивании по Граму или по результатам культуральных тестов ликвора из желудочков, а также при повышенном давлении в желудочках мозга. При подозрении на вентрикулит или абсцесс мозга диагностике может помочь ультрасонография или МРТ, или КТ с контрастированием, расширенные желудочки также подтверждают наличие вентрикулита.
Прогноз
Без лечения смертность от бактериального менингита новорожденных приближается к 100%. При проведении лечения на прогноз влияет масса тела при рождении, тяжесть состояния ребенка и клинических проявлений. Уровень смертности среди новорожденных, которых лечили от бактериального менингита, составляет 5-20%. Микроорганизмы, вызывающие васкулит или абсцесс мозга (некротический менингит), могут обусловливать смертность до 75%. Неврологические осложнения (например, гидроцефалия гидроцефалия Гидроцефалия развивается из-за накопления избыточного количества спинномозговой жидкости, вызывая расширение желудочков головного мозга и/или повышение внутричерепного давления. Первые проявления. Прочитайте дополнительные сведения , потеря слуха Нарушение слуха у детей Распространенными причинами потери слуха являются генетические дефекты у новорожденных, ушные инфекции и серная пробка у детей. Многие случаи обнаруживаются при обследовании, но потерю слуха. Прочитайте дополнительные сведения , умственная отсталость Умственная отсталость Умственная отсталость характеризуется значительным недоразвитием интеллектуальной функции (часто выражающимся коэффициентом интеллектуальности 70–75) в сочетании с ограничением адаптивных функций. Прочитайте дополнительные сведения ) развиваются у 20–50% выживших детей, имевших неблагоприятный прогноз вследствие того, что возбудителями были грамотрицательные кишечные бациллы.
Прогноз также частично зависит от числа микроорганизмов, выявленных в СМЖ на момент постановки диагноза. Продолжительность получения положительных результатов культуральных тестов СМЖ имеет прямую корреляцию с частотой осложнений. Обычно, культура цереброспинальной жидкости (ЦСЖ) новорожденных с инфекцией, вызванной стрептококками группы B, становится стерильной в течение первых 24 часов антимикробной терапии. При менингите грамотрицательной этиологии культуральные тесты остаются положительными дольше – в среднем 2 дня.
Смертность при менингите, вызванном стрептококками группы B, значительно ниже, чем при раннем сепсисе, вызванном этими же возбудителями.
Лечение
Эмпирически: ампициллин + гентамицин, цефотаксим или оба препарата с последующим определением специфической антибиотикочувствительности
Эмпирическая антибактериальная терапия
Начальное эмпирическое лечение зависит от возраста пациента и по-прежнему обсуждается. Для новорожденных многие эксперты рекомендуют применять ампициллин с аминогликозидами (см. таблицу рекомендованной дозировки некоторых аминогликозидов для новорожденных Рекомендованные дозировки некоторых аминогликозидов для новорожденных У новорожденных внеклеточная жидкость (ECF) составляет до 45% от общей массы тела, что требует введения относительно больших доз некоторых антибактериальных препаратов (например, аминогликозидов). Прочитайте дополнительные сведения [Table Recommended Dosages of Select Aminoglycosides for Neonates]). При подозрении на менингит, вызванный грамотрицательным возбудителем, также добавляют цефалоспорины 3-го поколения (например, цефотаксим) пока результаты культурального исследования и чувствительности не будут доступны. Тем не менее, устойчивость может развиваться быстрее при регулярном применении цефотаксима для эмпирической терапии, а длительное использование цефалоспоринов 3-го поколения является фактором риска развития инвазивного кандидоза. Ампициллин активен в отношении стрептококков группы B, энтерококков и Listeria. Гентамицин обеспечивает синергизм в отношении этих организмов, а также лечит многие инфекции, вызванные грамотрицательной флорой. Цефалоспорины третьего поколения обладают достаточной активностью в отошении большинства грамотрицательных микроорганизмов.
Госпитализированные новорожденные, ранее получавшие антибиотики (например, при сепсисе с ранним началом), могут иметь резистентные микроорганизмы; грибковые заболевания могут также возникать после длительной госпитализации у новорожденных без врожденной инфекции. Больным новорожденным с внутрибольничной инфекцией необходимо сначала ввести ванкомицин (см. таблицу Дозировки ванкомицина для новорожденных Дозирование ванкомицина для новорожденных У новорожденных внеклеточная жидкость (ECF) составляет до 45% от общей массы тела, что требует введения относительно больших доз некоторых антибактериальных препаратов (например, аминогликозидов). Прочитайте дополнительные сведения плюс аминогликозиды вместе с цефалоспоринами 3-го поколения или без них либо карбапенемами, активными в отношении Pseudomonas aeruginosa, такими как цефепим или меропенем, в зависимости от опасения развития менингита.
Антибиотикотерапию корректируют после получения результатов культурального исследования СМЖ и данных о чувствительности микроорганизмов. Не следует использовать результаты окрашивания по Граму для сужения спектра действия, пока не станут известны результаты посева.
Патогенспецифическая терапия антибиотиками
Рекомендованное стартовое лечение менингита, вызванного стрептококками группы Б (GBS meningitis), у новорожденных в возрасте 1 недели, включает применение пенициллина G в дозе 100 000 единиц/кг внутривенно каждые 6 ч или ампициллина в дозе 100 мг/кг внутривенно каждые 8 ч для детей ≤ 7 дней или 75 мг/кг каждые 6 ч для детей > 7 дней. Кроме того, гентамицин назначается для достижения синергизма в дозе, соответствующей возрастной норме ( Рекомендованные дозировки некоторых аминогликозидов для новорожденных Рекомендованные дозировки некоторых аминогликозидов для новорожденных У новорожденных внеклеточная жидкость (ECF) составляет до 45% от общей массы тела, что требует введения относительно больших доз некоторых антибактериальных препаратов (например, аминогликозидов). Прочитайте дополнительные сведения ). При выявлении клинического улучшения или стерильной СМЖ применение гентамицина можно прекратить.
При инфекциях, вызванных энтерококками или L. monocytogenes, лечение, как правило, состоит из ампициллина в комбинации с гентамицином в течение всего курса.
Менингит, вызванный грамотрицательными бактериями, трудно поддается лечению. При применении традиционной схемы ампициллина с аминогликозидами смертность может достигать 15–20% с высоким уровнем осложнений у выживших. Следует применить цефалоспорины 3-го поколения (например, цефотаксим) у новорожденных с доказанным грамотрицательным менингитом. При подозрении на наличие антибиотикорезистентности можно использовать аминогликозиды и цефалоспорины 3-го поколения или бета-лактамы широкого спектра (например, меропенем) до установления чувствительности.
Парентеральное введение препаратов при грамположительном менингите продолжают в течение как минимум 14 дней, а при тяжелом грамположительном или грамотрицательном менингите – как минимум 21 день. Внутрижелудочковое введение антибиотиков не рекомендуется.
Дополнительные меры
Поскольку менингит может рассматриваться как часть продолжающегося неонатального сепсиса, для лечения этого заболевания у новорожденных также нужно применять дополнительные меры, используемые при лечении сепсиса у новорожденных Другие виды лечения Неонатальный сепсис является инвазивной инфекцией, как правило, бактериальной, развивающейся в неонатальном периоде. Симптомы сепсиса многообразны, неспецифичны и включают снижение спонтанной. Прочитайте дополнительные сведения . Глюкокортикоиды при лечении менингита у новорожденных не применяют. У пациентов следует четко отслеживать неврологические осложнения в течение раннего детства, в том числе нейросенсорную потерю слуха.
Основные положения
Наиболее распространенными причинами являются стрептококки группы В, кишечная палочка (E. coli,) и L. monocytogenes.
Проявления часто неспецифические (например, нестабильность температуры, дыхательная недостаточность, желтуха, апноэ).
Хотя признаки со стороны центральной нервной системы (например, летаргия, судороги, рвота, раздражительность) могут присутствовать, классические симптомы, такие как выпуклый родничок или его набухание и ригидность затылочных мышц не являются распространенными.
Решающее значение имеет культуральное исследование цереброспинальной жидкости (ЦСЖ), поскольку у некоторых новорожденных с менингитом показатели ЦСЖ находятся в пределах нормы (например, уровни лейкоцитов, белка и глюкозы).
Эмпирическое лечение начинают с применения ампициллина, гентамицина и цефотаксима, с последующим назначением препаратов в соответствии с результатами культурального исследования и тестирования на чувствительность.
Читайте также:

