Менингоэнцефалит герпетической этиологии что это
Обновлено: 23.04.2024
Менингоэнцефалит - заболевание нейроинфекционной природы, которое протекает с сочетанным поражением мозгового вещества и оболочек.
Основными причинами развития менингоэнцефалита у взрослых являются:
- Попадания возбудителя (вирусов, бактерий, простейших, патогенных грибов) в носоглотку. Заражение происходит воздушно-капельным и алиментарным способами (через загрязненную пищу, воду). Проникновение в головной мозг осуществляется гематогенным путём, в результате чего возникают воспалительные изменения в тканях, приводящие к развитию менингоэнцефалита;
- Укусы насекомых. Трансмиссивный путь передачи является основным для ряда вирусных менингоэнцефалитов и энцефалитов, таких как японский комариный энцефалит, клещевой энцефалит, энцефалит Сент-Луис). При укусе возбудитель проникает в кровоток и заносится в церебральные ткани, таким образом провоцируя заболевание;
- Наличие различных инфекций в организме. Гематогенное распространение бактериальных инфекций осуществляется при наличии туберкулёзных (туберкулезный менингоэнцефалит), сифилитических очагов, гнойных процессов в околоносовых пазухах, челюстно-лицевой области, при хроническом гнойном отите. Вирусный менингоэнцефалит может возникнуть в результате осложнения ОРВИ;
- Черепно-мозговые травмы. Инфицирование контактным путем происходит вследствие открытой травмы с нарушением целостности черепных костей. По статистике, посттравматический менингоэнцефалит наблюдается у 1,5-4% пациентов с черепно-мозговой травмой;
- Вакцинация. Введение живой вакцины при наличии ослабленного иммунитета опасно развитием инфекционного процесса в организме. Проникновение возбудителей происходит через гематоэнцефалический барьер, что приводит к появлению менингоэнцефалита;
- Наличие иммунодефицита;
- Незрелость системы иммунитета.

Менингоэнцефалит: симптомы у взрослых
Клиническая картина состоит из общеинфекционных, менингеальных, очаговых и ликворно-гипертензионных симптомов. Наиболее типичными симптомами являются:
- Повышение температуры тела;
- Общее недомогание;
- Отсутствие аппетита;
- Высыпания на кожных покровах;
- Ликворная гипертензия (сильная головная боль, тошнота, рвота, не приносящая облегчения);
- Расстройство сознания (сонливость\ возбуждение, нарушение ориентации в месте и пространстве, возможно кома);
- Менингеальный синдром (повышенная чувствительность на свет, звук, прикосновениям, гипертонус задних мышц шеи, мышц-сгибателей конечностей, судороги, сильная головная боль);
- Гемипарезы (неполный паралич);
- Сенсомоторная афазия (утрата речи);
- Гиперкинезы (непроизвольные движения);
- Мозжечковый синдром (расстройство координации движения);
- Вестибулярная атаксия (нарушение походки и координации);
- Когнитивные нарушения (снижение умственной деятельности, памяти);
- Глазодвигательные и зрительные расстройства (при поражениях черепно-мозговых нервов) – двоение, косоглазие, ограничение подвижности и т.д.;
- Перекос лица, опущение век;
- Снижение слуха;
- Нарушения глотания;
- Дизартрия (нарушение речевого аппарата).
Менингоэнцефалит: код по МКБ 10
МКБ-10 представляет собой нормативный документ с общепринятой статистической классификацией медицинских диагнозов, которая используется в здравоохранении.
По международной классификации менингоэнцефалит входит в состав следующих кодов:
- G04.2 — Бактериальный менингоэнцефалит и менингомиелит, не классифицированный в других рубриках;
- G05 — Энцефалит, миелит и энцефаломиелит при болезнях, классифицированных в других рубриках. Включены: менингоэнцефалит и менингомиелит.
Гнойный менингоэнцефалит
Гнойный менингоэнцефалит — это нейроинфекционное заболевание, характеризующееся поражением мозговой ткани и всех оболочек головного мозга (твердой, мягкая и паутинная). Клинически заболевание проявляется интоксикационным, общемозговым и менингеальным синдромами. Диагноз верифицируется в результате проведения:
- тщательного неврологического осмотра;
- МРТ/КТ головного мозга;
- исследования ликвора (люмбальная пункция);
- лабораторной диагностики.
Лечение гнойного менингоэнцефалита базируется на проведении этиотропной (антибиотики, антивирусные, противогрибковые, противопаразитарные фармакологические препараты) в комбинации с патогенетической и симптоматической терапиями.
Инфицирование возможно в следующих случаях:
- Попадания возбудителя в носоглотку воздушно-капельным либо алиментарным путем. Возбудитель проникает в полость черепа через кровь, провоцирует воспалительные изменения поражённых тканей, приводящие к развитию гнойного менингоэнцефалита;
- Укуса насекомого. Трансмиссивный путь (через укус) передачи характерен для ряда вирусных менингоэнцефалитов и энцефалитов (японского комариного энцефалита, клещевого энцефалита, энцефалита Сент-Луис);
- Наличия инфекционных заболеваний в организме. При наличии туберкулёзных, сифилитических очагов, хронического гнойного отита, гнойных процессов челюстно-лицевой области, околоносовых пазух существует большая вероятность распространение бактериальной инфекции гематогенным путем. Вирусный менингоэнцефалит может возникнуть как осложнение отдельных ОРВИ;
- Черепно-мозговой травмы. При открытой травме с нарушением целостности костей черепа инфицирование происходит контактным путём;
- Вакцинации. Введение живой вакцины на фоне ослабленного иммунитета может спровоцировать развитие инфекционного процесса. Поствакцинальное осложнение с проникновением возбудителей через гематоэнцефалический барьер приводит к возникновению менингоэнцефалита.
Не всегда при попадании возбудителя в организм человека развивается заболевание. Причинами, способствующими возникновению болезни, считают ослабленное состояние организма, наличие первичного или вторичного иммунодефицита, незрелость системы иммунитета.
На сегодняшний день, врачи-неврологи подразделяют менингоэнцефалит на различные типы по нескольким критериям: этиологии, характеру морфологических изменений и типу течения. По этиологии различают следующие виды энцефалита:
- Вирусный - возбудителями могут стать вирусы гриппа, простого герпеса, кори, бешенства, цитомегаловирус, энтеровирусы. Преобладает серозный характер воспалительных изменений;
- Бактериальный – возбудителями могут стать стрепто-, менинго-, пневмококки, клебсиелла, гемофильная палочка. Воспаление имеет гнойный характер воспалительных изменений;
- Протозойный - встречается крайне редко. Инфекционными агентами являются амебы, токсоплазмы и другие простейшие;
- Грибковый – преимущественно наблюдается у иммунокомпрометированных лиц. Может диагностироваться в рамках нейроСПИДа.
Клиническая картина гнойного менингоэнцефалита характеризуется интоксикационным, ликворно-гипертензионным, менингеальным, очаговым синдромами. Типичными признаками инфекции являются:
- повышение температуры тела;
- недомогание;
- отсутствие аппетита;
- усталость;
- вялость;
- апатия;
- головные боли, миалгия, артралгия.
Не исключено появление высыпаний на кожных покровах. Ликворная гипертензия проявляется как интенсивная головная боль, тошнота, не приносящая облегчение рвотой. Быстро нарастающее повышение внутричерепного давления приводит к снижению уровня сознания, вплоть до комы.
Диагностика менингоэнцефалита
Диагностика пациентов начинается со сбора анамнеза жизни и болезни, врач узнает о текущей или недавно перенесенной инфекционной болезни, наличие в анамнезе черепно-мозговых травм, факта вакцинации, укусов насекомых и т. п. Дальнейшие диагностические манипуляции заключаются в следующем:
- Неврологический осмотр. Выявляются менингеальные симптомы, оценивается состояние сознания пациента, очаговый неврологический статус. Полученные данные будут говорить о том, вовлечены ли в патологический процесс оболочки мозга и вещество;
- Лабораторные исследования. Для бактериального менингоэнцефалита будут характерны лейкоцитоз и ускоренная СОЭ. Также для определения возбудителя проводят посев крови на стерильность и ПЦР-анализ;
- Компьютерная и магнитно-резонансная томография. Позволяют оценить состояние головного мозга, выявить утолщение и уплотнение церебральных оболочек, изменения мозговых тканей. При наличии паразитов, на снимках будут визуализироваться гетерогенные круглые очаги с кольцевидным усилением по периферии;
- Люмбальная пункция. С её помощью исследуется спинномозговая жидкость, которая при гнойном воспалении будет мутной и иметь осадок в виде хлопьев, при серозном поражении — прозрачная, геморрагическом — с примесью крови;
- Стереотаксическая биопсия головного мозга. Позволяет диагностировать паразитарный менингоэнцефалит, исключить злокачественный процесс.
Лечение менингоэнцефалита в Москве
Терапия в Юсуповской больницы проводится наилучшими специалистами, которые применяют комплексный подход в лечении менингоэнцефалита. Лечение проходит в условиях отделения реанимации или интенсивной терапии и включает в себя этиотропные, патогенетические, а также симптоматические компоненты. Средствами, применяемые врачами Юсуповской больницы являются:
- Антибиотики. Чаще всего назначаются цефалоспорины в сочетании с ампициллином. Коррекция терапии ведется с учетом чувствительности выделенной флоры;
- Противовирусные препараты. Антивирусное лечение комбинируется с введением препаратов интерферона;
- Противогрибковые средства. В основном назначают амфотерицин В и флуконазол. При необходимости используют их сочетание;
- Антипаразитарные препараты. Применяются вместе с противогрибковыми средствами или антибиотиками.
В борьбе с церебральным отёком применяют:
- Мочегонные препараты;
- Глюкокортикостероиды.
- Для поддержания жизнедеятельности нейронов используют нейропротекторы и нейрометаболические препараты.
Симптоматическая терапия включает:
- Сердечно-сосудистые препараты;
- Оксигенотерапия;
- Искусственная вентиляция легких;
- Противосудорожные средства;
- Антипиретики;
- Психотропные препараты.
В Юсуповской больницы помимо лечения заболевания, занимаются реабилитацией пациентов, которая направлена на максимально быстрое восстановление нарушенных нервных функций.
Реабилитационные мероприятия включают в себя:
- Массаж;
- Лечебная физкультура;
- Акупунктура.
Медицинский персонал больницы с удовольствие поможет Вам с решением любых вопросов. На сайте Юсуповской больницы Вы можете ознакомиться с ценами на услуги, а также узнать больше о менингоэнцефалите и отзывах пациентов, прошедших курс терапии.
За свое непродолжительное существование Юсуповская больница может похвастаться отменной репутаций, а также огромным количеством благодарных пациентов. Записаться на прием или консультацию Вы можете по телефону.
Герпетический энцефалит — это диффузное или очаговое поражение мозгового вещества, вызванное герпесвирусами ВПГ-1, ВПГ-2, Varicella Zoster. Основные симптомы болезни: фебрильная лихорадка, прогрессирующее угнетение сознания, судорожные приступы. По завершении острого периода инфекции в течение длительного времени сохраняются резидуальные неврологические нарушения. Для установления диагноза необходимо проведение ПЦР-диагностики ликвора, томографии головного мозга, электроэнцефалограммы. Лечение патологии включает противовирусные препараты, противоотечную, нейрометаболическую и противосудорожную терапию.
МКБ-10
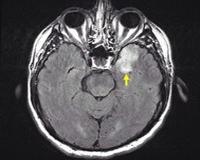
Общие сведения
Энцефалит герпетического происхождения составляет до 15-20% всех вирусных воспалительных процессов в мозговой ткани. Симптомы встречаются с частотой 4-5 случаев на 1 млн. населения, причем до трети больных составляют дети, а еще около 20% приходится на возрастную категорию старше 60 лет. Заболевание не теряет своей актуальности в современной неврологии, поскольку для успешного исхода патологии необходимо вовремя поставить диагноз и начать лечение, а промедление в оказании медицинской помощи чревато смертью пациента.

Причины
Болезнь в 95% случаев вызывается вирусом простого герпеса 1 типа, что объясняется высокой распространенностью возбудителя. По данным ВОЗ, около 2/3 населения мира в возрасте до 50 лет инфицированы ВПГ-1. На втором месте по частоте находится Varicella Zoster Virus (VZV) — возбудитель ветряной оспы, опоясывающего герпеса. Энцефалит, вызванный ВПГ-2, встречается редко, преимущественно у иммунокомпрометированных пациентов.
Ведущим среди факторов риска служит сниженный иммунный статус. Герпетическая инфекция протекает латентно, активизируется на фоне нарушения общей резистентности организма (при переохлаждении, стрессе, менструации у женщин). В группе риска находятся люди с врожденными и приобретенными иммунодефицитами, больные, получающие лечение иммуносупрессивными препаратами. К триггерам относят реинфицирование другими штаммами герпесвирусов, сопровождающееся аутоиммунными реакциями.
Патогенез
Первичное заражение ВПГ-1, как правило, происходит в детстве при попадании вирусных частиц на слизистые оболочки, после чего возбудитель начинает размножаться, мигрирует в нервные ганглии, где длительное время находится в состоянии латентной инфекции. Заражение ВПГ-2 наблюдается после начала сексуальной жизни через слизистые половых путей, а дальнейший путь развития патогена сходен с ВПГ-1.
Симптомы болезни в большинстве случаев возникают при реактивации инфекции под действием провоцирующих факторов. Герпесвирусы проникают в головной мозг гематогенным путем либо по нервным стволам (через тройничный или обонятельный нерв). Из гассерова узла они распространяются на таламус, подкорковые ядра, кору больших полушарий. При распространении по ольфакторному тракту первой страдает лимбическая система (гиппокамп, височная кора).
Симптомы герпетического энцефалита
В типичном течении острого мозгового воспаления выделяется несколько последовательных стадий: ранняя, период разгара болезни, регресс признаков, стадия остаточных явлений. В 70% патология манифестирует с внезапно возникшей высокой лихорадки (более 39°С), сопровождающейся интенсивными головными болями в лобно-височной зоне, сильной сонливостью, рвотой, не связанной с приемом пищи.
На вторые-третьи сутки симптомы дополняются нарушениями сознания: больные начинают путаться во времени и пространстве, не узнают родственников, испытывают разнообразные галлюцинации. По мере усугубления тяжести состояния появляются фокальные или генерализованные судорожные припадки. Изредка наблюдается оперкулярный автоматизм — повторяющиеся причмокивающие или сосательные движения.
В среднем через 3 дня заболевание переходит в стадию разгара. Основное проявление — глубокое угнетение сознания вплоть до комы. Пациенты не отвечают на звуковые и тактильные раздражители, однако двигательные реакции на болевые стимулы остаются в пределах нормы. Также могут возникать симптомы декортикации или децеребрации, аритмичное дыхание, двусторонние моторные нарушения.
Если пациенту было предоставлено комплексное лечение, с 3-4 недели начинается обратное развитие симптомов герпетического энцефалита. Этот этап длится от нескольких месяцев до 1 года, характеризуется постепенным восстановлением временно утраченных неврологических функций. По окончании третьей стадии около 80% больных имеют стойкие резидуальные (остаточные) явления, которые могут сохраняться пожизненно.
Осложнения
В остром периоде прогностическим неблагоприятным является прогрессирование отека мозга, что чревато его вклинением. При височно-тенториальной форме вклинения возникает триада признаков: потеря сознания, гемипарез, анизокория. Симптомами транстенториальной формы являются отсутствие реакции зрачков на свет, фиксация глазных яблок по срединной линии, двусторонний гипертонус мышц. Зачастую нарушается работа дыхательного центра.
Патология имеет тяжелое течение, при отсутствии своевременной медицинской помощи летальность достигает 70%. Даже если проводится этиотропное лечение, смертельный исход регистрируется у 15-20% пациентов, чаще у младенцев, пожилых людей, больных из группы риска. У выздоровевших полный регресс неврологической симптоматики наблюдается только в 20% случаев, а остальные сталкиваются с резидуальными симптомами.
Наиболее опасным хроническим осложнением заболевания считается прогрессирующее вегетативное состояние (акинетический мутизм), характеризующийся необратимым разрушением высших психических функций. У больных сохранено сознание, витальные функции (дыхание, кровообращение), однако полностью отсутствует познавательная деятельность. Такие пациенты не говорят, не реагируют на внешние раздражители, требуют постоянного ухода.
К типичным последствиям герпетической формы энцефалита относится синдром Клювера-Бьюси, при котором развиваются тяжелые длительные расстройства психической и когнитивной сферы. Симптомы расстройства включают ажитированное состояние, агрессивность, патологическую гиперсексуальность. Также наблюдаются интеллектуальные нарушения, проблемы с концентрацией внимания, ослабление памяти.
Диагностика
Обследованием пациента занимаются инфекционисты, неврологи, врачи экстренной помощи и реанимационного отделения. Заподозрить энцефалит удается по острому началу, наличию фебрильной лихорадки, сочетанию общемозговых и очаговых симптомов. Для подтверждения заболевания, уточнению этиологии воспалительного процесса назначаются следующие методы исследования:
Лечение герпетического энцефалита
Консервативная терапия
Герпетический энцефалит характеризуется быстрым нарастанием неврологического дефицита, прогрессированием общемозговых симптомов, поэтому комплексное лечение должно начинаться в максимально ранние сроки. Наилучшие шансы на полное выздоровление у пациентов, которые начали получать этиотропные препараты в первые сутки манифестации болезни. Лечение заболевания включает следующие группы медикаментов:
Реабилитация
Благотворное влияние на состояние ЦНС после перенесенного герпетического энцефалита оказывают витаминные комплексы (витамины группы В, аскорбиновая кислота) в сочетании с антиоксидантами. Восстановительное лечение также включает ноотропы и нейрометаболические препараты для улучшения когнитивных мозговых функций. Коррекция иммунологического статуса проводится адаптогенами, актопротекторами, неспецифическими иммуномодуляторами.
Для восполнения энергозатрат организма, стимуляции репаративных процессов показано адекватное по калорийности и витаминному составу энтеральное питание. Большое внимание уделяется физиотерапевтическим процедурам, массажу и лечебной физкультуре, направленным на улучшение двигательной функции. При наличии показаний рекомендуются занятия с логопедами, дефектологами.
Прогноз и профилактика
Несмотря на проводимое этиотропное лечение, прогноз при герпетическом энцефалите остается неблагоприятным, показатель летальности составляет 15-20%. У большинства выздоровевших сохраняется неврологический дефицит. Для предупреждения заболевания необходима рациональное лечение герпеса кожи и слизистых оболочек, своевременное консультирование больных с диссеминированной герпетической инфекцией.
2. Менингиты и энцефалиты: уч. пос. для врачей/ Д. А. Валишин, Р. Т. Мурзабаева, А. П. Мамон, М. А. Мамон, Л. В. Мурзагалеева. — 2012.
3. Герпетическое поражение нервной системы/ М.Н. Лебедюк, М.Э. Запольский, Ю.И. Горанский// Украинский журнал дерматологии, венерологии, косметологии. — 2011. — №2.
4. Герпетический энцефалит/ Т.В. Матвеева, Н.В. Токарева, Г.А. Шакирзянова// Неврология. — 2006. — №16.
Исследование спинномозговой жидкости является единственным методом, позволяющим быстро диагностировать менингит. Отсутствие воспалительных изменений в ликворе всегда позволяет исключить диагноз менингита. Этиологический диагноз менингита устанавливают с помощью бактериоскопических и бактериологических методов, вирусологических и серологических исследований.
Плеоцитоз - характернейшая черта изменений СМЖ. По числу клеток различают серозный и гнойный менингиты. При серозном менингите цитоз составляет 500-600 в 1 мкл, при гнойном – более 600 в 1 мкл. Исследование должно быть проведено не позже чем через 1 час после ее получения.
По этиологической структуре 80-90% бактериологически подтвержденных случаев приходится на Neisseria meningitides, Streptococcus pneumoniae и Haemophilus. Бактериоскопия СМЖ благодаря характерной морфологии менингококков и пневмококков дает при первой люмбальной пункции положительный результат в 1, 5 раза чаще, чем рост культуры.
СМЖ при гнойном менингите от слегка мутноватой, как бы забеленной молоком, до густо зеленой, гнойной, иногда ксантохромной. В начальной стадии развития менингококкового менингита имеет место повышение внутричерепного давления, затем в ликворе отмечается нейтрофильный маловыраженный цитоз, а у 24, 7% больных СМЖ нормальная в первые часы болезни. Затем у многих больных уже в первые сутки заболевания цитоз достигает 12000-30000 в 1 мкл, преобладают нейтрофилы. Благоприятное течение заболевания сопровождается уменьшением относительного числа нейтрофилов и увеличение лимфоцитов. Встречающиеся случаи гнойного менингита с типичной клинической картиной и сравнительно небольшим цитозом могут быть объяснены, вероятно, частичной блокадой субарахноидального пространства. Отчетливой корреляции между выраженностью плеоцитоза и тяжестью заболевания может не наблюдаться.
Содержание белка в СМЖ при гнойном менингите обычно повышено до 0, 6-10 г/л и уменьшается по мере санации ликвора. Количество белка и цитоз обычно параллельны, но в отдельных случаях при высоком цитозе уровень белка остается нормальным. Большое содержание белка в СМЖ чаще встречается при тяжелых формах с синдромом эпендидимита, а наличие его в высоких концентрациях в период выздоровления указывает на внутричерепное осложнение (блок ликворных путей, дуральный выпот, абсцесс мозга). Сочетание низкого плеоцитоза с высоким содержанием белка - особенно неблагоприятный прогностический признак.
У большинства больных гнойным менингитом с первых дней болезни отмечается понижение уровня глюкозы (ниже 3 ммоль/л), при летальных исходах содержание глюкозы было в виде следов. У 60% больных содержание глюкозы ниже 2, 2 ммоль/л, а отношение уровня глюкозы к таковому в крови у 70% составляет менее 0, 31. Увеличение содержания глюкозы – почти всегда прогностически благоприятный признак.
При туберкулезном менингите бактериоскопическое исследование СМЖ часто дает отрицательный результат. Микобактерии чаще обнаруживают в свежих случаях заболевания (у 80% больных туберкулезном менингитом). Нередко отмечается отсутствие микобактерий в люмбальном пунктате при обнаружении их в цистернальной СМЖ. В случае отрицательного или сомнительного бактериоскопического исследования туберкулез диагностируют методом посева или биологической пробой. При туберкулезном менингите СМЖ прозрачна, бесцветна или слегка опалесцирует. Плеоцитоз колеблется от 50 до 3000 в 1 мкл, в зависимости от стадии заболевания, составляя к 5-7 дню болезни 100-300 в 1 мкл. При отсутствии этиотропного лечения число клеток нарастает от начал до конца заболевания. Может быть внезапное падение цитоза при повторной люмбальной пункции, проведенной через 24 часа после первой. Клетки преимущественно лимфоциты, однако нередко в начале болезни встречается смешанный лимфоцитарно-нейтрофильный плеоцитоз, что считается типичным для миллиарного туберкулеза с обсеменением мозговых оболочек. Характерным для туберкулезного менингита является пестрота клеточного состава, когда наряду с преобладанием лимфоцитов встречаются нейтрофилы, моноциты, макрофаги и гигантские лимфоциты. Позднее – плеоцитоз приобретает лимфоплазмоцитарный или фагоцитарный характер. Большое количество моноцитов и макрофагов свидетельствует о неблагоприятном течении заболевания.
Общий белок при туберкулезном менингите всегда повышен до 2-3 г/л, причем ранее исследователи отмечали, что белок увеличивается до появления плеоцитоза и исчезает после значительного его уменьшения, т. е. в первые дни заболевания имеет место белковоклеточная диссоциация. Для современных атипичных форм туберкулезного менингита характерно отсутствие типичной белковоклеточной диссоциации.
При туберкулезном менингите рано отмечается снижение концентрации глюкозы до 0, 83-1, 67 ммоль/л и ниже. У части больных выявляется снижение содержания хлоридов. При вирусном менингите около 2/3 случаев возбудителями являются вирус эпидемического паротита и группа энтеровирусов.
При серозных менингитах вирусной этиологии СМЖ прозрачна или слегка опалесцирует. Плеоцитоз небольшой (редко до 1000) с преобладанием лимфоцитов. У части больных в начале заболевания могут преобладать нейтрофилы, что характерно для более тяжелого течения и менее благоприятного прогноза. Общий белок в пределах 0, 6-1, 6 г/л или нормальный. У части больных выявляется снижение концентрации белка, обусловленное гиперпродукцией ликвора.
ЗАКРЫТАЯ ЧЕРЕПНО-МОЗГОВАЯ ТРАВМА
Проницаемость мозговых сосудов в остром периоде черепно-мозговой травмы в несколько раз превышает проницаемость периферических сосудов и находится в прямой зависимости от степени тяжести травмы. Для определения тяжести поражения в остром периоде можно использовать ряд ликворологических и гематологических тестов. Сюда относятся: степень выраженности и длительность наличия гиперпротеинорахии как теста, характеризующего глубину дисгемических расстройств в мозге и проницаемости гематоликворного барьера; наличие и выраженность эритроархии как теста, достоверно характеризующего продолжающееся внутримозговое кровотечение; наличие в течение 9-12 дней после травмы выраженного нейтрофильного плеоцитоза, что служит указанием на ареактивность тканей, ограничивающих ликворные пространства и угнетение санирующих свойств клеток паутинной оболочки или присоединения инфекции.
- Сотрясение головного мозга: СМЖ обычно бесцветна, прозрачна, не содержит эритроцитов или их количество незначительно. В 1-2 день после травмы цитоз нормальный, на 3-4 день появляется умеренно выраженный плеоцитоз (до 100 в 1 мкл), который снижается до нормальных цифр на 5-7 день. В ликворограмме лимфоциты с наличием незначительного количества нейтрофилов и моноцитов, макрофаги, как правило, отсутствуют. Уровень белка в 1-2 день после травмы нормальный, на 3-4 день он повышается до 0, 36-0, 8 г/л и к 5-7 дню возвращается к норме.
- Ушиб головного мозга: количество эритроцитов колеблется от 100 до 35000 а при массивном субарахноидальном кровоизлиянии достигает 1-3 млн. В зависимости от этого цвет СМЖ может быть от сероватого до красного. Из-за раздражения мозговых оболочек развивается реактивный плеоцитоз. При ушибах легкой и средней степени тяжести плеоцитоз на 1-2 день в среднем равен 160 в 1 мкл, а при тяжелой степени достигает несколько тысяч. На 5-10 сутки плеоцитоз достоверно снижается, но не достигает нормы и в последующие 11-20 сутки. В ликворогамме лимфоциты, часто макрофаги с гемосидерином. Если характер плеоцитоза меняется на нейтрофильный (70-100% нейтрофилов) – развился гнойный менингит как осложнение. Содержание белка при легкой и средней тяжести в среднем 1 г/л и не приходит к норме к 11-20 суткам. При тяжелых повреждениях головного мозга уровень белка может достигать 3-10 г/л (часто заканчивается летальным исходом).
При черепно-мозговой травме энергетический обмен мозга переключается на путь анаэробного гликолиза, что ведет к накоплению в нем молочной кислоты, и, в конечном итоге, к ацидозу мозга.
Исследование параметров, отражающих состояние энергетического обмена мозга, позволяет судить о тяжести течения патологического процесса. Снижение артериовенозной разницы по рО2 и рСО2, увеличение потребления мозгом глюкозы, нарастание веноартериальной разницы по молочной кислоте и увеличение ее в ликворе. Наблюдаемые изменения являются результатом нарушения деятельности ряда ферментных систем и не могут быть компенсированы кровоснабжением. Необходимо стимулировать нервную деятельность больных.
Вторым важным признаком изменения СМЖ при геморрагическом инсульте является ксантохромия, выявляемая у 70-75% больных. Она появляется на 2-е сутки и исчезает через 2 недели после инсульта. При очень большом количестве эритроцитов ксантохромия может появиться уже через 2-7 часов.
Увеличение концентрации белка наблюдается у 93, 9% больных и количество его колеблется от 0, 34 до 10 г/л и выше. Гипрепротеинорахия и повышенное содержание билирубина могут сохраняться длительное время и, наряду с ликвородинамическими нарушениями, могут быть причиной менингеальных симптомов, в частности головных болей, даже спустя 0, 5 – 1 год после субарахноидального кровоизлияния.
Плеоцитоз выявляют почти у 2/3 пациентов, он носит нарастающий в течение 4-6 дней характер, количество клеток колеблется от 13 до 3000 в 1 мкл. Плеоцитоз связан не только с прорывом крови в ликворные пути, но и с реакцией оболочек мозга на излившуюся кровь. Представляется важным определять в таких случаях истинный цитоз ликвора. Иногда при кровоизлияниях в мозг цитоз остается нормальным, что связано с ограниченными гематомами без прорыва в ликворное пространство, либо с ареактивностью оболочек мозга.
При субарахноидальных кровоизлияниях примесь крови может быть настолько велика, что ликвор визуально почти не отличим от чистой крови. В 1-й день количество эритроцитов, как правило, не превышает 200-500 х 109/л, в дальнейшем их количество увеличивается до 700-2000х109/л. В самые первые часы после развития небольших по объему субарахноидальных кровоизлияний при люмбальной пункции может быть получен прозрачный ликвор, однако к концу 1-х суток в нем появляется примесь крови. Причины отсутствия примеси крови в СМЖ могут быть те же, что при геморрагическом инсульте. Плеоцитоз, в основном нейтрофильный, свыше 400-800х109/л, к пятым суткам сменяется лимфоцитарным. Уже через несколько часов после кровоизлияния могут появиться макрофаги, которые можно считать маркерами субарахноидального кровоизлияния. Повышение общего белка обычно соответствует степени кровоизлияния и может достигать 7-11 г/л и выше.
СМЖ бесцветна, прозрачна, у 66% цитоз остается в пределах нормы, у остальных повышается до 15-50х109/л, в этих случаях вы- являются характерные инфаркты мозга, близко расположенные к ликворным путям. Плеоцитоз, преимущественно лимфоидно-нейтрофильный, обусловлен реактивными изменениями вокруг обширных ишемических очагов. У половины больных содержание белка определяется в пределах 0, 34-0, 82 г/л, реже до 1 г/л. Повышение концентрации белка обусловлено некрозом мозговой ткани, повышением проницаемости гематоэнцефалического барьера. Содержание белка может увеличиваться к концу первой недели после инсульта и держатся свыше 1, 5 мес. Довольно характерным для ишемического инсульта является белково-клеточная (увеличение содержания белка при нормальном цитозе) или клеточно-белковая диссоциация.
АБСЦЕСС ГОЛОВНОГО МОЗГА
Для начальной фазы формирования абсцесса характерны нейтрофильный плеоцитоз и небольшое повышения белка. По мере развития капсулы, плеоцитоз уменьшается и нейтрофильный его характер сменяется лимфоидным, причем, чем больше развитие капсулы, тем менее выражен плеоцитоз. На этом фоне внезапное появление резко выраженного нейтрофильного плеоцитоза свидетельствует о прорыве абсцесса. Если же абсцесс располагался вблизи желудочковой системы или поверхности мозга цитоз составит от 100 до 400 в 3 мкл. Незначительный плеоцитоз или нормальный цитоз может быть тогда, когда абсцесс был отграничен от окружающей мозговой ткани плотной фиброзной или гиалинизированной капсулой. Зона воспалительной инфильтрации вокруг абсцесса в этом случае отсутствует или слабо выражена.
Наряду с белково-клеточной диссоциацией, считающейся характерной для опухолей, может иметь место плеоцитоз при нормальном содержанни белка в ликворе. При глиомах больших полушарий, независимо от их гистологии и локализации, повышение белка в ликворе наблюдается в 70, 3% случаев, причем при незрелых формах – в 88%. Нормальный или даже гидроцефальный состав желудочковой и спинальной жидкости может иметь место как при глубинных, так и при врастающих в желудочки глиомах. Это, в основном, наблюдается при зрелых диффузнорастущих опухолях (астроцитомы, олигодендроглиомы), без явных очагов некроза и кистообразования и без грубого смещения желудочковой системы. В то же время те же опухоли, но с грубым смещением желудочков, обычно сопровождаются повышением количества белка в ликворе. Гиперпротеинорахия (от 1 г\л и выше) наблюдается при опухолях, расположенных на основании мозга. При опухолях гипофиза содержание белка колеблется от 0, 33 до 2, 0 г\л. Степень сдвига протеинограммы находится в прямой зависимости от гистологической природы опухоли: чем злокачественнее опухоль, тем грубее изменения в белковой формуле ликвора. Появляются бета-липопротеиды, не обнаруживаемые в норме, снижается содержание альфа-липопротеидв.
У больных с опухолями мозга, независимо от их гистологической природы и локализации, довольно часто имеет место полиморфный плеоцитоз. Клеточная реакция обусловлена особенностями биологических процессов, протекающих в опухоли на определенных этапах ее развития (некрозы, геморрагии), обусловливающих реакцию. Окружающих опухоль тканей мозга и оболочек. Клетки опухоли больших полушарий мозга в жидкости из желудочков могут быть обнаружены в 34, 4%, а в спинальном ликворе – от 5, 8 до 15 % всех наблюдений. Основным фактором, обусловливающим попадание клеток опухоли в ликвор, является характер строения ткани опухоли (бедность связующей стромы), отсутствие капсулы, а также расположение новообразования вблизи ликворных пространств.
ХРОНИЧЕСКИЕВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ (арахноидиты, арахноэнцефалиты, перивентрикулярные энцефалиты)
Содержание белка в спинномозговой жидкости у большинства больных остается в пределах нормы или незначительно повышено (до 0, 5 г/л). Увеличение белка до 1 г/л наблюдается крайне редко и чаще при менингоэнцефалитах, нежели при арахноидитах.
Менингоэнцефалит – это тяжелое воспалительное заболевание инфекционной природы, поражающее центральную нервную систему (оболочки мозга, его вещество, в иных случаях – спинной мозг). Болезнь представляет собой как бы сочетание двух патологических состояний: менингита, при котором поражаются мягкие мозговые оболочки, и энцефалита, протекающего с поражением мозгового вещества.
Заболевание могут вызывать различные микроорганизмы: бактерии, вирусы, простейшие и даже свободноживущие в пресных водоемах амебы. Многие из них переносятся иксодовыми клещами, поэтому пик заболеваемости отмечается в периоды активной жизнедеятельности насекомого. Кроме этого, болезнь может быть самостоятельной или стать осложнением других инфекционных процессов в организме (грипп, пневмония, туберкулез, корь, паротит и многие другие).
Менингоэнцефалит, как самостоятельное заболевание, чаще диагностируется у детей (менингококковая инфекция), хотя не исключено и у взрослых, нередко имеет летальный исход, часто оставляет последствия в виде более или менее грубых изменений структур головного мозга, реже – проходит абсолютно бесследно.

Лечение менингоэнцефалита всегда сложно, поскольку для его начала необходимо выявить возбудителя (терапия вирусных и лечение бактериальных инфекций между собой не имеют ничего общего).
Причины воспалительного процесса в ЦНС
Менингоэнцефалит отличается особой полиэтиологичностью, ведь посодействовать развитию патологического процесса могут самые разные обстоятельства. Наряду с инфекционными возбудителями, свою отрицательную роль могут сыграть инфекционно-аллергические и токсические факторы. Все причины, вызывающие менингит и энцефалит, являются одновременно предпосылками формирования сочетанного заболевания (воспаление мозга и мягкой мозговой оболочки). От этого тяжесть изолированного заболевания и его прогноз, естественно, усугубляются.
И все же наиболее частой причиной опасного воспаления, локализованного в ЦНС, являются инфекции:

- Бактериальные – это всевозможная кокковая флора (стрепто-, стафило-, пневмо-, менингококки), листерии, туберкулезная палочка и пр.;
- Вирусные – и широко распространенные, и редкие даже для необъятной территории РФ вирусы: клещевого энцефалита, кори, ветрянки, гриппа, герпеса, бешенства, паротита, лихорадки Западного Нила и др.;
- Инфекции, вызываемые простейшими, такими, как токсоплазма, малярийный плазмодий;
- Болезни, обусловленные проникновением в организм мутантных видов амеб, обитающих в пресных водоемах.
Предрасполагающим фактором при данной патологии является возраст – у детей, ввиду недостаточного развития системы иммунитета и несостоятельности гематоэнцефалического барьера, менингоэнцефалит диагностируется намного чаще, нежели у взрослых. Правда, пожилых людей в данном случае можно приравнять к детям – иммунитет у них низкий, противостоять инфекциям организм в полной мере уже не может. Группу риска в отношении этого воспалительного процесса также составляют пациенты, имеющие острую или хроническую патологию ЛОР-органов – синуситы, гаймориты, мастоидиты и пр. У таких больных, как правило, в качестве осложнения развивается гнойный менингоэнцефалит.
Как возбудителю удается проникнуть в головной мозг из внешней среды?
Каким способом инфекционный агент попадает в организм – зависит от вида возбудителя, например:
иксодовый клещ: переносчик клещевого энцефалита
Наиболее частый путь проложен иксодовыми клещами, которые при укусе приносят нейротропный вирус. Кстати, клещ способен внести сразу несколько возбудителей (микст-инфекция), которые весьма сложно идентифицировать лабораторными методами в кратчайшие сроки. Такой вариант нередко встречается у взрослых, которые любят проводить время в парках, и лесах, но не очень заботятся, чтобы по максиму одеждой и обувью защитить свою кожу;
Инфицирование возбудителем оболочек мозга происходит преимущественно гематогенным путем, на втором месте лежит лимфогенный путь распространения, однако прямое попадание бактериальной флоры при прорыве гнойных полостей либо открытых черепно-мозговых травмах также не исключается.
Как классифицируют данный воспалительный процесс?
Пациента может и не интересовать, как называют данный процесс врачи, однако они различают следующие формы заболевания:
- Первичный менингоэнцефалит, который развивается вследствие инфицирования арбовирусом (при укусе клеща), вирусом герпеса, бешенства, возбудителем тифа, в результате проникновения в ЦНС бледной трепонемы (нейросифилис);
- Вторичный процесс – он, как правило, выступает в качестве осложнения другой патологии инфекционной природы (ветрянка, корь, туберкулез, гнойные заболевания ЛОР-органов, вызванные бактериальной флорой).

Характер течения воспалительного процесса в центральной нервной системе также может включать несколько форм:
- Молниеносный вариант – болезнь развивается бурно, состояние пациента резко ухудшается в считанные часы, нередко в подобной ситуации наступает смерть;
- Острый менингоэнцефалит – клиническая картина разворачивается довольно быстро, однако не так стремительно, как в случае молниеносной формы, поэтому у врачей есть больше времени для оказания помощи;
- Подострое течение – здесь отмечается медленное развитие стертой симптоматики;
- Хронический воспалительный процесс – вялое развитие событий, признаки воспаления в головном мозге выражены слабо, болезнь протекает с ремиссиями и обострениями.
Кроме этого, менингоэнцефалиты различаются по характеру воспалительной реакции, которую определяет качество цереброспинальной жидкости:
- Серозные – ликвор прозрачный, небольшое количество белка, численность лимфоцитов резко повышена;
- Гнойные – на фоне мутного (гнойного) ликвора огромное количество лейкоцитов;
- Геморрагические – ликвор из-за примеси крови приобретает красноватый оттенок, в ликворе, помимо белых клеток крови, большое количество эритроцитов.
Причиной гнойного менингоэнцефалита в большинстве случаев выступает бактериальная инфекция (гноеродная кокковая флора, синегнойная палочка и др.), развитие серозной и геморрагической формы преимущественно обязано воздействию вирусов.
Общие симптомы
общие менингеальные знаки
Высокая температура тела;
Безусловно, сам пациент или его родственники вряд ли могут разобраться во всех менингеальных знаках, но некоторые из них многие люди легко могут освоить самостоятельно. Например, попробовать голову пациента наклонить так, чтобы подбородок коснулся грудины: при отсутствии менингеальных симптомов это получается легко, больной будет реагировать даже на малейшее движение вниз.
Заподозрив опасный недуг, можно попросить человека с подозрением на менингоэнцефалит пассивно согнуть ногу (лежа на спине) под углом 90 градусов (тазобедренный и коленный сустав), а затем заставить его разогнуть конечность. При раздражении мозговых оболочек это не получится, поэтому данное состояние следует расценивать как менингеальный знак (симптом Кернига).

Отдельные формы
Описываемое патологическое состояние классифицируют еще и по роду возбудителя и если он достоверно установлен, болезнь представляют в более точном варианте, указывающем на ее виновника. К примеру, герпетический менингоэнцефалит (он же, естественно, и вирусный), туберкулезный, подразумевающий бактериальную природу, название амебный уже указывает на то, что виновником заболевания стали простейшие.
Вирусный менингоэнцефалит ( на примере герпетического)

Что ожидать от герпетического менингоэнцефалита, заранее предугадать невозможно, его течение довольно вариабельно:
- Острый менингоэнцефалит;
- Хронический процесс;
- Развитие болезни под маской других патологических состояний центральной нервной системы (новообразования, эпилепсия, инсульты, слабоумие);
- Почти бессимптомное течение.
Первые признаки данного заболевания:
- Интенсивная головная боль, локализующаяся в большинстве случаев в лобной и теменной области;
- Высокая температура тела;
- Нарушение сознания, изменение поведенческих функций, вплоть до полной неадекватности;
- Общемозговая симптоматика, на фоне которой нередко можно наблюдать очаговые проявления.
Вирусный характер болезни (особенно в случае острого менингоэнцефалита) не сулит пациенту ничего хорошего: нередко к деструктивным изменениям в головном мозге прибавляется ДВС-синдром, усугубляющий и без того тяжелое состояние больного.
Терапевтическое воздействие производится преимущественно за счет противовирусного препарата – ацикловира (виролекс), который заметно повышает шансы на жизнь, однако, к сожалению, не защищает от тяжелых последствий.
Видео: лекция о герпетическом энцефалите у детей
Бактериальный менингоэнцефалит (туберкулезный и др.)
Виновниками туберкулеза ЦНС и мозговых оболочек, который в 70% случаев приводит к туберкулезному менингоэнцефалиту, являются микобактерии (Mycobacterium tuberculosis). Представляя собой самую тяжелую форму туберкулезного поражения головного мозга, данная форма заболевания дает довольно яркую клиническую картину:
- Выраженную головную боль, неподвластную анальгезирующим средствам;
- Прогрессирующее недомогание и общую слабость, потерю аппетита;
- Тошноту, рвоту, светобоязнь;
- Снижение концентрации внимания;
- Вегетативные расстройства;
- Выраженную общемозговую симптоматику;
- Присутствие менингеальных знаков;
- Симптомы очаговых поражений (нарушение двигательных функций, поражение ЧМН), что говорит о вовлечении мозговых оболочек и вещества мозга;
- Развитие гидроцефалии.

Течение болезни при более-менее благоприятных обстоятельствах (летальность составляет приблизительно 30%) – долгое и мучительное, оставляющие серьезные последствия.
Основное лечение менингоэнцефалита бактериальной природы – антибиотики.
Видео: лекция о туберкулезном менингоэнцефалите
Амебный менингоэнцефалит
Амебный менингоэнцефалит является результатом проникновения в организм (обычно посредством верхних дыхательных путей) мелких свободноживущих простейших, называемых амебами.
Помимо пресных водоемов, не исключено встретить амебу в воде из-под крана, в горячих водах минеральных источников или в сбрасываемых электростанциями, а также в почве, на овощах и грибах. В редких случаях амеба может населять носовые ходы детей, не причиняя им особого вреда.
Амебный менингоэнцефалит наиболее часто диагностируют у детей и у взрослых людей молодого возраста. Патологическое состояние может проявлять себя в виде двух форм:

- Острый менингоэнцефалит с инкубационным периодом от 2 дней до 2 недель и довольно внезапным началом. Клинические проявления дебютируют резкой головной болью, тошнотой и рвотой, быстрым подъемом температуры тела. При этом варианте болезни сначала проявляют себя симптомы менингита (менингеальные знаки, общемозговая симптоматика), признаки поражения вещества мозга несколько задерживаются и развиваются позже. Данная форма крайне опасна, большей части пациентов не удается прожить более недели от появления начальных признаков;
- Гранулематозный амебный менингоэнцефалит характеризуется вялым течением, могут пройти недели, а то и месяцы. Симптомы на начальной стадии больше похожи на развитие объемного образования в головном мозге либо многоочагового поражения, проявляясь, судорожными припадками, напоминающими эпилептические, гемипарезом, личностными изменениями. В иных случаях симптомы психического расстройства выходят на первый план, затрудняя диагностику.
- Амфотерицин В + рифампицин + хлорамфеникол;
- Амфотерицин В + рифампицин + кетоконизол.
Последствия менингоэнцефалита

Самые выраженные последствия ожидают в случае внутриутробного инфицирования вирусом. Если малыш не погиб в утробе матери, то впоследствии ей предстоит бороться с гидроцефалией, эпилепсией, психическими расстройствами. Такие дети хоть и плохо растут, но умственное развитие еще больше отстает. Кроме этого, учитывая поражение центральной нервной системы на ранних этапах ее становления, парезы и параличи считаются естественным явлением.
Менингоэнцефалит особую опасность представляет для детей, ведь в случае благоприятного завершения процесса, оболочки и вещество мозга все равно оказываются не настолько здоровы, как до болезни. Часто затормаживается дальнейшее развитие ЦНС, страдает интеллект и, хотя некоторые дети продолжают неплохо успевать в школе (кому повезло), точные науки начинают им даваться с трудом. Кроме этого, всегда остается опасность развития судорожного синдрома и эпилепсии.
У взрослых тоже возникают проблемы, наименьшие из них – снижение слуха и зрения. И еще, казалось бы, интеллектуальные способности сформированы, поэтому и неприятностей с этой стороны не ожидается. Ан нет, различные виды слабоумия, психические расстройства на фоне эпилептических припадков, парезов и параличей могут подстерегать любого человека, пусть он вчерашний ученый или простой работяга.
Однако некоторым действительно везет, кроме диспансерного учета у невролога и периодических осмотров, им больше ничто не напоминает о пережитых страданиях.
В отделение патологии недоношенных и новорождённых детей больницы скорой медицинской помощи города Краснодар 12 марта 2018 года из отделения реанимации и интенсивной терапии была переведена девочка на пятые сутки жизни.
Жалобы
Проведение антибактериальной, дегидратационной терапии не влияли на изменение неврологического статуса ребёнка.
Анамнез
В родильном отделении больницы скорой медицинской помощи города Краснодара 7 марта 2018 года родилась девочка на 35 неделе гестации с весом 2100 грамм, 5-6 баллов по Апгар, дыхательная недостаточность II степени по шкале Сильвермана. После рождения ребёнок был переведён в отделение реанимации, проводилась аппаратная поддержка дыхания, коррекция метаболических нарушений, проводилась антибактериальная терапия по поводу врождённой пневмонии.
Мать ребенка 28 лет, роды вторые (I беременность в 2014 году — мальчик, весом 3100 грамм, здоров; II беременность в 2016 году — медицинский аборт; III беременность — настоящая). В анамнезе матери не отмечалось соматической патологии. Беременность в первой половине протекала на фоне токсикоза. Во второй половине — острая респираторная вирусная инфекция на 28 неделе. Роды экстренные, безводный промежуток 10 часов. В анамнезе матери отмечались герпетические высыпания на лице. В области гениталий герпетических высыпаний не отмечалось.
Обследование
Ребёнок находился в позе полуфлексии. На осмотр открывал глаза. Рефлексы орального автоматизма снижены. Отмечалось угнетение спинальных автоматизмов и надсегментарных миелоэнцефальных рефлексов. При проведении осмотра отмечалось диффузное снижение мышечного тонуса в конечностях, мраморность кожных покровов. На момент осмотра судорог не отмечалось. Также регистрировалась лабильность пульса и артериального давления.
В общем анализе крови отмечалось увеличение уровня лейкоцитов. При проведении лабиальной пункции на шестые сутки отмечалось увеличение лейкоцитов до 100*106, смешанный плеоцитоз. Анализ ПЦР крови и ликвора на шестые сутки жизни на герпесвирусные инфекции был отрицательный. Лишь через десять дней (на шестнадцатые сутки жизни) плеоцитоз приобрёл лимфоцитарный характер, пришли положительные результаты ПЦР крови и ликвора на вирус простого герпеса I типа. При проведении нейросонографии регистрировалось повышение эхогенности перивентрикулярных областей.
Диагноз
Лечение
На шестые сутки жизни, после получения общего анализа ликвора, ребёнку были назначены антибиотики в менингитных дозировках и ацикловир (после консультации с инфекционистом и клиническим фармакологом). На шестнадцатые сутки жизни была откорректирована противовирусная терапия с учётом данных ПЦР.
Через три недели после рождения ребёнок начал самостоятельно сосать, мышечный тонус нормализовался, физиологические рефлексы вызывались, но быстро истощались. При осмотре ребёнок открывал глаза, проявлял двигательную активность. Пациентка находилась в позе флексии. Сохранялись редкие срыгивания после еды.
После выписки из отделения выхаживания было рекомендовано наблюдение за ребёнком у невролога на первом году жизни. Какого-либо медикаментозного лечения ребёнку не требовалось.
Заключение
Данный клинический случай подтверждает известные затруднения в дифференциальной диагностики этиологии неонатальных менингитов и энцефалитов. Своевременно начатое лечение позволяет избежать тяжёлых последствий инфекционного поражения нервной системы. Также заражение герпес-вирусной инфекцией возможно интранатально без явной клинической картины герпес-вирусной инфекции у матери.
Читайте также:

