Меры профилактики раневой инфекции перед плановой операцией
Обновлено: 22.04.2024
М.Н. ЗУБКОВ, доктор медицинских наук, профессор, вице-президент Межрегиональной ассоциации клинической микробиологии и антимикробной химиотерапии (МАКМАХ). ПРОФИЛАКТИКА И ТЕРАПИЯ ХИРУРГИЧЕСКОЙ ИНФЕКЦИИ
Основная роль антибиотикопрофилактики в хирургии заключается в предупреждении инфекций, возникающих вследствие операции или других инвазивных вмешательств либо имеющих прямую связь с ними, а побочная цель - в уменьшении продолжительности и стоимости пребывания больного в стационаре.
Ее суть состоит в достижении эффективных концентраций антибиотика в операционной зоне во время ее микробного загрязнения и поддержании бактерицидного уровня препарата в течение всей операции и первых 3-4 часов после оперативного вмешательства, поскольку этот отрезок времени является решающим для размножения и адгезии на клетках хозяина попавших в рану микробов, что служит пусковым механизмом для начала инфекционно-воспалительного процесса в ране. Антибиотикопрофилактика, начатая по истечении этого периода, является запоздалой, а ее продолжение после окончания операции в большинстве случаев излишним, поскольку профилактическая роль антибиотика в основном заключается в уменьшении пороговой концентрации бактерий в ране и препятствии адгезии возбудителя.
Антибиотикопрофилактика показана там, где особенно высок риск развития послеоперационной инфекции (например, при "условно чистых" операциях на органах брюшной, грудной полости и малого таза, затрагивающих слизистые оболочки, населенные микрофлорой) или если ее последствия могут представлять угрозу здоровью и жизни больного (при некоторых "чистых" операциях, связанных с имплантацией сосудистых шунтов или искусственных протезов, когда немногочисленные и малопатогенные микроорганизмы с поверхности кожи могут проникнуть глубоко в рану и вызвать ее нагноение). Если хирург заранее уверен, что встретится с инфекцией в процессе операции (например, при "условно чистых" или "загрязненных" вмешательствах), в качестве антибактериальной защиты проводят превентивную антибиотикотерапию, которая должна быть ограничена самыми жесткими показаниями: патофизиологическими предпосылками (например, перфорация органов желудочно-кишечного тракта в результате проникающего ранения или имеющая эндогенное происхождение, сопровождающаяся загрязнением кишечной микрофлорой брюшной полости и прилегающих к ней структур); наличием входных ворот инфекции (например, открытые переломы); биологией потенциального возбудителя. Раннее назначение антибиотиков, обычно в течение 12 часов с момента перфорации или травмы, расценивается как профилактика, более позднее, когда развились признаки серьезной инфекции, - как лечение.
В большинстве случаев для профилактики послеоперационной инфекции достаточно одной дозы антибиотика (во время премедикации; вторая доза вводится при 3-часовых и более длительных операциях) либо проводят сверхкраткий курс антибиотикопрофилактики, ограниченный двумя-тремя дозами препарата. Такая тактика, основанная на многочисленных клинических и экспериментальных наблюдениях, вполне эффективна, снижает вероятность побочных действий антибиотика, ограничивает возможность развития устойчивости бактерий к химиопрепаратам, обеспечивает меньшую стоимость лечения. Профилактическое применение антибиотиков задолго до операции или более 48 часов в послеоперационном периоде ведет к нарушению биоценоза желудочно-кишечного тракта и колонизации верхних его отделов микрофлорой толстой кишки с возможным развитием эндогенной инфекции путем бактериальной транслокации условных патогенов через лимфатическую систему тонкого кишечника. Кроме того, возрастает опасность суперинфекции у оперированных больных за счет селекции антибиотикорезистентных штаммов. Поэтому антибиотик следует вводить больному в соответствующей дозе непосредственно перед операцией (за 10-15 мин. внутривенно во время наркоза либо за 40-60 мин. до операции внутримышечно) с последующими повторными инъекциями по показаниям, но не более 24-48 часов.
Для профилактики раневой инфекции чаще всего назначают цефалоспорины 1-го и 2-го поколения (препараты 3-го поколения существенно дороже и используются в основном для лечения), так как они имеют достаточный спектр бактерицидной активности против наиболее распространенных возбудителей послеоперационных осложнений, и прежде всего стафилококков; при парентеральном введении создают высокие концентрации в операционной зоне; отличаются малой токсичностью и частотой побочных действий. К числу недостатков всех цефалоспоринов следует отнести неэффективность при энтерококковой инфекции; плохое проникновение через гематоэнцефалический барьер (кроме цефтазидима и некоторых других препаратов 3-го поколения); возможное увеличение нефротоксичности в комбинации с аминогликозидами.
Помимо цефалоспоринов при высоком риске стафилококковой хирургической инфекции у ортопедических и некоторых других категорий больных применяют ванкомицин. При колоректальных операциях наряду с пероральным промыванием кишечника изотоническим раствором за сутки до операции больному назначают внутрь неомицин, 1 г + эритромицин, 1 г в 13, 14 и 22 ч., а в день операции - цефалоспорины 1-2-го поколения в/в дважды с интервалом 8 ч. При катаральном и флегмонозном аппендиците достаточно однократного применения в/в цефазолина (1 г) или цефуроксима (1,5 г) либо проведения короткого курса (2-3 дозы). При гангренозном аппендиците дополнительно вводят метронидазол, 0,5 г в/в. Если в послеоперационном периоде возникает подозрение на перитонит и/или абсцедирование, продолжают применение антибиотиков в течение 3-5 суток. Схемы профилактики при других видах операций приведены в таблице 1.
Таблица 1
ВАРИАНТЫ АНТИБИОТИКОПРОФИЛАКТИКИ (АП) РАНЕВОЙ ИНФЕКЦИИ ПРИ НЕКОТОРЫХ ВИДАХ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВ*
1 Первую дозу цефалоспорина вводят в/в во время вводного наркоза (за 10-15 мин. до разреза); при операциях > 3 ч антибиотик вводят повторно; при реконструктивных операциях на сосудах и нервных окончаниях АП продлевают до 2-3 сут.
2 До 3 дней, по показаниям.
3 В/в капельно в течение 1 часа.
4 Профилактика газовой гангрены.
5 АП не показана при катетеризации сердца.
6 О преимуществах нетилмицино см. в тексте.
7 Цефалоспорины 2-го поколения, активные против анаэробов.
8 При брюшном доступе повторяют по 1 г в/в через 8 ч и 16 ч.
Антибиотикопрофилактику считают неэффективной, если в области первичного операционного разреза возникла послеоперационная инфекция; если появилась необходимость дренирования операционной зоны; если в течение 4-недельного периода после первичной операции понадобилось не находящее объяснений применение антимикробных препаратов.
При уже развившейся хирургической инфекции на начальном этапе лечения назначение антибиотиков носит эмпирический характер до получения результатов бактериологического исследования материалов из раны. При этом выбор тактики химиотерапии зависит от характера хирургической патологии и локализации гнойно-воспалительного процесса, определяющих специфику раневой инфекции. Вполне естественно, что при перитонитах, где превалирует анаэробная флора в ассоциации с энтеробактериями, и при инфекциях костей и мягких тканей, где ведущую роль играют стафилококки, алгоритмы эмпирической антибиотикотерапии будут различными.
При травматических ранах с признаками нагноения назначают комбинированную терапию, учитывая лидирующее положение стафилококков и высокий удельный вес микробных ассоциаций (до 70%) при посттравматических инфекциях. Обычно используют гентамицин (4,5 мг/кг/сут) в сочетании с оксациллином (4-6 г/сут), цефазолином (3 г/сут) или линкомицином (1200-1800 мг/сут) при высоком риске развития анаэробной инфекции.
Состав микрофлоры при перитонитах
Стрептококки - 11%
Энтеробактерии - 24%
Стафилококки - 5%
Псевдомонады - 12%
Анаэробы - 48%
Состав микрофлоры при инфекциях костей и мягких тканей
Стрептококки - 7%
Энтеробактерии - 15%
Стафилококки - 60%
Псевдомонады - 8%
Анаэробы - 10%
Но особенно следует выделить антисинегнойную активность пиперациллина и тазоцина, что позволяет использовать их для лечения внутрибольничных инфекций в виде монотерапии (4 г/0,5 г тазоцина) или в комбинации с нетилмицином (4,5 г/кг/сут).
При острых интраабдоминальных инфекциях (80% из них возникает вне стационара), когда точная локализация неизвестна, лечение направляют против смешанной флоры кишечника, включающей факультативные грамотрицательные бактерии и часто встречающиеся анаэробы (Clostridium spp. и Bacteroides spp.). Одна из применяемых в настоящее время схем противоинфекционной терапии предусматривает комбинацию аминогликозида с антианаэробным препаратом (метронидазол или клиндамицин). Многие хирурги предпочитают добавлять ампициллин для воздействия на энтерококки. Назначение тазоцина по эффективности не уступает комбинированному препарату имипенем-циластатин. Широко используются также комбинации цефалоспоринов 3-го поколения с клиндамицином или метронидазолом. Парентеральную терапию продолжают до исчезновения лихорадки, снижения числа лейкоцитов крови (< 1200 в 1 мкл), восстановления функции кишечника (обычно примерно после недельного курса лечения).
Инфицирование послеоперационных ран относится к разряду внутрибольничных инфекций, где возможны разные варианты эмпирической антибиотикотерапии в зависимости от тяжести течения раневой инфекции и особенностей формирования резистентности бактерий к антибиотикам. При неосложненных инфекциях мягких тканей, как правило, обходятся монотерапией, в то время как осложненные инфекции, требующие повторных оперативных вмешательств и нередко приобретающие системный характер, чаще нуждаются в назначении антибиотиков более широкого спектра действия или проведении комбинированной антибиотикотерапии.
При лечении тяжелых и жизнеугрожающих инфекций препаратами выбора становятся аминогликозиды, спектр действия которых охватывает подавляющее большинство аэробных грам(-) и грам(+) бактерий (за исключением стрептококков и пневмококков), а в комбинации с пенициллином они оказывают синергическое бактерицидное действие на энтерококки. Однако, несмотря на их активность против Staphylococcus spp., аминогликозиды не следует применять в качестве стартовой монотерапии при стафилококковой инфекции. Гентамицин наиболее широко применяется в практике, однако имеется много свидетельств о высоком удельном весе резистентных к нему микробных изолятов от стационарных больных, что снижает эффективность лечения хирургической инфекции. Наиболее активным среди аминогликозидов является нетилмицин (нетромицин), который, по нашим данным, превосходит другие антибиотики этой группы и некоторые цефалоспорины 3-го поколения и сопоставим по антимикробной эффективности лишь с фторхинолонами (см. табл. 2). У него наименее выражен ото- и нефротоксический эффект, что позволяет вводить суточную дозу препарата однократно без увеличения частоты побочных осложнений. Такой режим введения существенно увеличивает ударное антимикробное действие нетилмицина и имеет экономические преимущества. По стоимости он гораздо доступнее амикацина и, по нашему опыту, должен занять первостепенное положение среди аминогликозидов в лечении оппортунистических инфекций.
Таблица 2
АНТИБИОТИКОЧУВСТВИТЕЛЬНОСТЬ ГРАМ(-) БАКТЕРИЙ ПРИ ИНФЕКЦИЯХ КОСТЕЙ И МЯГКИХ ТКАНЕЙ (%)
| Антибиотики | E.col (n=28) | KES* (n=48) | Proteus spp. (n=22) | P.aeruginoza (n=37) | Acinetobacter (n=19) |
| Нетромицин | 100 | 90 | 73 | 74 | 88 |
| Амикацин | 75 | 40 | 57 | 67 | 75 |
| Тобрамицин | 58 | 34 | 22 | 63 | 43 |
| Гентамицин | 50 | 36 | 30 | 58 | 27 |
| Цефтазидим | 83 | 40 | 70 | 57 | 40 |
| Ципрофлоксацин | 100 | 88 | 79 | 83 | 80 |
Нельзя обойти вниманием и фторхинолоны, которые все чаще становятся препаратами выбора при системных инфекциях. Среди них ципрофлоксацин (ципробай, ципринол) занял прочное место в хирургической практике, в то время как другие препараты этой группы чаще используются для лечения больных терапевтического профиля. Наличие инфузионной формы препарата существенно повышает его конкурентоспособность при лечении больных в реанимационных отделениях, а возможность проведения так называемой ступенчатой терапии с переходом на пероральный прием антибиотика (без существенного снижения его концентрации в крови из-за высокой биоусвояемости при всасывании) значительно снижает стоимость курса лечения. Область применения ципрофлоксацина в хирургии с одинаковым успехом распространяется на инфекции костей и мягких тканей, интраабдоминальные инфекции, инфекции органов грудной полости и малого таза и, конечно, при лечении сепсиса.
Таким образом, применение антибиотиков в хирургии с профилактической и лечебной целью имеет свои особенности, а знание спектра возбудителей хирургических инфекций и антимикробного действия химиопрепаратов является основой правильного их применения в клинике.
Для профилактики раневой инфекции на этапах медицинской эвакуации (ЭМЭ) большое значение имеют как медицинские, так и организационные мероприятия. Рассмотрены основные принципы профилактики и лечения раневой инфекции на различных ЭМЭ в зависимости от сроков поступления раненого, а также профилактика местной и общей инфекции.
Medical as well as organizational measurements are essential in oder to prevent wound infection at the stage of medical evacuation(SME).these are the main prevention and treatment principles with the reference to SME depending on the terms the wounded was evacuated ,and also prevention of local and general infection
Любая огнестрельная рана является первично инфицированной. Это связано с тем, что в момент ранения с ранящим снарядом в рану заносятся микроорганизмы, находящиеся на одежде, коже. При несвоевременном оказании помощи в рану могут поступать микроорганизмы из окружающей среды. Такое микробное загрязнение называется вторичным инфицированием. И в первом, и во втором случаях этот путь микробной контаминации раны называется экзогенным, или инвазивным (микробная инвазия).
Более опасной является инвазия госпитальной флоры, устойчивой даже к современным бактериальным средствам. Она проникает через верхние дыхательные пути - в процессе ИВЛ и санационных мероприятий, через мочевые пути в процессе катетеризации, а также через кожный покров в ходе выполнения многочисленных инвазивных лечебных и диагностических манипуляций. Инфекционный процесс, вызванный госпитальной микрофлорой, получил название госпитальной или нозокомиальной инфекции.
Кроме того, у больных с огнестрельными ранениями на фоне развития травматической болезни возможны и другие пути попадания микроорганизмов в рану. Это так называемый эндогенный путь. Как указывает Е.К. Гуманенко [1], первым этиологическим фактором возникновения таких осложнений выступает эндогенная микрофлора. Причем могут развиваться не только местные, но и висцеральные и генерализованные инфекционные осложнения. Источником эндогенной инфекции является кишечная микрофлора, проникающая в систему кровообращения, так как при травматической болезни и нарушении микроциркуляции, в частности кишечника, стенка кишечных капилляров становится проницаемой для микроорганизмов: энтеробактерий, протея, кишечной палочки и других. Поступая в кровь, эти условно патогенные микроорганизмы попадают в поврежденные ткани, где обретают новую среду обитания. И если новая среда благоприятствует их существованию и развитию, то формируется новый метастатический патологический очаг раневой инфекции. Очень важным фактором его формирования является не только поступление эндогенной микробной флоры в зону раны (так называемая генерализованная транслокация (по Е.К. Гуманенко), но и состояние раны (объем первичного и вторичного некроза, степень нарушения кровообращения) и эффективность первичной хирургической обработки (удаление некротических тканей, восстановление кровообращения).
Местная и общая раневая инфекция - распространенное осложнение огнестрельных ранений. Качественная профилактика и лечение ее возможны только при четком и последовательном выполнении на каждом этапе алгоритма поставленных задач (таблица).
Алгоритм профилактики и лечения инфекционных осложнений огнестрельных ранений
- Обеспечение ППИ, АИ-1.
- Профилактические прививки противостолбнячные.
- Быстрый и щадящий вынос из очага
- Соблюдение асептики и антисептики.
- Асептические повязки.
- Введение антибиотиков широкого спектра действия.
- Транспортная иммобилизация.
- Профилактика и лечение травматического и геморрагического шока
- Ранняя и полноценная ПХО.
- Исключение первичного хирургического шва
- Активная и пассивная профилактика столбняка.
- Пассивная профилактика анаэробной инфекции
- Местная аэрация тканей (внутрикожное, подкожное введение кислорода и озона).
- Внутривенное озонирование.
- ГБО.
- Кислородная ингаляция
Профилактика раневой инфекции на этапе первой медицинской помощи (на поле боя)
Здесь нет никакой этиологической дифференциации в способе профилактики. Осуществляются, главным образом, организационные и медицинские мероприятия.
Организационные: быстрый и щадящий вынос раненого с поля боя.
Медицинские: асептическая повязка на рану, прием пероральных антибиотиков из АИ - 1, транспортная иммобилизация.
Профилактика раневой инфекции на этапе доврачебной помощи (МПБ)
На данном этапе появляются элементы дифференцированного подхода к этиологической профилактике раневой инфекции. В обязательном порядке должна учитываться угроза развития не только местной, но и общей раневой инфекции (столбняк, газовая гангрена). На данном этапе нужно проводить следующие виды профилактики: организационные и медицинские.
Организационные: быстрая и щадящая эвакуация на следующий этап. Дифференциация профилактических мер должна включать мероприятия, направленные на предупреждение столбняка и газовой гангрены.
Медицинские: дополнительные асептические повязки; транспортная иммобилизация табельными средствами; в/м введения антибиотиков широкого спектра действия. Дополнительные меры профилактики должны включать мероприятия, направленные на предупреждение столбняка и газовой гангрены: тщательная оценка правильности и времени наложения жгута, обязательная ингаляция кислорода, особенно у раненых группы риска развития анаэробной инфекции.
Профилактика раневой инфекции на этапе первой врачебной помощи (МПП)
На этом этапе подключается специфический вид профилактики.
Организационные: проведение эвакотранспортной сортировки раненых, относящихся к группе особого риска.
Медицинские: обкалывание раны антибиотиками пролонгированного типа и широкого спектра действия, подбинтовывание повязок, табельная транспортная иммобилизация. Контроль жгута (правильность, время), смена жгута, замена его на другие виды временной остановки кровотечения (более щадящие, менее травматичные), противошоковая терапия.
Специфическая: ингаляция кислорода, местная аэрация тканей вокруг раны, в/в введение озонированных растворов, введение специфических сывороток (противостолбнячной и противогангренозной).
Профилактика и лечение раневой инфекции
на этапе квалифицированной помощи (ОМедБ)
Организационные мероприятия - тщательная внутрипунктовая сортировка раненых (ведение группы первой и второй очереди); эвакуационно-транспортная сортировка: эвакуация раненых в первую очередь с ранениями крупных магистральных сосудов в ГБФ.
Медицинская профилактика: антибиотикотерапия, соблюдение принципов асептики - антисептики, послеоперационная лечебная иммобилизация, окончательное выведение раненого из шока.
На данном этапе на первый план выходит специфический вид профилактики раневой инфекции. Это, прежде всего, ранняя первичная хирургическая обработка раны. Устранение компартмент-синдрома. Обязательны местная и общая аэрация и озонирование. Исключение раннего первичного хирургического шва. Введение специфических сывороток. Помимо профилактических мер на данном этапе необходимо лечение раневой инфекции. Это касается главным образом газовой гангрены (молниеносная форма). Для этого на данном этапе имеется анаэробная палатка, в которой проводятся специфические лечебные мероприятия: хирургические (лампасные разрезы, ампутация), введение лечебных доз противогангренозной сыворотки, местная аэрация тканей в зоне развития инфекции, внутривенное введение озонированных растворов.
Профилактика и лечение раневой инфекции в ГБФ
На госпитальном этапе эвакуации профилактика раневой инфекции должна включать прежде всего специфические методы: первичную и вторичную хирургическую обработку ран, восстановление сосудистого кровотока. Общая и местная аэрация тканей, стабилизация костных отломков, ампутации по вторичным показаниям. Введение сывороток. Большое внимание должно уделяться медицинским видам профилактики, направленным на борьбу с инвазивной госпитальной или нозокомиальной инфекцией: обязательное соблюдение правил асептики и антисептики, использование одноразового инструментария (шприцы, инструменты, интубационные трубки, катетер и маски для ингаляций и т.д.), т.к. многоразовый является носителем госпитальной микрофлоры. Активное лечение в каждом периоде травматической болезни.
Наиболее тяжелую группу представляют ранения, осложненные анаэробной инфекцией. В зависимости от ЭМЭ частота этого осложнения составляет от 0,08 до 15 % раненых. Профилактические меры, направленные на предупреждение данного грозного и тяжелого осложнения, делятся на неспецифические (организационные и медицинские) и специфические. Эти меры должны быть соблюдены на всех этапах оказания медицинской помощи. На первом месте стоит правильная, своевременная и эффективная эвакуация на этапы МПП и ОМедБ. При оказании первой медицинской, доврачебной и первой врачебной помощи необходимо всегда помнить о том, что: 1) наложенный жгут - это огромная опасность, если он наложен неправильно, не по показаниям, просрочено время; 2) ранение крупных магистральных сосудов - это показание к эвакуации в первую очередь.
Специфическая профилактика - это, прежде всего, проведение ранней первичной хирургической обработки с широкой фасциотомией, наложение сосудистого шва в первые 6 часов с момента ранения, тщательное дренирование раны (проточные дренажи), аэрирование раны, категорическое исключение показаний для наложения первичного хирургического шва.
В случаях, когда раненые поступают с клинической картиной анаэробной инфекции, необходимо помимо традиционного хирургического вмешательства (лампасные разрезы, некрэктомия) использовать ГБО и озонированные растворы.
Под нашим наблюдением находилось 20 человек с газовой гангреной после ранения. Они поступили на различных сроках. Причины в основном связаны с нарушением вышеуказанных принципов оказания помощи пострадавшим. После проведения вторичной хирургической обработки раны (лампасные разрезы, иссечение нежизнеспособных тканей), назначения лечебных доз противогангренозной сыворотки были использованы методика гипербарической оксигенации (2 раза в день), в/в введение озонированных растворов, местная аэрация тканей (Каралин А.Н., Терентьев В.А., Азизова Р.Х. Способ лечения ран: Пат. №2219932 от 27.12.03), дезинтоксикационная терапия.
Результатом нашей тактики лечения больных газовой гангреной стали их выздоровление и отсутствие ампутации.
Заключение. На всех этапах оказания медицинской помощи нужно помнить о том, что: любое огнестрельное ранение представляет угрозу развития анаэробной инфекции, в частности газовой гангрены.
Из раненых выделяется группа риска, в которой вероятность развития этого осложнения велика: слепые ранения, ранения нижних конечностей, с массивным повреждением тканей. Кроме того, должна быть выделена группа больных особого риска, в которой частота развития газовой гангрены выше во много раз. Это ранение конечностей, сопровождающееся повреждением магистральных сосудов, компартмент-синдромом, с наложением жгута, шоком (травматическим, геморрагическим, плевропульмональным).
Согласно такому распределению больных устанавливается очередность их эвакуации и срочность оказания квалифицированной хирургической помощи. Раненые группы особого риска должны эвакуироваться в те же сроки, что и раненые с внутренними кровотечениями. Квалифицированная хирургическая помощь им должна оказываться как группе раненых, нуждающихся в ней по жизненным показаниям: после выведения из шока, в перевязочной. В случаях повреждения магистральных сосудов - лучше на этапе специализированной помощи.
Профилактика газовой гангрены должна быть комплексной, т.е. включать организационные мероприятия, медицинскую помощь на этапах эвакуации и своевременное качественное хирургическое вмешательство.
Специфическая профилактика анаэробной инфекции должна делиться на патогенетическую и саногенетическую. Патогенетическая - прямое воздействие на анаэробную инфекцию (введение противогангренозной сыворотки), тщательная хирургическая обработка раны, исключение первичного хирургического шва.
Саногенетическая - повышение защитной функции организма и, в частности, общей и местной, путем аэрации тканей.
Специфическая патогенетическая профилактика - введение противогангренозной сыворотки в объеме 1 профилактической дозы. Несмотря на мнение, что таковая мера не является эффективной профилактической защитой от развития газовой гангрены, ее следует использовать. Но при этом четко придерживаться организационных и медицинских мероприятий, в которых главными являются ранняя первичная хирургическая обработка огнестрельной раны и полное исключение первичного шва.
Рекомендованные в хирургии мирного времени виды швов - первичный, первично-отсроченный, провизорный в военно-полевой хирургии нередко во много раз увеличивают угрозу развития раневой инфекции. Это относится, главными образом, к первичным швам. Показания к наложению при огнестрельных ранениях очень субъективны и нередко вводят в заблуждение хирурга. Результатом является, как правило, раневая инфекция.
С учетом высокого риска развития раневой инфекции, в частности газовой гангрены, при огнестрельных ранениях следует запретить применение первичного хирургического шва после хирургической обработки раны.
В военно-полевой хирургии, чтобы исключить сомнения в отношении применения первичного хирургического шва при огнестрельных ранениях, оставить только 3 вида швов: первично-отсроченный (через 3-4 дня после ПХО) и вторичный - ранний (через 2 недели после ПХО) и поздний (через 3-4 недели после ПХО).
Причина увеличения возможности развития газовой гангрены при шоке травматического характера связана с особенностями его патогенеза. Как известно, травматический и геморрагический шок сопровождается снижением ОЦК, что ведет к циркуляторной гипоксии. Кроме того, резко нарушается микроциркуляция тканей, идет централизация кровообращения. Все это ведет к резкому уменьшению поступления кислорода к периферическим тканям (конечностям). На этом фоне создаются благоприятные условия для активизации анаэробной инфекции при огнестрельных ранениях в группе риска и особенно в группе особого риска. То же самое происходит и при ранениях, осложненных плевропульмональным шоком. При этом степень гипоксии еще более выражена, так как помимо циркуляторной гипоксии развивается и дыхательная. Поэтому эта группа раненых должна относится к 3 группе (особого риска) и подлежит эвакуации в первую очередь.
В целях медицинской профилактики развития анаэробной инфекции на ЭМЭ рекомендуется применение у раненых 2 и 3 групп местной и общей аэрации (в/в озонированный раствор, обкалывание мягких тканей кислородом или озоном).
Лечение газовой гангрены должно в обязательном порядке включать местную и общую аэрацию тканей путем использования предложенной методики внутривенного введения кислорода и озона, а также ГБО, что значительно улучшает результат лечения и полностью устраняет угрозу ампутации конечности.
Выводы. Эффективная профилактика и лечение раневой инфекции на этапах медицинской эвакуации возможны только при четком и последовательном выполнении на каждом этапе алгоритма поставленных задач.
1.Должны быть выделены неспецифические (медицинские и организационные) и специфические виды профилактики и лечения.
2.Необходимо всех раненых, с учетом риска развития раневой инфекции, разделить на 3 группы (1 - все огнестрельные ранения, 2 - группа риска, 3 - особого риска).
3.В целях профилактики развития раневой инфекции исключить из практики военно-полевой хирургии первичный хирургический шов. Оставить только первично-отсроченный и вторично-отсроченный (ранний и поздний).
Раневая инфекция – это комплекс общих и местных патологических проявлений, возникающих при развитии инфекции в случайных или операционных ранах. Патология проявляется болью, ознобом, лихорадкой, увеличением регионарных лимфатических узлов и лейкоцитозом. Края раны отечные, гиперемированные. Наблюдается выделение серозного или гнойного отделяемого, в отдельных случаях образуются участки некроза. Диагноз выставляется на основании анамнеза, клинических признаков и результатов анализов. Лечение комплексное: вскрытие, перевязки, антибиотикотерапия.
МКБ-10
Общие сведения
Раневая инфекция – осложнение раневого процесса, обусловленное развитием патогенной микрофлоры в полости раны. Все раны, в том числе и операционные, как в гнойной хирургии, так и в травматологии считаются первично загрязненными, поскольку какое-то количество микробов попадает на раневую поверхность из воздуха даже при безукоризненном соблюдении правил асептики и антисептики. Случайные раны загрязнены сильнее, поэтому в таких случаях источником инфекции обычно является первичное микробное загрязнение. При операционных ранах на первый план выступает эндогенное (из внутренней среды организма) или внутригоспитальное (вторичное) инфицирование.

Причины
В большинстве случаев возбудителем инфекции в случайных ранах становится стафилококк. Редко в качестве основного возбудителя выступает протей, кишечная и синегнойная палочка. В 0,1% случаев встречается анаэробная инфекция. Через несколько дней пребывания в стационаре флора меняется, в ране начинают преобладать устойчивые к антибактериальной терапии грамотрицательные бактерии, которые обычно становятся причиной развития раневой инфекции при вторичном инфицировании как случайных, так и операционных ран.
Раневая инфекция развивается в случае, когда количество микробов в ране превышает некий критический уровень. При свежих травматических повреждениях у ранее здорового человека этот уровень составляет 100 тыс. микроорганизмов на 1 г ткани. При ухудшении общего состояния организма и определенных особенностях раны этот порог может существенно снижаться.
К числу местных факторов, повышающих вероятность развития раневой инфекции, относится присутствие в ране инородных тел, сгустков крови и некротических тканей. Также имеет значение плохая иммобилизация при транспортировке (становится причиной дополнительной травмы мягких тканей, вызывает ухудшение микроциркуляции, увеличение гематом и расширение зоны некроза), недостаточное кровоснабжение поврежденных тканей, большая глубина раны при малом диаметре раневого канала, наличие слепых карманов и боковых ходов.
Общее состояние организма может провоцировать развитие раневой инфекции при грубых расстройствах микроциркуляции (централизация кровообращения при травматическом шоке, гиповолемические расстройства), нарушениях иммунитета вследствие недостаточного питания, нервного истощения, химических и радиационных поражений, а также хронических соматических заболеваний. Особенно значимы в таких случаях злокачественные новообразования, лейкемия, уремия, цирроз, сахарный диабет и ожирение. Кроме того, снижение сопротивляемости инфекции наблюдается при проведении лучевой терапии и при приеме ряда лекарственных средств, в том числе – иммунодепрессантов, стероидов и больших доз антибиотиков.
Классификация
В зависимости от преобладания тех или иных клинических проявлений гнойные хирурги выделяют две общие формы раневой инфекции (сепсис без метастазов и сепсис с метастазами) и несколько местных. Общие формы протекают тяжелее местных, вероятность летального исхода при них повышается. Самой тяжелой формой раневой инфекции является сепсис с метастазами, который обычно развивается при резком снижении сопротивляемости организма и раневом истощении вследствие потери больших количеств белка.
К числу местных форм относятся:
- Инфекция раны. Является локализованным процессом, развивается в поврежденных тканях с пониженной сопротивляемостью. Зона инфицирования ограничена стенками раневого канала, между ней и нормальными живыми тканями есть четкая демаркационная линия.
- Околораневой абсцесс. Обычно соединен с раневым каналом, окружен соединительнотканной капсулой, отделяющей участок инфекции от здоровых тканей.
- Раневая флегмона. Возникает в случаях, когда инфекция выходит за пределы раны. Демаркационная линия исчезает, процесс захватывает прилежащие здоровые ткани и проявляет выраженную тенденцию к распространению.
- Гнойный затек. Развивается при недостаточном оттоке гноя вследствие неадекватного дренирования или зашивании раны наглухо без использования дренажа. В подобных случаях гной не может выйти наружу и начинает пассивно распространяться в ткани, образуя полости в межмышечных, межфасциальных и околокостных пространствах, а также в пространствах вокруг сосудов и нервов.
- Свищ. Образуется на поздних стадиях раневого процесса, в случаях, когда на поверхности рана закрывается грануляциями, а в глубине сохраняется очаг инфекции.
- Тромбофлебит. Развивается через 1-2 мес. после повреждения. Является опасным осложнением, обусловлен инфицированием тромба с последующим распространением инфекции по стенке вены.
- Лимфангит и лимфаденит. Возникают вследствие других раневых осложнений, исчезают после адекватной санации основного гнойного очага.
Симптомы раневой инфекции
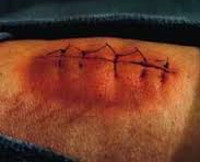
Как правило, патология развивается спустя 3-7 дней с момента ранения. К числу общих признаков относится повышение температуры тела, учащение пульса, ознобы и признаки общей интоксикации (слабость, разбитость, головная боль, тошнота). В числе местных признаков – пять классических симптомов, которые были описаны еще во времена Древнего Рима врачом Аулусом Корнелиусом Сельсусом: боль (dolor), местное повышение температуры (calor), местное покраснение (rubor), отек, припухлость (tumor) и нарушение функции (functio laesa).
Характерной особенностью болей является их распирающий, пульсирующий характер. Края раны отечны, гиперемированы, в полости раны иногда имеются фибринозно-гнойные сгустки. Пальпация пораженной области болезненна. В остальном симптоматика может варьироваться в зависимости от формы раневой инфекции. При околораневом абсцессе отделяемое из раны нередко незначительное, наблюдается выраженная гиперемия краев раны, резкое напряжение тканей и увеличение окружности конечности. Образование абсцесса сопровождается снижением аппетита и гектической лихорадкой.
При раневых флегмонах выявляется существенное повышение местной температуры и резкое ухудшение состояния больного, однако рана выглядит относительно благополучно. Формирование гнойного затека также сопровождается значительным ухудшением состояния пациента при относительном благополучии в области раны. Температура повышается до 40 градусов и более, отмечаются ознобы, вялость, адинамия и снижение аппетита. Гнойное отделяемое отсутствует или незначительное, гной выделяется только при надавливании на окружающие ткани, иногда – удаленные от основного очага инфекции. При свищах общее состояние остается удовлетворительным или близким к удовлетворительному, на коже формируется свищевой ход, по которому оттекает гнойное отделяемое.
Осложнения
Осложнения обусловлены распространением инфекции. При гнойных тромбофлебитах общее состояние ухудшается, в зоне поражения определяются умеренные признаки воспаления, при расплавлении стенки вены возможно формирование флегмоны или абсцесса. Лимфангит и лимфаденит проявляются болезненностью, отечностью мягких тканей и гиперемией кожи в проекции лимфатических узлов и по ходу лимфатических сосудов. Отмечается ухудшение общего состояния, ознобы, гипертермия и повышенное потоотделение. При сепсисе состояние тяжелое, кожа бледная, наблюдается снижение АД, выраженная тахикардия, бессонница и нарастающая анемия.
Лечение раневой инфекции
Лечение заключается в широком вскрытии и дренировании гнойных очагов, а также промывании раны антисептиками. В последующем при перевязках используются сорбенты и протеолитические ферменты. В фазе регенерации основное внимание уделяется стимуляции иммунитета и защите нежных грануляций от случайного повреждения. В фазе эпителизации и рубцевания при больших, длительно незаживающих ранах выполняют кожную пластику.
Прогноз и профилактика
Прогноз определяется тяжестью патологии. При небольших ранах исход благоприятный, наблюдается полное заживление. При обширных глубоких ранах, развитии осложнений требуется длительное лечение, в ряде случаев возникает угроза для жизни. Профилактика раневой инфекции включает в себя раннее наложение асептической повязки и строгое соблюдение правил асептики и антисептики в ходе операций и перевязок. Необходима тщательная санация раневой полости с иссечением нежизнеспособных тканей, адекватным промыванием и дренированием. Пациентам назначают антибиотики, проводят борьбу с шоком, алиментарными нарушениями и белково-электролитными сдвигами.
Профилактика раневой инфекции. Антибиотикопрофилактика
Среди предоперационных факторов важное место отводится обработке кожи в области планируемой операции.
Так, для предоперационного удаления волос с кожи желательно использование методик, которые в отличие от бритья не вызывают микроабразий кожи (эпиляция, депилятории). Эта рекомендация поддерживается результатами рандомизированного исследования, проведенного у 1013 пациентов, у которых РИ возникали в 3,2 % случаев после удаления волос методом эпиляции утром в день операции в сравнении с 10% случаев у пациентов, кожу которых подвергали бритью в день операции.
У больных носителей золотистого стафилококка целесообразно приложить усилия по уменьшению колонизации им носоглотки. Рандомизированное плацебо-контролируемое исследование обнаружило, что обработка мупироцином носовых ходов у больных, подвергавшихся плановым кардиоторакальным, нейрохирургическим, онкологическим, гинекологическим и общехирургическим операциям, начиная за день до операции и продолжая в течение 5 дней подряд, снизила число НКИ с 7,7 до 4,0% у больных с колонизацией S. aureus.
Однако общая частота раневых инфекций (РИ) при использовании мупироцина независимо от носительства золотистого стафилококка не уменьшалась.
Среди факторов, влияющих на развитие раневых инфекций (РИ), как уже было сказано выше, важное значение имеет борьба с периоперационным повышением уровня глюкозы свыше 200 мг/дл (> 10,1 ммоль/л). Интенсивный контроль глюкозы в первые 2 дня после операции, как было показано в исследовании, проведенном более чем у 2400 больных сахарным диабетом, способствовал уменьшению глубоких РИ у пациентов, подвергшихся операциям на сердце, с 2 до 0,8 % (р = 0,01).
Кроме того, важнейшая роль в предотвращении раневых инфекций (РИ) принадлежит антибиотикопрофилактике (АБП).

Понятие антибиотикопрофилактики
Помимо исследования D.C. Classen недавно было проведено исследование TRAPE, изучавшее связь между раневой инфекции (РИ) и временем профилактического введения антибиотика у кардиохирургических, ортопедических и гинекологических (гистерэктомия) больных. Риск был наименьшим у больных, которые получали АБП в течение 30 мин (цефалоспорины) или 1 ч (ванкомицин или фторхинолоны) до кожного разреза. С другой стороны, введение антибиотика непосредственно перед разрезом может не обеспечить достаточного количества времени для создания необходимой концентрации антибиотика.
Отмечалось двукратное повышение риска раневой инфекции (РИ), если профилактическое введение цефуроксима осуществлялась менее чем за 30 мин до разреза, в сравнении с теми, кому антибиотик вводили в течение 30-59 мин до разреза.
Систематический обзор 28 рандомизированных исследований по применению одной или многократных доз антибиотикопрофилактики (АБП) не выявил преимуществ последнего подхода. В то же время пролонгированная АБП (> 48 ч) статистически значимо связана с повышенным риском приобретения резистентного к антибиотикам возбудителя инфекции.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Послеоперационные раневые инфекции. Факторы риска
Анализ данных Национальной сети по безопасности в здравоохранении США (NHSN) показал, что на 26,6 млн хирургических операций, выполняемых ежегодно в США, приходится 250 000-1 000 000 раневая инфекция (РИ). При этом РИ добавляют 3,7 млн койко-дней и увеличивают затраты на 1,6 млрд долларов. Пациент, у которого во время госпитализации развивается раневая инфекция (РИ), имеет более 60% риск поступления в отделение реанимации и в 15 раз больший риск повторного поступления в стационар в течение 30 дней после выписки.
При этом пребывание больного в стационаре увеличивается в среднем на 6,5 дня, а стоимость лечения возрастает более чем на 3000 долларов.
Послеоперационная инфекция никогда не возникает случайно. Она зависит от присутствия различных, в большей или меньшей степени влияющих на риск РИ факторов.
В группу факторов риска, связанных с макроорганизмом, входит пожилой возраст (> 60 лет), нарушение питания (кахексия, ожирение), курение (вызывает вазоконстрикцию и замедляет заживление раны), алкоголизм, наличие сопутствующих заболеваний и др.
К важнейшим факторам риска относятся сахарный диабет/периоперационная гипергликемия, низкий сывороточный альбумин, антибиотикотерапия в дооперационном периоде, длительная предшествующая госпитализация, наличие отдаленного очага инфекции в момент операции и колонизация кожи и слизистых оболочек золотистым стафилококком.
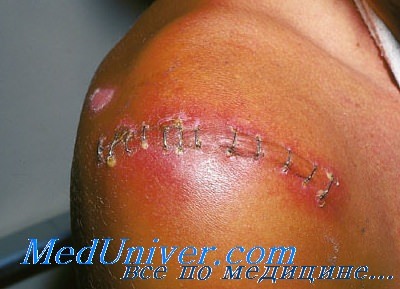
Важные факторы риска у онкологических больных — наличие злокачественной опухоли (независимый фактор раневых инфекций (РИ)), угнетение иммунитета из-за наличия новообразования и проводимого противоопухолевого лечения (химио- и лучевая терапия), осложнения противоопухолевого лечения (лейкопения, нейтропения, лучевые дерматиты и др.).
Колонизация золотистым стафилококком носовых ходов пациента — важнейший фактор риска раневых инфекций (РИ), вызванной данным микроорганизмом, особенно у больных сахарным диабетом или на фоне гемодиализа, у которых подобная колонизация превышает 50%. Исследование у больных, подвергнутых плановым операциям в кардиоторакальных, общехирургических, онкологических, гинекологических и неврологических отделениях, показало 4-кратное увеличение риска РИ, вызванной золотистым стафилококком у больных с колонизацией по сравнению с отсутствием таковой.
Под факторами, связанными с операцией, подразумевается нерациональная обработка кожи операционного поля (использование бритвы для удаления волос вызывает микроабразии), удаление волос вечером перед операцией (разумнее — утром в день операции), неправильная обработка кожи и многое другое.
Некоторые авторы к факторам риска раневых инфекций (РИ) относят отсутствие периоперационной АБП. Если последнее встречается нечасто, то нерациональное назначение профилактического антибиотика (несвоевременное введение, отсутствие дополнительной дозы, неадекватная доза, неправильно выбранный антибиотик) тоже может способствовать развитию РИ.
К факторам риска также относятся периоперационная гипотермия и гипоксия тканей, а также переливание крови во время операции. Периоперационная гипотермия в результате нарушения терморегуляции под действием анестетиков запускает вазоконстрикцию и приводит к низкому напряжению кислорода в тканях, что само по себе служит фактором риска, а также воздействует на нейтрофилы, уменьшая хемотаксис, снижая продукцию супероксида, и т. д.
Роль переливаний крови в развитии раневых инфекций (РИ), возможно, связана с тем, что лейкоциты донора индуцируют иммуносуирессию, однако эти исследования не раз критиковались, т. к. не были стандартизованными и проводился только однофакторный анализ.
Неадекватная вентиляция операционной, нарушение стерильности и асептики, неправильная стерилизация инструментов, пребывание большого количества людей в операционной в процессе операции также играют роль в развитии РИ. В частности, исследование, включавшее около 3000 операций, показало 4-кратное увеличение частоты РИ, если во время операции в операционной находилось более 17 человек (по сравнению с 0-8 человек).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

