Методические рекомендации по выделению и идентификации стрептококков
Обновлено: 24.04.2024
При изучении антибиотикограмм сопутствующей микрофлоры стрептококковых инфекций выявлен антибиотик, обладающий бактерицидным действием на сопутствующую микрофлору, но не снижающий репродуктивную активность стрептококков. На основании проведенных исследований предложен способ получения изолированных колоний стрептококков, заключающийся в следующем: для выделения аэробных стрептококков проводят посев исследуемого материала на 5% кровяной МПА, а затем на поверхность питательной среды с посевом наносят диски с гентамицином в количестве 8–9 штук. Через 18–20 часов роста бактерий при температуре 37°С на поверхности плотной питательной среды вокруг дисков с гентамицином наблюдается рост изолированных колоний стрептококков. Для выделения стрептококков, обладающих анаэробными свойствами, предварительно делали посев исследуемого материала на печеночный бульон Китта-Тароцци, а затем через 18–20 часов проводили пересев на 5% кровяной МПА для получения изолированных колоний стрептококков. Предложенный способ позволяет повысить процент выделения стрептококков из исследуемого материала, сократить время проведения микробиологических исследований по выделению изолированных колоний стрептококков.

2. Клиническая лабораторная аналитика. Т. IV. Частные аналитические технологии в клинической лаборатории / под ред. В.В. Меньшикова. – М.: Медицинское информационное агентство, 2004. – 691 с.
3. Лабинская А.С.. Микробиология с техникой микробиологических исследований. – М.: Медицина, 1978. – 394 с.
4. Медицинская микробиология / под ред. В.И. Покровского, О.К. Поздеева. – М.: ГЭОТАР Медицина, 1999. – 1200 с.
6. Медицинская микробиология, вирусология и иммунология / под ред. А.А. Воробьева. – М.: Медицинское информационное агентство, 2004. – 691 с.
7. Национальная концепция профилактики инфекций, связанных с оказанием медицинской помощи. – М.: Минздрав России, 2011. – 22 с.
Стрептококковые инфекции продолжают оставаться в числе наиболее острых проблем здравоохранения во всех странах мира. Бактерии рода Streptococcus классифицируют по антигенным свойствам (на основании имеющихся полисахаридов), выделяя серогруппы, изучают биохимические и гемолитические свойства. Наиболее патогенным для человека является Streptococcus pyogenes группы А, вызывающий у человека гнойно-воспалительные и инфекционно-аллергические заболевания. Диагностика стрептококковых инфекций включает использование бактериоскопического метода, определение стрептококковых антигенов в патологическом материале с помощью ИФА или латекс-агглютинации, бактериологического метода идентификации возбудителей инфекции и серологического метода по определению антител к стрептококкам группы А. В последнее время широко распространен метод ПЦР, позволяющий установить диагноз заболевания в 3 раза чаще по сравнению с классическими бактериологическими методами исследований [1, 2, 4]. Эти данные свидетельствуют о необходимости совершенствования микробиологической диагностики стрептококковых инфекций. Стрептококки колонизируют кожные покровы, слизистые оболочки, носоглотку, желудочно-кишечный тракт и влагалище [5]. Для возбудителей инфекции характерна множественность механизмов и факторов передачи, но наиболее характерен воздушно-капельный механизм передачи. У школьников в холодный сезон года носительство стрептококков в носоглотке достигает 25% [6].
В большинстве случаев возникновение стрептококковых инфекций связано с оказанием медицинской помощи (ИСМП). Причинами роста заболеваемости гнойно-воспалительными стрептококковыми инфекциями являются селекция и формирование госпитальных штаммов, обладающих высокой вирулентностью и множественной лекарственной устойчивостью, что требует совершенствования систем надзора и контроля за ИСМП [7].
Описан общепринятый способ получения чистой культуры стрептококков [6], который имеет следующие недостатки: изолированные колонии можно получить только на 3-й день микробиологического исследования, в процессе культивирования бактерий не удаляется посторонняя сопутствующая микрофлора слизистых оболочек зева и миндалин, на 2-й день пересева материала на кровяной мясопептонный агар (МПА) не всегда удается определить микробы, подозрительные на стрептококк, и поэтому приходится делать пересев на кровяной МПА бактерий, не относящихся к стрептококкам, что требует большего расхода питательных сред для выделения изолированной колонии стрептококков. Известно также, что гемолитические свойства стрептококков не являются диагностическим тестом для выявления патогенных стрептококков. Патогенные стрептококки под влиянием антибиотиков и факторов внешней среды могут утратить гемолитическую активность, что существенно затрудняет выделение стрептококков из исследуемого материала.
Итак, сложность лабораторной диагностики и эпидемиологические предпосылки циркуляции стрептококков в лечебно-профилактических учреждениях (ЛПУ) дают основания для совершенствования методов лабораторной диагностики стрептококковых инфекций.
Цель исследования - повышение эффективности выделения возбудителей стрептококковых инфекций из исследуемого материала при возникновении ИСМП.
Задача исследования. На основании изучения антибиотикограмм сопутствующей микрофлоры стрептококковым инфекциям выявить антибиотик, обладающий бактерицидным действием на сопутствующую микрофлору, но не влияющим на снижение репродуктивной активности стрептококков. Добавление данного антибиотика в питательную среду для роста стрептококков позволит разработать способ получения изолированных колоний стрептококков.
Материал и методы исследования
В период с 1997 по 2011 г. обследовано 5300 больных. В содержимом из зева выделена сопутствующая микрофлора стрептококковой инфекции. Для определения чувствительности выделенной сопутствующей микрофлоры к антибиотикам использовали диско-диффузионный метод. В опытах использовано 16-20 часовых культур бактерий. Концентрацию бактерий доводили по стандарту мутности до 0,5 ед. по McFarland на физиологическом растворе хлорида натрия (рН 7,2-7,4). Приготовленную взвесь вносили на чашки Петри с 5% кровяным МПА в количестве 0,2 мл и равномерно распределяли на поверхности питательной среды. Через 15 минут на поверхность питательной среды наносили диски с антибиотиками. Посевы инкубировали при 37°С в течение 24 часов с последующим определением задержки роста бактерий вокруг дисков с антибиотиками. Использовали следующие диски с антибиотиками: стрептомицин, эритромицин, гентамицин, амикацин, линкомицин, бензилпенициллин, олеандомицин, цефаклор, цефуроксим, цефатоксим, цефалексин.
Предложенный способ получения изолированных колоний стрептококков поясняется графическим материалом. На рисунке представлена схема получения изолированных колоний стрептококков.

Схема получения изолированных колоний стрептококков. Обозначения: 1 - сбор исследуемого материала от больного (слизь из зева и с миндалин), 2-5% кровяной МПА, 3 - среда Кита-Тароцци для выращивания бактерий с анаэробным типом дыхания, 4 - диски с гентамицином, 5 - выросшие изолированные колонии стрептококков на кровяном МПА, обладающих аэробными и анаэробными свойствами
Результаты исследований и их обсуждение
По сравнению с традиционными методами микробиологической диагностики стрептококковых инфекций предложенный способ позволяет уменьшить расход питательных сред, повысить процент выделения стрептококков из исследуемого материала, что позволяет своевременно и в более полном объеме проводить противоэпидемическое расследование и осуществлять мероприятия, направленные на предупреждение возникновения ИСМП стрептококковой этиологии.
Следует отметить, что сложность и низкая эффективность выделения стрептококков из исследуемого материала при диагностике инфекционных заболеваний связана с тем, что сопутствующая микрофлора по сравнению со стрептококками более устойчива во внешней среде, неприхотлива к питательным средам, как правило, обладает антагонистическими свойствами и поэтому при инфекционных заболеваниях выделенную микрофлору от больных часто выделяют и идентифицируют преимущественно из группы условно-патогенной сопутствующей микрофлоры. При обследовании ожоговых больных в популяциях сопутствующей микрофлоры наиболее часто определялся эпидермальный стафилококк.
Итак, стрептококки, в отличие от условно-патогенной микрофлоры и стафилококков, менее устойчивы во внешней среде, часто обладали анаэробными свойствами и медленнее размножались на питательных средах. Поэтому не всегда удается выделять чистую культуру стрептококков традиционными микробиологическими методами.
Предложенный способ позволил повысить процент выделения стрептококков из исследуемого материала, сократить время проведения микробиологических исследований по выделению изолированных колоний стрептококков, уменьшить количество ложноотрицательных результатов исследований и снизить расход питательных сред в процессе лабораторной диагностики стрептококковых инфекций. Сокращение сроков проведения лабораторных исследований позволяет в ранние сроки и в более полном объеме проводить противоэпидемические мероприятия при возникновении ИСМП, вызываемых стрептококками.
Микробиологическая диагностика стрептококка. Диагностика стрептококковой инфекции. Выявление стрептококка. Выделение стрептококка.
Основу микробиологической диагностики стрептококковой инфекции составляют выделение и идентификация возбудителя. При этом обычно биохимические характеристики изолятов не изучают. Прочие методы диагностики стрептококковой инфекции имеют различные ограничения.
Через 24 ч на КА стрептококки группы А образуют блестящие вязкие колонии (рис. 2, см. цветную вклейку). В жидких средах бактерии дают придонный, иногда поднимающийся вверх рост. Весьма информативные методы раннего выявления стрептококков — определение чувствительности к антимикробным агентам методом дисков.
Наиболее часто их используют для идентификации стрептококков в мазках из зева. Для дифференцировки стрептококков группы А от прочих b-гемолитических стрептококков применяют тест чувствительности к бацитрацину. Более чем в 99% случаев изоляты стрептококков группы А чувствительны к бацитрацину, тогда как представители других серогрупп обычно устойчивы (рис. 12-8). Также можно применить тест чувствительности к триметоприм-сульфаметоксазолу.

Стрептококки групп А и В обычно чувствительны к действию антимикробного агента.
По сравнению с чувствительностью к бацитрацину более специфичен тест гидролиза пиррол идонил-b-нафтиламида (ПИР-тест). S. pyogenes — единственный стрептококк, дающий положительную реакцию. Для этого в пробирки вносят полоски фильтровальной бумаги, пропитанные ПИР. Под действием бактериальных пептидаз ПИР расщепляется до b-нафтиламида, и после внесения 0,01% раствора p-диметиламиноциннамальальдегида полоски окрашиваются в вишнёво-красный цвет.
Стрептококки группы А легко можно выявить в мазках из зева, используя коммерческие наборы; групповой А-Аг экстрагируют химическими реагентами или ферментами и идентифицируют в реакциях латекс-агглютинации, коагглютинации или ИФА. Для экспресс-диагностики ревматического процесса и гломерулонефрита можно определять AT к стрептолизину О или стрептодорназе; серологические исследования также позволяют выявить носителей. Следует помнить, что AT к стрептолизину О не образуются при кожных инфекциях, вызываемых стрептококками группы А.
Лечение стрептококковой инфекции
Основу лечения стрептококковой инфекции составляет адекватная антибактериальная химиотерапия. Лечение ревматизма проводят пенициллинами короткого действия, профилактику — пенициллинами длительного действия (бициллин-5), причём антибиотикопрофилактику предпочтительно проводить круглогодично.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
1.1 . В настоящих методических указаниях представлена информация о роли метициллинрезистентных штаммов золотистого стафилококка в возникновении внутрибольничных инфекций, их микробиологических и эпидемиологических особенностях, изложены традиционные и молекулярно-генетические методы идентификации и типирования.
1.2 . Методические рекомендации разработаны в помощь специалистам органов и учреждений, осуществляющих государственный санитарно-эпидемиологический надзор, и лечебно-профилактических учреждений, осуществляющих организацию и проведение профилактических и противоэпидемических мероприятий по борьбе с внутрибольничными инфекциями.
2.2 . Положение о государственной санитарно-эпидемиологической службе Российской Федерации, утвержденное постановлением Правительства Российской Федерации № 554 от 24 июля 2000 г.
В последнее десятилетие проблема внутрибольничных инфекций (ВБИ) приобрела исключительно большое значение для всех стран мира. Это обусловлено, прежде всего, значительным ростом числа госпитальных штаммов микроорганизмов, обладающих устойчивостью к широкому кругу антимикробных препаратов. Несмотря на значительный недоучет, в Российской Федерации ежегодно регистрируется около 30 тыс. случаев внутрибольничных инфекций, при этом минимальный экономический ущерб составляет более 5 млрд. рублей ежегодно. Среди возбудителей ВБИ одно из первых мест, по-прежнему, принадлежит микроорганизмам рода Staphylococcus , наиболее патогенным представителем которого является S . aureus . Эпидемиологическая ситуация осложняется в связи с широким распространением в стационарах, а также появлением и во внебольничной среде, клинических изолятов S.aureus, устойчивых к оксациллину (ORSA или MRSA). MRSA способны вызывать разнообразные клинические формы внутрибольничных инфекций, включая наиболее тяжелые, такие как: бактериемия, пневмония, синдром септического шока, септический артрит, остеомиелит и другие, которые требуют длительного и дорогостоящего лечения. Появление осложнений, вызванных MRSA, приводит к увеличению сроков госпитализации, показателей летальности, значительным экономическим потерям. Показано, что рост частоты ВБИ, наблюдаемый в стационарах различных стран мира, обусловлен распространением эпидемических штаммов MRSA, многие из которых способны вырабатывать пирогенные токсины - суперантигены, подавляющие иммунный ответ на S . aureus.
С конца 90-х годов прошлого века в стационарах России отмечается рост частоты выделения MRSA, которая в ряде больниц достигла 30 - 70 %. Это делает неэффективным использование многих антимикробных препаратов и существенно ухудшает качество оказания медицинской помощи населению. В этих условиях совершенствование методов эпидемиологического и микробиологического мониторингов, направленных на выявление эпидемически значимых штаммов, приобретает все более актуальное значение.
4.1. Таксономия и биологические особенности
4.2. Клиническое значение
В настоящее время MRSA являются ведущими возбудителями внутрибольничных инфекций в стационарах многих странах мира. Частота их выделения в стационарах США, Японии, многих стран Западной Европы достигает 40 - 70 %. Исключение составляют, по-видимому, только ряд скандинавских стран, где исторически были приняты жесткие противоэпидемические меры по контролю за распространением таких штаммов. В стационарах Российской Федерации частота выделения MRSA колеблется от 0 до 89 %. Наибольшая частота выделения отмечается в реанимационных, ожоговых, травматологических и хирургических отделениях стационаров, расположенных в крупных городах. Одной из основных причин этой закономерности является концентрация в таких стационарах пациентов с нарушениями целостности кожных покровов и поврежденными иммунологическими барьерами. Наиболее частым местом локализации инфекции являются послеоперационные и ожоговые раны и дыхательные пути. Первичные и вторичные бактериемии наблюдаются примерно у 20 % инфицированных больных. В случае инфицирования ожоговых больных частота бактериемии нередко возрастает до 50 %. Факторами, способствующими развитию бактериемии, является присутствие центрального венозного катетера, анемия, гипотермия и назальное носительство. Развитие бактериемии значительно увеличивает вероятность летального исхода. Особенно высокая смертность, обусловленная бактериемией, наблюдается среди пациентов, находящихся в ожоговых и отделениях интенсивной терапии, где она может достигать 50 % по сравнению с 15 % в контрольной группе. Риск развития летального исхода возрастает почти в три раза среди пациентов, у которых бактериемия обусловлена MRSA по сравнению с пациентами, инфицированными метициллинчувствительными штаммами S . aureus. Развитие госпитальной бактериемии приводит к значительному увеличению стоимости госпитализации. В современных условиях лечение таких пациентов требует, как правило, внутривенного введения ванкомицина, тейкопланина или линезолида, однако клиническая эффективность этих препаратов нередко оказывается значительно ниже, чем у антибиотиков, используемых для лечения пациентов с осложнениями, вызванными метициллинчувствительными S.aureus. По данным Центра по контролю за заболеваниями (США) средняя продолжительность пребывания пациента в больнице в случае хирургического вмешательства составляет 6,1 дня, тогда как при возникновении осложнений, вызванных MRSA она увеличивается до 29,1 дней, при этом средние расходы возрастают с 29455$ до 92363$ в пересчете на каждый случай. Заболевания, вызванные MRSA, могут начинаться на фоне терапии антибиотиками, в том числе аминогликозидами и цефалоспоринами. В этой связи необходимо отметить, что неадекватное назначение антибиотиков в случае тяжелых ВБИ драматически ухудшает прогноз заболевания. Летальность при осложнениях, вызванных MRSA, значительно колеблется и зависит как от возраста пациента, сопутствующего заболевания (артериальная гипертензия, диабет и др.), так и от присоединения дополнительной микрофлоры. Наиболее распространенными вторичными проявлениями инфекции, обусловленной MRSA, являются эндокардиты, гематогенный остеомиелит, септический артрит. Одним из наиболее грозных осложнений, вызываемых MRSA, является синдром токсического шока (СТШ). Клинические проявления СТШ включают следующий симптомокомплекс: гипертермия, сыпь, рвота, диарея, гипотензия, генерализованный отек, острый респираторный дистресс синдром, полиорганная недостаточность, диссеминированная интраваскулярная коагуляция. СТШ может развиться как осложнение после родов, хирургических вмешательств, при суперинфицировании S . aureus трахеальных повреждений, вызванных вирусом гриппа. Недавно описанные стафилококковая скарлатина и синдром упорной десквамации эпителия рассматривают как варианты СТШ.
4.3. Факторы патогенности и вирулентность
Вопрос о вирулентности MRSA остается дискутабельным. Они практически не вызывают заболевания у здоровых лиц из числа медицинского персонала. Вместе с тем, в многочисленных исследованиях показано, что прогноз при тяжелых формах внутрибольничных инфекций, таких как пневмония и бактериемия, значительно хуже среди пациентов, инфицированных MRSA, по сравнению с пациентами, инфицированными метициллинчувствительными S.aureus.
4.4. Генетический контроль устойчивости к метициллину и особенности фенотипической экспрессии
Мишенью действия b -лактамных антибиотиков (как пенициллинов, так и цефалоспоринов) являются транс- и карбоксипептидазы - ферменты, участвующие в биосинтезе основного компонента клеточной стенки микроорганизмов - пептидогликана. Благодаря своей способности связываться с пенициллином и другими b -лактамами данные ферменты получили название пенициллинсвязывающих белков (ПСБ). У Staphylococcus aureus имеются 4 ПСБ, отличающиеся как по молекулярной массе, так и по функциональной активности. Устойчивость метициллинрезистентных штаммов золотистого стафилококка (MRSA) к b -лактамным антибиотикам обусловлена продукцией дополнительного пенициллинсвязывающего протеина - ПСБ-2 ¢ , отсутствующего у чувствительных микроорганизмов. При подавлении В -лактамным антибиотиком активности основных пенициллинсвязывающих белков ПСБ-2 ¢ , в силу своего более низкого сродства к препаратам данной группы, продолжает функционировать и сохраняет микробной клетке жизнеспособность. Синтез ПСБ-2 ¢ кодируется геном mec A , расположенным на хромосоме S.aureus, в специфической области, обнаруживаемой только у метициллинрезистетных штаммов стафилококка - тес ДНК. Ме c ДНК представляет новый класс мобильных генетических элементов, который получил название стафилококковая хромосомная кассета тес (Staphylococcal chromosomal cassette тес = SCCmec ). Выявлено существование 4 типов SCCmec , различающихся как размерами (от 21 до 66 т.п.н.), так и набором генов, составляющих данные кассеты. Разделение на типы основано на различиях в генах, образующих собственно комлекс тес, и в наборе генов, кодирующих рекомбиназы сс rА и сс r В, входящих в различных сочетаниях в стафилококковую хромосомную кассету (рис. 1 ). Комлекс тес может включать: тесА - структурный ген, детерминирующий синтез ПСБ-2 ¢ ; mec I - регуляторный ген, влияющий на транскрипцию тесА; mecR1 - ген, передающий внутрь клетки сигнал о наличии в среде b -лактамного антибиотика; а также инсерционные последовательности IS 431 и IS 1272. В настоящее время известны 4 варианта комплекса тес (рис. 2 ).
Кроме того, различия между типами кассет тес обусловлены присутствием ряда дополнительных генов, расположенных в генетических областях J1а, J 1 b.
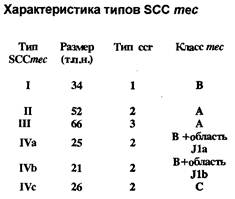
Рис. 1. Типы SCCmec.
Генетическая структура комплексов тес различных классов
• Класс A, IS431 - mecA-mecR1-mec1
• Класс В , IS431 - mecA- D mec R1-IS1272
• Класс С , IS431 - mecA- D mec R1-IS431
• Класс D, IS431 - mec A- D mec R 1
Рис. 2. тесА - структурный ген, детерминирующий синтез ПСБ-2 ¢ ;
mecI - регуляторный ген, влияющий на транскрипцию тесА;
mecR1 - ген, передающий внутрь клетки сигнал о наличии в среде b -лактамного антибиотика; IS431 и IS1272 - инсерционные последовательности
Уникальность метициллинрезистентности заключается также и в существовании феномена гетерорезистентности, суть которого состоит в том, что в условиях инкубации при 37 °С не все клетки популяции проявляют устойчивость к оксациллину. Генетический контроль феномена гетерорезистентности до настоящего времени полностью не выяснен. Известно только, что на экспрессию устойчивости могут влиять регуляторные гены b -лактамазы, а также ряд дополнительных генов, так называемые fem (factors essential for methicillin resistance) или aux, локализованные в различных частях хромосомы S.aureus, вне SCCmec . Сложность регуляции проявляется в фенотипических различиях. Выделяют 4 стабильных фенотипа (класса) резистентности. Первые три класса являются гетерогенными. Это означает, что в популяциях стафилококков, относящихся к этим классам, присутствуют субпопуляции микробных клеток с разным уровнем резистентности. При этом клоны стафилококков, получаемые из изолированных колоний (образовавшихся при рассеве первичной культуры) по популяционному составу полностью совпадают с исходной культурой.
Класс 1. Рост 99,99 % клеток подавляется оксациллином в концентрации 1,5 - 2 мкг/мл, рост 0,01 % микробов подавляется только при 25,0 мкг/мл.
Класс 2. Рост 99,9 % клеток подавляется при концентрации оксациллина 6,0 - 12,0 мкг/мл, тогда как рост 0,1 % микробов подавляется при концентрации > 25,0 мкг/мл.
Класс 3. Рост 99,0 - 99,9 % клеток подавляется при концентрации 50,0 - 200,0 мкг/мл и только рост 0,1 - 1 % микробной популяции подавляется при концентрации оксациллина 400,0 мкг/мл.
Класс 4. Представители этого класса характеризуются гомогенным уровнем устойчивости, который превышает 400,0 мкг/мл для всей популяции.
В связи с наличием гетерогенности по устойчивости к оксациллину могут возникать трудности при идентификации MRSA традиционными микробиологическими методами.
4.5. Особенности эпидемиологии MRSA
Будучи однажды занесенными в стационар, MRSА могут выживать там в течение длительного времени. Это определяет стратегию противоэпидемических мероприятий: очень важно не допустить занос и распространение в стационаре эпидемических штаммов.
Следует отметить, что периодически происходит смена эпидемического штамма, доминирующего на отдельных территориях. Так, по данным стафилококковой референс-лаборатории в Colindale ( London), в 1996 г. штаммы EMRSA-15 и EMRSA-16 были ответственны за более чем 1500 инцидентов, охвативших трех и более пациентов, в 309 больницах Англии, тогда как остальные эпидемические штаммы были ответственны только за 361 инцидент в 93 больницах. Распространение этих эпидемических штаммов привело к росту смертности от MRSA в 15, а частоты бактериемии в 24 раза за период с 1993 по 2002 г.г. согласно данным национального департамента статистики Великобритании.
Продолжает нарастать спектр антибиоткорезистентности эпидемических штаммов MRSA. Они гораздо быстрее, чем метициллинчувствительные, приобретают устойчивость к препаратам из группы фторхинолонов. Характерной чертой многих эпидемических штаммов MRSA является устойчивость практически ко всем известным классам антимикробных препаратов, за исключением гликопептидов и оксазолидинонов. В последние годы участились случаи выделения изолятов MRSA, обладающих умеренной чувствительностью к ванкомицину и даже ванкомицинрезистентных. Распространение таких штаммов в стационарах России может иметь драматические последствия.
С проблемой госпитальных штаммов MRSA тесно переплетается и проблема MRSA вне госпитального происхождения. Эти штаммы пока не обладают множественной резистентностью к антибиотикам, генетически отличаются от госпитальных штаммов, их происхождение остается неизвестным. Предполагается, что они сформировались из спорадических госпитальных штаммов. Внегоспитальные штаммы MRSA способны вызывать некротизирующую форму пневмонии, характеризующуюся крайне тяжелым течением и требующей госпитализации пациента, в связи с чем возникает угроза заноса и распространения таких штаммов в стационарах.
Оценка уровня доказательности и значимости рекомендаций проводилась в соответствии с данными, изложенными далее.
Уровни доказательности рекомендаций приводятся при изложении текста далее.

Уровень доказательности рекомендаций
1. Введение
Стрептококк группы В (СГВ, GBS, Streptococcus agalactiae) вызывает тяжело протекающие заболевания у новорожденных детей и представляет опасность для пациентов других возрастных групп.
Неонатальные инфекции, вызванные стрептококком группы В, остаются в центре внимания многих специалистов в области перинатальной медицины. Ранние СГВ-септицемии и пневмонии новорожденных отличаются тяжелым течением и высокой летальностью, что обратило на себя внимание еще в 70-е годы прошлого века, когда в развитых странах СГВ вытеснил грамотрицательные бактерии с первых позиций в этиологической структуре неонатальных инфекций. С тех пор прошли десятилетия, но ведущая роль СГВ в структуре бактериальных перинатальных инфекций остается незыблемой, несмотря на предпринимаемые лечебные и профилактические мероприятия. СГВ-инфекции новорожденных относятся к плохо управляемым инфекциям [5].
В подавляющем большинстве случаев новорожденные инфицируются СГВ во время родов от матери, причем чаще это происходит при вагинальном родоразрешении [1, 6]. Риск заболевания доношенного ребенка составляет 1—2% [1, 6, 7], недоношенного — 15—20%, а при сроке гестации менее 28 нед — практически 100% [8, 9]. СГВ вызывает ранние неонатальные инфекции, такие как сепсис, менингит, пневмония, остеомиелит, артрит и пиелонефрит, частота которых в разных странах колеблется от 0,2 до 5 и более на 1000 живорожденных детей [6, 10].
В акушерской практике со стрептококком группы В связывают бактериемию, инфекции мочевых путей, хориоамнионит, преждевременное излитие околоплодных вод, преждевременные роды, послеродовой эндометрит и др. [8, 11—18].
На основании 4-летнего мониторинга в Городском клиническом перинатальном центре Омска выявлено носительство S. agalactiae у 6—8% пациенток различных категорий. Отмечается, что перинатальное инфицирование СГВ недоношенных новорожденных с низкой массой тела при рождении в 50% случаев приводит к клинической манифестации генерализованного инфекционного процесса, а инфицирование доношенных новорожденных — в половине случаев к развитию локальных гнойно-воспалительных процессов [19].
В ГБУ НИИОЗММ ДЗМ проведен ретроспективный анализ распространенности СГВ среди новорожденных пяти родильных домов Москвы. По результатам микробиологического исследования 4534 проб клинического материала от 2265 новорожденных групп высокого инфекционного риска развития СГВ в среднем выделен у 4,9%. В ряде родильных домов отмечен низкий уровень выявления СГВ вследствие отсутствия целенаправленной диагностики с применением хромогенных сред или ПЦР детекции S. agalactiae [20].
Внедрение современных методов лабораторной диагностики и программы профилактики СГВ-инфекций позволит добиться стойкого снижения заболеваемости среди новорожденных детей, беременных и родильниц.
1.1. Этиология
Streptococcus agalactiae относится к бактериям рода Streptococcus и является единственным представителем стрептококков группы В по классификации Р. Лендсфилд. СГВ — грамположительные кокки, образующие цепочки вариабельной длины. По типу дыхания СГВ являются факультативными анаэробами. Типичные штаммы слабо лизируют in vitro эритроциты жвачных животных (гемолиз типа β), что стало основой для отнесения бактерии к β-гемолитической группе стрептококков. Однако 25—30% штаммов атипичны по данному признаку и проявляют α-гемолиз или не обладают выраженными гемолитическими свойствами.
СГВ образует два типа полисахаридных антигенов: группоспецифический, который является общим для всех штаммов, интегрированный в стенку бактерии, и капсульный. Выявление первого позволяет дифференцировать бактерию от стрептококков других групп, а по капсульным антигенам штаммы бактерии делят на 10 известных в настоящее время серотипов (Ia, Ib, II-IX). Дополнительными идентификационными маркерами разных вариантов СГВ служат поверхностные антигены α, β и Rib. С их помощью дифференцируют серотипы, имеющие одинаковый капсульный антиген (например, Ia и Ib). Серотипирование СГВ проводят иммунологическими методами (иммуноэлектрофорез, иммунопреципитация, иммунофлюоресценция, иммуноферментный анализ, коагглютинация, капиллярная преципитация, агглютинация, латекс-агглютинация). К сожалению, наборы для серотипирования СГВ в Российской Федерации недоступны, однако в последние годы отечественные производители интенсивно разрабатывают тест-системы ПЦР в режиме реального времени для определения серотипов и сиквенс-типов S. agalactiae. Из иммунологических методов в рутинной практике чаще используют метод латекс-агглютинации. Часть штаммов СГВ не удается серотипировать, что обусловлено наличием до настоящего времени неизвестных капсульных антигенов и механизмов, регулирующих их экспрессию. В эпидемиологических целях для типирования штаммов S. agalactiae применяют молекулярно-генетические методы (ПЦР, ПЦР с рассеянными затравками, риботипирование, IS-типирование, пульс-электрофорез и др.).
СГВ в организме человека могут колонизировать ротоглотку, анальную область прямой кишки, влагалище (чаще преддверие), урогенитальный тракт, кожу. Наличие у части штаммов СГВ дополнительных факторов вирулентности делает их инвазивными, способными вызывать сепсис, поражать разные ткани и органы (легкие, головной мозг, суставы и др.). Инвазивность штаммов и их адаптация к определенным возрастным группам людей коррелирует с их принадлежностью к ряду серо- и генотипов, определение которых предоставляет информацию для предварительной оценки клинической и эпидемиологической опасности [23—25].
Из числа экскреторных факторов наибольшее значение имеет β-гемолизин/цитолизин, вызывающий повреждение клеток, в том числе эритроцитов, и индуцирующий нарушения функционального состояния сердца и печени, способствующий проникновению бактерии через эпителиальные барьеры и развитию сепсиса, препятствующий фагоцитозу. Важен также CAMP-фактор: его патогенетическое значение не доказано, но он является дифференцирующим маркером культур S. agalactiae и S. pyogenes.
СГВ проявляет стабильную чувствительность к пенициллину и другим β-лактамным антибиотикам. В последние годы значительно возросла резистентность S. agalactiae к линкозамидам и макролидам (во многих странах частота выделения устойчивых к клиндамицину штаммов достигла 13—20%, а к эритромицину — 25—32%). Особенно часто устойчивыми к эритромицину оказываются штаммы, относящиеся к V серотипу. Многие из них проявляют устойчивость к обоим упомянутым антибиотикам [26]. Нередка устойчивость к тетрациклинам, причем в ряде случаев она сочетается с резистентностью к макролидам, линкозамидам и хлорамфениколу. До 2003 г. резистентность S. agalactiae к фторхинолонам не регистрировали. В последующий период в Японии и США выделили штаммы СГВ с высоким уровнем устойчивости к широкому спектру фторхинолонов. Обнаруженные в Японии штаммы, устойчивые к фторхинолонам, относились к серотипу Ib [26, 27].
1.2. Эпидемиология
S. agalactiae распространен повсеместно. Природный резервуар бактерии обширен и включает различные виды млекопитающих (человек, обезьяна, крупный рогатый скот, верблюд, лошадь, дельфин, собака, кошка, хомяк, мышь), птиц (курица) и холоднокровных животных (лягушка, рыба, ящерица). Инфекция может передаваться от животных человеку, но большинство выделяемых от людей штаммов бактерий циркулируют среди населения, минуя зоонозный резервуар. Различия между штаммами бактерий, выделяемыми от людей и сельскохозяйственных животных, достаточно велики, что указывает на наличие нескольких самостоятельных эковаров агента, патогенных для основных хозяев.
СГВ является комменсалом микробиоты кишечника человека. Колонизируя дистальную часть прямой кишки, СГВ периодически распространяются и на другие локусы (влагалище, урогенитальный тракт, кожу и пр.). У большей части инфицированных взрослых людей колонизация протекает бессимптомно в виде здорового носительства.
Установлено, что у 5—35% женщин СГВ можно обнаружить во влагалище и часто в уретре их половых партнеров [8, 16, 33, 46, 48, 72]. Показана достоверная связь носительства СГВ во влагалище не только с ранними септицемиями новорожденных, но и с самопроизвольными выкидышами, преждевременными родами, преждевременным излитием околоплодных вод, мочевой инфекцией у беременных, рождением детей с низкой массой тела, развитием хориоамнионита в родах, эндометритом и сепсисом у родильниц [28—30]. Однако связь акушерской патологии и СГВ-носительства оказалась далеко не прямолинейной. Носительство СГВ во влагалище не является постоянным и чаще всего носит интермиттирующий характер. Наиболее высок уровень колонизации у женщин репродуктивного возраста и беременных [31—33]. У беременных СГВ выделяют из перечисленных областей в 7—30% случаев (чаще у молодых, имеющих высокую половую активность или пользующихся внутриматочными средствами контрацепции). Из них 60—75% остаются СГВ-носителями до конца беременности. Обследование во время беременности не дает адекватного прогноза о возможности колонизации родовых путей во время родов. И хотя контаминация плода в родах происходит у каждой второй роженицы — носительницы СГВ, только у 2—5% инфицированных новорожденных развиваются тяжелые формы СГВ-инфекций с летальностью 20—70% [34] и высокими показателями при преждевременных родах. Тяжелые инфекции ассоциированы с длительными родами и ранним разрывом плодных оболочек. Чаще всего СГВ-сепсис регистрируют у новорожденных, рожденных от матерей с высокой степенью колонизации влагалища, тем не менее около 30% неонатального СГВ-сепсиса регистрируют при низких титрах СГВ в родовых путях [35]. Механизм заражения плода всегда связан с восходящим из влагалища инфицированием околоплодных вод, размножением и накоплением в них СГВ. Заражение плода происходит при заглатывании и аспирации инфицированных околоплодных вод. Однако возможно инфицирование плода через неповрежденные оболочки — интраканаликулярно [36, 37].
Эпидемиология поздней формы болезни детей мало изучена. Предполагают, что она возникает в результате передачи возбудителя как во время родов, так и в последующий период и в половине случаев связана с отсроченным началом развития заболевания при заражении от матери в родах либо с горизонтальным путем передачи от инфицированных медицинских работников в стационаре или взрослого во внебольничной среде [1, 15].
В настоящее время в мире отсутствует вакцина против СГВ-инфекций, хотя интенсивно идут разработки в разных странах мира в этом перспективном направлении [40—45].
2. Клинические формы инфекций, вызванные стрептококком группы В
В зависимости от сроков манифестации различают две формы клинического проявления СГВ-инфекции у новорожденных: раннюю и позднюю. Однако их симптоматика неспецифична.
Ранняя форма СГВ-инфекций в 90% случаев проявляется в первые 12 ч после рождения ребенка. В подавляющем большинстве случаев ее проявлениями являются сепсис и/или пневмония, реже — гнойный менингит или менингоэнцефалит, чаще у недоношенных детей спорадически проявляются поражения других органов.
Выраженность клинических проявлений ранней формы СГВ-инфекции вариабельна. У недоношенных детей возможно молниеносное течение заболевания, сопровождающееся септическим шоком, респираторным дистресс-синдромом и летальным исходом, наступающим в течение нескольких часов.
Пневмония сопровождается дыхательной недостаточностью вплоть до персистирующей легочной гипертензии. Нарушения дыхания проявляются уже в первые часы после рождения ребенка.
Начальная стадия менингита нередко остается незамеченной из-за слабой выраженности и вариабельности клинических нарушений, ассоциированных с поражением центральной нервной системы.
Поздняя форма СГВ-инфекций новорожденных проявляется в период 2—12 нед жизни, реже — в возрасте до 6 мес. У 80—85% заболевших она проявляется менингитом, реже сепсисом, остеомиелитом и/или септическим артритом, спорадически этмоидитом, лимфаденитом, конъюнктивитом, эндокардитом, эпиглоттитом, эмпиемой, некротизирующим фасциитом и токсическим шоком.
У беременных женщин инфекция может сопровождаться воспалительными заболеваниями мочевых путей, хориоамнионитом, эндометритом, ассоциированной с кесаревым сечением раневой инфекцией.
Бессимптомная бактериурия у беременных женщин
По данным литературы, бактериурия, вызванная СГВ, обнаруживается в моче 2—7% беременных женщин и является маркером массивной колонизации родовых путей [46—50]. СГВ-бактериурия родильниц связана с повышенным риском ранних СГВ-инфекций у новорожденных [46—49] и поэтому является абсолютным показателем для антибиотикопрофилактики в родах даже при низких концентрациях возбудителя в моче (С III) [54, 55].
Факторы, сочетающиеся с инфицированием плода (новорожденного) [11, 56—65]:
— преждевременные роды (AII);
— повышение температуры тела у роженицы выше 38 °C (AII);
— безводный промежуток более 18 ч (критический период 24 ч);
— низкая масса тела, недоношенность (рост заболеваемости СГВ-инфекцией увеличивается в 7—15 раз);
— инфицированность плаценты и/или амниотической жидкости (хориоамнионит, внутриматочная инфекция).
Прогностические маркеры инфицирования плода (новорожденного) во время беременности (родов):
— анамнестические факторы риска: в анамнезе дети, рожденные с признаками заболевания, вызванного СГВ (AII) [66—69];
— СГВ в моче во время настоящей беременности (маркер высокого риска колонизации плода) (AIII) [31, 33, 46, 48, 65];
— интактные плодные оболочки и родоразрешение путем операции кесарева сечения не исключают инфицирования новорожденного (CIII) [70, 71].
Риск передачи СГВ новорожденному:
— при инфицировании матери составляет 42—72%;
— у 2/3 колонизированных новорожденных от матерей с выявленным СГВ развивается бессимптомное носительство [72];
— на каждые 100 инфицированных доношенных новорожденных приходится 1 случай тяжелой СГВ-инфекции, в сроки гестации 28—37 нед — 15—20% случаев на 100 новорожденных и при сроке менее 28 нед беременности достигает 100% [8];
— потенциальным источником СГВ-инфекции является не только мать ребенка, но и медицинский персонал (в 16—47% случаев) [72].
Читайте также:

