Микробиологический мониторинг в системе инфекционного контроля
Обновлено: 07.05.2024
Цель: определить эффективность микробиологического мониторинга среди новорожденных детей в системе мер профилактики инфекционно-воспалительных заболеваний на примере конкретного стационара. Проведен ретроспективный анализ результатов микробиологического обследования 952 новорожденных (нестерильные локусы — кал, зев), нозологической и этиологической структуры инфекционно-воспалительных заболеваний в 2007 и 2011 г. Установлено, что изменение антибиотикополитики отделения отразилось на составе микробных сообществ, заселяющих слизистые оболочки желудочно-кишечного тракта новорожденных. Показано, что изменение состава микробной колонизации слизистых оболочек отражает изменения этиологической и нозологической структуры инфекционно-воспалительных заболеваний новорожденных. Заключение. Микробиологический мониторинг позволяет получить полноценный микробный пейзаж отделения при регулярном обследовании нестерильных локусов, наиболее доступных для исследования и формирующих самые многочисленные микробиоты (кал и посев из зева). Наблюдение за динамикой колонизации нестерильных локусов позволяет обнаружить предвестники возможных массовых клинических случаев инфекций и предотвратить их.
Ключевые слова
Об авторах
д.м.н., зав. отделом неонатологии и педиатрии
врач клинический фармаколог отдела микробиологии и клинической фармакологии
д.м.н., зав. отделением патологии новорожденных и недоношенных детей
к.м.н., гл.н.с. лаборатории микробиологии
Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова, Москва
Россия
д.м.н., проф., научн. консультант
Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова, Москва
Россия
д.м.н., гл. врач
Список литературы
1. Брудастов Ю.А. Гриценко В.А., Журлов О.С. и др. Свойства E.coli как факторы транслокации из кишечника во внутренние органы. Вестник ОГУ. Приложение Биология и медицина 2005; 5: 9—14. (Brudastov Y.A., Gricenco V.A.. Gurlov O.S. et al. E.coli properties as translocation factors from intestines in an internal. Vestnik OGU 2005; 5: 9—14.)
2. Клиническая лабораторная аналитика. Том IV. Частные аналитические технологии в клинической микробиологии. Под ред. В.В. Меньшикова. М: Агат-Мед 2003; 816. (Menschikov V.V. Clinical laboratory analyst. Private analytical technologies in clinical microbiology. Moscow: Agat-Med 2003; 816.)
4. Любимова А.В., Зуева Л.П., Пулин А.М. и др. Микробиологический мониториг в отделениях реанимации новорожденных. Эпидемиол и вакцинопрофилакт 2011; 5: 25— 29. (Ljubimova A.V., Zueva L.P., Pulin A.M. Microbiological monitoring in neonatal intensive care units. EHpidemiol i vaktsinoprofilakt 2011; 5: 25—29.)
5. Любасовская Л.А., Припутневич Т.В., Анкирская А.С. и др. Особенности микробной колонизации новорожденных в отделении реанимации и интенсивной терапии. Рос вестн перинатол и педиатр 2013; 3: 87—91. (Lyubasovskaya L.A., Priputnevich T.V., Ankirskaya A.S. et al. Features of microbic colonization of newborns in NICU. Ros Vestn Perinatol i Pediatr 2013; 3: 87—91.)
6. Сергевнин В.И., Маркович Н.И., Авдеева Н.С. Пути совершенствования микробиолоического мониторинга в системе эпидемического надзора за внутрибольничными гнойно-септическими инфекциями. Казанский мед журн 2008; 5: 725—728. (Sergevnin V.I., Markovich N.I., Avdeeva N.S. Ways of improvement of mikrobioloichesky monitoring in system of epidemic supervision of the intrahospital it is purulent — septic infections. Kazanskij med zhurn 2008; 5: 725—728.)
7. Sohn A.H., Garrett D.O., Sinkowitz-Cochran R.L. et al. Prevalence of nosocomial infections in neonatal intensive care unit patients: results from the first national point-prevalence survey. J Pediatr 2001; 139: 6: 821—827.
8. Зубков В.В., Рюмина И.И., Евтеева Н.В. и др. Результаты проведения клинического аудита инфекционно-воспалительных заболеваний у новорожденных. Акушерст- во и гинекология 2012; 7: 74—80. (Zubkov V.V., Ryumina I.I., Evteeva N.V. et al. Results of carrying out clinical audit of infectious and inflammatory diseases at newborns. Аkusherstvo i ginekologiya 2012; 7: 74—80.)
9. Перинатальный аудит при преждевременных родах. М: Водолей Publishers, 2005;. 224 (Perinatal audit in preterm labor. Moscow: Vodoley 2005; 224.)
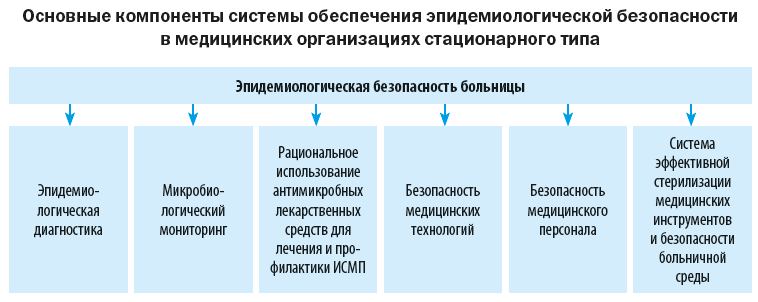
Высококвалифицированная и безопасная медицинская помощь — приоритетная задача современного здравоохранения. Одним из критериев качества медицинских услуг является эпидемиологическая безопасность пациентов и профилактика инфекций, связанных с оказанием медицинской помощи (ИСМП). Данный раздел работы должен контролироваться главными врачами или их заместителями, а также главными медицинскими сестрами в ходе реализации программы внутреннего контроля и аудита.
Эпидемиологическая безопасность медицинской помощи – это условия, при которых отсутствует недопустимый риск возникновения у пациентов и медицинского персонала инфекций, связанных с оказанием медицинской помощи.
Ключевая роль в реализации требований по эпидбезопасности принадлежит госпитальному эпидемиологу, а также администрации медицинской организации.
Рассмотрим их подробно.
1. Эпидемиологическая диагностика
Включает в себя совокупность приемов и способов, направленных на выявление причин и факторов риска возникновения ИСМП.
И чтобы эпидемиологическая диагностика была эффективной, в стационаре должна функционировать система активного выявления, учета, регистрации и анализа ИСМП.
Методы выявления инфекций делятся на пассивные и активные.
Пассивные методы предполагают, что врачи и медицинские сестры сами сообщают госпитальному эпидемиологу о случаях ИСМП. Однако такой подход малоэффективен и позволяет выявить не более 35 % всех инфекций.
Поэтому более предпочтительны активные методы, которые подразумевают постоянное наблюдение за пациентами, цель которого — выявить случаи ИСМП.
Активное эпидемиологическое наблюдение может быть тотальным или целенаправленным. В первом случае наблюдение организуют за всеми пациентами стационара и исходами их заболеваний. Во втором случае наблюдение может проводиться в отношении:
- конкретных видов ИСМП (например, инфекции в области хирургического вмешательства, внутрибольничные пневмонии, катетер-ассоциированные инфекции кровотока, внутрибольничные инфекции мочевыводящих путей);
- определенных групп пациентов (хирургические пациенты, пациенты, находящиеся на искусственной вентиляции легких, пациенты с центральными сосудистыми катетерами);
- отделений повышенного риска (отделения реанимации, ожоговые отделения, хирургические отделения).
С целью выявления случаев ИСМП в медицинской организации разрабатывают перечень стандартных определений случаев ИСМП, т. е. набор критериев, позволяющих определить, есть или нет у пациента инфекционного заболевания или состояния, связанного с лечебно-диагностическим процессом. Данные критерии используют лечащие врачи и врачи-эпидемиологи для постановки клинического или эпидемиологического диагноза.
Если у пациента выявлены признаки ИСМП, заполняется карта эпидемиологического наблюдения. В ней указываются:
- общие данные о пациенте;
- сведения о факторах риска возникновения ИСМП;
- критерии, на основании которых был поставлен диагноз ИСМП.
К сведению
В стационаре должны быть разработаны карты эпидемиологического наблюдения для различных видов ИСМП, актуальных для данной медицинской организации.
Выявленные ИСМП регистрируются в установленном порядке. На каждый случай заполняется экстренное извещение об инфекционном заболевании по форме 058/у, которое направляется в органы, уполномоченные осуществлять государственный санитарно-эпидемиологический надзор, информация вносится в журнал учета инфекционной заболеваемости (форма 060/у).
Ретроспективный анализ заболеваемости ИСМП у пациентов позволяет выявить фоновый уровень заболеваемости, основные источники инфекции, ведущие факторы передачи. На его основе разрабатываются профилактические и противоэпидемические мероприятия, адекватные конкретной эпидемиологической обстановке как в медицинской организации в целом, так и в конкретных отделениях.
Ретроспективный анализ заболеваемости медицинского персонала позволяет выявить источники инфекции и провести мероприятия, ограничивающие их роль в распространении ИСМП.
Сведения об ИСМП вносятся в электронные таблицы. Это позволяет накапливать, систематизировать и анализировать информацию.
К сведению
Используя базы данных, врач-эпидемиолог может рассчитать относительные частотные показатели заболеваемости, чтобы сравнивать и сопоставлять заболеваемость ИСМП в различные временные промежутки, а также в разных группах пациентов, выявлять факторы, влияющие на эпидпроцесс.
Чтобы рассчитать относительные частотные показатели заболеваемости, необходима информация об основных действующих факторах риска, таких как:
- количество дней искусственной вентиляции легких;
- количество дней катетеризации сосудов;
- количество дней катетеризации мочевого пузыря и т. д.
Данные собираются обо всех пациентах, подвергающихся фактору риска, вне зависимости от того, развивается у них ИСМП или нет.
Собирать данные должен персонал, который непосредственно осуществляет уход за пациентами, например медицинские сестры.
2. Микробиологический мониторинг
Программа микробиологического мониторинга разрабатывается для анализа микроорганизмов, циркулирующих в медицинской организации, выделенных от пациентов, персонала и с объектов внешней среды, а также для раннего выявления формирования госпитальных штаммов и вспышек ИСМП.
Мониторинг должен включать:
- бактериологические исследования биологического материала пациентов отделений стационара при наличии клинических или эпидемиологических показаний;
- санитарно-бактериологические исследования объектов больничной среды в плановом порядке и при наличии эпидемиологических показаний;
- анализ чувствительности/резистентности выделенных микроорганизмов с целью раннего выявления госпитальных штаммов и вспышек ИСМП;
- внесение данных, полученных в ходе проведения бактериологических исследований, в электронную базу данных аналитической компьютерной программы;
- анализ микробиологического пейзажа отделений стационара;
- разработку и корректировку протоколов определения чувствительности микроорганизмов к антимикробным препаратам, дезсредствам, бактериофагам;
- оценку и корректировку проводимой антимикробной терапии, коррекция лекарственного формуляра;
- оценку и корректировку дезинфекционных мероприятий в стационаре.
Микробиологический мониторинг — важнейший компонент системы эпидемиологической безопасности любой медицинской организации, неотъемлемое звено в обеспечении эпидемиологического наблюдения за инфекциями, связанными с оказанием медицинской помощи (ИСМП). Это комплексное и динамическое наблюдение за патогенными и условно-патогенными микроорганизмами, выделенными от пациентов, персонала и с объектов больничной среды, их свойствами и особенностями циркуляции.
Реализация мониторинга позволяет:
• изучить этиологическую структуру ИСМП;
• своевременно обнаружить циркуляцию госпитальных штаммов, оценить качество дезинфекционно-стерилизационного режима;
• вовремя выявить предвестники эпидемиологического неблагополучия, чтобы целенаправленно и эффективно провести необходимые профилактические и противоэпидемические мероприятия.
Расскажем, как это сделать.
ЗАДАЧИ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА
Основная функция микробиологического мониторинга — оценка этиологических факторов возникновения ИСМП. Помимо этого реализация мониторинга позволяет решать и другие важные задачи:
• оценивать частоту колонизации пациентов и контаминации объектов внешней среды различными микроорганизмами, в том числе имеющими эпидемиологическое значение;
• изучать свойства микроорганизмов, циркулирующих в больничной среде, такие как вирулентность, антибиотикорезистентность, устойчивость к дезсредствам и антисептикам;
• выявлять штаммы, получившие приоритетное распространение в конкретной медицинской организации, оценивать микробный пейзаж учреждения в целом и его подразделений;
• прогнозировать развитие эпидемиологической ситуации по ИСМП;
• принимать управленческие решения по лечению и профилактике ИСМП, разработке лекарственного формуляра антибиотиков, протоколов периоперационной антибиотикопрофилактики и терапии.
ПЛАНОВЫЙ И ВНЕПЛАНОВЫЙ МИКРОБИОЛОГИЧЕСКИЙ МОНИТОРИНГ
Плановый микробиологический мониторинг проводится, если нет предпосылок для неблагоприятной эпидемиологической ситуации, и включает обследования пациентов с признаками инфекционно-воспалительных заболеваний, пациентов, имеющих предпосылки развития ИСМП, плановые микробиологические исследования объектов больничной среды, цель которых — оценить качество текущей и заключительной дезинфекции.
Внеплановый микробиологический мониторинг (по эпидемиологическим показаниям) проводится по результатам эпидемиологической диагностики, если по данным ретроспективного анализа и результатам текущего наблюдения выяснилось, что эпидемиологическая ситуация ухудшилась.
Как проводят внеплановый мониторинг?
1. Проводят сплошные обследования пациентов (не менее 10–15 чел.) независимо от наличия клинических показаний в отделениях, где сформировалась неблагоприятная эпидемиологическая ситуация.
2. Выполняют забор проб с поверхностей объектов внешней среды, имеющих высокое эпидемиологическое значение (берут пробы с рук медицинского персонала, блоков управления медицинским оборудованием, составных частей сложной медицинской техники и инвазивных устройств, объектов, находящихся в непосредственном контакте с пациентами).
Как определить количество проб?
Объем проб и перечень объектов, подлежащих изучению, определяет врач-эпидемиолог исходя из особенностей лечебно-диагностического процесса и ведущих факторов передачи ИСМП в медорганизации.
В отличие от планового контроля все пробы отбирают в обычном режиме во время работы структурного подразделения.
7 ЭТАПОВ ОРГАНИЗАЦИИ СИСТЕМЫ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА В УЧРЕЖДЕНИИ
Этап 1. Определяем заинтересованных специалистов и распределяем обязанности.
При организации системы микробиологического мониторинга в медицинском учреждении прежде всего необходимо определить заинтересованных специалистов. Как правило, это заместитель главного врача, заведующий бактериологической лабораторией, заведующий эпидемиологическим отделом, клинический фармаколог.
Функциональные обязанности этих специалистов при реализации программы мониторинга мы свели в таблицу.
Этап 2. Определяем показания к проведению исследований.
Чтобы система микробиологического мониторинга была эффективной, нужно заблаговременно определить объем исследований, подготовить методологическую базу и необходимое программное обеспечение. И в первую очередь — конкретизировать перечень клинических и эпидемиологических показаний, при которых необходимо производить отбор биологического материала у пациентов для проведения лабораторных исследований.
от 30 ноября 2006 года N 457
Об утверждении клинико-организационного руководства по микробиологическому обеспечению системы инфекционного контроля лечебно-профилактического учреждения
1. Утвердить прилагаемое Клинико-организационное руководство "Микробиологическое обеспечение системы инфекционного контроля лечебно-профилактического учреждения".
2. Руководителям органов управления, государственных и муниципальных учреждений здравоохранения Челябинской области рекомендовать принять в качестве дополнительных рекомендаций для работы с федеральными и территориальными стандартами Клинико-организационное руководство "Микробиологическое обеспечение системы инфекционного контроля лечебно-профилактического учреждения", утвержденное п. 1 настоящего приказа.
3. Контроль за исполнением настоящего приказа возложить на первого заместителя Министра здравоохранения Челябинской области Москвичеву М.Г.
Министр здравоохранения
Челябинской области
В.А.ШЕПЕЛЕВ
Утверждено
приказом
Министерства здравоохранения
Челябинской области
от 30 ноября 2006 года N 457
МИКРОБИОЛОГИЧЕСКОЕ ОБЕСПЕЧЕНИЕ СИСТЕМЫ ИНФЕКЦИОННОГО КОНТРОЛЯ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОГО УЧРЕЖДЕНИЯ
Клинико-организационное руководство
Выгоняйлов Александр Витальевич, - ГМЛПУЗ "Челябинская
главный внештатный госпитальный областная клиническая
эпидемиолог Министерства здравоохранения больница", руководитель
Челябинской области, заместитель рабочей группы
главного врача ГМЛПУЗ "Челябинская
областная клиническая больница",
кандидат медицинских наук.
Брызгалова Ирина Викторовна, - ГОУ ВПО Росздрава
заместитель главного врача "Челябинская
Молчанова Ирина Витальевна, главный - ГМЛПУЗ "Челябинская
внештатный бактериолог Министерства областная клиническая
здравоохранения Челябинской области, больница"
Клинико-организационное руководство "Микробиологическое обеспечение системы инфекционного контроля лечебно-профилактического учреждения" предназначено для применения в учреждениях здравоохранения Челябинской области.
СПИСОК СОКРАЩЕНИЙ И ОСНОВНЫЕ ОПРЕДЕЛЕНИЯ
Инфекционный контроль (ИК) - система эффективных организационных, профилактических и противоэпидемических мероприятий, направленных на предупреждение возникновения и распространения инфекционных заболеваний в стационаре, базирующихся на результатах эпидемиологической диагностики.
Госпитальные инфекции (ГИ) - любые инфекционные заболевания (состояния), проявившиеся или возникшие в условиях стационара. Понятие ГИ включает в себя заносы инфекции и внутрибольничные инфекции.
ГСИ - гнойно-септическая инфекция.
Заносы инфекции - это инфекционные заболевания, с местом заражения вне лечебно-профилактического учреждения, но проявившиеся при поступлении в стационар, либо во время пребывания в стационаре.
Внутрибольничные (нозокомиальные) инфекции (ВБИ) - это инфекционные заболевания (состояния), возникшие в данном лечебном учреждении и не имевшиеся до поступления в стационар даже в инкубационном периоде, проявившиеся в условиях стационара или после выписки пациента в течение инкубационного периода. Либо связанные с проведением медицинских манипуляций в амбулаторно-поликлинических условиях.
Примечание: инфекции, вызванные условно-патогенными микроорганизмами, могут считаться внутрибольничными в пределах 30 дней после выписки из стационара, если установлен факт внутрибольничного заражения. К внутрибольничным инфекциям относятся также случаи инфицирования работников лечебно-профилактических учреждений, возникшие в результате их профессиональной деятельности.
Эпидемиологический надзор (ЭН) - динамическая оценка состояний и тенденций развития эпидемического процесса и своевременное вмешательство в его ход с целью достижения конечного результата - профилактики и снижения инфекционной заболеваемости.
Микробиологическое обеспечение инфекционного контроля (МН) - слежение за микробиологическим пейзажем культур, выделяемых от больных с учетом антибиотикорезистентности, чувствительности к дезинфектантам и возможной смене возбудителей по видовому и типовому признакам.
ЛПУ - лечебно-профилактическое учреждение
КИК - комитет инфекционного контроля лечебно-профилактического учреждения.
Микробиологическое обеспечение инфекционного контроля
Система эпидемиологического надзора за внутрибольничными инфекциями, помимо учета и регистрации внутрибольничных инфекций, включает в себя:
- расшифровку этиологической структуры ВБИ;
- санитарно-бактериологические исследования объектов окружающей среды в ЛПУ;
- изучение циркуляции патогенных и условно-патогенных микроорганизмов;
- определение широты распространения и спектра устойчивости микроорганизмов к антибиотикам, антисептикам, дезинфектантам.
1. Расшифровка этиологии внутрибольничных инфекций имеет важное значение для выбора рациональных методов лечения, оценки эпидемической ситуации в стационаре и организации целенаправленных противоэпидемических мероприятий.
Для расшифровки этиологии внутрибольничного заболевания проводится:
- Микробиологическое обследование патологического материала от больного с использованием методов количественного учета микроорганизмов в исследуемом материале;
- Идентификация выделенных микроорганизмов и внутривидовая дифференциация;
- Определение спектра чувствительности выделенных штаммов к антибиотикам;
- В отдельных случаях определение специфических антител в динамике в сыворотке заболевшего.
Этиологическая роль условно-патогенного микроорганизма при внутрибольничном заболевании может быть основана на следующих признаках: выделение данного микроорганизма из патологического материала в монокультуре или его доминирование в микробных ассоциациях, массивность выделения, обнаружение данного микроорганизма при повторных исследованиях, наличие специфических иммунологических сдвигов в организме больного.
Микробиологическое обеспечение системы инфекционного контроля в ЛПУ включает:
- Разработку перечня показаний для микробиологического обследования;
- Стандартизацию техники забора образцов материала и транспортировки их в микробиологическую лабораторию;
- Стандартизацию тестирования микроорганизмов на чувствительность к антибиотикам, внедрение в деятельность лаборатории системы внутреннего контроля качества;
- Внедрение компьютерной аналитической программы WHONET;
- Внедрение в работу микробиологической лаборатории методики определения чувствительности микрофлоры к антисептикам и дезинфектантам;
- Проведение дополнительного обучения сотрудников учреждения методикам забора, хранения, транспортировки проб для бактериологических исследований.
Внедрение данных мероприятий в сочетании с совершенствованием системы эпидемиологической диагностики (эффективный оперативный и ретроспективный эпидемиологический анализ) позволяет организовать слежение за формированием госпитальных штаммов микроорганизмов.
С целью соблюдения в ЛПУ единой рациональной тактики и стратегии организации антибиотикопрофилактики и антибиотикотерапии, а также создания единой системы микробиологической диагностики внутрибольничных инфекций необходимо разработать и внедрить систему микробиологического мониторинга, соответствующую международным стандартам.
В учреждении должен быть принят приказ "О введении стандартов микробиологических исследований" во всех отделениях. Приказом также регламентируется введение стандартной формы направления на микробиологическое исследование.
Предлагаются следующие варианты:
Регламент микробиологического исследования беременных, рожениц и родильниц
В целях улучшения качества организации микробиологического мониторинга за микробиологическим пейзажем и уровнем антибиотикорезистентности циркулирующих микроорганизмов среди пациентов акушерского отделения, является целесообразным ввести следующую конкретную схему бактериологического обследования. Примером создания такой схемы может служить ниже следующий вариант:
4. МЕТОДЫ КОНТРОЛЯ
МИКРОБИОЛОГИЧЕСКИЙ МОНИТОРИНГ ПРОИЗВОДСТВЕННОЙ СРЕДЫ
Дата введения 1999-05-10
УТВЕРЖДЕНЫ Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации Г.Г.Онищенко, 1999 г.
1. Область применения
Данный документ предназначен в основном для производителей медицинских иммунобиологических препаратов (МИБП) и может служить в качестве руководства по методам общего микробиологического контроля в чистых помещениях, который включает в себя контроль воздуха рабочих зон, контроль поверхностей помещений и оборудования, контроль рук и одежды персонала.
Методические указания "Микробиологический мониторинг производственной среды" являются приложением к Санитарным правилам СП 3.3.2.015 "Производство и контроль медицинских иммунобиологических препаратов для обеспечения их качества. Good Manufacturing Practice", утвержденных постановлением Госкомсанэпиднадзора России от 12.08.94 г., N 8, а также продолжением соответствующих разделов Методических рекомендаций МУ-44-116 "Асептическое производство медицинских иммунобиологических препаратов", утвержденных МЗ России 19.05.97 г.
Микробиологический контроль воды, сжатого воздуха и других технологических газов, контроль механических частиц в данных методических указаниях не рассматриваются.
2. Общие положения
В данных методических указаниях рассматриваются ключевые факторы, которые необходимо учитывать при разработке и проведении программ микробиологического контроля производственной среды, составлении планов отбора проб, выборе методов и приборов для проведения исследований, установлении уровней тревоги и действия.
Приводимые в данном документе цифровые данные, методы отбора проб, приборы являются рекомендуемыми. Целесообразно их применение с учетом конкретных производственных условий и технологий.
Для достижения соответствующего микробиологического статуса производственной среды (см. Таблицу 1.3 Приложения 1 к Методическим рекомендациям МУ-44-116 "Рекомендуемые максимальные пределы контаминации окружающей среды в рабочих условиях") могут использоваться методы, эквивалентные тем, которые вошли в данные методические указания.
3. Определения
В данных методических указаниях используются следующие определения:
3.1. асептическое наполнение: часть асептического процесса, в котором стерильный продукт разливается и упаковывается с использованием стерильных емкостей и крышек в критических производственных зонах;
3.2. асептическое производство: включает все операции приготовления МИБП, в том числе и асептическое наполнение емкостей продуктом в контролируемых условиях среды, где воздухоподача, материалы, оборудование и персонал соответствующим образом контролируются на приемлемые уровни микробной контаминации и контаминации механическими частицами;
3.3. асептические производственные зоны (АПЗ): контролируемая среда, состоящая из нескольких зон, в которых воздухоподача, материалы, оборудование и персонал контролируются на приемлемые уровни микробной контаминации и контаминации механическими частицами;
3.4. аэрозольный пробоотборник: прибор, используемый для отбора заданных объемов воздуха за определенный временной промежуток в целях определения количественного содержания микроорганизмов или механических частиц;
3.5. биологическая нагрузка: общее количество живых микроорганизмов в продукте перед процессом стерилизации;
3.6. валидация (аттестация): получение документированного подтверждения того, что конкретный производственный процесс обеспечит с высокой степенью надежности получение продукта, отвечающего заранее установленным спецификациям и показателям качества;
3.7. контролируемая среда: среда производственных помещений, в которой содержание механических и живых частиц поддерживается на определенных уровнях;
3.8. корректирующие действия: действия, которые необходимо предпринимать в случае, если результаты контроля окружающей среды выявляют превышение уровня действия;
3.9. колониеобразующая единица (КОЕ): число живых микроорганизмов, определяемое по проросшим единичным колониям на плотных питательных средах, содержащееся в определенных объемах исследуемых проб;
3.10. критические производственные зоны: локальные зоны асептического производства, в которых совершаются асептические манипуляции с продуктом, асептический монтаж оборудования, операции наполнения и укупорки, где продукт подвергается наибольшему риску контаминации. Данные зоны, как правило, располагаются в классах чистоты А, В (100) в соответствии с МУ-44-116;
3.11. критические поверхности: поверхности, находящиеся в зоне выполнения асептических операций, непосредственно контактирующие со стерильным материалом (емкостями, инструментарием и пр.);
3.12. окружающая флора: микроорганизмы, выделенные из производственной среды совокупностью микробиологических методов исследования;
3.13. план отбора проб: документ, описывающий методику отбора проб в контролируемой среде, устанавливающий точки отбора проб, частоту и количество регулярно проводимых исследований, методы анализа данных и интерпретацию полученных результатов;
3.14. программа мониторинга окружающей среды: документально определенная программа, которая описывает правила текущего мониторинга производственной среды по всем контролируемым параметрам: влажность, температура, скорость воздушных потоков, уровень перепада давления между помещениями, уровень контаминации бактериальными и механическими частицами и включает в себя план мероприятий при превышении результатов контроля уровня действия;
3.15. стерилизация: валидируемый процесс, используемый для освобождения продукта от живых микроорганизмов;
3.16. стерильный: заявленный как свободный от живых микроорганизмов;
3.17. терминальная стерилизация: процесс, при котором продукт стерилизуется в своей конечной емкости;
3.18. точка отбора пробы: отраженное в документах место в контролируемой зоне, где производится отбор пробы для дальнейших микробиологических исследований. Точка выбирается, исходя из потенциального влияния на стерильность продукта;
3.19. уровень действия: установленный критический уровень содержания микробов или механических частиц, требующий немедленного вмешательства и корректирующих действий, если он превышен;
3.20. уровень тревоги: установленный докритический уровень содержания микробов или механических частиц, дающий раннее предупреждение о возможном отклонении от нормальных рабочих условий производства, не требующий немедленного вмешательства и исправляющих действий, но который является поводом для проведения дополнительных контролей;
3.21. чистая зона: заданное пространство, где концентрация живых и механических частиц в воздушной среде поддерживается в установленных пределах в соответствии с классом чистоты;
3.22. чистая комната: комната, где концентрация живых и механических частиц в воздушной среде поддерживается на заданном уровне, определяемым классом чистоты.
4. Программа микробиологического мониторинга контролируемой среды
Основной целью программы оценки микробиологического состояния производственной среды является постоянная гарантия стабильности асептических условий производства МИБП, выявление начальных отклонений и выработка корректирующих действий до возникновения ситуаций, приводящих к появлению нестерильной продукции.
Метод контроля стерильности готового препарата (ГФ IX, вып.2, с.187) основан на выборочном исследовании части серии и не дает полной гарантии стерильности каждой емкости в серии. Поэтому необходимо проводить промежуточные тесты на стерильность препарата в процессе производства, а также качественный и количественный контроль асептических условий (класса чистоты рабочих зон).
4.1. Программа микробиологического мониторинга окружающей среды в АПЗ должна охватывать:
- оценку бактериальной контаминации воздуха (КОЕ/м);
- оценку бактериальной контаминации критических поверхностей, рук и одежды персонажа, работающих в АПЗ;
- оценку эффективности очистки и дезинфекции помещений и оборудования;
- тестирование активности дезинфектантов;
- оценку эффективности работы стерилизующих воздушных фильтров;
- оценку качества стерилизации.
4.2. Текущий контроль в принципе не может и не должен выявить или подсчитать все микроорганизмы, присутствующие в контролируемой среде. Он может только показать, что все ключевые системы, контролирующие состояние производственной среды, работают в соответствии с установленными требованиями и лимиты бактериальной нагрузки не превышены.
4.3. Задачей микробиологического контроля является получение репрезентативной оценки бактериальной нагрузки производственной среды.
4.4. Стабильность асептических условий производственной среды должна обеспечиваться:
- соответствующим проектом производства;
- технологичным оборудованием (легко моющимся и дезинфицирующимся);
- адекватной системой воздухоподготовки (фильтрация, перепад давлений);
- системой ведения документации (рабочие инструкции и регистрация результатов контроля):
- валидированными и сертифицированными процессами деконтаминации;
- надежным контролем технологического процесса;
- практикой качественного поддержания чистоты (уборка, дезинфекция);
- контролем доступа персонала в АПЗ (соответствующая одежда, процедура переодевания);
- эффективными программами обучения персонала;
- гарантией качества материалов и оборудования.
4.5. Перечисленные поддерживающие функции должны обеспечиваться персоналом соответствующей квалификации, обученным правилам работы в АПЗ.
4.6. Программа микробиологического мониторинга производственной среды является документом, который периодически пересматривается и совершенствуется, (см. также раздел 17 Методических рекомендаций МУ-44-116).
5. Общие принципы процедуры микробиологического мониторинга
5.1. Вне зависимости от выбора метода тестирования, подготовка, технологический процесс, стерилизация, асептические процессы, контрольные тесты, очистка и дезинфекция оборудования и помещений, качество оборудования и используемых материалов должны полностью отвечать требованиям GMP.
5.2. При контроле используются только откалиброванное оборудование и приборы, прошедшие метрологическую аттестацию.
5.3. Любой метод, выбранный для текущего контроля должен предварительно пройти валидацию.
5.4. При текущем мониторинге предпочтительно использовать те же методы, что и при первичной аттестации чистого помещения или зоны. Любые изменения методов контроля могут повлиять на результаты.
5.5. Ростовые свойства питательных сред, используемых для микробиологических исследований, должны подтверждаться использованием соответствующих штаммов микроорганизмов.
5.6. В письменных инструкциях, описывающих процедуру микробиологического мониторинга, следует четко излагать шаг за шагом последовательность проведения исследований.
5.7. Полученные результаты должны регистрироваться в утвержденных по форме протоколах (журналах). В случаях превышения установленных верхних лимитов бактериальной нагрузки в АПЗ должны быть отражены все проведенные расследования и мероприятия.
5.8. Персонал, выполняющий программу микробиологического мониторинга должен быть компетентен в соответствующих научных дисциплинах, адекватно обучен и иметь необходимые полномочия.
5.9. Все исследования обычно проводятся производственными отделениями. Однако Отдел гарантии качества или Технологический отдел должен проводить периодические, независимые исследования, повторяющие программу микробиологического мониторинга. Периодичность обследования и протоколы утверждаются руководством предприятия.
5.10. Установление соответствующего уровня тревоги и уровня действия, выбор адекватных методов контроля являются предметами, постоянно требующими пересмотра. Все соответствующие решения должны приниматься уполномоченным персоналом.
5.11. Уровни тревоги и действия, частота контроля, число точек отбора проб обычно являются более строгими параметрами при процессе асептического розлива, чем при производстве терминально стерилизуемого продукта.
5.12. Процедуры микробиологического мониторинга обычно включают следующие шаги:
- выделения микроорганизмов из производственной среды (на агаровую поверхность, в питательный бульон или жидкость, на мембрану фильтра);
- посев, если требуется, на питательную среду и культивирование;
- анализ совокупности полученных при мониторинге данных.
5.13. Данные мониторинга следует учитывать для совершенствования практики уборки и дезинфекции.
5.14. Основные факторы, которые необходимо учитывать при определении методологии проведения тестов, приводятся в приложении.
6. Выбор точек отбора проб
6.1. Расположение точек отбора проб из воздуха и с поверхностей является индивидуальным для каждого производителя и устанавливается в процессе первичной или повторной аттестации чистого помещения или чистой зоны.
6.2. При запуске в эксплуатацию нового чистого помещения или зоны проводится изучение ее функционирования.
Читайте также: