Микробиология стафилококки пневмококки стрептококки
Обновлено: 16.04.2024
Инфекция вызванная пневмококком (Streptococcus pneumoniae): диагностика, лечение, профилактика
Streptococcus pneumoniae (пневмококк) — грамположительный кокк, который при росте на питательных средах образует ланцетовидные пары. Чувствителен к оптохину, подвержен лизису в присутствии солей жёлчи.
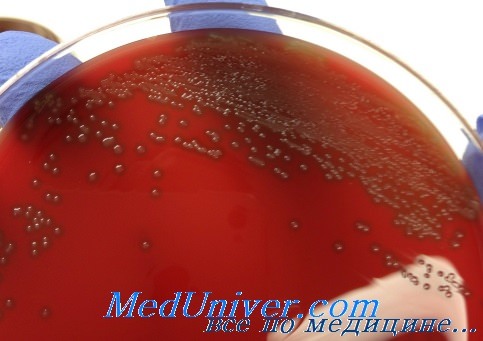
При росте на кровяном агаре штаммы пневмококка обычно обладают частичным гемолизом (а-гемолиз), в то же время гемолитическая активность различных штаммов может меняться. Инфекционные заболевания, вызванные пневмококком, — одна из самых распространённых причин смерти пациентов во всём мире. В группу риска входят дети, пожилые пациенты, а также лица с сопутствующими заболеваниями.
Патогенез пневмококковой инфекции (Streptococcus pneumoniae)
Пневмококки окружены полисахаридной капсулой, препятствующей фагоцитозу. Существует более девяноста различных капсульных серотипов возбудителя с различным уровнем патогенности и способностью к инвазии. Полисахарид, входящий в состав капсулы, обладает выраженными антигенными свойствами.
Антитела к капсульным полисахаридам у различных серотипов пневмококка — протективные, в то же время возможны перекрёстные иммунные реакции между различными серотипами. Компоненты клеточной стенки микроорганизма также способны вызывать выраженный воспалительный процесс.
Кроме того, пневмококки имеют несколько факторов адгезии, способствующих прикреплению возбудителя к полисахаридам поверхности клеток, что способствует колонизации организма.
Колонизация пневмококковой инфекции (Streptococcus pneumoniae)
Единственный источник инфекции — человек; носительство обычно протекает бессимптомно. Распределение серотипов зависит от региона, возраста пациента и социальной группы. Наиболее подвержены острой пневмонии дети первого года жизни.
Факторы, предрасполагающие к развитию тяжёлой инфекции: недостаточность комплемента, агаммаглобулинемия, ВИЧ-инфекция, алкоголизм и спленэктомия (удаление селезёнки). Немаловажную роль в развитии инфекционного процесса играют пневмококковые токсины: пневмолизин, нейраминидаза, гиалуронидаза и адгезины (например, пневмококковый поверхностный белок типа А).
Бактерии способны прикрепляться к пневмоцитам и проникать в кровоток, связываясь с рецепторами фактора агрегации тромбоцитов и активируя выработку пневмолизина или комплемент-индуцированного повреждения альвеол.
Клинические признаки инфекции вызванной пневмококком (Streptococcus pneumoniae)
Чаще всего Streptococcus pneumoniae вызывает острые отиты, синуситы и пневмонию. В 50—70% случаев причиной возникновения внебольничной пневмонии становятся пневмококки, при этом у 25—30% пациентов развивается бактериемия.
Прямое или гематогенное распространение инфекции приводит к развитию менингита и реже к целлюлиту, абсцессам, перитониту и эндокардиту. Бактериемия — тяжелейшее осложнение пневмококковой инфекции с высокой летальностью даже при соответствующем лечении.
Пневмококк считают второй из наиболее распространённых причин развития внебольничного менингита у детей, вакци-низированных против Haemophilus influenzae типа В, и основной причиной менингита у пациентов старше сорока лет. При этом отмечают достаточно высокий уровень смертности и вероятности развития осложнений.
Чувствительность пневмококка (Streptococcus pneumoniae) к антибиотикам
Ранее при лечении пневмококковых инфекций самым эффективным препаратом был пенициллин, но позднее благодаря генетической модификации пенициллинсвязывающего белка большинство штаммов приобрело к нему устойчивость. В настоящее время в клинической практике используют эритромицин, цефалоспорины, тетрациклин, рифампицин и хлорамфеникол, но всё чаще сталкиваются с мультирезистентными штаммами.
Препаратом выбора продолжает оставаться пенициллин, а при менингите, вызванном менее чувствительными штаммами, применяют цефотаксим или цефтриаксон. В случае высокой устойчивости к пенициллину дополнительно назначают гликопептидные препараты (ванкомицин).
Профилактика заболевания вызванной пневмококком (Streptococcus pneumoniae)
Для профилактики пневмококковой инфекции применяют поливалентную капсульную полисахаридную вакцину для профилактики пневмококковых инфекций, эффективную при назначении пациентам в зрелом возрасте и менее действенную у лиц со сниженным иммунитетом и детей младше двух лет.
Недавно созданная конъюгированная вакцина обладает достаточно высокой иммуностимулирующей способностью у детей младшего возраста.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
- Вернуться в раздел "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Пневмококк. Streptococcus pneumoniae. Эпидемиология пневмококка. Морфология пневмококка. Культуральные свойства пневмококка.
Впервые пневмококк выделил Пастер (1881) во время работы над антирабической вакциной и первоначально считал его возбудителем бешенства. Этиологическую роль пневмококка в развитии пневмоний у человека доказали К. Френкель и А. Вайхзельбаум (1884).
Бактерии пневмококка не содержат группового Аг и серологически неоднородны — по Аг капсульных полисахаридов выделяют 84 серовара. Известны штаммы, колонизирующие организмы человека и животных.
Эпидемиология пневмококка
Пневмококк — один из основных возбудителей внебольничных бактериальных пневмоний (2-4 случая на 1000 человек). Ежегодно в мире регистрируют не менее 500 000 случаев пневмококковых пневмоний, причём наиболее подвержены инфекции дети и лица преклонного возраста.
Резервуар пневмококковой инфекции — больные и носители (20-50% детей дошкольного возраста и 20-25% взрослых), основной путь передачи пневмококка — контактный, а в период вспышек также воздушно-капельный. Пик заболеваемости приходится на холодное время года.
В подавляющем большинстве случаев клинические формы пневмококковой инфекции развиваются при нарушениях резистентности организма (в том числе вследствие Холодовых стрессов), а также на фоне сопутствующей патологии (серповидноклеточной анемии, болезни Ходжкена, ВИЧ-инфекции, миеломы, сахарного диабета, состояний после спленэктомии) или алкоголизма.
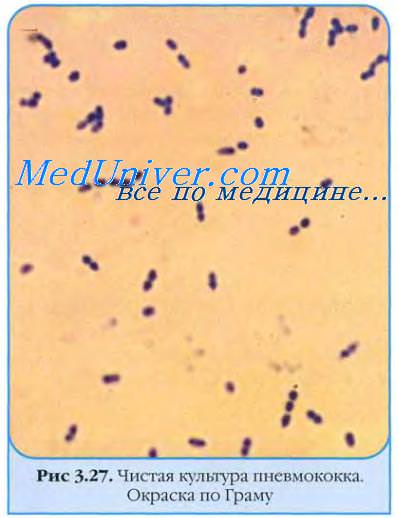
Морфология пневмококка. Культуральные свойства пневмококка
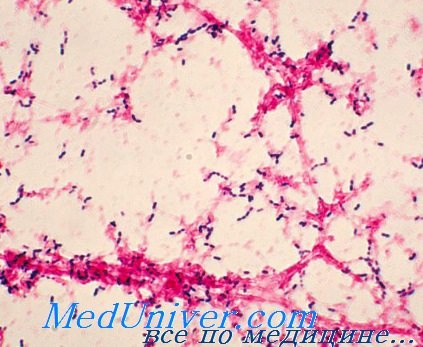
Пневмококки представлены овальными или ланцетовидными кокками диаметром около 1 мкм. В мазках из клинического материала пневмококки располагаются парами, каждая пара окружена толстой капсулой (рис. 12-10).
Образование капсул пневмококками стимулирует внесение в среду крови, сыворотки или асцитической жидкости. На агаре пневмококки образуют нежные полупрозрачные, чётко очерченные колонии диаметром около 1 мм; иногда они могут быть плоскими с углублением в центре. Подобно прочим стрептококкам, колонии никогда не сливаются между собой. На КА колонии окружает зона а-гемолиза в виде зеленоватой обесцвеченной зоны.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
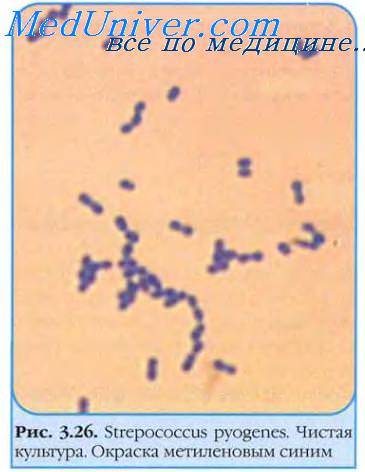
Стрептококки группы А. Streptococcus pyogenes. Пиогенные стрептококки. Инфекции вызываемые стрептококками. Эпидемиология стрептококков. Патогенез поражений стрептококками.
Эпидемиология стрептококков
Стрептококки группы А обнаруживают повсеместно. Они часто колонизируют кожные покровы и слизистые оболочки человека, а в холодный сезон частота носительства в носоглотке у школьников может достигать 25%. Резервуаром служит больной человек или носитель; основные пути передачи — контактный (с заносом в рот грязными руками) и воздушно-капельный, а также через инфицированные пищевые продукты, хранящиеся при комнатной температуре (например, молоко).

Инфекции вызываемые стрептококками
Патогенез поражений стрептококками
Первый этап инфекционного процесса — адгезия микроорганизма к эпителию слизистых оболочек. Основные адгезины — липотейхоевые кислоты, покрывающие поверхностные фимбрии. Не менее важную роль в прикреплении к субстратам играют гиалуронидаза, стрептокиназа и стрептодорназа.
Белок М стрептококков [от англ. mucoid, слизистый, так как колонии штаммов-продуцентов имеют слизистую консистенцию] по структуре напоминает фимбрии грамотрицательных бактерий. Белок М— основной фактор вирулентности и типоспецифтеский Аг. AT к нему обеспечивают длительную невосприимчивость к повторному заражению, однако выделяют более 80 сероваров белка М, что значительно снижает эффективность гуморальных защитных реакций. Белок М ингиби-рует фагоцитарные реакции, непосредственно действуя на фагоциты либо маскируя рецепторы для компонентов комплемента и опсонинов, адсорбируя на своей поверхности фибриноген, фибрин и продукты его деградации. Белок также проявляет свойства суперантигена, вызывая поликлональную активацию лимфоцитов и образование AT с низким аффинитетом. Подобные свойства играют существекную роль в нарушении толерантности к тканевым изоантигенам и развитии аутоиммунной патологии.
Капсула стрептококков — второй по значимости фактор вирулентности. Она защищает бактерии от антимикробного потенциала фагоцитов и облегчает адгезию к эпителию. Капсула образована гиалуроновой кислотой, аналогичной входящей в состав соединительной ткани. Соответственно капсула проявляет минимальную иммуногенную активность и не распознаётся как чужеродный агент. Интерес представляет способность бактерий самостоятельно разрушать капсулу при инвазии в ткани за счёт синтеза гиалуронидазы. Роль гиалуронидазы в патогенезе поражений изучена плохо: с одной стороны, она участвует в разрушении соединительнотканной стро-мы, с другой — имеет сходство со многими аутоантигенами и, возможно, участвует в запуске аутоиммунных реакций.
С5а-пептидаза стрептококков — третий фактор патогенности, подавляющий активность фагоцитов. Фермент расщепляет и инактивирует С5а компонент комплемента, выступающий мощным хемо-аттрактантом.
Стрептолизин О стрептококков[от англ. oxygen sensitive, чувствительный к кислороду] проявляет свойства гемолизина, разрушая эритроциты в анаэробных условиях. Проявляет иммуногенные свойства, титры AT к нему имеют прогностическое значение. Стрептолизин S [от англ. stable, устойчивый] резистентен к кислороду, не несёт антигенной нагрузки и вызывает поверхностный гемолиз на кровяных средах. Оба фермента разрушают не только эритроциты, но и другие клетки; например, стрептолизин О вызывает повреждение кардиомиоцитов, а стрептолизин S — фагоцитов, поглотивших бактерии.
Эритрогенные (пирогенные) токсины стрептококков весьма схожи с токсинами стафилококков. Имму-нологически их разделяют на три типа (А, В и С); способность к образованию токсинов детерминирована заражением бактериальной клетки умеренным фагом, несущим ген токсинообразо-вания. Эритрогенные токсины проявляют свойства суперантигенов: оказывают митогенное действие на Т-клетки, а также стимулируют секрецию макрофагами ИЛ-1 и ФНО.
Кардиогепатический токсин стрептококков синтезируют некоторые штаммы стрептококков группы А. Он вызывает поражения миокарда и диафрагмы, а также образование гигантоклеточных гранулём в печени.
Прочие экзоферменты стрептококков. Стрептокиназа (фибринолизин) активирует плазминоген, что приводит к образованию плазмина и растворению фибриновых волокон (фермент не проявляет прямой фибринолитической активности). Гиалуронидаза облегчает перемещение бактерий по соединительной ткани. Роль ДНКазы (стрептодорназа) и НАДаз изучена плохо, но выявление AT к стрептодорназе В используют в диагностике различных осложнений, вызванных стрептококками группы А. Медицинское применение нашла очищенная смесь стрептокиназы, стрепто-дорназы и других протеолитических ферментов стрептококков (стрсптокиназа-стрептодорназа), используемая для рассасывания тромбов, фибринозных и гнойных экссудатов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Новость
Структурная формула нового пептидного антибиотика.
Автор
Редакторы
- Антибиотики
- Биомолекулы
- Биотехнологии
- Здравоохранение
- Микробиология
- Фармакология
Немецкие ученые обнаружили новое оружие для борьбы с больничным монстром — мультирезистентным золотистым стафилококком. Долгие годы оно скрывалось не в вечной мерзлоте или Марианской впадине, а прямо под нашим носом. Вернее — в нём.
В последние годы во всем мире увеличилось количество инфекционных заболеваний, вызванных устойчивыми к антибиотикам бактериями. Организмы с множественной лекарственной резистентностью (multidrug-resistant organisms, MDRO), такие как метициллин-резистентный золотистый стафилококк, нечувствительные к ванкомицину энтерококки или резистентные к цефалоспоринам третьего поколения грамотрицательные бактерии, в ближайшие десятилетия могут стать более частыми причинами смерти, чем рак [1].
Несколько лет назад удалось обнаружить, что представители человеческой микробиоты способны производить бактериоцины, поражающие близкородственных бактерий [2]. Например, в 2014 году из человеческого комменсала Lactobacillus gasseri выделили и описали новый синтезируемый рибосомами тиопептидный антибиотик — лактоциллин [3].
Семейные разборки
Немецкий исследователь Александр Ципперер со своими сотрудниками в июле 2016 года сообщил о том, что обнаружил в человеческом носу бактерию Staphylococcus lugdunensis IVK28, которая подавляет рост метициллин-резистентного золотистого стафилококка (methicillin-resistant Staphylococcus aureus, MRSA) [1].
Золотистый стафилококк
Стафилококки относятся к типичным бактериям-комменсалам, колонизирующим кожу и поверхности слизистых оболочек. Staphylococcus aureus — шаровидные грамположительные бактерии, вырабатывающие каротиноидный пигмент, который придает их клеткам золотистый цвет (рис. 1). Эти микроорганизмы чрезвычайно устойчивы к внешним воздействиям и выживают в воздухе, пыли, почве, продуктах питания, на оборудовании пищевых производств и предметах быта [6], [7].

Рисунок 1. Staphylococcus aureus и лейкоциты.

Рисунок 2. Метициллин-резистентные золотистые стафилококки.
Staphylococcus aureus — бактерия условно-патогенная, проявляющая свои патологические свойства только в благоприятных условиях, а создает их, как правило, ослабление иммунитета носителя. Активная жизнедеятельность стафилококка может привести к разнообразным заболеваниям [5], [7], [8]:
- кожи (прыщи, фурункулы, синдром ошпаренной кожи);
- органов дыхания (плеврит, пневмония);
- костной и соединительной тканей (артрит, остеомиелит);
- нервной системы и органов чувств (отит, менингит);
- сердечно-сосудистой системы (эндокардит, флебит, стафилококковая бактериемия).
Факторы патогенности S. aureus — это микрокапсула, компоненты клеточной стенки, ферменты агрессии и токсины. Микрокапсулы защищают клетки бактерий от фагоцитоза, способствуют их адгезии и распространению по организму хозяина. Составляющие клеточной стенки (например пептидогликан, тейхоевые кислоты и белок А) вызывают развитие воспаления, обездвиживают фагоциты и нейтрализуют иммуноглобулины. Коагулаза, главный фермент агрессии, вызывает свертывание плазмы крови [7], [9].
Наиболее опасны метициллин-резистентные стафилококки (methicillin-resistant S. aureus, MRSA) (рис. 2). Метициллин — это модифицированный пенициллин, с помощью которого еще недавно успешно боролись со стафилококковой инфекцией. MRSA устойчивы не только к метициллину, но и к другим антибиотикам пенициллиновой группы (диклоксациллину, оксациллину, нафциллину и др.), а также к цефалоспоринам. В последнее время выявлены штаммы и с более широким спектром устойчивости: ванкомицин-резистентные (VRSA) и гликопептид-резистентные (GISA) [6], [9], [10].
Штамм S. lugdunensis IVK28 эффективно боролся со своим вредоносным родственником лишь в условиях недостатка железа и только на твердых агаризованных средах (рис. 3, слева). Механизм противостояния был неясен, а потому Ципперер провел транспозонный мутагенез клеток выделенного штамма — чтобы выявить ген, ответственный за синтез смертельного для S. aureus вещества.

В итоге удалось получить мутанта IVK28, который не мог подавлять рост MRSA. Анализ места встройки транспозона показал, что тот нарушил структуру гена предполагаемой нерибосомной пептидсинтетазы (НРПС). Оказалось, что этот ген вместе с другими последовательностями, связанными с биосинтезом антибиотиков, входит в состав оперона размером 30 т.п.н. Это указывало на то, что предполагаемая молекула ингибитора может быть комплексом нерибосомных пептидов.
Оперон методом ПЦР обнаружили во всех культурах S. lugdunensis, а значит, он характерен для всего вида, а не только для штамма IVK28. Однако GC-состав оперона (26,9%) отличался от GC-состава остального генома S. lugdunensis (33,8%), что свидетельствовало о возможном заимствовании этого полезного генетического кластера у других видов бактерий — путем горизонтального переноса .
Оперон состоит из генов lugA, B, C и D, кодирующих пептидсинтетазные белки (см. врезку ниже), а также из других генов, чьи продукты необходимы для синтеза и транспорта нерибосомного пептида.
Чтобы окончательно вменить оперону участие в антибактериальной деятельности S. lugdunensis, наименьший ген (lugD) удалили. Мутант ΔlugD, как и ожидалось, не мог подавлять рост золотистого стафилококка, но когда в него ввели плазмиду с работающим геном lugD, агрессивный фенотип восстановился (рис. 3, в центре и справа).
Секретное оружие
Выделенный Ципперером продукт lug-оперона оказался нерибосомным циклическим пептидом, состоящим из пяти аминокислот (двух D-валинов, L-валина, D-лейцина и L-триптофана) и тиазолидинового гетероцикла (рис. 4). Назвали антибиотик лугдунином.

Химическим синтезом удалось получить продукт с идентичными природному лугдунину химическими свойствами и антибактериальным эффектом. Ученые предположили, что этот антибиотик ингибирует синтез бактериальных биополимеров — белков, ДНК и пептидогликанов [5].
Нерибосомные пептиды
Этот класс пептидов синтезируется в клетках низших грибов и бактерий без участия рибосом. Нерибосомные пептиды (НРП) также встречаются и у высших организмов, которые имеют бактерий-комменсалов [12].
НРП подразделяются на несколько функциональных групп [13]:
- антибиотики (ванкомицин);
- предшественники антибиотиков (ACV-трипептид — предшественник пенициллина и цефалоспорина);
- иммуносупрессоры (циклоспорин);
- противоопухолевые пептиды (блеомицин);
- сидерофоры (пиовердин);
- токсины (HC-токсин);
- сурфактанты (сурфактин).
Строение
Синтез
Каждый модуль состоит как минимум из трех доменов:
- конденсирующего (принимающего пептидную цепь из предыдущего модуля);
- аденилирующего (выбирающего нужную аминокислоту);
- пептидильного (образующего пептидную связь).
Нередко модули включают и другие домены, в том числе эпимеризующий, который преобразует L-аминокислоты в D-формы [14].
По аналогии с триплетным рибосомным кодом для синтеза белка существует и нерибосомный, код НРПС, определяемый 10 остатками аминокислот в субстрат-связывающем кармане аденилирующего домена. От комбинации этих остатков зависит то, какая аминокислота будет встроена в пептид конкретным модулем НРПС. Зная этот код, можно предсказывать субстратную специфичность аденилирующих доменов и даже произвольно изменять ее посредством замены аминокислот в домене [14].
В экспериментах немецких ученых лугдунин действовал не только на метициллин-резистентных стафилококков, но и на гликопротеин-резистентных, и даже на других грамположительных бактерий типа листерии и ванкомицин-резистентного энтерококка (табл. 1). Минимальная ингибирующая концентрация (МИК) нового бактериоцина — 1,5–12 мкг × мл −1 , что говорит о высокой активности вещества. При этом такие концентрации никак не влияли на человеческую сыворотку, не вызывали лизис нейтрофилов или эритроцитов и не ингибировали метаболическую активность моноцитов. Бактериальные же клетки под действием лугдунина в концентрации даже ниже МИК прекращали синтезировать ДНК, РНК, белки и компоненты клеточной стенки. В этом отношении лугдунин напоминает даптомицин, дающий такой же эффект, но способ действия которого пока не изучен. Не было отмечено возникновения резистентности клеток S. aureus к лугдунину даже после их месячного выращивания на малых концентрациях.
| Виды и штаммы | Резистентность | МИК лугдунина (мкг × мл −1 ) |
|---|---|---|
| Staphylococcus aureus USA300 (LAC) | MRSA | 1,5 |
| + 50% человеческой сыворотки крови | 1,5 | |
| Staphylococcus aureus USA300 (NRS384) | MRSA | 1,5 |
| Staphylococcus aureus Mu50 | GISA | 3 |
| Staphylococcus aureus SA113 | 3 | |
| Staphylococcus aureus RN4220 | 3 | |
| Enterococcus faecium BK463 | VRE | 3 |
| Enterococcus faecalis VRE366 | VRE | 12 |
| Listeria monocytogenes ATCC19118 | 6 | |
| Streptococcus pneumoniae ATCC49619 | 1,5 | |
| Bacillus subtilis 168 (trpC2) | 4 | |
| Pseudomonas aeruginosa PAO1 | >50 | |
| Escherichia coli DH5α | >50 | |
| Условные обозначения: MRSA — метициллин-резистентные S. aureus; GISA — устойчивые к гликопротеинам S. aureus; VRE — ванкомицин-резистентные Enterococcus. Таблица из [1]. | ||
Испытания в боевых условиях
Как и полагается, способность лугдунина лечить стафилококковые инфекции продемонстрировали in vivo на мышиной модели (рис. 5). У шести мышей сбрили шерсть на спине и, повредив кожу многократным приклеиванием/отклеиванием пластыря, нанесли на это место золотистого стафилококка. Затем кожу обработали мазью, содержащей 1,5 мкг лугдунина, и спустя шесть часов оценили результат. Обработка новым антибиотиком сильно сокращала или даже полностью уничтожала популяцию S. aureus. Причем не только на поверхности кожи, но и в более глубоких ее слоях.

Рисунок 5. Общая схема подхода к идентификации природного антибиотика. Из бактериальных популяций человеческого тела отбирают представителей, которые не могут сосуществовать с интересующими патогенными бактериями. Этих возможных конкурентов тестируют по отдельности на средах с инфекционным агентом. Из культуры, успешно подавляющей рост патогенов, выделяют антибиотик, действие которого проверяют на животных моделях.
[5], рисунок модифицирован и адаптирован
Чтобы понять, может ли S. lugdunensis помешать колонизации носовой полости позвоночных животных золотистым стафилококком в естественных условиях, ученые провели следующий эксперимент. В носы хлопковых хомяков ввели два вида смешанных культур (S. aureus + S. lugdunensis IVK28 и S. aureus + S. lugdunensis IVK28ΔlugD) и каждую по отдельности. В контрольных случаях, когда вводили по одному штамму, все три культуры стабильно колонизировали носовую полость. Однако при введении смеси S. aureus + S. lugdunensis IVK28 количество золотистого стафилококка через 5 дней значительно уменьшилось по сравнению со смесью S. aureus + S. lugdunensis IVK28ΔlugD. Этот эксперимент показал, что продукция лугдунина позволяет штамму IVK28 эффективно конкурировать с золотистым стафилококком in vivo.
Оставалось разобраться, предотвращает ли присутствие S. lugdunensis в носу человека колонизацию бактериями S. aureus. Ципперер и его коллеги исследовали мазки из носовых ходов 187 госпитализированных больных. Из них у 60 человек (32,1%) обнаружили золотистого стафилококка и у 17 человек (9,1%) — S. lugdunensis. И только у одного пациента с S. lugdunensis в носу обитал S. aureus. У всех выделенных штаммов S. lugdunensis ПЦР-анализ продемонстрировал наличие lug-оперона, а все обнаруженные штаммы S. aureus оказались восприимчивы к лугдунину.
Перспективы
Лугдунин оказался первым обнаруженным бактериоцином нового класса — макроциклических тиазолидиновых пептидных антибиотиков. Все проверенные штаммы S. aureus (как природные, так и лабораторные) не смогли выработать резистентности к нему. Это дает надежду на то, что лугдунин в будущем станет коммерческим препаратом для борьбы с золотистым стафилококком.
И наконец, сам факт обнаружения нового антибиотика у представителя человеческой микробиоты должен послужить стимулом для активизации поиска других продуцентов бактериоцинов в составе именно таких сообществ. В дальнейшем это поможет медикам успешнее сдерживать наступление мультирезистентных патогенов.

Пневмококк (лат. Streptococcus pneumoniae) — вид грамположительных факультативно анаэробных α-гемолитических бактерий. Клетки Streptococcus pneumoniae, как и других стрептококков, имеют сферическую форму. Чаще всего располагаются парами, но в жидких средах образует цепочки.
Streptococcus pneumoniae является наиболее частым (в 20–60%) возбудителем опасного заболевания — внебольничной пневмонии, смертной от которой составляет 5%. Кроме того, Streptococcus pneumoniae может вызывать такие заболевания человека, как средний отит, острый негнойный синусит, ринит, ларингит, бронхит, менингит, сепсис, остеомилит, септический артрит, эндокардит, перитонит и другие.
Streptococcus pneumoniae является вторым (после Haemophilus influenzae) по распространённости и важности пневмотропным микроорганизмом в микробном спектре при хронических бронхолегочных заболеваниях у детей в периоде обострения.
Пневмония
Пневмония является одной из форм острой респираторной инфекции, воздействующей на легкие. При пневмонии альвеолы лёгких заполняются гноем и жидкостью, что делает дыхание болезненным и ограничивает поступление кислорода.

Пневмония является важнейшей отдельно взятой инфекционной причиной смертности детей во всем мире. В 2013 году от пневмонии умерли 935 тысяч детей в возрасте до 5 лет. Она является причиной 15% всех случаев смерти детей в возрасте до 5 лет во всем мире.
Существует несколько путей распространения пневмонии. Бактерии, которые обычно присутствуют в носе или горле ребенка, могут инфицировать легкие при их вдыхании. Они могут также распространяться воздушно-капельным путем при кашле или чихании. Кроме того, пневмония может передаваться через кровь, особенно во время родов или сразу после них.
У детей в возрасте до 5 лет с симптомами кашля и/или затрудненного дыхания, сопровождающимися или не сопровождающимися высокой температурой, диагноз пневмонии ставится при наличии учащенного дыхания или втяжения нижней части грудной клетки, если грудная клетка втягивается или отводится назад при вдохе (у здорового человека при вдохе грудная клетки расширяется).
Пневмонию, вызванную бактериями, можно излечить антибиотиками. Предпочтительным антибиотиком является амоксициллин в диспергируемых таблетках (ВОЗ. Инф. бюлл. №131).
Ухудшение эпидемиологической ситуации в Москве по внебольничным пневмониям пневмококковой этиологии в 2016 г.
- за 6 месяцев 2016 года по сравнению с аналогичным периодом отмечен рост заболеваемости внебольничными пневмониями на 27 %, в том числе пневмококковой этиологии — в 1,9 раза
- показатели смертности москвичей от внебольничной пневмонии возросли в 1,5 раза, летальности — в 2 раза
- наибольшее количество заболевших приходится на москвичей старше 40 лет, страдающих хроническими заболеваниями
- растёт удельный вес госпитализированных из числа заболевших внебольничной пневмонией:
- в 2014 году — 70,9%
- в 2015 году — 75,8%
- за 6 месяцев 2016 года — 77,0%
- 20-25% имеют хроническую обструктивную болезнь лёгких
- до 15,8% имеют ишемическую болезнь сердца
- 14,3% — хроническую сердечно-сосудистую недостаточность
- 9,6% — сахарный диабет
Streptococcus pneumoniae в систематике бактерий
По современным представлениям вид Streptococcus pneumoniae относится к роду стрептококков, (Streptococcus), который входит в семейство Streptococcaceae, порядок Lactobacillales, класс Bacilli, тип Firmicutes, Terrabacteria group, царство Бактерии.
Антибиотики, активные в отношении Streptococcus pneumoniae. Вакцины
К ципрофлоксацину Streptococcus pneumoniae чувствителен умеренно.
Streptococcus pneumoniae в МКБ-10
![]()
Читайте также:


