Микроскопический метод диагностики инфекционных заболеваний микробиология
Обновлено: 24.04.2024
Инфекции вызывают, в основном, следующие виды микроорганизмов: бактерии, вирусы, грибы, простейшие. Их обнаружение — достоверный признак инфекционного процесса.
Лаборатория располагает арсеналом методов, однако только 5 из них наиболее широко распространены:
Культуральный метод (метод посева)
Выявляет чистую культуру возбудителя. Метод сводится к тому, что полученный материал (мазок со слизистой оболочки, кровь, гной, кал и т.д) высевается на питательные среды. Среды могут содержать различные компоненты. Но суть сводится к следующему: микроорганизмы должны дать рост и колонии. Если есть рост патогенных микроорганизмов, то определяется их чувствительность к лекарствам: антибиотикам и бактериофагам.
Серологический метод (метод антител к возбудителю)
Тоже позволяет поставить диагноз. Метод основан на обнаружении в крови антигенов возбудителя или антител — специальных белков, которые образуются в организме в ответ на присутствие и размножение болезнетворных микроорганизмов. Антитела образуются постепенно, поэтому в крови их можно обнаружить только к концу первой недели инфицирования. Это главный недостаток метода.
Молекулярно-биологический метод (метод полимеразной цепной реакции (ПЦР), метод амплификации РНК (NASBA))
Определяет генетический материал возбудителя — ДНК или РНК в образцах (соскоб со слизистой, кровь, моча, кал и т.д). Чтобы уловить малые концентрации ДНК или РНК, необходимо увеличить количество копий. Для этого исследуемый образец помещают в прибор — амплификатор, который позволяет увеличить число копий ДНК в геометрической прогрессии. Для этого метода диагностики крайне важен правильный забор биоматериала.
Микроскопический метод (исследование под микроскопом)
Подразумевает приготовление препаратов на стекле. Материал: кровь, отделяемое слизистых оболочек и т.д. Стекла могут быть окрашенными или неокрашенными, в зависимости от типа инфекции. Врач исследует препарат под микроскопом и выдает результат на основании визуальной оценки: размер, форма, отношение к красителям и т.д.
Метод газовой хроматографии (ГХ-МС)
Выявляет возбудителей по продуктам их жизнедеятельности. Материал: кровь, моча, кал, отделяемое ран, слизистых оболочек.
Микроскопический метод диагностикиинфекционных заболеваний включает приготовление мазка, его окраску с использованием простых и сложных методов окраски, проведение иммерсионной микроскопии для изучения морфологических (формы и расположения) и тинкториальных свойств (отношение к красителю) с целью идентификации до рода (Staphylococcus, Streptococcus) или семейства (Епterobactericeae).
Первым этапом микроскопического метода является приготовление мазка (рис. 6). Мазок выполняют на чистом, обезжиренном предметном стекле, по поверхности которого капля воды должна растекаться равномерно. Для очистки стекла необходимо натереть его кусочком мыла и удалить мыло с помощью марлевой салфетки или протереть спиртом. Для приготовления мазка на обратной стороне предметного стекла маркируют зону и наносят небольшую каплю воды или изотонического раствора хлорида натрия в которой распределяют исследуемый материал. Если мазок готовят из жидкого исследуемого материала или микроорганизмов, культивированных в жидкой питательной среде, берут каплю жидкости петлей и равномерно распределяют в обозначенной зоне. Препарат высушивают при комнатной температуре на воздухе. Хорошо приготовленный тонкий мазок высыхает равномерно и быстро. Если же высушивание препарата замедлено, то препарат подогревают, держа стекло мазком вверх, в потоке теплого воздуха высоко над пламенем горелки. Это нужно производить крайне осторожно, не допуская перегревания мазка, так как при этом может произойти слишком быстрое и грубое свертывание белков в протоплазме микробов, что нарушит их структуру. Если препарат высушен не полностью, то при фиксации он окажется также испорченным. Фиксация препарата проводится с целью: 1) убить микробов и сделать безопасным дальнейшее обращение с ними; 2) прикрепить (фиксировать) мазок к стеклу, чтобы он не смывался при дальнейших манипуляциях; 3) сделать микробов более восприимчивыми к окраске, там как убитые микробные клетки окрашиваются лучше, чем живые.
Способы фиксации.Существует два основных способа фиксации: физическая (термическая) и химическая (использование фиксаторов). В практической бактериологии обычно применяют фиксацию в пламени горелки (фиксация жаром) — метод грубый, но сохраняющий морфологию и отношение к красителям у бактерий. Для этого предметное стекло в положении мазком вверх 3 раза (в течение 3-5 сек) проводят через наиболее горячую часть пламени горелки. В ряде случаев используют жидкие фиксирующие растворы (этиловый и метиловый спирт, ацетон, формалин и др.), которые предотвращают ферментативный аутолиз бактерий и стабилизируют макромолекулы путем их химического сшивания, оказывая более щадящее действие. Для проведения химической фиксации препараты погружают в раствор фиксирующей жидкости на 5-20 минут. Выбор способа фиксации зависит от окрашиваемого препарата (жидкие фиксаторы используются для мазков крови, гноя и др.) и метода окраски.
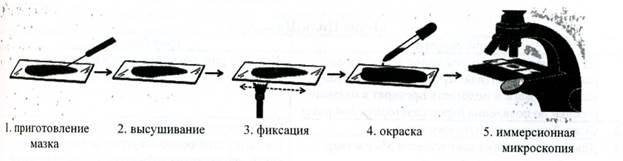
Рис. 6. Схема проведения микроскопического метода
7. Простые и сложные методы окраски
Простой метод окраски. Является одноэтапным и заключается в окраске микропрепарата одним красителем. Используют основные анилиновые красители, такие как, фуксин, генцианвиолет, метиленовый синий в виде водных растворов или пропитанных красителем фильтровальных бумажек, которые помещают на мазок и смачивают водой. Продолжительность окраски составляет 1-5 минут, после чего микропрепарат промывают водой, высушивают и микроскопируют. В препаратах, окрашенных простым методом, можно получить представление о форме, расположении и размерах микробных клеток.
Сложные методы окраски. Сложные (дифференцирующие) методы окраски (по Граму, Цилю-Нильсену и др.) включают последовательное использование нескольких красителей и дополнительных способов обработки препаратов. Эти методы позволяют дифференцировать бактерии в зависимости от строения их структур, чаще всего поверхностных. Например, метод окраски по Граму позволяет дифференцировать бактерии по строению их клеточной стенки: грамположительные (фиолетовые) с толстой и грамотрицательные (красные) бактерии с тонкой клеточной стенкой.
Существуют специальные сложные методы окраски, которые используют для выявления структурных компонентов бактериальной клетки: капсул, цитоплазматических включений, спор, жгутиков.
Люминесцентная (или флюоресцентная) микроскопия.Основана на явлении фотолюминесценции.
Люминесценция — свечение веществ, возникающее после воздействия на них каких-либо источников энергии: световых, электронных лучей, ионизирующего излучения. Фотолюминесценция — люминесценция объекта под влиянием света. Если освещать люминесцирующий объект синим светом, то он испускает лучи красного, оранжевого, желтого или зеленого цвета. В результате возникает цветное изображение объекта.
Темнопольная микроскопия.Микроскопия в темном поле зрения основана на явлении дифракции света при сильном боковом освещении взвешенных в жидкости мельчайших частиц (эффект Тиндаля). Эффект достигается с помощью параболоид- или кардиоидконденсора, которые заменяют обычный конденсор в биологическом микроскопе .
Фазово-контрастная микроскопия. Фазово-контрастное приспособление дает возможность увидеть в микроскоп прозрачные объекты. Они приобретают высокую контрастность изображения, которая может быть позитивной или негативной. Позитивным фазовым контрастом называют темное изображение объекта в светлом поле зрения, негативным — светлое изображение объекта на темном фоне.
Для фазово-контрастной микроскопии используют обычный микроскоп и дополнительное фазово-контрастное устройство, а также специальные осветители.
Электронная микроскопия.Позволяет наблюдать объекты, размеры которых лежат за пределами разрешающей способности светового микроскопа (0,2 мкм). Электронный микроскоп применяется для изучения вирусов, тонкого строения различных микроорганизмов, макромолекулярных структур и других субмикроскопических объектов.
Микроскопический метод широко применяют в диагностике инфекционных болезней бактериальной этиологии, паразитарных и (реже) вирусных заболеваний.
В повседневной практике бактериологической лаборатории микроскопическое исследование, как правило, используют для ускоренной ориентировочной диагностики. Основные задачи микроскопии: выявление возбудителя в клиническом материале, ориентировочная идентификация на основе определения характерных морфологических и тинкториальных признаков микроорганизмов, а также изучение окрашенных мазков из колоний чистых культур. При некоторых инфекционных болезнях, для возбудителей которых характерна специфичность морфологии (протозойные болезни, гельминтозы, грибковые заболевания, спирохетозы), микроскопическое исследование — основной или один из основных методов диагностики.
Материалом для микроскопического исследования могут служить кровь, костный мозг, СМЖ, пунктаты лимфатических узлов, фекалии, дуоденальное содержимое и жёлчь, моча, мокрота, отделяемое мочеполовых путей, биоптаты тканей, мазки со слизистых оболочек (ротовой полости, нёбных миндалин, носа, влагалища и др.).
Методы окраски микробов и их отдельных структур.
Методы окраски. Окраску мазка производят простыми или сложными методами. Простые заключаются в окраске препарата одним красителем; сложные методы (по Граму, Цилю — Нильсену и др.) включают последовательное использование нескольких красителей и имеют дифференциально-диагностическое значение. Отношение микроорганизмов к красителям расценивают как тинкториальные свойства. Существуют специальные методы окраски, которые используют для выявления жгутиков, клеточной стенки, нуклеоида и разных цитоплазматических включений.
При простых методах мазок окрашивают каким-либо одним красителем, используя красители анилинового ряда (основные или кислые). Если красящий ион (хромофор) — катион, то краситель обладает основными свойствами, если хромофор - анион, то краситель имеет кислые свойства. Кислые красители — эритрозин, кислый фуксин, эозин. Основные красители — генциановый фиолетовый, кристаллический фиолетовый, метиленовый синий, основной фуксин. Преимущественно для окраски микроорганизмов используют основные красители, которые более интенсивно связываются кислыми компонентами клетки. Из сухих красителей, продающихся в виде порошков, готовят насыщенные спиртовые растворы, а из них — водно-спиртовые, которые и служат для окрашивания микробных клеток. Микроорганизмы окрашивают, наливая краситель на поверхность мазка на определенное время. Окраску основным фуксином ведут в течение 2 мин, метиленовым синим — 5—7 мин. Затем мазок промывают водой до тех пор, пока стекающие струи воды не станут бесцветными, высушивают осторожным промоканием фильтровальной бумагой и микроскопируют в иммерсионной системе. Если мазок правильно окрашен и промыт, то поле зрения совершенно прозрачно, а клетки интенсивно окрашены.

Сложные методы окраски применяют для изучения структуры клетки и дифференциации микроорганизмов. Окрашенные мазки микроскопируют в иммерсионной системе. Последовательно нанести на препарат определенные красители, различающиеся по химическому составу и цвету, протравы, спирты, кислоту и др.
Микроскопический метод диагностики инфекционных заболеваний включает приготовление мазка, его окраску с использованием простых и сложных методов окраски, проведение иммерсионной микроскопии для изучения морфологических (формы и расположения) и тинкториальных свойств (отношение к красителю) с целью идентификации до рода (Staphylococcus, Streptococcus) или семейства (Епterobactericeae).
Первым этапом микроскопического метода является приготовление мазка (рис. 6). Мазок выполняют на чистом, обезжиренном предметном стекле, по поверхности которого капля воды должна растекаться равномерно. Для очистки стекла необходимо натереть его кусочком мыла и удалить мыло с помощью марлевой салфетки или протереть спиртом. Для приготовления мазка на обратной стороне предметного стекла маркируют зону и наносят небольшую каплю воды или изотонического раствора хлорида натрия в которой распределяют исследуемый материал. Если мазок готовят из жидкого исследуемого материала или микроорганизмов, культивированных в жидкой питательной среде, берут каплю жидкости петлей и равномерно распределяют в обозначенной зоне. Препарат высушивают при комнатной температуре на воздухе. Хорошо приготовленный тонкий мазок высыхает равномерно и быстро. Если же высушивание препарата замедлено, то препарат подогревают, держа стекло мазком вверх, в потоке теплого воздуха высоко над пламенем горелки. Это нужно производить крайне осторожно, не допуская перегревания мазка, так как при этом может произойти слишком быстрое и грубое свертывание белков в протоплазме микробов, что нарушит их структуру. Если препарат высушен не полностью, то при фиксации он окажется также испорченным. Фиксация препарата проводится с целью: 1) убить микробов и сделать безопасным дальнейшее обращение с ними; 2) прикрепить (фиксировать) мазок к стеклу, чтобы он не смывался при дальнейших манипуляциях; 3) сделать микробов более восприимчивыми к окраске, там как убитые микробные клетки окрашиваются лучше, чем живые.
Способы фиксации. Существует два основных способа фиксации: физическая (термическая) и химическая (использование фиксаторов). В практической бактериологии обычно применяют фиксацию в пламени горелки (фиксация жаром) — метод грубый, но сохраняющий морфологию и отношение к красителям у бактерий. Для этого предметное стекло в положении мазком вверх 3 раза (в течение 3-5 сек) проводят через наиболее горячую часть пламени горелки. В ряде случаев используют жидкие фиксирующие растворы (этиловый и метиловый спирт, ацетон, формалин и др.), которые предотвращают ферментативный аутолиз бактерий и стабилизируют макромолекулы путем их химического сшивания, оказывая более щадящее действие. Для проведения химической фиксации препараты погружают в раствор фиксирующей жидкости на 5-20 минут. Выбор способа фиксации зависит от окрашиваемого препарата (жидкие фиксаторы используются для мазков крови, гноя и др.) и метода окраски.
Диагностика инфекционных заболеваний является одной из самых сложных проблем в клинической медицине. Лабораторные методы исследования при ряде нозологических форм играют ведущую, а в целом ряде клинических ситуаций решающую роль не только в диагностике, но и в определении конечного исхода заболевания.
Диагностика инфекционных заболеваний почти всегда предусматривает использование комплекса лабораторных методов.
- бактериологические;
- серологические;
- метод полимеразной цепной реакции (ПЦР) для обнаружения ДНК или РНК возбудителя инфекционного заболевания в исследуемом материале.
У одних пациентов для диагностики этиологии инфекционно-воспалительного процесса достаточно провести бактериологическое исследование, в других клинических ситуациях решающее значение имеют данные серологических исследований, в третьих, предоставить полезную информацию может только метод ПЦР. Однако наиболее часто в клинической практике врачу-клиницисту необходимо использовать данные различных методов лабораторных исследований.
Бактериологические методы исследования
Бактериологические исследования наиболее часто проводят при подозрении на гнойно-воспалительные заболевания (составляют 40-60% в структуре хирургических заболеваний) с целью их диагностики, изучения этиологической структуры, определения чувствительности возбудителей к антибактериальным препаратам. Результаты бактериологических анализов способствуют выбору наиболее эффективного препарата для антибактериальной терапии, своевременному проведению мероприятий для профилактики внутрибольничных инфекций.
Возбудителями гнойно-воспалительных заболеваний являются истинно-патогенные бактерии, но наиболее часто условно-патогенные микроорганизмы, входящие в состав естественной микрофлоры человека или попадающие в организм извне. Истинно-патогенные бактерии в большинстве случаев способствуют развитию инфекционного заболевания у любого здорового человека. Условно-патогенные микроорганизмы вызывают заболевания преимущественно у людей с нарушенным иммунитетом.
Бактериологические исследования при заболеваниях, вызываемых условно-патогенными микроорганизмами, направлены на выделение всех микроорганизмов, находящихся в патологическом материале, что существенно отличает их от аналогичных исследований при заболеваниях, вызванных истинно патогенными микроорганизмами, когда проводится поиск определенного возбудителя.
Для получения адекватных результатов бактериологического исследования при гнойно-воспалительных заболеваниях особенно важно соблюдать ряд требований при взятии биоматериала для анализа, его транспортировки в лабораторию, проведения исследования и оценки его результатов.
- микроскопическое исследование мазка (бактериоскопия) из доставленного биоматериала;
- выращивание культуры микроорганизмов (культивирование);
- идентификацию бактерий;
- определение чувствительности к антимикробным препаратам и оценку результатов исследования.
Доставленный в бактериологическую лабораторию биоматериал первоначально подвергается микроскопическому исследованию.
Микроскопическое исследование мазка (бактериоскопия), окрашенного по Граму или другими красителями, проводят при исследовании мокроты, гноя, отделяемого из ран, слизистых оболочек (мазок из цервикального канала, зева, носа, глаза). Результаты микроскопии позволяют ориентировочно судить о характере микрофлоры, ее количественном содержании и соотношении различных видов микроорганизмов в биологическом материале, а также дают предварительную информации об обнаружении этиологически значимого инфекционного агента в данном биоматериале, что позволяет врачу сразу начать лечение (эмпирическое). Иногда микроскопия позволяет выявить микроорганизмы, плохо растущие на питательных средах. На основании данных микроскопии проводят выбор питательных сред для выращивания микробов, обнаруженных в мазке.
Культивирование микроорганизмов. Посев исследуемого биоматериала на питательные среды производят с целью выделения чистых культур микроорганизмов, установления их вида и определения чувствительности к антибактериальным препаратам. Для этих целей используют различные питательные среды, позволяющие выделить наибольшее количество видов микроорганизмов. Оптимальными являются питательные среды, содержащие кровь животного или человека, а также сахарный бульон, среды для анаэробов. Одновременно производят посев на дифференциально-диагностические и селективные (предназначенные для определенного вида микроорганизмов) среды. Посев осуществляют на стерильные чашки Петри, в которые предварительно заливают питательную среду для роста микроорганизмов.
Микроскопия мазков, окрашенных по Граму
1 - стрептококки; 2 - стафилококки; 3 - диплобактерии Фридленда; 4 - пневмококки
Колонии отсевают на плотные, жидкие, полужидкие питательные среды, оптимальные для культивирования определенного вида бактерий.
Выделенные чистые культуры микроорганизмов подвергают дальнейшему изучению в диагностических тестах, основанных на морфологических, ферментативных, биологических свойствах и антигенных особенностях, характеризующих бактерий соответствующего вида или варианта.
Определение чувствительности к антибактериальным препаратам. Чувствительность к антимикробным препаратам изучают у выделенных чистых культур микроорганизмов, имеющих этиологическое значение для данного заболевания. Поэтому в направлении на бактериологические анализы требуется указать диагноз заболевания у больного. Определение чувствительности бактерий к спектру антибиотиков помогает лечащему врачу правильно выбрать препарат для лечения больного.
Оценка результатов исследования. Принадлежность условно-патогенных микроорганизмов к естественной микрофлоре организма человека создает ряд трудностей при оценке их этиологической роли в развитии гнойно-воспалительных заболеваний. Условно-патогенные микроорганизмы могут представлять нормальную микрофлору исследуемых жидкостей и тканей или контаминировать их из окружающей среды. Поэтому для правильной оценки результатов бактериологических исследований необходимо знать состав естественной микрофлоры изучаемого образца. В тех случаях, когда исследуемый биоматериал в норме стерилен, как, например, спинномозговая жидкость, экссудаты, все выделенные из него микроорганизмы могут считаться возбудителями заболевания. В тех случаях, когда исследуемый материал имеет собственную микрофлору, как, например, отделяемое влагалища, кал, мокрота, нужно учитывать изменения ее качественного и количественного состава, появление несвойственных ему видов бактерий, количественную обсемененность биоматериала. Так, например, при бактериологическом исследовании мочи степень бактериурии (число бактерий в 1 мл мочи), равная и выше 10 5 , свидетельствует об инфекции мочевых путей. Более низкая степень бактериурии встречается у здоровых людей и является следствием загрязнения мочи естественной микрофлорой мочевых путей.
Установить этиологическую роль условно-патогенной микрофлоры помогают также нарастание количества и повторность выделения бактерий одного вида от больного в процессе заболевания.
Врач-клиницист должен знать, что положительный результат бактериологического исследования в отношении биологического материала, полученного из в норме стерильного очага (кровь, плевральная жидкость, спинномозговая жидкость, пунктат органа или ткани), всегда тревожный результат, требующий немедленных действий по оказанию медицинской помощи.
Серологические методы исследования
В основе всех серологических реакций лежит взаимодействие антигена и антитела. Серологические реакции используются в двух направлениях.
2. Установление родовой и видовой принадлежности микроба или вируса. В этом случае неизвестным компонентом реакции является антиген. Такое исследование требует постановки реакции с заведомо известными иммунными сыворотками.
Серологические исследования не обладают 100%-й чувствительностью и специфичностью в отношении диагностики инфекционных заболеваний, могут давать перекрестные реакции с антителами, направленными к антигенам других возбудителей. В связи с этим оценивать результаты серологических исследований необходимо с большой осторожностью и учетом клинической картины заболевания. Именно этим обусловлено использование для диагностики одной инфекции множества тестов, а также применение метода Western-blot для подтверждения результатов скрининговых методов.
В последние годы прогресс в области серологических исследований связан с разработкой тест-систем для определения авидности специфических антител к возбудителям различных инфекционных заболеваний.
Авидность - характеристика прочности связи специфических антител с соответствующими антигенами. В ходе иммунного ответа организма на проникновение инфекционного агента стимулированный клон лимфоцитов начинает вырабатывать сначала специфические IgM-антитела, а несколько позже и специфические IgG-антитела. IgG-антитела обладают поначалу низкой авидностью, то есть достаточно слабо связывают антиген.
Затем развитие иммунного процесса постепенно (это могут быть недели или месяцы) идет в сторону синтеза лимфоцитами высокоспецифичных (высокоавидных) IgG-антител, более прочно связывающихся с соответствующими антигенами. На основании этих закономерностей иммунного ответа организма в настоящее время разработаны тест-системы для определения авидности специфических IgG-антител при различных инфекционных заболеваниях.
Высокая авидность специфических IgG-антител позволяет исключить недавнее первичное инфицирование и тем самым с помощью серологических методов установить период инфицирования пациента. В клинической практике наиболее широкое распространение нашло определение авидности антител класса IgG при токсоплазмозе и цитомегаловирусной инфекции, что дает дополнительную информацию, полезную в диагностическом и прогностическом плане при подозрении на эти инфекции, в особенности при беременности или планировании беременности.
Метод полимеразной цепной реакции
Полимеразная цепная реакция (ПЦР), являющаяся одним из методов ДНК-диагностики, позволяет увеличить число копий детектируемого участка генома (ДНК) бактерий или вирусов в миллионы раз с использованием фермента ДНК-полимеразы. Тестируемый специфический для данного генома отрезок нуклеиновой кислоты многократно умножается (амплифицируется), что позволяет его идентифицировать.
Сначала молекула ДНК бактерий или вирусов нагреванием разделяется на 2 цепи, затем в присутствии синтезированных ДНК-праймеров (последовательность нуклеотидов специфична для определяемого генома) происходит связывание их с комплементарными участками ДНК, синтезируется вторая цепь нуклеиновой кислоты вслед за каждым праймером в присутствии термостабильной ДНК-полимеразы. Получается две молекулы ДНК. Процесс многократно повторяется. Для диагностики достаточно одной молекулы ДНК, то есть одной бактерии или вирусной частицы.
Введение в реакцию дополнительного этапа - синтеза ДНК на молекуле РНК при помощи фермента обратной транскриптазы - позволило тестировать РНК-вирусы, например, вирус гепатита С. ПЦР - это трехступенчатый процесс, повторяющийся циклично: денатурация, отжиг праймеров, синтез ДНК (полимеризация). Синтезированное количество ДНК идентифицируют методом иммуноферментного анализа или электрофореза.
В ПЦР может быть использован различный биологический материал - сыворотка или плазма крови, соскоб из уретры, биоптат, плевральная или спинномозговая жидкость и т.д. В первую очередь ЦПР применяют для диагностики инфекционных болезней, таких как вирусные гепатиты В, С, D, цитомегаловирусная инфекция, инфекционные заболевания, передающиеся половым путем (гонорея, хламидийная, микоплазменная, уреаплазменная инфекции), туберкулез, ВИЧ-инфекция и т.д.
Читайте также:

