Могут ли быть выделения при цитомегаловирусе
Обновлено: 19.04.2024
Цитомегаловирусная и папилломавирусная инфекции: возможности лечения и прегравидарной подготовки с применением противовирусного препарата на растительной основе
Журнал: Российский вестник акушера-гинеколога. 2015;15(4): 12‑17
Ежедневно человек вступает в контакт с огромным количеством микроорганизмов и вирусов, которые могут вызывать изменения функций систем организма, приводя к различным по тяжести и длительности заболеваниям, а также к неблагоприятным последствиям этих болезней.
Основными этапами взаимодействия вирусов с клеткой хозяина являются адсорбция (взаимодействие специфических рецепторов вируса и клетки хозяина), слияние суперкапсида с мембраной клетки, выделение нуклеиновых кислот нуклеокапсида и активация вирусной нуклеиновой кислоты, синтез нуклеиновых кислот и вирусных белков, сборка вирионов и выход новых вирусных частиц из клеток в межклеточное пространство, кровь или лимфу [1, 2].
К наиболее распространенным инфекциям относится инфекция, вызванная вирусами простого герпеса (ВПГ), основными особенностями которой по современным представлениям являются глобальный нозоареал распространенности, множество путей и способов передачи вирусов, чрезвычайно высокая инфицированность во всем мире, корреляция серопозитивности с социально-экономическими условиями, существование вирусов в ассоциациях с коинфекциями, высокая естественная восприимчивость людей и ряд других факторов. В Российской Федерации и странах СНГ ежегодно регистрируется около 22 млн случаев рецидивов герпесвирусной инфекции [3].
К группе вирусов, являющихся возбудителями герпетической инфекции, относятся цитомегаловирусы (ЦМВ). Актуальность изучения заболеваний, вызванных этими вирусами, обусловлена неблагоприятными последствиями, которые могут возникать в случае инфицирования в периоде новорожденности или на первом году жизни ребенка, или при первичном заболевании матери во время беременности [4]. По данным статистики, на первом году жизни антитела к цитомегаловирусной инфекции (ЦМВИ) обнаруживаются у 20% детей. У посещающих детские сады детей распространенность инфекции составляет 25—80%, во взрослой популяции антитела к ЦМВ встречаются у 85—90% населения [5].
Источником инфицирования может быть вирусоноситель, больной острой формой (в случае первичного инфицирования) или больной в период обострения инфекции. Пути передачи инфекции: воздушно-капельный, половой, контактный, пероральный, парентеральный, энтеральный и вертикальный, при этом передача вирусов может осуществляться через все биологические жидкости и выделения организма (слюна, моча и др.). При проникновении в организм иммунокомпетентных лиц, после первичного инфицирования, вирус может оставаться в организме пожизненно, в этом случае инфекция протекает бессимптомно (вирусоносительство), так как вирус защищен лимфоцитами от действия специфических антител и интерферона [6].
В современной медицинской литературе латентное течение инфекции, вызванной ЦМВ, обозначается как ЦМВ-инфекция, а клинически выраженное течение с поражением органов — как ЦМВ-болезнь. Развитие ЦМВ-болезни характеризуется лейкоцитарной инфильтрацией различных органов, что косвенно свидетельствует об участии в этом патологическом процессе интерлейкина-8, макрофагального воспалительного протеина-1α (MIP-1α) и других хемокинов и адгезивных молекул [7].
Клинически выраженное заболевание может развиваться при первичном инфицировании, при активации латентной инфекции на фоне снижения резистентности организма, что может наблюдаться у детей, беременных, взрослых со сниженным иммунитетом.
Клиническая картина ЦМВИ неспецифична и во многом зависит от пути инфицирования, состояния иммунной системы. Наиболее типичными симптомами ЦМВ-болезни являются лихорадка выше 38 °C, лейкопения, тромбоцитопения, повышение активности печеночных ферментов [8]. При ЦМВ-болезни могут развиваться поражение желудочно-кишечного тракта, гриппоподобные симптомы, воспалительные процессы носо- и ротоглотки. Наиболее тяжелая форма заболевания — ЦМВ-пневмония, характеризуется развитием тяжелой дыхательной недостаточности нередко с резистентностью к антибиотикам.
Вирусоносительство, проявляющееся стойким обнаружением антител класса G к ЦМВ, наблюдается у 90—95% взрослого населения (ЦМВ-позитивность), при этом вирусоноситель не опасен для окружающих, однако при снижении иммунитета носительство может перейти в активную форму, что вызывает появление антител класса М или многократное повышение уровня антител класса G. Генерализованная форма может возникать у лиц с выраженным иммунодефицитом и проявляться воспалением околоушных и подчелюстных слюнных желез, печеночной ткани, надпочечников, селезенки, суставов и других органов. Проявлениями локализованной формы у женщин может быть цервицит, эндометрит, сальпингоофорит, воспаление слюнных желез, шейных лимфатических узлов, у мужчин может быть бессимптомное носительство или вялотекущий уретрит.
У беременных женщин в 50—85% случаев обнаруживаются антитела к цитомегаловирусам, а у 1—12% беременных может наблюдаться первичное инфицирование, представляющее опасность для плода [5].
Первичная ЦМВИ и реактивация хронического процесса могут вызывать такие осложнения как неразвивающаяся беременность или невынашивание беременности, фетоплацентарная недостаточность, синдром задержки роста плода, многоводие, преждевременная отслойка плаценты и другие. Следует отметить, что при первичном инфицировании риск передачи вируса плоду выше, чем при обострении хронической инфекции, а последствия для плода зависят от срока гестации, при котором произошло первичное заражение или реактивация инфекции [9]. В случае, если первичное инфицирование женщины произошло в первой половине беременности, то у 8—10% детей, рожденных этими матерями, могут возникать клинические проявления в виде гепатоспленомегалии, гепатита, тромбоцитопении, петехиальной сыпи, микроцефалии, ретинита, гипербилирубинемии, гипотрофии, синдрома задержки роста плода, пневмонии и других проявлений [10, 11].
Инфицирование во второй половине беременности может приводить к хронической врожденной ЦМВИ, в тяжелых случаях — к нарушению функции центральной нервной системы, печени, нарушению зрения и слуха. Интранатальное и раннее постнатальное инфицирование, возникающее при вскармливании новорожденных серопозитивными матерями, протекает, как правило, без клинических проявлений и встречается чаще, чем трансплацентарное.
Трудности диагностики ЦМВИ связаны с отсутствием сезонной цикличности заболеваемости, характерных клинических проявлений заболевания, частой распространенностью латентных форм течения инфекционного процесса.
Другая широко распространенная вирусная инфекция — папилломавирусная (ПВИ) является ведущей причиной рака шейки матки, возникновения кондилом, плоскоклеточных неоплазий различной локализации. Распространенность инфекции вируса папилломы человека (ВПЧ) в мире среди женщин в возрасте 15—74 лет с отрицательными результатами цитологических мазков варьирует в зависимости от региона и составляет от 5 до 40%. Наиболее широко инфекция распространена среди сексуально активных подростков и женщин молодого возраста; 85% женщин в течение своей жизни инфицируются вирусом [12].
В литературе описано более 200 типов папилломавируса, которые являются строгими эпителиотропами, поражающими эпителий кожи и слизистых оболочек гениталий и других органов (гортань, ротовая полость, глаза и др.) [13].
ВПЧ подразделяют на две группы: ВПЧ низкого и высокого онкогенного риска. Высокоонкогенные типы ВПЧ ассоциированы в первую очередь с плоскоклеточными интраэпителиальными поражениями аногенитальной области (шейки матки — CIN, вульвы — VIN, влагалища — VaIN, ануса — AIN). ВПЧ является причиной рака шейки матки в 91—99,7%, рака вульвы (69%), влагалища (75%), полового члена (63%), предстательной железы, яичника — в 10—30%, рака гортани и ротовой полости — в 10—30% случаев [10].
Способность к неограниченно долгому персистированию ВПЧ в организме больного обусловлена особенностями жизненной стратегии этих вирусов, основанной на блокировании механизмов врожденного и адаптивного антивирусного иммунитета [11]. Механизм развития рака связывают с интеграцией вирусного генома в хромосомы клеток хозяина и длительной его персистенцией [13].
Противовирусная защита организма хозяина — очень сложный и многокомпонентный механизм. Отличительным свойством вирусов в целом, ЦМВ и ВПЧ в частности, является то, что они не могут самостоятельно размножаться, но способны эффективно репродуцироваться в чувствительных клетках макроорганизма, где реализуют свою генетическую программу по созданию потомства [14—16]. При первичном взаимодействии с вирусами инфекционным агентам противостоят неспецифические защитные механизмы организма, к которым относятся эпителий кожи, слизистые оболочки. После проникновения вируса внутрь клетки основную роль в обеспечении местного иммунитета играют интерфероны, другие цитокины, вырабатываемые зараженными клетками, а также лимфоциты, макрофаги, обеспечивающие фагоцитоз и разрушение вирусов. Образующиеся при вирусных инфекциях антитела действуют непосредственно на вирусы или на клетки, инфицированные ими [17].
Практически все вирусы индуцируют выработку интерферонов, их образование является одной из наиболее ранних защитных реакций организма на внедрение вирусов; интерфероны способны подавлять внутриклеточные этапы репродукции вирусов в зараженных клетках, обеспечивать невосприимчивость к вирусам окружающих здоровых клеток и предотвращать диссеминацию вирусов в организме. Поэтому применение иммунотропных препаратов, интерферона и его индукторов становится необходимой частью общепринятого патогенетического лечения различных инфекционных заболеваний [18].
Основным методом диагностики ЦМВ является серологический с выявлением специфических антител к антигенам вируса. Для выявления особенностей течения инфекции рекомендуется определение авидности иммуноглобулинов классов M и G и антител к вирусному белку. Молекулярно-биологические методы (ДНК-гибридизация, лигандная цепная реакция, полимеразная цепная реакция) при диагностике ЦМВИ, ПВИ и других инфекций позволяют выявлять ранние стадии, латентную и персистентную инфекцию, количественные параметры возбудителей. Цитологический метод применяется для проведения экспресс-диагностики ЦМВИ на поверхности хориона, плодных оболочек.
Лечение. Этиотропные препараты для лечения пациентов с вирусными (цитомегаловирусной, герпесвирусной, папилломавирусной и др.) инфекциями отсутствуют. При лечении больных с тяжелыми, генерализованными формами ЦМВИ возможно применение препаратов, обладающих противовирусным действием (ацикловир, ганцикловир, валацикловир, фамцикловир, фоскарнет и др.), которые прямо или опосредованно ингибируют вирусную ДНК-полимеразу, снижают вирусную продукцию у пациенток с клиническими симптомами, характерными для герпесвирусных инфекций. Однако эти агенты весьма токсичны, и требуется строгий контроль, особенно при длительном применении, за содержанием препарата в крови. Как правило, эти препараты назначают пациенткам после трансплантации или при выраженном снижении иммунитета [19, 20].
Токсичность препаратов в значительной степени ограничивает их применение. Препараты противопоказаны беременным, кормящим матерям и новорожденным, а также не рекомендуются женщинам, планирующим беременность.
Пациенткам с активной инфекцией в прегравидарный период с целью профилактики и лечения внутриутробной инфекции, а также лечения генерализованных форм возможно проведение профилактического лечения, позволяющего обеспечить в подавляющем большинстве случаев наступление беременности и благоприятное ее течение. С этой целью в прегравидарный период показано применение растительных противовирусных препаратов, рекомбинантного интерферона α-2, иммуноглобулина нормального человеческого и др. [21, 22].
В настоящее время весьма перспективным является препарат растительного происхождения, основным действующим компонентом которого служит очищенный экстракт побегов растения Solanum tuberosum, оказывающий противовирусное действие. На основе этого экстракта создан препарат Панавир, представляющий собой полисахарид, относящийся к классу гексозных гликозидов. Панавир способен повышать неспецифическую резистентность организма к инфекциям и индукцию интерферона, приводить к стабилизации показатели тканевого и гуморального иммунитета, что чрезвычайно важно для женщин, планирующих беременность.
Формы выпуска Панавира: раствор для внутривенных инъекций, ректальные и вагинальные суппозитории, гель для наружного применения и гель-спрей Панавир-Интим и Панавир-Инлайт. Панавир показал свою эффективность в лечении больных с папилломавирусной [23], цитомегаловирусной и герпетической инфекциями [24—26], вирусным гапатитом С [27], клещевым энцефалитом [28] и рядом других заболеваний.
Лечение пациенток с экзофитными кондиломами, хирургическое лечение при кондиломатозных высыпаниях (криодеструкция, радиоволновая хирургия, медикаментозная коагуляция, лазерная вапоризация), особенно проводимое в целях подготовки к беременности, можно комбинировать с местным лечением Панавиром. При этом обработка кондилом гелем Панавир, вагинальное орошение спреем или применение вагинальных (ректальных) суппозиториев способствуют более быстрому заживлению кожных рубцов, уменьшению частоты рецидивов, что важно для женщин, планирующих беременность. Экзофитные формы папилломавирусной инфекции могут возникать на фоне герпетических высыпаний или у женщин-носительниц ВПГ при хламидийной или других инфекциях. Перед назначением лечения рекомендуется проведение предварительного обследования женщин, а в случае выявления инфекций — проведение этиотропной терапии с последующим восстановлением микробиоценоза влагалища, что улучшает результаты лечения. По данным Г.Г. Анташян [23], при комплексном лечении больных с экзофитными формами ПВИ отмечается достоверное снижение частоты проведения деструктивных процедур, а также увеличение межрецидивных интервалов.
Обоснованным является применение Панавира при лечении пациенток с герпетическими поражениями кожи и слизистых оболочек, а также вирусоносительства. При лечении пациентов с рецидивирующим генитальным герпесом выявлено достоверное иммунокорригирующее и противовоспалительное действие препарата, увеличение длительности периодов ремиссии, что свидетельствует об эффективности Панавира [29—31]. Проведение лечения в период планирования беременности позволит снизить риск обострения инфекции в гестационный период.
Проведенные исследования показали хорошую переносимость препарата. Клинические испытания показали отсутствие мутагенного, тератогенного, канцерогенного, аллергизирующего и эмбриотоксического действия препарата при наличии слабого цитотоксического и антипролиферативного эффектов [32]. Назначение Панавира возможно в период прегравидарной подготовки, во II и III триместрах беременности в случае первичной инфекции или реактивации инфекционного процесса.
Для лечения пациенток с заболеваниями, вызванными вирусами, могут быть рекомендованы парентеральные формы Панавира, при этом терапевтическая доза препарата составляет 200 мкг действующего вещества. Кратность внутривенного введения и длительность лечения зависят от возбудителя заболевания. В случае подготовки к беременности, лечения цитомегаловирусной и папилломавирусной инфекций раствор Панавира применяют трехкратно в течение 1-й недели с интервалом 48 ч и двукратно в течение 2-й недели с интервалом 72 ч внутривенно медленно струйно. Возможно также применение Панавира в форме ректальных суппозиториев ежедневно на ночь в течение 10 дней с возможным повтором курса лечения через 1 мес.
Возможно интравагинальное введение суппозиториев при лечении больных с ПВИ-ассоциированной патологией шейки матки или ВПГ-инфицированием, при этом рекомендуемая длительность лечения также составляет 10 дней. Для лечения больных с экзофитными кондилломами рекомендуется нанесение геля Панавир тонким слоем на пораженные участки кожи и/или слизистых оболочек 5 раз в сутки. Продолжительность лечения составляет 4—5 дней, при необходимости курс лечения может быть продлен до 10 дней.
М.М. Дамиров и соавт. [33] показали высокую эффективность комплексного лечения пациенток с плоскоклеточными интраэпителиальными поражениями шейки матки низкой степени выраженности на фоне персистирующей ВПЧ-инфекции 0,004% раствором Панавира по схеме: 5 мл раствора внутривенно медленно курсом в 5 инъекций с и нтервалом 48 ч между первым и вторым введениями с последующим интервалом в 72 ч при одновременном местном применении препарата Панавир-Интим в форме геля интравагинально 2 раза в день в течение 10 дней с экспозицией 10—15 мин после введения препарата.
В 2012 г. проведено открытое рандомизированное сравнительное многоцентровое контролируемое клиническое исследование по изучению безопасности, переносимости и терапевтической эффективности раствора панавира для внутривенного введения 0,04 мг/мл в комплексной терапии беременных с хронической цитомегаловирусной инфекцией в стадии обострения во II и III триместрах беременности [34].
Цель исследования — провести оценку безопасности, переносимости и эффективности Панавира для внутривенного введения в составе комплексной терапии цитомегаловирусной инфекции у беременных во II и III триместре. Было выявлено, что терапия ЦМВ-инфекции Панавиром способствовала эрадикации вирусов, при этом ЦМВ серологическим методом не был обнаружен у женщин, получавших лечение, а также вирусная инфекция не оказала неблагоприятного влияния на течение беременности, развитие плодов и здоровье новорожденных.
Обобщение результатов проведенных исследований позволяет сделать заключение о перспективности дальнейшего изучения терапевтических свойств препарата Панавир в отношении вирусных инфекций, они убедительно доказали, что противовирусный препарат Панавир является эффективным средством при лечении больных с ЦМВИ, ВПЧ, ВПГ, клещевым энцефалитом, может применяться в период прегравидарной подготовки женщин группы высокого риска активизации этих инфекций во время беременности. Препарат показан в случае подготовки к беременности женщин с отягощенным анамнезом, при персистенции папилломавирусной инфекции, хронической, недавно перенесенной острой или с обострением других вирусных инфекций, а также женщинам, у которых диагностировано нарушение интерферонового статуса.
Поиск натуральных природных фармакологических агентов и анализ механизмов их действия является весьма актуальным аспектом в вопросе создания нового поколения противовирусных лекарственных препаратов с целью лечения инфекций человека.
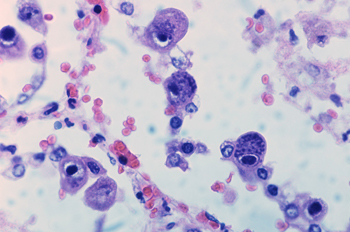
Цитомегаловирусная инфекция (ЦМВИ) – хроническая инфекционная болезнь вирусной этиологии, характеризующаяся многообразием форм патологического процесса от латентной инфекции до клинически выраженного генерализованного заболевания (цитомегаловирусная болезнь). Тяжесть и спектр проявлений ЦМВИ весьма разнообразны.
Продолжительность инкубационного периода при заражении ЦМВ составляет 4-12 недель. Клиническая картина приобретенной ЦМВИ у взрослых зависит от формы инфекции (первичное заражение, реинфекция, реактивация латентного вируса), путей и механизмов заражения (аспирация инфицированной слюны, гемотрансфузии, половой путь, трансплантация инфицированного органа), состояния иммунной системы (отсутствие или наличие иммуносупрессии и степень ее выраженности).
Первично латентная цитомегалия – самая частая форма инфекции. Латентная цитомегаловирусная инфекция продолжается пожизненно и клинически не проявляется, однако под влиянием каких-либо причин может активизироваться и переходить в манифестную клинически выраженную форму.
Первичное инфицирование ЦМВ иммунокомпетентных лиц обычно протекает бессимптомно или с нерезко выраженным мононуклеозоподобным синдромом. Данным синдромом острая ЦМВИ проявляется лишь у 5% взрослых (соответственно, не более, чем у 3-5% беременных). Основные отличительные признаки — высокая лихорадка, слабость, утомляемость, сильное недомогание, выраженный и длительный астенический синдром, в крови — относительный лимфоцитоз, атипичные лимфоциты.
Острая форма ЦМВИ чаще всего наблюдается у лиц, зараженных вирусом при переливании крови от больного человека или половым путем. Обычно ее течение похоже на простуду и сопровождается такими симптомами, как слабость, общее недомогание, головные боли и насморк. Часто возникает воспаление и увеличение слюнных желез с обильным отделением слюны и белесоватыми налетами на деснах и языке.
Характерны высокая лихорадка длительностью более двух недель, общее недомогание, выраженная утомляемость, лимфаденопатия. Отмечаются головная боль, миалгии, артралгии, гепатоспленомегалия, повышение активности аминотрансфераз и щелочной фосфатазы. Возможно развитие гепатита и пневмонии. Большинство больных выздоравливает полностью, хотя астенический синдром сохраняется длительное время. При отсутствии выраженных иммунологических нарушений острая ЦМВИ переходит в латентную с пожизненным присутствием
Острая ЦМВИ у беременных протекает бессимптомно или с умеренно выраженными признаками фарингита, незначительного повышения температуры тела, признаками астении. Заражение вирусом в первые 20 недель беременности может быть причиной самопроизвольного выкидыша, внутриутробной гибели плода, мертворождения, пороков развития. При заражении в более поздние сроки у ребенка может быть врожденная цитомегалия, симптомы которой обнаруживаются с первых дней внеутробной жизни.
У людей с нормальным иммунитетом (иммунокомпетентных) ЦМВИ, как правило, протекает латентно. Однако на фоне имеющихся иммунологических нарушений резко повышается риск развития клинически выраженных (манифестных) форм заболевания. Например, манифестная ЦМВИ занимает одно из первых мест в структуре оппортунистических заболеваний у ВИЧ-инфицированных пациентов. Кроме того, клинически выраженная ЦМВИ — одно из самых частых и серьёзных инфекционных осложнений при трансплантации органов или в случае проведения длительной иммуносупрессивной терапии.
Развитие тяжёлой ЦМВИ описано у онкогематологических больных, пациентов, страдавших пневмоцистной пневмонией, туберкулёзом, лучевой болезнью, ожоговой травмой, у лиц, находящихся на длительной кортикостероидной терапии, перенёсших различные стрессовые ситуации.
Развитие манифестной ЦМВИ в этом случае может быть обусловлено первичным инфицированием ЦМВ, повторным попаданием вируса в организм (реинфекцией) или реактивацией вируса в заражённом организме . Вероятность возникновения и тяжесть течения ЦМВИ связывают со степенью иммуносупрессии.
Через 1-3 месяца при наличии выраженной иммуносупрессии наступает тяжелая органная патология с тенденцией к генерализации процесса.
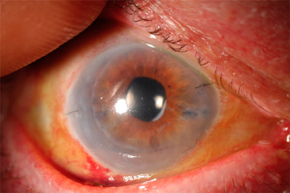
При генерализованной форме чаще наблюдается поражение легких, почек и кишечника, реже - печени и других органов. Один из тяжёлых признаков ЦМВИ — ретинит. Потеря зрения необратима, поскольку данный процесс развивается в результате воспаления и некроза сетчатки. Как возможные клинические симптомы ЦМВИ диагностируют также восходящий миелит и полиневропатию (подострого течения); энцефалит, характеризующийся деменцией; цитомегаловирусный гепатит с одновременным поражением жёлчных путей и развитием склерозирующего холангита; адреналит, проявляющийся резкой слабостью и снижением АД. Иногда возникает эпидидимит, цервицит, панкреатит.
По оценкам специалистов, только в США ежегодно рождается 30—40 тысяч детей с врожденной ЦМВ-инфекцией, т. е. она далеко опережает по частоте и значимости все остальные врожденные инфекции. Важно отметить, что врожденная цитомегаловирусная инфекция всегда имеет генерализованный характер, тогда как приобретенная может быть локализованной с изолированным поражением слюнных желез.
Для врожденной цитомегалии характерна внутриутробная задержка развития, желтуха, увеличение печени и селезенки, уменьшение числа тромбоцитов, ретикулоцитоз и прогрессирующая анемия. Врожденная генерализованная ЦМВИ характеризуется также геморрагическими высыпаниями на коже и слизистых оболочках, кровоизлияниями во внутренние органы и головной мозг, значительной анемией, развитием очагов миелоэритробластоза в печени и почках.
Самое тяжелое проявление данной формы — энцефалит, который практически не встречается при приобретенной цитомегаловирусной инфекции. Часто развиваются микроцефалия, расширение желудочков мозга, нейросенсорная тугоухость. Отмечается поражение глаз - увеит, помутнение хрусталика и субатрофия радужной оболочки.
Резервуаром цитомегаловируса в природе является только человек — хронический носитель вируса или больной какой-либо из форм этого заболевания. Передача инфекции осуществляется практически через все биологические жидкости и выделения организма, а также посредством органов и тканей, используемых для трансплантации. Из зараженного организма вирус выделяется с мочой, слюной, слезной жидкостью, кровью, спермой и др. Инфекция передается различными путями - воздушно-капельным, половым, контактным, пероральным, парентеральным, внутриутробным, трансфузионным или трансплантационным.
Если иммунитет заразившегося человека нормальный, то цитомегалия чаще всего протекает в латентной, то есть скрытой форме, без видимых клинических проявлений заболевания. Инфекция существует в виде бессимптомного вирусоносительства, ничем не обнаруживая себя и не вызывая каких-либо патологических явлений. У взрослого человека и ребенка старшего возраста благодаря высокой эффективности иммунного ответа, значительно чаще наблюдается латентное течение ЦМВИ.
В случае иммуносупрессии, т.е. при ослаблении иммунной системы, резистентность организма снижается и активируется латентная инфекция, которая может представлять серьезную угрозу жизни. В группе риска - новорожденные дети, беременные женщины, онкобольные, пациенты после трансплантации органов или костного мозга/стволовых клеток, больные СПИДом, а также пациенты, подвергшихся переливанию крови. На фоне резкого снижения иммунитета, цитомегалия может перейти в клинически выраженное заболевание разной степени тяжести, вплоть до генерализованных форм с тяжелыми поражениями внутренних органов, центральной нервной системы и в ряде случаев летальными исходами.
Для человека с неповрежденной иммунной системой уменьшить риск заражения цитомегаловирусной инфекцией поможет выполнение обычных правил личной гигиены: мытье рук после посещения мест общего пользования (туалет, общест венный транспорт и т.д.), перед едой, а также использование чистой посуды. В транспланталогии важной мерой профилактики ЦМВИ является подбор серонегативного донора, если серонегативен реципиент.
Генерализованная форма ЦМВИ (цитомегалии, цитомегаловирусной инфекции), как правило, возникает на фоне какого-либо другого заболевания, резко снижающего иммунитет (лейкозы, злокачественные опухоли, СПИД), или после тяжелых хирургических операций. Следствием цитомегалии в этом случае могут быть воспаление надпочечников, селезенки, поджелудочной железы, почек и других внутренних органов. ЦМВИ также может проявляться в виде гепатита. Доказано, что до 30% гепатитов неясной этиологии обусловлены поражением печени герпесвирусами, а именно цитомегаловирусом или вирусом простого герпеса.
Как сопутствующие явления возникают пневмонии, поражения сосудов глаза, стенок кишечника, головного мозга и периферических нервов. В составе крови уменьшается количество тромбоцитов. Кроме основного заболевания и ЦМВИ, ухудшение состояния больного может вызвать наслаивающаяся септическая бактериальная инфекция.
По статистике Всемирной Организации Здравоохранения генерализованная форма цитомегалии является причиной наибольшего количества летальных случаев в мире после гриппа и ОРВИ.
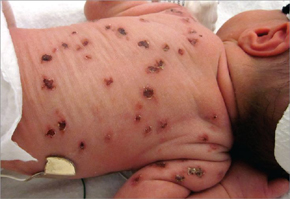
Внутриутробная ЦМВИ считается наиболее опасной, так как может вызвать серьезные поражения плода вплоть до его гибели или привести к рождению детей с тяжелыми неврологическими расстройствами, патологией зрительного и слухового нервов, различными соматическими повреждениями. Характер поражения зависит от сроков инфицирования плода ЦМВ. На ранних сроках (4–6 недель беременности) возможна его гибель или самопроизвольный выкидыш. При инфицировании цитомегаловирусом (ЦМВ) в поздние сроки беременности прогноз более благоприятен. Инфицирование ЦМВ плода во второй половине беременности может не приводить к клинически выраженной патологии при рождении, но быть причиной развития заболевания в первые недели - месяцы жизни ребенка.
Инфицирование в первые 3 месяца гестации может привести к тератогенному действию на плод, а в более поздние сроки – к врожденной цитомегалии, не сопровождающейся пороками развития. У части детей внутриутробное инфицирование ЦМВ проявляется лишь к 5–7 годам в виде нарушения зрения, ухудшения слуха, судорожных расстройств, или задержки физического и умственного развития.
В связи с этим крайне важно обследование женщин на ранних сроках беременности (оптимально – при ее планировании) с целью установления иммунного статуса в отношении ЦМВИ и выявления группы риска, требующей более серьезного и регулярного обследования вплоть до родов.
Возможность онкогенного действия вируса окончательно не изучена. Полагают, что выделение вируса цитомегалии из опухоли больных саркомой Капоши, карциномы простаты, злокачественной лимфомы, рака шейки матки, аденокарциномы толстой кишки и др. является косвенным свидетельством этиологической роли отдельных штаммов ЦМВ человека в развитии онкологических заболеваний.
Цитомегаловирусная инфекция наиболее часто поражает реципиентов трансплантируемых органов. У 38–96% пациентов после трансплантации встречается активная форма ЦМВИ, при которой каждый орган может быть вовлечен в инфекционный процесс. Клинически выраженная ЦМВИ – одно из серьезных инфекционных осложнений при трансплантации солидных органов и костного мозга, являясь одной из частых причин длительной госпитализации больных и их смерти.
Имеются данные, подтвержденные при экспериментальной инфекции у животных, что у больных, перенесших пересадку сердца, ЦМВИ является одной из причин атеросклероза. Доказано, что сосудистые поражения почечного трансплантанта с дисфункцией почки обусловлены ЦМВИ.
Период максимального риска инфицирования приходится на 1–4-й мес. после трансплантации. Максимальный риск заболевания выше при первичном инфицировании. При первичном инфицировании заболевание протекает более тяжело, чем при активизации латентной ЦМВИ.
Основными проявлениями ЦМВИ у больных после трансплантации органов является гепатит, пневмония, ретинит, тяжелые поражения желудочно-кишечного тракта, лейкопения. Присоединение бактериальной, грибковой или протейной инфекции на фоне ЦМВИ могут приводить к угрожающим жизни последствиям. Так, у пациентов после трансплантации костного мозга самым тяжелым осложнением считается интерстициальная пневмония, которая диагностируется в 15–20% случаев. У 80–90% больных пневмония заканчивается летальным исходом.
Читайте также:

