Может быть мышечная слабость при сепсисе
Обновлено: 25.04.2024
Сепсис представляет собой заражение крови продуктами гнилостного распада, имеющего место в организме вследствие воспалительного неадекватного леченого процесса. По сути, сепсис - это воспаление, распространившееся на весь организм. Это системный ответ на обильное пребывание в крови бактерий, независимо от места их проникновения и скопления.
Это достаточно опасное для организма состояние, стремительно идущее к летальному исходу и потому требующее немедленной и адекватной терапии.
Вопреки постоянно совершенствующимся медицинским технологиям сепсис сегодня, как и много лет назад остается актуальной проблемой. Для лечения сепсиса используются новые поколения антибактериальных препаратов, однако и это не устраняет болезнь из рейтинга причин смерти в отделениях интенсивной терапии. Примечательно, что 18% из тех, по отношению к кому применялась интенсивная терапия лечения в условиях медицинского учреждения, сталкивались с развитием сепсиса, еще в 63% случаев он сопровождал внутрибольничные инфекции.
К инфекциям, распространение которых по организму рискует завершиться сепсисом, относят:
- бактерии
- стафилококк,
- стрептококк,
- пневмококк,
- синегнойная палочка,
- клебсиелла,
- кандида,
- герпес,
- токсоплазмоз.
Для того чтобы инфекционный процесс в организме перерос в сепсис необходимо сочетание трех обстоятельств:
- наличие возбудителя инфекции;
- отрицательное состояние первичного очага инфекции;
- соответственная реактивность организма.
Риск развития сепсиса обуславливается не столько свойствами инфекции, сколько ее концентрацией в первичном очаге, распространением отсюда вглубь организма и ток крови. Непоследнюю роль играет и резистентность организма, которая легко подавляется под воздействием неблагоприятных факторов. Среди последних:
- любые заболевания
- эндокринные и обменные, в частности сахарный диабет,
- онкологические,
- гематологические,
- иммунологические,
- низкое содержание белка,
- хронические гиповитаминозы,
Механизм развития сепсиса берет начало с того, что из первичного очага инфицирования через кровеносные или лимфатические сосуды происходит, соответсвенно, гематогенная или лимфогенная диссеминация инфекции. Следственно, происходит образование вторичных септических очагов, так называемых метастазов, из которых инфекция также распространяется в кровь. Каковой будет локализация метастазов, зависит от типа возбудителя. Гнойники могут образовываться в любых внутренних органах.
![сепсис]()
При сепсисе случаются органно-системные повреждения, чем продолжается механизм заболевания. Это случается в силу отсутствия контроля над распространением провоспалительных медиаторов из первичного очага инфекции. Затем происходит их активация под влиянием макрофагов, нейтрофилов, лимфоцитов и других клеток в любых органах и тканях; повторно выделяются те же провоспалительные медиаторы и повреждается эндотелий.
Разновидности сепсиса
Чаще всего сепсис случается после воспалительного процесса конкретной локализации. Однако не менее распространен и раневой сепсис. И тот, и другой развивается на фоне сниженной резистентности макроорганизма к распространяющейся патогенной микрофлоре и на фоне ослабленного иммунитета. Упадок защитных способностей организма вследствие воспаления, раны, операционного вмешательства или тяжелого заболевания нередко дополняется крупной кровопотерей и недостаточным питанием.
Частыми источниками септической инфекции медики называются нагноения при выше описанных условиях. Нечто подобное способно развиться и при местных гнойных заболеваниях как то фурункул, карбункул, флегмона.
Зависимо от первичного очага сепсиса и его происхождения различают:
- хирургический сепсис - вследствие нагноения в ране, локализированных гнойниках;
- акушерско-гинекологический сепсис - вследствие родов или абортов, случившихся в нестерильных условиях, когда микротрещины или разрывы в родовых путях становятся "входными воротами" для инфекции;
- урологический сепсис - вследствие гнойных процессов и отяжеленных воспалений в мочеполовых органах, что обычно сопровождается и застоем, инфицированием мочи;
- риногенный, тонзилогенный, отогенный сепсис - редкие формы заражения крови, которые берут начало с локализации инфекции в полости рта, носу, околоносовых пазухах, носоглотке, ухе; для того чтобы течение инфекции обрело столь тяжелую форму необходимым условием становится тромбофлебит кавернозного синуса или тромбоз вен клетчатки глазницы, тромбофлебит сигмовидного и каменистого синусов.
Кроме того, выделяют септичемическую и септикопиемическую разновидность сепсиса:
- септицемическая - не сопровождается образованием метастатических очагов гнойной инфекции, однако склонная к перерастанию в септикопиемическую;
- септикопиемическую - характеризуется образованием метастатических очагов гнойной инфекции, откуда происходит все более глубокое распространению инфекции.
Заражение крови может протекать в четырех формах:
- молниеносная - несколько суток;
- острая - 5-7 суток;
- подострая - менее 6 недель;
- хроническая - более 6 недель.
Симптомы сепсиса
Коварство заболевания заключается в риске его симптомов оказаться размытыми. Объясняется это тем, что в разгар первичного заболевания свойства возбудителей поддаются изменениям из-за массивной антибиотикотерапии, несколько угнетаются, однако не всегда сам возбудитель уничтожается. Такое латентное его пребывание в организме чревато дальнейшим распространением даже при относительно невысокой температуре тела. Хотя именно устоявшаяся лихорадка гектического типа считается отличительным признаком сепсиса при наличии предпосылок к тому, то есть выше перечисленных факторов. Кроме нее возможны:
- обильное потоотделение при снижении температуры тела,
- в соответствии со скачками температуры скачкообразным становится и пульс,
- ознобы и головная боль, общая слабость,
- рвота и понос,
- утрата аппетита,
- обезвоживание и стремительная утрата веса,
- землистый цвет кожных покровов (если нарушается функция печени, кожа желтеет), утрата ими эластичности и упругости;
- образование флегмон и абсцессов различной локализации.
Возможны изменения психоэмоционального статуса вплоть до грубых общемозговых расстройств - коматозное состояние. В последующем присоединяются воспалительные изменения со стороны внутренних органов: почек, эндокарда, печени, кишечника, селезенки.
При сепсисе наблюдается тахикардия (более 90 ударов в минуту) и тахипноэ (более 20 вдохов в минуту).
Диагностика сепсиса
Заподозрить сепсис стоит если при инфекционно-воспалительном заболевании, вследствие ранения или операционного вмешательства лихорадка держится более 5 дней, и скачки температуры становятся немотивированными. Лабораторные анализы крови показывают:
- лейкоцитоз;
- лейкопению;
- палочко-ядерный сдвиг влево;
- тромбоцитопению.
Положительные результаты бактериологического исследования крови - обнаружение гемокультуры. Для получения достоверного результата необходим 3-кратный забор крови в объеме 20-30 мл. с интервалами 1 ч. во время подъема температуры по возможности до начала антибиотикотерапии.
При диагностике на предмет наличия сепсиса важно различить:
- синдром системного воспалительного ответа - системная реакция организма на воздействие различных сильных раздражителей (инфекция, травма, операция и т.д.);
- сепсис - та же совокупность изменений, что и при ССВО, но дополнительно обнаруживаются патогенны в одной или нескольких тканях, признаки перитонита, пурпуры, пневмонии и пр.;
- отяжеленный сепсис - клиническая картина сепсиса дополняется гипотензией и гипоперфузией, нарушением функций отдельных органов, например, печени или почек;
- септический шок - тяжелая форма заражения формы, когда нарушение функций не удается восстановить даже интенсивной терапией и реанимирующими мероприятиями; отличается высокой летальностью.
Лечение сепсиса
Лечение сепсиса представляет собой комплекс процедур, которые проводятся преимущественно в условиях медицинского учреждения. Так называемая интенсивная терапия состоит из мер, нацеленных на санацию очага инфекции, и дополняется антибиотикотерапией, призванной устранить инфекцию в крови. Отмечается, что сохранение жизни больного и устранение органных дисфункций не будет возможным без назначения интенсивной терапии.
Этиотропное лечение сепсиса должно быть не просто своевременным, а максимально ранним. Изначально препараты назначаются в столь высоких дозировках, чтобы обеспечить достаточную концентрацию действующего вещества в зараженной крови, а также в очагах инфекции. Этиотропная терапия может быть эффективной лишь при условии выявления возбудителя, конкретной инфекции, а также его чувствительности к выбираемым антибиотикам. Верный выбор антибиотика лежит в основе качественного лечения сепсиса.
Этиотропная терапия длится вплоть до достижения устойчивой положительной динамики состояния пациента и исчезновения основных симптомов инфекции. Если этого не происходит в течение первой недели лечения, необходимо провести дополнительное обследование для выявления осложнений или очага инфекции другой локализации.
Если установить первичный очаг инфекции не удается, равно как и выявить тип возбудителя, как минимум необходимо определить условия возникновения сепсиса - вследствие пребывания пациента в клинических условиях и развития инфекции на фоне определенной болезни (госпитальная форма) или внебольничная.
Как показывает практика, внебольничный сепсис поддается лечению:
- нефалоспоринами 3-го и 4-го поколения,
- фторхинолонами - благодаря широкому спектру действия являются препаратами выбора при лечении инфекций неизвестной этиологии
Госпитальная форма сепсиса лечится:
- карбапенемами - препаратами с широким спектром действия, к которым внутрибольничные штаммы грамнегативных бактерий низкорезистентны.
Лечение разных форм сепсиса определяется его происхождением:
- при анаэробном сепсисе применяются метронидазол, линкомицин, клиндамицин;
- для лечения сепсиса, вызванного грамотрицательными бактериями, уместен препарат с моноклональными антителами против эндотоксина грамотрицательных бактерий;
- сепсис вследствие распространения грибковой инфекции лечится амфотерными оксидами и флуконазолом;
- при стафилококковом сепсисе эффективен противостафилококковый иммуноглобулин, а также внутривенное введение противостафилококковой плазмы;
- когда инфекционный процесс достиг уровня генерализированной септической болезни, назначают ацикловир, ганцикловир, фамцикловир.
Параллельно с этиотропными средствами целесообразно использование пассивной иммунотерапии, среди разнообразия которых предпочтение отдается иммуноглобулину, идеально подходящему для внутривенного введения.
Ведущую роль в лечении сепсиса любой локализации играет инфузионная терапия. Она относится к первичным мероприятиям поддержания гемодинамики и сердечного выброса. Основными задачами, которые стоят перед врачом и которые удается решить посредством инфузионной терапии, оказываются:
- восстановление адекватной тканевой перфузии,
- нормализация клеточного метаболизма,
- коррекция расстройств гомеостаза,
- снижение концентрации медиаторов септического каскада и токсических метаболитов.
Использование этого алгоритма действий способствует выживаемости при септическом шоке и тяжелом сепсисе. Объем инфузионной терапии рекомендуют поддерживать на таком уровне, чтобы давление заклинивания в легочных капиллярах не превышало коллоидно-онкотическое давление плазмы. Это позволяет исключить риск отека легких и увеличить сердечный выброс.
Инфузионная терапия - это составляющая общей целенаправленной интенсивной терапии сепсиса. Для инфузий применяют кристаллоидные и коллоидные инфузионные растворы. Отмечается, что адекватная коррекция венозного возврата и уровня перенапряжения требует вдвое, а порой и вчетверо большего введения кристаллоидов, нежели коллоидов. Инфузия кристаллоидов более связана с риском отека тканей, а их гемодинамический эффект менее продолжителен, чем у коллоидов. Вместе с тем кристаллоиды не влияют на коагуляционный потенциал и не вызывают анафилактических реакций. В связи с этим выбор того или иного раствора диктуется особенностями течения сепсиса в конкретном случае:
- степенью гиповолемии,
- фазой ДВС-синдрома,
- наличием периферических отеков,
- уровнем альбумина крови,
- тяжестью острого легочного повреждения.
При выраженном дефиците объема циркуляционной крови показаны плазмозаменители:
- декстраны,
- гидроксиэтилкрохмал - имеет потенциальное преимущество перед декстранами вследствие низкого риска утечки через мембрану и отсутствия клинически значимого влияния на гемостаз.
В ранние сроки в связи с наличием тромбогеморрагического синдрома назначают гепарин, введение которого проводят под контролем клинических проявлений и коагулограммы.
В случае развития тяжелой степени сепсиса проноз неблагоприятен, оправданным становится гемодиализ. Для профилактики стрессовых язв в пищеварительном канале обязательны ингибиторы протонной помпы или блокаторы гистаминорецепторов. Назначают также препараты, ингибирующие протеолиз.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Мышечная слабость - причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Задумывались ли вы когда-нибудь, сколько мышц в нашем теле? Каким образом происходит их сокращение? Какие функции, помимо перемещения тела в пространстве, выполняют мышцы? Что произойдет, если мышечные волокна утратят способность к сокращению, и разовьется мышечная слабость? На эти и другие вопросы мы постараемся ответить в этой статье.
Выделяют два вида мышечной ткани: поперечно-полосатую, из которой состоят сердечная мышца и скелетная мускулатура, позволяющая нам двигаться, и гладкую, выстилающую поверхность внутренних органов и сосудов.
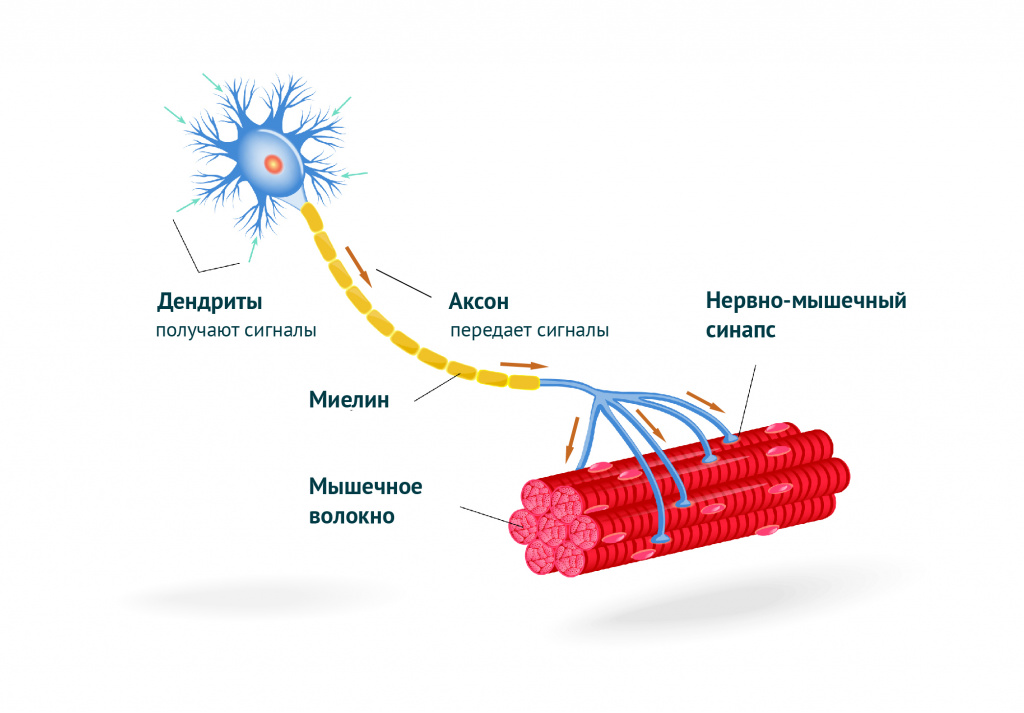
В теле человека насчитывается более шестисот скелетных мышц. Мышца – это орган, в котором осуществляется интенсивное кровоснабжение, что обеспечивает высокий уровень обмена веществ. Сокращение мышечных волокон происходит под действием нервных импульсов, исходящих из соответствующих центров нервной системы. Нервный импульс проходит через нервно-мышечный синапс (место соединения нервного окончания с мышцей) и вызывает сокращение мышцы.
![структура двигательного нейрона.jpg]()
Мышечная ткань выполняет не только двигательную функцию, но и функцию защиты, теплообмена, активно участвует в работе всех внутренних органов.
Сердечная мышца обеспечивает постоянную циркуляцию крови по организму, благодаря чему осуществляется транспорт веществ.
Мышечная слабость (миопатия, миастения) – состояние, для которого характерна быстрая утомляемость мышц. Мышечное утомление не всегда зависит от физической нагрузки и может быть симптомом многих хронических заболеваний.
Сила мышечного сокращения определяется интенсивностью нервного импульса, поступающего в мышцу, и строением мышечного волокна. Поэтому все заболевания, основным симптомом которых является мышечная слабость, делятся на две большие группы: миопатии и миастении.
К миопатиям относятся болезни, в основе которых лежит первичное поражение мышечных волокон. Миастении – заболевания, развивающиеся в результате расстройства нервно-мышечной передачи импульса.
Отдельно выделяют парезы и параличи, возникающие при первичном поражении нервной системы, когда к нервно-мышечному синапсу приходит импульс недостаточной силы, или импульс не доходит вообще.
Заболевания, вызывающие мышечную слабость, могут быть наследственными и приобретенными. Мышечная слабость бывает тотальная, поражающая большую часть мускулатуры тела, или избирательная с поражением отдельных групп мышц; симметричная (слабость одноименных мышц с двух сторон: справа и слева) или асимметричная.
Среди механизмов, приводящих к недостаточной силе сокращения и быстрой утомляемости мышц, можно выделить следующие.
Во-первых, это первичные поражения нервной системы, такие как повреждение головного или спинного мозга, а также нервных волокон в результате травм, нарушения кровоснабжения, воспалительных процессов и др.
Здесь же стоит сказать о ботулизме – токсикоинфекционном заболевании, при котором ботулотоксин, вырабатываемый бактериями Clostridium botulinum, блокирует проведение нервного импульса.
Во-вторых, изменения в нервно-мышечном соединении (синапсе). Например, выработка аутоантител к структурам синапса приводит к нарушению передачи нервного импульса с нервного волокна на мышечное.
Наконец, существует множество причин поражения непосредственно мышечного волокна при относительной сохранности нервных структур. Например, обширная группа наследственных заболеваний, в основе которых лежат мутации генов, определяющих структуру белков мышечных волокон, а также аутоиммунные заболевания, при которых неправильное функционирование иммунной системы приводит к выработке антител или размножению иммунных клеток, поражающих собственные ткани организма.
К заболеваниям, основным или второстепенным проявлением которых является мышечная слабость, относятся:
- наследственные мышечные дистрофии: дистрофия Дюшенна-Беккера, наследственная дилатационная кардиомиопатия и др.;
- наследственные миотонии, проявляющиеся нарушением расслабления мышц: миотония Томсена, миотония Беккера, периодические параличи;
- наследственные особенности нарушения биохимических процессов, протекающих в мышцах: болезни накопления липидов (нарушения липидного обмена), митохондриальные болезни (связанные с дефектами в функционировании митохондрий);
- воспалительные изменения, вызванные инфекциями и аутоиммунными заболеваниями (дерматомиозит, коллагенозы, саркоидоз);
- эндокринные заболевания, среди которых болезни щитовидной железы (гипо- и гипертиреоз), паращитовидных желез (гипо- и гиперпаратиреоз), гипофиза (болезнь Кушинга, акромегалия), надпочечников (синдром Кушинга, болезнь Аддисона, синдром Конна);
- побочное действие лекарственных средств, алкоголя, наркотиков;
- несбалансированная диета и дефицит витаминов и минералов, длительная рвота или диарея при кишечных инфекциях, приводящая к недостатку калия в организме;
- влияние факторов окружающей среды (хроническое воздействие на организм человека паров бензина, толуола);
- ботулизм;
- травматическое повреждение мышц, нервных стволов, головного и спинного мозга;
- нарушения кровоснабжения мышц при атеросклерозе, сердечно-сосудистой недостаточности;
- злокачественные опухоли и др.
- терапевт ;
- невролог ;
- эндокринолог ;
- ревматолог;
- инфекционист;
- генетик.
Первоначально стоит обратиться к врачу широкого профиля – терапевту, который сможет предположить поражение той или иной системы органов и направит вас к врачу-специалисту.
Диагностика синдрома мышечной слабости начинается с подробного опроса пациента, в ходе которого выясняют, в каких мышцах ощущается слабость, время ее появления, остроту, возможные провоцирующие факторы, сопутствующие признаки заболевания (боль, мышечные спазмы, нарушение дыхания, глотания, нарушения чувствительности и др.), наличие подобных симптомов у родственников пациента и т. д. Далее врач проводит тщательный осмотр и анализ двигательной активности при помощи различных диагностических упражнений и проверки рефлексов.
В связи с широчайшим спектром заболеваний, приводящих к развитию мышечной слабости, диагностика требует многих лабораторных и инструментальных обследований. Это:
- определение уровня мышечных ферментов, к которым относятся креатинфосфокиназа (КФК),
Синонимы: Анализ крови на креатинкиназу. CK; Creatine Phosphokinase (CPK). Краткая характеристика определяемого вещества Креатинкиназа Креатинкиназа катализирует обратимый перенос фосфорильного остатка с АТФ на креатин и с креатинфосфата на АДФ. Содержится преимущественно в скелетной мускулатуре.
Синонимы: Глутамино-щавелевоуксусная трансаминаза; Глутамат-оксалоацетат-трансаминаза сыворотки крови (СГОТ); L-аспартат 2-оксоглутарат аминотрансфераза; ГЩТ. Aspartateaminotransferase; Serum Glutamicoxaloacetic Transaminase; SGOT; GOT. Краткая характеристика определяемого вещества АсАТ .
Аланинаминотрансфераза − внутриклеточный фермент, участвующий в метаболизме аминокислот. Тест используют в диагностике поражений печени, сердечной и скелетных мышц. Синонимы: Глутамат-пируват-трансаминаза; Глутамат-пируват-трансаминаза в сыворотке; СГПТ. Alanine aminotransferase; S.
Синонимы: Анализ крови на ЛДГ; Лактатдегидрогеназа; L-лактат; НАД+Оксидоредуктаза; Дегидрогеназа молочной кислоты. Lactate dehydrogenase, Total; Lactic dehydrogenase; LDH; LD. Краткая характеристика определяемого вещества Лактатдегидрогеназа ЛДГ – цитоплазматический.
- определение концентрации электролитов в крови (кальция, калия), дисбаланс которых приводит к периодической или стойкой мышечной слабости;
Синонимы: Анализ крови на электролиты; Электролиты в сыворотке крови. Electrolyte Panel; Serum electrolyte test; Sodium, Potassium, Chloride; Na/K/Cl. Краткая характеристика определяемых веществ (Калий, Натрий, Хлор) Калий (К+) Основной внутриклеточный катион. Кал.
- иммунологическое исследование крови, цель которого – выявление антител (иммунных белков) как причины повреждения нервно-мышечных структур – антитела к ацетилхолиновому рецептору; антитела к скелетным мышцам IgG;
Серологический тест для диагностики миастении. Миастения представляет собой классическое аутоиммунное заболевание, обусловленное иммунной блокадой нервно-мышечного проведения, которое проявляется быстрой утомляемостью и мышечной слабостью. Заболевание имеет два возрастных пика, .
Серологический тест для диагностики паранеопластической миастении. Миастения является аутоиммунным неврологическим заболеванием, обусловленным иммунной блокадой нервно-мышечного проведения, которое проявляется быстрой утомляемостью и мышечной слабостью. У 20-40% пациентов с миастени.
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
Безопасное и информативное сканирование структур головного мозга для диагностики его патологий.
- анализ ДНК на наличие специфических мутаций, который проводится после обязательной консультации генетика.
В основе лечения мышечной слабости лежит терапия основного заболевания, вызвавшего появление данного симптома.
Терапия заключается в устранении причинного фактора, а при невозможности (в случае наследственных заболеваний) – в коррекции и компенсации нарушения работы мышц и внутренних органов.
В случае аутоиммунных заболеваний, являющихся причиной хронической мышечной слабости, пациенту назначают гормональные и цитостатические препараты, подавляющие выработку антител и клеточную агрессию к тканям собственного организма. При инфекционно-воспалительных процессах в мышцах проводят антибактериальную, противовирусную, противогрибковую или противопротозойную терапию в зависимости от возбудителя.
При миастении, вызванной действием аутоантител на нервно-мышечный синапс, применяют препараты, способствующие улучшению проведения нервного импульса к мышце, возможно удаление тимуса (вилочковой железы) – тимэктомия, при необходимости назначают терапию кортикостероидами и иммуносупрессорами.
Если причиной развития мышечной слабости являются нарушения функционирования эндокринных желез, то пациенту назначают препараты, возмещающие недостаток того или иного гормона или, наоборот, подавляющие избыточную активность эндокринной железы.
При врожденных миопатиях и миотониях, радикальное лечение которых пока невозможно, значительная роль отводится физиотерапии, лечебной гимнастике, ортопедическим приспособлениям. Из медикаментозных средств пациенту назначают препараты, увеличивающие силу мышц и нормализующие обмен веществ в мышечной ткани. При сопутствующих поражениях внутренних органов (в первую очередь сердечной мышцы) проводят коррекцию нарушений при помощи лекарственных средств, установки кардиостимулятора и т. д. Если это необходимо, то медикаментозно и при помощи диеты корректируют дисбаланс электролитов и других веществ.
В случае появления периодически возникающей или стойкой хронической мышечной слабости не стоит откладывать визит к врачу. Не стоит экспериментировать с самолечением, поскольку это может нанести непоправимый вред здоровью. Проанализируйте, какие изменения со стороны других органов предшествовали мышечной слабости, какие изменения в вашем образе жизни и диете произошли в последнее время.
При резко нарастающей мышечной слабости, зачастую начинающейся с мышц лица, нарушения зрения, глотания, затруднения дыхания в сочетании с признаками отравления (тошнота, рвота, боли в животе) после употребления консервированных в домашних условиях продуктов (особенно грибов) не исключено заражение ботулизмом.
![Признаки и симптомы ботулизма.jpg]()
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Мышечная дистрофия: причины появления, симптомы, диагностика и способы лечения.
Определение
Мышечные дистрофии - это большая группа наследственных заболеваний, которые характеризуются прогрессирующей слабостью и дегенерацией скелетных мышц, то есть потерей мышечной массы. К наиболее распространенным миодистрофиям относятся миодистрофия Ландузи-Дежерина (плече-лопаточно-лицевая миопатия), мышечная дистрофия Дюшенна и дистрофия Беккера. Также в эту группу входят дистрофия Эмери-Дрейфуса, миодистрофия Эрба-Рота и другие.
![Миодистрофия.jpg]()
Миодистрофия Дюшенна поражает в основном мальчиков, а распространенность этого заболевания составляет 3,3 на 100 000 населения, 1 из 3500 новорожденных мальчиков страдает данной патологией. Этот вид дистрофии часто выделяют в одну группу с миодистрофией Беккера (частота встречаемости 1 на 20 000 новорожденных). Миодистрофии Дюшенна и Беккера наследуются по Х-сцепленному рецессивному типу. Это означает, что повреждение находится в Х-половой хромосоме и передается от матери к сыну, а дочери являются носительницами и, как правило, сами не болеют.
Миопатия Ландузи-Дежерина (плече-лопаточно-лицевая миопатия) встречается с частотой 0,9-2 на 100 000 населения. Заболевание наследуется по аутосомно-доминантному, аутосомно-рецессивному (самый редкий) или Х-связанному типу. Для аутосомно-доминантного типа наследования достаточно одной копии дефектного гена от одного из родителей.
Частота развития мышечной дистрофии Эмери-Дрейфуса точно не известна, описано 7 генетических форм, но частота установлена лишь для одной из них - Х-сцепленной рецессивной формы, она составляет 1 на 100 000.
Причины появления мышечной дистрофии
Причиной развития разных миодистрофий являются патологии в генах - известно порядка 25 генов, ответственных за развитие врожденных миодистрофий.
При мышечной дистрофии Дюшенна вследствие мутации нарушается выработка белка дистрофина, который обеспечивает прочность, стабильность и функциональность мышечных волокон, и его нехватка приводит к повреждению мембран мышечных клеток (миоцитов).
Классификация заболеваний
Мышечные дистрофии могут классифицироваться в зависимости от того, какой белок подвергся мутации. Кроме того, их подразделяют по типу наследования: аутосомно-доминантные, аутосомно-рецессивные, Х-сцепленные.
Симптомы мышечной дистрофии
Мышечная дистрофия Дюшенна обычно манифестирует в возрасте 2-3 лет. Патологические процессы сначала происходят в мышцах ног, дети могут ходить на пальцах, вразвалку, отмечается избыточное выгибание позвоночника вперед – лордоз. Детям становится сложно бегать, прыгать, подниматься по лестнице, вставать с пола. Для разных типов миодистрофий характерным является симптом Говерса – вследствие слабости мышц бедер и тазового пояса больному, чтобы подняться из положения на корточках, приходится опираться руками об пол, затем подниматься, опираясь руками об колени. Мышечная слабость прогрессирует, у детей развивается сколиоз и сгибательные контрактуры – когда ребенок не может полностью разогнуть конечность. Дети часто падают, поэтому велик риск переломов рук или ног. Отдельные мышечные группы могут замещаться жировой или фиброзной тканью, в результате чего появляется псевдогипертрофия мышц, особенно заметная на лодыжках. Если страдает миокард (сердечная мышца), то существует предрасположенность к развитию нарушений ритма и проводимости сердца, а также дилатационной кардимиопатии (состояния, когда камеры сердца увеличены, а стенки истончены), приводящей к сердечной недостаточности.
![Сердце.jpg]()
В 20-30% случаев при мышечной дистрофии Дюшенна появляются нарушения интеллекта и памяти.
К 12 годам большинство детей вынуждено пользоваться инвалидной коляской. В возрасте 15-20 лет пациентам уже требуется респираторная поддержка, умирают больные миодистрофией Дюшенна от дыхательных или кардиальных осложнений в возрасте 12-25 лет.
Миодистрофия Беккера дебютирует в 10-20 лет и медленно прогрессирует, способность к самостоятельной ходьбе сохраняется в течение 15-20 лет от начала заболевания. Симптоматика схожа с миодистрофией Дюшенна, слабость распространяется на мышцы бедер, таза, плеч, пациенты ходят на носочках или вразвалку, также наблюдается гипертрофия мышц голеней.
Развитие заболевания очень индивидуально, некоторым пациентам требуется инвалидное кресло к 30 годам, некоторые длительное время обходятся тростью.
У пациентов с миодистрофией Беккера также отмечается поражение сердечной мышцы с развитием сердечной недостаточности.
Для миодистрофии Эмери-Дрейфуса характерны контрактуры локтевых и голеностопных суставов, возникающие в раннем детстве (укорочение ахилловых сухожилий приводит к тому, что ребенок не может опуститься на пятки), тугоподвижность позвоночника, медленно прогрессирующая слабость лопаточно-плечевых и тазово-перонеальных мышц (мышц бедра и голени), а также выраженная кардиомиопатия с нарушениями ритма и проводимости. Тяжесть заболеваний сердца часто определяет прогноз течения болезни вследствие высокой вероятности внезапной сердечной смерти или развития прогрессирующей сердечной недостаточности.
Диагностика мышечной дистрофии
Предварительный диагноз врач может установить уже при осмотре, наблюдая за попытками ребенка побежать, прыгнуть, подняться по ступенькам, встать с пола.
Для подтверждения диагноза проводятся:
-
Анализ крови на сывороточную креатинкиназу, АСТ, АЛТ.
Синонимы: Анализ крови на креатинкиназу. CK; Creatine Phosphokinase (CPK). Краткая характеристика определяемого вещества Креатинкиназа Креатинкиназа катализирует обратимый перенос фосфорильного остатка с АТФ на креатин и с креатинфосфата на АДФ. Содержится преимущественно в скелетной мускулатуре.
![Терапия]()
Сепсис – это серьезное заболевание, вызванное подавлением иммунного ответа на инфекцию. Более известное бытовое название сепсиса – заражение крови. Для борьбы с инфекцией организм вырабатывает химические вещества, которые могут вызвать сильное воспаление по всему организму. Это воспаление в свою очередь может привести к повреждению органов.
Свертывание крови при сепсисе уменьшает приток крови к конечностям и внутренним органам, лишая их питательных веществ и кислорода. В особо тяжелых случаях инфекция приводит к угрожающему жизни падению артериального давления. Это состояние называется септический шок, и оно действительно очень серьезно. Септический шок может быстро привести к отказу ряда органов – легких, почек и печени, вызывая смерть.
2. Причины и факторы риска
Бактериальные инфекции являются самой частой причиной сепсиса. Но сепсис может развиться и из-за других инфекций. Инфекция может начаться в любом месте – там, где бактерии или другие инфекционные агенты могут попасть в организм. Заражение крови может стать как результатом безобидной, на первый взгляд, царапины, так и следствием серьезной медицинской проблемы – аппендицита, пневмонии, менингита или инфекции мочевыводящих путей. Сепсис может появиться при инфекциях костей – остеомиелите.
Теоретически сепсис может развитья у любого человека. Но часть людей подвергается повышенному риску развития сепсиса. Среди них:
- Люди, чья иммунная система плохо функционирует из-за таких заболеваний, как ВИЧ/СПИД или рак. В эту же группу входят пациенты, для лечения которых используются наркотические препараты, подавляющие иммунную систему (например, для предотвращения отторжения пересаженных органов).
- Младенцы.
- Пожилые люди, особенно если у них есть проблемы со здоровьем.
- Госпитализированные в стационар пациенты, в том числе, которым делались инвазивные медицинские процедуры. По статистике, распространенными зонами первичной инфекции при сепсисе являются хирургические разрезы, мочевые катетеры и пролежни.
- Пациенты с сахарным диабетом.
3. Симптомы сепсиса
Поскольку сепсис может начаться в разных частях тела, симптомы сепсиса могут быть разными. Учащенное дыхание, изменение психического состояния (спутанность сознания, например) могут быть первыми признаками сепсиса. Другие общие симптомы сепсиса это:
- Лихорадка, высокая температура, озноб или наоборот, очень низкая температура тела;
- Редкое мочеиспускание;
- Учащенный пульс;
- Быстрое дыхание;
- Тошнота и рвота;
- Диарея.
4. Лечение болезни
Самое важное в лечении сепсиса – это быстрая диагностика. Если есть основания подозревать заражение крови, врач может провести исследования и тесты, чтобы обнаружить:
- Бактерии при анализе крови или других жидкостей организма;
- Источник инфекции с помощью рентгена, компьютерной томографии или УЗИ;
- Высокое или низкое количество лейкоцитов;
- Низкое содержание тромбоцитов;
- Низкое артериальное давление;
- Слишком большое количество кислоты в крови (ацидоз);
- Изменения в почках или работе печени.
В случаях с тяжелым сепсисом, как правило, требуется помещение пациента в реанимацию, где врачи пытаются остановиться инфекцию, поддержать работу жизненно- важных органов и регулировать артериальное давление.
Для лечения сепсиса обычно применяются:
- Антибиотики широкого спектра действия, которые способны убить многие виды бактерий;
- Терапия для поддержания артериального давления, в том числе – введение жидкости в организм;
- Кислородная терапия для поддержания нормального уровня кислорода в крови.
После того, как при заражении крови удается определить инфекционный агент, врачи могут начать лечение сепсиса с помощью специальных препаратов направленного действия. В зависимости от тяжести состояния пациента и последствий сепсиса может понадобиться искусственная вентиляция легких или почечный диализ. Иногда для лечения сепсиса и обработки зоны инфицирования необходима операция.
Сепсис, а тем более септический шок – очень опасные состояния. При септическом шоке выживаемость пациентов составляет в среднем 40%, при сепсисе – около 80%. У людей, которым удалось выжить после сепсиса, может развиться постоянное повреждение какого-то органа. Поэтому при малейшем подозрении на сепсис и заражение крови очень важно как можно быстрее получить квалифицированную медицинскую помощь.
Заболевания
![частые заболевания]()
Жалобы и симптомы
![Жалобы и симптомы]()
- Высокая температура тела
- Иммунитет снижен
- Боли различной локализации
- Резкое снижение или набор веса
- Плохая работы желудка тракта
- Частые ОРЗ, ОРВИ
- Слабость, головокружение, недомогания
Если вы обнаружили у себя подобные симптомы, возможно, это сигнал заболевания, поэтому рекомендуем проконсультироваться с нашим специалистом.
Диагностика
![Диагностика]()
- ЭКГ (электрокардиограмма)
- Общий анализ крови
- Биохимический анализ крови
- Общий анализ мочи
- Пульсоксиметрия
Наши цены
![Типичные жалобы]()
- Консультация терапевта - от 1500 р.
- Биохимический анализ крови (стандартная, 10 показателей) - 2470 р.
- Биохимический анализ крови (расширенаяая, 14 показателей) - 3565 р.
- Общий анализ крови - 675 р.
- ЭКГ (электрокардиография) - 1500 р.
- Общий анализ мочи - 320 р.
- Пульсоксиметрия - 500 р.
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Читайте также: