Может ли выходить слизь из за дисбактериоза
Обновлено: 24.04.2024
Симптомы
Тенезмы прямой кишки обычно сопровождаются сильными режущими или тянущими болями в нижней части живота. Боль является спастической, то есть возникает и угасает приступообразно.
Особенно интенсивно болезненность ощущается в районе сфинктера, где могут впоследствии появляться эрозии кожи и слизистой кишечника. При отсутствии лечения частота приступов способна увеличиваться, а интенсивность болей нарастать.
Из-за ложных позывов человек вынужден постоянно идти в уборную, однако акта дефекации не происходит. В процессе может выделяться небольшой объем кала, слизи или крови.
Причины появления тенезмов
В норме процесс испражнения запускается при раздражении стенок кишечника каловыми массами. В случае, если позывы имеются, а дефекации не происходит – кишечник раздражается по другим причинам. Рассмотрим основные причины ложных позывов к дефекации.
Геморрой
Геморроем называется патология, характеризующаяся образованием варикозно расширенных узлов вокруг прямой кишки. Заболевание сопровождается расширением и извилистостью вен, часто сопутствующим воспалительным процессом и тромбозом. Таким образом, ложные позывы в туалет возникают из-за выпячивания вен в просвет кишки.
К основным факторам возникновения геморроя относятся: гиподинамия, чрезмерные физические нагрузки и сидячая работа.
Синдром раздраженного кишечника
Синдром раздраженного кишечника можно заподозрить по интенсивным болям в области живота и нарушению стула. Часто при этом возникают болезненные тенезмы. Синдром раздраженного кишечника развивается на фоне стресса, неправильного питания и гормонального сбоя.
Проктит
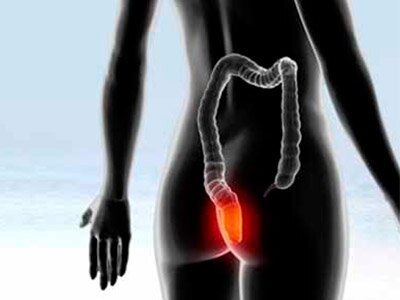
Проктитом называется хроническое воспаление слизистой кишечника. Болезнь сопровождается дискомфортом, болью, жжением и зудом в области прямой кишки, а также тенезмами. В каловых массах могут выявляться слизь, гной или кровь.
Болезнь развивается частом употреблении острых блюд, паразитарных заболеваниях, кишечных инфекциях, при злоупотреблении алкоголем
Сигмоидит
Сигмоидит – воспалительный процесс сигмовидной кишки. К основным симптомам заболевания относятся: боль с левой стороны нижней части живота, вздутие, жидкий стул с примесью слизи и ложные позывы. Появление тенезм сигнализирует об активном воспалительном процессе.
Заболевание возникает из-за аномального строения сигмовидной кишки, проникновения инфекции, раздражения или механического повреждения этого отдела кишечника.
Дисбактериоз
Одним из основных признаков дисбактериоза считаются болезненность живота, диарея, прожилки и сгустки крови в каловых массах. Помимо этого нередко возникают позывы к дефекации без кала. Болезнь обусловлена проникновением болезнетворных микроорганизмов в желудочно-кишечный тракт человека.
Анальные трещины
Данная патология чаще возникает у женщин и характеризуется повреждением кожи и слизистой анального отверстия. Возникновение трещин связано с запорами, воспалением ЖКТ и механическими травмами. Нередко патология развивается у женщин при беременности и родах.
Доброкачественные и злокачественные новообразования
Наиболее частыми образованиями, провоцирующими ложные позывы, являются:
- Полипы – опухолевидные новообразования слизистой оболочки кишечника. Могут быть единичными или множественными. В тканях активируется деление клеток, что сопровождается образованием полипов с атипией или без атипии.
- Аденомы – доброкачественные опухоли из железистой ткани.
- Аденокарцинома – раковые опухоли, развивающиеся из железистых клеток, выстилающих кишечник.
Иные причины
Также данное состояние может носить психологический характер. Тенезмы являются частым спутником стрессов, неврозов и в редких случаях нарушений работы нервной системы.
Диагностика
1. Лабораторная диагностика:
- Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с микроскопией мазка крови при выявлении патологических изменений)
- Копрограмма
- Анализ кала на скрытую кровь
- Исследование на лямблии (антигенный тест в кале) Giardia lamblia, антиген
- Скрининговое обследование на гельминтозы (Opisthorchis IgG, Toxocara IgG, Trichinella IgG, Echinococcus IgG)
Лабораторное исследование кала позволяет судить о характере патологического процесса в кишечнике. Так, например, выявление прожилок или сгустков крови может сигнализировать о тяжелом поражении кишечника.
2. Колоноскопия. Это эндоскопические методы диагностики, позволяющие осмотреть слизистую кишечника при помощи маленькой камеры, которая вводится через анальное отверстие. В ходе исследований врач может взять биопсию – небольшой фрагмент стенки кишечника для дальнейшей диагностики.
3. МРТ или КТ. Дополнительные инструментальные методы диагностики необходимы при сложных диагностических ситуациях. С их помощью врач послойно изучает структуру органов брюшной полости, тем самым определяя и уточняя локализацию патологических изменений.
Лечение
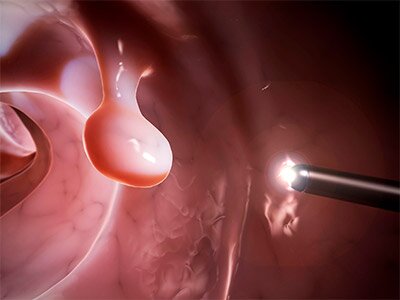
Лечение зависит от причины, вызвавшей ложные позывы к дефекации у мужчин и женщин. Внимательно изучив полученные в ходе исследований результаты, врачи нашей клиники индивидуально подбирают методы терапии. Может применяться консервативное (медикаментозное лечение) или могут потребоваться дополнительные процедуры.
Цель медикаментозной терапии – восстановить моторику кишечника, снять воспаление, устранить инфекцию и нормализовать микрофлору. Для этого врачи назначают противовоспалительные, антибактериальные, ранозаживляющие, противодиарейные или слабительные средства в виде таблеток, кремов или свечей. Кроме того, пациенту назначаются препараты, позволяющие уменьшить частоту и интенсивность позывов, а также снять болезненные ощущения.
В некоторых случаях может потребоваться проведение манипуляции – удаление полипов, удаление геморроя и др.
Неотъемлемой частью лечения тенезмов является соблюдение принципов правильного питания. Человеку необходимо употреблять достаточное количество питьевой воды (не менее 1,5 л), исключить кислые, острые, сильносоленые, копченые и жареные блюда, раздражающие слизистую кишечника. Рекомендуется дробное питание небольшими порциями 5-6 раз в день. Рацион должны составлять супы, каши, нежирное мясо в отварном или тушеном виде.
Куда обратиться при ложных позывах?
Записаться на прием можно по контактным телефонам клиники или оставив заявку предварительной записи.
Изучение микрофлоры кишечника началось в 1886 г., когда F. Escherich описал кишечную палочку (Bacterium coli communae). В 1908 году Нобелевский лауреат русский ученый Илья Ильич Мечников доказал необходимость кишечных бактерий для здоровья и долголетия. К
Изучение микрофлоры кишечника началось в 1886 г., когда F. Escherich описал кишечную палочку (Bacterium coli communae). В 1908 году Нобелевский лауреат русский ученый Илья Ильич Мечников доказал необходимость кишечных бактерий для здоровья и долголетия. К настоящему времени в кишечнике здорового человека установлено наличие 500 видов микробов. Нормальная микробная флора является одним из барьеров на пути бактерий, попадающих в кишечник. Она стимулирует иммунную защиту, увеличивает секрецию IgA в просвет кишки. Кишечные палочки, энтерококки, бифидобактерии, ацидофильные палочки обладают антагонистическими свойствами и способны подавлять рост патогенных микроорганизмов. Нарушение состава микрофлоры приводит к снижению сопротивляемости организма кишечным инфекциям.
Различают мукоидную микрофлору (М-микрофлора) — микроорганизмы, ассоциированные со слизистой оболочкой кишечника, и полостную микрофлору (П-микрофлору) — микроорганизмы, локализующиеся в просвете кишечника.
По отношению к макроорганизму представителей кишечного биоценоза делят на 4 группы:
облигатная микрофлора (основная микрофлора кишечника — бифидобактерии, лактобациллы, нормальные кишечные палочки, пропионобактерии, пептострептококки, энтерококки);
факультативная (условно-патогенные и сапрофитные микроорганизмы — бактероиды, стафилококки, стрептококки, пептококки, дрожжеподобные грибы, вейонеллы, фузобактерии, бациллы);
транзиторная (случайные микроорганизмы, не способные к длительному пребыванию в организме, — флавобактерии, псевдомонады);
При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями, улучшая трофику слизистой оболочки. Недостаточное количество клетчатки в диете ведет к снижению синтеза короткоцепочечных жирных кислот. В результате возникают дистрофические изменения эпителия и повышается проницаемость кишечного барьера для антигенов пищевого и микробного происхождения.
Под влиянием микробных ферментов в подвздошной кишке происходит деконъюгация желчных кислот (ЖК) и преобразование первичных ЖК во вторичные ЖК. В физиологических условиях 80–95% ЖК реабсорбируется, остальные выделяются с калом в виде метаболитов. Последние способствуют формированию каловых масс, тормозят всасывание воды, препятствуя излишней дегидратации кала. Избыточное бактериальное обсеменение тонкой кишки ведет к преждевременной деконъюгации ЖК и секреторной диарее.
Таким образом, морфологическое и функциональное состояние кишечника зависит от состава его микрофлоры.
В тощей кишке здоровых людей находится до 100 000 бактерий в 1 мл содержимого. Основную часть их составляют стрептококки, стафилококки, молочнокислые палочки. В дистальном отделе подвздошной кишки количество микробов увеличивается за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий.
Микробный состав кала не отражает полную картину кишечного биоценоза, не дает оперативной информации о составе микроорганизмов в кишечнике. На практике учитываются данные лишь о 15–20 видах микробов, содержащихся в кале. Обычно исследуют количество бифидобактерий, лактобацилл, энтеробактерий, кишечных палочек, протея, энтерококка, золотистого стафилококка, синегнойной палочки и кандид.
Степень тяжести дисбиоза определяется степенью снижения бифидобактерий и других облигатных микроорганизмов и повышения числа условно-патогенных и патогенных видов.
I степень — снижение количества облигатных представителей (бифидобактерий и/или лактобацилл) на 1–2 порядка, без увеличения условно-патогенной микрофлоры (УПМ), нарастание количества УПМ при нормальном числе бифидобактерий. II степень — умеренное или значительное снижение числа бифидобактерий, сочетающееся с выраженными изменениями аэробной микрофлоры (редукция лактобацилл, появление измененных форм кишечной палочки, УПМ в высоких количествах). III степень — большое количество УПМ как одного вида, так и в ассоциациях, выделение патогенных микроорганизмов (Мехтиев С. Н., Гриневич В. Б., Захаренко С. М.).
В клинике дисбиоза выделяют следующие ключевые синдромы:
интестинальный синдром (вздутие живота, урчание кишечника, склонность к запорам или жидкий стул с непереваренными остатками пищи);
вторичный синдром мальабсорбции (упорная диарея с нарушением всасывания моносахаридов, электролитов),
Новые подходы в диагностике дисбиоза
Альтернативу рутинным бактериологическим исследованиям составляют химические методы дифференциации микроорганизмов и, в частности, газовая хроматография (ГХ) в сочетании с масс-спектрометрией (ГХ-МС). Метод основан на определении компонентов бактериальных клеток, появляющихся в результате их естественного отмирания или атаки иммунной системы. В качестве маркеров используют минорные липидные компоненты мембран микробов. По их содержанию можно в течение нескольких часов определить до 170 видов бактерий и грибов в различных биосредах.
Почти 50% биомассы пристеночной микрофлоры составляют актиномицеты, занимающие промежуточное положение между бактериями и грибами. Около 25% микробной флоры представлено аэробными кокками (стафилококки, стрептококки, энтерококки и коринеформные бактерии). Число бифидо- и лактобацилл колеблется от 20 до 30%. Другие анаэробы (пептострептококки, бактероиды, клостридии, пропионобактерии) составляют около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной численности микрофлоры слизистой оболочки.
До 90–95% микробов толстой кишки составляют анаэробы (бифидобактерии и бактероиды) и только 5–10% всех бактерий — строгая аэробная и факультативная флора (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Свойства микробов, населяющих кишечник, не всегда учитываются при назначении антибиотиков. Антибактериальные препараты подавляют рост не только патогенных микроорганизмов, но и нормальную микрофлору. В результате размножаются сапрофитные микробы с высокой устойчивостью к лекарственным препаратам, приобретающие патогенные свойства.
Диарея, ассоциированная с применением антибиотиков
У больных, получающих антибактериальную терапию, может развиваться диарея, вызванная дисбиозом кишечника (ААД — антибиотик-ассоциированная диарея). Частота такой диареи колеблется в пределах 5–25%. Причиной ее является снижение количества микробов, чувствительных к антибиотику, и появление резистентных штаммов, отсутствующих в норме. Наиболее известным представителем таких микроорганизмов является патогенный штамм Clostridium difficile (Cl. difficile), но причиной диареи, ассоциированной с антибиотиками, могут быть и другие микробы, способные усиливать секрецию ионов и воды, повреждать стенку кишки. Это стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка, клебсиелла. По типу диареи ААД обычно относят к секреторному и воспалительному типам.
Антибиотик-ассоциированную диарею наиболее часто вызывают линкомицин, ампициллин, клиндамицин, бензилпенициллин, цефалоспорины, тетрациклины, эритромицин. Способ введения антибиотика не имеет большого значения. При приеме внутрь помимо эрадикации микроорганизмов происходит воздействие антибиотика на слизистую оболочку тонкой кишки. При парентеральном введении антибиотики воздействуют на биоценоз кишечника, выделяясь со слюной, желчью, секретами тонкой и толстой кишок.
Симптомы ААД у большинства больных обычно появляются во время лечения, а у 30% — в пределах 7–10 дней после его прекращения.
Этиологическим фактором ААД большинство исследователей считают клостридии, в частности Cl. difficile. Среди взрослого населения уровень ее носительства низкий и равен 2–3%. Условиями размножения Cl. difficile являются анаэробная среда и угнетение нормальной микрофлоры кишечника.
Клинические проявления ААД варьируют от легкой диареи до тяжелого псевдомембранозного колита (ПМК). ПМК — острое заболевание кишечника, являющееся осложнением антибактериальной терапии. Установлено, что его вызывает Cl. difficile.
Симптоматика
Основным симптомом ААД является обильная водянистая диарея, началу которой предшествует назначение антибиотиков в течение нескольких дней и более. Затем появляются схваткообразные боли в животе, стихающие после стула. В случаях, когда возникает лихорадка, в крови нарастает лейкоцитоз, а в кале появляются лейкоциты, нужно заподозрить ПМК.
После отмены антибиотика у ряда больных симптомы быстро исчезают. При ПМК, несмотря на прекращение антибиотикотерапии, в большинстве случаев частота стула растет, появляются дегидратация и гипопротеинемия. В тяжелых случаях быстро наступает обезвоживание, развиваются токсическое расширение и перфорация толстой кишки, возможен летальный исход.
Диагноз
Диагноз ААД устанавливают на основании связи диареи с применением антибиотиков. Диагноз ПМК подтверждается бактериологическим исследованием кала и определением в нем токсина Cl. difficile. Частота обнаружения токсина в кале больных с ААД не превышает 15%.
У больных диареей, ассоциированной с Cl. difficile, наблюдается значительный лейкоцитоз. Имеются данные, что у больных с лейкоцитозом 15800 и выше высока вероятность развития ПМК, вызванного Cl. difficile. Это объясняется тем, что токсин А, выделяемый Cl. difficile, вызывает воспаление, секрецию жидкости, лихорадку и судороги. Поэтому у всех больных с ААД, протекающей с интоксикацией и лейкоцитозом 15800 и выше, следует считать причиной диареи Cl. difficile.
Парфенов А. И., Осипов Г. А., Богомолов П. О применили метод ГХ-МС для оценки состава микробной флоры тонкой кишки у 30 больных ААД и установили, что диарея может быть связана не только с инфекционным агентом (Cl. difficile), но с существенным изменением нормальной микрофлоры в сторону увеличения численности от 7 до 30 из 50 контролируемых микроорганизмов. При этом общая колонизация тонкой кишки увеличивается в 2–5 раз по сравнению с нормой.
У больных ААД чаще всего морфологические изменения толстой кишки отсутствуют. В тяжелых случаях при эндоскопии выявляют 3 типа изменений: 1) катаральное воспаление (отек и гиперемия) слизистой оболочки; 2) эрозивно-геморрагическое поражение; 3) псевдомембранозное поражение.
Дифференциальный диагноз
Связь диареи с антибиотикотерапией обычно не создает трудностей в диагностике ААД. В тяжелых случаях картина ПМК может напоминать холеру или фульминантную форму язвенного колита, болезнь Крона. Однако для последних характерна более или менее выраженная кровавая диарея, нехарактерная для ПМК. Тем не менее возможность развития эрозивно-геморрагических изменений слизистой оболочки при ААД не исключает появления кровянистых выделений из прямой кишки у некоторых больных.
Лечение ААД
Этиотропной терапией ААД и ПМК, вызванных Cl. difficile, большинство авторов считает назначение ванкомицина и метронидазола (трихопола, метрогила).
Немедленно отменяют антибиотик, вызвавший диарею. Назначают ванкомицин в начальной дозе 125 мг внутрь 4 раза в сутки, при необходимости дозу увеличивают до 500 мг 4 раза в сутки. Лечение продолжают в течение 7–10 сут. Метронидазол дают по 0,5 г внутрь 2 раза в сутки (или по 0,25 г 4 раза в сутки).
Применяют также бацитрацин по 25 тыс. ME внутрь 4 раза в сутки. Лечение проводят в течение 7–10 сут. Бацитрацин почти не всасывается, в связи с чем в толстой кишке создается высокая концентрация препарата. При обезвоживании применяют инфузионную терапию и оральную регидратацию (Регидрон, Цитроглюкосолан). Для связывания токсина А назначают Холестирамин.
Поскольку количество микробов, обеспечивающих лечебный эффект, на несколько порядков превышает дозы обычных бакпрепаратов, обсуждается вопрос о локальной доставке пробиотиков в кишечник. Это можно делать с помощью клизм на основе солевых растворов, через назодуоденальный зонд или колоноскоп. Привлекает внимание последний способ, т. к. как при этом пробиотики вводятся непосредственно в проксимальный отдел ободочной кишки.
Линекс содержит молочнокислые бактерии, резистентные к действию антибиотиков. Взрослым и детям старше 12 лет назначают по 2 капсулы 3 раза/сут после еды, запивая небольшим количеством жидкости. Длительность лечения составляет в среднем 1–2 мес. При применении препарата в рекомендуемых дозах побочное действие не отмечено. Противопоказания — повышенная чувствительность к компонентам препарата или молочным продуктам. Проведенные исследования не выявили наличия у Линекса тератогенного действия, не сообщалось об отрицательном влиянии препарата при беременности и в период лактации. Для сохранения жизнеспособности компонентов препарата не рекомендуется запивать Линекс горячими напитками, следует воздерживаться от употребления алкоголя.
Клинические проявления аллергии на молочнокислые бактерии сходны с проявлениями аллергии на молочные продукты, поэтому при появлении симптомов аллергии прием препарата следует прекратить для выяснения ее причин. О случаях передозировки Линекса не сообщалось. Не отмечено его нежелательного взаимодействия с другими препаратами. Состав препарата Линекс позволяет принимать его одновременно с антибактериальными средствами.
Для симптоматического лечения диареи применяются также: адсорбент аттапульгит, по 1,2–1,5 г после каждого жидкого стула; лоперамид, 2–4 мг внутрь после каждой дефекации (не более 8 мг/сут); дифеноксилат/атропин (Ломотил), 5 мг внутрь 4 раза в сутки до прекращения поноса; настойка белладонны, 5–10 капель внутрь 3 раза в сутки перед едой; гиосциамин (Левсин) 0,125 мг под язык по мере необходимости или по 0,375 мг внутрь 2 раза в сутки; спазмолитик дицикловерин, 20 мг внутрь 4 раза в сутки; кодеин, 30 мг внутрь 2–4 раза в сутки; октреотид (100–600 мг/сут п/к в 2–4 приема) — синтетический аналог соматостатина; энтеросорбенты (Смекта, Эспумизан).
Лечение собственно дисбиоза
Стандартная терапия дисбиоза нацелена на устранение избыточного бактериального обсеменения тонкой кишки, восстановление нормальной микрофлоры, улучшение кишечного пищеварения и всасывания, восстановление моторики кишечника и повышение иммунореактивности организма.
Антибактериальные препараты применяют по показаниям для подавления роста патогенной микрофлоры в тонкой кишке. Обычно назначают антибиотики из группы фторхинолонов, пенициллинов, цефалоспорины, тетрациклины или метронидазол. Препараты принимают внутрь в обычных дозах в течение 7–10 дней.
Оптимальным является использование средств, оказывающих минимальное влияние на симбионтную микрофлору и подавляющих рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов. К ним относятся антисептики: Интетрикс, Энтерол, Бактисубтил, Нифуроксазид и др. При тяжелых формах стафилококкового дисбиоза применяют антибиотики: офлоксацин, оксациллин, амоксициллин. Их назначают на срок 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение натамицина, флуконазола и иных микостатиков.
Бактериальные препараты (пробиотики) можно назначать без предварительной антибактериальной терапии или после нее. Применяют Бифидумбактерин, Пробифор, Бификол, Лактобактерин, Линекс, Бифиформ, Нормофлорины Л, Д, Б, Полибактерин, Наринэ, Аципол, Нутролин В, Тревис.
Еще один способ лечения дисбиоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов (пребиотиками). Один из таких препаратов — Хилак-форте, стерильный концентрат продуктов обмена веществ нормальной микрофлоры: молочная кислота, лактоза, аминокислоты и жирные кислоты. Эти вещества способствуют восстановлению биологической среды в кишечнике, необходимой для существования нормальной микрофлоры, подавляют рост патогенных бактерий, улучшают трофику и функцию эпителиоцитов и колоноцитов. Один миллилитр препарата содержит биологически активные вещества 100 миллиардов нормальных микроорганизмов. Хилак-форте назначают по 60 капель 3 раза в день на срок 4 нед в сочетании с антибактериальными препаратами или после их применения.
Кроме того, применяется сироп лактулозы (Дюфалак, Порталак), подкисляющий кишечный сок и угнетающий рост патогенной микрофлоры. Активное вещество — синтетический дисахарид, который не гидролизуется в тонкой кишке и поступает в ободочную кишку в неизмененном виде, где расщепляется под действием флоры толстой кишки с образованием низкомолекулярных органических кислот, что приводит к снижению рН содержимого кишечника.
Под действием препарата увеличивается поглощение аммиака толстой кишкой и выведение его из организма, стимулируется рост ацидофильных бактерий (в т. ч. лактобактерий), подавляется размножение протеолитических бактерий и уменьшается образование азотсодержащих токсических веществ. Клинический эффект наступает через 2 дня лечения. Препарат в форме сиропа для приема внутрь назначают взрослым в дозе 15–45 мл/сут, поддерживающая доза равна 10–25 мл/сут. Препарат следует принимать 1 раз/сут утром во время еды, с водой, любой другой жидкостью или пищей.
Побочное действие со стороны пищеварительной системы: в первые дни — метеоризм (проходящий самостоятельно через 2 дня); при длительном применении в высоких дозах возможны боли в области живота, диарея. Противопоказания: галактоземия; непроходимость кишечника; повышенная чувствительность к компонентам препарата. Лактулозу можно применять при беременности и в период лактации по показаниям. Препарат следует с осторожностью назначать больным сахарным диабетом.
Из других пребиотиков нужно отметить кальция пантотенат (участвует в процессах ацетилирования и окисления в клетках, углеводном и жировом обмене, синтезе ацетилхолина, утилизируется бифидобактериями и способствует увеличению их массы), аминометилбензойную кислоту (Памба, Амбен) — ингибитор фибринолиза, подавляет протеолитические ферменты условно-патогенных бактерий, стимулируя рост нормальной микрофлоры, лизоцим (обладает бифидогенным, иммуномодулирующим, противовоспалительным действием, улучшает пищеварение, подавляет патогенную флору).
В лечении дисбиоза рекомендуется использовать фитопрепараты. Они являются кишечными антисептиками, подавляют патогенную и сохраняют сапрофитную микрофлору. Фитосборы нормализуют аппетит, улучшают пищеварение, моторику кишечника, оказывают противомикробное и иммуномодулирующее действие, способствуют регенерации слизистой оболочки. Выраженный бактерицидный эффект дают зверобой, календула, эвкалипт, тысячелистник, лапчатка, шалфей, душица, брусника, подорожник. Иммунокорригирующее действие оказывают крапива, мелисса, мать-и-мачеха, подорожник, фиалка трехцветная, череда. Богаты витаминами брусника, крапива, малина, смородина, рябина, шиповник.
Больным с нарушенным полостным пищеварением назначают панкреатические ферменты (Креон, Панцитрат). С целью улучшения функции всасывания используют Эссенциале форте Н, лоперамид (Имодиум) и тримебутин.
Для повышения реактивности организма ослабленным больным при тяжелом дисбиозе целесообразно назначать Анаферон, Иммунал, Ликопид и другие иммуномодуляторы. Курс лечения должен продолжаться в среднем 4 нед. Одновременно назначают витаминно-минеральные комплексы (Витаминерал, Алфавит и др.).
По вопросам литературы обращайтесь в редакцию.
В. В. Скворцов, доктор медицинских наук
ВолГМУ, Волгоград
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 10 14 , что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 10 11 бактерий, что составляет 30% сухого остатка кишечного содержимого.
Нормальная микробная флора кишечника
В тощей кишке здоровых людей находится до 10 5 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 10 7 –10 8 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 10 11 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м 2 . Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические особенности дисбактериоза
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В 12 -дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
Лечение
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Выделения из заднего прохода могут быть симптомом серьезных патологий органов ЖКТ. В норме кишечник способен вырабатывать небольшое количество слизи для обеспечения легкого продвижения каловых масс. Однако если выделения из прямой кишки стали содержать кровь, гной и другие патологических вещества – это признак наличия воспалительного процесса в организме.
Причины
В некоторых случаях выделения из ануса считаются вполне физиологичным явлением и не требуют медицинского вмешательства. Так, слизь может появляться у новорожденных детей по причине незрелости пищеварительного тракта. У взрослых слизь с заднего прохода может выделяться при заболеваниях дыхательной системы (выделения образовываются в дыхательных путях, через пищевод попадают в кишечник и выходят через толстую кишку при дефекации).
Помимо этого причина выделений из заднего прохода у мужчин и женщин может скрываться в большом употреблении в пищу некоторых продуктов (например, бананы, рисовая или овсяная каши).
При частом образовании слизи необходимо своевременно обратиться за консультацией в медицинское учреждение, так как это может оказаться симптомом опасных заболеваний:
- неспецифический язвенный колит;
- болезнь Крона;
- геморрой; ;
- опухолевые образования;
- параректальные свищи и другие.
Симптомы патологии
Выделения из заднего прохода могут носить разнообразный характер. Так, у одних пациентов выделения встречаются только в кале, а у других – могут постоянно выходить из анального отверстия.
Также отличается характер самой слизи. Она может быть однородной или содержать хлопьевидные вкрапления, прожилки и сгустки. Оттенок может быть прозрачным, мутным, зеленоватым или беловатым. При воспалении геморроидальных узлов может выделяться слизь из прямой кишки с кровью. Также слизь с кровью из заднего прохода может сигнализировать о наличии новообразований.
При поражении грибковой инфекцией выделения могут содержать белые примеси. Мутные желто-зеленые выделения – признак гнойной инфекции, а оранжевый оттенок и резкий запах – нередко указывают на заболевания печени или избыточной выброс желчи в кишечник.
Диагностика и лечение
Выделения из ануса являются серьезным поводом для обращения к врачу. Игнорирование проблемы может стать причиной различных осложнений, вплоть до летального исхода. Ранняя диагностика позволит обнаружить заболевание на начальной стадии, что обеспечит более простое и результативное лечение.
Так как слизь с кровью при дефекации может быть симптомом опасных болезней, пациенту назначается комплексное обследование, включающее следующие методы:
- Осмотр и пальпация – исследования, необходимые для выявления новообразований, воспалений и изменений структуры тканей кишечника. – лабораторное исследование содержимого каловых масс с целью выявления наличия лейкоцитов, эритроцитов, слизи и других примесей для определения заболевания, вызвавшего патологию.
- Бактериологический посев – развернутый анализ для установления наличия разнообразных возбудителей болезней бактериальной природы. – анализ, назначающийся при подозрении на наличие глистов в организме. (колоноскопия) – осмотр слизистой толстой кишки для обнаружения язвенных участков, источника кровотечения, доброкачественных или злокачественных новообразований.
Помимо этого могут назначаться дополнительные исследования: рентгенография с контрастом, МРТ, КТ.
Лечение подбирается в зависимости от причины возникновения патологии. Основная цель терапии – устранение не только симптома, но и заболевания, послужившего началом появления выделения из заднего прохода.
Хирургическое вмешательство проводится в том случае, если болезнь зашла слишком далеко, или консервативное лечение не оправдало ожиданий.
Рекомендации специалиста

После проведения диагностики, врачи нашей клиники дают все необходимые рекомендации по результативному лечению патологии и профилактике возможных рецидивов.
Для того, чтобы не допустить повторного появления слизи с кровью из прямой кишки, а также заболеваний желудочно-кишечного тракта, пациенту необходимо придерживаться следующих рекомендаций:
Если у вас появились неприятные симптомы, не медлите, обратитесь к врачу! Современное диагностическое оборудование, индивидуальный подход и внимательное отношение помогут верифицировать проблему и избавиться от нее в минимальные сроки.
Записаться к врачу – гастроэнтерологу, проктологу можно позвонив по контактным телефонам или оставив онлайн заявку на предварительную запись.
Физические и химические характеристики кала могут многое рассказать о состоянии здоровья человека, в частности, о работе его пищеварительного тракта. При однообразном образе жизни и питания стул стабилен, имеет почти одинаковый цвет, оттенок которого меняется незначительно. Резкая смена окраса требует внимания, поскольку может сигнализировать о серьезных нарушениях в организме. Особенно насторожиться стоит, если кал поменял цвет на черный. В ряде случаев такой окрас связан с серьезными патологиями пищеварительного тракта. Промедление с их лечением может стоить человеку жизни.
Каким должен быть кал здорового человека?
Каловые массы формируются из химуса (пищевого комка) в результате его ферментативной обработки. Качество преобразования и усвоения еды зависит от активности пищеварения, которое включает множество факторов (активность секреции органов ЖКТ, моторика, состав рациона). Образование стула завершается в кишечнике. После полной обработки каловые массы покидают организм в виде оформленных элементов различных оттенков коричневого (от желтоватого до темно-коричневого). В норме стул должен быть регулярным и ежедневным (от 2 раз в день до 1 раза в 2 дня).
При изменении рациона и режима питания, избытке отдельных категорий продуктов, употреблении экзотической еды параметры кала меняются. Возможно изменение цвета, консистенции, запаха, появление небольшого количества непереваренных частиц, что считается нормой. Эти явления обусловлены особенностями пищеварения отдельных продуктов.
Серьезные изменения цвета и консистенции могут свидетельствовать о сбоях в работе желудочно-кишечного тракта, недостаточной выработке пищеварительных соков (соляной кислоты, панкреатического сока, желчи), дисбалансе микрофлоры кишечника. Установить причины помогает обследование, назначенное гастроэнтерологом, в первую очередь много информации предоставляет копрограмма (развернутый анализ кала).
Слишком темные каловые массы — это отклонение от физиологической нормы. Симптом требует пристального внимания и детального изучения вопроса, почему кал имеет черный цвет. Важно в кратчайшие сроки исключить опасные для жизни причины.
Возможные причины появления черного стула?
Основные причины изменения цвета кала, следующие:
- употребление специфических продуктов;
- прием лекарственных препаратов;
- побочные эффекты некоторых медикаментов;
- развитие заболеваний желудочно-кишечного тракта.
Ниже рассмотрим особенности проявления симптома при каждой из перечисленных причин.
Как меняет цвет кала еда

Первым делом стоит рассмотреть, в каких случаях черный цвет кала не является опасным симптомом. Потемнение экскрементов чаще всего связано с употреблением особых видов пищи, которые либо прямо окрашивают стул, либо меняют свои свойства в процессе переваривания. Каловые массы могут стать непривычно темными после употребления следующих продуктов:
- столовая свекла;
- темные ягоды (ежевика, смородина, черника);
- чернослив;
- виноград;
- крепкий кофе и чай;
- гранат;
- томаты;
- мясо слабой и средней прожарки;
- печень.
На фоне употребления перечисленных продуктов потемнение стула наблюдается спустя 1-2 дня. Симптом сохраняется 1-3 суток. После исключения продукта кал приобретает обычный цвет.
Как правило, почернение фекалий не сопровождается резким изменением консистенции стула, экскременты остаются оформленными. При обильном употреблении продуктов-провокаторов может развиваться послабляющий эффект или запор. Если темный окрас стула связан с присутствием в меню специфических продуктов или блюд, общее состояние пациента не меняется и других жалоб не возникает.
Какие медикаменты могут изменить цвет стула
Спровоцировать изменение цвета стула, вплоть до полностью черного, способны некоторые медикаменты. Дело в том, что в процессе продвижения по пищеварительному тракту, лекарственные препараты подвергаются воздействию пищеварительных соков. Это может сказаться на свойствах фармакологически активных веществ. Почернение стула наблюдается при приеме препаратов следующих групп:
- противоанемические (средства на основе железа);
- обволакивающих (препараты висмута, например Де-Нол);
- витаминно-минеральные комплексы (с железом в составе).
Если симптом спровоцирован лекарственным препаратом, беспокоиться не о чем. Вскоре после отмены медикамента кал приобретает привычную окраску. Желательно прочитать инструкцию и убедиться в способности средства изменять цвет экскрементов. Нужно учитывать, что никаких проявлений (кроме симптомов основного заболевания) быть не должно.
Придать фекалиям черную окраску способен активированный уголь и препараты на его основе. Окрашивание обусловлено выведением из организма вещества в неизмененном виде. Как правило, через день после отмены препарата цвет кала становится нормальным.
Побочные эффекты лекарств
Причиной выделения черного кала может быть прием медикаментов, способных спровоцировать внутреннее кровотечение. К таковым относят:
- нестероидные противовоспалительные средства;
- антиагреганты на основе ацетилсалициловой кислоты;
- некоторые антибиотики.
В данном случае могут меняться другие физические характеристики стула (консистенция, частота), а также общее самочувствие пациента. Признаками внутренних кровопотерь являются слабость, сонливость, бледность кожных покровов, тошнота, рвота, снижение аппетита и пр.
Если в недавнем времени человек принимал препараты из перечисленных групп, и стул внезапно потемнел, необходимо в ближайшее время обратиться к врачу. С целью диагностики внутреннего кровотечения будет назначено дополнительное обследование, т.к. такая ситуация требует оказания экстренной помощи.
При каких заболеваниях чернеет кал
Наиболее опасным вариантом является черный кал, как симптом развивающегося заболевания. Он указывает на внутреннее кровотечение на уровне пищевода, желудка или начальных отделов толстого кишечника. Гораздо реже кровь попадает в пищеварительный тракт при заболеваниях ЛОР-органов и респираторной системы. Клиника обусловлена преобразованием гемоглобина крови в гемин под действием соляной кислоты желудка. Черный кал у человека говорит о довольно массивной кровопотере (более 60 мл), поэтому обращение к врачу обязательно.
Стул при кровотечении меняет не только цвет, но и консистенцию. Экскременты становятся неоформленными, вязкими и липкими, напоминая деготь. Симптом может сопровождать следующие патологии:
- острый эрозивный эзофагит;
- узелковый периартериит;
- разрыв аневризмы аорты в просвет тонкого кишечника;
- гастрит;
- язвенная болезнь желудка и 12-перстной кишки;
- синдром Меллори-Вейса;
- опухоли желудка;
- геморрагическая лихорадка;
- брюшной тиф;
- лихорадка Денге;
- гемофилия;
- тромбоцитопения;
- анкилостомидоз;
- гистоплазмоз;
- цирроз печени;
- острый лимфобластный лейкоз и пр.
Опасные формы внутренних кровотечений сопровождаются тошнотой и рвотой (с алым или кофейным цветом масс), общей слабостью, снижением артериального давления, частоты пульса. Внутренним кровотечениям при инфекционных заболеваниях сопутствует повышение температуры тела, потливость, озноб.
При наличии одного из перечисленных заболеваний или сочетании черного стула с общим ухудшениям состояния, необходимо незамедлительно обратиться за помощью в медицинское учреждение.
Черный кал у ребенка – норма или патология?
Заболевания, которые провоцируют внутренние кровотечения, крайне редко диагностируют у детей. На серьезные проблемы со здоровьем указывает присутствие и других симптомов (лихорадка, боль в животе, слабость, рвота и пр.) В таких ситуациях следует без промедления обращаться за медицинской помощью.
В большинстве случаев потемнение детского стула обусловлено особенностями питания или применением лекарственных препаратов. Из-за сниженной активности ферментов возможно неполное переваривание отдельных продуктов и изменение их цвета в результате взаимодействия с пищеварительными соками. Примером может быть тревога родителей по поводу небольших черных волокон в кале, которые часто принимают за паразитов. На самом деле это частицы банана, которые не полностью переварились.
Черный, с зеленоватым оттенком стул у новорожденных является нормой. Это меконий или содержимое кишечника, которое образовалось в процессе внутриутробного развития. С началом употребления материнского молока или детской смеси, фекалии приобретают характерный для грудничкового возраста окрас (горчичный, светло-коричневый или желтоватый).
Не стоит беспокоиться по поводу цвета стула в случаях, если ребенок принимает поливитаминный комплекс или препараты железа. Изменение окраса кала в данной ситуации также является нормой.
Черный стул при беременности

Темный стул у беременной женщины может возникать на фоне лечения анемии препаратами железа или изменений в меню. Это абсолютно нормально и не несет угрозы здоровью матери или малыша.
При появлении черных фекалий следует насторожиться, если в анамнезе девушки есть заболевания пищеварительного тракта, печени или крови. Беременность в разы повышает нагрузку на женский организм, что может приводить к обострению хронических патологий. При внезапном почернении кала в сочетании с неудовлетворительным самочувствием необходимо обратиться к акушеру-гинекологу, который наблюдает за течением гестационного процесса.
Что делать, если почернел кал?
Оформленный черный кал у взрослого или ребенка не должен быть поводом для паники. С этим явлением можно разобраться самостоятельно в несколько этапов:
- Нужно проанализировать состояние человека на данный момент. Если есть тревожные симптомы — вызвать скорую помощь или доставить в больницу собственными силами.
- Если пациент остается дома, необходимо спросить его или вспомнить самостоятельно особенности самочувствия в последние несколько недель (были ли какие-то симптомы, обнаружены ли заболевания, проводилось ли лечение медикаментами). Если ответ утвердительный, необходимо обратиться в клинику. Если человек чувствовал и чувствует себя нормально, можно перейти к следующему шагу.
- Уточнить, какие медикаменты пациент принимает на регулярной основе или принимал в последнее время. В случае употребления препаратов, способных спровоцировать внутреннее кровотечение, следует обратиться к врачу. Если человек не употреблял никаких лекарств, можно перейти к следующему этапу.
- Проанализировать рацион пациента за последние 2-3 дня (были ли изменения в рационе, вводились ли необычные блюда, специи, напитки, употреблялись ли продукты из списка специфических). Если связь с питанием подтвердилась, необходимо исключить провоцирующий продукт и ожидать нормализации стула в течение 1-3 дней.
Когда нужно срочно обратиться к врачу?
На фоне черного стула нельзя игнорировать следующие симптомы:
- интенсивный кашель;
- носовые кровотечения;
- боли в области грудной клетки;
- боли в животе;
- снижение давления;
- замедление сердечного ритма;
- тошнота, рвота;
- потеря сознания;
- слабость;
- быстрая утомляемость при выполнении привычных действий;
- повышение температуры тела;
- потливость;
- бледность кожных покровов.
При наличии одного или нескольких из перечисленных признаков, откладывать визит к врачу недопустимо.
Какое обследование нужно пройти при черном стуле?
С проблемой необычного цвета фекалий следует обращаться к гастроэнтерологу. В тяжелых ситуациях нужна помощь хирурга. При подозрении на внутреннее кровотечение, обследование включает следующие процедуры:
- анализ крови (обычно назначают общий клинический, а также анализ на свертываемость);
- анализ каловых масс (проводят тест на скрытую кровь, копрограмму, а также бактериологический анализ);
- эндоскопия (эзофагогастродуоденоскопия и колоноскопия позволяют не только определить расположение кровотечения, но также купировать его, взять фрагменты тканей для гистологического анализа);
- рентгенография / МРТ с контрастным усилением (позволяет выявить локализацию кровоточащего дефекта).
В персональном порядке перечень диагностических процедур может быть дополнен.
Куда обращаться по поводу черного стула?
Читайте также:

