Можно ли давать безлактозную смесь при кишечной инфекции
Обновлено: 15.04.2024
Безлактозные продукты – для кого они? Безлактозные продукты – это молочные продукты, из которых удалена лактоза. Предназначены они для людей с непереносимостью лактозы.
Лактазная недостаточность - что это такое?
Как часто встречается лактазная недостаточность у детей?
Первичная врожденная лактазная недостаточность, то есть генетический дефект, при котором у малыша с рождения полностью отсутствует лактаза – крайне редкое заболевание, всего в мире описано 40 таких случаев. Вместе с тем, в норме с возрастом активность фермента постепенно снижается, особенно после 2 лет. Скорость этого снижения индивидуальна и симптомы непереносимости молока могут появиться в любом возрасте. Интересно, что в регионах, где с давних времен развито молочное животноводство, лактазная недостаточность и у взрослых встречается очень редко, а в странах, где традиционно после отлучения от груди молоко в питании не используется, напротив, очень часто. Так, в Северной Европе только 1-5% населения не переносят молоко, в Центральной Европе – 20-30%, а в странах тропической Африки и Юго-Восточной Азии – 90-100% У недоношенных детей, практически у всех, активность лактазы снижена в той или иной степени, что связано с еще незаконченным формированием ферментной системы к моменту рождения. Однако прикладывание к груди и поступление лактозы в кишечник стимулирует созревание фермента. Исследования, проведенные в последние годы, показывают, что большая часть здоровых новорожденных тоже имеют небольшую лактазную недостаточность, и активность фермента у них еще продолжает повышаться в течение 2-3 месяцев. Считается, что это может быть одной из причин младенческих колик.
По каким признакам можно заподозрить, что ребенку нужны безлактозные продукты?
Заподозрить лактазную недостаточность у ребенка старшего возраста нетрудно. После употребления молока или мороженого, реже – кисломолочных продуктов, у ребенка появляется дискомфорт или боли в животе, бурление, метеоризм, срочные позывы в туалет и разжиженный стул, температура тела остается нормальной. Если молоко больше не пить, то эти симптомы проходят сами по себе и опять появляются после употребления молока. Часто дети, которые плохо переносят молоко, инстинктивно избегают его и не любят. Кисломолочные продукты, как правило, переносятся хорошо, так как часть лактозы там уже переработана бактериями, и их вполне достаточно для удовлетворения потребностей ребенка в молочном белке и кальции. Для тех же, кто молоко любит, в продаже появилось молоко со сниженным содержанием лактозы. Диагностировать лактазную недостаточность у грудных детей сложнее, поскольку молоко является их основной пищей. Признаками непереносимости лактозы могут быть беспокойство ребенка во время или после кормления, частый, очень жидкий, впитывающийся в подгузник или пенистый стул, недостаточные прибавки веса, но так могут проявляться и другие заболевания. Последний симптом самый тревожный и требует обязательной консультации врача. Какие анализы и исследования назначаются для диагностики? Обычно детям с нарушениями пищеварения назначают общий анализ кала – копрограмму, а при проведении этого анализа определяют кислотность Выраженная кислотность кала, а именно значение pH ниже 5,5 может указывать на лактазную недостаточность. Очень популярен анализ кала на углеводы, но он, к сожалению, часто дает ложные результаты. Существуют дыхательные тесты, но они пока не нашли широкого применения в практике. Для диагностики врач может назначить пробное лечение – лактазу в виде препарата или безлактозную смесь, в случае положительной динамики лечение продолжают, длительность определяется врачом в зависимости от вида и тяжести недостаточности, сопутствующих заболеваний.
Можно ли продолжать естественное вскармливание, если у ребенка лактазная недостаточность?
Да, конечно, естественное вскармливание продолжать можно и нужно. Как я уже сказала, первичная врожденная лактазная недостаточность, которая требует полного исключения лактозы, встречается казуистически редко. У большинства же малышей с транзиторной лактазной недостаточностью имеется лишь некоторое временное снижение активности фермента. Вспомните, что лактоза нужна для развития мозга и для роста нормальной микрофлоры кишечника. Да и по остальным своим ингредиентам материнское молоко лучше подходит ребенку, чем любой заменитель. Детей, которые переносят кишечную инфекцию, тоже нельзя переводить на смесь, наоборот, рекомендуется прикладывать их к груди чаще, чем обычно. Недоношенных детей также лучше кормить материнским молоком. Известно, что состав молока преждевременно родивших женщин в большей степени соответствует потребностям недоношенного ребенка, чем родивших в срок, в частности, в нем меньше лактозы. Посоветуйтесь с вашим педиатром, в необходимых случаях врач назначит ребенку препараты фермента-лактазы.
В каких случаях нужны безлактозные смеси?
Безлактозные смеси назначают детям, которые уже находятся на искусственном вскармливании и имеют симптомы непереносимости лактозы. Поскольку в большинстве случаев речь идет лишь о частичном снижении активности фермента, то нет необходимости полностью переводить ребенка на безлактозную смесь. Здесь возможны варианты: можно в одной бутылочке смешивать обычную и безлактозную смесь, можно часть кормлений полностью заменить безлактозной смесью, а в остальные давать обычную. Количество безлактозной смеси подбирается индивидуально. В случае острой кишечной инфекции по назначению педиатра можно кормить ребенка безлактозной смесью, а после выздоровления постепенно возвращать обычную. Безлактозные смеси применяются и в том случае, если у ребенка вторичная лактазная недостаточность вызвана хроническим заболеванием желудочно-кишечного тракта. Однако в таких случаях зачастую речь идет о подборе специальных лечебных смесей, в которых изменены так же и белковый, и жировой компоненты, а лактоза может отсутствовать или быть в небольшом количестве. Смеси, предназначенные для вскармливания недоношенных детей, делают с учетом их физиологических потребностей и содержание лактозы в них также зачастую снижено.
Кроме лактазной недостаточности, в каких еще случаях детям будут полезны именно безлактозные продукты?
Лечебное питание является мощным терапевтическим фактором, при котором правильно составленная диета становится ключевым механизмом, позволяющим воздействовать на нарушенные звенья метаболизма, нормализовать функции пищеварительной системы, активизировать
Лечебное питание является мощным терапевтическим фактором, при котором правильно составленная диета становится ключевым механизмом, позволяющим воздействовать на нарушенные звенья метаболизма, нормализовать функции пищеварительной системы, активизировать защитные силы организма, что во многом определяет течение и исход болезни. При отдельных видах патологии лечебное питание является единственным средством лечения.
Для организации лечебного питания больного ребенка первого года жизни важен правильный выбор продукта со специальным заданным составом, отвечающим особенностям заболевания и характеру нарушенных при этом обменных процессов.
В настоящее время в нашей стране существует широкий спектр специализированных продуктов лечебного и профилактического предназначения отечественного и зарубежного производства для диетологической коррекции различных заболеваний у грудных детей.
Специализированные смеси для детей с функциональными нарушениями желудочно-кишечного тракта
Камедь рожкового дерева представляет собой растворимые полисахариды, не содержащие крахмал, которые набухают в желудке ребенка, тем самым препятствуют срыгиваниям. Углеводы, входящие в состав камеди, являются пищевыми волокнами — неперевариваемыми полисахаридами, которые не подвергаются расщеплению в верхних отделах гастроинтестинального тракта, а ферментируются микроорганизмами толстой кишки, способствуя селективному росту индигенной микрофлоры.
Максимально допустимое содержание камеди в продукте составляет 1 г в 100 мл. В антирефлюксных смесях содержание камеди колеблется от 0,34 до 0,5 г в 100 мл. Пищевая камедь подразделяется на инстантную (быстрорастворимую) и натуральную (требующую разведения горячей водой для набухания), получаемую из семян среднеземноморской акации и содержащую 85% углеводов, 5% белка, 10% влаги.
Антирефлюксные продукты, содержащие камедь, вводятся в рацион ребенка постепенно, в каждое кормление. Возможно их добавление в бутылочку со стандартной молочной смесью, которую получает ребенок, но более эффективным является самостоятельное применение в начале кормления. Объем лечебного продукта подбирается индивидуально до прекращения срыгиваний.
Антирефлюксные молочные смеси в первую очередь используются при регургитации (срыгиваниях) у детей грудного возраста. Срыгивания — обратный заброс пищевого химуса после проглатывания съеденной пищей. Нередко срыгивания обусловлены неадекватно проводимым вскармливанием (быстрое сосание, аэрофагия, перекорм, нарушения режима кормлений, неадекватный выбор смесей), а также перинатальными поражениями центральной нервной системы, пилороспазмом и др. Поэтому назначению антирефлюксных смесей должно предшествовать выявление причин, вызывающих срыгивания [3].
Смеси, содержащие камедь, могут также применяться в питании детей с функциональными запорами: хронической задержкой опорожнения кишечника более чем на 36 ч, увеличением интервалов между актами дефекации по сравнению с физиологической нормой, затруднением акта дефекации, отхождением малого количества кала повышенной плотности. Известно, что камедь обладает свойствами пищевых волокон: удерживает дополнительное количество воды и способствует мягкой стимуляции перистальтики кишечника, что приводит к устранению запоров. Наиболее эффективными из этой группы продуктов являются смеси с преобладанием сывороточной фракции в белковом компоненте, поскольку казеины обладают закрепляющим воздействием. При лечении запоров молочные смеси с камедью могут вводиться не в каждое кормление, а самостоятельно в качестве отдельного кормления — 2–3 раза в сутки [3].
Низколактозные и безлактозные смеси
К низко- и безлактозным детским смесям относят продукты, созданные на основе белков коровьего молока и предназначенные для вскармливания детей первого года жизни с лактазной недостаточностью.
В безлактозных смесях количество лактозы (молочного сахара) практически приближается к нулю. Основным углеводным компонентом таких смесей является декстрин-мальтоза. В низколактозных смесях количество лактозы составляет приблизительно 1 г на 100 мл (от 0,9 до 1,33 г), для сравнения — в женском молоке и стандартных молочных смесях содержится 6–7 г лактозы на 100 мл.
При первичной (конституциональной) лактазной недостаточности низколактозная (безлактозная) диета назначается пожизненно. При вторичной лактазной недостаточности основное внимание уделяется лечению патологии, приведшей к данному состоянию, а ограничение лактозы в рационе является временным, однако необходимым мероприятием.
При искусственном вскармливании следует подбирать смесь с максимальным количеством лактозы, которое переносит пациент, не допуская появления клинической симптоматики и повышения экскреции углеводов с калом. Это связано с тем, что лактоза является единственным источником галактозы, которая образуется при ее расщеплении. Галактоза используется для синтеза галактолипидов, включая цереброзиды, которые необходимы для формирования центральной нервной системы и миелинизации нервных волокон. Кроме того, считается что ежедневное употребление малых количеств лактозы необходимо для адаптации к ней кишечной микрофлоры и поддержания нормального микробиоценоза кишечника. Безлактозные продукты назначаются только при тяжелых формах лактазной недостаточности, когда использование низколактозных смесей неэффективно.
В отдельных случаях безлактозные продукты могут временно вводиться и при грудном вскармливании, когда назначение фермента лактазы неэффективно и необходимо ограничение лактозы. Назначение безлактозных смесей (в отличие от низколактозных продуктов) позволяет сохранить использование материнского молока в максимально возможном объеме.
Диетическая коррекция при лактазной недостаточности заключается в постепенной замене детской молочной смеси низколактозным или безлактозным продуктом, который вводится в каждое кормление. Необходимый объем лечебной смеси определяется клинической симптоматикой: в случае, если удается добиться устранения диареи и колик комбинацией низколактозной или безлактозной смеси со стандартной молочной смесью, последнюю полностью отменять не следует [8].
Кисломолочные смеси и продукты
Кисломолочные продукты занимают важное место в лечебном питании детей первого года жизни, так как они благоприятно влияют на секреторную деятельность пищеварительного тракта, перистальтику кишечника, оказывают ингибирующее действие на патогенные микроорганизмы, стимулируют рост индигенной микрофлоры, способствуют улучшению всасывания кальция, фосфора, магния и железа, оказывают иммуномодулирующее действие и повышают защитные силы организма [2, 6, 9].
Ингибирование роста патогенных микроорганизмов при использовании кисломолочных смесей происходит за счет продукции антимикробных субстанций, конкуренции за питательные вещества, препятствия адгезии патогенной флоры на рецепторы энтероцитов. Иммуномодулирующий эффект данных продуктов заключается в усилении фагоцитоза, активизации пролиферации лимфоцитов, препятствии деградации секреторного иммуноглобулина А, стимуляции выработки интерферона, лизоцима, пропердина, влиянии на цитокиновую систему, регуляции выработки интерлейкинов.
Если кисломолочные продукты содержат живые микроорганизмы (бифидо- и лактобактерии) — представители нормальной микрофлоры кишечника человека, то их называют продуктами-пробиотиками. Они обладают двойным функциональным эффектом, обусловленным присутствием пробиотических штаммов микроорганизмов и продуцируемой ими молочной кислоты.
При разработке продуктов пробиотического действия используются различные виды микроорганизмов, преимущественно бифидобактерии и лактобактерии, к которым, как и к продуктам, созданным на их основе, предъявляются строгие требования, касающиеся безопасности, функциональной эффективности, технологичности [10].
Основные требования к безопасности продукта и входящих в него компонентов сформулированы в документах санитарного законодательства Российской Федерации, а также в международных рекомендациях ФАО/ВОЗ и заключаются в использовании штаммов микроорганизмов, выделенных от человека; отсутствии патогенности, токсичности и побочных реакций, антибиотикоустойчивости, высоких адгезивных свойствах к эпителию слизистой кишечника, стабильности генетического кода [11, 12].
Каждый штамм бифидобактерий имеет свои характеристики и диапазон действия. Так, Bifidobacterium (B.) bifidum и B. infantis превалируют в кишечнике у детей, находящихся на грудном вскармливании, а B. adolescentis — при искусственном вскармливании. В последнее время для получения кисломолочных смесей с пробиотическими свойствами широко используются штаммы B. lactis (Bв 12), обладающие выраженной функциональной активностью и хорошей устойчивостью в желудочно-кишечном тракте ребенка.
Лактобактерии чаще используются в комбинированных заквасках при создании кисломолочных продуктов. Известно, что лактобактерии Lactobacillus (L.) acidofilus, L. rhamnosus (LGG), L. casei обладают хорошей сохранностью в продукте, устойчивостью к внешним воздействиям, высоким пробиотическим эффектом (табл. 4).
Кисломолочные продукты могут быть жидкими и сухими, они также подразделяются на адаптированные и неадаптированные (табл. 5).
Новым в детской диетологии является создание сухих адаптированных кисломолочных смесей (табл. 6).
При использовании кисломолочных продуктов у детей первого года жизни отмечается уменьшение выраженности функциональных нарушений процессов пищеварения, таких как колики, склонность к запорам, диспепсические проявления, сниженный аппетит, а также улучшение состава микрофлоры кишечника. Указанные продукты нашли применение у грудных детей из группы риска по развитию алиментарно-зависимых заболеваний, а также страдающих рахитом, анемией, гипотрофией. При этом отмечены более высокая усвояемость железа и повышение уровня гемоглобина у детей с анемией, улучшение процессов остеогенеза у детей с рахитом и более выраженное увеличение массы тела у детей с гипотрофией, что обусловлено высокой усвояемостью из них белка, кальция и железа [3, 4, 13].
Гипоаллергенные продукты, созданные на основе гидролизатов молочного белка
Появление смесей, созданных на основе гидролизатов молочного протеина, знаменует собой начало новой эры в профилактике и лечении пищевой аллергии, а также ряде тяжелых заболеваний, сопровождающихся синдромом нарушенного кишечного всасывания, снижением нутритивного статуса ребенка [14].
В зависимости от степени расщепления молочного белка, выделяют смеси на основе его полного (высокого) или частичного (умеренного) гидролиза. Гидролизу могут подвергаться как казеиновая, так и сывороточная фракции молочных протеинов.
Установлено, что чем выше молекулярная масса пептидов гидролизата, тем больше риск развития аллергических реакций. По сравнению с белком коровьего молока аллергенность белкового компонента продуктов, созданных на основе высоко гидролизованного белка, снижена в 10 000–100 000 раз, частично гидролизованного — в 300–1000 раз. Молекулярная масса пептидов, при которых аллергенность гидролизата становится минимальной, составляет 1,5 кDа, пептиды с молекулярной массой 3–3,5 кDа в отдельных случаях могут вызывать аллергические реакции.
Все смеси данного класса обогащены комплексом витаминов и минеральных веществ в соответствии с физиологическими потребностями детей первого года жизни и соответствуют требованиям ВОЗ по ингредиентному составу, биологической и пищевой ценности, влиянию на физическое и психомоторное развитие детей первого года жизни [15].
В соответствии с клиническим предназначением смеси на основе гидролизатов молочного белка подразделяются на лечебные, лечебно-профилактические и профилактические (табл. 7).
К лечебным относятся только смеси, полученные в результате глубокого гидролиза молочного белка, которые, как правило, являются полуэлементными, так как помимо модифицированного белкового компонента содержат среднецепочечные жирные кислоты, моносахариды, полимеры глюкозы и полностью лишены лактозы. Указанные продукты предназначены для детей с тяжелыми проявлениями пищевой аллергией, обусловленной гиперчувствительностью к белкам коровьего молока и другим пищевым протеинам, а также больных с синдромом мальдигестии и мальабсорбции на фоне целиакии, панкреатической недостаточности, дистрофии слизистой кишечника, после резекций участков тонкой кишки и пр.
При использовании лечебных гидролизатов белка удается достичь существенного улучшения со стороны кожных и желудочно-кишечных проявлений через 2–3 нед от начала их применения, а клинической ремиссии — спустя еще 2–3 мес. При этом у детей с дефицитом массы тела происходит нормализация нутритивного статуса. Продолжительность применения указанных продуктов индивидуальна, в среднем она составляет 3–4 и более месяцев.
Все продукты, созданные на основе гидролизатов молочного белка, имеют горьковатый вкус и специфический запах, при их назначении в период адаптации возможен несколько разжиженный и учащенный стул, зеленоватого или коричневого цвета, что не должно служить причиной для отмены продукта.
Смеси на основе изолята соевого белка
Современные соевые смеси разработаны на основе изолята соевого белка, в котором содержание протеинов составляет более 90%, а нежелательные компоненты (неперевариваемые углеводы, ингибитор трипсина, лектины и сапонины) удаляются в процессе технологического производства. При производстве соевых смесей для детского питания не используется генетически модифицированная соя.
Биологическая ценность изолята соевого белка повышена за счет дополнительного введения L-метионина и других аминокислот и сопоставима с молочным казеином. Жировой состав соевых смесей представлен смесью растительных жиров, а углеводы состоят из декстрин-мальтозы, кукурузного крахмала (табл. 8). Таким образом, все соевые смеси являются безмолочными и безлактозными.
Смеси на основе изолята соевого белка обогащены витаминно-минеральным комплексом, а применение современных технологий позволяет повысить усвоение кальция, фосфора и железа.
Смеси на основе изолята соевого белка можно достаточно эффективно использовать при лечении пищевой аллергии, индуцированной белками коровьего молока. Однако клинические наблюдения показывают, что у 20–25% детей первого года жизни они могут быть причиной возникновения или обострения атопического дерматита или гастроинтестинальных проявлений аллергии. Наши исследования свидетельствуют о том, что наиболее часто аллергические реакции развиваются при быстром (в течение 1–2 дней) введении соевых смесей, раннем их назначении (детям первых месяцев жизни), отягощенном аллергоанамнезе [14, 17].
Для предотвращения развития нежелательного эффекта при использовании соевых смесей у детей необходимо соблюдать определенные условия: у ближайших родственников должна отсутствовать аллергия к сое и бобовым, возраст ребенка — не менее 5–6 мес (особенно при кожно-гастроинтестинальной или гастроинтестинальной формах пищевой аллергии), постепенное (в течение 5–7 дней) введение продукта в рацион ребенка. Следует также учитывать индивидуальную переносимость смеси, применять ее нужно не менее 3 мес [16].
Кроме того, эти соевые смеси могут использоваться для лечебного питания у детей с галактоземией (при данной патологии они являются первыми продуктами выбора), лактазной недостаточностью, целиакией в качестве альтернативы молочным продуктам и смесям. Признавая в целом нутритивную адекватность промышленных соевых смесей, не следует рекомендовать их недоношенным детям.
Таким образом, использование в педиатрической практике детских специализированных смесей, полученных с применением самых современных технологий, позволяет в максимально короткие сроки организовать патогенетически обоснованное лечебное питание, обеспечить потребности больного ребенка в макро- и микронутриентах, облегчить течение патологического процесса, улучшить нутритивный статус и ускорить достижение клинической ремиссии заболевания или выздоровление.
Литература
Т. Э. Боровик, доктор медицинских наук, профессор
В. А. Скворцова, доктор медицинских наук
К. С. Ладодо, доктор медицинских наук, профессор
Е. А. Рославцева, кандидат медицинских наук
Н. Н. Семенова, кандидат медицинских наук
Т. Н. Степанова, кандидат медицинских наук
НЦЗД РАМН, Москва

Неоднократно участвовала в международных конференциях по педиатрии, детской диетологии, гастроэнтерологии и аллергологии. Участник съездов педиатров Беларуси, Конгрессов и съездов педиатров России, Конгрессов педиатров стран СНГ. Организатор и участник круглых столов и семинаров для молодых мам и пап по тематике грудного вскармливания, правильного питания ребенка раннего возраста, по уходу за ребенком первого года жизни. Автор многочисленных статей и публикаций для родителей по вопросам питания и ухода за детьми первого года жизни.
Про кишечные инфекции
Мы неумолимо приближаемся к теплым солнечным дням - времени поездок на море, в деревню к бабушке, времени песочниц, времени фруктов-овощей, и к сожалению - времени, когда наши дети чаще всего подвержены кишечным инфекциям.

Несколько важных акцентов для мамы:
Острые кишечные инфекции у детей – заболевание опасное. И тем опаснее, чем младше ребенок. Ежегодно, ОКИ уносят жизни сотен тысяч детей. Коварство этих болезней в том, что для лечения просто нужна вода. Регидратация (восполнение потерь воды) и диетотерапия – основа лечения всех ОКИ, и большинство смертей происходит в странах, живущих в условиях дефицита чистой питьевой воды.
В большинстве случаев, при легких и среднетяжелых инфекциях все полностью восстановится за 1-2 недели. С рядом болезней организм справится самостоятельно! Иммунитет не дремлет. Только надо за тот период, пока главное не дать малышу обезводиться. Повторюсь. Возмещение потери воды и солей, и диетотерапия - это основа лечения ОКИ!
В ряде случаев понадобится тяжёлая артиллерия – дать специфическую антимикробную терапию, позволяющую победить возбудителя. Понятно, что самолечением при диарее заниматься не стоит. Вы в любом случае обратитесь к врачу. Но дело в том, что маленькие дети способны обезводится ещё до прихода врача. Особенно если понос сопровождается рвотой и температурой. Температура, тоже уводит из организма воду.
Как возмещать воду?
Вы примерно видите, сколько потерял с рвотой и поносом - столько нужно и дать выпить. Как это сделать, спросите вы? Если его все время рвет, или тут же все оказывается в подгузнике? Жидкость даем дробно. Если поить с чашки и он выпьет полную чашку - не сомневайтесь, его тут же стошнит. Поэтому, нужно взять чайную ложку и выпаивать. Под мультик. Каждые пять минут по ложке. Глоток, снова глоток. Организм не тратит свои ресурсы на то, чтобы стошнить глоток. И эти 5 мл жидкости усвоятся. Чем выпаивать? Организм теряет не только воду, но и соли. Поэтому специальными глюкозо-солевыми растворами лучше всего. Если вы ждете врача и нет возможности отлучиться из дома в аптеку - ромашковый или фенхелевый чай, можно пакетированный, можно гранулированный, но в составе не должно быть лактозы или же просто слабозаваренный чай. Все зависит от ваших возможностей - вдруг вы в деревне у бабушки, 50 км от райцентра, нет аптеки - тогда детскую питьевую воду, кипяченую воду.
- Детям постарше - компот из сухофруктов.
- У ребенка на грудном вскармливании сохраняется грудное вскармливание. Это обязательно. Это и регидратация и диетотерапия. Это мощный набор защитных компонентов грудного молока. Единственное что может понадобиться – ферментация сцеженной порции молока перед кормлением специальными ферментами, снижающими лактозную нагрузку. Если ребенок отказывается от груди - не может сосать, тогда сцеживать и опять же с ложки давать.
- Если ребенок на искусственном вскармливании - смесь на период ОКИ лучше будет заменить на смесь низко- либо безлактозную. Правильнее всего это будет сделать, выбрав смесь в ассортиментной линейке того производителя, которым пользуетесь. Варианты включения безлактозной смеси в рацион ребенка с ОКИ подскажет ваш педиатр. Все зависит от формы тяжести и длительности болезни. В некоторых случаях необходимо заменить часть рациона, иногда перейти полностью и сохранить безлактозную смесь еще на неделю-две восстановительного периода после инфекции -это то время в течении которого полностью восстановится фермент лактаза в кишечнике. После этого можно будет постепенно вернуться к привычному молочному рациону.
Все предыдущие моменты касались восполнения жидкости и молочного компонента питания.
А как же деткам постарше, у которых прикормы или же общий стол?
Это как раз тот момент, когда прикормы промышленного производства будут просто как нельзя кстати. Они и есть основа диетотерапии. Если ребенок их получает - продолжаем. Это безмолочные, безглютеновые каши, мясные пюре, овощное из брокколи. Соки можно убрать, а вот фруктовое пюре - особенно черника - оставить в рационе.
Если вы ушли на общий стол, во время кишечных инфекций скоррегируйте его диету с учетом продуктов прикорма промышленного производства. Режим питания при ОКИ меняется – ребенок ест дробно, маленькими порциями – философия та же, как и при восполнении жидкости – чтобы не стошнил и чтобы не прошло транзитом по кишечнику. Поэтому пищу даем дробно, часто, маленькими порциями, в подогретом виде.
Ориентировочная диета:
(Этот режим очень ориентировочный. Если ваш ребенок ест в час по чайной ложке – и это единственный способ его накормить, значит кормим так, чтоб усвоил – каждый час)
6.00—7.00 Первый завтрак — грудное молоко или заменитель грудного молока (смесь),
10.00—11.00 Второй завтрак — каша безмолочная густая, чай ромашка
13.00—14.00 Обед — овощное пюре + мясное пюре, чай фенхель
16.00—17.00 Полдник — грудное молоко или заменитель грудного молока
19.00—20.00 Первый ужин — каша на воде и фруктовое пюре, компот из сухофруктов (после 12 мес)
22.00—23.00 Второй ужин — грудное молоко или заменитель грудного молока, или кисломолочный продукт.
Особое значение для детей первых месяцев жизни имеет лактазная недостаточность (ЛН), так как лактоза содержится в грудном молоке, которое является основным питанием ребенка этого возраста. Дисахарид лактоза расщепляется в тонкой кишке ферментом, известным под названием лактаза. Снижение активности этого фермента приводит к развитию симптомокомплекса ЛН, проявляющейся у детей раннего возраста диареей, а также другими диспептическими нарушениями, беспокойством и др. Основным методом лечения ЛН является диетотерапия, направленная на уменьшение или полное исключение лактозы из рациона питания [3, 4]. Особую сложность представляет лечение ЛН у детей грудного возраста, так как в грудном молоке или в современных адаптированных детских молочных смесях углеводный компонент представлен преимущественно лактозой. При искусственном вскармливании детей с лактазной недостаточностью используются низколактозные смеси. Безлактозные смеси в качестве монотерапии используют только при первичной алактазии и при тяжелом течении вторичной гиполактазии [2, 5].
Учитывая, что поддержка естественного вскармливания детей первого года жизни является приоритетной задачей педиатрии, проблема профилактики и лечения ЛН у детей, находящихся на естественном вскармливании, представляется чрезвычайно важной и актуальной. При этом наиболее целесообразным в лечении ЛН является не исключение женского молока, а проведение заместительной терапии в виде назначения детям фермента лактазы. Использование ферментных препаратов лактазы в терапии ЛН позволяет довольно быстро купировать симптомы заболевания, сохранив при этом грудное вскармливание [1, 6, 7].
Учитывая значительные колебания в активности и свойствах препаратов лактазы, выпускаемых различными производителями и выделенных из различных источников, представляется необходимой обязательная клиническая оценка препарата лактазы, впервые выпускаемого в РФ или поступающего из-за рубежа в виде фармацевтического средства или биологически активной добавки (БАД).
Дизайн исследования. Исследование носило характер открытого проспективного медицинского наблюдения.
Материалы и методы
Критерии отбора детей для исследования:
Критерии исключения детей из исследования:
Критерии оценки эффективности проводимой терапии:
— содержание общих углеводов в кале*;
— копрологические исследования*;
— клинические анализы крови и мочи;
— измерение массы тела 1 раз в 2 недели с использованием стандартизированных весов;
— измерение роста — до и после проведения исследования с использованием стандартного ростомера.
Под наблюдением находилось 25 детей (12 мальчиков и 13 девочек) в возрасте от 2 недель до 3 месяцев жизни. Все дети находились на естественном вскармливании. Под наблюдение дети поступали по обращению матерей к участковому педиатру в детской поликлинике. Дети наблюдались в амбулаторных условиях, еженедельно осматривались врачом-педиатром. Дома матери заполняли специально предложенную им анкету, в которой содержались вопросы о показателях эффективности исследуемого БАД (частота и характер стула, частота и объем срыгиваний и пр.). Дополнительные сведения получали путем телефонного интервью.
Данные о наблюдавшихся детях и их возрастно-половая характеристика представлены в табл.1 и табл.2
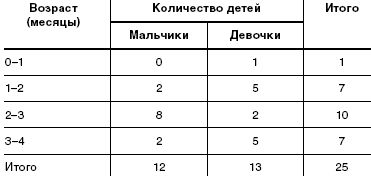
Все дети были доношенными, от первых (20), вторых (4) и третьих (1) родов; у 84% матерей имело место патологическое течение беременности (гестозы, анемия, наличие хронических заболеваний, хроническая фетоплацентарная недостаточность и пр.). Все кормящие матери соблюдали предложенную им диету [8]. Из рационов кормящих матерей исключали цельное коровье молоко с целью профилактики развития у детей аллергии к белкам коровьего молока и снижения тем самым возможности формирования вторичной ЛН.
При изучении анамнеза жизни было установлено, что более чем у половины обследованных детей кто-либо из членов семьи не переносит или не любит молоко и молочные продукты. Так, у 60% детей не переносит молоко один из родителей, у 20% — один из членов семьи (сестры, братья, дедушки, бабушки и др.); у остальных детей непереносимости молочных продуктов в семье, со слов матерей, не отмечено.
Диагноз ЛН устанавливали на основании характерных клинических симптомов (типичные изменения частоты и консистенции стула, усиленный метеоризм, болевой синдром и др.) и результатов клинико-лабораторных исследований (повышенного содержания общих углеводов в кале).
Результаты исследования и обсуждение
Результаты исходного обследования детей
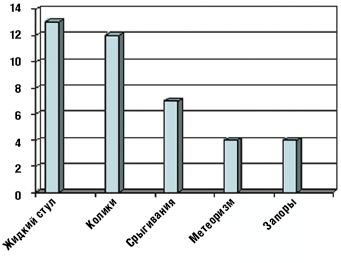
Как видно из табл. 3 и рис. 1 и 2, клинические проявления ЛН у обследованных детей были весьма вариабельны.
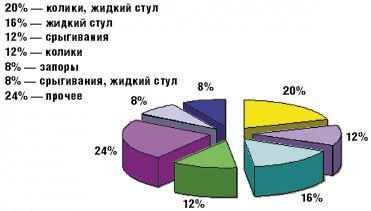
Такой наиболее характерный симптом ЛН, как жидкий стул, был обнаружен у 13 детей (52%), причем у 5 из них жидкий стул сочетался с коликами (табл. 3). У остальных детей имели место другие проявления функциональных нарушений пищеварения (срыгивания, метеоризм, запор). Срыгивания разной степени выраженности наблюдались у 7 детей (28%), причем у 2 детей (8%) срыгивания были единственной жалобой. У 4 детей (16%) отмечались запоры, причем как единственная жалоба запоры наблюдались у 2 детей. У 8 детей на момент взятия под наблюдение нарушений частоты и консистенции стула не было, стул у этих детей наблюдался 2–3 раза в день, кашицеобразной консистенции.
У 2 детей отмечалась недостаточная прибавка массы тела (300–400 г в месяц) и снижение аппетита (дети употребляли не весь объем порции молока, необходимый ему из расчета на массу тела и возраст); именно это послужило причиной обращения к педиатру.
Таким образом, полученные нами данные свидетельствуют о том, что клиническая картина ЛН весьма многообразна и часто не совпадает с общепринятым представлением о диарее как ведущем симптоме этого заболевания.
Проведенные исследования показали хорошую переносимость БАД у всех наблюдавшихся детей (из исследования не был выведен ни один ребенок) и ее эффективность в устранении симптомов ЛН.
Нормализация частоты стула и его консистенции была отмечена уже к концу первой недели, причем положительная динамика имела место в среднем на 5-й день терапии. При этом кратность и консистенция стула изменялись у детей неодинаково. Нормализация консистенции стула у детей с частым жидким стулом отмечалась на 3–5 день применения БАД; а у детей с запорами восстановление регулярного стула с кратностью 3–4 раза в день, имевшего цвет и консистенцию, обычные для детей данной возрастной группы, находящихся на естественном вскармливании, — на 6–8 день. Частота стула у детей с диареей до начала терапии составляла в среднем 5,7 ± 1,2 раза в сутки, а после ее завершения — 3,8 ± 0,9 раза в сутки. У детей с запорами частота стула была равна соответственно 0,8 ± 0,6 и 2,5 ± 1,7.
Болевой синдром, проявлявшийся кишечными коликами, и метеоризм купировались у всех 25 детей на 3–5 день применения БАД. Частота и объем срыгиваний значительно уменьшились в конце первой недели терапии и полностью исчезли после двух недель приема препарата у большинства детей. Только у одного ребенка к концу исследования изредка отмечались срыгивания.
Экскреция углеводов с калом достоверно снизилась у большинства детей с 1,1 ± 0,3% до начала терапии до 0,6 ± 0,1% после ее завершения, разброс значений составил 0,4–1,8% и 0,25–0,6% соответственно (рис. 4).
Однако у 6 детей достоверного снижения уровня экскреции углеводов с калом не отмечено (0,7–0,8% до исследования и 0,5–0,6% — после); хотя клинические симптомы нарушений пищеварения были купированы на первой неделе приема БАД. Полученные нами данные согласуются с литературными данными, указывающими на отсутствие четкой корреляции между выраженностью клинических проявлений ЛН и уровнем экскреции углеводов с калом [1, 3, 4]. В связи с этим необходимо отметить, что в соответствии с современными научными представлениями основным критерием эффективности терапии является устранение клинических симптомов заболевания, а не снижение до нормы экскреции углеводов.
Показатели клинических анализов крови и мочи у обследованных детей до и после проведения терапии были в пределах возрастной нормы. Содержание гемоглобина в крови у детей до и после исследования составило 135,3 ± 1,5 г/л и 132,3 ± 1,2 г/л соответственно.
прием БАД ведет к быстрому и эффективному устранению основных симптомов ЛН, благодаря чему может быть использован в терапии детей раннего возраста с ЛН, находящихся на естесственном вскармливании;
Литература
Мухина Ю. Г., Чубарова А. И., Гераськина В. П. Современные аспекты проблемы лактазной недостаточности у детей раннего возраста // Вопросы детской диетологии, 2003, том 1, № 1, стр. 50–56.
Питание здорового и больного ребенка/Пособие для врачей. Под редакцией В. А. Тутельяна, И. Я. Коня, Б. С. Каганова. М., 2007, с. 100–103.
Мухина Ю. Г., Шумилов П. В., Дубровская М. И. с соавт. Современные подходы к диагностике и терапии дисахаридазной недостаточности у детей // Трудный пациент. Педиатрия, 2006, № 9.
Бельмер С. В., Мухина Ю. Г., Чубарова А. И., Гераськина В. П., Гаилина Т. В. Непереносимость лактозы у детей и взрослых // Лечащий Врач. Январь 2005, № 1, с. 34–36.
Конь И. Я. Специализированные продукты лечебного питания: характеристика и применение у детей раннего возраста // Детский доктор, 2000, № 3, с. 43–47.
Корниенко Е. А., Митрофанова Н. И., Ларченкова Л. В. Лактазная недостаточность у детей раннего возраста // Вопросы современной педиатрии, № 4, 2006, том 5.
Чубарова А. И., Гераськина В. П., Кыштымов М. В. c cоавт. Эффективность применения ферментотерапии и диетотерапии при лактазной недостаточности у новорожденных // Вопросы детской диетологии, 2003, том 1, № 4, с. 21–24.
Конь И. Я., Фатеева Е. М., Гмошинская М. В., Басова Л. И., Каменева Г. В. Современные подходы к организации рационального питания беременных женщин и кормящих матерей // Методические рекомендации, М., 2002.
Т. В. Абрамова, кандидат медицинских наук И. Я. Конь, доктор медицинских наук, профессор, академик РАЕН НИИ питания РАМН, Москва
Читайте также:

