Можно ли отравится от циннаризина
Обновлено: 24.04.2024
Фармакологическое действие - сосудорасширяющее, улучшающее мозговое кровообращение, улучшающее периферическое кровообращение.
Фармакология
Блокирует кальциевые каналы L-типа. Ингибирует поступление в клетки ионов кальция и уменьшает их содержание в депо. Снижает тонус гладкомышечных элементов артериол, улучшает коронарное и периферическое кровообращение. Имеет высокую тропность к сосудам головного мозга, улучшает мозговое кровообращение, уменьшает головную боль, шум в ушах. Подавляет реакции на биогенные сосудосуживающие вещества (адреналин, норадреналин, брадикинин). Повышает эластичность мембран эритроцитов и понижает вязкость крови. Повышает резистентность клеток к гипоксии. Уменьшает возбудимость вестибулярного аппарата, в т.ч. подавляет нистагм. Обладает умеренной антигистаминной активностью. У пациентов с нарушением периферического кровообращения улучшает кровоснабжение тканей и потенцирует постишемическую гиперемию.
При приеме внутрь быстро всасывается. С белками плазмы связывается на 91%. Cmax определяется через 1–3 ч. Полностью метаболизируется в печени. 1/3 метаболитов выводится с мочой, 2/3 — с фекалиями. T1/2 — 4 ч. Не обладает тератогенностью.
Применение вещества Циннаризин
Нарушения мозгового кровообращения: атеросклероз сосудов мозга, ишемический инсульт, период после геморрагического инсульта и черепно-мозговых травм, дисциркуляторная энцефалопатия; головокружение, шум в ушах, подавленность и раздражительность, быстрая психическая утомляемость, мигрень, сенильная деменция, снижение и потеря памяти, нарушение мышления и невозможность концентрации внимания; лечение и профилактика нарушений периферического кровообращения (болезнь Рейно, облитерирующий атеросклероз, облитерирующий тромбангиит (болезнь Бюргера), диабетическая ангиопатия, акроцианоз, перемежающаяся хромота, трофические и варикозные язвы, парестезии, холодные конечности); поддерживающая терапия при симптомах лабиринтных нарушений, включая головокружение, шум в ушах (тинитус), нистагм, тошноту и рвоту; профилактика кинетозов.
Противопоказания
Гиперчувствительность, кормление грудью.
Ограничения к применению
Беременность, болезнь Паркинсона.
Применение при беременности и кормлении грудью
При беременности возможно, если ожидаемый эффект терапии превышает потенциальный риск для плода. На время лечения следует прекратить грудное вскармливание.
Побочные действия вещества Циннаризин
Со стороны нервной системы и органов чувств: сонливость, утомляемость, головная боль.
Со стороны органов ЖКТ: сухость во рту, диспептические явления, боль в эпигастральной области, холестатическая желтуха.
Со стороны кожных покровов: повышенное потоотделение, проявления красной волчанки или красного плоского лишая.
Прочие: аллергические кожные реакции, увеличение массы тела; очень редко — тремор конечностей, повышенный мышечный тонус.
Взаимодействие
Химическая несовместимость не известна.
Усиливает действие алкоголя, седативных средств, антигипертензивных и сосудорасширяющих препаратов. Усиливает эффект ноотропных средств. Уменьшает эффект средств для лечения артериальной гипотензии.
Передозировка
Лечение: промывание желудка, прием активированного угля, симптоматическая терапия. Специфического антидота нет.
Способ применения и дозы
Внутрь, желательно после еды. Нарушение мозгового кровообращения: по 25–50 мг 3 раза в сутки, нарушение периферического кровообращения: по 50–75 мг 3 раза в сутки, нарушение равновесия: по 25 мг 3 раза в сутки, профилактика кинетозов: взрослым — 25 мг за 30 мин до поездки, при необходимости повторно через 6 ч до максимальной рекомендуемой дозы — 225 мг. Детям назначают половину дозы для взрослых. При высокой чувствительности к циннаризину лечение начинают с 1/2 дозы, увеличивая ее постепенно.
Меры предосторожности
С осторожностью применять во время работы водителям транспортных средств и людям, профессия которых связана с повышенной концентрацией внимания (возможна сонливость, особенно в начале лечения). Пациентам с болезнью Паркинсона может назначаться только если ожидаемый эффект терапии превышает риск ухудшения основного заболевания. При длительном применении рекомендуется контроль функции печени, почек и картины периферической крови.
Отравление флунаризином, циннаризином и их побочные эффекты
В некоторых европейских странах циннаризин и флунаризин назначают для лечения "хронического цереброваскулярного заболевания" и считают "церебральными ва-зодилататорами". Однако эффективность флунаризина и циннаризина в качестве церебральных вазодилататоров не подтверждена контролируемыми клиническими исследованиями. Сообщалось о нескольких случаях намеренных передозировок циннаризина и флунаризина.
а) Структура и классификация. Флунаризин — дифторированное пиперазиновое производное, антагонист кальция, структурно близкий к циннаризин.
б) Применение. Флунаризин применяется как профилактическое средство для предупреждения мигрени и подавления эпилептических припадков, для лечения вертиго и недостаточности мозгового кровообращения.
в) Терапевтическая доза. Терапевтические дозы флунаризина составляют 10 мг/сут для взрослых и 5 мг/сут для детей, масса тела которых меньше 40 кг.
г) Токсичная доза. После приема флунаризина по 10—20 мг/сут и циннаризина 45—180 мг/сут возникают экстрапирамидальные эффекты.
д) Летальная доза. Летальная доза не установлена.
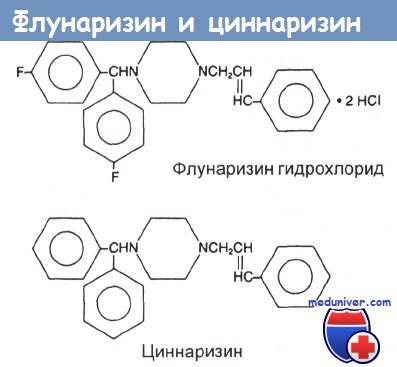
Структура флунаризина и циннаризина
е) Токсикокинетика отравления флунаризином и циннаризином:
- Всасывание. Пиковая концентрация флунаризина в плазме (от 39 до 115 мкг/л) отмечается через 2—4 ч после перорального приема одной дневной дозы 10 мг. Около 90 % лекарства связывается в плазме с белками.
- Распределение. Средний объем распределения равен около 43 л/кг.
- Выведение. Флунаризин активно метаболизируется в основном, повидимому, с желчью. Терминальный период полужизни примерно 18 дней. Период полужизни циннаризина в плазме составляет около 3 ч.
- Взаимодействие лекарственных средств. Вещества, индуцирующие активность ферментов печени (например, фенитоин, карбамазин, вальпроевая кислота), стимулируют метаболизм флунаризина.
ж) Механизм действия. Циннаризин — избирательный блокатор входа кальциевых ионов, обладающий антигистаминной, антисеротониновой и антидофаминовой активностью.
з) Клиническая картина отравления. У пациентов, принимающих флунаризин или циннаризин, развивается сонливость. Иногда наблюдаются увеличение массы тела, головные боли, депрессия, тошнота, сухость во рту и сыпь. Описаны случаи возникновения экстрапирамидальных реакций, включая дискинезию, акатизию и депрессию, которые часто напоминают паркинсонизм.
и) Лабораторные данные. Наиболее предпочтительный метод анализа циннаризина в плазме — жидкостная хроматография высокого разрешения, порог чувствительности метода составляет 20 мкг/л.
к) Лечение отравления флунаризином и циннаризином. При передозировках лечение главным образом симптоматическое и поддерживающее. Специфические антидоты неизвестны. Врач должен быть готов принять адекватные меры в случае возникновения припадков и угнетения дыхания.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление блокаторами кальциевых каналов и их побочные эффекты
При передозировках блокаторов кальциевых каналов часто наблюдаются брадикардия (депрессия синусового узла, депрессия предсердно-желудочкового узла, аритмии). Острые передозировки дилтиазема и нифедипина отмечаются редко.
а) Структура и классификация. Блокаторы кальциевых каналов, выпускаемые в США, включают фенилалкиламины (верапамил), дигидропиридины (нифедипин, никардипин, нимодипин, амлодипин, бепридил, фелодипин, израдипин) и бензотиазепины (дилтиазем).
Флунаризин, двуфтористое производное пиперазина, обладающее способностью блокировать вход кальция, может быть применен для лечения ряда неврологических и цереброваскулярных расстройств, например мигрени, припадков и головокружения, но он может индуцировать паркинсонизм. Циннаризин — это антагонист Н1-рецептора, обладающий свойствами блокатора кальциевых каналов.
б) Токсичная доза. Передозировка дилтиазема (4,8 г) приводит к снижению уровня сывороточного кальция. Одна капсула нифедипина, содержащая 10 мг лекарства, оказалась летальной для 14-месячного ребенка. Токсичность не зависит от концентрации препарата в плазме.
У 50-летнего мужчины, проглотившего 5880 мг дилтиазема с пивом, развилась гипотензия и был короткий период желудочковой асистолии; больной выжил.
- Нифедипин. Нифедипин, проглоченный 14-месячным ребенком в количестве 800 мг (70 мг/кг), вызвал кому, гипотензию, гипергликемию, предсердно-желудочковую блокаду III степени, остановку сердца, припадки и дефекты поля зрения; ребенок медленно выздоровел. Доза 200 мг нифедипина вызвала синусовую тахикардию у ребенка в возрасте 1 года, а у 72-летнего мужчины — гипотензию.
9-летний ребенок проглотил 100 мг нифедипина без токсических симптомов. 25-Летний мужчина проглотил 50 мг нифедипина без каких-либо симптомов. У взрослого человека с хронической почечной недостаточностью 280 мг нифедипина вызвали глубокую гипотензию, но тканевая перфузия оставалась нормальной.
- Верапамил. Доза 960 мг медленно высвобождающегося препарата ве-рапамила вызвала у 66-летнего пациента брадикардию, головокружение и угнетение дыхания. Доза 1,9 г оказалась нетоксичной для 33-летней женщины. Двухлетний ребенок проглотил 240 мг верапамила без каких-либо признаков токсичности.
Исследование, в котором были изучены 18 случаев проглатывания детьми блокаторов кальциевых каналов, показало, что проглатывание одной таблетки нифедипина (10 мг) или верапамила (80 мг или 120 мг) обычно не оказывает значительного действия на детей, но проглатывание верапамила детьми в возрасте до 2 лет приводило к летальному исходу. 73-Летняя женщина проглотила 2,88 г медленно высвобождающегося верапамила и через 24 ч была доставлена в клинику.
Внутривенное введение глюкагона (5 мг, затем 3 мг/ч), по-видимому, оказало благотворное действие при лечении гемодинамической раздражимости.
в) Летальная доза. Дилтиазем в дозах до 12 г вызывал брадикардию, гипотензию, атриовентрикулярную блокаду I, II и III степени, синусовую брадикардию, остановку синусового узла с узловым ускользанием и асистолию. У большинства пациентов в течение 3 дней улучшились признаки и симптомы. В 6 случаях из тридцати девяти передозировки привели к летальному исходу.
Мужчина в возрасте 33 лет проглотил 4,16 г верапамила. У него развилась асистолия, и он умер после проведенного лечения — промывания желудка, применения сиропа ипекакуаны, активированного угля, хлорида кальция, атропина, налоксона, инфузионной терапии, дофамина, чрескожной кардиостимуляции, внутривенного введения калия и эпинефрина.
У 22-летнего пациента, проглотившего 7,2—9,6 г медленно высвобождающегося верапамила, развилось угнетение дыхания, и он умер. Одна капсула нифедипина (10 мг) оказалась смертельной для 14-месячного ребенка.
г) Токсикокинетика. Блокаторы кальциевых каналов хорошо абсорбируются перорально и подвергаются экстенсивному гепатическому метаболизму и клиренсу первого порядка. Они все активно связываются с белками, но различаются по объему распределения. Степень связывания дилтиазема с белками составляет 80—90 %, а объем распределения — приблизительно 5,3 л/кг.
Клиренс дилтиазема после перорального приема протекает в соответствии с кинетикой реакций первого порядка, период полужизни составляет 5—10 ч независимо от принятой дозы. Однако для медленно высвобождающихся препаратов время максимальной абсорбции задерживается и период полужизни может быть более длительным из-за продолжающейся желудочно-кишечной абсорбции.
Токсическое действие медленно высвобождающихся блокаторов кальциевых каналов может быть задержано более чем на 12 ч после приема препарата. Все пациенты с передозировками медленно высвобождающихся блокаторов кальциевых каналов должны быть госпитализированы и находиться под наблюдением, даже если нет явных симптомов.
- Беременность и лактация. Пациентка, родившая близнецов, в период беременности принимала дилтиазем. Младенцы родились на 37-й неделе беременности. Во время беременности, в неона-тальном периоде и в последующие 6 мес не было признаков неблагоприятного действия ни на материнский организм, ни на плод. Менее 5 % терапевтической дозы нифедипина попадает в материнское молоко. Его пиридиновый метаболит также экскретируется в материнское молоко.
Концентрации нифедипина и его метаболита могут достичь максимальных значений, близких к обнаруживаемым в крови матери.
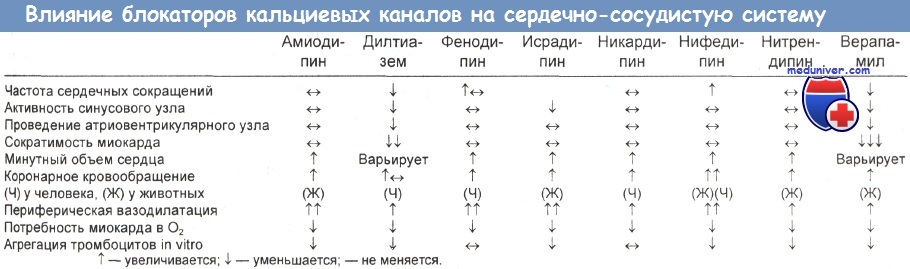
- Взаимодействие лекарственных средств. В таблице ниже приведены данные о взаимодействии лекарственных средств с участием блокаторов кальциевых каналов.
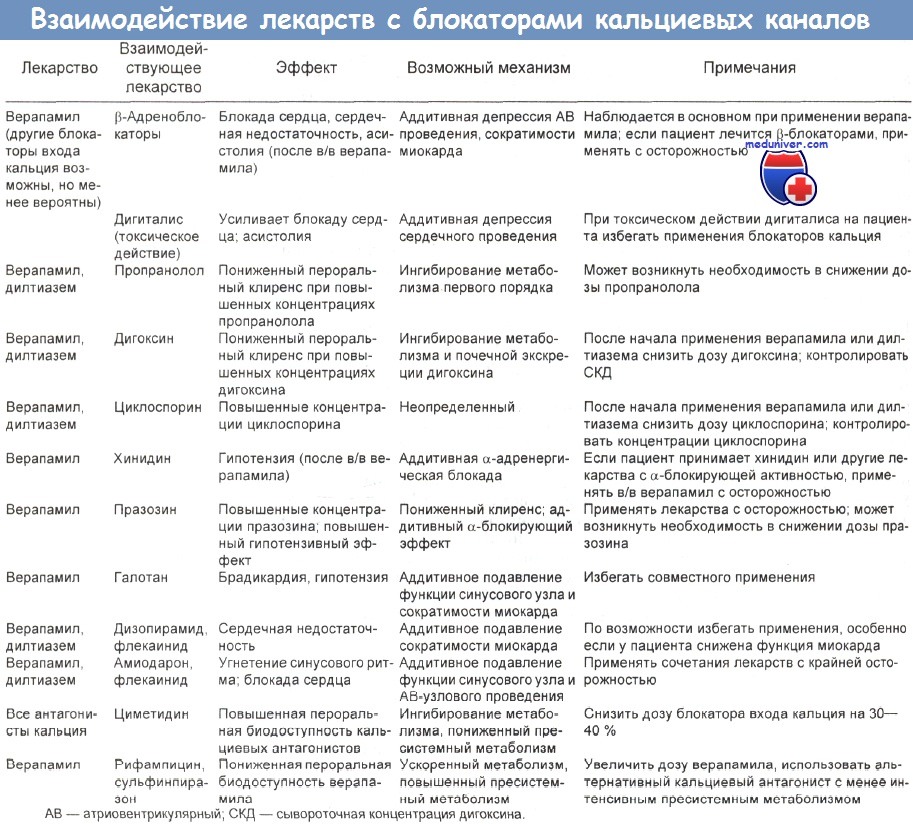
д) Механизм действия. Сердечно-сосудистые и почечные, метаболические и неблагоприятные эффекты блокаторов кальциевых каналов суммированы в таблице ниже. Ионы кальция (Са2+) играют определяющую роль в регулировании клеточного движения и транспорта, электрической активации возбудимых клеток и различных ферментативных реакций. Кальциевые каналы регулируют движение Са2+ из внеклеточного пространства во внутриклеточное.
Существует 3 основных типа кальциевых каналов: рецепторзависимые кальциевые каналы, зависимые от растяжения кальциевые каналы и чувствительные к напряжению (потенциалзависимые) кальциевые каналы. Рецепторзависимые кальциевые каналы стимулируются определенными лигандами, например нейрогормонами. Зависимые от растяжения кальциевые каналы могут стимулироваться при растягивании стенок некоторых сосудов.
Чувствительные к напряжению (потенциалзависимые) кальциевые каналы реагируют на изменения напряжения в клеточных мембранах, например такие, как деполяризация мембраны при открывании натриевых каналов. Потенциалзависимые кальциевые каналы состоят из гомологичных белковых субъединиц, обнаруживаемых также в натриевых и калиевых каналах.
Существует по меньшей мере 3 подтипа потенциалзависимых кальциевых каналов, классифицируемых по их проводимости и чувствительности к напряжению, — подтипы L, N и Т. Блокаторы кальциевых каналов воздействуют только на L-каналы.
Внеклеточная концентрация Са2+ примерно в 5000—10 000 раз выше концентрации внутри клеток, и этот градиент поддерживается обменными насосами Са 2+ /2Н+-АТФаза и 3Na 2+ /Ca 2+ . Открывание кальциевого канала обеспечивает приток Са2+ и повышает концентрацию Са2+ в цитозоле.
Антагонисты кальциевых каналов представляют собой разнородный класс лекарственных средств, которые блокируют движение ионов кальция из внеклеточной среды внутрь клеток через так называемые "медленные каналы". Эти средства очень сильно различаются по своей структуре. Они ингибируют фазу 0 деполяризации в пейсмекерных клетках сердца и фазу 2 плато в миоцитах, клетках Пуркинье и клетках гладких мышц стенок сосудов. Действуя таким образом, они вызывают расширение сосудов и обусловливают подавление сократимости миокарда, синусового и предсердно-желудочкового узлового проведения.
Лекарственные средства, входящие в класс блокаторов кальциевых каналов, различаются по своему фармакологическому действию. Нифедипин оказывает более сильное сосудорасширяющее действие, чем другие препараты, расслабляя гладкую мускулатуру периферических сосудов. Верапамил оказывает более сильное воздействие на коронарное кровообращение, снижая проводимость атриовентрикулярного узла и сократимость миокарда.
Дилтиазем влияет как на коронарное, так и на периферическое кровообращение, хотя воздействие на коронарные сосуды преобладает, т. е. в спектре препаратов этого типа он располагается ближе к верапамилу. Дилтиазем и верапамил оказывают отрицательное инотропное действие.

е) Клиническая картина. Факторы, предрасполагающие к токсическому действию блокаторов кальциевых каналов, перечислены в таблице ниже.
- Синдром отмены. Отмена препаратов, блокирующих кальциевые каналы, у пациентов с тяжелой гипертензией, даже в отсутствие в анамнезе стенокардии или инфаркта миокарда, может спровоцировать инфаркт миокарда. После отмены лекарств, блокирующих кальциевые каналы, у пациентов с нормальной коронарной ангиографией, лечившихся по поводу ишемической боли в груди, обострились стенокардия и инфаркт миокарда. Конкретный механизм интоксикации не установлен.
Препараты верапамила пролонгированного действия способны индуцировать образование конкремента из-за желатинового покрытия пилюль. Гипотензия и брадиаритмии могут развиться даже через 18 ч после приема препарата, несмотря на промывание желудка и применение активированного угля.
Интоксикация медленно высвобождающимся верапамилом может вызвать атриовентрикулярную блокаду, брадикардию, приводящую к асистолии или гипертензии, остановку сердца в систоле или функциональный ритм с предсердно-желудочковой диссоциацией даже через 26 ч после первых очищающих и поддерживающих процедур, призванных стабилизировать состояние пациента. Тяжелая гипотензия может привести к инфаркту головного мозга после передозировки верапамила.
- Медленно высвобождающийся верапамил. Проявления передозировок верапамила быстрого и пролонгированного действия сходны. При передозировках верапамила пролонгированного действия часто отмечается замедленное и более длительное проявление токсических признаков и симптомов.
При передозировках, в 5—10 раз превышающих терапевтическую дозу, клинические проявления обычно обнаруживаются через 30—60 мин после приема препарата. Признаки токсического действия на центральную нервную систему включают сонливость, спутанность сознания и в редких случаях припадки. Кома обычно вторична относительно острой сердечно-сосудистой недостаточности. Признаки желудочно-кишечной интоксикации могут включать тошноту и рвоту.
К числу метаболических токсических эффектов относятся гипергликемия, являющаяся следствием пониженного образования инсулина, и метаболический ацидоз, являющийся вторичным относительно молочнокислого ацидоза, развивающегося вследствие слабой тканевой перфузии. Гипотензия — это наиболее распространенный показатель токсического воздействия на сердечнососудистую систему. Она вызывается главным образом расширением сосудов и пониженной сократимостью миокарда.
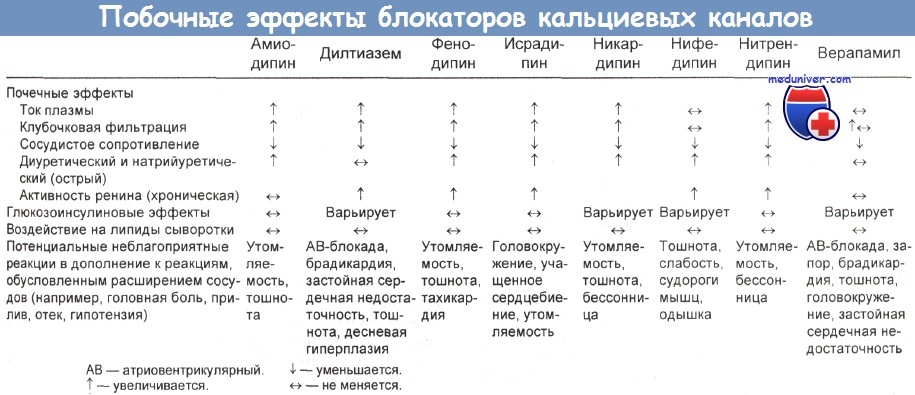
ж) Лабораторные данные. Стандартные методы анализа лекарственных средств непригодны для обнаружения блокаторов кальциевых каналов.
- Аналитические методы. Для определения концентраций верапамила, норверапамила и его дезалкилированных производных в плазме целесообразно применять метод ВЭЖХ с обращенной фазой. Порог обнаружения для всех соединений ниже 5 нг/мл.
Для количественного анализа дилтиазема и его метаболитов применим метод газовой хроматографии. Методами ВЭЖХ установлено, что дилтиазем устойчив по меньшей мере в течение 6 нед при температурах ниже 25 °F (-3,89 °С).
- Уровни в крови:
Верапамил. Данные об уровнях верапамила подтверждают факт интоксикации, но не могут помочь при неотложной терапии.
Дилтиазем. Терапевтический диапазон концентраций дилтиазема в крови примерно от 100 до 200 мкг/л. Анализ литературных данных показывает, что при концентрациях дилтиазема в крови до 500 мкг/л у асимптоматических пациентов могут наблюдаться блокада сердца I степени и синусовая брадикардия. При концентрациях от 500 до 1000 мкг/л наблюдается гипотензия. При концентрациях от 1000 до 1500 мкг/л отмечались аномалии проводимости и гипотензия.
При концентрациях выше 1500 мкг/л возникает необходимость использования временных водителей ритма. При концентрациях выше 6100 мкг/л большая часть пациентов умирают.
Нифедипин. Примерно через 2 ч после приема 250 мг нифедипина с этиловым спиртом концентрация нифедипина в крови 34-летнего пациента составила 181 нг/мл (терапевтический уровень 25—100 нг/мл). Через 2 ч концентрация снизилась до 70 нг/мл. Пациент выздоровел. Через 10 ч после приема сверхвысокой дозы нифедипина таблеток пролонгированного действия (600 мг) концентрация нифедипина в крови возросла до 604 нг/мл, уровень основного метаболита составлял 100 нг/мл.
- Гипергликемия. Гипергликемия и метаболический ацидоз могут развиться при очень больших передозировках верапамила. Гипергликемия развивается также после передозировок нифедипина. При сильных передозировках необходимо контролировать концентрации Са2+, Mg2+, К+ и Na+.
- Сывороточный кальций. После передозировок обычно выявляются аномальные концентрации кальция в сыворотке. После того как 24-летний пациент проглотил 4 г верапамила, концентрация Са2+ в сыворотке составляла 1,5 ммоль/л (6,1 мг/100 мл). Электрокардиограмма показала предсердно-желудочковую блокаду III степени. После внутривенного вливания 10 мл 10 % глюконата кальция сердечный ритм преобразовался в предсердно-желудочковую блокаду II степени.
Кальций может улучшить проведение, но обычно он мало влияет на гипотензию. В случае тяжелой гипокальциемии благоприятное действие может оказать применение высоких доз кальция, однако, хотя введение солей кальция часто бывает очень полезным в качестве одного из первоочередных мероприятий при лечении передозировок верапамила, в случаях, не поддающихся лечению, следует предусмотреть возможность использования инотропных препаратов или электрокардиостимуляции.
- Электрокардиограмма. Электрокардиографические аномалии после передозировок верапамила включают пролонгированное проведение (удлиненные интервалы QRS, P—R, Q—T), различные степени предсердно-желудочковой блокады и ассистолию.
Видео фармакологические, побочные эффекты блокаторов кальциевых каналов
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление цетиризином и его побочные эффекты
Токсикокинетика и дозы антагонистов Н1-рецепторов приведены в отдельных таблицах ниже соответственно. В отдельной таблице обобщены фармакологические свойства неседативных и классических антигистаминных средств. Структурные формулы этих веществ приведены на рисунке ниже.
Цетиризин, антагонист Н1-рецепторов второго поколения, является производным пиперазина и основным метаболитом гидроксизина в человеческом организме. Он лишен сродства к мускариновым, холинергическим, альфа-адренергическим, 5-гидрокситриптаминовым (серотониновым), дофаминергическим (D2) и связанным с кальциевыми каналами рецепторам.
Рекомендуемая суточная доза составляет 10 мг. Цетиризин быстро всасывается (примерно на 100 %) и дает пик плазменной концентрации (около 250—500 мг/мл) через 1 ч после приема внутрь 10 и 20 мг. Объем распределения близок к 0,6 л/кг.
Приблизительно 93 % средства связывается с белками плазмы. Период полужизни в фазе выведения 7 ч. Цетиризин выводится главным образом почками в исходной форме. Общий клиренс равен примерно 0,05 л/ч на 1 кг. Доза 10 мг вызывает седативный эффект с такой же частотой, как и другие "неседативные" антигистаминные средства.
При сильной передозировке (150—300 мг) седатация может быть единственным клиническим осложнением и со временем полностью проходит. Лечение передозировки главным образом симптоматическое и поддерживающее. Летальных исходов не отмечалось.
Циннаризин и флунаризин — это производные пиперазина, структурно близкие к некоторым фенотиазинам, что, возможно, объясняет их тенденцию индуцировать экстрапирамидные эффекты. Для определения флунаризина в сыворотке существует чувствительный метод газовой хроматографии.
bid — 2 раза в день; tid — 3 раза в день; qid — 4 раза в день; В — взрослые; Д — дети.
* Детская доза предназначена для пациентов с массой тела не более 40 кг.
** Таблетка этого размера соответствует препарату с пролонгированным действием.
*** Для таблеток пролонгированного действия.
**** Не утвержден для применения в США. Структура гистамина и типичных антагонистов Н1-рецепторов.
Для практических целей Н1-антагонисты сейчас часто делят на средства первого поколения с относительно выраженным седативным действием и средства второго поколения, у которого это действие заметно слабее.
Последняя группа включает большинство Н1-антагонистов, появившихся после 1981 г., из которых лучше всего известны терфенадин, астемизол, лоратадин и цетиризин.
Некоторые Н1-антагонисты второго поколения трудно отнести к какому-либо традиционному классу — алкиламинам (пример — хлорфенирамин),
этаноламинам (пример—дифенгидрамин), пиперазинам (пример — гидроксизин), пиперидинам, этилендиаминам и фенотиазинам. Например, хотя терфенадин,
астемизол, лоратадин, кетотифен и левокабастин содержат в своих молекулах пиперидиновое кольцо, их нельзя объединить в одну группу химических соединений.
Цетиризин, кетотифен и азеластин не утверждены для использования в США.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Б.Б. Яцинюк, Ю.В. Мешкова
КЛИНИЧЕСКИЙ СЛУЧАЙ ОСТРОГО ЛЕТАЛЬНОГО ОТРАВЛЕНИЯ ЦИННАРИЗИНОМ У РЕБЕНКА
Введение. Острые отравления циннаризином относятся к редким видам острых лекарственных отравлений (орфанные заболевания) как у взрослых, так и у детей, которые проявляются депрессией синусовой зоны и гемодинамическими нарушениями , степень выраженности которых зависит от принятой дозы. По данным Г.Н. Суходоловой, (2011) в структуре острых отравлений - отравления лекарственными препаратами занимают более 60 %. В ХМАО-Югре за 2007-2011 гг. острые отравления у детей увеличились на 54,9% . Особенности реакций организма ребенка на поступление токсической дозы вещества может качественно и количественно отличаться от таковых у взрослых, учитывая морфологические и функциональные особенностей детского организма. Поэтому, описание даже одного случая является интересным в плане накопления клинических и патоморфологических особенностей течения химической травмы .
Описание случая. Нами описывается клинический случай острого отравления циннаризином у ребенка 2 лет, закончившийся летальным исходом. Препарат принимался ребенком в течение 1-2 часов ( 14.00-15.00), дома, в виду его доступности . После принятия 1 гр. циннаризина в 17.30 наблюдалась рвота (родители обнаружили отсутствие 40 таблеток, по 25 мг, в упаковке). На догоспитальном этапе промыт желудок и введен энтеросорбент. При промывании в желудочном содержимом растворенные таблетированные формы не обнаружены. В 18.00 при поступлении в стационар: ЧСС - 100 в мин., АД 100/50 мм рт. ст., ЧДД - 20 в мин., уровень сознания - сопор (оценка по шкале Глазго - 12 баллов). В 18.05 в отделении реанимации (АД - 99/45 мм.рт.ст., ЧСС - 117 в мин.) катетеризирована периферическая вена и начата инфузионная терапия кристаллоидными растворами 80 мл в час, введен глюконат кальция 2,0 мл в/в , дофамин в дозе 8 мкг/кг мин и дексаметазон 8 мг в/в. Общее состояние в 18.10 оценено как крайне тяжелое: кожный покров бледный, АД - 65/29 мм.рт.ст., ЧСС - 52 в мин., зрачки D = S , фотореакция снижена, мышечный тонус диффузно снижен, наблюдаются спонтанные движения во всех конечностях. В 18.15 возникли клонико-тонические судороги, которые не купировались введением сибазона 0,5 % - 1,0 мл. Больная переведена на ИВЛ аппаратом Drager . Pin 15 cm Н20, PEEP + 4 cm H 2 0,1: E = 1:1,5, ЧД 30 в мин, Fi 02 40 % (ЧСС 117 в мин., АД 100/50 мм.рт.ст., Sp 02 98 %). Дальнейшее падение уровня АД - 75/45 мм.рт.ст. (19.07) и ЧСС - менее 50 мин и введение атропина 0,1 % - 0,2 мл в/в, не увеличило ЧСС. Начатые реанимационные мероприятия при мониторном контроле успеха не имели, в 19.47 констатирована биологическая смерть.
Проведенное судебно-химическое исследование обнаружило циннаризин в крови, моче, желчи, печени, почке, желудке, тонком кишечнике (таблетки, изъятые в ходе оперативных мероприятий, установили содержание циннаризина). При гистологическом исследовании: в головном мозге выявлено нарушение кровообращения в виде полнокровия сосудов с наличием гиалиновых тромбов, разделение плазмы и форменных элементов крови в сосудах микроциркуляции, периваскулярное плазматическое пропитывание и умеренный отек вещества мозга; в миокарде: очаговый коронароспазм - спазмирование отдельных мелких интрамуральных артерий, гиперхромия ядер эндотелия, венозное полнокровие, очаговая фрагментация волокон миокарда и их волнообразная деформация; в легких: полнокровие сосудов, мелкие кровоизлияния в ткань легкого, умеренный внутриальвеолярный отек (в двух препаратах просветы альвеол заполнены светло-эозинофильной пенистой жидкостью, в других препаратах просветы альвеол свободные, в которых определяется незначительное количество макрофагов); в надпочечниках: полнокровие сосудов паренхимы, в соединительнотканной капсуле единичные мелкие кровоизлияния в виде скоплений рыхло расположенных эритроцитов; в почках и поджелудочной железе изменений не выявлено; в печени и селезенке - полнокровие сосудов; в тимусе: полнокровие сосудов, умеренный отек стромы; в тонком кишечнике: крупно- и мелкоочаговые поверхностные кровоизлияния в слизистом слое.
Анализируя описанный случай острого отравления циннаризином, можно говорить, что принятая доза 1 гр. вызывает кардиогемодинамические нарушения и может быть летальной. Выявленная патоморфологическая картина констатирует выраженные нарушения микроциркуляторного русла, свидетельствуя о остром состоянии. Одной из мер профилактики острых отравлений у детей, по нашему мнению, должно являться знание родителями юридических мер ответственности и недоступности в домашних условиях различных лекарственных форм и других химических веществ.
Читайте также:

