Можно ли применять азитромицин при коклюше
Обновлено: 18.04.2024
Коклюш (wooping-cough - англ.; Keuchhusten - нем; Coqueluche - франц.) и паракоклюш - острые инфекционные болезни, клинически неотличимые друг от друга. Характеризуется острым катаром дыхательных путей и приступами спазматического кашля.
Этиология.
Возбудитель коклюша (Bordetella pertussis) представляет собой короткую палочку с закругленными концами (0,2-1,2 мкм), грамотрицательную, неподвижную, хорошо окрашивающуюся анилиновыми красками. В антигенном отношении неоднородна. Антиген, который обусловливает образование агглютининов (агглютиноген), состоит из нескольких компонентов. Они названы факторами и обозначаются цифрами от 1 до 14. Фактор 7 является родовым, фактор 1 содержит В. pertussis, 14 - 5. parapertussis, остальные встречаются в разных комбинациях; для возбудителя коклюша это факторы 2, 3, 4, 5, 6, для паракоклюша - 8, 9, 10. Реакция агглютинации с адсорбированными факторными сыворотками позволяет дифференцировать виды бордетелл и определять их антигенные варианты. Возбудители коклюша и паракоклюша очень неустойчивы во внешней среде, поэтому посев нужно делать сразу же после взятия материала. Бактерии быстро погибают при высушивании, ультрафиолетовом облучении, под влиянием дезинфицирующих средств. Чувствительны к эритромицину, левомицетину, антибиотикам тетрациклиновой группы, стрептомицину.
Эпидемиология.
Патогенез.
Воротами инфекции является слизистая оболочка респираторного тракта. Коклюшные микробы прикрепляются к клеткам мерцательного эпителия, где они размножаются на поверхности слизистой оболочки, не проникая в кровоток. На месте внедрения возбудителя развивается воспалительный процесс, угнетается деятельность ресничного аппарата клеток эпителия и увеличивается секреция слизи. В дальнейшем происходит изъязвление эпителия дыхательных путей и очаговый некроз. Патологический процесс наиболее выражен в бронхах и бронхиолах, менее выраженные изменения развиваются в трахее, гортани и носоглотке. Слизисто-гнойные пробочки закупоривают просвет мелких бронхов, развивается очаговый ателектаз, эмфизема. Наблюдается перибронхиальная инфильтрация. В генезе судорожных приступов имеет значение сенсибилизация организма к токсинам коклюшной палочки. Постоянное раздражение рецепторов дыхательных путей обусловливает кашель и приводит к формированию в дыхательном центре очага возбуждения типа доминанты. Вследствие этого типичные приступы спазматического кашля могут быть вызваны и неспецифическими раздражителями. Из доминантного очага возбуждение может иррадиировать и на другие отделы нервной системы, например на сосудодвигательный (повышение АД, спазм сосудов). Иррадиацией возбуждения объясняется также появление судорожных сокращений мышц лица и туловища, рвоты и других симптомов коклюша. Перенесенный коклюш (как и противококлюшные прививки) не обеспечивает напряженного пожизненного иммунитета, поэтому возможны повторные заболевания коклюшем (около 5% случаев коклюша приходится на взрослых людей).
Симптомы и течение.
Инкубационный период продолжается от 2 до 14 дней (чаще 5-7 дней). Катаральный период характеризуется общим недомоганием, небольшим кашлем, насморком, субфебрильной температурой. Постепенно кашель усиливается, дети становятся раздражительными, капризными. В конце 2-й недели болезни начинается период спазматического кашля. Приступы судорожного кашля проявляются серией кашлевых толчков, затем следует глубокий свистящий вдох (реприз), сменяющийся рядом коротких судорожных толчков. Число таких циклов во время приступа колеблется от 2 до 15. Приступ заканчивается выделением вязкой стекловидной мокроты, иногда в конце приступа отмечается рвота. Во время приступа ребенок возбужден, лицо цианотично, вены шеи расширены, язык высовывается изо рта, уздечка языка часто травмируется, может наступить остановка дыхания с последующей асфиксией. У детей раннего возраста репризы не выражены. В зависимости от тяжести заболевания число приступов может варьировать от 5 до 50 в сутки. Период судорожного кашля длится 3-4 нед, затем приступы становятся реже и наконец исчезают, хотя "обычный" кашель продолжается еще в течение 2-3 нед (период разрешения). У взрослых заболевание протекает без приступов судорожного кашля, проявляется длительным бронхитом с упорным кашлем. Температура тела остается нормальной. Общее самочувствие удовлетворительное. Стертые формы коклюша могут наблюдаться у детей, которым проведены прививки.
Осложнения.
Наиболее частым осложнением является пневмония, обусловленная коклюшной палочкой или вторичной бактериальной инфекцией. У детей до 3 лет около 90% летальных исходов обусловлено пневмонией. Может наступить обострение туберкулеза. Из других осложнений наблюдается острый ларингит со стенозом гортани (ложный круп), бронхиолиты, ателектазы, энцефалопатия, остановка дыхания, пупочная, паховая грыжа, разрыв диафрагмы, выпадение прямой кишки. У взрослых осложнения бывают редко.
Диагноз и дифференциальный диагноз.
Достоверный диагноз в катаральном периоде может быть поставлен после получения результатов бактериологических исследований. Основанием для исследования в этих случаях обычно служат эпидемиологические данные (контакт с больными коклюшем, отсутствие данных о прививках и др.). В периоде спазматического кашля диагноз коклюша поставить значительно легче, так как появляются типичные приступы. Однако нужно учитывать, что иногда приступы кашля, сходные с коклюшными, могут быть обусловлены другими причинами (аденовирусная инфекция, вирусные пневмонии, сдавление дыхательных путей при злокачественных новообразованиях, инфекционном мононуклеозе и др.), с другой стороны, коклюш может протекать атипично без характерных приступов (у привитых детей, у взрослых). Основным методом лабораторного подтверждения диагноза является выделение возбудителя коклюша. Частота выделения зависит от сроков взятия материала; на 1-й неделе заболевания положительные результаты удается получить у 95% больных, на 4-й - лишь у 50%, а начиная с 5-й недели, микроб выделить уже не удается. Материал из носоглотки берут сухим тампоном с немедленным посевом на чашки с селективной питательной средой. Используют также метод "кашлевых пластинок", при котором чашка Петри с питательной средой устанавливается перед ртом кашляющего ребенка (на расстоянии около 10 см), удерживается в таком положении несколько секунд, чтобы уловить 5-6 кашлевых толчков. Чашку с посевом быстро закрывают крышкой и помещают в термостат. При транспортировке оберегают от охлаждения (заворачивают в бумагу, вату, в контейнер помещают грелку, заполненную горячей водой). Однако по частоте выделения возбудителей коклюша метод "кашлевых пластинок" значительно уступает взятию материала тампоном. Серологические методы можно использовать для ретроспективной диагностики, а также у больных с отрицательными результатами бактериологических исследований. Из старых методов можно использовать РСК, РПГА, реакцию агглютинации. Диагностическим считается нарастание титров антител в 4 раза и более, а также высокие титры антител (1:80 и выше).
В последнее время успешно используют иммуноферментный метод для обнаружения антител в сыворотке (иммуноглобулины класса М) и в носоглоточной слизи (иммуноглобулины класса А). Эти антитела появляются со 2-3-й недели болезни и сохраняются в течение 3 мес. Дифференцируют в катаральном периоде болезни от ОРЗ, в период спазматического кашля от других заболеваний, сопровождающихся упорным кашлем при нормальной температуре тела и отсутствии признаков обшей интоксикации.
Лечение.
Больных в возрасте до 1 года, а также больных с осложнениями, тяжелыми формами коклюша госпитализируют. Остальные больные могут лечиться дома. Антибиотики могут быть эффективными в катаральном периоде. Они могут подавить возбудителя и купировать дальнейшее развитие болезни. Назначение антибиотиков в период спазматического кашля не влияет на клиническую симптоматику. При легких и стертых формах антибиотики не назначают. Их назначают при тяжелых и осложненных формах коклюша, когда отмечается наслоение вторичной инфекции. Возбудитель коклюша чувствителен ко многим антибиотикам, однако предпочтительнее назначать эритромицин или азитромицин. Эффективны также левомицетин и тетрациклин, однако левомицетин более токсичен, а тетрациклин противопоказан детям до 8 лет. При наслоении вторичной инфекции можно назначать пенициллин и стрептомицин. Специфические противококлюшные иммуноглобулины не оказывали влияния ни на длительность бактериовыделения, ни на длительность и выраженность клинической симптоматики и в настоящее время не рекомендуются. Для лечения больных коклюшем важен общий режим, чистый воздух, спокойная обстановка, устранение всех факторов, способствующих возникновению приступов, назначение витаминов, оксигенотерапия. Периодически рекомендуется отсасывание слизи из дыхательных путей, особенно важно это во время апноэ, при необходимости проводят искусственную вентиляцию легких. Рекомендуют препараты антигистаминного действия (димедрол, пипольфен), ингаляции аэрозолей с протеолитическими ферментами (химопсин, химотрипсин), которые облегчают отхождение вязкой мокроты. При тяжелых формах коклюша некоторые авторы отмечали эффективность кортикостероидных препаратов.
Профилактика и мероприятия в очаге.
Специфическая профилактика проводится всем детям от 3 мес до 3 лет, не болевшим коклюшем. Курс вакцинаций состоит из 3 внутримышечных инъекций 0,5 мл вакцины (АКДС) с интервалом 1,5 мес. Ревакцинацию делают через 1,5-2 года после законченной 3-кратной вакцинации. Детей старше 3 лет вакцинируют только против дифтерии и столбняка. Вакцинация или полностью предупреждает возникновение заболевания (у 70-80%) или же заболевание протекает в легкой форме. При вакцинации (коклюш - дифтерия - столбняк) отмечались различные побочные реакции, связанные преимущественно с коклюшным компонентом, в частности, асептический менингит, многоформная экссудативная эритема, синдром Гийена-Барре, периферические мононевриты, тромбоцитопения, гемолитическая анемия, энцефалопатия (10 на 1 млн привитых), анафилактические реакции (2 на 100 000 привитых). Однако положительный эффект вакцинации намного превышает риск развития серьезных неврологических осложнений. Так, в США до появления вакцины от коклюша погибало столько же детей, сколько от всех других инфекционных болезней вместе взятых [R. Feigin, F. Murphy, 1989, 1993]. В настоящее время для иммунизации взрослых апробируется цельноклеточная противококлюшная вакцина, она менее реактогенна, чем бесклеточная.
Из дошкольных учреждений изолируют всех больных коклюшем и детей в возрасте до 1 года, больных паракоклюшем. Эти больные при отсутствии клинических противопоказаний допускаются в детские учреждения на 25-й день болезни. Здоровых бактерионосителей при коклюше изолируют до получения двух отрицательных результатов бактериологических исследований, но не ранее 14 дней со дня выделения возбудителя. Детей в возрасте до 7 лет, контактировавших с больным коклюшем, разобщают на 14 дней со дня изоляции больного; на такой же срок устанавливают карантин для детей в дошкольном учреждении. Если здоровым бактерионосителям, контактировавшим с больным коклюшем, а также больным в начальный период болезни назначить эритромицин (в возрастных дозах в течение 5-7 дней), то это быстро прекращает бактериовыделение и купирует развитие болезни у контактировавших лиц.
Паракоклюш - острая инфекционная болезнь, сходная по клинической картине с коклюшем, но протекающая более легко. Возбудитель паракоклюша по биохимическим, антигенным и культуральным свойствам легко дифференцировать от возбудителя коклюша. На паракоклюш приходится 12-76% всех выделенных культур. После паракоклюша возможно заболевание коклюшем; паракоклюшем могут заболеть привитые против коклюша и перенесшие коклюш. Заразный период обычно не превышает 2 нед. Осложнения при паракоклюше наблюдаются редко. Случаев смерти не бывает.
Существует большое количество публикаций и практических рекомендаций международных обществ, посвященных применению макролидов, в целом, и азитромицина, в частности, при терапии острого среднего отита [3], острого стрептококкового тонзиллита/фарингита [4], острого бактериального риносинусита [5] и внебольничной пневмонии [6,7] у детей. В то же время значительно меньше внимания уделяется месту азитромицина в лечении коклюша, муковисцидоза, рецидивирующих респираторных инфекций, болезни кошачьей царапины, кишечных инфекций, хламидийной инфекции у новорожденных, о которых и пойдет речь в данном обзоре.
Клинико-фармакологические свойства азитромицина
Антимикробная активность. Азитромицин дает преимущественно бактериостатический эффект. Опыты in vitro и результаты клиническим исследований свидетельствуют о том, что азитромицин активен в отношении многих грамположительных кокков, таких как Streptococcus pneumoniae, Streptococcus pyogenes или β-гемолитический стрептококк группы А (БГСА), Streptococcus agalactiae, метициллиночувствительные штаммы Staphylococcus aureus. Стафилококки и стрептококки, устойчивые к эритромицину, резистентны к азитромицину. Из грамотрицательных микроорганизмов азитромицин активен в отношении Neisseria gonorrhoeae, Haemophilus ducreyi, Moraxella catarrhalis и является самым активным среди макролидов против Haemophilus influenzae, включая β-лактамазопродуцирующие штаммы. Кроме того, азитромицин активен против Campylobacter spp., Bordetella pertussis, Bartonella spp. В отличие от других макролидов, азитромицин in vitro действует на отдельных представителей семейства Enterobacteriaceae, кишечную палочку, шигеллы, сальмонеллы. К азитромицину чувствительны также внутриклеточные патогены (Chlamydia trachomatis, Chlamydophila pneumoniae, Mycoplasma pneumoniae, Ureaplasma urealyticum, Mycoplasma hominis, Legionella pneumophila), спирохеты (Borrelia burgdorferi, Treponema pallidum), некоторые простейшие (Toxoplasma gondii, Cryptosporidium spp.) [1,8,9,10].
Фармакокинетика. Биодоступность азитромицина при назначении внутрь составляет около 40%. Препарат устойчив к действию соляной кислоты желудочного сока. Максимальная концентрация в сыворотке крови достигается через 2,5-3 ч. При 3- или 5-дневном приеме возможны колебания концентрации вследствие поглощения антибиотика тканями с его последующим высвобождением [1,10]. Азитромицин рекомендуют принимать перед едой, так как под влиянием пищи его биодоступность, по некоторым данным, может снизиться [11]. Однако в трех исследованиях было показано, что пища существенно не влияет на биодоступность азитромицина [12].
Связывание с белками плазмы крови зависит от концентрации азитромицина в крови и может варьировать от 7 до 51%. Благодаря высокой липофильности азитромицин хорошо распределяется в организме, проникая во многие органы и ткани и накапливаясь в них в высоких концентрациях [13]. Концентрации азитромицина в тканях в десятки-сотни раз превышают сывороточные уровни и сохраняются в течение длительного времени. Наиболее высокие бактерицидные концентрации азитромицина наблюдаются в миндалинах, аденоидах, бронхиальном секрете, слизистой оболочке бронхов, альвеолярной жидкости, экссудате среднего уха [10,14]. В тканях азитромицин локализуется преимущественно внутриклеточно, в основном, в лизосомах альвеолярных макрофагов, нейтрофилов, моноцитов и фибробластов. По степени накопления в этих клетках азитромицин имеет преимущества перед всеми другими макролидами [15]. Благодаря аккумуляции в фагоцитарных клетках, способных захватывать азитромицин из крови, интерстициальной жидкости и фибробластов, препарат избирательно распределяется в очаги бактериального воспаления [16]. Концентрации антибиотика в них на 24-36% выше, чем в здоровых тканях [17].
Таблица 1. Нежелательные лекарственные реакции (НЛР), связанные с применением азитромицина у детей
| Источник | Тип исследования | Число участников, получавших азитромицин | Частота НЛР | Наиболее частые НЛР |
| Hopkins S.. et al, 1993 [25] | Рандомизированное контролируемое исследование | 606 | 7,6% | ЖКТ (5,6%), со стороны кожи (1,5%), головная боль (0,3%) |
| Treadway G. et al, 1996 [26] | Мета-анализ 45 клинических исследований | 2655 | 8,7% | ЖКТ (5,3%), со стороны кожи (1,1%), головная боль (0,2%) |
| Treadway G. et al, 2001 [23] | Данные 16 клинических исследований | 1213 | 7,9% | ЖКТ (6,5%), со стороны кожи (1,1%), головная боль (0,2%) |
Лекарственные взаимодействия. В отношении лекарственных взаимодействий азитромицин безопаснее большинства других макролидов, поскольку он в минимальной степени влияет на активность печеночной ферментной системы цитохрома Р-450 [27]. Тем не менее, азитромицин может повышать сывороточную концентрацию циклоспорина. Антациды снижают пиковую концентрацию азитромицина в сыворотке крови. Назначение азитромицина с нелфинавиром приводит к повышению сывороточной концентрации азитромицина. Применение азитромицина у пациентов, получающих статины (ловастатин, симвастатин), может быть фактором риска развития миопатии или рабдомиолиза [10].
Перспективные области клинического применения азитромицина в педиатрии
Инфекции желудочно-кишечного тракта. Ограниченные возможности антибактериальной терапии инфекций желудочно-кишечного тракта у детей и рост резистентности возбудителей к антибиотикам диктуют необходимость поиска новых подходов к терапии шигеллезов у детей [28]. Одним из них является изучение эффективности азитромицина с учетом его фармакокинетических и фармакодинамических данных и клинического опыта применения у взрослых [29,30]. Проведены и первые успешные клинические исследования эффективности азитромицина при шигеллезах у детей.
Во время вспышки шигеллеза в Израиле в 2003 г. было инфицировано 73 человека, среди которых 83% составили дети в возрасте от 6 месяцев до 18 лет. Всем детям с бактериологически подтвержденным шигеллезом назначали налидиксовую кислоту в дозе 55 мг/кг/сут в 4 приема внутрь в течение 5 дней. Поскольку к моменту завершения курса лечения у 25 детей сохранялась диарея, было принято решение о замене налидиксовой кислоты азитромицином, который назначали внутрь в дозе 10 мг/кг/сут в течение 3 дней. У всех детей, принимавших азитромицин, диарея прошла через 48 ч после начала терапии, в то время как у пациентов, получавших только налидиксовую кислоту, диарея была купирована лишь в 65% случаев [31].
Таким образом, результаты описанных исследований демонстрируют клиническую и микробиологическую эффективность азитромицина при шигеллезах у детей. Простой режим дозирования, быстрые темпы клинического улучшения и достаточный уровень эрадикации шигелл, обусловленный высокими внутриклеточными концентрациями азитромицина, являются основанием для проведения дальнейших исследований, направленных на подтверждение правильности данной терапевтической стратегии.
Коклюш. Препаратом выбора при лечении и постэкспозиционной профилактике коклюша считают эритромицин, который назначают на 14 дней [33]. Необходимость применения препарата 4 раза в сутки и достаточно высокая частота нежелательных реакций со стороны желудочно-кишечного тракта снижают приверженность к лечению эритромицином [34]. В последние десятилетия в исследованиях in vitro была продемонстрирована активность азитромицина в отношении В. pertussis, а в клинических исследованиях подтверждена эффективность данного препарата (табл. 2).
Таблица 2. Исследования, в которых изучалась эффективность азитромицина при лечении коклюша у детей
Кларитромицин 10 мг/кг один раз в сутки 7 дней, n=9
Эритромицин (исторический контроль) 40-50 мг/кг/сут (в 3 приема) 14 дней, n=34
Азитромицин 10 мг/кг/сут 3 дня, n=20
89,5, 100 и ??7,1% через 7, 14 и 21 день
Эритромицин 40-50 мг/кг/сут 14 дня, n=15
Эритромицин 40 мг/кг/сут (в 3 приема) 10 дней, n=238
По данным Кокрановского систематизированного обзора, посвященного применению антибиотиков для лечения и профилактики коклюша (12 рандомизированных и квазирандомизированных контролируемых исследований, n=1720), не отмечено статистически значимых различий между клинической и микробиологической эффективностью, а также частотой возникновения микробиологических рецидивов инфекции, вызванной В. pertussis, при использовании длительного режима терапии (эритромицин 14 дней) и коротких курсов терапии (азитромицин 3 дня, кларитромицин 7 дней или эритромицина эстолат 7 дней). Однако при использовании коротких курсов антибактериальной терапии была достоверно ниже частота возникновения нежелательных явлений. По мнению авторов, для лечения коклюша с точки зрения клинической и микробиологической эффективности и переносимости лучше всего назначать азитромицин на 3 дня или кларитромицин на 7 дней, при этом применение антибиотиков для постэкспозиционной профилактики коклюша не оправдано [33].
В настоящее время азитромицин включен в рекомендации по лечению коклюша. Его необходимо назначать детям до 6 месяцев в дозе 10 мг/кг один раз в сутки в течение 5 дней, детям старше 6 месяцев - 10 мг/кг в первый день (не более 500 мг), далее по 5 мг/кг (2-5-й дни терапии) [34].
Рецидивирующие инфекции дыхательных путей. Традиционно считалось, что большинство случаев так называемых острых респираторных заболеваний (ОРЗ), острого бронхита и ларинготрахеита вызваны вирусами и не требуют назначения антибиотиков. Однако в последнее время появляется все больше информации о роли атипичных возбудителей (М. pneumoniae, С. pneumoniae и др.) в этиологии подобных инфекций, особенно у лиц молодого возраста без сопутствующей патологии [39, 40] и у детей [41]. Так, частота обнаружения С. pneumoniae и М. pneumoniae при острых респираторных инфекциях составляет, в среднем, до 10% во внеэпидемический период и может достигать 25-50% во время эпидемических вспышек [39]. Препаратами выбора при лечении инфекций, предположительно вызванных атипичными возбудителями (хламидиями и микоплазмами), являются макролиды.
S.Esposito и соавт. изучали роль М. pneumoniae и С. pneumoniae в развитии острых инфекций дыхательных путей у детей с рецидивирующими ОРЗ и влияние антибактериальной терапии на состояние пациентов при остром заболевании и частоту возникновения рецидивов. В исследовании приняли участие 353 ребенка в возрасте от 1 до 14 лет, контрольную группу составили 208 здоровых детей. Рандомизированные пациенты получали азитромицин (10 мг/кг/сут 3 дня в неделю на протяжении 3 недель) в сочетании с симптоматической терапией и только симптоматическое лечение. Острую инфекцию, вызванную М. pneumoniae и/или С. pneumoniae, диагностировали, если у ребенка отмечалось значительное нарастание титра специфических антител в парных сыворотках и/или обнаруживали ДНК бактерии в назофарингеальном аспирате. Инфекции, вызванные атипичными возбудителями, были диагностированы у 54% пациентов (и только у 3,8% здоровых детей, р<0,0001). Краткосрочный (на протяжении 1 месяца) клинический эффект у пациентов, получавших азитромицин, отмечался значительно чаще, чем у детей, получавших только симптоматическую терапию, однако различия были статистически значимыми только в группе пациентов с инфекцией, вызванной атипичными возбудителями. В то же время долговременный клинический эффект (на протяжении 6 месяцев) достоверно чаще отмечался у детей, получавших азитромицин, независимо от того, была ли инфекция у этих пациентов вызвана атипичными или другими возбудителями. Авторы полагают, что атипичные бактерии, играют определенную роль в возникновении рецидивирующих инфекций дыхательных путей у детей, а длительная терапия азитромицином может значительно улучшить течение острого эпизода и уменьшить риск возникновения рецидивов [42].
Муковисцидоз. Муковисцидоз характеризуется постоянным рецидивирующим течением с развитием воспалительных явлений в легких и присоединением вторичной инфекции. Рекомендуемые схемы терапии легочного муковисцидоза предполагают применение антибиотиков, муколитиков и противовоспалительных препаратов [43,44]. Антибиотики назначают в связи с развитием легочных инфекций, которые являются характерным клиническим признаком муковисцидоза. Однако спектр микроорганизмов, вызывающих данные инфекции, может затруднять адекватный выбор антибактериальных препаратов. Так, синегнойная палочка (Pseudomonas aeruginosa), которая является частым возбудителем инфекций у данной категории пациентов, устойчива к подавляющему большинству антибиотиков, предназначенных для приема внутрь. И хотя макролиды напрямую не обладают активностью против P. aeruginosa, существуют доказательства их непрямого действия в отношении этого микроорганизма, и, как следствие, положительного эффекта в терапии муковисцидоза [45, 46]. Необходимо отметить, что при муковисцидозе происходит колонизация дыхательных путей синегнойной палочкой, продуцирующей альгинат, который способствует образованию биопленок. Предполагается, что макролиды, в том числе азитромицин, с одной стороны, препятствуют адгезии P. aeruginosa к слизистой оболочке, а, с другой стороны, нарушают продукцию альгината, подавляя образование биопленок синегнойной палочкой и облегчая фагоцитирование бактерий нейтрофилами [47,48].
При изучении влияния азитромицина на профиль транскрипции генов и экспрессии белков в культурах PAOl P. aeruginosa в сравнении с контрольными культурами, не подвергавшимися воздействию антибиотика, оказалось, что азитромицин способен подавлять у синегнойной палочки межклеточную сигнальную систему "quorum sensing" (механизм, который следит за плотностью клеток бактериальной популяции и отвечает за контроль продукции многих внеклеточных факторов патогенности, что позволяет бактериям преодолеть защитные сил хозяина), в результате чего снижается продукция факторов вирулентности бактерий и ухудшается ответная реакция микроорганизмов на оксидативный стресс [49].
В настоящее время проведено достаточное количество исследований, посвященных применению макролидов при муковисцидозе. Установлено, что азитромицин значительно уменьшает воспаление и улучшает легочную функцию и качество жизни пациентов с муковисцидозом [43,46,50,51]. Необходимым условием является длительное применение азитромицина [52]. По данным метаанализа, выполненного группой Cochrane Collaboration, азитромицин вызывает статистически значимое улучшение функции внешнего дыхания (объема форсированного выдоха за 1 с [ОФВ1] и форсирований жизненной емкости легких) у больных муковисцидозом [53]. Результаты российских исследований также показали, что длительный прием малых доз макролидов замедляет прогрессирование хронического бронхолегочного процесса у больных муковисцидозом, улучшает ОФВ1 что позволяет рекомендовать применение азитромицина при хронической колонизации синегнойной палочкой [54,55].
У детей используются различные варианты дозировки и длительность лечения. При назначении азитромицина пациентам с муковисцидозом делается акцент на длительную терапию (3-6 месяцев) [46]. В исследованиях азитромицин дозировали по-разному: по 250 мг 2 раза в неделю в течение 12 недель [56], по 250 мг (при массе тела менее 40 кг) или по 500 мг (при массе более 40 кг) 3 раза в неделю в течение 168 дней [48] или 6 месяцев [57], по 250 мг/сут ежедневно в течение 3 месяцев [58]. В российских исследованиях азитромицин применяли в дозе 250 мг через 2 дня в течение 6 месяцев [55] или по 250 мг один раз в 3 дня курсами по 6 месяцев в течение 2 лет [54]. Тем не менее, общепринятых рекомендаций по режиму дозирования и длительности применения азитромицина при лечении муковисцидоза пока не разработано.
Болезнь кошачьей царапины. Болезнь кошачьей царапины впервые была описана в 1931 г., однако ее возбудитель - Bartonella henselae - был идентифицирован только в 1983 г. [59]. Заболевание распространено повсеместно и чаще всего поражает детей и молодых людей. Типичные проявления у лиц без иммунодефицита включают в себя возникновение через 3-10 дней на месте повреждения, нанесенного животным, красно-коричневой безболезненной папулы. Спустя 1-3 недели развивается односторонняя регионарная лимфаденопатия. Заболевание медленно прогрессирует. Состояние пациентов, как правило, удовлетворительное, наблюдаются легкие неспецифические проявления, такие как общее недомогание, потеря аппетита, боли в животе, а также мышечные или суставные боли. В 25% случаев заболевание протекает бессимптомно. Длительность инфекционного процесса обычно не превышает 6 месяцев [59].
Хотя болезнь кошачьей царапины у людей с сохраненным иммунитетом склонна к самоизлечению, и без терапии выздоровление наступает через 2-3 месяца, было показано ускоренное разрешение лимфаденопатии (в течение 1 меса) при лечении коротким курсом азитромицина 61. У детей азитромицин назначают на 5 дней в дозе 10 мг/кг в первый день, а в последующие 4 дня по 5 мг/кг [62,63]. К числу других антибактериальных препаратов, потенциально активных в отношении В. henselae, относятся рифампицин, доксициклин, гентамицин, котримоксазол и ципрофлоксацин (монотерапия или комбинация двух препаратов) [59,64]. Часть из них не разрешена для применения в педиатрии, другие характеризуются неблагоприятным профилем безопасности, поэтому при лечении детей целесообразно отдавать предпочтение азитромицину.
Хламидийная инфекция у новорожденных. С. trachomatis является одним из самых распространенных возбудителей микробных инфекций, передаваемых половым путем. Перинатальная передача С. trachomatis происходит обычно при естественных родах, но инфекция может иметь и вторичный характер, возникая в результате повреждения оболочек плода, прямой контаминации носоглотки и легких новорожденного. Описаны случаи хламидийной инфекции у новорожденных после кесарева сечения. У 35-50% новорожденных, матери которых инфицированы хламидиями, развивается конъюнктивит и у 11-20% - пневмония. Хламидийная инфекция представляет собой наиболее частую причину неонатального конъюнктивита, развивающегося между 5-м и 12-м днями жизни. Поскольку хламидии распространяются по слезному протоку и в носоглотку, по меньшей мере, у 33% новорожденных развивается хламидийная пневмония. В тех случаях, когда признаки конъюнктивита отсутствуют, пневмония развивается у 11-20% новорожденных детей инфицированных и не получавших лечение женщин [65].
Заключение
На основании представленных данных можно сделать вывод о том, что наряду с хорошо известными традиционными показаниями к применению азитромицина, существует еще целый ряд перспективных областей для его клинического использования в педиатрии, включающих в себя достаточно широкий перечень дополнительных клинических состояний, при которых уже получены достоверные данные об его эффективности и безопасности.
Что такое коклюш? Причины возникновения, диагностику и методы лечения разберем в статье доктора Каминской Ольги Николаевны, инфекциониста со стажем в 21 год.
Над статьей доктора Каминской Ольги Николаевны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Коклюш (от франц. coqueluche) — острое инфекционное заболевание, вызываемое бактерией Bordetella pertussis. Клинически характеризуется респираторным синдромом (поражением верхних дыхательных путей) с приступообразным кашлем. Имеет характерное название "стодневный кашель", так как симптомы держатся длительно — 3-4 месяца [1] [2] [3] [4] [5] .

Этиология
Вид — Bordetella pertussis
Бактерия представляет собой мелкую палочку с закруглёнными концами. Она неподвижная, хорошо окрашивается анилиновыми красителями (при микроскопии данные красители окрашивают коклюшный микроб в красный цвет ) [6] [7] .
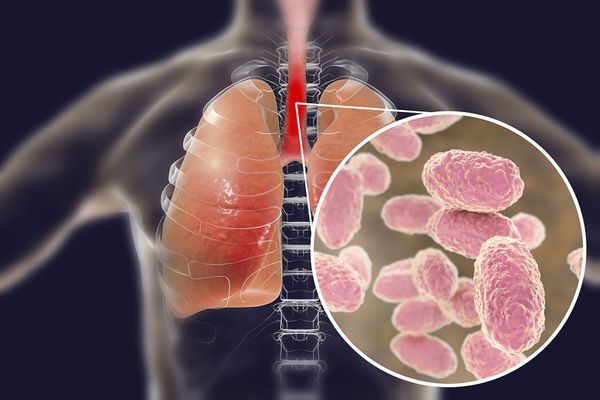
Строение Bordetella pertussis
Возбудитель коклюша (Bordetella pertussis) содержит чужеродные вещества (антигены), которые стимулируют образование в организме антител. Антигены, участвующие в реакции агглютинации (склеивания бактерий антителами) называются агглютиногенами , а антитела вызывающие этот процесс — агглютининами . А гглютиноген иначе называют фактором и обозначают цифрами от 1 до 14. Коклюшная палочка в своём строении имеет несколько таких факторов.
Именно по наличию в организме определённых факторов-агглютиногенов с помощью специальных лабораторных исследований возможно определить принадлежность микроба к данному виду. Схожее строение имеет Bordetella parapertussis, которая вызывает похожее заболевание. Отличие возможно только по лабораторным тестам.
Возбудитель неустойчив во внешней среде, поэтому посев нужно делать сразу после взятия материала. При высушивании, облучении ультрафиолетом, под действием дезинфицирующих веществ бактерия быстро погибает [4] [5] .
Эпидемиология
Заболевание коклюш является антропонозом, т. е. им болеют только люди. Источник инфекции — больные коклюшем, носители. В эпидемиологическом плане наиболее опасны бактериовыделители, которые не имеют жалоб и клинических симптомов, ведут активный образ жизни, но выделяют микроб во внешнюю среду, заражая окружающих.
Для коклюша характерен аэрозольный механизм передачи, т. е. заболевание передается воздушно-капельным путём, особенно часто заражение происходит при близком, семейном контакте. Чаще болеют дети дошкольного возраста.
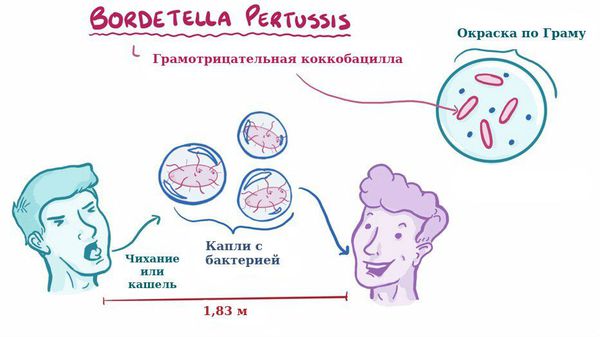
Отмечается высокая восприимчивость к инфекции, индекс контагиозности до 90 %, т. е из 100 человек, которые не болели коклюшем и не прививались, после контакта заболевает до 90 человек. В зимне-весенний период отмечается подъём заболеваемости.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы коклюша
Инкубационный период продолжается до 14 суток. В этот период пациент не предъявляет жалоб, но уже с конца данного периода становится опасен для окружающих, так как начинает выделять коклюшный микроб во внешнюю среду при кашле и чихании. Начало болезни постепенное без лихорадки с умеренно выраженной интоксикацией.
По мере развития заболевания появляются следующие синдромы:
- респираторный (кашель, скудный насморк без гнойного отделяемого);
- интоксикации — выражен умеренно, характеризуется кратковременной невысокой температурой. Высокая температура возможна при развитии осложнений (пневмонии).
Болезнь начинается с появления кашля на фоне слабой интоксикации и насморка. Интенсивность кашля постепенно нарастает, с 10-14 дня кашель становится мучительным, приступообразным с формированием характерных реприз с остановкой дыхания и затруднённым вздохом. Реприза представляет собой кашлевые толчки, сменяющиеся глубоким вдохом по типу "петушиного крика". В приступе кашля у больного синеет лицо, кончик языка при кашле направлен вверх, возможны кровоизлияния в кожу лица и склеры. В одном приступе может быть от 2 до 15 реприз. У детей приступы часто заканчиваются рвотой.
При тяжёлом течении с частотой реприз более 15 в сутки, большой частотой рвоты, связанной с кашлем, отмечается ухудшение физического состояния. Дети до года теряют в весе, начинают отставать в физическом и нервно-психическом развитии, теряют приобретённые навыки: перестают держать головку, переворачиваться, не сидят, хотя до развития заболевания данные навыки присутствовали.

При аускультации (выслушивании дыхания через фонендоскоп) выслушивается жёсткое дыхание, хрипов нет [4] [5] [6] .
Патогенез коклюша
Ворота инфекции — верхние дыхательные пути. Коклюшные палочки прикрепляются к слизистой дыхательных путей, вызывают воспаление без проникновения в кровоток. Коклюшная палочка не имеет факторов агрессии (ферментов), способных растворять клеточные мембраны, сосудистую стенку, поэтому её размножение происходит на поверхности бронха. На месте внедрения увеличивается секреция слизи, реснитчатый эпителий угнетается, формируются очаги некрозов (омертвения). Больше всего процесс затрагивает бронхи и бронхиолы.
В патогенезе судорожных приступов играет роль действие токсина коклюшной палочки. Токсин, попадая в кровоток, вызывает постоянное раздражение рецепторов бронхов, что приводит к перевозбуждению дыхательного центра. Также приступ может быть спровоцирован неинфекционными факторами, например холодным воздухом.
После перенесённого коклюша и вакцинации пожизненного иммунитета не формируется, он сохраняется до 5-6 лет, в дальнейшем возможны повторные заболевания.
Около 5 % случаев коклюша приходится на взрослых. Последние исследования показывают увеличение доли школьников среди заболевших коклюшем, что подтверждается результатами обследования длительно-кашляющих подростков на коклюш [4] [5] [6] [9] .
Классификация и стадии развития коклюша
Критерии тяжести протекания коклюша :
- лёгкая форма (до 15 реприз в сутки);
- средне-тяжёлая (15-25 реприз в сутки);
- тяжёлая (более 25 реприз в сутки) [7] .
По форме:
- Типичная форма коклюша — характерно наличие приступообразного кашля, этапность появления симптомов.
- Атипичная форма коклюша — характеризуется нетипичным покашливанием, отсутствием последовательной смены периодов болезни. Длительность кашля составляет до 50 дней, в среднем около 30 дней. Кашель носит сухой, навязчивый характер, наблюдается напряжение лица, чаще ночью с усилением на второй неделе от начала болезни. Иногда удаётся наблюдать появление единичных типичных приступов кашля при волнении ребёнка, во время еды или в связи с наслоением респираторной вирусной инфекции. Для этой формы характерно редкое повышение температуры и слабая выраженность катарального синдрома (воспаления) слизистых носа и зева [1][2][5][7] .
Клинические периоды (стадии) коклюша:
- Инкубационный период (3-14 дней) — симптомы не проявляются, пациент не предъявляет жалоб .
- Катаральный период (10-13 дней) — наблюдается клиническая картина, характерная для множества простудных заболеваний .
- Пароксизмальный, или спазматический период (1-6 недель) — проявления становятся более выраженными, пациента беспокоит мучительный приступообразный кашель.
- Период обратного развития, или реконвалесценции — приступы кашля становятся редкими , улучшается общее состояние. Этот период, в свою очередь, делят на ранний (развивается через 2-8 недель от начала клинических проявлений) и поздний (спустя 2-6 месяцев) [12] .
Осложнения коклюша
Наиболее частым осложнением является пневмония, которая может быть вызвана самой коклюшной палочкой или быть вторичной из-за активизации микрофлоры бронха.
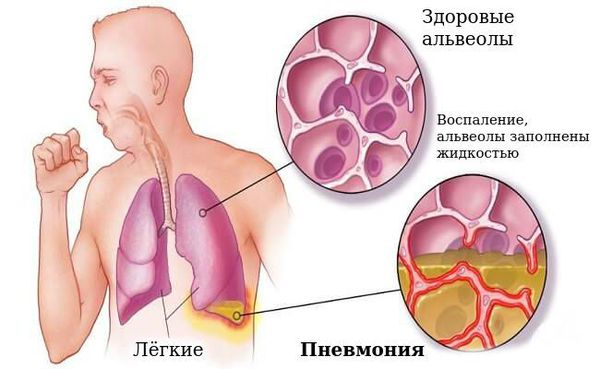
В период спазматического кашля возможны: остановка дыхания, ателектазы (спадение доли лёгкого), пупочная и паховая грыжи, энцефалопатия (нарушение поведения, расстройство внимания, у детей до года отставание в психомоторном развитии, беспокойный сон, раздражительность).
Данные осложнения чаще развиваются у грудных детей. У взрослых осложнения встречаются редко [5] [7] [9] .
Диагностика коклюша
К какому врачу обратиться при коклюше
При подозрении на коклюш следует обратиться к врачу-инфекционисту.
Лабораторная диагностика коклюша
К методам лабораторной диагностики относятся:
- Клинический анализ крови: при коклюше наблюдается лимфоцитарный лейкоцитоз, СОЭ (скорость оседания эритроцитов) повышена или в норме.
- Бактериальный посев с носоглотки (мазок) на коклюш.
- ПЦР диагностика (мазок с носоглотки).
- ИФА (иммуноферментный анализ) крови с определением маркеров проникновения инфекции — антител IgG и IgM, IgА к Bordetella pertussis. Исследование проводится двукратно с интервалом 10-14 дней, оценивается нарастание антител IgG (отвечают за устойчивый иммунитет к инфекции) в четыре раза в динамике. Наличие в крови IgM (первый ответ на инфекцию), IgА (обеспечивают местную защиту на уровне слизистых оболочек) к Bordetella pertussis является подтверждением диагноза [5][7][8][10] .
Дифференциальная диагностика
Длительный кашель может указывать не только на инфекционные заболевания, но и на патологии ЖКТ и других систем.
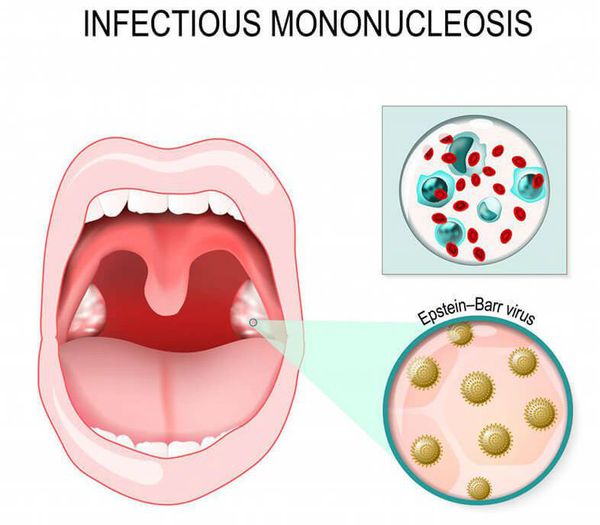
Инфекционный мононуклеоз может характеризоваться длительным кашлем из-за увеличения всех групп лимфоузлов, в том числе расположенных около бронха. Возникает синдром сдавления бронха, что вызывает длительный сухой кашель. Отличительная особенность — высокая и длительная лихорадка, кашель протекает без реприз. Диагноз подтверждается результатами обследования крови: в клиническом анализе крови на фоне повышения общего числа лейкоцитов с преобладанием лимфоцитов определяются специфичные клетки — мононуклеары, при серологическом исследовании крови определяются антитела класса IgM к вирусу Эбштейна — Барр.
Паракоклюш — заболевание, клинически не отличимое от коклюша. Вызывается схожей бактерией Bordetella parapertussis. Диагностика совпадает с таковой при коклюше. Возможно только лабораторное подтверждение: выделение Bordetella parapertussis при бактериологическом посеве со слизистой носоглотки, при ПЦР-исследовании, нарастание титров антител к Bordetella parapertussis при обследовании крови метом ИФА.
Туберкулёз — заражение туберкулёзной палочкой приводит к состоянию, для которого характерно поражение внутригрудных лимфоузлов (чаще у детей), лёгких (чаще у взрослых). В клинике преобладает длительный, навязчивый кашель, интоксикация, снижение массы тела. Репризы не характерны, необходимо дообследование у фтизиатра для исключения туберкулёза. Для уточнения диагноза применяют рентгенологические методы исследования лёгких, мультиспиральную компьютерную томографию (МСКТ) грудной клетки, учёт реакций туберкулиновых проб (реакция Манту, Диаскинтест), бактериологические методы исследования (посев мокроты на туберкулёзную палочку).
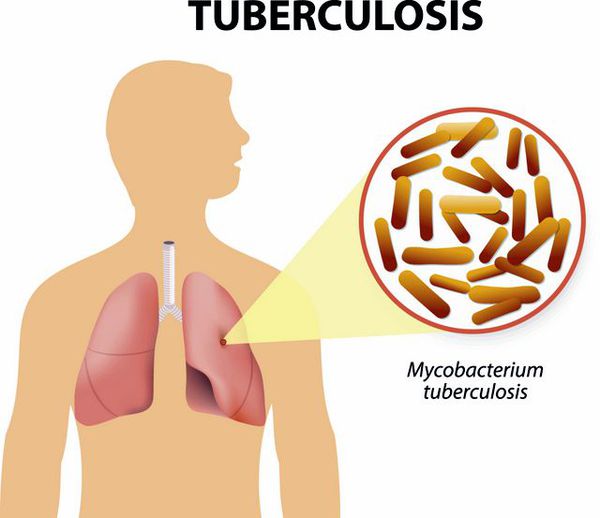
Рефлюкс-эзофагит — при данном состоянии возникает заброс кислого содержимого желудка в пищевод. Из-за близкого расположения пищевода и бронхов происходит раздражение последних и в клинике появляется кашель. Характерно появление кашля в положении лёжа, ночной кашель преобладает над дневным. Диагноз подтверждается проведением ультразвукового исследования желудка. Лечение рефлюкс-эзофагита проводит врач-гастроэнтеролог [5] [7] .
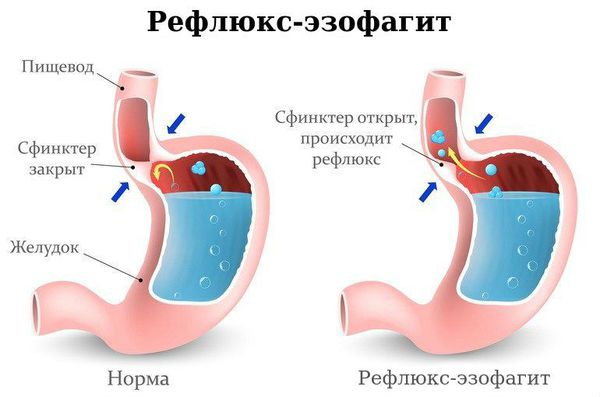
Дополнительные методы обследования: на рентгенограмме органов грудной клетки при неосложнённом коклюше отмечаются признаки усиления лёгочного рисунка: из-за отёка и воспаления на рентгеновском снимке тень лёгкого более выражена.
Лечение коклюша
В домашних условиях осуществляется лечение лёгких форм при условии отсутствия в семье непривитых детей.
Нужен ли постельный режим пациенту с коклюшем
Режим — домашний, постельный режим по самочувствию.
Когда необходимо лечение в стационаре
Тяжёлые формы подлежат госпитализации в инфекционный стационар. Показания для госпитализации: остановка дыхания, более 10 реприз в день, возраст до двух лет.
Диета при коклюше и общие рекомендации
Диета при коклюше — общий стол. Общие рекомендации: увлажнение воздуха (снижает раздражение рецепторов бронхов, уменьшает частоту реприз), витаминотерапия, исключение пассивного курения, проветривание и влажная уборка помещения.
Какие медикаменты и физиотерапевтические процедуры помогут при коклюше
В катаральный период показано применение антибактериальной терапии. Коклюшный микроб чувствителен к макропенам (азитромицин) и защищённым аминопенициллинам (амоксициллина клавуанат). В период спазматического кашля антибиотики малоэффективны, так как в этот период микроба уже нет в организме человека, клиника развивается на основании уже выделенного токсина.
Показаны ингаляции через небулайзер с гормонами (будесонид) [5] [6] [7] .

Как облегчить кашель при коклюше. Симптоматическая терапия
Облегчить кашель помогут препараты на основе кодеина или либексина, насморк — сосудосуживающие препараты в каплях или спрее.
Народные методы лечения коклюша
Народные методы не имеют доказанной эффективности, поэтому применение их может нанести вред здоровью. Отсутствие своевременного адекватного лечения коклюша, особенно у маленьких детей, опасно осложнениями — пневмонией и остановкой дыхания.
Прогноз. Профилактика
Прогноз обычно благоприятный. Симптомы коклюша нарастают в течение месяца, стихают за 2-4 месяца. Рецидивы связаны с наслоением ОРЗ, так как снова возникает раздражение слизистой бронха, усиливается кашель, учащаются репризы. На фоне лечения ОРЗ симптомы коклюша угасают.
Вакцинация против коклюша
Основным профилактическим мероприятием является вакцинация. Вакцинация позволяет сформировать иммунитет к коклюшу после введения в организм специальных иммунобиологических препаратов. Современные вакцины против коклюша входят в состав комплексных вакцин отечественного и зарубежного производства. В состав комплексных вакцин кроме коклюшного компонента может входить дифтерийный и столбнячный анатоксин, вакцина против гепатита В, гемофильной инфекции и полиомиелита (таблица 1).
В соответствии с Национальным календарём профилактических прививок вакцинация показана детям с трёх месяцев жизни. Курс прививок в первый год состоит из трёх вакцинаций с интервалом 45 дней. Дальнейшие прививки проводят на втором году жизни (через год от последней вакцинации). Вакцинацию против коклюша можно сочетать с другими прививками Национального календаря прививок: грипп, пневмококковая инфекция. Все вакцины, содержащие коклюшный компонент, взаимозаменяемы.
Таблица 1. Компоненты комплексных вакцин для профилактики коклюша
Комплексные вакцины имеют ограничение применения по возрасту пациента (таблица 2). У детей вакцинация от коклюша возможна до 4-6 лет. Длительность иммунного ответа после вакцинации составляет до 5-6 лет.
Клиника, диагностика, лечение и профилактика инфекционных заболеваний у детей
Коклюш
Общая информация
Этиология
Возбудителем коклюша является бактерия Haemophilis (Bordetella) pertussis. Коклюшная палочка – обязательный аэроб, имеет вид овоидной палочки длиной
0,5-2 мкм, неподвижная, грамотрицательная, гемоглобинофильная. В широкой практике для выращивания коклюшной палочки чаще используют казеиново-угольный агар.
Резистентность коклюшной палочки в окружающей среде небольшая. Она быстро погибает под воздействием повышенной температуры, прямого солнечного света, высушивания, различных дезинфицирующих средств. Наиболее изученными факторами микробной клетки являются протективные агглютиногены, термолабильный токсин и гемагглютинины. В зависимости от наличия ведущих агглютининов, выделяют 4 серотипа коклюшной палочки (1.2.0; 1.0.3; 1.2.3; 1.0.0). Серотипы 1.2.0 и 1.0.3 чаще вызывают легкие и атипичные формы коклюша, серотип 1.2.3 – среднетяжелые и тяжелые формы заболевания.
Эпидемиология
Коклюш относится к наиболее контагиозным заболеваниям и встречается у 70%-100% восприимчивых к нему лиц. Риск заболевания наиболее высок у детей в возрасте до 5 лет.
Заболеваемость коклюшем характеризуется сезонностью. Увеличение заболеваемости начинается в июле-августе и достигает пика в осенне-зимний период. В последние годы циркуляция возбудителя среди населения не прекращается в течение всего года.
Источником инфекции является больной человек с любой формой инфекционного процесса: тяжелой, средней тяжести, легкой, бессимптомной (бактериовыделение). Инфекция передается воздушно-капельным путем при непосредственном общении с больным, так как возбудитель рассеивается вокруг больного не более чем на 2-2,5 м и малоустойчив во внешней среде. Наибольшую опасность представляют больные в катаральный период заболевания и в первую неделю спазматического кашля – в 90-100% из них выделяется коклюшная палочка. На второй неделе заразность больных снижается, возбудитель можно выделить только у 60-70% больных. Через 4 недели от начала заболевания больные для окружающих не опасны. Восприимчивость людей не зависит от возраста, но зависит от наличия иммунитета. У непривитых людей в обычных условиях восприимчивость высока. Особую группу восприимчивых к коклюшу лиц составляют новорожденные, которые не получают пассивного иммунитета от матери, даже если она имеет антитела к коклюшу. После перенесенного заболевания остается стойкий, практически пожизненный иммунитет.
Воротами проникновения возбудителя коклюша является слизистая оболочка дыхательных путей. Коклюшные палочки фиксируются на клетках мерцательного эпителия, где они локализуются и распространяются на поверхности слизистой оболочки, не попадая в кровоток. На месте попадания инфекции начинается воспаление, блокируется функциональность ресничного аппарата клеток эпителия и повышается количество вырабатываемой слизи. Затем происходит изъязвление эпителия респираторного тракта и очаговый некроз. Патологические изменения максимально выражены в бронхах и бронхиолах, менее выраженные патологические процессы возникают в трахее, гортани и носоглотке. Пробочки слизисто-гнойного характера заслоняют просвет мелких бронхов, образуя очаговый ателектаз, эмфизему, отмечается перибронхиальная инфильтрация. Постоянное раздражение рецепторов респираторного тракта вызывает кашель и формирует в дыхательном центре очаг возбуждения. По этой причине характерные приступы спазматического кашля могут вызываться и неспецифическим раздражителем. Из доминантного очага возбуждение может распространиться и на другие части нервной системы, к примеру, на сосудодвигательный отдел (увеличение артериального давления, спазм сосудов). Распространением процесса возбуждения объясняется также возникновение судорожных мышечных сокращений на лице и теле, рвоты и других проявлений заболевания.
Механизм одного из ведущих симптомов коклюша – спазматического кашля – состоит в следующем: непрерывный поток импульсов, поступающий со стороны рецепторов слизистой оболочки дыхательных путей, ведет к возникновению в центральной нервной системе стойкого очага возбуждения, характеризующегося признаками доминанты. Образованию очага возбуждения в центральной нервной системе, очевидно, способствует описанное выше действие на нее коклюшного токсина. Приступы коклюшного кашля развиваются не только в результате импульсов, идущих со стороны дыхательных путей, но и в ответ на раздражение рецептивных полей, не имеющих никакого отношения к кашлевому рефлексу (например, при осмотре зева, инъекциях, сильных звуковых раздражения и др.). Вследствие инертности, свойственной доминантному очагу, приступы судорожного коклюшного кашля могут наблюдаться длительное время после ликвидации коклюшной инфекции. При возникновении других более сильных центров возбуждения доминантный очаг подвергается торможению. Этим механизмом, по-видимому, следует объяснить прекращение приступов коклюшного кашля во время увлекательной игры.
Клиническая картина
Особенности коклюша у детей первого года жизни
У детей грудного возраста коклюш имеет ряд особенностей. Отмечается укорочение инкубационного (до 3-5 дней) и катарального (до 2-6 дней) периодов. Иногда катаральный период отсутствует и судорожный кашель появляется уже в первый день болезни. Приступы кашля у большинства грудных детей не сопровождаются репризами. Реже, чем у детей старшего возраста, наблюдается рвота, геморрагические симптомы и отеки. Приступы кашля нередко ведут к появлению апноэ. Расстройства газообмена выражены сильнее, чем у детей старшего возраста, чаще наблюдается выраженный цианоз. Маленькие дети особенно чувствительны к кислородной недостаточности: гипоксия отягощает течение процесса, вызывает развитие осложнений. У грудных детей чаще, чем у детей старшего возраста, нарушается сознание, эпилептиформные судороги, судорожные подёргивания мимической мускулатуры. Особенно тяжело протекает коклюш у детей в возрасте до 6 месяцев. Поскольку отсутствуют зубы, образование ранки на уздечке языка у детей в возрасте 6-8 мес. наблюдается очень редко. Спазматический период может увеличиваться до 2-3 мес. Чаще, чем у детей старшего возраста, развиваются осложнения со стороны органов дыхания: бронхиты, бронхопневмонии. Пневмонии у детей грудного возраста характеризируются ранним развитием, чаще имеют сливной характер, склонны к длительному течению и отличаются высокой летальностью; они являются основной причиной смерти от коклюша.
Осложнения
- Затруднённое дыхание.
- Гипоксия мозга.
- Пневмония.
- Отит.
- Расширение бронхов.
- Обезвоживание.
- Грыжи.
- Энцефалопатия.
- Энцефалит.
- Кровоизлияние в мозг.
- Кровоизлияние в сетчатку глаза.
- Гипоксическое повреждение головного мозга.
- Апноэ.
Отдаленные осложнения коклюша
- Эмфизема легких.
- Бронхоэктатическая болезнь.
- Ателектазы легких.
- Астма.
- Задержка умственного развития.
- Эпистатус.
При коклюше, особенно у детей первого года жизни, снижается неспецифическая резистентность организма, развиваются расстройства пищеварения и гиповитаминоз. В результате этого, коклюш может провоцировать обострение и генерализацию многих инфекций, в том числе и туберкулеза.
Диагностика
Лечение
Успех лечения коклюша, в значительной мере, зависит от создания для больных надлежащего режима и условий внешней среды. Постельный режим назначают только при наличии лихорадки и тяжелых осложнений. Всех детей в возрасте до одного года, заболевших коклюшем, желательно госпитализировать ввиду опасности развития апноэ и других серьезных осложнений. Детей первого года жизни с тяжелыми формами коклюша рекомендуется помещать в затемненных тихих комнатах, как можно реже их беспокоить, поскольку воздействие внешних раздражителей может вызвать тяжелый пароксизм кашля с развитием апноэ.
Рациональная организация внешней среды при коклюше должна предусматривать правильный режим для больного. Почти половина приступов кашля за сутки возникает в непосредственной связи с различными манипуляциями, введением лекарств, врачебным осмотром и другими внешними раздражителями. Отмечено также, что у больных коклюшем детей имеют место выраженные нарушения сна, при которых приступы кашля возникают значительно чаще, чем во время глубокого и спокойного сна.
Большое внимание необходимо уделять воспитательной работе с детьми старшего возраста: организации их досуга, различным отвлекающим занятиям, играм. Дети, увлеченные игрой, реже кашляют. Необходимо исключить различные раздражители – эмоциональные, физические, которые могут спровоцировать приступы кашля.
Большое значение в терапии коклюша имеет рациональное питание. У больных коклюшем детей, особенно раннего возраста, нередко наблюдается рвота, возникающая в связи с приступами спазматического кашля. Кроме того, у этих больных обычно отмечается снижение аппетита. Поэтому пища больного коклюшем ребенка должна быть полноценной и калорийной, полужидкой, богатой витаминами; ее следует вводить в небольших количествах и с меньшими интервалами, чем здоровым детям соответствующего возраста. При частой рвоте следует докармливать ребенка небольшими порциями, спустя 20-30 минут после рвоты.
Многолетними исследованиями установлено, что длительное пребывание на свежем воздухе оказывает благоприятное влияние на самочувствие больного коклюшем и на течение болезни (улучшается вентиляция легких, кислородный обмен, и возможно, рефлекторно влияет на центральную нервную систему).
B летнее время желательно пребывание больных на свежем воздухе, по возможности, в течение всего дня. B холодное время года прогулки более ограничены: учитывается температура воздуха (они не показаны при морозе ниже -10 °С и сильном ветре) и состояние больного (необходима осторожность при поражении носоглотки, при пневмонии с выраженными нарушениями сердечно-сосудистой системы). Температура воздуха в комнате, в которой находится ребенок, не должна превышать 21-23 °С. Необходимо также обеспечить тщательное постоянное проветривание помещения, в котором находится больной.
В терапии больных коклюшем используют антибиотики в качестве специфического (этиотропного) лечения. Наиболее эффективна антибиотикотерапия при коклюше в первые 2 недели от начала заболевания. После 4 недель заболевания назначение антибиотиков при неосложненных формах коклюша нецелесообразно.
Антибиотиками первого ряда у больных коклюшем является эритромицин в дозе 40-50 мг/кг массы тела (не более 2 г в сутки), другие макролидные антибиотики (азитромицин, кларитромицин) или ампициллин в дозе 100 мг/кг массы тела в сутки. Препаратом второго ряда при коклюше у детей рекомендован котримоксазол, который назначают в дозе 8 мг/кг массы тела по триметоприму или 40 мг/кг массы тела в сутки по сульфаметоксазолу.
Использование коротких курсов антибактериальной терапии (азитромицин в течении 3 дней, кларитромицин в течении 7 дней или эритромицин 7 дней) являются столь же эффективными, как и рекомендуемая в некоторых руководствах более длительная антибактериальная терапия (эритромицин в течение 14 дней). У детей до 1 года азитромицин предпочтительнее эритромицина. Как показали некоторые исследователи, имеется связь между использованием эритромицина и возникновением у детей пилоростеноза.
Рекомендуемые дозы и схемы антибиотиков при коклюше:
Азитромицин: у детей до 6 мес. – 10 мг/кг орально (5 дней),
старше 6 мес. – 10 мг/кг (max 500 мг) орально 1 день, затем 5 мг/кг (max 250 мг) последующие 4 дня.
Кларитромицин: дети старше 1 мес. – 7,5 мг/кг (max 500 мг) орально каждые 12 часов в течение 7 дней.
Эритромицин: дети старше 1 мес. – 10 мг/кг (max 250 мг) орально каждые 6 часов в течение 7 дней.
Принимая во внимание увеличение в последние годы частоты легкого и стертого течения коклюша, не следует считать обязательным назначение антибиотиков всем больным коклюшем детям. Оно может быть ограничено следующими показаниями:
1) ранний возраст больного;
2) тяжелые и осложненные формы коклюша;
3) наличие сопутствующих заболеваний, требующих назначения антибиотиков.
Важным заданием в лечении тяжелых форм коклюша является борьба с гипоксией, которая развивается в результате снижения поступления кислорода через дыхательные пути во время приступа кашля. Первым шагом к решению этого вопроса должно быть предотвращение новых приступов кашля. Для профилактики и уменьшения приступов кашля применяется введение внутримышечно 2,5% раствор аминазина в дозе 1-2,5 мг/кг массы тела 2 раза в день перед дневным и ночным сном. У детей первого года жизни предпочтение отдают титрованному раствору аминазина, который готовится с расчета 1 мл 2,5% аминазина на 3 мл 0,25% раствора новокаина. Расчет дозы производится по аминазину.
Кроме аминазина, для уменьшения приступов кашля используют диазепам в дозе 0,3 мг/кг массы тела в один прием в день. Детям старшего возраста диазепам можно давать орально.
У детей с тяжелыми формами коклюша обязательной является кислородотерапия.
Профилактика
Изоляция больного должна осуществляться как можно в более ранние сроки. На практике диагноз коклюша часто устанавливают лишь в стадии конвульсивного кашля. Соответственно опаздывает изоляция больного, что, конечно, очень снижает ее эпидемиологическую эффективность. Таким образом, важнейшим условием успешного проведения противоэпидемических мероприятий при коклюше является ранняя диагностика. Изоляцию больного в домашних условиях проводят в отдельной комнате или за ширмой.
Госпитализации подлежат больные с тяжелой и осложненной формами коклюша, особенно дети в возрасте до 2 лет, больные дети из семей, проживающих в неблагоприятных бытовых условиях, а также из семей, в которых есть дети в возрасте до 6 месяцев, которые не болели коклюшем. Изоляция больного продолжается до 25-го дня от начала болезни. Организация режима в стационаре требует особого внимания. Необходимо проветривать помещения и проводить обеззараживание носовых платков, полотенец, посуды больного. Требуется тщательная защита больных от присоединения сопутствующей инфекции, что является причиной обострений и осложнений.
На детей до 7 лет, которые были в контакте с больными, которые ранее не болели коклюшем и не привитые против него, накладывают карантин сроком до 14 дней с момента изоляции больного. Если больной не был изолирован и общение с ним продолжалось в течение всего периода болезни, карантин накладывают до окончания периода заразности у больного. Возбудитель, вследствие малой устойчивости, быстро погибает, поэтому потребности в полной заключительной дезинфекции после изоляции больного нет. За очагом устанавливают медицинское наблюдение. При подозрении на коклюш проводят бактериологическое обследование.
С целью активной иммунизации, используют коклюшную вакцину, которая представляет собой суспензию первой фазы коклюшных микробов, обезвреженных формалином или мертиолятом. Этот препарат применяется в ассоциации с дифтерийным и столбнячным анатоксинами (коклюшная-дифтерийно-столбнячная или АКДС-вакцина).
С целью предупреждения осложнений со стороны нервной системы, разработана ацеллюлярная вакцина, которая в своем составе не содержит остатки оболочек коклюшной палочки. Из-за высокого риска поствакцинальных осложнений, встречающихся при введении цельноклеточной АКДС-вакцины, в настоящее время для иммунопрофилактики коклюша рекомендуется использовать АаКДС-вакцину – вакцину с ацеллюлярным коклюшным компонентом.
В Украине вакцинацию против коклюша начинают у детей в возрасте 3 месяца трехкратно, с интервалом 1 месяц; ревакцинацию проводят однократно, в возрасте 18 месяцев.
Исследования показали, что использование с целью химиопрофилактики коклюша эритромицина не предотвращает развития заболевания, но уменьшает процент выделения возбудителя при бактериологическом исследовании. Однако, несмотря на недостаточную доказательную базу, химиопрофилактику коклюша рекомендуют проводить макролидными антибиотиками у непривитых детей в возрасте до 6 мес., в связи с тем, что в этой возрастной группе имеет место высокий процент развития тяжелых форм заболевания и развития осложнений.
Читайте также:

