Можно ли занести инфекцию катетером
Обновлено: 19.04.2024
Инфекция мочевыводящих путей является одной из самых распространенных внутрибольничных инфекций и в большинстве случаев наблюдается на фоне катетеризации мо¬чевого пузыря. Основной причиной развития инфекций мочевых путей считаю патогенную и условно-патогенную микрофлору толстого кишечника пациента. Возбудителями катетер-ассоциированной инфекции в более, чем 40% случаев являются грамотрицательные микроорганизмы, реже — энтерококки, стафилококки и грибы. Из госпитальных штаммов микроорганизмов следует выделить Pseudomonas aeruginosa, Enterobacter agglomerans, Klebsiella spp., E. coli, Staphylococcus spp., Enterococcus faecalis, Proteus mirabilis, Candida albicans и др. Важным фактором риска развития бактериурии при катетеризации являет¬ся продолжительность нахождения катетера в мочевом пузыре. Если катетер находится там незначительное время, то большинство периодов бактериурии про¬текают бессимптомно или же краткосрочно. В большинстве случаев, они вызваны моно¬инфекцией. Другие патогенные и условно-патогенные микроорганизмы чаще всего проникают в организм человека при нахождении катетера в мочевом пузыре более 30 дней или же при нарушении правил катетеризации пациентов в случае однократной установки катетера. Аннотация: в данной статье рассматриваются основные факторы и причины развития катетер-ассоциированной инфекции мочеполовых путей. На основе современных статистических данных выявлена взаимосвязь между длительностью катетеризации и течением бактериемии, между нарушениями в процессе постановки мочевого катетера и вероятностью развития КАИМП.

2.Шуб Г.М., Швиденко И.Г., Корженевич В.И., Лунева И.О., Турковская О.В. Основы медицинской бактериологии, вирусологии и иммунологии/Под ред. Шуба Г.М.: Учебное пособие. – М.: Логос, 2001. – 264 с.
3. Коза, Н. М. Факторы риска и профилактика внутрибольничных инфекций мочевыводящих путей / Н. М. Коза // Пермский медицинский журнал. — 2015. — Т.32, № 1. — С. 135–140.
4. Эпидемиологическая безопасность — важнейшая составляющая обеспечения качества и безопасности медицинской помощи / Н. И. Брико, Е. Б. Брусина, Л. П. Зуева, Г. Е. Ефимов, О. В. Ковалишена, В. Л. Стасенко, И. В. Фельдблюм, В. В. Шкарин // Вестник РОСЗДРАВНАДЗОРА. — 2014. — № 4 — С. 8–13.
5. Васильев А.О., Говоров А.В., Пушкарь Д.Ю. Роль уретрального катетера в развитии катетер-ассоциированной инфекции. Урологические ведомости. 2017;7:19–20.
Европейско-Азиатские рекомендации по ведению пациентов с инфекциями, связанными с уретральным катетером, и по профилактике катетер-ассоциированных инфекций / П.Тенке, Б.Ковач, T. E. Бьерклунд Йохансен, T. Мацумото, П. А. Тамбья, К. Г. Набер // Клиническая микробиология и антимикробная химиотерапия. — 2008. — Т.10, № 3. — С.201–216.
Инфекции мочевыводящих путей это одна из наиболее актуальных проблем современной урологии. Эти инфекции зачастую приводят к развитию тяжелых гнойно-септических осложнений, бактериемии, сепсиса. Существует множество факторов, осложняющих течение инфекций мочевыводящих путей, такие как: нарушение уродинамики по обструктивному типу, наличие инородных тел в мочевыводящих путях.
Основной источник распространения патогенных микроорганизмов — катетеризация мочевого пузыря. В ходе оценки лечебно-диагностического процесса установлено, что доля катетеризаций мочевого пузыря среди всех госпитализированных пациентов составила 49,6 %, причем большая часть, примерно 69%, из них представлена мужчинами. [1, стр. 51]
Отдельной группой выделяют катетер-ассоциированные инфекции, при которых происходит инфицирование антибиотикорезистентными госпитальными штаммами или же представителями собственной кишечной микрофлоры пациента. По данным Клинических рекомендаций Европейской ассоциации урологов, опубликованных в 2007 г., более 5% пациентов ежегодно колонизируются патогенными микроорганизмами [6, стр. 202].
Мочевыводящие пути представляют собой один из главных источников нозокомиальных инфекций, в частности при наличии катетера в мочевом пузыре.. По данным ВОЗ, среди взрослых пациентов отделений реанимации и интенсивной терапии (ОРИТ) в странах с высоким уровнем дохода плотность инцидентности ИМП составляет 4,1 на 1000 катетеро-дней (95 % ДИ 3,7–4,6), в странах со средним и низким уровнем доходов (в том числе и в Российской Федерации) данный показатель выше — 8,8 на 1000 катетеро-дней (95 % ДИ 7,4–10,3) [1, стр. 52].
Ведущим фактором риска развития катетер-ассоциированной бактериурии является длительность катетеризации. Именно поэтому целью моей работы является на основе современных статистических данных проследить зависимость между вероятностью развития КАИМП и длительностью катетеризации.
Материал исследования: современные литературные исследования, статьи и публикации, касающиеся данной темы, и статистика заболеваемости КАИМП за последние 10 лет.
Методы исследования: статистический анализ данных.
Нормальная микрофлора человека как совокупность множества микробиоценозов, характеризующихся определенным составом, представлена в виде биопленки. Биопленка это скопление микроколоний микроорганизмов на полисахаридном каркасе, построенном из микробных полисахаридов и муцина, которые вместе образуют структурную популяцию на какой-либо твердой поверхности. Биопленки распространенны повсеместно, исключая отдельные стерильные органы человека. Так, нормальная микрофлора наружной части уретры и у мужчин, и у женщин представлена коринебактериями, микобактериями, грамотрицательными бактериями фекального происхождения и неспорообразующими анаэробами: пептококки, пептосптрептококки, бактероиды. Эти микроорганизмы обычно определяются в количестве 10 2 -10 4 в 1 мл мочи. [2, стр. 36]
Однако биопленка можно образовываться и на катетерах, мочеприемниках и других инородных телах. Такая биопленка состоит из 3х слоев: связующей, базальной прослойки, непосредственно прикрепляющейся к ткани; основного слоя и поверхностного, от которого отщепляются свободно плавающие микроорганизмы. Микроорганизмы, оказавшиеся внутри биопленки, защищены от агрессивных факторов окружающей среды и организма человека, свободно размножаются и заполняют весь основной слой биопленки. [3, стр. 137]
Уретральные катетеры могут принимать участие в подавлении некоторых защитных механизмов микроорганизмов (например, гликозаминогликановый слой на поверхности эпителия уретры), которые в норме сводят к минимуму контакт бактерий с эпителием и препятствуют образованию биопленок. [4, стр. 11]
Помимо этого, следует обратить внимание на характер поверхности катетера, от этого зависят скорость и характер роста микробной пленки. По данным последних исследований, риск возникновения ИМП на фоне уретрального катетера возрастает на 4-7,5% в зависимости от материала, из которого изготовлен катетер и особенности его поверхности.[5, стр.19]
Однако, патогенные и условно-патогенные штаммы микроогранизмов, несмотря на защитную роль катетеров, способны проникать в мочевыводящие пути человека. Например, во время постановки катетера вследствие недостаточной обработки места введения катетера может развиться бактериурия даже при интермитирующей катетеризации. Вопрос преимущественной обработки непосредственного места постановки катетера остается открытым, однако у госпитализированных пациентов попадание бактерий именно во время катетеризации остается ведущим.
Что же касается длительной катетеризации, она способствует образованию слизистой муфты, свободно располагающейся между стенкой катетера и слизистой оболочкой уретры, создавая благоприятную среду для инвазии и проникновения бактерий. В связи с этим ведущим фактором развития катетер-ассоциированной инфекции является длительность катетеризации.
Способы катетеризации и риски КАИМП
В зависимости от способа катетеризации выделяют однократную, кратковременную и длительную катетеризацию.
Так, при однократной катетеризации риск развития КАИМП повышен у женщин (вследствие высокой вероятности ретроградного направления развития инфекции), пациентов с задержкой мочи, при катетеризации в родах и послеродовом периоде (70-80%), при обструкции мочевыводящих путей увеличенной предстательной железой, при сахарном диабете, у ослабленных лежачих больных и пожилых людей (20-30%). [1, стр. 49]
Кратковременная катетеризация, проводимая у пациентов с нарушением произвольного мочеиспускания и недержанием мочи, может являться следствием развития бактериемий. Большинство эпизодов не сопровождается клиническими симптомами и вызывается, как правило, одним возбудителем. Согласно данным Азиатской ассоциации урологов, более 25% пациентов катетеризированы на 2-4 сутки госпитализации; у 10-30% из них развивается бактериурия. [4, стр.9] По современным данным, наиболее часто выделяют E. coli, P. aeruginosa, Klebsiella pneumoniae, Proteus mirabilis, Staphylococcus epidermidis, Enterococcus spp. и Candida spp.
Однако, многие современные исследования подтверждают корреляцию между полом пациента и преобладающим возбудителем ИМП [5стр.19]. При проведении бактериологических исследований посевов мочи от катетеризированных пациентов были сделаны выводы о том, что на посевах мочи мужчин и женщин были выявлены разные спектры возбудителей. Так, у пациентов урологического отделения мужского пола с КАИМП можно обнаружить грамположительные микроорганизмы S.epidermidis (50,0 %), у женщин чаще инфекцию вызывали грамотрицательные — E.coli (33,2 %), A. calcoaceticus (16,7 %).[3, стр.8]
Частота развития бактериемии значительно у пациентов с длительно установленными катетерами, подвергающихся эндоскопическим вмешательствам.
Несмотря на то, что вероятность развития КАИМП выше у пациентов с длительно установленным катетером, клинические проявления как следствие восходящей инфекции или бактериемии, наблюдаются редко. В длительных исследованиях показано, что ИМП являются причиной лихорадки менее чем в 10% случаев.[6, стр. 203] Именно поэтому, у катетеризированного пациента крайне важно исключить другие возможные причины развития бактериурии.
Важно отметить, что риск развития бактериемии при первичной установке катетера соответствует риску развития бактериемии при замене катетера у длительно катетеризированных пациентов. Относительно низкая частота развития ИМП с лихорадкой и бактериемии может быть обусловлена колонизацией менее вирулентными микроорганизмами. Например, при катетер-ассоциированных инфекциях, вызванных E. coli, у штаммов E. coli могут отсутствовать Р-фимбрии. По данным ВОЗ, до 20% пациентов колонизируются сразу после катетеризации.[1, стр. 51]
Доказательства того, что наличие постоянного катетера является фактором риска выраженной заболеваемости являются спорными.
Однако очевиден факт, что длительное персистирование патогенных возбудителей в организме человека значительно повышает вероятность развития КАИМП. При длительно катетеризировании нередко выделяются Pseudomonas, Proteus, Morganella и Acinetobacter spp. Приблизительно в 95% случаев бактериурия имеет полимикробный характер.[1, стр. 51]
Важно отметить, что в большинстве случаев микроорганизмы при длительной катетеризации населяют только катетер, что подтверждают результаты мочи, взятые путем надлобковой пункции.
Очевидно, что длительная катетеризация приводит к развитию различных осложнений: образованию мочевых камней, развитию простатита и абсцессу мошонки. Ряд данных подтверждает прямую зависимость риска развития данных заболеваний и длительностью катетеризации. Но, данные, касающиеся вероятности развития КАИМП остаются неоднозначными.
Таким образом, однозначное утверждение о том, что ведущим фактором развития КАБ является длительность катетеризации нельзя считать достоверным. Современные исследования не выявляют зависимости между длительностью катетеризации и вероятностью развития бактериурии, результаты их исследования считаются спорными.
Однако подтверждены данные о том, что бактериурии, связанные с кратковременной катетеризацией, в большинстве случаев протекают бессимптомно и вызываются, как правило, одним возбудителем. При увеличении времени катетеризации бактериурии становятся полимикробными. По региональным данным показатель заболеваемости ИМП в общей структуре ИСМП колеблется в пределах 0,004–0,02 на 1000 пролеченных пациентов.[1, стр. 50]
Следует сделать вывод о том, что для снижения риска развития КАИМП врачу прежде всего важно следить за тем, чтобы дренажная система оставалась закрытой, снизить риск перекрестной передачи инфекции между катетеризированными пациентами, рассматривать альтернативы постоянным уретральным катетерам и стремиться к снижению длительности катетеризации, в том числе и для снижения риска развития других сопутствующих заболеваний. [4, стр.12]
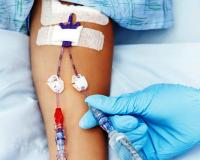
Катетер-ассоциированные инфекции кровотока (КАИК) – это нозокомиальные инфекционные осложнения, связанные с использованием внутрисосудистых катетеров. Клинически проявляются местными воспалительными изменениями (отек, болезненность, гиперемия в области катетера) или генерализованной инфекцией (фебрильная лихорадка, озноб, бактериемия). Для лабораторного подтверждения КАИК осуществляется посев крови на гемокультуру и микробиологическое исследование сосудистого катетера. При первых признаках КАИК производится удаление катетера, назначается антибактериальная, инфузионная терапия.
МКБ-10
Общие сведения

Причины
Установка внутрисосудистого устройства (ВСУ) – инвазивная манипуляция, сопряженная с нарушением целостности кожных покровов и сосудистой стенки, внедрением и оставлением в просвете сосуда инородного предмета. Катетерные инфекции кровотока в большинстве случаев ассоциированы с установкой центрального венозного катетера (ЦВК), инфузионной порт-системы, периферической венозной канюли. Чаще КАИК развиваются при катетеризации бедренной вены, реже – подключичной и внутренней яремной.
Развитию ангиогенных инфекций предшествует контаминация сосудистого устройства патогенными или условно-патогенными микроорганизмами. Источниками и причинами обсеменения могут стать:
- инфекции кожи в области сосудистого протеза (пиодермии);
- несоблюдение требований асептики при манипуляциях с ЦВК (ненадлежащая обработка операционного поля, рук врача);
- неадекватный выбор доступа, размера, типа и материала катетера;
- частые пункции сосудистого русла;
- плохой уход за сосудистым протезом.
Среди этиологических агентов, вызывающих КАИК, преобладают возбудители, которые являются самой частой причиной ВБИ: стафилококки (47%, из них золотистый стафилококк ‒ 25%), энтеробактерии (27%), ацинетобактеры (13%), синегнойная палочка (9%), кандиды (5%), энтерококки (3%) и др. Большую роль в возникновении внутрисосудистых инфекций, играет срок катетеризации: по опубликованным данным, через 7 дней нахождения катетера в вене КАИК развивается у 5%пациентов, через 1 месяц и более – у 36%.
Факторы риска
Инфицированию внутривенных катетеров способствуют сопутствующие состояния: сахарный диабет, иммунодефициты и иммуносупрессия, гипоальбуминемия. В группу повышенного риска по развитию катетер-ассоциированных инфекций кровотока входят пациенты, имеющие значительную катетеризационную нагрузку (длительную и неоднократную пункцию центральных вен):
- находящиеся на гемодиализе;
- получающие массивную инфузионно-трансфузионную терапию;
- проходящие химиотерапию;
- требующие проведения эфферентных методов детоксикации;
- нуждающиеся в парентеральном питании.
Патогенез
Механизм развития КАИК реализуется тремя основными путями. Чаще всего инфекция проникает в кровоток с обсемененных кожных покровов по наружной поверхности катетера (экстралюминально). Такой путь наиболее актуален в ранние сроки после постановки катетера (первые 10-15 суток). В последующем увеличивается доля интралюминального инфицирования, когда инфекция распространяется по внутренней стороне протеза через контаминированные инфузионные среды, канюли шприцев и систем для переливания. Также возможно гематогенное инфицирование, при котором возбудители оседают на катетере, разносясь с током крови из других источников (при пневмонии, панкреатите и пр.).
Внутрисосудистое устройство является инородным телом, поэтому в ответ на его введение организм вырабатывает различные белковые вещества, отграничивающие его от собственных тканей. В их числе ‒ фибрин и фибронектин, к которым легко прикрепляется коагулаза – фермент, продуцируемый многими патогенами, в частности, золотистым стафилококком и кандидой.
В результате такой адгезии внутри сосудистого протеза образуется биопленка, защищающая микробные колонии от воздействия антибиотиков и клеток иммунной системы. Это способствует переходу инфекции в персистирующую хроническую форму. Микробные биопленки образуются на внутренней поверхности имплантируемых устройств в 40% случаев.
Наличие биопленки снижает чувствительность патогенов к антибиотикам в сотни раз, способствует увеличению в структуре ВБИ доли антибиотикорезистентных штаммов, устойчивых практически ко всем известным противомикробным препаратам. Рост колоний микроорганизмов сопровождается фрагментацией биопленки и попаданием патогенов в кровоток, что приводит развитию бактериемии и сепсиса.
Классификация
В настоящее время в медицинских кругах используется классификация катетер-ассоциированных инфекций кровотока, рекомендованная Комитетом по контролю за госпитальными инфекциями (США). Согласно ей, различают следующие формы КАИК:
- Колонизация катетера, подтвержденная микробиологическим исследованием, при отсутствии любых клинических проявлений.
- Флебит: эритема, уплотнение, болезненность катетеризированной вены при пальпации.
- Ограниченная инфекция в месте установки катетера: инфильтрат, болезненность тканей, гиперемия, наличие гнойного отделяемого, очаг не более 2 см.
- Инфекция подкожного кармана, содержащего установленную порт-систему: гиперемия и некроз кожи над имплантируемым устройством, гнойное отделяемое в подкожном кармане.
- Туннельная инфекция: признаки воспаления, распространяющегося по ходу катетера более 2-х см от места его установки.
- Инфекции кровотока: бактериемия, фунгемия, сепсис, при которых один и тот же возбудитель высевается из кровотока и из удаленного ВСУ.
- КАИК, ассоциированные с инфузионной средой: контаминированными растворами, гемокомпонентами.
Симптомы КАИК
Катетер-асоциированные инфекции кровотока могут быть локальными (37%) и генерализованными (63%). Первые из них ограничены местом установки сосудистого протеза, вторые характеризуются бактериемией и системным поражением. Местные инфекции представлены инфильтратами, абсцессами, флебитами, непосредственно связанными с установленным внутрисосудистым устройством. Генерализованные КАИК проявляются сепсисом.
На высокую вероятность КАИК указывает появление признаков воспаления вокруг сосудистого катетера: уплотнение и покраснение кожи, боли, отделение гнойного экссудата, нарушение проходимости протеза. Общие симптомы инфекционного процесса ‒ лихорадка с ознобом ‒ обычно возникают через 20 минут–1,5 часа после использования катера (забора крови, вливания растворов). В тяжелых случаях лихорадка становится фебрильной и практически постоянной, снижается АД, нарастают признаки интоксикации. Развивается катетер-ассоциированный ангиогенный сепсис.
Осложнения
Длительное нахождение катетера в сосудистом просвете повышает риск развития тромбофлебита, тромбоза глубоких вен. КАИК могут осложниться септикопиемией ‒ формированием метастатических гнойных отсевов различной локализации. Среди них – бактериальный эндокардит, абсцедирующая пневмония, септический артрит, гематогенный остеомиелит и др. Причиной гибели пациентов становится септический шок, полиорганные нарушения, фатальные тромбоэмболии.
Диагностика
Клиническим критерием КАИК считается появление у пациента симптомов инфекции кровотока спустя 48 часов и более после установки ЦВК при отсутствии других источников инфекции. Однако из-за низкой специфичности клинических данных диагноз катетер-ассоциированной инфекции требует обязательного лабораторного подтверждения. Для этого производится парный посев:
- крови из периферической вены и дистального конца внутрисосудистого катетера (либо смыва из него). КАИК считается достоверной при одновременном выделении одной и той же гемокультуры из периферической крови и сосудистого зонда (>15 КОЕ полуколичественно и >102 КОЕ количественно);
- крови из сосудистого протеза и вены. На КАИК указывает более чем 3-кратное превышение количества колоний в образце крови из катетера по сравнению с венозным образцом.
Забор крови необходимо производить двукратно, до начала антибиотикотерапии, на высоте лихорадки. Для уточнения осложнений осуществляются инструментальные исследования. При подозрении на гнойный тромбофлебит выполняется УЗДС сосудов, флебография. Исключить или подтвердить септический эндокардит помогает трансторакальная ЭхоКС. Методами диагностики гнойных процессов костно-суставной системы является рентген, УЗИ суставов.
Ангиогенные инфекции дифференцируют с бактериемией, ассоциированной с другими первичными источниками: пневмонией, гнойными ранами, интраабдоминальными абсцессами и др.
Лечение катетер-ассоциированных инфекций кровотока
Системную антибиотикотерапию начинают, не дожидаясь результатов бакпосева, при необходимости в дальнейшем ее корректируют с учетом выделенной флоры и чувствительности. Обычно используются пенициллины, цефалоспорины, гликопептиды, аминогликозиды длительностью не менее 14 дней. Для терапии грибковой инфекции назначают амфотерицин В, флуконазол. При явлениях тромбофлебита показано введение антикоагулянтов, фибринолитиков. В отношении флегмон, гнойного артрита, остеомиелита, абсцессов различной локализации применяется соответствующая хирургическая тактика.
Прогноз
Катетер-ассоциированные инфекции кровотока являются серьезным вызовом современной медицине ввиду их распространенности и антибиотикорезистентности. Они удлиняют сроки госпитализации, утяжеляют исход основного заболевания, требуют значительных финансовых затрат для лечения. Неосложненные ангиогенные инфекции обычно разрешаются в течение нескольких суток. КАИК, осложненные местным нагноительным процессом или бактериемией, имеют серьезный прогноз и высокую летальность.
Профилактика
Современные протоколы четко регламентируют правила установки и ухода за ВСУ. Наибольшее внимание при этом уделяется соблюдению норм асептики и антисептики (дезинфекция операционного поля и рук персонала, хранение крышек катетеров в растворе хлоргексидина, обработка кожи и смена повязок вокруг ВСУ). Необходимо правильно осуществлять выбор внутрисосудистого устройства и места для катетеризации, максимально ограничивать срок эксплуатации внутривенных зондов, использовать гепариновые и антибактериальные замки.
1. Профилактика катетер-ассоциированных инфекций кровотока и уход за центральным венозным катетером (ЦВК). Клинические рекомендации. – 2017.
2. Комплексная клинико-этиологическая и эпидемиологическая характеристика катетер-ассоциированных инфекций кровотока/ Квашнина Д. В., Ковалишена О.В., Белянина Н.А.// Медицинский альманах. – 2017.
3. Распространенность и критерии диагностики катетер-ассоциированных инфекций кровотока/ Везирова З.Ш.// Вестник хирургии Казахстана. – 2014.
4. Инфекции, связанные с внутрисосудистыми устройствами: терминология, диагностика, профилактика и терапия/ Багирова Н.С.// Злокачественные опухоли. – 2014.
Снижение риска инфицирования при установленном мочевом катетере
Десять ключевых принципов по уходу за мочевыми катетерами
17 сентября 2009
Уретральные катетеры — одно из наиболее распространенных инвазивных вмешательств при оказании неотложной помощи и, следовательно, одна из частых причин развития внутрибольничных инфекций.
В данной статье описывается 10 основных принципов, которые необходимо учитывать при уходе за пациентами с мочевыми катетерами, установленными на относительно короткий срок — в пределах 30 дней.
Статья перед публикацией прошла рецензирование у 2-х независимых экспертов
Преамбула
Мочевые катетеры — одно из наиболее частых инвазивных устройств, используемых при неотложных состояниях. Мочевые катетеры — являются частой причинной развития ятрогенных внутрибольничных инфекций. Катетер-связанные инфекции мочевыводящих путей (КСИМП) (Catheter associated urinary tract infection (CAUTI)) вызывают дополнительные страдания для пациентов и значительно задерживают сроки выздоровления. Правильный уход за мочевым катетером — ключевой принцип предотвращения КСИМП (DH, 2007). Соблюдение научно обоснованных принципов сестринской практики позволяет значительно снизить риск заражения.
Насколько необходима постановка мочевого катетера?
Основными причинами, требующими постановки мочевых катетеров в условиях неотложной терапии являются:
- Острая и хроническая задержка мочи;
- Точный контроль диуреза;
- Контроль мочевыделения во время операции;
- Исследование мочевыводящих путей;
- Орошение мочевого пузыря;
- Введение лекарственных веществ непосредственно в полость мочевого пузыря.
Мочевые катетеры никогда не должны использоваться без крайней необходимости только для удобства персонала. При оценки необходимости мочевого катетера риск развития инфекций мочевыводящих путей должен обязательно приниматься во внимание.
Введение катетера в мочевой пузырь в нарушение обычных механизмов защиты организма позволяет микроорганизмам мигрировать по внешней поверхности катетера в мочевой пузырь (Curran and Murdoch, 2009).
После того, как катетер установлен на место, бактерии, скапливающиеся в мочеприемнике и в точках соединения системы образуют устойчивую биопленку, которая может быть предшественником КСИМП (Barford and Coates, 2009).
Ежедневный риск развития бактериурии у катетеризированного пациента составляет при чем риск возрастает с течением времени (Pratt et al, 2007). Таким образом, около 50% госпитализированных пациентов с мочевыми катетерами, установленными на срок более будут иметь бактериурию (Pratt et al, 2007).
Хотя бактериурия нередко протекает бессимптомно, у пациентов будет развиваться картина КСИМП (Pratt et al, 2007). Развитие инфекции мочевыводящих путей значительно увеличивает показатели заболеваемости и смертности. Существуют многочисленные иные доступные способы, и их следует рассмотреть до постановки мочевого катетера.
Принцип качественной практики. Используйте постоянный мочевой катетер только когда это действительно необходимо и когда все иные варианты были рассмотрены и отклонены.
Какой катетер лучше?
Есть много видов катетеров, выбор в каждом конкретном случае зависит от ожиданий пациента, причины катетеризации и ожидаемого времени постановки. Наиболее часто используется латексный катетер Фолея, который вошел в практику с годов. Однако многие пациенты чувствительны к латексу, вследствие чего требуются другие материалы. (Elvy and Colville, 2009). Есть доказательства, что катетеры с напылением серебра клинически эффективны в снижении заболеваемости КСИМП, хотя вопрос о рентабельности такого метода пока остается открытым. (Brosnahan et al, 2008; Schumm and Lam, 2008). Катетеры, пропитанные антибиотиками, также снижают бактериурию у катетеризированных взрослых пациентов стационаре, увеличивая срок до ее появления в среднем на неделю. (Schumm and Lam, 2008).
На основании исследований показано, что независимо от вида выбранного катетера должен использоваться наименьший размер, обеспечивающий свободный отток мочи, а объем раздуваемой манжеты не должен превышать 10 мл. Эти меры помогают свести к минимуму травму уретры, раздражение слизистых оболочек и количество остаточной мочи — то есть факторы, способствующие развитию КСИМП (Pratt et al, 2007).
Принцип качественной практики. Используйте подходящий для пациента тип катетера и используйте наименьший возможный диаметр.
Техника катетеризации
Как уже отмечалось, катетер, введенный в мочевой пузырь потенциально служит фактором риска попадания микроорганизмов в мочевой пузырь (Barford and Coates, 2009). Для минимизации риска катетеризация должна проводиться в асептических условиях только квалифицированным, специально обученным персоналом. (Pratt et al, 2007).
Экспертные заключения показывают, что обработка уретры асептическим раствором перед введением катетера не дает никакого преимущества и вполне достаточно использования стерильного физиологического раствора (Dunn et al, 2000; Kunin, 1997).
Травма и дискомфорт могут быть сведены к минимуму использованием соответствующих стерильных и содержащих анестетик гелей. (Pratt et al, 2007).
Принцип качественной практики. Катетеризация уретры должна проводиться в асептических условиях квалифицированным персоналом, подтвердившим свою компетенцию.
Документирование
После установки причины катетеризации, ход процедуры, тип и серийный номер катетера должны быть зафиксированы в истории болезни. После того, как катетер был установлен, необходимость катетеризации должна оцениваться ежедневно так, чтобы катетер был удален в кратчайшие сроки. Существуют некоторые данные, позволяющие предположить, что компьютерные (алгоритмизированные) системы документооборота улучшают контроль и, таким образом, сокращают сроки катетеризации. (Cornia et al, 2003).
Принцип качественной практики. Документирование и ежедневная оценка потребности в катетеризации минимизируют время стояния катетера.
Поддержание герметичности системы
Одним из основных способов минимизации риска КСИМП является поддержание герметичности системы, Это означает, что доступ к катетеру и случаи разрыва системы должны быть сведены к минимуму. Дизайн современных систем позволяет производить очистку мочеприемников с помощью специальных кранов без разбора системы в течение длительного времени. Инструкции по использованию мочеприемников были пересмотрены в последнее время, рекомендовав более длительный период использования. Проведенный систематический обзор показал, что использование запечатанных систем (где катетер и мочеприемник поставляются совместно в заводской упаковке) способствует предотвращению бактериурии (Dunn et al, 2000). Это положение было подтверждено недавно проведенным в Великобритании исследованием, которое показало сокращение на 41% случаев КСИМП при использовании герметичных систем. (Madeo et al, 2009).
Принцип качественной практики. Герметичность системы снижает риск КСИМП.
Уход за катетером
Поскольку рефлюкс и застой мочи значительно повышают риск развития КСИМП, мочеприемник всегда должен находиться ниже мочевого пузыря и должен быть закреплен на подставке, чтобы избежать контаминации (Pratt et al, 2007). Принцип нахождения мочеприемника ниже мочевого пузыря должен соблюдаться и при перемещении пациента (например, при пересаживании с кровати на стул), чтобы не допустить обратного тока мочи. Использование специальных приспособлений по расширению наружного отверстия мочеиспускательного канала уменьшает повреждение уретры, особенно у мужчин, у которых расширение уретры часто затруднено и снижает риск инфицирования. Существующая доказательная база не указывает никаких преимуществ для посткатетеризационной обработки наружных отделов уретры антисептическими растворами против обычной гигиены (ванна или душ) (Webster et al, 2001; Dunn et al, 2000).
Принцип качественной практики. Закрепляйте мочеприемник ниже уровня мочевого пузыря, чтобы избежать обратно затекания мочи. Поощряйте ежедневный прием ванны или мытье под душем для поддержания гигиены наружных отделов уретры.
Орошения, инстилляции и промывания
Систематический обзор показал, что добавление антимикробных препаратов в мочеприемник не влечет снижения заболеваемости КСИМП (Saint and Lipsky, 1999). Кроме того, нет никаких доказательств, свидетельствующих о пользе орошений, инстилляций или промывания мочевого пузыря с антимикробными или антисептическими препаратами в предотвращении КСИМП (Muncie et al, 1989; Saint and Lipsky, 1999; Kennedy et al, 1992).
Доказательства в области EBN подтверждают, что подобные процедуры не только создают угрозу из-за разгерметизации системы, но и могут вызывать местное токсическое повреждение тканей, а также способствовать появлению устойчивых форм микроорганизмов (Kunin, 1997). Тем не менее, постоянные или периодические орошения мочевого пузыря могут быть назначены в ходе урологических операций или при обструкции катетера.
Принцип качественной практики. Избегайте орошений, инстилляций и промываний мочевого пузыря без четких клинических показаний.
Гигиена рук
Хотя указано, что только герметичная система в полной мере соответствует принципам качественной практики, бывают случаи, когда целостность контура приходится нарушать, например, при опорожнении мочеприемника или заборе пробы мочи. В подобных ситуациях медицинские сестры должны обработать руки антисептиком и одеть нестерильные перчатки прежде чем начинать работу с системой (Pratt et al, 2007; WHO, 2006). В некоторых случаях дополнительно может потребоваться пластиковый фартук для защиты форменной одежды. После того как процедура будет завершена, перчатки должны быть утилизированы, а руки обработаны в соответствии с правилами (Pratt et al, 2007; WHO, 2006).
Принцип качественной практики. Использование нестерильных перчаток и обеззараживание рук при работе с катетером.
Образование и профессиональная подготовка
Принцип качественной практики. Все сотрудники должны пройти специальную подготовку по вопросам предупреждения КСИМП.
Высокая значимость ухода в комплексе медицинской помощи
Мероприятия ухода были разработаны Institute of Health Improvement и включены департаментом здравоохранения в перечень важнейших вмешательств (DH, 2007). Комплексный уход представляет собой совокупность методов, которые, выполняемые последовательно, улучшают результаты лечения пациентов. Помимо тщательного соблюдения научно обоснованных принципов ухода требуется тщательный протокол вмешательств, отражающий соблюдение установленного протокола. Проведение тщательного аудита показывает слабые места организации ухода и свидетельствует о приверженности организации принципам качественной помощи.
Принцип качественной практики. Во всех отделениях, где используется краткосрочная постановка мочевых катетеров, специалисты должны оценивать результаты своей работы, используя установленные протоколы ухода.
Заключение
Вероятность инфильтрации и экстравазального введения значительно уменьшается, если медицинская сестра понимает причины этих явлений, правильно выбирает вену для пункции или катетеризации и оборудование, а также тщательно следит за пациентом.
В соответствии со стандартами сестринской практики, инфильтрацией называется непреднамеренное введение раствора лекарственного средства в ткани, окружающие вену. Такие лекарственные средства могу вызывать раздражение окружающих тканей, если они окажутся в подкожной клетчатке, если же они выливаются на кожу, может развиваться контактный дерматит. Экстравазация — это введение значительного количества раствора лекарства мимо вены, и в некоторых случаев она сопровождается даже тканевыми некрозами.
В связи с этим, надо помнить, что некоторые растворы лекарственных средств не предназначены для ведения в периферические вены. Инфильтрация и экстравазация возникают чаще всего тогда, когда катетер не полностью находится в просвете вены, или же в стенке вены есть разрыв, который способствует утечке раствора. Причины этого явления:
- Катетер введен в вену неправильно;
- Вена повреждена, вокруг имеется отек клетчатки, который препятствует правильному току крови, раствор задерживается и вытекает в окружающие ткани;
- Внутри вены или вокруг катетера формируется тромб, который задерживает раствор, он выходит в окружающие ткани. Также при этом развиваются флебит или тромбофлебит;
- Катетер прокалывает или развивает противоположную стенку вены, что также может сопровождаться флебитом или тромбофлебитом;
- Катетер вытягивается из просвета вены при движении пациента или вследствие ненадежной фиксации.
Хотя чаще всего инфильтраты и экстравазаты возникают при инфузии в периферическую вену, эти осложнения могут развиваться и при использовании центральных венозных катетеров и имплантируемых портов. В этом случае последствия могут быть катастрофическими вследствие большого объема используемого раствора, и еще потому, что эти устройства используются для введения концентрированных и вязких растворов.
В большинстве случаев инфильтраты не приводят к тяжелому поражению тканей, но для пациента они очень некомфортны. Также приходится удалять катетер из вены и устанавливать новый, что может уменьшить число потенциально доступных вен, отнимает время и увеличивает затраты.
Самые серьезные последствия наступают, когда вне просвета сосудов оказываются раздражающие растворы, например, содержащие кальций, калий или препараты для химиотерапии. Повреждение тканей может напрямую зависеть от рН раствора: сильно щелочные или кислые растворы вызывают самые настоящие химические ожоги. Значительно концентрированные лекарственные препараты могут даже вызывать некроз тканей.
Степень повреждения при инфильтрации или экстравазации может зависеть от того, как быстро будут предприняты все меры, так как даже небольшое количество жидкости создает компрессию и повреждение. При раннем выявлении и лечении инфильтратов и экстравазатов можно предупредить повреждение нервов и тканей, и предупредить хирургическое вмешательство. Неспособность своевременно распознать эти осложнения может привести к стойкой деформации, и потере функции, даже в том случае, если пациенту будет проведена реконструктивная операция. Часто такие ошибки заканчиваются судебным процессом.
Чтобы избежать проблем, нужно быть настороженным в отношении признаков и симптомов инфильтрации и экстравазации, которые включают в себя:
Дискомфорт и жжение при инфузии раздражающего или вязкого раствора может указывать на повреждение сосуда. Жалоба на боль в месте установки катетера или иглы в вену — это основной признак того, что нужно быстро вмешиваться. В этом случае необходимо принять следующие меры:
- Прекратить инфузию;
- Если нет противопоказаний, установить катетер в вену на другой руке;
- При инфильтрате — наложить компресс, если произошла экстравазация, особенно хлорида кальция — срочно приглашайте врача.
До введения вязкого, могущего вызвать сужение сосуда, или токсичного раствора лекарственного средства, необходимо знать, какие нейтрализующие вещества (антидоты) применяются при экстравазации и инфильтрации.
Для предотвращения инфильтрации, нужно выбирать подходящую вену. Выбирайте гладкую и упругую вену, которая не похожа на веревку с узлами. Избегайте сгибательных поверхностей суставов, так как здесь смещение катетера происходит особенно часто. Если такое место — единственное, куда можно установить катетер, используйте шину. Если пациент в сознании, инфузия долгая, а ему хочется двигаться, и например, читать книжку, то лучше избегать использования вен кисти.
Чаще всего оптимально катетеризировать вены предплечья, особенно внутренней его части. Кости — это естественная шина, вены достаточно хорошо фиксированы, поэтому вероятность смещения катетера значительно уменьшается.
Начинайте выбирать вену на предплечье так низко, насколько это вообще возможно (не стоит использовать место сделанной недавно венепункции), но не стоит ипользовать вены на внешней поверхности предплечья около запястья, так как там близко проходят нервы. Лучше не использовать вены внутренней части ниже локтя (антекубитальная ямка) — инфильтрацию в этой зоне очень легко просмотреть и она бывает немаленькой. При значительно инфильтрации в антекубитальной ямке жидкость сдавливает важные анатомические структуры и может привести к повреждению нервов и некрозу тканей.
Чтобы раствор лекарственного препарата максимально смешивался с кровью, выбирайте катетер минимально возможного диаметра, это позволит крови смешиваться с инфузатом, и обеспечить его адекватное разведение.
Всегда водите иглу срезом вверх, чтобы уменьшить риск сквозного прокола вены, тщательно фиксируйте катетер, чтобы он не смещался, особенно у детей и пожитых.
После того, как врач установит катетер в центральную вену, или медсестра — периферическую, место пункции проверяют каждые час-два, особенно если проводится длительная инфузия. Убедитесь, что место пункции вены хорошо видно (лучше применять прозрачные заклейки, а не марлевые салфетки).
Регулярно проверяйте, не появилось ли напряжения и отека в месте введения катетера. Спрашивайте пациента, нет ли боли, если говорить он не может, проверяйте место пункции чаще. Если вы заметите инфильтрацию или экстравазацию, сразу же прекращайте инфузию, и проверяйте, что произошло. Если инфильтрат большой, или раствор был раздражающий — немедленно зовите врача. Если катетер остался на месте, можно попробовать шприцом аспирировать часть попавшей в ткани жидкости, также через катетер можно вести антидот.
После удаления катетера больную руку надо держать в приподнятом положении (например, на подушке), и приложить холодный компресс, если это лекарства для химиотерапии — то теплый компресс. Если появляется некроз (обычно через может быть необходимой консультация хирурга.
Как документировать осложнения инфузионной терапии
Во-первых, нужно измерить участок измененных тканей, чтобы потом можно было оценить эффективность лечения. Обязательно нужно отслеживать состояние кожи и мягких тканей, чтобы избежать тяжелых осложнений, также это помогает оценить качество медицинской помощи.
Применение устройств для фиксации конечности, особенно в детской и гериатрической практике, может давать удивительные результаты: частота смещения катетеров может снизиться до нуля, и не будет тяжелых последствий. Соблюдение описанных выше несложных приемов может предотвратить осложнение. Ну а если оно все-таки возникло, то последствия можно сделать минимальными, если быстро и адекватно реагировать на случившееся.
Отдельно — о центральных венозных катетерах и имплантируемых портах
В соответствии с международными стандартами, раствор лекарственного средства, имеющий рН менее 5 и более 9, не должен вводиться через периферические вены. Например, это — ванкомицин (pH, ∼2.4) и фенитоин (pH, ∼12). То же самое касается и растворов, содержащих более 5% гидролизата белков, или 10% глюкозы.
Поскольку экстравазация такого раствора может иметь катастрофические последствия, то все их вводят через центральный венозный катетер или имплантируемый порт. Если приходится однократно вводить такой раствор в периферическую вену, то его вводят через толстый катетер, через боковой порт во время инфузии физиологического раствора, предпочтительнее иметь отдельный катетер для таких целей.
При введении вязкого или раздражающего раствора через центральный венозный катетер, всегда следует проверять обратный ток крови по катетеру, и часто делать это повторно во время инфузии. Если обратного тока крови нет, то это можно указывать на выход катетера из просвета вены, и утечке раствора в окружающие ткани. Также может быть тромбоз катетера — в этом случае срочно останавливайте инфузию и зовите врача во избежание тяжелых последствий.
Иногда врач проводит контрастное исследование под контролем рентгена, чтобы убедиться в проходимости катетера и может растворить тромб.
Если венозный доступ осуществляется через имплантируемый порт, важно выбирать иглу адекватной длины, чтобы она не выскочила из порта, и раствор не ушел бы в окружающую клетчатку. Если же игла окажется слишком длинной, то это может привести к повреждению мембраны порта, в результате чего экстравазация будет происходить уже через мембрану.
Когда инфузия лекарственного средства проводится через имплантируемый порт, нужно часто осматривать место установки порта, как и при работе с периферическим венозным катетером, чтобы своевременно выявить любую утечку или отек подкожной клетчатки рядом с портом. Если пациент жалуется на ЛЮБОЙ дискомфорт, немедленно прекращайте инфузию и посмотрите, что случилось. При подозрении на проблемы с портом — срочно зовите врача. Иногда порт может отсоединяться от катетера, и в этом случае пациенту нужна немедленная операция.
Шкала оценки инфильтравии в месте инфузии (Journal of Infusing Nursing, 2006)
0 баллов — нет никаких симптомов
1 балл — напряженная кожа, отек до 2.5 см в диаметре, холодная наощупь кожа, боль может быть, а может и не быть
2 балла — Кожа натянута, отек от 2 до 12 см в любом направлении, кожа холодная наощупь, боль может быть, а может и не быть
3 балла — кожа напряжена и просвечивает, большой отек — больше 15 см, в любом направлении, кожа холодная наощупь, боль средняя или умеренная, может быть онемение
4 балла — Кожа напряжена, просвечивает, плотная, может быть даже повреждена, обесцвечена, имеется выраженный отек, более 15 см, в любом направлении, отек глубокий, есть нарушения кровотка, боль от умеренной до выраженной, могут быть синяки
К последней, самой тяжелой степени инфильтрации, также относится утечка любого препарата крови, раздражающего или очень вязкого раствора.
Читайте также:

