Mrsa инфекция что это такое чем лечить
Обновлено: 23.04.2024
Эта информация позволит вам узнать, что представляет собой метициллин-резистентный золотистый стафилококк (МРЗС), как он распространяется и как лечатся вызываемые МРЗС инфекции.
Что представляет собой метициллин-резистентный золотистый стафилококк?
Стафилококк (Staphylococcus) — это вид бактерий, обитающих в окружающей среде, в том числе и на поверхности кожи человека. Метициллин-резистентный золотистый стафилококк (МРЗС) — это стойкий к определенным антибиотикам вид стафилококка. Это означает, что некоторые методы лечения не справятся с ним или будут менее эффективными.
МРЗС может вызывать различные заболевания, например:
- инфекции мочеполовой системы (ИМС);
- воспаление легких;
- кровяные инфекции;
- раневые или кожные инфекции.
В чем состоит разница между колонизацией и инфицированием МРЗС?
Человек может быть либо колонизирован, либо инфицирован МРЗС. Колонизация означает наличие бактерий на коже или в организме человека при отсутствии каких-либо симптомов. Инфицирование означает наличие бактерий на коже или в организме, приводящее к появлению симптомов.
Как распространяется МРЗС?
Большинство инфекций, вызываемых МРЗС, распространяется через прямой контакт с физиологическими жидкостями инфицированного человека, такими как кровь, выделения из раны, моча, стул или мокрота (флегма). Также они могут распространяться через контакт с оборудованием или поверхностями, на которых могут находиться эти бактерии. МРЗС не распространяются при простом контакте, например через прикосновение или объятие.
Кто подвержен риску инфицирования МРЗС?
Заразиться инфекцией, вызываемой МРЗС, с большей вероятностью могут лица:
- старшего возраста;
- с ослабленной иммунной системой;
- страдающие хроническими заболеваниями, такими как рак или диабет;
- ранее принимавшие антибиотики;
- недавно перенесшие операцию;
- лежавшие в больнице много раз или длительное время;
- с открытыми ранами или язвами;
- с установленными трубками или дренажами.
Каковы симптомы инфекции МРЗС?
Ваши симптомы будут зависеть от места возникновения инфекции и от типа инфекции.
Каковы методы лечения инфекции, вызываемой МРЗС?
Инфекции, вызываемые МРЗС, лечатся антибиотиками, к которым у вызвавших их бактерий нет устойчивости.
Какие меры по изоляции принимаются в больнице, если у меня обнаружена инфекция, вызываемая МРЗС?
Меры по изоляции - это мероприятия, которые мы проводим, чтобы предотвратить распространение инфекции среди пациентов. Если во время пребывания в больнице у вас диагностировали инфекцию, вызываемую МРЗС, или вы подверглись риску заражения этой инфекцией:
- Вас поместят в отдельную палату.
- На вашей двери повесят табличку с информацией о том, что весь персонал и посетители должны вымыть руки с мылом или протереть их спиртосодержащим антисептиком для рук перед входом и после выхода из вашей палаты.
- Весь персонал и все посетители, входящие в вашу палату, должны надеть желтый халат и перчатки. Они выдаются за пределами вашей палаты и могут быть утилизированы в вашей палате.
- Если вы выходите из палаты для проведения исследований, вам следует надеть желтый халат и перчатки или покрыться чистой простыней.
- Если вы выходите из своей палаты, чтобы прогуляться по отделению, вам следует надеть желтый халат и перчатки.
- Вам запрещен доступ в следующие зоны больницы:
- кладовая для продуктов в вашем отделении;
- центр отдыха в M15;
- детские зоны отдыха в M9;
- кафетерий;
- основной вестибюль;
- любые другие зоны общего пользования на территории больницы.
Врач скажет вам, когда можно будет прекратить соблюдать эти меры предосторожности. Это произойдет после того, как вы пройдете курс лечения и у вас исчезнут все симптомы.
Какие меры по изоляции мне следует принять дома, если у меня обнаружится инфекция, вызываемая МРЗС?
Дома обязательно делайте следующее:
- Часто мойте руки водой с мылом, особенно после посещения туалета.
- Мойте руки после контакта с кровью, мочой или выделениями из раны.
- Пользуйтесь дезинфицирующим средством (например Clorox ® или Lysol ® ) для очистки поверхностей, которые могли быть заражены бактериями, например дверной ручки.
Где я могу получить дополнительную информацию о МРЗС?
Если у вас есть вопросы, обратитесь к своему врачу или медсестре/медбрату. Кроме того, для получения дополнительной информации вы можете посетить веб-сайты:
Атипичная микобактериальная инфекция — комплекс гранулематозных поражений, вызываемых микобактериями, отличающимися от классических патогенов — возбудителей туберкулёза и лепры.
Этиология. Возбудители — кислотоустойчивые бактерии Mycobacterium ulcerans, M. marinum (M. balnei), M. kansasii, M. avium-intracellulare, M. xenopi, M. scrofulaceum.
Эпидемиология. Большинство возбудителей широко распространено в окружающей среде; некоторые обитают в воде и прибрежной зоне, вызывая заболевания у рыб, другие (например, Mycobacterium avium-intracellulare) — у птиц. Наиболее часто заражение происходит при вдыхании микобактерий, употреблении заражённых продуктов и проникновении возбудителя через микротравмы кожи и слизистых оболочек.
Патогенез. Проникшие микобактерии фагоцитируются макрофагами и транспортируются в регионарные лимфатические узлы; фагоцитарные реакции незавершённые, и возбудитель персистирует в цитоплазме макрофагов. Воспалительная реакция незначительная, но в месте проникновения развивается первичный аффект. В динамике по ходу регионарных лимфатических путей и узлов формируется первичный комплекс, характеризующийся развитием гранулём. Микроскопия биоптатов выявляет в последних очаги неказеозного некроза, содержащие кислотоустойчивые бактерии.
Клиническая картина
• Туберкулёзоподобные поражения. В патологический процесс вовлекаются лёгкие, почки, кожные покровы и костно-суставная система. Часто осложняют течение эмфизематозных процессов. У 40–50% больных с иммунодефицитными состояниями вызывают генерализованные поражения.
• Лимфадениты. Клинически чаще проявляются поражениями шейных лимфатических узлов (так называемые скрофулы); последние безболезненны, могут изъязвляться либо дренироваться наружу; системные проявления слабые или чаще отсутствуют.
• Кожные поражения. Типичным считают инфицирование ран конечностей, полученных при ударе о стенку бассейна или любой объект на дне и берегах водоёма. Чаще наблюдают образование изъязвляющейся гранулёмы, спонтанно ограничивающейся в течение нескольких недель, в более редких случаях формируется хроническая инфекция.
Методы исследования • Выделение и идентификация возбудителя по скорости роста, образованию пигментов (на свету или в темноте) и патогенности для лабораторных животных • АТ к Mycobacterium kansasii перекрёстно реагируют с Аг Mycobacterium tuberculosis и у инфицированных лиц отмечают положительную реакцию Манту.
Дифференциальная диагностика • Лепра • Туберкулёз • Боррелиоз • Чума.
Лечение • При лёгочных поражениях •• Рекомендовано сочетание изониазида 600 мг, рифампицина 300 мг, стрептомицина 1 г и этамбутола 15–25 мг/кг 1 р/сут •• При поражении M. marinum — миноциклин по 100 мг каждые 12 ч в течение 6–8 нед •• При поражении M. kansasii и M. xenopi эффективна стандартная противотуберкулёзная терапия с обязательным назначением рифампицина •• Оперативное вмешательство рекомендовано при локализованных поражениях у пациентов молодого возраста без патологии других органов и систем • При лимфадените — у детей от 1 до 5 лет показано хирургическое лечение • При кожных поражениях, вызванных M. marinum, — тетрациклин (1–2 г/сут) и сочетание рифампицина и этамбутола в течение 3–6 мес • При инфекциях, вызванных ранами или инородными телами •• Хирургическая обработка раны и удаление инородного тела •• Лекарственная терапия: доксициклин (200–400 мг/сут), цефокситин (200 мг/кг/сут), амикацин (10–15 мг/сут) в течение 3–6 мес • При диссеминированных поражениях — сочетание противотуберкулёзных средств (как при лёгочных поражениях) лишь уменьшает бактериемию и временно ослабляет симптомы.
Течение и прогноз. Течение — прогрессирующее. Более чем у 20% пациентов отмечают рецидивы заболевания в течение 5 лет.
МКБ-10. A31 Инфекции, вызванные другими микобактериями
Код вставки на сайт
Атипичная микобактериальная инфекция — комплекс гранулематозных поражений, вызываемых микобактериями, отличающимися от классических патогенов — возбудителей туберкулёза и лепры.
Этиология. Возбудители — кислотоустойчивые бактерии Mycobacterium ulcerans, M. marinum (M. balnei), M. kansasii, M. avium-intracellulare, M. xenopi, M. scrofulaceum.
Эпидемиология. Большинство возбудителей широко распространено в окружающей среде; некоторые обитают в воде и прибрежной зоне, вызывая заболевания у рыб, другие (например, Mycobacterium avium-intracellulare) — у птиц. Наиболее часто заражение происходит при вдыхании микобактерий, употреблении заражённых продуктов и проникновении возбудителя через микротравмы кожи и слизистых оболочек.
Патогенез. Проникшие микобактерии фагоцитируются макрофагами и транспортируются в регионарные лимфатические узлы; фагоцитарные реакции незавершённые, и возбудитель персистирует в цитоплазме макрофагов. Воспалительная реакция незначительная, но в месте проникновения развивается первичный аффект. В динамике по ходу регионарных лимфатических путей и узлов формируется первичный комплекс, характеризующийся развитием гранулём. Микроскопия биоптатов выявляет в последних очаги неказеозного некроза, содержащие кислотоустойчивые бактерии.
Клиническая картина
• Туберкулёзоподобные поражения. В патологический процесс вовлекаются лёгкие, почки, кожные покровы и костно-суставная система. Часто осложняют течение эмфизематозных процессов. У 40–50% больных с иммунодефицитными состояниями вызывают генерализованные поражения.
• Лимфадениты. Клинически чаще проявляются поражениями шейных лимфатических узлов (так называемые скрофулы); последние безболезненны, могут изъязвляться либо дренироваться наружу; системные проявления слабые или чаще отсутствуют.
• Кожные поражения. Типичным считают инфицирование ран конечностей, полученных при ударе о стенку бассейна или любой объект на дне и берегах водоёма. Чаще наблюдают образование изъязвляющейся гранулёмы, спонтанно ограничивающейся в течение нескольких недель, в более редких случаях формируется хроническая инфекция.
Методы исследования • Выделение и идентификация возбудителя по скорости роста, образованию пигментов (на свету или в темноте) и патогенности для лабораторных животных • АТ к Mycobacterium kansasii перекрёстно реагируют с Аг Mycobacterium tuberculosis и у инфицированных лиц отмечают положительную реакцию Манту.
Дифференциальная диагностика • Лепра • Туберкулёз • Боррелиоз • Чума.
Лечение • При лёгочных поражениях •• Рекомендовано сочетание изониазида 600 мг, рифампицина 300 мг, стрептомицина 1 г и этамбутола 15–25 мг/кг 1 р/сут •• При поражении M. marinum — миноциклин по 100 мг каждые 12 ч в течение 6–8 нед •• При поражении M. kansasii и M. xenopi эффективна стандартная противотуберкулёзная терапия с обязательным назначением рифампицина •• Оперативное вмешательство рекомендовано при локализованных поражениях у пациентов молодого возраста без патологии других органов и систем • При лимфадените — у детей от 1 до 5 лет показано хирургическое лечение • При кожных поражениях, вызванных M. marinum, — тетрациклин (1–2 г/сут) и сочетание рифампицина и этамбутола в течение 3–6 мес • При инфекциях, вызванных ранами или инородными телами •• Хирургическая обработка раны и удаление инородного тела •• Лекарственная терапия: доксициклин (200–400 мг/сут), цефокситин (200 мг/кг/сут), амикацин (10–15 мг/сут) в течение 3–6 мес • При диссеминированных поражениях — сочетание противотуберкулёзных средств (как при лёгочных поражениях) лишь уменьшает бактериемию и временно ослабляет симптомы.
Течение и прогноз. Течение — прогрессирующее. Более чем у 20% пациентов отмечают рецидивы заболевания в течение 5 лет.
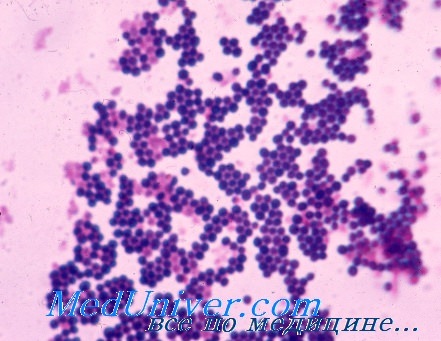
Золотистый стафилококк (S. aureus) как причина раневых инфекций. Резистентность к антибиотикам MRSA
Посев крови редко может помочь клиницистам в диагностике послеоперационных раневых инфекций в области брюшной полости. Интраабдоминальные инфекции это распространенная проблема, стоящая на 2-м месте среди наиболее частых причин летальности от инфекции. По зарубежным данным, рост из крови микроорганизма, идентичного микроорганизму из инфицированной послеоперационной раны, регистрируется в 0% случаев при аппендэктомии и достигает 5% при наличии чрескожных дренажных устройств. При инфицированных послеоперационных ранах наиболее целесообразно назначать посев крови больным отделения реанимации, где летальность от инфекции высока.
В хирургии 15,2% бактериемии обусловлены S. aureus и статистически значимо связаны с летальностью. Зависимость развития послеоперационной бактериемии от вида микроорганизма, выделенного из рапы, более значима, чем от типа хирургической операции. Выявление S. aureus в ране - независимый фактор риска послеоперационной стафилококковой бактериемии с летальностью до 16%.
Анализ чувствительности Staphylococcus spp. касается в первую очередь препаратов, имеющих основное клиническое значение.В отношении метициллин-чувствительных стафилококков (MSSA, MSSE), следует упомянуть группу фторхинолонов, применяемых для лечения стафилококковых инфекций (особенно кожи и мягких тканей), например левофлоксацин (Таваник) и моксифлоксацин (Авелокс), которые обладают более высокой активностью при стафилококковых инфекциях в сравнении с традиционными препаратами данной группы. Между этими антибиотиками нет полной перекрестной резистентности. По нашим данным, для трех наиболее часто выделяемых видов стафилококков (S. aureus, S. epidermidis, S. haemolylicus) моксифлоксацин статистически значимо более эффективен in vitro по сравнению с левофлоксацином.
![золотистый стафилококк S. aureus MRSA]()
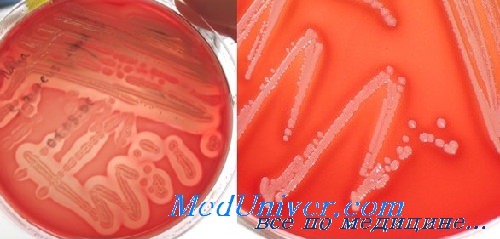
Как правило, препаратами выбора для лечения стафилококковых инфекций служат b-лактамные антибиотики. Существует два основных механизма устойчивости стафилококков к этой группе препаратов: продукция b-лактамаз или наличие дополнительного пенициллинсвязывающего белка (ПСБ2а). Выявление этих механизмов и четкое их разграничение у конкретных штаммов стафилококков позволяют точно прогнозировать эффективность всей группы b-лактамных антимикробных препаратов без необходимости определения чувствительности к каждому препарату в отдельности.
В связи с этим следует руководствоваться следующими правилами при анализе антибиотикограммы стафилококков:• чувствительность к бензилпенициллину/ампициллииу: штамм не имеет механизмов резистентности. Можно прогнозировать чувствительность ко всем остальным b-лактамным антибиотикам (например, к цефазолипу, цефотаксиму и др.). Препараты выбора: природные пенициллины (например, бензилпенициллин — пенициллин G);
• устойчивость к бензилпенициллину/ампициллину, но чувствительность к оксациллину/метициллину: штамм продуцирует ферменты b-лактамазы (пенициллиназы), способные разрушать природные и полусинтетические пенициллины.
В данном случае можно применять b-лактампые антибиотики с потенциальной антистафилококковой активностью (антистафилококковые пенициллины, цефалоспорипы I, II, IV поколений, карбапеиемы). Препараты выбора: ингибиторзащищенные пенициллины (например, амоксициллин/клавуланат — Амоксиклав, Аугментин) или цефалоспорипы I (например, цефазолин - Кефзол) и II (например, цефуроксим) поколений;
• устойчивость и к бензилпенициллину/ампициллину, и к оксациллину/метициллину: штамм имеет ПСБ2а, следовательно, все b-лактамные антибиотики клинически будут неэффективны, даже если в антибиотикограмме будет указана чувствительность к ним.
Для штаммов с истинной оксациллин/метициллин-резистентностью характерна ассоциированная резистентность к антибиотикам и других групп (например, к гентамицину, клиндамицину, ципрофлоксацину и др.). Препараты выбора: гликопептиды (ванкомицин), вторая линия — оксазолидиноны (линезолид). Таким образом, определение чувствительности стафилококков к антибиотикам в рутинной работе при определенных обстоятельствах можно ограничить двумя тестами: определение чувствительности к бензилпенициллипу и оксациллипу (выявление истинной резистентности к оксациллипу подразумевает выявление гена тесА, кодирующего синтез ПСБ2а).
![золотистый стафилококк S. aureus MRSA]()
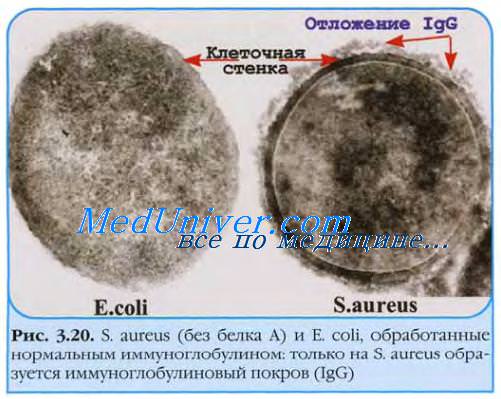
По нашим данным, при послеоперационных раневых инфекциях штаммы S. aureus, обладающие истинной резистентностью к оксациллину (MRSA), составляют всего 9,5% (39 из 410), что статистически значимо ниже в сравнении с коагулазонегативными стафилококками (КНС). Так, 66,9% (204 из 305) штаммов S. epidermidis и 100% (191 из 191) штаммов S. haemolyticus были расценены как метициллин-резистентные коагулазонегативные стафилококки (КНС).
MRSA важный нозокомиальный патоген, составляющий более 50% НКИ в США, один из основных возбудителей послеоперационных раневых инфекций (РИ). Доля MRSA в структуре послеоперационных раневых инфекций (РИ) в США выросла С 9% в 1995 г. до 30% в 2000 г. с атрибутивной летальностью 21 %.
J.J. Engemann и соавт. изучили влияние MRSA на исход при послеоперационных инфекциях у 479 больных и пришли к выводу, что летальность у больных без инфекции составила всего 2,1%, при инфекции, обусловленной метициллин-чувствительными S. aureus (MSSA), — 6,7%, что статистически значимо выше, чем в случае без инфекции. Для MRSA летальность была статистически значимо выше, чем в каждом из предыдущих случаев, — 20,7%. Кроме того, стоимость лечения возрастала с 29 455 долларов США в случае без инфекции до 52 791 долларов при MSSA и достигала 92 363 долларов при MRSA.
Таким образом, экономические потери и увеличение летальности при хирургических инфекциях, обусловленных MRSA и MR-КНС, очевидны.Пациенты больниц и медицинские работники по сути представляют собой потенциальный резервуар для штаммов MRSA, любые меры по уменьшению значимости этих резервуаров могут способствовать снижению НКИ, обусловленных MRSA. Весьма эффективным может быть выявление носителей штаммов MRSA среди медработников, а также обследование больных перед госпитализацией путем исследования слизистой оболочки полости носа с последующей санацией выявленных носителей или их изоляцией. Выделение специальных помещений для больных, колонизированных или инфицированных штаммами MRSA, с ограничением их передвижения в пределах больницы уже не только признано целесообразным, по и имеет место на практике во многих зарубежных клиниках.
Для лечения взрослых больных с послеоперационными раневыми инфекциями, обусловленными MRSA, рекомендован ряд препаратов: ванкомицин, линезолид, даптомицин, тигециклин, телеванцин. В недалеком будущем будет доступен новый антибиотик цефтаролин (цефалоспорин, Зинфоро). Хотя новые антибиотики с эффективностью против MRSA по сравнению с вапкомицином не демонстрируют особых преимуществ. Следует обращать внимание на то, какие штаммы циркулируют в конкретном стационаре: если МПК ванкомицина в отношении S. aureus не более 2 мкг/мл, назначать ванкомицин можно при его клинической эффективности, по в случае МПК > 2 мкг/мл (VISA штамм со сниженной чувствительностью ванкомицину, VRSA — ванкомицин резистентный штамм) следует переходить на альтернативные препараты.
По данным отечественных стационаров чувствительность к ванкомицину всех исследованных в ходе мониторинга штаммов стафилококков высока, но статистически значимо ниже для S. epidermidis по сравнению с S. aureus и S. haemolyticus. Эффективность линезолида (Зивокс) и тигециклина in vitro составляет 100% в отношении всех видов стафилококков.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Симптомы инфекции метициллинрезистентного золотистого стафилококка и ее лечение
Инфекция, вызываемая метициллинрезистентным стафилококком, является серьезной проблемой здравоохранения во многих странах; в Великобритании за последние 10 лет заболеваемость этой инфекцией возросла.
С 2001 г. случаи бактериемии, вызванной метициллинрезистентным стафилококком, подлежат регистрации санитарно-эпидемиологической службой. В настоящее время число случаев заболевания пошло на убыль. В 2008 г. всем лечебным учреждениям Великобритании была поставлена цель снизить заболеваемость инфекцией, вызываемой метициллинрезистентным стафилококком, на 50%.
а) Эпидемиология. Госпитальная инфекция, является международной проблемой; частота случаев госпитальной инфекции составляет 5-10%. Однако данные по частоте случаев сепсиса, вызываемого метициллинрезистентным стафилококком, по европейским странам колеблются в широких пределах. Так, в 2002 г. она составила 0,7% в Швеции и 45% в Греции (данные Европейской системы по надзору за антимикробной резистентностью, EARSS).
![Золотистый стафилококк]()
в) Профилактика. Основные усилия в решении проблемы инфекции, вызываемой метициллинрезистентным стафилококком, сосредоточены на профилактике. Все лечебные учреждения должны иметь собственную стратегию борьбы с этой инфекцией. Важную роль играет соблюдение чистоты рук, в частности тщательное их мытье в период между контактами с больными и смазывание спиртсодержащим гелем.
Все процедуры и манипуляции должны выполняться с соблюдением асептики, а различные устройства и приспособления, включая мочевые и венозные катетеры, должны быть промаркированы и отмечены в соответствии с протоколом, разработанным в данном учреждении.
Все больные при госпитализации проходят скрининг, призванный выявить принадлежащих к группе высокого риска. При этом исследованию подлежат полость носа, трахеостома, паховая область, раны и язвы, гастро- и энтеро-стома, внутривенные катетеры, мокрота.
г) Лечение. Больные с колонизацией метициллинрезистентным стафилококком должны принимать ванну или душ с триклозаном (Аквасепт) или октенидином (Октенизан) в течение 10 дней. Для эрадикации этого патогена из полости носа применяют мупироциновую мазь, которой смазывают ноздри 3-5 раз в день. Эрадикация считается достигнутой, если три последовательных анализа с интервалом 1 нед., дают отрицательный результат.
При бактериемии, вызванной метициллинрезистентным стафилококком, внутривенно вводят ванкомицин и тейкопланин. Однако в настоящее время отмечено появление форм метициллинрезистентного стафилококка, резистентных к ванкомицину, что требует консультации с микробиологом.
- Вернуться в оглавление раздела "отоларингология"
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также: