Мумие при красной волчанке
Обновлено: 19.04.2024
Владимир Трофимович Ивашкин, академик РАМН, доктор медицинских наук:
– Ну, что ж, мы съели довольно много времени у Игоря Львовича. Поэтому он должен сейчас продемонстрировать высочайшее мастерство, и вместо 25 минут изложить свой материал в течение 12 минут. Но тогда это будет класс, тогда мы действительно признаем ваше невероятное совершенство как лектора.
Игорь Львович Халиф, профессор:
– Спасибо, Владимир Трофимович. Давайте сразу же начнем. Самое главное, это определение. Я всегда об этом говорю. Когда хорошее определение, сразу понятно, о чем идет речь.
Болезнь Крона – это хроническое рецидивирующее, то есть неизлечимое, заболевание всего желудочно-кишечного тракта. Этиология неизвестна, характеризуется трансмуральным (поражение всей стенки кишки) сегментарным (чередование пораженных и непораженных сегментов) распространением воспалительного процесса, самое главное, с развитием местных и системных осложнений.
Вот фотография самого Баррила Крона, который умер в возрасте 99 лет. В 1932 году он вместе с Оппенгеймером и Гинзбургом впервые описал терминальный илеит.
Что же важно знать? Уже сегодня это звучало. Это в первую очередь внекишечные проявления, которые иной раз проходят мимо врача и лечатся у дерматологов, у хирургов. Посмотрите на гангренозную пиодермию. Если бы кто-то подумал о возможности, что это проявление болезни Крона, то никогда хирург не стал бы иссекать эти очаги. Потому что практически все внекишечные симптомы, проявляемые у больных воспалительными заболеваниями кишечника, связаны с активностью процессов в кишке. То же самое: артропатия, эписклерит, увеит, иридоциклит – длительное лечение у других специалистов, и нет никакой мысли о том, что нужно подумать и, самое главное, расспросить больного о возможном проявлении кишечной симптоматики. Афтозный стоматит, лечение у стоматологов и прочее – затрудняют начало точной диагностики заболевания.
А вот то, что иной раз бывает, к сожалению, и у колопроктологов, у хирургов, которые сталкиваются с трещинами, со свищами прямой кишки. Не обследуя больных, они делают свое дело – как говорится, иссекают хирургическим путем. Что возможно и к чему это может привести, посмотрите.
Юрий Анатольевич Шелыгин, профессор:
– Я тут не могу согласиться. Хочу защитить хирургов. Проявление самой болезни, это же не результаты сечения.
Халиф И.Л.:
– Но проявление болезни, которое не диагностировано было хирургами.
Шелыгин Ю.А.:
– Это да. И не назначено лечение.
Халиф И.Л.:
– Не просто не назначено, а ненужное хирургическое лечение привело к таким вот последствиям. То есть вопрос ставится именно о том, что всегда при наличии каких-либо проявлений нужно помнить, что эти проявления могут быть не основным заболеванием, а проявлением другого заболевания, более серьезного.
Второй момент, сегодня тоже об этом звучало, это гормональная зависимость и гормональная резистентность. Самый важный момент в том, что мы все должны полностью уйти от стероидов. Когда разговор вновь ведется о так называемой пульс-терапии (я этого не понимаю), о добавлении к этой пульс-терапии Циклофосфана, даются огромнейшие дозы, это абсолютно неверный подход. Это же относится и к поддерживающей терапии на гормонах. Сегодня об этом говорил Олег Самуилович.
Шелыгин Ю.А.:
– Разве мы рекомендуем пульс-терапию?
Халиф И.Л.:
Ивашкин В.Т.:
– Вы знаете, эта пресловутая пульс-терапия, это какое-то поветрие в нашей терапевтической практике.
Халиф И.Л.:
Ивашкин В.Т.:
– Сколько я с этим борюсь, я не видел ни одного случая, когда бы пульс-терапия приносила реальные результаты. Плохо делает, это абсолютно.
Халиф И.Л.:
Ивашкин В.Т.:
– Вместо терпеливого, спокойного назначения адекватной дозы стероидов и наблюдения за пациентом…
Халиф И.Л.:
Ивашкин В.Т.:
– Вообще, это непонимание того, мне кажется, что это хронический процесс, неизлечимый процесс.
Халиф И.Л.:
Ивашкин В.Т.:
– Я понимаю, когда острейший гломерулонефрит аутоиммунной природы, где быстро нарастает острая почечная недостаточность и где большие дозы глюкокортикоидов (00:05:00) могут в довольно значительной степени улучшить. Но при хроническом заболевании…
Халиф И.Л.:
– Так вот поэтому, конечно, об этом нужно помнить и всегда говорить, что отмена стероидов – это основа любого консервативного терапевтического мероприятия у данных больных.
Больные с болезнью Крона после любого лечения обязаны находится на противорецидивной терапии!
Шелыгин Ю.А.:
– В течение всей жизни, получается.
Халиф И.Л.:
– Практически да. Смотрим дальше. 2009 год, естественно, атака. Опять назначается Будесонид. Хороший эффект. Опять не назначается противорецидивная терапия. Опять получает снижение дозы Будесонида, оставляя его якобы на противорецидивную терапию. Хотя это не системный, а местный стероид, но получаем осложнения. И вот дальше начинается постоянный прием стероидного препарата в течение двух лет, хотя это Будесонид. Что же происходит? Естественно, на фоне этой терапии опять появляются обострения.
В апреле 2010 года больная обследуется: терминальный илеит, при илеоколоноскопии – фаза язв. То есть нет эффекта от проводимой терапии. И тогда больной назначается уже системная стероидная терапия из расчета 1 мг на 1 кг массы тела. В последующем добавляется Пентаса. Все верно, докторами проводится правильная оценка, снижается доза гормонов. И на фоне 15 мг – обострение. Больная попадает к нам в центр. Мы констатируем у нее гормональную зависимость и начинаем лечение Инфликсимабом. Это 2 года биологической терапии для того, чтобы преодолеть гормональную зависимость. Подсоединяем иммуносупрессоры – Азатиоприн. Получаем клиническую ремиссию. На протяжении двух лет (до января 2012 года) она принимает Инфликсимаб.
Смотрим дальше. Естественно, начинаются обострения, ноющие боли в правой подвздошной области, лихорадка до 39 градусов в вечернее время суток. При обследовании в декабре 2013 года у нас мы уже констатируем наличие глубоких язвенных дефектов, наличие инфильтрата, стриктуры в области илеоцекального отдела. А при исследовании тонкой кишки находим осложнение межкишечным илеоцекальным свищом, который уже, конечно же, никакими консервативными методами вылечить невозможно с наличием инфильтративного процесса. Поэтому больная подвергается хирургическому лечению. И восстанавливается вновь противорецидивная терапия уже Хумирой с назначением иммуносупрессии. Больная выписывается на длительную противорецидивную терапию.
Шелыгин Ю.А.:
Халиф И.Л.:
– Не менее двух лет.
Шелыгин Ю.А.:
Халиф И.Л.:
– А дальше, Юрий Анатольевич, рассматривается следующий вопрос. Мы все прекрасно понимаем, что биологическая терапия, это затратная терапия. И если мы получаем на фоне двухлетней терапии, как сейчас принято говорить, deep remission – глубокую ремиссию, то есть эндоскопическую и клиническую ремиссию, то мы можем рассмотреть вопрос о прекращении биологической терапии и оставлении этого больного на иммуносупрессивную терапию Азатиоприном в последующем, но с обязательным контролем. Потому что мы знаем, что ускользание эффекта от иммуносупрессивной терапии возможно, и тогда надо снова рассматривать вопрос о присоединении биологической терапии в этом случае.
Ивашкин В.Т.:
– Критерий 2 года сейчас стал общим для аутоиммунных заболеваний.
Халиф И.Л.:
Ивашкин В.Т.:
– То же самое при аутоиммунном гепатите. Мы обязаны лечить 2 года. То же самое при ревматоидном артрите. То же самое здесь.
Шелыгин Ю.А.:
Халиф И.Л.:
– Итак, второй случай. Пациент в возрасте 41 года. В 2005 году дебют болезни Крона. Появляется диарея, боли в правой подвздошной области, выявляется невыраженная легкая железодефицитная анемия. Колоноскопия не проводится, хотя, в общем-то, уже можно было бы подумать об этом. Проводится так называемая курсовая терапия пробиотиками, спазмолитиками с очень непостоянным эффектом. И до 2010 года больной переходит от одного врача к другому, плюс самостоятельное лечение. В 2010 году экстренная госпитализация с резкими болями в животе с повышением температуры до 40 градусов. Оперируется по месту жительства. Обнаруживаются изменения в тонкой кишке, характерные, как говорят хирурги, для болезни Крона. И больному ничего не производится, он выписывается на терапии Сульфасалазином без какого-либо дополнительного обследования.
Сентябрь 2011 года – больной, наконец, обследуется в стационаре. Посмотрите, это с 2008 года. При илеоколоноскопии выявляется картина перенесенного очагового воспаления.
Ивашкин В.Т.:
– Вы знаете, мне не хочется, чтобы у нашей аудитории создалось впечатление, что это только в России такое.
Халиф И.Л.:
Шелыгин Ю.А.:
– Нет, это везде, конечно.
Ивашкин В.Т.:
– Такое же в США, во Франции, в Англии.
Шелыгин Ю.А.:
– Это мировая ситуация.
Халиф И.Л.:
И пожалуйста, январь 2012 года – больной вновь экстренно оперируется. Интраоперационно выявлен диффузный перитонит, воспалительные изменения в области тощей уже кишки. И производится формирование еюно-еюноанастомоза с выключением пораженного участка тощей кишки из пищеварения. Больной продолжает принимать Азатиоприн. Буквально через несколько дней, так как появляются выделения кишечного содержимого по дренажу из малого таза, вновь повторно оперируется. При ревизии выявляется острая язва в отключенной тощей кишке. Выполняется резекция участка тощей кишки (ни много, ни мало, все-таки 30 см) и дальше больной опять продолжает лечение Азатиоприном, которое в принципе неэффективно.
В июле 2013 года у больного проводится контрольное обследование. Выявляется терминальный илеит, опять же наличие изъязвлений. И больному назначается Будесонид с наличием антибиотиков. Причем базисная терапия практически не корректируется.
Лето 2013 года – вновь обострение. Опять появляются боли. При этом обследуется фекальный кальпротектин. Сегодня Олег Самуилович говорил об этом. Посмотрите, какое его повышение. То есть это неспецифический фактор, говорящий о воспалительной реакции. При колоноскопии выявляются язвенные дефекты. И плюс ко всему появляются уже признаки распространения процесса, потому что выявляются язвенные дефекты в толстой кишке. Летом 2013 года мы констатируем неэффективность терапии иммуносупрессорами, назначаем больному биологическую терапию. И после первой инфузии получаем клиническую ремиссию. Сейчас больной находится на продолжающейся биологической терапии. В принципе, об этом можно было задуматься несколько лет назад.
Поэтому мне бы хотелось закончить свое выступление некоторыми международными литературными данными. Сегодня говорилось об ECCO. Так вот, положение ECCO говорит о том, что пациенты, имеющие неблагоприятные прогностические факторы, являются наиболее подходящими кандидатами именно для раннего назначения иммуносупрессии и…
Шелыгин Ю.А.:
– Игорь Львович, но почему-то вы ссылаетесь на ECCO, а не на наши национальные клинические рекомендации, написанные многими из здесь сидящих за столом.
Халиф И.Л.:
Но я продолжу. Посмотрите, что получается. Более высокая частота ремиссии доказана при более раннем назначении биологической терапии. Многочисленные исследования по проведению биологической терапии показывают, что чем раньше она начинается, тем выше процент оказания эффективности.
Каждый доктор, занимающийся проблемами воспалительных заболеваний кишечника, и врач, который сталкивается с этим, должен всегда помнить факторы прогрессирования болезни Крона. Это очень и очень важный момент, потому что у нашего больного, пример которого я приводил сейчас, они были изначально, и возможность о лечении этого больного встала бы гораздо раньше.
А сейчас я хочу завершить свое выступление тем, что действительно благодаря соединению и плодотворной работе Ассоциации гастроэнтерологов, Ассоциации колопроктологов России и обществу при Ассоциации колопроктологов России по изучению воспалительных заболеваний кишечника нами созданы рекомендации, которые опубликованы на сайтах Гастроэнтерологической ассоциации России и на нашем сайте Центра колопроктологии.
Ивашкин В.Т.:
– Вы так стыдливо упоминаете.
Халиф И.Л.:
– Нет, наоборот. Это не стыдливо. На самом деле мы приводим именно свои рекомендации, которые идут в ключе и европейских, и мировых рекомендаций (американских, канадских). Но обобщен наш российский опыт. И я думаю, что если врачи на местах будут следовать этим рекомендациям, то, во-первых, не будет ошибок, а во-вторых, будет понимание в этом направлении.
Благодарю за внимание.
Ивашкин В.Т.:
Халиф И.Л.:
– Мне, по-моему, удалось уложиться.
Ивашкин В.Т.:
– Нет, не удалось. Вы перебрали 10 минут.
Халиф И.Л.:
– Но у нас же была дискуссия.
Ивашкин В.Т.:
Шелыгин Ю.А.:
– Я понимаю так, что это нарушение кишечной проходимости.
Ивашкин В.Т.:
– Понимаете, в чем дело? Кишечная непроходимость либо есть, либо ее нет.
Шелыгин Ю.А.:
– Она либо есть, либо нет. Конечно.
Ивашкин В.Т.:
– Если она есть, она может быть рецидивирующей, персистирующей и т.д. Далее, при определении персистирующей или рецидивирующей кишечной непроходимости все-таки нам очень важно, особенно для терапевтов, понимать, это обструктивная кишечная непроходимость или это паралич кишки.
Шелыгин Ю.А.:
– При болезни Крона, однозначно, только стриктура.
Ивашкин В.Т.:
– Мне кажется, надо очень точно в этом отношении выражаться. Потому что терапевты (я не знаю, как хирурги) очень плохо диагностируют кишечную непроходимость. В терапевтической клинике обструктивной кишечной непроходимости намного меньше, чем случаев паралитической кишечной непроходимости. И во многом это обусловлено тем, что терапевты никогда не слушают живот. Не слушают живот, не перкутируют живот. И это очень часто приводит к большим ошибкам. Длительное время при тяжелых пневмониях, при циррозе печени, у пациентов с паралитической кишкой и у пациентов с тяжелым инфарктом миокарда она встречается.
Мне кажется, что нам, хирургам и терапевтам, нужно собраться и обсудить этот вопрос по кишечной непроходимости, потому что она во многом определяет исход, что делать. Очень часто терапевтическая кишечная непроходимость является результатом избыточного бактериального роста, сочетающегося с диареей и с дефицитом калия. Калий никто не смотрит, никто не связывает дефицит калия с развитием паралича кишки. И это проблема. Мне много приходится консультировать в разных местах, и я знаю, что определение и отношение к кишечной непроходимости в ряде случаев является решающим.
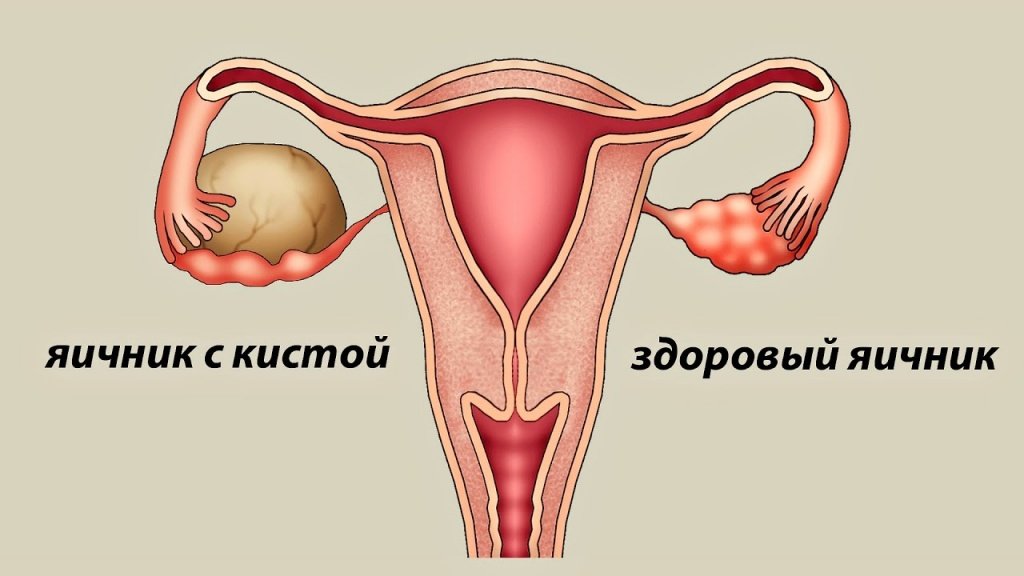
Исходя из причин возникновения, можно выделить два основных вида – функциональные и патологические. А в зависимости от места возникновения новообразования, выделяют следующие подвиды:
- Фолликулярная – киста, которая образуется в результате нарушения нормальной овуляции (у яйцеклетки нет возможности покинуть фолликул, который впоследствии растягивается из-за накопления в нем жидкости);
- Лютеиновая киста (киста желтого тела) – образование ткани яичника на месте нерегрессировавшего желтого тела, в центральной зоне которого, образуется геморрагическая жидкость из-за нарушения кровообращения. Рассасываются самостоятельно через один-три менструальных циклов и не требуют хирургическое лечение при небольших размерах (до 6 сантиметров);
- Параовариальная – киста, которая представляет собой тонкостенное образование в брыжеечной области маточной трубы. Может достигать внушительных размеров (от 12 до 20 см);
- Дермоидная киста - толстостенная капсула, заполненная слизеобразным содержимым (ткани костей и зубов, волосы, хрящи, жировые клетки и прочее). Диаметр достигает до 15 см;
- Эндометриоидная – имеют размер от 5 до 20 см и образуются в результате разрастания яичниковой ткани эндометрия. Как правило, имеют двухсторонний характер поражения.
Очень часто кисты яичника протекают бессимптомно и случайно выявляются при посещении врача, однако выделяют основные клинические проявления:
- Нарушение менструального цикла;
- Болевой синдром;
- Ощущение инородного тела или внутреннего сдавления;
- Метеоризм.
При появлении первых симптомов пациентке требуется немедленная госпитализация независимо от того, какие размеры имеет киста - 3 см или 20. Затягивание с лечением влечет за собой последствие-развитие перитонита, из-за разрыва образования.
Специалисты онкологического центра Юсуповской больницы занимаются диагностикой и лечением различных видов новообразований репродуктивной системы. В распоряжении больницы имеется мощная база для диагностики и современное высокотехнологичное оборудование, а также работают ведущие специалисты. На базе онкологической клиники также может проводиться реабилитация пациентов.
В Юсуповской клинике лечение кисты яичника можно проводить медикаментозно при небольших размерах, однако если их размеры достигают 20 см и оказывают влияние на соседние органы, то применяется хирургическое лечение.
Когда актуально консервативное лечение кисты яичника?
Консервативное лечение приемлемо только при функциональных кистах яичника (фолликулярные или кисты желтого тела). Это так называемые гормональные кисты, которые поддаются лечению благодаря нормализации гормонального фона женщины.
В Юсуповской онкологической клинике при грамотно подобранном медикаментозном лечении, функциональные кисты исчезают уже спустя трех месяцев. На протяжении всего пребывания в клиники, врачи наблюдают за динамикой применяемого лечения.
В лучшей больнице Москвы занимаются консервативным лечением кист яичника, применяя комплексный подход к патологии. Квалифицированные врачи назначают противовоспалительные, противогрибковые, противомикробные и гормональные препараты. Антибиотики при кисте яичника используют с целью уничтожения патогенной микрофлоры, которая может быть основной причиной развития заболевания или фактором, который препятствует быстрому и эффективному лечению. Наряду с инъекциями и таблетками от кисты яичника используют свечи, которые бывают вагинальными и ректальными (вводятся в прямую кишку). Свечи применяют в связи с тем, что одним из факторов возникновения кист является воспалительный процесс в малом тазу. В своем составе они имеют ферменты, которые растворяют спайки, сгустки крови, тромбы и гной. Вводятся ректально, доза и продолжительность курса лечения определяется врачом индивидуально для каждого пациента.
При нарушении гормонального фона (избытке эстрогенов и недостатке прогестерона) применяют гормональные вагинальные свечи. Действующим веществом является прогестерон — вещество, нормализирующее гормональный фон, обеспечивает уменьшение кистозных образований, а также снижает риск осложнений.
Свечи с лактобактериями применяются для восстановления микрофлоры влагалища после лечения воспалений антибиотиками и свечами вагинального применения.
Иммуномодуляторы в виде ректальных свечей применяют в борьбе с нарушениями иммунной системы, которые могут привести к кистозным образованиям.
Какие выбрать свечи?
Ихтиоловые свечи в гинекологии при кисте яичника имеют противовоспалительный и антисептический эффект. Действующим веществом является ихтиол. Это вещество чёрного цвета, имеющее резкий запах. Применяется ректально после естественного очищения кишечника 1-2 раза в день, может применяться и вагинально. Положительный эффект достигается достаточно быстро за счет хорошего всасывания вещества. Ихтиоловые свечи при кисте яичника имеют хорошие отзывы в связи с отсутствием противопоказаний и побочных действий.
Индометацин при кисте яичника снижает болевые ощущения и отечность путем блокирования ферментов, вызывающих воспаления. Относится к нестероидным противовоспалительным средствам. Эффективность препарата достигается в 90%. Принимается вагинально по 1-2 свечи в сутки, быстро всасывается. Не рекомендуется принимать пациентам, имеющим заболевания желудочно-кишечного тракта, печени, аллергиях, беременным женщинам и кормящим матерям. Побочное действие заключается в головокружении, сонливости, боли в животе, тошноте и рвоте.
Дикловит - нестероидное противовоспалительное средство. Применяется как противовоспалительный препарат органов малого таза. Вводят ректально после дефекации или очистительной клизмы по 1-2 свечи в сутки. Нельзя назначать при аллергических реакциях, бронхоспазмах, индивидуальной непереносимости вещества, беременным и кормящим женщинам. Побочные эффекты: мигрень, шум в ушах, аллергическая реакция, в редких случаях — отёк ног. В случае передозировки может наблюдаться спутанность сознания, тошнота, рвота, кровотечение. Препарат следует очень аккуратно применять в сочетании с другими лекарственными средствами.
В гинекологии лонгидаза используется для лечения и профилактики спаек, образующихся на фоне воспалительного процесса. Обладает иммуномодулирующим, антиоксидантным и незначительным противовоспалительным действием. Имеет хорошую всасываемость. Применяется одна свеча через два дня перерыва. Вводится вагинально или ректально, после очищения кишечника. Противопоказан для пациентов с онкологическими заболеваниями, беременных, детей до 12 лет, болезнях почек. Побочные явления проявляются в виде аллергической реакции.
Свечи с прополисом используются как противовоспалительные, антибактериальные, антиоксидантные, иммуномодулирующие средства. Применяются вагинально или ректально, после очищения кишечника.
Эндометриоидная киста яичника
Эндометриоидная киста яичника – это патологическое полостное образование на поверхности яичника, которое состоит из скопившейся менструальной крови, окруженной оболочкой из клеток эндометрия. В отличие от функциональных кист, эндометриоидные кисты имеют совершенно другой механизм развития и, как правило, двухстороннее поражение. В гинекологии такая киста яичника относится к проявлениям генитальной формы эндометриоза.
В Юсуповской клиники широко применяют свечи при эндометриозе кисты яичников, которые оказывают обезболивающий эффект.
Чаще всего используются суппозитории, имеющие нестероидные противовоспалительные средства в своем составе (например, индометацин и диклофенак). При эндометриозе кишечника, который сопровождается спастическими болями, применяют свечи, в состав которых входит папаверин или белладонна.
При спаечном процессе в яичниках, с профилактической и рассасывающей целью, хорошо помогают суппозитории, состоящие из лонгидазы (они вводятся либо ректально, либо вагинально).
Противозачаточные таблетки при кисте яичника
Некорректно подобранный фармацевтический продукт может спровоцировать обратный эффект, когда киста начинает увеличиваться в объеме и появляются внезапные кровянистые выделения. Поэтому так важно правильно подобрать клинику, в которой работают врачи высокого уровня, знающие свое дело.
В Юсуповской онкологической клиники больными занимаются высококвалифицированные врачи, которые ежедневно отслеживают происходящие изменения в организме. Подбор гормональных средств осуществляется индивидуально, учитывая особенности каждого пациента.
Какие таблетки пить?
Вобэнзим – это лекарственное средство, которое обладает противовоспалительным, иммуностимулирующим, фибринолитическим, анальгезирующим и противоотечным эффектом. Вобэнзим используется в комплексном лечении многих гинекологических заболеваний, к которым также относятся и кисты яичника.
Противопоказания к применению:
- Гемофилия или другие состояния, которое могут привести к кровотечению;
- Гемодиализ;
- Дети до 5 лет;
- Индивидуальная непереносимость.
Применение вобэнзима при кисте яичника имеет ряд побочных явлений: тошнота, рвота, расстройство стула, аллергические реакции.
Вобэнзим при кистах яичника имеет положительные отзывы, так как, применяясь в комплексном лечении, способен значительно повысить эффективность антибиотиков и снизить возможные побочные действия гормональных лекарственных средств.
Для того, чтобы получить консультацию или записаться на прием к специалисту Юсуповской больницы, больше узнать о таблетках от кисты яичника и их названиях, можно позвонить по телефону.
Системная красная волчанка (СКВ) – аутоиммунное заболевание, этиология которого остается неизвестной. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-
Systemic lupus erythematosus: alertness in the practice of a dermatologist / M. M. Tlish, Zh. Yu. Naatyzh1, T. G. Kuznetsova, E. A. Chernenko /State Budgetary educational institution of higher professional education Kuban State Medical University of the Ministry of Healthcare of the Russian Federation, Krasnodar, Russia
Abstract. Systemic lupus erythematosus (SLE) is an autoimmune disease, the etiology of which remains unknown. Skin syndrome in SLE is often of paramount diagnostic value – skin lesion is the earliest symptom in 20-30% of cases, and in 60-70% it manifests itself at various stages of the course of the disease, which leads to the patient's primary referral to a dermatologist. Frequent diagnostic errors are due to the absence of clinical symptoms of systemic lesions in the presence of cutaneous manifestations of lupus erythematosus (LE). In this case, laboratory tests are an integral part of the algorithm for managing patients with LE at the stage of contacting a dermatologist. The most specific laboratory test is the determination of antinuclear antibodies by an indirect immunofluorescence reaction, referred to as antinuclear factor (ANF). An elevated ANF titer is included in the list of diagnostic criteria for SLE, its detection allows one to suggest a diagnosis of SLE and determine a further algorithm for the provision of medical care. The article presents two clinical cases illustrating that against the background of an isolated skin lesion and the absence of visible somatic pathology, abnormalities in immunological tests were identified. This made it possible to suspect the systemic course of the process at an early stage and refer patients to a rheumatologist's consultation, where the diagnosis of SLE was confirmed. For citation: Tlish M. M., Naatyzh Zh. Yu., Kuznetsova T. G., Chernenko E. A. Systemic lupus erythematosus: alertness in the practice of a dermatologist // Lechaschy Vrach. 2020; vol. 23 (11): 23-26. DOI: 110.26295/OS.2020.35.78.005
Согласно современным представлениям, системная красная волчанка (СКВ) – аутоиммунное заболевание неустановленной этиологии, характеризующееся гиперпродукцией органонеспецифических аутоантител с развитием иммуновоспалительного повреждения тканей внутренних органов [1]. Широкий ряд вырабатываемых аутоантител и их прямое или опосредованное воздействие на клеточные мишени обуславливают многообразие клинических проявлений при красной волчанке (КВ) [2]. СКВ может проявляться изолированным или сочетанным поражением систем и органов, включающим поражение кожи и слизистых оболочек (волчаночная бабочка, дискоидная эритема, фотосенсибилизация, алопеция, телеангиэктазии, сетчатое ливедо, язвы в полости рта), сердечно-сосудистой системы (перикардит, миокардит, эндокардит, коронарит), почек (волчаночный нефрит), центральной нервной системы (судороги, психоз), опорно-двигательного аппарата (артралгии, артриты), легких (плеврит, волчаночный пневмонит), гематологическими нарушениями (гемолитическая анемия, лейкопения, тромбоцитопения) и т. д. [3].
Ключевую роль в диагностике СКВ играет обнаружение клинических проявлений заболевания и данные лабораторной диагностики [3]. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-70% проявляется на различных этапах течения болезни, что приводит к первичному обращению больного именно к дерматологу [4]. Поражения кожи при СКВ полиморфны и представлены различными изменениями – от незначительных телеангиэктазий до буллезных поражений [2]. Выделяют волчаночно-специфичные и волчаночно-неспецифичные поражения кожи, последние встречаются в несколько раз чаще. К волчаночно-специ-фичным относят различные проявления хронической, подострой и острой КВ [5]. Группа неспецифических поражений включает: фотосенсибилизацию, лейкоцитокластический и уртикарный васкулит, телеангиэктазии, сетчатое ливедо, злокачественный атрофический папулез и синдром Рейно [5]. Широкая вариабельность клинических проявлений кожного синдрома обуславливает необходимость проведения тщательного дифференциального диагноза [1].
Важным инструментом ранней диагностики системных заболеваний является обнаружение аутоантител с помощью лабораторных тестов [3]. Наиболее специ-фичными для СКВ являются антинуклеарные антитела (АНА) – это гетерогенная группа аутоантител к компонентам клеточного ядра, среди которых выделяют антитела к двуспиральной дезоксирибонуклеиновой кислоте (ДНК), гистонам, нуклеосомам, экстрагируемым ядерным антигенам, ядрышковым антигенам и другим клеточным структурам [6]. Стандартным методом обнаружения группы АНА является непрямая реакция иммунофлюоресценции (НРИФ) с использованием линии эпителиальных клеток аденокарциномы гортани человека (HЕp-2) [7]. Определение АНА методом НРИФ принято обозначать как антинуклеарный фактор (АНФ), содержание которого оценивается по максимальному выявленному титру в сыворотке крови, с указанием интенсивности и типа флюоресценции [8]. Количественное увеличение титра свыше 1:160 входит в перечень диагностических критериев СКВ согласно рекомендациям Американской коллегии ревматологов (American College of Rheumatology, ACR) и Европейской лиги борьбы с ревматизмом (European League Against Rheumatism, ULAR) и используется для оценки активности процесса, прогноза, так как является предиктором развития СКВ на доклинической стадии [8].
Длительное формирование патогномоничного клинического симптомокомплекса СКВ, отсутствие проведения необходимых лабораторных исследований и междисциплинарного взаимодействия являются причиной частых диагностических ошибок, приводящих к отсутствию своевременной противовоспалительной и иммуносупрессивной терапии у врача-ревматолога. Учитывая вышесказанное, считаем целесообразным привести собственные клинические наблюдения.
Клиническое наблюдение № 1
Данные со стороны других органов и систем: предъявляет жалобы на ноющие боли в мелких суставах кистей и коленных суставах, чувство утренней скованности. Соматически не обследована.
Объективно: кожный патологический процесс носит ограниченный симметричный характер, локализуется на коже крыльев носа, щек, подбородка. Представлен: эритематозные пятна, чешуйки, телеангиэктазии.
На коже лица (в области крыльев носа, щек, подбородка) расположены ярко-розовые эритематозные очаги, с четкими границами, слегка инфильтрированные, правильной округлой формы, диаметром 3-4 см, покрытые небольшим шелушением в центре очагов; в периферической зоне очагов визуализируются телеангиэктазии (рис. 1). Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского).
.jpg)
Определена биодоза 20 секунд.
Результаты гистоморфологического исследования кожи из патологического очага на правой щеке: фолликулярный гиперкератоз; эпидермис с тенденцией к атрофии; вакуольная дистрофия клеток базального слоя. Под эпидермисом сосуды расширены. Во всех отделах дермы – густые диффузные и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов и плазмоцитов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина может соответствовать красной волчанке.
Данные общеклинических исследований: общий и биохимический анализ крови – показатели в пределах нормы; общий анализ мочи – показатели в пределах нормы.
Настораживающими факторами в плане трансформации кожной формы в системный процесс у пациентки М. явились: дебют заболевания в молодом возрасте, длительная инсоляция в анамнезе, II фототип кожи, биодоза 20 секунд, наличие выраженного суставного синдрома.
Для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 1:320 титр (норма менее 160); мелкогранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 53 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) – 10,13 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 12,68 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
С полученными данными больная направлена к ревматологу в Краевую клиническую больницу № 2, где был подтвержден диагноз СКВ. Больная взята на диспансерный учет ревматологом для определения дальнейшей тактики ведения и лечения.
Клиническое наблюдение № 2
Объективно: кожный патологический процесс носит распространенный характер, локализован на коже лица, шеи. Представлен: пятна, телеангиэктазии, чешуйки.
На коже лица в области щек, левой околоушной области и шеи расположены отечные эритематозные очаги розовато-красного цвета, диаметром 2–3 см, преимущественно правильно-округлой формы с небольшим шелушением, визуализируются единичные телеангиэктазии. Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского) (рис. 2).
.jpg)
Результаты гистоморфологического исследования кожи из патологического очага: на коже левой щеки – фолликулярный гиперкератоз; участки паракератоза; эпидермис местами атрофичен; вакуольная дистрофия клеток базального слоя эпидермиса; подэпидермальные пузыри. В сосочковом слое – отек, стенки сосудов утолщены. В дерме – густые очаговые и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина больше соответствует красной волчанке.
Данные общеклинических исследований: в общем и биохимическом анализах крови выявлены следующие отклонения – лейкоциты 3,7 × 10 9 /л; холестерин 8,7 ммоль/л.
Учитывая длительность течения кожного патологического процесса, отсутствие результатов обследования смежных специалистов, для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 12 560 титр (норма менее 160); крупногранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 0,5 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) 16,65 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 14,68 МЕ/мл (референсные значения до 10 МЕ/мл – не обнаружено).
Таким образом, иммунологические исследования и их комплексный анализ являются неотъемлемой составляющей алгоритма ведения больных с КВ уже на этапе обращения к врачу-дерматологу и способствуют высокому качеству оказания медицинской помощи данному контингенту больных.
Литература/References
М. М. Тлиш, доктор медицинских наук, профессор
Ж. Ю. Наатыж 1 , кандидат медицинских наук
Т. Г. Кузнецова, кандидат медицинских наук
Е. А. Черненко
ФГБОУ ВО КубГМУ Минздрава России, Краснодар, Россия
Системная красная волчанка: настороженность в практике дерматолога/ М. М. Тлиш, Ж. Ю. Наатыж, Т. Г. Кузнецова, Е. А. Черненко
Для цитирования: Тлиш М. М., Наатыж Ж. Ю., Кузнецова Т. Г., Черненко Е. А. Системная красная волчанка: настороженность в практике дерматолога // Лечащий Врач. 2020; т. 23 (11), 23-26. DOI: 110.26295/OS.2020.35.78.005
Теги: аутоиммунное заболевание, кожный синдром, алгоритм лечения
Представлено описание клинического случая пациентки с системной красной волчанкой, трудности в постановке диагноза в связи с атипичным началом и клинической картиной заболевания, даны рекомендации с целью предотвращения поздней диагностики.
Difficulties in diagnostics of systemic lupus erythematosus N. V. Zilberberg, M. M. Kokhan, N. N. Filimonkova, Ya. V. Kascheeva, E. P. Topychkanova, O. G. Rimar, P. S. Gileva
The description of the clinical case of a patient with systemic lupus erythematosus, difficulties in diagnostics due to atypical onset and clinical manifestations were presented, recommendations to prevent late diagnosis are given.
Красная волчанка (КВ) – мультифакториальное аутоиммунное воспалительное заболевание соединительной ткани, характеризующееся гиперпродукцией органонеспецифических аутоантител к различным компонентам клеточного ядра с развитием иммуновоспалительного повреждения тканей и внутренних органов и имеющее широкий спектр клинических проявлений: артрит, серозит, поражение почек и центральной нервной системы (ЦНС), нерубцовая алопеция, язвы слизистых оболочек [1, 2].
В Российской Федерации, как и во всем мире, с середины 1980-х годов наблюдается рост заболеваемости системной красной волчанкой (СКВ) [3, 4]. Распространенность СКВ составляет от 48 до 250 случаев на 100 тыс. населения, а ежегодная первичная заболеваемость — около 50–70 случаев на 1 млн человек в год [5].
Дискоидная красная волчанка (ДКВ) — заболевание кожи из группы коллагенозов, обусловленное повышенной чувствительностью к ультрафиолетовому излучению и характеризующееся последовательным развитием эритематозных высыпаний, фолликулярного гиперкератоза и рубцовой атрофии [3].
Системная и кожная форма КВ имеют ряд общих черт: болеют преимущественно женщины молодого и среднего возраста, отмечается сосудистая эритема, фотосенсибилизация. При кожной форме КВ наблюдается изолированное или преимущественное поражение кожи, для СКВ характерна многосиндромность [7].
В основе терапии больных ДКВ лежит использование системных противомалярийных препаратов и глюкокортикостероидов (ГКС) для наружного применения. Основное место в лечении СКВ занимают ГКC, цитостатики и аминохинолиновые препараты.
Клинический случай
Пациентка Н., 24 лет, поступила в клинику ГБУ СО УрНИИДВиИ в ноябре 2018 г. с жалобами на распространенные высыпания на коже лица, верхних конечностей, ушных раковин, в носовой полости, без субъективных ощущений; ноющие боли в суставах.
Считает себя больной с августа 2018 г., когда впервые появились ноющие боли в плечевых, локтевых суставах, мелких суставах кистей, что связывала с работой официантки. С сентября 2018 г. начала постоянно отмечать усталость, слабость, головную боль, головокружение, субфебрильную температуру тела. Больная расценила данные симптомы как вирусное заболевание и самостоятельно принимала противовирусные препараты, парацетамол, амоксициллин 500 мг 2 раза в день в течение 5 дней, без эффекта.
ОАК от 12.10.2018 г.: СОЭ — 31 мм/ч, лейкопения (2,7 × 10 9 /л). УЗИ органов брюшной полости, почек, щитовидной железы от 12.10.2018 г.: патологии не выявлено. Обследована на ВИЧ, гепатиты В и С (28.10.2018 г.) — результаты отрицательные.
Проведено амбулаторное лечение: дипроспан 1,0 в/м, № 1; глюконат кальция по 2 таблетки (1,0) 3 раза в день, панкреатин 25 тыс. ед. 3 раза в день, Магнерот по 2 таблетки (1,0) 3 раза в день, дезлоратадин 5 мг в сутки. Наружно — Цинковая мазь, мазь Белодерм. Эффекта от лечения не наблюдала.
С ноября 2018 г. отметила появление нового пятна на подушечке большого пальца правой стопы. Постепенно стали нарастать боли в суставах, отметила затруднения при самообслуживании (невозможность носить сумки, открывать бутылки), снижение массы тела на 7 кг при хорошем аппетите в течение последних 6 месяцев.
В связи с отсутствием эффекта от амбулаторного лечения, нарастанием симптоматики, прогрессированием заболевания пациентка направлена в клинику УрНИИДВиИ с целью уточнения диагноза и подбора терапии.
Из анамнеза жизни заслуживает внимания: страдает папилломатозом гортани с 2 лет (лечение хирургическое — 11 операций); дермоидная киста правого уха (оперирована в детстве); курит в течение 3 лет по 4 сигареты в день. Наследственность по кожным заболеваниям отягощена: у двоюродного брата псориаз. В течение 3 лет использовала гормональную контрацепцию: Зоэли (номегэстрол + эстрадиол), последние 2 месяца — пластырь Евра.
Объективно: состояние удовлетворительное, сознание ясное, положение активное, температура тела — 36,8 °С. Периферические лимфоузлы не увеличены. Дыхание везикулярное, хрипов нет, ЧДД — 16 в минуту. Тоны сердца ясные, ритмичные, шумы не выслушиваются. Пульс — 72 удара в минуту, артериальное давление — 110/60 мм рт. ст. Язык обложен белым налетом. Слизистые оболочки губ, щек, дужек миндалин, неба, задней стенки глотки розовые, чистые, гладкие, блестящие. Живот мягкий безболезненный. Симптом поколачивания отрицательный. Почки не пальпируются. Отеков нет. Физиологические отправления в норме.
Status localis. Кожный процесс носит распространенный симметричный полиморфный характер, локализуется на коже лица, верхних и нижних конечностей; представлен пятнами без четких границ застойно красно-розового цвета, 1,0–3,0 см в диаметре; папулами с четкими границами темно-розового цвета, отечными, 2,0–3,5 см в диаметре. На поверхности отдельных элементов визуализируются точечные экскориации в небольшом количестве, покрытые геморрагическими корочками. В области пальцев — пятна застойно-розового цвета, размерами 2,0–3,0 см, местами мишеневидной формы, склонные к слиянию. Дермографизм розовый. Ногтевые пластинки кистей и стоп не изменены (рис. 1, А, Б, В).
.jpg)
Лабораторные данные: ОАК: лейкопения (2,9 × 10 9 /л); незначительный моноцитоз — 9,9%; гемоглобин — 122 г/л; тромбоцитопения (162 × 10 9 /л); повышение СОЭ до 21 мм/ч. Ревмопробы: С-реактивный белок — 3,92 мкг/мл (отрицательный). Иммуноглобулины: повышение IgG до 17,2 г/л. LE-клетки 04.12.2018 г. — не обнаружены. ИФА на ГПИ: обнаружены антитела к описторхам (1:100). Биохимический анализ крови: гиперглобулинемия (40 г/л), понижение креатинина — 58 мкмоль/л, повышение АСТ — 51,1 МЕ/л, повышение СРБ-ультра до 2,26 мг/л, незначительное повышение ЛДГ до 255,2 МЕ/л. Молекулярно-биологическое исследование (ПЦР) на вирус простого герпеса (Herpes simplex virus) — результат отрицательный, ПЦР на вирус Эпштейна–Барр (Epstein–Barr virus) — обнаружено. Микробиологическое исследование материала с кожи лица: Staph. epidermidis умеренный рост. Микробиологическое исследование слизи с миндалин и задней стенки глотки — Candida albicans умеренный рост, чувствительный к флуконазолу.
Пациентке проведена конфокальная лазерная сканирующая микроскопия (КЛСМ) образования на коже лица. В эпидермальном слое (глубина 13,72 мкм) отмечается наличие фолликулярного гиперкератоза (рис. 2, красная звезда), перифолликулярных полей вакуольной дистрофии клеток с единичными воспалительными гиперрефрактильными клетками (рис. 2, голубой круг).
В эпидермально-дермальном соединении (глубина — 74,68 мкм) также визуализируются фолликулярные гиперкератотические пробки (рис. 3, красная звезда), очаги перифолликулярного инфильтрата из воспалительных клеток (рис. 3, красный круг), расположенные перифолликулярно утолщенные коллагеновые волокна (рис. 3, голубой круг).
При поступлении выполнена инцизионная биопсия кожи из очага поражения в области спины. В исследуемом препарате эпидермис тонкий за счет атрофии шиповатого слоя с диффузным и фолликулярным гиперкератозом, умеренным неравномерным акантозом, резкой вакуольной дистрофией клеток, в том числе базального слоя. Пигмент в базальном слое отсутствует. Роговые массы в устьях фолликулов содержат клетки дрожжеподобных грибов.
В сосочковом слое дермы выражен интерстициальный отек с формированием крупной субэпидермальной, унилокулярной полости, содержащей некротизированные эпидермоциты и акантолитические клетки. Эпидермис в области пузыря с серозным пропитыванием и клеточным детритом. Мелкие сосуды расширены, полнокровны. Определяются базофильная дегенерация и фокальный муциноз коллагеновых волокон. Инфильтрат очаговый эпидермо- и фолликулотропный, лимфогистиоцитарный с примесью плазмоцитов и меланофагов (рис. 4, А, Б, В).
_575x.jpg)
Заключение: морфологическая картина соответствует острому интерфейс-дерматиту, возможна при дерматомиозите, СКВ и многоформной экссудативной эритеме.
Консультирована гинекологом: отмена гормональной контрацепции (пластырь Евра), рекомендованы только барьерные методы контрацепции.
На фоне проводимой терапии больная отмечала значительное улучшение общего состояния, уменьшение болезненности и слабости в области суставов, отсутствие головных болей, положительную динамику по кожному процессу (рис. 5, А, Б, В).
.jpg)
Пациентка была направлена на консультацию к ревматологу ГБУЗ СО Свердловская ОКБ № 1. Выполнена рентгенография кистей: костно-суставных изменений не выявлено. Ревматологом выполнены внутрисуставные инъекции препарата дипроспан 1,0 в области проксимальных межфаланговых суставов (ПМФ) с обеих сторон.
Проведенная терапия: преднизолон 20 мг/сут, гидроксихлорохин 200 мг 2 раза/сут, диклофенак 50 мг/сут, омепразол 20 мг/сут. На фоне проводимой терапии достигнута стойкая положительная динамика по кожному процессу — высыпания регрессировали полностью, оставив гиперпигментированные пятна, суставные боли отсутствуют, слабости, температуры, головных болей нет. Выписана с рекомендациями продолжить прием метилпреднизолона по 16 мг/сут в течение 1 месяца, гидроксихлорохина — 200 мг 2 раза в день, далее снижение дозы метилпреднизолона по 1/2 таблетки в 2 недели, далее по 1/4 раз в 2 недели до 6 мг (поддерживающая доза).
На фоне лечения: антитела к двухцепочечной ДНК снизились до 7,6 МЕ/мл (норма до 10). Положительная динамика сохраняется и в настоящее время: суставные боли отсутствуют, слабости, головных болей нет, увеличение массы тела на 2 кг, кожный процесс стабилен — свежих высыпаний нет, сохраняются гиперпигментированные пятна. Пациентка удовлетворена результатами лечения (рис. 6, А, Б, В).
.jpg)
При постановке диагноза ДКВ в первую очередь следует исключить признаки системного заболевания, от чего зависят тактика лечения и прогноз для жизни больного. При СКВ, в отличие от ДКВ, фолликулярный кератоз отсутствует, а атрофия выражена незначительно. Для СКВ клинически характерны артралгия, полисерозиты, эндокардит с поражением митрального клапана, поражения центральной нервной системы, почек, тяжелые васкулиты [8]. LE-клетки при СКВ в острой фазе заболевания обнаруживаются у 90–100%, при ДКВ — в 3–7%, что расценивается как неблагоприятный фактор. Антинуклеарные антитела при СКВ встречаются более чем у 95% больных, при ДКВ — у 30–40% больных. Аутоиммунная гемолитическая анемия, лейкопения и лимфопения с ускоренной СОЭ в крови, белок и цилиндры в моче — косвенные признаки системного заболевания [4].
Поражение кожи при КВ характеризуется значительной гетерогенностью клинических проявлений. В масштабном многоцентровом исследовании, проведенном C. Biazar и соавт. (2013 г.), две и более клинические формы кожной КВ наблюдались у 34,6% больных, острая кожная КВ была ассоциирована с дискоидной КВ у 30,3%, с подострой кожной КВ — у 13,8%, с дискоидной и подострой кожной КВ — у 15,3% пациентов [3].
Острая кожная форма КВ всегда служит проявлением СКВ, которая манифестирует с поражения кожи в 70—85% случаев. Острая форма КВ характеризуется развитием на коже лица в области скул и носа эритемы с цианотичным оттенком в центре и отеком. Реже встречаются распространенные пятнисто-папулезные высыпания [3, 9].
Подострая кожная КВ проявляется развитием папуло-сквамозных или кольцевидных эритематозных высыпаний. При псориазиформной КВ элементы представлены гиперемическими папулами и небольшими бляшками в области плеч, верхней части груди и спины, редко — на коже лица, ушных раковин, волосистой части головы, которые могут сливаться между собой. На поверхности пятен и бляшек имеются плотно сидящие чешуйки и незначительный гиперкератоз, усиливающийся в области устьев волосяных фолликулов. Высыпания при подострой кожной КВ могут разрешаться без рубцов, образуя длительно существующие очаги гипопигментации (гиперпигментации) с телеангиэктазиями на поверхности, или формировать поверхностную рубцовую атрофию. У данной категории больных часто имеются относительно нетяжелые системные проявления КВ: артралгии, артриты без вовлечения почек, ЦНС и серозных оболочек [1].
У большинства пациентов с подострой кожной формой КВ выявляются ANA (60-80%). При проведении дифференциальной диагностики важно учитывать, что для СКВ характерно наличие антител к экстрагируемому ядерному антигену Sm (Smith) — анти-Sm и положительные тесты на анти-dsDNA (антитела к двухцепочечной ДНК) [3].
Следует отметить, что не у всех пациентов будут положительными все иммунологические показатели, характерные при СКВ.
Неврологические симптомы возникают у 25–80% пациентов при СКВ. Нарушения когнитивных функций представлены снижением памяти, внимания, эмоционально-личностными расстройствами. В клинической картине неврологических проявлений встречаются головные боли, чаще мигренозного характера [3].
Заключение
В последние годы участились случаи стертых, молниеносных, атипичных форм диффузных заболеваний соединительной ткани, в частности СКВ. Разнообразие клинической картины, малые кожные проявления в сочетании с яркой, выступающей на первый план патологией внутренних органов приводят к поздней верификации данной нозологической единицы [4, 10].
Дифференциальный диагноз СКВ и кожной формы КВ на сегодняшний день представляется достаточно сложным и трудоемким процессом.
Диагноз СКВ должен устанавливаться на основании клинико-лабораторных данных и в соответствии с классификационными критериями: критерии диагноза Американской коллегии ревматологов (American College of Rheumatology — ACR, 1997 г.) — наличие 4 и более из 11 критериев (чувствительность 90%, специфичность 80%) и критерии диагноза Клиники международного сотрудничества по системной красной волчанке (The Systemic Lupus International Collaborating Clinics — SLISS, 2012 г.) — 4 критерия, один из которых должен быть клинический и один — иммунологический (любой из следующих лабораторных показателей: а-ДНК, АНФ, Sm, aКЛ, C3, C4) (чувствительность 95%, специфичность 74%) [6, 10].
Данное клиническое наблюдение приведено с целью привлечения внимания врачей к проблеме ранней диагностики СКВ и своевременного начала лечения до развития фатальных событий, особенно учитывая, что больными чаще являются женщины репродуктивного возраста. Ошибки диагностики связаны с отсутствием настороженности врачей в отношении СКВ. В связи с этим следует обращать внимание на такие клинические особенности, как начало заболевания в молодом возрасте, суставные боли, наличие высыпаний на коже, язв в ротовой полости, нарушение общего состояния, фотосенсибилизация, гематологические нарушения, предшествующий прием препаратов, способных исказить истинную картину заболевания, и необходимость иммунологических исследований в ранние сроки.
Литература
Н. В. Зильберберг, доктор медицинских наук, профессор
М. М. Кохан, доктор медицинских наук, профессор
Н. Н. Филимонкова, доктор медицинских наук, профессор
Я. В. Кащеева 1 , кандидат медицинских наук
Е. П. Топычканова, кандидат медицинских наук
О. Г. Римар
П. С. Гилёва
ГБУ СО УрНИИДВиИ, Екатеринбург
Сложности в диагностике системной красной волчанки. Клиническое наблюдение/ Н. В. Зильберберг, М. М. Кохан, Н. Н. Филимонкова, Я. В. Кащеева, Е. П. Топычканова, О. Г. Римар, П. С. Гилёва
Для цитирования: Лечащий врач № 5/2020; Номера страниц в выпуске: 36-41
Теги: кожа, иммуновоспалительное повреждение, коллагеноз, высыпания
Читайте также:

