На фоне спида токсоплазмоз протекает в форме
Обновлено: 13.05.2024
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
ГКУЗ ИКБ №2, Москва
Локализация очагов при токсоплазмозе головного мозга у больных ВИЧ-инфекцией
Журнал: Терапевтический архив. 2014;86(11): 24‑28
Ермак Т.Н., Перегудова А.Б. Локализация очагов при токсоплазмозе головного мозга у больных ВИЧ-инфекцией. Терапевтический архив. 2014;86(11):24‑28.
Ermak TN, Peregudova AB. Location of foci in cerebral toxoplasmosis in HIV-infected patients. Terapevticheskii Arkhiv. 2014;86(11):24‑28. (In Russ.).
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
ГКУЗ ИКБ №2, Москва
Токсоплазмоз головного мозга (ТГМ; церебральный токсоплазмоз) - основная причина поражения центральной нервной системы (ЦНС) у больных инфекцией, вызванной вирусом иммунодефицита человека (ВИЧ). ТГМ отличается высоким уровнем летальных исходов, что обычно связано с трудностями клинической диагностики. В последние годы растет число поздно выявленных больных ВИЧ-инфекцией, которые, не зная о своем заражении ВИЧ, доживают до развития тяжелых вторичных/оппортунистических поражений. Такие больные попадают в различные стационары, где они могут находиться достаточно долго без адекватного лечения, и только после установления ВИЧ-статуса их переводят в специализированные отделения. Как правило, предположить то или иное вторичное заболевание, не зная особенностей его течения при ВИЧ-инфекции, бывает трудно. Это относится к большинству вторичных поражений, в частности, к ТГМ, который является основной причиной поражения ЦНС у больных на поздних стадиях ВИЧ-инфекции. В настоящее время достаточно четко установлены критерии лабораторного подтверждения этого диагноза у больных ВИЧ-инфекцией, которые включают обнаружение высоких титров IgG к Toxoplasma gondii в сыворотке крови, ДНК токсоплазмы в цереброспинальной жидкости (ЦСЖ). Большое значение для диагностики этого процесса имеет также обнаружение очагов поражения в ЦНС при проведении магнитно-резонансной томографии (МРТ).
Материалы и методы
Результаты и обсуждение
Клиницистам важно знать, что такой важный признак поражения ЦНС, как головная боль, имелся только у 55% больных, подъем температуры тела до высоких цифр (выше 38 °С) также регистрировали только 50% пациентов. У 93% больных отмечены низкие параметры иммунитета - число лимфоцитов CD4 у 66,2% менее 50 в 1 мкл, еще у 26,8% больных - от 50 до 200 в 1 мкл. В то же время у 14 (7%) больных число лимфоцитов CD4 превышало 200 в 1 мкл, а у 1 из них составило 720 в 1 мкл. Причина развития ТГМ у больного ВИЧ-инфекцией с нормальным количеством лимфоцитов CD4, возможно, связана с функциональной недостаточностью Т-лимфоцитов-хелперов. Известны случаи развития ТГМ и у лиц без ВИЧ-инфекции, с нормальными показателями иммунитета [3]. Следует отметить, что у 9,2% больных ТГМ протекал в виде генерализованного процесса, сочетаясь с поражением других органов (чаще сердца, печени, глаз, легких), а у 54% больных имелись и другие вторичные инфекции (ЦМВ-инфекция, кандидоз пищевода, пневмоцистная пневмония, туберкулез легких и генерализованный, бактериальная пневмония и пр.).
При проведении МРТ головного мозга у 113 (98,3%) больных при госпитализации выявлены патологические изменения. Чаще всего на томограммах выявляли полиморфные очаги повышенного МР-сигнала в режимах Т2-взвешанного и FLAR и пониженного в режиме Т1 с поражением преимущественно белого или на границе белого и серого вещества головного мозга. Вокруг очагов часто регистрировали образование перифокального отека. При использовании внутривенного контрастирования препаратами гадолиния эти очаги накапливали контрастное вещество по периферии по типу мишеней. Следует отметить, что формирование очагового поражения ЦНС является самым характерным признаком токсоплазмозного поражения, хотя у некоторых больных выявляют не очаговый, а диффузный энцефалит; считается, что у таких пациентов болезнь быстро прогрессирует до летального исхода [4]. Мы наблюдали диффузное поражение вещества головного мозга у 3 (2,7%) больных; действительно, один из них умер на ранних сроках госпитализации, но два других после успешного лечения выписаны. У 86 (76,1%) больных выявлены множественные очаги (3 и более) поражения.
Приводим клинический пример.
У 24 (21,2%) больных выявлены единичные (1-2) очаги повышенного сигнала (рис. 3). Рисунок 3. МРТ головного мозга больного ВИЧ-инфекцией и ТГМ. Очаг в левой височно-теменной области с выраженным перифокальным отеком и сдавлением левого желудочка.
У 2 (1,7%) пациентов на МРТ головного мозга при первом исследовании патологических изменений не выявлено. Впоследствии один из них умер, и ТГМ установлен при аутопсии, а у второго пациента при повторном исследовании на фоне этиотропного лечения обнаружены кисты в веществе головного мозга (выявлены специфические IgG в сыворотке крови и ЦМЖ, а также ДНК к токсоплазме в ЦМЖ).
Очаги поражения наиболее часто располагались в обоих полушариях - у 71,7% больных. Одностороннее поражение имелось у 28,3% больных. Контуры очагов были четкими (40,7%) или нечеткими (59,3%). Отек вокруг очагов наблюдался у 69% больных.
Наиболее часто очаги локализовались в лобных и теменных долях (70,8 и 61,1% соответственно). В таблице представлена локализация очагов на картине МРТ при госпитализации пациентов. У 44,2% больных кроме белого вещества были поражены и подкорковые ядра. Мозолистое тело страдало редко, очаги выявлены в нем лишь у 8 (7,1%) больных. Перивентрикулярно очаги располагались почти у ¼ больных.
Единичные очаги чаще располагались в лобных (у 6 больных), теменных (у 5), затылочных (у 6) долях и таламусе (у 5).
При попытке обнаружения связи между количеством очагов на МРТ и давностью процесса статистически значимой зависимости этих переменных друг от друга мы не получили.
При остром начале болезни очаги поражения располагались в одном из полушарий в 45% случаев, тогда как при постепенном начале - только в 24,7%. Таким образом, поражение обоих полушарий чаще наблюдалось при постепенном начале (75,3%), а при остром - в 55%. Кроме того, при остром начале болезни в 30% случаев определяли единичный очаг поражения, тогда как при постепенном начале единичные очаги встречались у 19% больных. Но эти различия также оказались статистически незначимыми.
Одинаково часто при остром и постепенном начале поражаются лобная, теменная, затылочная доли, мост, мозолистое тело и ножки мозга.
Несколько реже при остром начале болезни были поражены таламус (25 и 34,4%), височные доли (30 и 41,9%) и мозжечок (15 и 23,7%). При остром начале болезни значительно реже поражались ядра (30%) и перивентрикулярные зоны (10%) в отличие от таковых при постепенном начале - 47,3 и 28% соответственно. Однако отек вокруг очагов чаще имелся при остром начале заболевания (80%), чем при постепенном (66,7%). Это обусловило более тяжелое течение болезни и большую частоту летальных исходов - 47,7% при остром начале болезни в отличие от 30,1% при постепенном.
На фоне лечения (через 4-6 нед) МРТ головного мозга проведена 74 больным. У 64 (86,5%) больных наблюдали значительную положительную динамику: уменьшение количества и размеров очагов, зоны отека вокруг них, а у 29 больных очаги воспаления преобразовывались в кисты как благоприятный исход некротического энцефалита. Полное рассасывание очагов произошло только у 7% пациентов. У 4% больных улучшения при проведении контрольного исследования не выявлено. У 1 из них в течение 1-го месяца после выписки развился ранний рецидив, и пациент умер. У 2 других больных клинически отмечена положительная динамика в виде уменьшения неврологической симптоматики. У 2 пациентов на контрольной МРТ отмечена отрицательная динамика. Одному из них проведено нейрохирургическое вмешательство в связи с подозрением на опухоль мозга, и впоследствии пациент умер в отсутствие этиотропного лечения; второй пациент также умер, несмотря на лечение.
Картина МРТ у ряда больных, которые были обследованы еще через несколько месяцев после выписки, отражала глиозные и рубцово-атрофические изменения в веществе головного мозга, что свидетельствует о положительной динамике на фоне лечения.
Заключение
В статье представлен обзор литературных данных развития токсоплазмоза на фоне ВИЧ-инфекции. Актуальность проблемы токсоплазмоза у больных ВИЧ-инфекцией определяется высокой инфицированностью паразитом Toxoplasma gondii. Проведен анализ распространенности токсоплазмоза среди ВИЧ-инфицированных больных. Токсоплазмоз занимает одно из ведущих мест среди оппортунистических инфекций у больных ВИЧ-инфекцией. Токсоплазмоз развивается на поздних стадиях ВИЧ-инфекции. При токсоплазмозе у ВИЧ-инфицированных больных преобладает поражение одного какого-нибудь органа (энцефалит, миокардит, хориоретинит), в некоторых случаях в процесс вовлекаются многие органы и системы организма. В статье рассматриваются клинические проявления токсоплазмоза при разных органных поражениях. Указаны лабораторно-диагностические подходы обследования токсоплазмоза у больных ВИЧ-инфекцией.

1. ВИЧ/СПИД сегодня и рядом. Пособие для людей, принимающих решения / Под ред. Н.А. Белякова, А.Г. Рахмановой. – Спб: Балтийский медицинский образовательный центр, 2013. – 110 с.
2. ВИЧ-инфекция и СПИД: национальное руководство / Под ред. В.В. Покровского. – М.: ГЭОТАР-Медиа, 2013. – 608 с.
3. Дифференциальная диагностика инфекционных болезней: Руководство для врачей / Зубик Т.М., Иванов К.С., Казанцев А.П., Лесников А.Л. – Л.: Медицина, 1991. – 336 с.
4. Инфекционные болезни: национальное руководство / Под ред. Н.Д. Ющука, Ю.Я. Венгерова. – M.: GEOTAR-Media, 2009. – 1056 c.
6. Перегудова А.Б., Шахгильдян В.И., Гончаров Д.Б. и др. Церебральный токсоплазмоз у больных ВИЧ-инфекцией // Терапевтический архив. – 2007. – № 11. – С. 36–39.
7. Шувалова Е.П. Инфекционные болезни: Учебник. – 3-е изд., перераб. и доп. – М.: Медицина, 1990. – 560 с.
8. Couvreur J., Thulliez P. Toxoplasmose acquise a localization osulairu on neurologique: 49 cas // Presse. Med. – 1996. – V. 25, № 9. – P. 438–442.
9. Eye manifestations of congenital toxoplasmosis / Mets M.B, Holfels E., Boyer K.M. et al. // Am. J. Ophthalmol. – 1996. – Vol. 122, № 3. – P. 309–324.
10. Michalova K., Rihova E., Havlicova V. Neurotoxoplasmosis // Cesk Slov. Oftalmol. – 1996. – V. 52, № 3. – P. 173–178.
Токсоплазмоз является одной из частых причин гибели больных ВИЧ-инфекцией. Токсоплазмоз – заболевание, вызываемое Toxoplasma gondii, чаще всего возникающее у ВИЧ-инфицированных пациентов на фоне СПИДа. К факторам риска развития токсоплазмоза у больных ВИЧ-инфекцией относится количество CD4-лимфоцитов менее 100 клеток/мкл. Хотя токсоплазмы могут поражать все органы и ткани, но, как правило, у ВИЧ-инфицированных пациентов регистрируют церебральную форму заболевания. Церебральный токсоплазмоз в странах Европы и Северной Америки регистрируют все реже – с внедрением АРВТ в Европе заболеваемость им сократилась в 4 раза, однако он по-прежнему остается самым важным оппортунистическим поражением ЦНС у больных с ВИЧ-инфекцией. Распространенность токсоплазмоза в Центральной Европе достигает 90 %, что связано прежде всего с традицией жителей некоторых стран (Франция, Германия) употреблять в пищу сырые и полусырые мясные блюда [1, 2, 4].
Токсоплазмоз характеризуется выраженным полиморфизмом клинических проявлений при отсутствии патогномоничных симптомов. Это объясняется тем, что у токсоплазм нет какой-либо тканевой специфичности, а также наличием в патогенезе заболевания стадии гематогенной диссеминации возбудителя. Основная роль в развитии токсоплазмоза у лиц с иммуносупрессией отводится нарушениям продукции цитокинов. Показано, что при развитии токсоплазмоза на фоне ВИЧ-инфекции резко снижается как концентрация сывороточного гамма-интерферона, так и его способность активировать макрофаги. Нормальная реакция организма на инфекцию T. gondii опосредуется в основном клеточной иммунной системой. Дефект клеточной иммунной системы у больных с ВИЧ-инфекцией приводит к снижению сопротивления по отношению к внутриклеточным токсоплазмам, в результате происходит реактивация латентной инфекции и генерализация процесса: тахизоиты поступают в кровь, а затем разносятся во внутренние органы и ткани [2, 5].
Внемозговые локализации токсоплазмоза (например, хориоретинит, интерстициальная пневмония, миокардит и поражение органов пищеварительной системы) у больных СПИДом регистрируют в 1,5–2 % случаев. Диссеминация (по меньшей мере две локализации) происходит в 11,5 % случаев [4].
Максимальное количество очагов внемозговых локализаций обнаруживают при исследовании зрительного аппарата глаза (примерно в 50 % случаев). При токсоплазмозе поражения глаз встречаются в виде переднего и заднего увеита, экссудативного и пролиферативного ретинита, диссеминированного хориоретинита. Наиболее часто наблюдается центральный хориоретинит, который начинается с клинической картины острого серозного ретинита. На заднем полюсе обнаруживаются различной величины ограниченные очаги. В сетчатке или под ней видны кровоизлияния. Поражения глаз в виде хориоретинита, увеита наиболее часты, но атрофия зрительного нерва может быть иногда единственным клиническим проявлением токсоплазмоза. Диагностика токсоплазмозного поражения органа зрения должна быть основана на тщательном изучении анамнеза, офтальмологического статуса и серологических реакций. Выявление этих хориоретинитов и увеитов возможно лишь при консультации офтальмолога, и при обычном клиническом обследовании врачом-инфекционистом они нередко остаются нераспознанными [3–5, 9].
При токсоплазмозе весьма часто отмечаются также изменения со стороны органов дыхания, в частности очаговая пневмония, хронический бронхит, плеврит токсоплазмозной этиологии. Наиболее частой формой поражения легких являются интерстициальные пневмонии [5].
Со стороны сердечно-сосудистой системы, помимо расширения границ сердца, глухости тонов, гипотонии и тахикардии, отмечается экстрасистолия. При токсоплазмозе имеются существенные электрокардиографические сдвиги, выражающиеся в уменьшении вольтажа зубцов, различных нарушениях ритма (экстрасистолия, неполная предсердно-желудочковая блокада, блокада ножек пучка Гиса, синусовая тахикардия и брадикардия), увеличение систолического показателя, изменения зубца T и комплекса QRS и др. Эти изменения говорят о выраженных нарушениях миокарда преимущественно диффузного характера. При ЭКГ почти у всех больных выявляются очаговые или диффузные изменения миокарда. Перикард и эндокард не поражаются [2, 5].
Со стороны органов пищеварения отмечаются снижение аппетита, больные жалуются на сухость во рту, тошноту, тупые боли в подложечной области, вздутие живота, задержку стула, нередко наблюдается похудание. При исследовании желудочного сока выявляются снижение секреции и уменьшение кислотности [7].
Токсоплазмоз ЦНС занимает 2–3 место среди оппортунистических инфекций у больных СПИДом. Попадание токсоплазм в организм человека приводит к формированию объемных образований в ЦНС (в 50–60 % случаев) и развитию первичных эпилептических припадков (в 28 % случаев). Симптомы токсоплазмоза развиваются приблизительно у 18–20 % больных на поздних стадиях ВИЧ-инфекции. Появление симптомов токсоплазмозного энцефалита отмечается у 6–12 % больных в стадии СПИДа. Если у таких больных развивается энцефалит, то на долю токсоплазмоза приходится от 25 до 80 % всех случаев. При этом отмечают лихорадку, головные боли, возникновение в 90 % случаев разнообразной очаговой неврологической симптоматики (гемипарез, афазия, психические и некоторые другие нарушения). Иногда токсоплазмоз протекает без формирования объемных образований в головном мозге (по типу герпетического энцефалита или менингоэнцефалита). Токсоплазмозный энцефалит нередко сочетается с хориоретинитом [2, 4, 6].
Диагностировать токсоплазмоз крайне сложно. Диагноз ставят на основании клинической картины, данных магнитно-резонансной томографии или компьютерной томографии, а также при наличии антител к токсоплазме в сыворотке крови. Вместе с тем обнаружение положительных серологических реакций без учета динамики титра антител и клинической симптоматики не всегда дает возможность говорить о болезни из-за широкого распространения носительства. Полагают, что развитие токсоплазмоза – реактивация латентной инфекции, поскольку при наличии в сыворотке крови антител к токсоплазме вероятность возникновения токсоплазмоза увеличивается в 10 раз. Однако примерно у 5 % ВИЧ-инфицированных пациентов на момент постановки диагноза токсоплазмоза антитела к T. gondii отсутствуют. В форме цист токсоплазмы сохраняются до 10–15 лет, преимущественно в тканях головного мозга и органах зрения, а также во внутренних органах [2, 4, 8].
В большинстве случаев развитие токсоплазмозного энцефалита не сопровождается появлением противотоксоплазменных антител в сыворотке крови. Некоторое диагностическое значение имеет появление антител в ликворе при отсутствии их в сыворотке. Ликвор при спинномозговой пункции может быть интактным. В цереброспинальной жидкости отмечается плеоцитоз, повышенное содержание белка и нормальное содержание глюкозы. После ее центрифугирования в мазке можно обнаружить трофозоиты токсоплазм [2, 4, 10].
При выполнении МРТ или КТ с контрастированием обнаруживают множественные очаги с кольцевидным усилением и перифокальным отеком, реже – единичный очаг. Биопсию головного мозга выполняют при невозможности правильно установить диагноз, в биоптатах мозга выявляются трофозоиты токсоплазм. В диагностике церебрального токсоплазмоза используется ПЦР для определения ДНК T. gondii в спинномозговой жидкости [2, 4, 6].
Диагностическое значение имеет пробное назначение пириметамина в сочетании с сульфаниламидным препаратом. Если в течение 7–10 дней наступает заметное улучшение, то это говорит о токсоплазмозной природе энцефалита у больного СПИДом [8].
Таким образом, при комплексном применении нескольких лабораторных методов повышается надежность диагностики токсоплазмоза у ВИЧ-инфицированных больных.
Заключение
Токсоплазмоз у ВИЧ-инфицированных больных характеризуется множественными органными поражениями: нервной системы, органов зрения, миокарда и т.д. Среди них ведущее место отводится церебральному токсоплазмозу. Церебральный токсоплазмоз диагностируют на стадии СПИДа, при этом чаще отмечается снижение CD4-лимфоцитов менее 100 в 1 мкл. Оппортунистические инфекции при ВИЧ/СПИД требуют применения широкого спектра диагностических методов, а именно иммунологических, серологических, инструментальных (МРТ, КТ). С учетом многообразия клинических проявлений токсоплазмоза у ВИЧ-инфицированных больных по показаниям необходимы консультации нескольких специалистов, в частности инфекциониста, невропатолога, офтальмолога и др.
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
Этиология
Таксономия:
Вид — Toxoplasma gondii
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
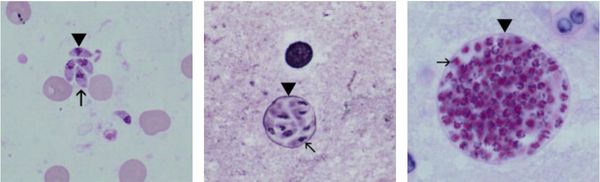
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
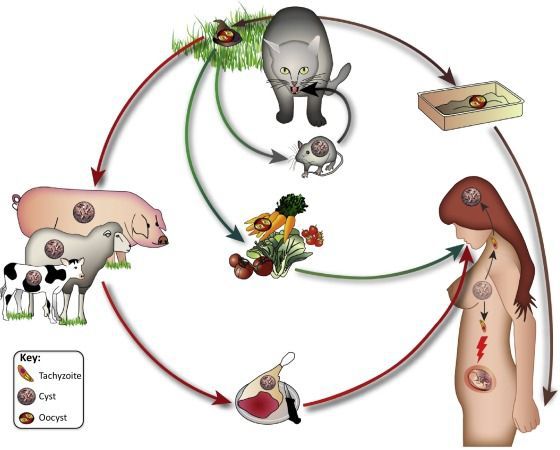
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
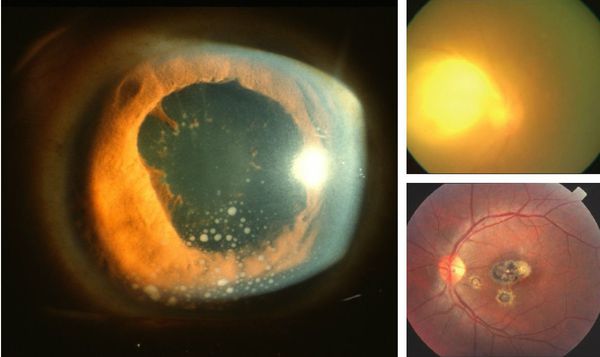
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
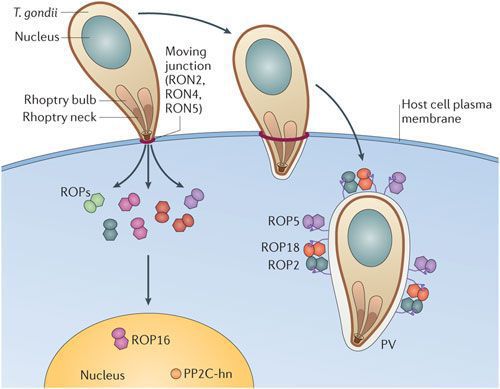
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым - 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода "двойной сэндвич" или "иммунозахват" IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
-
(ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови; — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
ГКУЗ ИКБ №2, Москва
Катамнез больных ВИЧ-инфекцией, перенесших церебральный токсоплазмоз
Журнал: Терапевтический архив. 2015;87(11): 42‑45
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
ГКУЗ ИКБ №2, Москва
Церебральный токсоплазмоз (ЦТ) — основная причина поражения центральной нервной системы у больных c инфекцией, вызванной вирусом иммунодефицита человека (ВИЧ). Для него свойственны высокая смертность, а также частое развитие рецидивов у выживших больных, что чаще связано с низкой мотивацией к лечению.
Материалы и методы
Результаты и обсуждение

Рис. 1. Исходы Ц.Т. у больных ВИЧ-инфекцией.
Больным с рецидивами этиотропное лечение начинали сразу после поступления, кроме одного больного, так как при госпитализации в клинической картине преобладали признаки выраженной анемии, и рецидив болезни не предполагался. Смерть больного наступила на 3-й день пребывания в стационаре, а патоморфологические проявления болезни оказались находкой патологоанатомов. Этот 30-летний пациент госпитализирован через 1,5 мес после перенесенного ЦТ с жалобами на слабость, повторные приступы потери сознания. Обращала внимание резкая бледность кожи, количество гемоглобина в крови составляло 20 г/л. Больной получал антиретровирусную терапию — АРВТ (эфавиренз в сочетании с комбинированным препаратом зидовудин + ламивудин), валганцикловир со времени первой госпитализации по поводу ЦТ и активной ЦМВ-инфекции, однако режим вторичной профилактики ЦТ не соблюдал. В отделении начато лечение анемии. Через 2 дня развился судорожный припадок с потерей сознания, нарушением деятельности сердечно-сосудистой системы и дыхания. Интенсивная терапия эффекта не дала, смерть наступила на 3-й день. Диагноз при вскрытии: токсоплазмоз головного мозга и сердца — множественные очаги некротического энцефалита и паренхиматозно-межуточного миокардита с поражением проводящей системы.
Из остальных 60 реконвалесцентов после выписки умерли еще 11. Из них 3 не закончили лечебный курс ЦТ, выписавшись из стационара по настоятельной просьбе и самостоятельно прервав лечение, — они умерли в результате прогрессирования ЦТ (по данным аутопсии). У 3 больных причиной смерти послужили прогрессирование ВИЧ-инфекции и развитие других вторичных заболеваний (генерализованный туберкулез, атипичный микобактериоз) через 0,5—3 года после выписки. У 5 больных смерть наступила через 1—5 лет после выписки, при этом причины смерти не связаны с ВИЧ-инфекцией (передозировка наркотиков, стафилококковый сепсис, острый панкреонекроз).

Рис. 2. Выживаемость больных ВИЧ-инфекцией после перенесенного ЦТ (кривая Каплана—Майера).
Заключение
Перенесшим ЦТ больным при диспансерном наблюдении нужно уделять более пристальное внимание в плане возможного развития рецидивов, особенно в течение первых 3 лет после выписки независимо от количества клеток CD4 + .
Токсоплазмоз — широко распространенная зоонозная паразитарная инфекция, характеризующаяся полиморфизмом клинических проявлений и значительной вариабельностью течения процесса: от здорового, бессимптомного носительства до тяжелых, летальных форм болезни.
.jpg)
Токсоплазмоз — широко распространенная зоонозная паразитарная инфекция, характеризующаяся полиморфизмом клинических проявлений и значительной вариабельностью течения процесса: от здорового, бессимптомного носительства до тяжелых, летальных форм болезни.
Этиология. Возбудитель токсоплазмоза Toxoplasma gondii относится к царству Protozoa, классу Coccidia, отряду Eucoccidiorida, типу Apicomplexa. T. gondii — условно патогенный внутриклеточный паразит, поражающий в организме промежуточных хозяев, в том числе человека, любые ядерные клетки гистеофагоцитарной системы.
Эпидемиология. Пораженность или инфицированность токсоплазмами населения Российской Федерации в среднем составляет около 20,0%. Показатели пораженности выше в регионах с теплым климатом; среди лиц ряда профессиональных групп: рабочие мясокомбинатов и звероводческих ферм, животноводы, ветеринарные работники и др. Инфицированность женщин, как правило, в 2–3 раза выше, чем у мужчин.
Заболеваемость токсоплазмозом во много раз ниже показателей инфицированности, однако трудности диагностики, несмотря на обязательную регистрацию, не позволяют судить об истинном уровне инфекции.
Восприимчивость к токсоплазмозу — практически поголовная. Распространение инфекции — повсеместное в виде носительства и спорадических заболеваний. Основной источник инфекции — дикие и домашние кошки.
Основной фактор передачи токсоплазм — сырое или недостаточно термически обработанное мясо, мясные продукты с находящимися в нем цистами токсоплазм. К дополнительным факторам передачи инфекции относятся плохо вымытая зелень, овощи, фрукты (с земли), грязные руки с находящимися на них ооцистами возбудителя.
Основные пути передачи:
- пищевой — связанный с употреблением в пищу термически плохо обработанного мяса, содержащего цисты паразита;
- контактный — ассоциированный с больными кошками, выделяющими токсоплазмы с фекалиями;
- трансплацентарный — при котором становится возможным проникновение токсоплазм в плод, с последующим развитием врожденного токсоплазмоза у новорожденного;
- парентеральный — при котором не исключается передача инфекции реципиенту при переливании крови, пересадке органов и тканей.
Беременная с токсоплазмозом не представляет эпидемиологической опасности ни для окружающих, ни для медицинского персонала, что делает возможным лечение этих пациентов как в амбулаторных условиях, так и в любом соматическом стационаре.
Патогенез. Вышедшие из цист или ооцист возбудители внедряются в эпителиальные клетки тонкого кишечника, где они размножаются, образую первичный аффект и проникая затем в региональные лимфатические узлы, а из них с током лимфы — в кровь. Диссеминация возбудителя приводит к поражению самых различных органов и тканей.
При беременности, в условиях сниженного иммунитета, наряду с первичным заражением токсоплазмами, опасным является и реактивация паразита (при инфицировании до беременности), что в значительной степени определяет течение и исход беременности.
При выходе токсоплазм из цист происходит диссеминация возбудителей. Их концентрация в тканях ассоциирована со способностью токсоплазм проникать трансплацентарно, что приводит к развитию внутриутробной патологии на любом сроке беременности.
Заражение плода наблюдается у беременных как с первичным инфицированием токсоплазмами, так и реактивацией возбудителя во время беременности у серопозитивных женщин. Поражение плода может возникать на любом сроке гестации, но особую опасность представляет его инфицирование в первом и втором триместрах. При заражении в третьем триместре беременности преобладают бессимптомные формы течения заболевания, а поздние клинические признаки проявляются через месяцы и годы.
Заражение на ранних сроках эмбриогенеза заканчивается спонтанным выкидышем, мертворождением, вызывает тяжелые нарушения развития — анэнцефалию, анофтальмию, гидроцефалию, гепатоспленомегалию и др. (табл.).
Формирование иммунитета приводит к исчезновению возбудителя из крови, прекращается его размножение в клетках. Образуются истинные тканевые цисты, которые могут длительно, десятилетиями, в интактном состоянии сохраняться в организме (носительство токсоплазм).
Клиника. Приобретенный токсоплазмоз по характеру течения делится на острый и хронический. Кроме того, в зависимости от длительности болезни и выраженности клинических симптомов возможно подострое, а также инаппарантное (субклиническое) течение инфекции, которое характеризуется определенной динамикой либо высоким уровнем специфических антител в крови, при отсутствии клинических проявлений болезни. Таким образом, наиболее удобной для практического здравоохранения, с нашей точки зрения, является следующая классификация приобретенного токсоплазмоза: острый, подострый, хронический, инаппарантный и носительство.
Клинические проявления токсоплазмоза у беременных не имеют каких-либо существенных отличий от уже известной клинической картины заболевания.
Лабораторная диагностика. Для лабораторной диагностики токсоплазмоза чаще всего применяют серологические методы: реакцию непрямой иммунофлюоресценции (РНИФ) и иммуноферментный анализ (ИФА). Диагноз подтверждается достоверно нарастающей динамикой показателей этих тестов, их высоким уровнем либо наличием антител класса IgM. Существенное значение в диагностике токсоплазмоза, особенно в дифференциации острого и хронического процессов, имеет определение классов иммуноглобулинов, в частности антител класса IgM. Надежно диагностировать токсоплазменную инфекцию можно лишь при сравнении результатов серологических реакций в динамике. Антитела всех классов существенно повышаются к концу второй — началу третьей недели от момента инфицирования и достигают диагностического уровня. Диагноз токсоплазмоза при наличии соответствующей клиники может быть поставлен при положительной серологической конверсии, когда второй анализ сыворотки становится положительным.
Диагностика токсоплазмоза у беременных женщин включает в себя весь комплекс необходимых клинических, параклинических и специальных (иммунобиологических) исследований, которые применяются для диагностики токсоплазмоза вообще.
Обязательным условием обследования беременной на токсоплазмоз должна быть консультация врача-инфекциониста для подтверждения либо исключения текущего инфекционного манифестного или бессимптомного (инаппарантного) токсоплазменного процесса.
Учитывая исключительную важность результатов иммунологического обследования в диагностике токсоплазмоза у беременных, необходимо правильно интерпретировать полученные данные.
Вариант 3: клинические проявления инфекции отсутствуют; серологические реакции положительные в низких, средних, иногда высоких титрах (РНИФ 1:640, ИФА IgG ≥ 200 Ед/мл; ИФА IgM — положительно). При исследовании парных сывороток (через 3–4 недели) регистрируется достоверное нарастание уровня специфических антител класса IgM.
Заключение: инаппарантный токсоплазмоз — реальная угроза инфицирования плода.
Вариант 4: имеются клинические проявления токсоплазмоза; серологические реакции положительные в низких и средних (иногда высоких) титрах: РНИФ 1:1280, ИФА IgG ≥ 200 Eд/мл; ИФА IgM — положительно, при исследовании парных сывороток в динамике регистрируется достоверное нарастание уровня специфических антител; выявляются специфические антитела класса IgM-класса. Заключение: острый токсоплазмоз.
Рекомендации: экстренная превентивная этиотропная терапия (не ранее чем со II триместра беременности); в I триместр — рассмотреть вопрос о прерывании беременности; проводят кордо- и амниоцентез на 22–23 неделях беременности; новорожденный обследуется на токсоплазмоз, и при подтверждении диагноза проводится этиотропная терапия (диспансерное наблюдение 5 лет).
Вариант 5: имеются клинические проявления инфекции; серологические реакции положительные в высоких или средних показателях; при исследовании парных сывороток в динамике регистрируется снижение уровня специфических антител (РНИФ ≤ 1:1280, ИФА IgG — 200 Eд/мл; ИФА IgM — положительно). Заключение: подострый токсоплазмоз. Рекомендации: этиотропная терапия (не ранее чем со II триместра); в I триместр — ставится вопрос о прерывании беременности; новорожденный обследуется на токсоплазмоз и при подтверждении диагноза проводится этиотропная терапия (диспансерное наблюдение 5 лет).
Вариант 6: имеются клинические проявления токсоплазмоза; серологические реакции положительны в низких или средних показателях (РНИФ 1:640, ИФА IgG — 200 Eд/мл; ИФА IgM — отрицательно); при исследовании парных сывороток (через 3–4 недели) динамики уровня антител нет; антитела класса IgM отсутствуют. Заключение: хронический приобретенный токсоплазмоз. Рекомендации: этиотропная терапия не проводится; при необходимости специфическая терапия вне беременности; прерывание беременности не показано.
Лечение. Показанием к назначению этиотропной терапии у беременных женщин являются острый, подострый и инаппарантный токсоплазмоз. Лечение хронического токсоплазмоза следует проводить строго по клиническим показаниям либо до, либо после беременности. При отсутствии жалоб и клинических показаний не нуждаются в лечении женщины, переболевшие токсоплазмозом до беременности. Эти женщины расцениваются как практически здоровые лица, не требующие специального медицинского наблюдения. Лечение беременных женщин следует проводить не ранее 12–16 недель беременности (со II триместра беременности).
Назначаются препараты группы пириметамина (Фансидар, Ровамицин).
Фансидар содержит сульфадоксин 500 мг и пириметамин 25 мг. Этиотропная терапия состоит из 2–3 циклов. Назначается 1 таблетка 1 раз в 3 дня № 8 таблеток на цикл. Учитывая возможность угнетения кроветворения под действием этиотропных препаратов, рекомендуется назначение фолиевой кислоты (в средних терапевтических дозах), а также проведение общих анализов крови и мочи. При непереносимости препаратов группы пириметаминов назначают Ровамицин, 1 таблетка которого содержит спиромицина 3 млн МЕ. Назначают по 3 млн МЕ 3 раза в день с семидневным перерывом. Хорошая переносимость Ровамицина больными, отсутствие лекарственного взаимодействия, высокая эффективность позволяют назначать его для лечения токсоплазмоза у беременных. При непереносимости пириметаминов возможна замена на антибиотики, например, эритромицин.
Противопоказаниями для назначения Фансидара и его аналогов, а также сульфаниламидных препаратов и антибиотиков являются: нарушения эритропоэза с анемией, заболевания почек с нарушением их функций, заболевания печени, декомпенсация сердечной деятельности.
В зависимости от сроков беременности целесообразно проведение не менее двух полных курсов этиотропной терапии с перерывами между ними 1–1,5 месяца.
Как показала практика, у пациенток с инаппарантным течением острого токсоплазмоза хороший эффект дает комплексное применение Фансидара с иммуномодуляторами (Галовит, Полиоксидоний). Уже после первого цикла лечения наблюдается значительное снижение IgM.
Профилактика врожденного токсоплазмоза. Профилактика врожденного токсоплазмоза должна строиться с учетом того факта, что только первичное заражение женщины во время беременности может привести к инфицированию плода. Оптимально профилактика врожденного токсоплазмоза должна включать в себя обследование женщин детородного возраста на токсоплазмоз до или, в крайнем случае, во время беременности. Неиммунные беременные женщины должны быть обязательно взяты на диспансерное наблюдение и обследоваться на токсоплазмоз 1 раз в триместр.
Литература
- О выявлении и профилактике токсоплазмоза в Москве. Методические рекомендации (№ 25). М., 2007.
- Лысенко А. Я. Клиническая паразитология. Женева, 2002.
- Hill D., Dubey J. P. Toxoplasma gondii: transmission, diagnosis and prevention // Clin. Microbiol. Infect. 2002. № 10.
- Desmonts G., Couvreur J. Toxoplasmosis in pregnancy and its transmission to the fetus // Bull. N. Y. Acad. Med. 1974. № 2.
Ф. К. Дзуцева*
Г. Ю. Никитина**
Ю. В. Борисенко*
Л. П. Иванова***, кандидат медицинских наук, доцент
С. Х. Зембатова***
*Городской центр по токсоплазмозу, **ГКБ им. С. П. Боткина, ***РМАПО, Москва
Читайте также:

