Ниациновый тест при туберкулезе
Обновлено: 24.04.2024
При применении документа следует учитывать, что Приказом Минздрава России от 15.11.2012 N 932н утвержден Порядок оказания медицинской помощи больным туберкулезом.
5.2.1. Ниациновый тест
Принцип метода. Ниациновая проба основана на том, что продуцируемая микобактериями никотиновая кислота, вступая в реакцию с цианистыми соединениями, дает ярко-желтое окрашивание. Наибольшее количество никотиновой кислоты обнаруживается у штаммов, выращенных на среде Левенштейна-Йенсена, поэтому именно эта среда используется для проведения ниациновой пробы. Подлежащая дифференциации культура микобактерий должна быть выращена на среде Левенштейна-Йенсена в течение не менее 3 - 4 недель и должна иметь достаточно массивный (не менее 50 колоний) рост.
При отрицательном результате реакции следует повторить ее после 6 или более недель инкубации посева, так как возможно, что молодая культура микобактерий не выделила достаточное для реакции количество никотиновой кислоты.
При постановке ниациновой пробы необходимо иметь в виду, что M.tuberculosis выделяют продуцируемую ими никотиновую кислоту в питательную среду, на которой они выращиваются. В связи с этим при наличии на поверхности косяка с питательной средой сливного роста микобактерий возможен ложноотрицательный результат реакции, так как экстрагирующий ниацин реактив не всегда может проникнуть в глубь питательной среды. Для облегчения проникновения экстрагирующего реактива в питательную среду необходимо при наличии на ее поверхности сливного роста микобактерий либо снять и удалить часть колоний, либо проколоть поверхность культуры.
Реакция требует свободного доступа кислорода на протяжении всего исследования, поэтому следует пользоваться либо ватно-марлевыми пробками, либо специальными металлическими колпачками, обеспечивающими свободный доступ воздуха в пробирку.
Ниациновый тест можно выполнять либо с растворами химических реактивов, приготавливаемыми непосредственно перед постановкой пробы, либо с заранее приготовленными в лабораторных условиях или коммерческими бумажными полосками.
Ниациновый тест с растворами химических реактивов требует соблюдения максимальной осторожности, так как цианистые соединения чрезвычайно токсичны при ингаляции паров и вызывают слезотечение, а анилин обладает онкогенным воздействием и способен проникать через кожный барьер. Пробу следует проводить только в вытяжном шкафу! Эти обстоятельства ограничивают применение ниациновой пробы с растворами химических реактивов.
В большинстве бактериологических лабораторий для постановки ниациновой пробы пользуются специально приготовленными бумажными полосками. Преимущество этого метода заключается в использовании вместо цианистых соединений роданистого калия - вещества более безопасного и доступного для бактериологических лабораторий, а также в быстроте реакции, позволяющей через 3 - 4 часа получить ответ о принадлежности выделенной на плотной питательной среде культуры к микобактериям человеческого вида или к другим микобактериям.
Следует иметь в виду, что из-за нестабильности растворов и реагентов необходимо строго соблюдать правила хранения и сроки использования как растворов и реагентов, так и бумажных полосок. В сомнительных случаях реагенты и полоски должны сравниваться со свежеприготовленными.
Реактивы для пропитывания бумажных полосок:
Раствор 1. 20% раствор ПАСК (парааминосалициловой кислоты)
В пробирку с 1,75 мл 96° этанола добавляют 0,25 мл диметилсульфоксида и 400 мг ПАСК.
Смесь подогревают на водяной бане при 56 °C в течение 5 - 10 минут при периодическом встряхивании до полного растворения ПАСК.
Раствор 2. 60% раствор роданистого калия
Навеску 1,5 г роданистого калия растворяют в пробирке с 2,5 мл 8% раствора лимонной кислоты (200 мг лимонной кислоты и 2,5 мл дистиллированной воды).
Раствор 3. 50% раствор хлорамина "Б"
3,125 г хлорамина "Б" растворяют в 6,25 мл дистиллированной воды на водяной бане при температуре 56 - 60 °C при периодическом встряхивании.
Индикаторные бумажные полоски размером 60 x 80 мм готовят из фильтровальной бумаги Filtrak 11 или аналогичной. Один конец полоски отмечают простым карандашом. Оттянутыми пастеровскими пипетками на полоски наносят по 1 капле свежеприготовленных растворов в следующем порядке:
- 20% раствор ПАСК - на отмеченный карандашом конец полоски;
- 60% раствор роданистого калия - на середину полоски;
- 50% горячий раствор хлорамина "Б" - на свободный конец полоски;
- между каплями должны оставаться сухие промежутки.
Индикаторные полоски высушивают в темноте при комнатной температуре в течение 24 часов. Затем для получения более четких результатов наносят повторно 1 каплю хлорамина "Б" на уже высохшую каплю этого раствора. Полоски вновь высушивают, затем помещают в пробирки, закрывают резиновыми пробками и хранят в холодильнике. Полоски пригодны к употреблению в течение 3 месяцев.
- добавить в пробирку с исследуемой культурой микобактерий 1 - 1,5 мл стерильной дистиллированной воды. При наличии сливного роста проткнуть поверхность среды в нескольких местах пипеткой для облегчения доступа раствора к питательной среде;
- поместить пробирку в термостат на 2 - 3 часа в полугоризонтальном положении с тем, чтобы жидкость покрывала всю поверхность среды;
- вынуть пробирку из термостата и перевести ее в вертикальное положение, позволив жидкости стечь на дно в течение 5 - 6 минут;
- в чистую стерильную пробирку перенести пипеткой 0,5 - 0,6 мл экстракта;
- индикаторную полоску помеченным карандашом концом, на который нанесена ПАСК, опустить с помощью пинцета в пробирку с экстрактом, не допуская смачивания экстрагирующей жидкостью средней части полоски, на которую был нанесен роданистый калий;
- немедленно закрыть пробирку резиновой пробкой;
- оставить при комнатной температуре на 15 - 30 минут; допустимо осторожно покачивать пробирку, пока вся полоска не пропитается экстрактом;
- наблюдать за окрашиванием жидкости на дне пробирки на белом фоне.
При положительном ниациновом тесте экстракт окрашивается в желтый цвет разной интенсивности. Любая окраска индикаторной полоски не принимается во внимание, так как это может происходить вследствие окисления реактивов в верхней части полоски. Для дегазации пробирок после проведения реакции пользуются 10% раствором нашатырного спирта, 10% раствором едкого натра или любым щелочным дезинфицирующим средством.
Принцип метода. Ниациновая проба основана на том, что продуцируемая микобактериями никотиновая кислота, вступая в реакцию с цианистыми соединениями, дает ярко-желтое окрашивание. Наибольшее количество никотиновой кислоты обнаруживается у штаммов, выращенных на среде Левенштейна-Йенсена, поэтому именно эта среда используется для проведения ниациновой пробы. Подлежащая дифференциации культура микобактерий должна быть выращена на среде Левенштейна-Йенсена в течение не менее 3-4 недель и должна иметь достаточно массивный (не менее 50 колоний) рост.
При отрицательном результате реакции следует повторить ее после 6 или более недель инкубации посева, так как возможно, что молодая культура микобактерий не выделила достаточное для реакции количество никотиновой кислоты.
При постановке ниациновой пробы необходимо иметь в виду, что М.tuberculosis выделяют продуцируемую ими никотиновую кислоту в питательную среду, на которой они выращиваются. В связи с этим при наличии на поверхности косяка с питательной средой сливного роста микобактерий возможен ложноотрицательный результат реакции, так как экстрагирующий ниацин реактив не всегда может проникнуть в глубь питательной среды. Для облегчения проникновения экстрагирующего реактива в питательную среду необходимо при наличии на ее поверхности сливного роста микобактерий либо снять и удалить часть колоний, либо проколоть поверхность культуры.
Реакция требует свободного доступа кислорода на протяжении всего исследования, поэтому следует пользоваться либо ватно-марлевыми пробками, либо специальными металлическими колпачками, обеспечивающими свободный доступ воздуха в пробирку.
Ниациновый тест можно выполнять либо с растворами химических реактивов, приготавливаемыми непосредственно перед постановкой пробы, либо с заранее приготовленными в лабораторных условиях или коммерческими бумажными полосками.
Ниациновый тест с растворами химических реактивов требует соблюдения максимальной осторожности, так как цианистые соединения чрезвычайно токсичны при ингаляции паров и вызывают слезотечение, а анилин обладает онкогенным воздействием и способен проникать через кожный барьер. Пробу следует проводить только в вытяжном шкафу! Эти обстоятельства ограничивают применение ниациновой пробы с растворами химических реактивов.
В большинстве бактериологических лабораторий для постановки ниациновой пробы пользуются специально приготовленными бумажными полосками. Преимущество этого метода заключается в использовании вместо цианистых соединений роданистого калия - вещества более безопасного и доступного для бактериологических лабораторий, а также в быстроте реакции, позволяющей через 3-4 часа получить ответ о принадлежности выделенной на плотной питательной среде культуры к микобактериям человеческого вида или к другим микобактериям.
Следует иметь в виду, что из-за нестабильности растворов и реагентов необходимо строго соблюдать правила хранения и сроки использования как растворов и реагентов, так и бумажных полосок. В сомнительных случаях реагенты и полоски должны сравниваться со свежеприготовленными.
Реактивы для пропитывания бумажных полосок:
Раствор 1. 20% раствор ПАСК (парааминосалициловой кислоты)
В пробирку с 1,75 мл 96° этанола добавляют 0,25 мл диметилсульфоксида и 400 мг ПАСК.
Смесь подогревают на водяной бане при 56°С в течение 5-10 минут при периодическом встряхивании до полного растворения ПАСК.
Раствор 2. 60% раствор роданистого калия Навеску 1,5 г роданистого калия растворяют в пробирке с 2,5 мл 8% раствора лимонной кислоты
(200 мг лимонной кислоты и 2,5 мл дистиллированной воды).
Раствор 3. 50% раствор хлорамина "Б" 3,125 г хлорамина "Б" растворяют в 6,25 мл дистиллированной воды на водяной бане при температуре 56-60°С при периодическом встряхивании.
Индикаторные бумажные полоски размером 60 х 80 мм готовят из фильтровальной бумаги Filtrak 11 или аналогичной. Один конец полоски отмечают простым карандашом. Оттянутыми пастеровскими пипетками на полоски наносят по 1 капле свежеприготовленных растворов в следующем порядке:
- 20% раствор ПАСК - на отмеченный карандашом конец полоски;
- 60% раствор роданистого калия - на середину полоски;
- 50% горячий раствор хлорамина "Б" - на свободный конец 1 полоски.
- Между каплями должны оставаться сухие промежутки.
Индикаторные полоски высушивают в темноте при комнатной температуре в течение 24 часов. Затем для получения более четких результатов наносят повторно 1 каплю хлорамина "Б" на уже высохшую каплю этого раствора. Полоски вновь высушивают, затем помещают в пробирки, закрывают резиновыми пробками и хранят в холодильнике. Полоски пригодны к употреблению в течение 3 месяцев.
Туберкулез известен с глубокой древности. Легочные формы туберкулеза описаны еще Гипократом, Галеном, Авиценной. В древнем Китае и Индии были отмечены классические симптомы заболевания легких у людей, которые страдали чахоткой.
Возбудитель заболевания открыт в 1882 г. Р. Кохом.
В 60-80 г.г. XX века были достигнуты значительные успехи в борьбе с туберкулезом. Этому способствовали регулярное обследование населения флюорографическим методом и методом туберкулинодиагностики, обязательная вакцинация БЦЖ новорожденных, назначение эффективных противотуберкулезных препаратов, проведение полных курсов лечения болезни с контролем излеченности, выполнение химиопрофилактики людям с повышенным риском заболевания.
Кроме возбудителей туберкулеза, важную роль в патологии стали играть другие микобактерии. Они являются причиной тяжелых оппортунистических инфекций у лиц с иммунодефицитами, особенно у пациентов с ВИЧ-инфекцией.
Классификация
Микобактерии относятся к порядку Actinomycetales, cемейству Mycobacteriaceae, роду Mycobacterium. К настоящему времени среди них выделяют более 130 видов и подвидов.
По роли в патологии все представители рода микобактерий подразделяются на 4 группы:
I. Комплекс Mycobacterium tuberculosis включает возбудителей туберкулеза у человека и животных.
M. tuberculosis вызывает туберкулез у 85-90 % больных; M. bovis – у 10-15% больных.
M. africanum иногда выделяется у больных туберкулезом в Западной и Центральной Африке.
Остальные виды возбудителей, входящих в этот комплекс (M. canetti, M. caprae и некоторые другие) весьма редко вызывают заболевания у человека. К этой же группе относится вакцинный штамм M. bovis BCG.
II. Возбудители микобактериозов – более 60 видов, которые выделены из организма людей, теплокровных и холоднокровных животных. У человека вызывают оппортунистические инфекции. Наиболее часто встречающиеся возбудители микобактериозов –кислоустойчивые бактерии M. avium-intracellulare, M. kansasii M. ulcerans и др.
III. Возбудитель проказы – М. leprae.
IV. Кислотоустойчивые сапрофиты, типичным представителем которых является M. smegmatis.
Выражен полиморфизм, встречаются палочковидные, ветвящиеся, нитевидные, фильтрующиеся L-формы. Спор, жгутиков, капсул не имеют, но есть оболочка, напоминающая микрокапсулу. Кислото-, щелоче- и спиртоустойчивы, реже встречаются кислотоподатливые формы. Это связано с высоким содержанием липидов, фосфатидов и восков в клеточных стенках (до 60%), поэтому бактерии плохо воспринимают анилиновые красители и обычные способы окраски.
Относятся к грамположительным, хотя по Граму их обычно не окрашивают. Используют методику выявления кислотоустойчивых бактерий – окраску по Циль-Нильсену в красный цвет. Более чувствительным является метод люминисцентной микроскопии с окраской аурамином (яркий желтый цвет) или родамином.
Культуральные свойства
Требовательны к питательным средам и условиям культивирования. Строгие аэробы, растут медленно от 2 до 8 недель только при температуре 37 0 С. Лучшими средами являются яичные, например среда Левенштейна-Иенсена (в нее входят МПА, картофельный сок, яйца, молоко, глицерин, аспарагин, краситель малахитовый зеленый для угнетения роста посторонней микрофлоры); среда Финна (состав тот же, но вместо аспарагина – сложный солевой раствор). Для глубинного посева применяют цитратную кровь.
Вирулентны в R-форме. На жидких средах дают рост в виде морщинистой пленки. На плотных средах образуют сухие, кремовые, бородавчатые колонии. Характер роста связан с выраженной гидрофобностью за счет большого количества липидов в клеточной стенке.
Биохимические свойства
Микобактерии туберкулеза ферментируют многие углеводы и спирты, обладают протеолитической активностью. Имеют ряд ферментов: термолабильную каталазу-пероксидазу, супероксиддисмутазу, уреазу, фосфатазу, лецитиназу.
Антигенные свойства
Антигены микобактерий включают белковые, полисахаридные и липидные компоненты. Преобладающие липидные фракции обладают умеренной антигенностью, однако в комплексе с белками способны вызывать активный иммунный ответ. Ведущими в иммунитете к возбудителю являются клеточно-опосредованные реакции (ГЧЗТ).
В 1890 г. Р. Кох получил туберкулин – фильтрат культуры возбудителя, содержащий смесь его антигенов. В настоящее время туберкулин представляет собой препарат из высокоочищенных белковых фракций возбудителя, который используется для иммунодиагностики туберкулеза.
Резистентность
Микобактерии туберкулеза проявляют выраженную устойчивость в окружающей среде. В пыли и высушенной мокроте они сохраняются несколько месяцев, в воде – больше года, в почве – до 6 месяцев.
Возбудители туберкулеза погибают при температуре 100 0 С. Пастеризация инактивирует M. bovis в молочных продуктах. Микобактерии чувствительны к солнечному свету и УФ-облучению.
Вследствие высокой химической устойчивости дезинфицирующие растворы действуют на них медленно; обработка основными дезинфектантами требует более длительной экспозиции.
Микобактерии туберкулеза природно устойчивы к большинству антибиотиков.
Факторы вирулентности
Возбудитель не обладает классическими факторами вирулентности, такими как экзо- или эндотоксины.
Токсические компоненты микобактерий связаны с микробными клетками и обычно высвобождаются при их разрушении.
Микобактерии туберкулеза имеют корд-фактор –гликолипид, который является фактором адгезии, поражает митохондрии клеток, нарушает тканевое дыхание. При культивировании вызывает склеивание вирулентных особей в виде кос, тяжей.
Туберкулопротеины обладают аллергизирующим действием, вызывают развитие ГЧЗТ.
Гликолипиды наружного слоя клеточной стенки (микозиды) и маннозные рецепторы микобактерий способствуют адгезии бактерий и подавляют фагоцитоз.
Ферменты каталаза и супероксиддисмутаза препятствуют дыхательному взрыву в макрофагах.
Туберкулостеариновая, фтионовая, миколевая и другие жирные кислоты оказывают токсическое действие на ткани.
Белки-сидерофоры обеспечивают микобактерий ионами железа, что способствует их выживанию в макрофагах.
Мутации в генах, кодирующих ферменты каталазу и РНК-полимеразу, обеспечивают устойчивость микобактерий к основным противотуберкулезным препаратам – изониазиду и рифампицину.
Патогенез и характеристика заболевания
Туберкулез (от латинского слова tuberculum – бугорок) – хроническое системное инфекционное заболевание, поражающее человека, животных, птиц.
В начале XXI века туберкулез вновь стал ведущей инфекционной патологией во всем мире. Ежегодно регистрируется более 9 млн новых случаев туберкулеза, а около 2 млн больных в год погибают от этого заболевания, что уступает лишь ВИЧ-инфекции.
В отсутствие лечения вероятность летального исхода от туберкулеза и его осложнений в течение жизни больного превышает 50%.
Распространенность инфекции гораздо выше. Считается, что около 2 млрд человек в мире инфицированы микобактериями туберкулеза. Тем не менее, для человека характерна высокая естественная резистентность к возбудителю. Лишь у 5-10% инфицированных появляются клинические признаки болезни.
Отсюда туберкулез во многом представляет собой социальное заболевание. Развитию болезни способствуют низкий уровень медико-санитарной помощи и санитарной культуры, недостаточный уровень питания, жилищных условий, скученность населения при совместном проживании, усиление миграции из эндемичных по туберкулезу регионов.
Резкое обострение ситуации также связано с продолжающейся пандемией ВИЧ-инфекции. Совместная инфекция ВИЧ и M. tuberculosis приводит к ускоренной гибели больных. Это происходит как из-за подавления реакций клеточного иммунитета с тяжелым течением туберкулеза, так и вследствие усиленной репликации ВИЧ.
Наконец, наибольшую угрозу представляет появление и неуклонное распространение штаммов возбудителей, устойчивых к основным противотуберкулезным средствам. Вероятность успешного лечения таких больных снижается.
Различают множественную (МЛУ) и широкую лекарственную устойчивость (ШЛУ) микобактерий к химиопрепаратам.
При МЛУ возбудитель устойчив к ведущим противотуберкулезным препаратам I ряда – изониазиду и рифампицину.
При ШЛУ возбудитель дополнительно устойчив к трем и более препаратам II ряда, включая фторхинолоны.
Скорость распространения устойчивых штаммов среди населения является более высокой. Ежегодно возникает до 500 тыс новых случаев МЛУ-туберкулеза. В определенных регионах (Южная Африка, отдельные провинции КНР, Индии и области Российской Федерации, страны Восточной Европы) частота МЛУ-туберкулеза превышает 10-20%.
В Республике Беларусь заболеваемость туберкулезом составляет около 44 случаев на 100 тыс населения, что ниже чем в Российской Федерации и Украине. Однако постепенно нарастает доля лиц с лекарственно устойчивым туберкулезом.
Источники инфекции при туберкулезе – больные люди и больные животные (крупный рогатый скот), выделяющие микобактерии.
Пути передачи – чаще воздушно-капельный, реже контактный и алиментарный (через молоко больных животных). Заражению способствует постоянный контакт, проживание с больным туберкулезом.
Наиболее часто встречается туберкулез легких (до 75% случаев), реже – внелегочный туберкулез (мочеполовой системы, костей, лимфоузлов, кишечника, туберкулезный менингит).
Ингалированные бактерии фагоцитируются альвеолярными макрофагами и дендритными клетками и транспортируются в регионарные лимфоузлы. Фагоцитоз носит незавершенный характер, так как микобактерии блокируют фаголизосомальное слияние. Кроме того, они могут вызывать апоптоз макрофагов.
Гликолипиды-микозиды усиливают токсическое действие корд-фактора, поражая мембраны митохондрий. Корд-фактор тормозит активность полиморфноядерных фагоцитов.
Иммунное воспаление является ведущим фактором в патогенезе туберкулезной инфекции.
У входных ворот легких в ацинусах развивается первичный аффект, идущие от него лимфатические сосуды и регионарные лимфоузлы воспаляются, формируется первичный туберкулезный комплекс. В ацинусе возникает гранулема в виде бугорка. Этому способствует накопление в очаге молочной кислоты, низкое значение рН, высокая концентрация углекислого газа. В гранулеме накапливается большое количество лимфоидных, плазматических клеток и фибробластов. В центре гранулемы возникают участки творожистого некроза из-за гибели клеток и действия тканевых протеаз. Здесь располагаются возбудители, вокруг них находятся эпителиоидные и гигантские клетки; развивается ГЧЗТ.
Высокая сенсибилизация организма приводит к токсико-аллергическим реакциям. Клинически этот период сопровождается кашлем, кровохарканьем, снижением массы тела, потливостью, субфебрилитетом или лихорадкой.
У лиц с иммунодефицитом наблюдаются тяжелые формы туберкулеза – казеозная пневмония с распадом легочной ткани и диссеминированный (милиарный) туберкулез – в органах и тканях развиваются множественные мелкие гранулемы. Данные формы характеризуются высокой летальностью.
Очаговый туберкулез поражает отдельные органы (чаще всего легкие); генерализованные формы инфекции (милиарный туберкулез, туберкулезный менингит, внелегочный туберкулез) протекают наиболее тяжело.
При благоприятном течении инфекции клеточные иммунные реакции останавливают размножение возбудителя. Очаг воспаления уменьшается, подвергается кальцификации и фиброзу, при этом формируются кальцинаты (очаги Гона). Клинические проявления болезни затихают.
Часть бактерий переходит в латентное состояние, и они долгое время персистируют внутриклеточно в макрофагах и клетках эпителия.
При ослабленном клеточном иммунитете создаются условиия для дальнейшего размножения микобактерий. Подавляется HLA-зависимое представление антигенов, тормозится пролиферация Т-лимфоцитов.
Реактивация возбудителей ведет к обострению инфекционного процесса. Возникает вторичный туберкулез. Для него характерно развитие хронического воспаления с чередованием очагов распада и фиброза. Без лечения заболевание неуклонно прогрессирует с развитием осложнений (легочного кровотечения, дыхательной недостаточности), что значительно ухудшает прогноз.
При туберкулезе развивается нестерильный иммунитет, преимущественно клеточный. Основную роль играют макрофаги и дендритные клетки. Имеют значение Т-лимфоциты и их медиаторы, усиливающие фагоцитоз (в первую очередь – γ-интерферон). Антитела и другие компоненты гуморального иммунитета играют вспомогательную роль в элиминации возбудителя.
Лабораторная диагностика
Материалом для исследования служат мокрота, моча, ликвор, пунктат лимфоузла, биоптаты тканей.
Бактериоскопический метод. Окрашивают мазки по Циль-Нильсену, выявляют мелкие красные палочки. При окраске флюоресцентными красителями (аурамином, родамином) микобактерии дают желто-белое свечение в люминесцентном микроскопе.
При малом количестве возбудителя используют методы обогащения.
Гомогенизация – материал обрабатывают щелочью, фибрин при этом растворяется, а возбудитель высвобождается. Из осадка после центрифугирования готовят мазки.
Флотация – гомогенизированную мокроту обрабатывают ксилолом или бензолом и тщательно встряхивают. Возбудитель всплывает в силу гидрофобности вместе с пеной. Из нее готовят мазок и окрашивают по Цилю-Нильсену.
Бактериологический метод. Материал обрабатывают серной кислотой и засевают на яичные среды.
Для идентификации M. tuberculosis определяют основные свойства возбудителя.
Оценивают характер роста – обнаруживают сухие, бородавчатые, кремовые колонии (R-форма); длительность роста составляет 20-60 дней. Для микобактерий туберкулеза характерен рост только при температуре 37-38 0 С; они не растут на простых средах и средах с салицилатами;
У микобактерий туберкулеза наблюдается положительный ниациновый тест (среда с хлорамином В желтеет при накоплении никотиновой кислоты). Также они обладают термолабильной каталазой; восстанавливают нитраты в нитриты; выделяют уреазу; к микобактериям туберкулеза чувствительны морские свинки.
Для внутривидовой дифференциации используют фаготипирование штаммов микобактериофагами.
Mycobacterium bovis вирулентны в S-форме; колонии кремовые, гладкие; ниациновый тест отрицательный; рост до 40 дней; каталаза термолабильная; выделяют уреазу; не восстанавливают нитраты; рост только при температуре 37-40 0 С.
Mycobacterum africanum – рост 31-40 дней; ниациновый тест положительный; вирулентны в S-форме; каталаза термолабильна; не восстанавливают нитраты; выделяют уреазу. Остальные свойства как у M. tuberculosis.
Микобактерии туберкулеза необходимо дифференцировать от атипичных кислотоустойчивых бактерий, вызывающих микобактериозы.
Атипичные кислотоустойчивые бактерии имеют оранжевый пигмент, вирулентны в S-форме, растут на средах с салицилатами, имеют термостабильную каталазу, рост через 10-20 дней при температуре 22-45 0 С, нет корд-фактора.
Кислотоустойчивые сапрофиты (M. smegmatis и др.) в отличие от предыдущих возбудителей, растут на простых средах, длительность роста 3-4 дня, имеют S-форму, оранжевый пигмент, нет признаков болезнетворности, чувствительны к спирту.
Туберкулез известен с глубокой древности. Легочные формы туберкулеза описаны еще Гипократом, Галеном, Авиценной. В древнем Китае и Индии были отмечены классические симптомы заболевания легких у людей, которые страдали чахоткой.
Возбудитель заболевания открыт в 1882 г. Р. Кохом.
В 60-80 г.г. XX века были достигнуты значительные успехи в борьбе с туберкулезом. Этому способствовали регулярное обследование населения флюорографическим методом и методом туберкулинодиагностики, обязательная вакцинация БЦЖ новорожденных, назначение эффективных противотуберкулезных препаратов, проведение полных курсов лечения болезни с контролем излеченности, выполнение химиопрофилактики людям с повышенным риском заболевания.
Кроме возбудителей туберкулеза, важную роль в патологии стали играть другие микобактерии. Они являются причиной тяжелых оппортунистических инфекций у лиц с иммунодефицитами, особенно у пациентов с ВИЧ-инфекцией.
Классификация
Микобактерии относятся к порядку Actinomycetales, cемейству Mycobacteriaceae, роду Mycobacterium. К настоящему времени среди них выделяют более 130 видов и подвидов.
По роли в патологии все представители рода микобактерий подразделяются на 4 группы:
I. Комплекс Mycobacterium tuberculosis включает возбудителей туберкулеза у человека и животных.
M. tuberculosis вызывает туберкулез у 85-90 % больных; M. bovis – у 10-15% больных.
M. africanum иногда выделяется у больных туберкулезом в Западной и Центральной Африке.
Остальные виды возбудителей, входящих в этот комплекс (M. canetti, M. caprae и некоторые другие) весьма редко вызывают заболевания у человека. К этой же группе относится вакцинный штамм M. bovis BCG.
II. Возбудители микобактериозов – более 60 видов, которые выделены из организма людей, теплокровных и холоднокровных животных. У человека вызывают оппортунистические инфекции. Наиболее часто встречающиеся возбудители микобактериозов –кислоустойчивые бактерии M. avium-intracellulare, M. kansasii M. ulcerans и др.
III. Возбудитель проказы – М. leprae.
IV. Кислотоустойчивые сапрофиты, типичным представителем которых является M. smegmatis.
Выражен полиморфизм, встречаются палочковидные, ветвящиеся, нитевидные, фильтрующиеся L-формы. Спор, жгутиков, капсул не имеют, но есть оболочка, напоминающая микрокапсулу. Кислото-, щелоче- и спиртоустойчивы, реже встречаются кислотоподатливые формы. Это связано с высоким содержанием липидов, фосфатидов и восков в клеточных стенках (до 60%), поэтому бактерии плохо воспринимают анилиновые красители и обычные способы окраски.
Относятся к грамположительным, хотя по Граму их обычно не окрашивают. Используют методику выявления кислотоустойчивых бактерий – окраску по Циль-Нильсену в красный цвет. Более чувствительным является метод люминисцентной микроскопии с окраской аурамином (яркий желтый цвет) или родамином.
Культуральные свойства
Требовательны к питательным средам и условиям культивирования. Строгие аэробы, растут медленно от 2 до 8 недель только при температуре 37 0 С. Лучшими средами являются яичные, например среда Левенштейна-Иенсена (в нее входят МПА, картофельный сок, яйца, молоко, глицерин, аспарагин, краситель малахитовый зеленый для угнетения роста посторонней микрофлоры); среда Финна (состав тот же, но вместо аспарагина – сложный солевой раствор). Для глубинного посева применяют цитратную кровь.
Вирулентны в R-форме. На жидких средах дают рост в виде морщинистой пленки. На плотных средах образуют сухие, кремовые, бородавчатые колонии. Характер роста связан с выраженной гидрофобностью за счет большого количества липидов в клеточной стенке.
Биохимические свойства
Микобактерии туберкулеза ферментируют многие углеводы и спирты, обладают протеолитической активностью. Имеют ряд ферментов: термолабильную каталазу-пероксидазу, супероксиддисмутазу, уреазу, фосфатазу, лецитиназу.
Антигенные свойства
Антигены микобактерий включают белковые, полисахаридные и липидные компоненты. Преобладающие липидные фракции обладают умеренной антигенностью, однако в комплексе с белками способны вызывать активный иммунный ответ. Ведущими в иммунитете к возбудителю являются клеточно-опосредованные реакции (ГЧЗТ).
В 1890 г. Р. Кох получил туберкулин – фильтрат культуры возбудителя, содержащий смесь его антигенов. В настоящее время туберкулин представляет собой препарат из высокоочищенных белковых фракций возбудителя, который используется для иммунодиагностики туберкулеза.
Резистентность
Микобактерии туберкулеза проявляют выраженную устойчивость в окружающей среде. В пыли и высушенной мокроте они сохраняются несколько месяцев, в воде – больше года, в почве – до 6 месяцев.
Возбудители туберкулеза погибают при температуре 100 0 С. Пастеризация инактивирует M. bovis в молочных продуктах. Микобактерии чувствительны к солнечному свету и УФ-облучению.
Вследствие высокой химической устойчивости дезинфицирующие растворы действуют на них медленно; обработка основными дезинфектантами требует более длительной экспозиции.
Микобактерии туберкулеза природно устойчивы к большинству антибиотиков.
Факторы вирулентности
Возбудитель не обладает классическими факторами вирулентности, такими как экзо- или эндотоксины.
Токсические компоненты микобактерий связаны с микробными клетками и обычно высвобождаются при их разрушении.
Микобактерии туберкулеза имеют корд-фактор –гликолипид, который является фактором адгезии, поражает митохондрии клеток, нарушает тканевое дыхание. При культивировании вызывает склеивание вирулентных особей в виде кос, тяжей.
Туберкулопротеины обладают аллергизирующим действием, вызывают развитие ГЧЗТ.
Гликолипиды наружного слоя клеточной стенки (микозиды) и маннозные рецепторы микобактерий способствуют адгезии бактерий и подавляют фагоцитоз.
Ферменты каталаза и супероксиддисмутаза препятствуют дыхательному взрыву в макрофагах.
Туберкулостеариновая, фтионовая, миколевая и другие жирные кислоты оказывают токсическое действие на ткани.
Белки-сидерофоры обеспечивают микобактерий ионами железа, что способствует их выживанию в макрофагах.
Мутации в генах, кодирующих ферменты каталазу и РНК-полимеразу, обеспечивают устойчивость микобактерий к основным противотуберкулезным препаратам – изониазиду и рифампицину.
Патогенез и характеристика заболевания
Туберкулез (от латинского слова tuberculum – бугорок) – хроническое системное инфекционное заболевание, поражающее человека, животных, птиц.
В начале XXI века туберкулез вновь стал ведущей инфекционной патологией во всем мире. Ежегодно регистрируется более 9 млн новых случаев туберкулеза, а около 2 млн больных в год погибают от этого заболевания, что уступает лишь ВИЧ-инфекции.
В отсутствие лечения вероятность летального исхода от туберкулеза и его осложнений в течение жизни больного превышает 50%.
Распространенность инфекции гораздо выше. Считается, что около 2 млрд человек в мире инфицированы микобактериями туберкулеза. Тем не менее, для человека характерна высокая естественная резистентность к возбудителю. Лишь у 5-10% инфицированных появляются клинические признаки болезни.
Отсюда туберкулез во многом представляет собой социальное заболевание. Развитию болезни способствуют низкий уровень медико-санитарной помощи и санитарной культуры, недостаточный уровень питания, жилищных условий, скученность населения при совместном проживании, усиление миграции из эндемичных по туберкулезу регионов.
Резкое обострение ситуации также связано с продолжающейся пандемией ВИЧ-инфекции. Совместная инфекция ВИЧ и M. tuberculosis приводит к ускоренной гибели больных. Это происходит как из-за подавления реакций клеточного иммунитета с тяжелым течением туберкулеза, так и вследствие усиленной репликации ВИЧ.
Наконец, наибольшую угрозу представляет появление и неуклонное распространение штаммов возбудителей, устойчивых к основным противотуберкулезным средствам. Вероятность успешного лечения таких больных снижается.
Различают множественную (МЛУ) и широкую лекарственную устойчивость (ШЛУ) микобактерий к химиопрепаратам.
При МЛУ возбудитель устойчив к ведущим противотуберкулезным препаратам I ряда – изониазиду и рифампицину.
При ШЛУ возбудитель дополнительно устойчив к трем и более препаратам II ряда, включая фторхинолоны.
Скорость распространения устойчивых штаммов среди населения является более высокой. Ежегодно возникает до 500 тыс новых случаев МЛУ-туберкулеза. В определенных регионах (Южная Африка, отдельные провинции КНР, Индии и области Российской Федерации, страны Восточной Европы) частота МЛУ-туберкулеза превышает 10-20%.
В Республике Беларусь заболеваемость туберкулезом составляет около 44 случаев на 100 тыс населения, что ниже чем в Российской Федерации и Украине. Однако постепенно нарастает доля лиц с лекарственно устойчивым туберкулезом.
Источники инфекции при туберкулезе – больные люди и больные животные (крупный рогатый скот), выделяющие микобактерии.
Пути передачи – чаще воздушно-капельный, реже контактный и алиментарный (через молоко больных животных). Заражению способствует постоянный контакт, проживание с больным туберкулезом.
Наиболее часто встречается туберкулез легких (до 75% случаев), реже – внелегочный туберкулез (мочеполовой системы, костей, лимфоузлов, кишечника, туберкулезный менингит).
Ингалированные бактерии фагоцитируются альвеолярными макрофагами и дендритными клетками и транспортируются в регионарные лимфоузлы. Фагоцитоз носит незавершенный характер, так как микобактерии блокируют фаголизосомальное слияние. Кроме того, они могут вызывать апоптоз макрофагов.
Гликолипиды-микозиды усиливают токсическое действие корд-фактора, поражая мембраны митохондрий. Корд-фактор тормозит активность полиморфноядерных фагоцитов.
Иммунное воспаление является ведущим фактором в патогенезе туберкулезной инфекции.
У входных ворот легких в ацинусах развивается первичный аффект, идущие от него лимфатические сосуды и регионарные лимфоузлы воспаляются, формируется первичный туберкулезный комплекс. В ацинусе возникает гранулема в виде бугорка. Этому способствует накопление в очаге молочной кислоты, низкое значение рН, высокая концентрация углекислого газа. В гранулеме накапливается большое количество лимфоидных, плазматических клеток и фибробластов. В центре гранулемы возникают участки творожистого некроза из-за гибели клеток и действия тканевых протеаз. Здесь располагаются возбудители, вокруг них находятся эпителиоидные и гигантские клетки; развивается ГЧЗТ.
Высокая сенсибилизация организма приводит к токсико-аллергическим реакциям. Клинически этот период сопровождается кашлем, кровохарканьем, снижением массы тела, потливостью, субфебрилитетом или лихорадкой.
У лиц с иммунодефицитом наблюдаются тяжелые формы туберкулеза – казеозная пневмония с распадом легочной ткани и диссеминированный (милиарный) туберкулез – в органах и тканях развиваются множественные мелкие гранулемы. Данные формы характеризуются высокой летальностью.
Очаговый туберкулез поражает отдельные органы (чаще всего легкие); генерализованные формы инфекции (милиарный туберкулез, туберкулезный менингит, внелегочный туберкулез) протекают наиболее тяжело.
При благоприятном течении инфекции клеточные иммунные реакции останавливают размножение возбудителя. Очаг воспаления уменьшается, подвергается кальцификации и фиброзу, при этом формируются кальцинаты (очаги Гона). Клинические проявления болезни затихают.
Часть бактерий переходит в латентное состояние, и они долгое время персистируют внутриклеточно в макрофагах и клетках эпителия.
При ослабленном клеточном иммунитете создаются условиия для дальнейшего размножения микобактерий. Подавляется HLA-зависимое представление антигенов, тормозится пролиферация Т-лимфоцитов.
Реактивация возбудителей ведет к обострению инфекционного процесса. Возникает вторичный туберкулез. Для него характерно развитие хронического воспаления с чередованием очагов распада и фиброза. Без лечения заболевание неуклонно прогрессирует с развитием осложнений (легочного кровотечения, дыхательной недостаточности), что значительно ухудшает прогноз.
При туберкулезе развивается нестерильный иммунитет, преимущественно клеточный. Основную роль играют макрофаги и дендритные клетки. Имеют значение Т-лимфоциты и их медиаторы, усиливающие фагоцитоз (в первую очередь – γ-интерферон). Антитела и другие компоненты гуморального иммунитета играют вспомогательную роль в элиминации возбудителя.
Лабораторная диагностика
Материалом для исследования служат мокрота, моча, ликвор, пунктат лимфоузла, биоптаты тканей.
Бактериоскопический метод. Окрашивают мазки по Циль-Нильсену, выявляют мелкие красные палочки. При окраске флюоресцентными красителями (аурамином, родамином) микобактерии дают желто-белое свечение в люминесцентном микроскопе.
При малом количестве возбудителя используют методы обогащения.
Гомогенизация – материал обрабатывают щелочью, фибрин при этом растворяется, а возбудитель высвобождается. Из осадка после центрифугирования готовят мазки.
Флотация – гомогенизированную мокроту обрабатывают ксилолом или бензолом и тщательно встряхивают. Возбудитель всплывает в силу гидрофобности вместе с пеной. Из нее готовят мазок и окрашивают по Цилю-Нильсену.
Бактериологический метод. Материал обрабатывают серной кислотой и засевают на яичные среды.
Для идентификации M. tuberculosis определяют основные свойства возбудителя.
Оценивают характер роста – обнаруживают сухие, бородавчатые, кремовые колонии (R-форма); длительность роста составляет 20-60 дней. Для микобактерий туберкулеза характерен рост только при температуре 37-38 0 С; они не растут на простых средах и средах с салицилатами;
У микобактерий туберкулеза наблюдается положительный ниациновый тест (среда с хлорамином В желтеет при накоплении никотиновой кислоты). Также они обладают термолабильной каталазой; восстанавливают нитраты в нитриты; выделяют уреазу; к микобактериям туберкулеза чувствительны морские свинки.
Для внутривидовой дифференциации используют фаготипирование штаммов микобактериофагами.
Mycobacterium bovis вирулентны в S-форме; колонии кремовые, гладкие; ниациновый тест отрицательный; рост до 40 дней; каталаза термолабильная; выделяют уреазу; не восстанавливают нитраты; рост только при температуре 37-40 0 С.
Mycobacterum africanum – рост 31-40 дней; ниациновый тест положительный; вирулентны в S-форме; каталаза термолабильна; не восстанавливают нитраты; выделяют уреазу. Остальные свойства как у M. tuberculosis.
Микобактерии туберкулеза необходимо дифференцировать от атипичных кислотоустойчивых бактерий, вызывающих микобактериозы.
Атипичные кислотоустойчивые бактерии имеют оранжевый пигмент, вирулентны в S-форме, растут на средах с салицилатами, имеют термостабильную каталазу, рост через 10-20 дней при температуре 22-45 0 С, нет корд-фактора.
Кислотоустойчивые сапрофиты (M. smegmatis и др.) в отличие от предыдущих возбудителей, растут на простых средах, длительность роста 3-4 дня, имеют S-форму, оранжевый пигмент, нет признаков болезнетворности, чувствительны к спирту.
Морфология туберкулёза человека. Палочка Коха. Тинкториальные свойства туберкулеза. Культуральные свойства возбудителя туберкулеза.
М. tuberculosis (палочка Коха) — тонкая, прямая или слегка изогнутая палочка, размером 1-10*0,2-0,6 мкм, со слегка закруглёнными концами (рис. 22-1). В молодых культурах палочки более длинные, а в старых склонны к ветвлению.
Бактерии туберкулёза способны образовывать L-формы, сохраняющие способность к инфицированию, а также фильтрующиеся формы, патогенетическая роль которых остаётся плохо изученной. Капсул не имеют, но образуют микрокапсулу.
Методом Циля-Нильсена окрашиваются в ярко-красный цвет. Содержат кислотонеустойчивые гранулы (зёрна Муха), располагающиеся в цитоплазме.
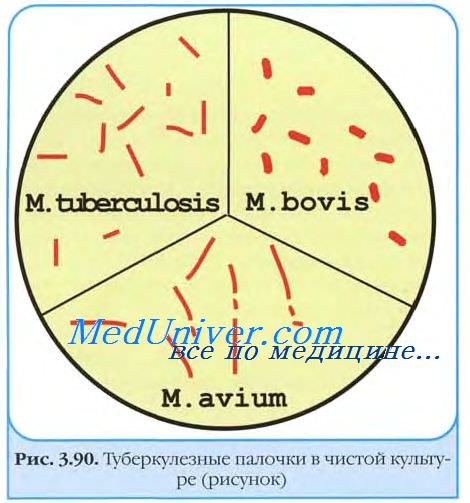
Культуральные свойства возбудителя туберкулеза
Туберкулёзные палочки могут расти как в аэробных, так и факультативно анаэробных условиях. Повышенное содержание СО2 (5-10%) способствует более быстрому росту. Оптимальная температура 37-38 °С; рН 7,0-7,2. Нуждаются в присутствии белков, глицерина, факторов роста (биотин, никотиновая кислота, рибофлавин и др.), ионов (Mg2+ K+, Na+ Fe2+) и др.
Для выращивания бактерий туберкулеза наиболее часто применяются глицериновые, картофельные с жёлчью, яичные, полусинтетические и синтетические среды. Наиболее оптимальна среда Лёвенштайна-Йёнсена.
На средах туберкулёзные палочки обычно образуют R-колонии; под влиянием антибактериальных препаратов бактерии могут диссоциировать с образованием мягких и влажных S-колоний.
В жидких средах палочки туберкулеза образуют сухую морщинистую пленку (на 7-10-е сутки), поднимающуюся на края пробирки; среда остаётся прозрачной. В жидких средах выявляют корд-фактор — важный дифференциальный признак вирулентности. Наличие корд-фактора обусловливает сближение бактериальных клеток в микроколониях и их рост в виде серпантинообразных кос.
На плотных средах рост палочек туберкулеза отмечают на 14-40-е сутки в виде сухого морщинистого налёта желто-, вато-кремового цвета. Зрелые колонии напоминают цветную капусту, крошковатые, плохо смачиваются водой и имеют приятный запах. Культуры плохо снимаются со среды, а при прокаливании трещат. Отличительная особенность М. tuberculosis— способность к синтезу значительного количества никотиновой кислоты (ниацина); ниациновый тест — важный метод дифференцировки микобактерий.
Читайте также:

