Норма для анализов на токсоплазмоз у детей
Обновлено: 22.04.2024
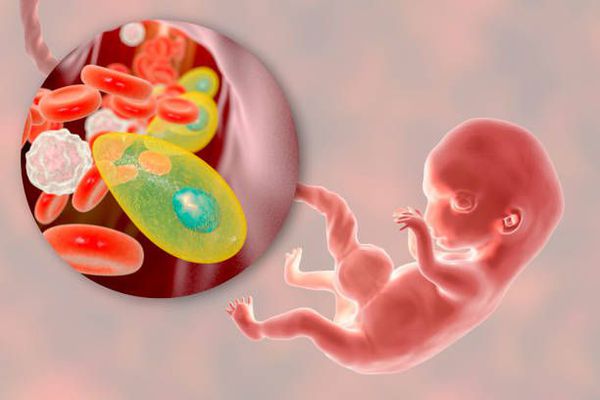
Токсоплазмоз – это одна из TORCH-инфекций, инфекций которые связаны одним единственным признаком - возбудители могут передаваться внутриутробно: от матери к ребенку. Данные инфекции нередко являются причиной проблем с вынашиванием беременности и виновниками врожденных пороков развития у малыша.
Что провоцирует / Причины Токсоплазмоза у беременных:
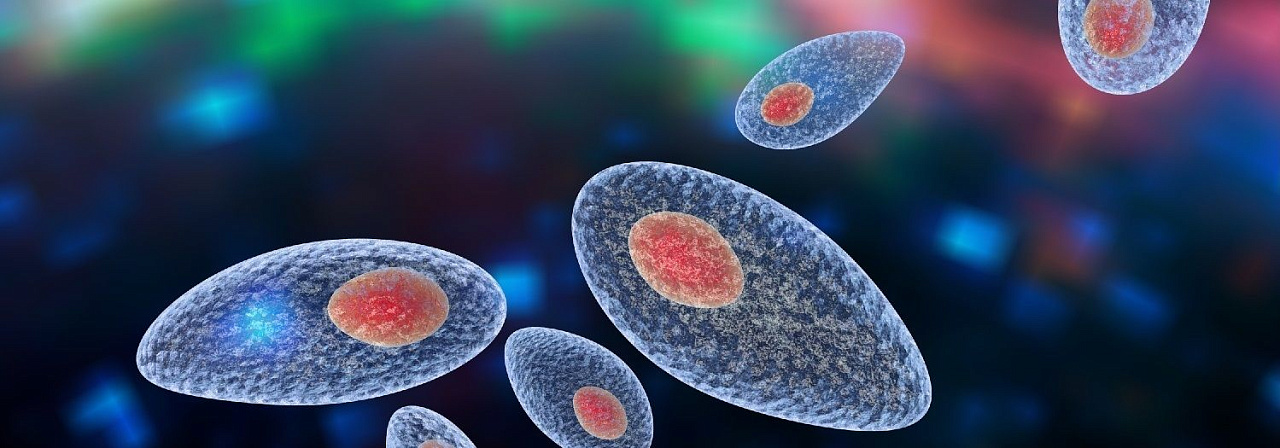
Актуальность проблемы токсоплазмоза определяется высокой инфицированностью населения паразитом Toxoplasma gondii. Распространенность токсоплазмоза широко варьирует в зависимости от особенностей питания в тех или иных странах. Так, во Франции более 70 % женщин заражаются токсоплазмой до беременности и приобретают иммунитет еще до зачатия. Несмотря на это, подсчитано, что во Франции 1 из 140 женщин заболевает токсоплазмозом во время беременности, тогда как в Великобритании эта величина значительно ниже и составляет 1:400 женщин.
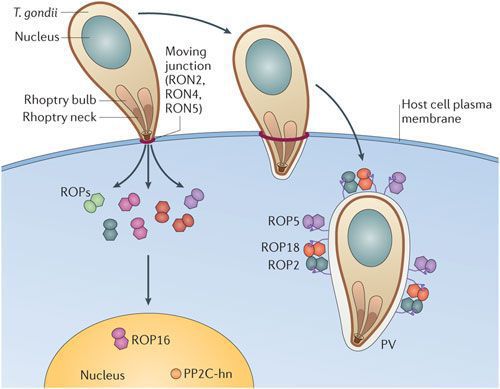
Токсоплазма является внутриклеточным паразитом из класса Sporozoa, основным хозяином которого являются животные семейства кошачьих. В эпителии кишечника кошек происходит половое размножение паразита с образованием ооцист, которые в острую фазу инфекции выделяются с испражнениями и длительно сохраняются в почве. Алиментарным путем ооцисты попадают в кишечник промежуточных хозяев - травоядных и плотоядных животных, в том числе и человека. В результате неполового деления образуется тахизоит - паразит размером 4-7 мкм, способный мигрировать и размножаться в клетках различных органов (ЦНС, лимфоидных, мышечных и др.), где быстро формируются псевдоцисты и цисты. В цистах паразит в форме брадизоита может находиться пожизненно в состоянии vita minima, активизируясь в случае значительного снижения иммунитета.
Патогенез (что происходит?) во время Токсоплазмоза у беременных:
Клеточный и гуморальный иммунитет обеспечивает надежную и пожизненную защиту от повторного инфицирования и активации брадизоитов, находящихся в цисте. Иммуногенез, в частности непрерывная продукция антител, индуцируется за счет контакта клеток иммунной системы с цистными антигенами паразита, такой иммунитет называется нестерильным. Состояние клеточного звена иммунитета учитывают только при манифестных формах заболевания.
Человек заражается тканевыми цистами при употреблении полусырого мяса или ооцистами - при употреблении немытых овощей либо непосредственно от кошек. Возможна трансплацентарная передача инфекции. До 80 % населения инфицированы токсоплазмами, они находятся в стадии латентной токсоплазменной инфекции. Риск инфекции в течение 9 мес беременности для серонегативных женщин составляет примерно 1 %.
Имеются 4 пути заражения человека токсоплазмозом.
- Прием через рот цист в мясе и колбасных изделиях, не подвергнутых достаточной термической обработке.
- Пероральное поступление ооцист в организм через продукты питания (например, салат), воду, а также через предметы и почву, которые загрязнены кошачьим калом (например, во время работы в саду); заразным кошачий кал становится только на 3-й день после экстракорпорального созревания.
- Трансплацентарная передача плоду во время острой токсоплазменной инфекции у будущей матери.
- Трансплантация органов и гемотрансфузии. Повреждение клетки паразитом приводит к ограниченному и/или генерализованному воспалению: лимфадениту, энцефалиту, гепатиту, миозиту, миокардиту. Выраженность воспалительных изменений бывает разной и, как правило, незначительной, но во всех случаях преобладает некроз с последующим фиброзом и кальцинацией ткани. В период острого процесса и цитолиза свободные формы (тахизоиты) находятся вне клеток, циркулируют в жидких средах организма, где атакуются фагоцитами с последующей быстрой элиминацией из крови.
Инфицирование и паразитемия в большинстве случаев бессимптомны, и только примерно у 10 % инфицированных людей отмечается малосимптомная картина заболевания: головная боль, небольшая лихорадка, локальный лимфаденит, легкий миозит. В редких, более тяжелых, случаях заболевание сопровождается генерализованной лимфаденопатией, пятнистой сыпью, мигрирующей артралгией и гепатоспленомегалией. Тяжелые варианты заболевания (миокардит, пневмония, увеит, хориоретинит) встречаются только у взрослых с иммунодефицитами и внутриутробно инфицированных детей.
Риск инфицирования плода значителен при первичном инфицировании беременной паразитом. Иммунитет женщины, инфицированной до беременности, надежно предохраняет плод при повторных контактах с токсоплазмой в случае возможной реинфекции в период беременности, за исключением редко встречающихся иммунодефицитных состояний. Число неиммунных беременных в России составляет 60-70 %. Во время беременности инфицируется около 11% женщин, которые в 30-40 % случаев передают инфекцию плоду. Таким образом, инфицируется 1 из 1000 плодов.
Для решения вопросов о профилактике и лечении токсоплазмоза плода и ребенка необходима своевременная диагностика инфицирования беременной, что возможно на основании результатов повторных серологических исследований, проведенных в определенные сроки беременности.
При заболевании в I и во II триместрах риск самопроизвольного аборта и преждевременных родов достигает 10-15 %. Риск врожденного токсоплазмоза и его тяжесть зависят от срока заражения беременной: чем раньше произошло заражение, тем меньше риск заболевания и больше выраженность проявлений. Так, при заражении матери в III триместре риск врожденного токсоплазмоза составляет 75-90 %, при этом у 90 % новорожденных заболевание протекает бессимптомно. При заражении же в I триместре риск врожденного токсоплазмоза всего 10-25 %, однако заболевание в 65 % случаев протекает в тяжелой форме. Если же женщина заразилась токсоплазмозом до беременности, то врожденный токсоплазмоз у ее будущего ребенка вообще маловероятен.
При внутриутробном заражении токсоплазмозом возможны смерть плода и преждевременные роды. Среди ранних проявлений врожденного токсоплазмоза следует отметить ЗВУР, микроцефалию, внутричерепные кальцификаты, гидроцефалию, хориоретинит, гепатоспленомегалию, желтуху и тромбоцитопению. Поздние проявления - задержка психического развития и эпилептические припадки. Лечение беременной снижает риск врожденного токсоплазмоза на 60 %.
При первичной инфекции у матери плод инфицируется или непосредственно, или косвенно от очагов токсоплазмоза в плаценте. После латентного периода инфекция может перейти от матери к плоду. Риск инфицирования и заболевания плода зависит от срока беременности. В ранние сроки беременности инфекция от матери к плоду переходит редко и медленно, в поздние сроки ребенок инфицируется быстрее и с более высокой вероятностью.
Только в редких случаях инфекция беременной ведет к инфицированию ребенка в I триместре. Хотя такие дети тяжело поражены, у них не отмечается аномалий закладки органов. Эмбриопатии, обусловленные токсоплазмой, у человека неизвестны, хотя имеются данные о токсическом нарушении эмбриогенеза в результате хорионита без непосредственного контакта паразита с эмбрионом. Для объяснения этого феномена есть две гипотезы: либо инфекция эмбриона ведет к выкидышу в ранние сроки, либо возбудитель переходит от матери к плоду из-за своего внутри-маточного латентного периода только после окончания периода эмбриогенеза и у ребенка есть возможность пережить инфекцию.
Симптомы Токсоплазмоза у беременных:
Заболевание часто протекает бессимптомно. Иногда по клиническому течению оно напоминает инфекционный мононуклеоз с появлением атипичных лимфоцитов в мазке крови и крайне редко приводит к скоротечно текущему пневмониту или летальному энцефаломиелиту. Как при врожденном, так и при приобретенном токсоплазмозе возможно поражение глаз в виде хориоретинита. Инфицирование детей и взрослых с недостаточностью иммунитета может вызвать генерализованный или локальный процесс с необратимыми последствиями. При ВИЧ-инфекции по мере нарастания иммунодефицита возможна реактивация токсоплазмоза, проявляющаяся множественными абсцессами головного мозга.
Размножение возбудителя ведет к воспалительным реакциям с некрозом и обызвествлением тканей. В более ранний период фетального развития при недостаточной собственной иммунокомпетентности ребенка или при массивной инфекции возможно очень сильное размножение возбудителя в плоде с гидроцефалией, асцитом, гепатозом. С тропизмом паразита к ЦНС связаны поражения мозга (менингоэнцефалит) и глаз (хориоретинит). Возможны генерализованный токсоплазмоз и поражение отдельных паренхиматозных органов (гепатит, миокардит). Если воспалительный процесс не приводит к выкидышу, то при рождении наблюдают остаточные явления: фиброзно-склеротические изменения в органах с их деформацией и нарушением функции - так называемые ложные пороки развития.
Поздняя фетопатия может проявляться широким спектром клинических признаков - от легких до крайне тяжелых вариантов. Клинически выраженные формы характеризуются лихорадкой, лимфаденитом, гепатоспленомегалией, желтухой, судорогами, анемией, тромбоцитопенией, экзантемой. Есть данные, что бессимптомные и субклинические формы также не проходят бесследно: у ряда детей спустя годы находят неврологические отклонения, последствия хориоретинита, глухоту, отставание в психическом развитии.
Диагностика Токсоплазмоза у беременных:
Если в крови беременной выявлены IgM-антитела, то это могут быть следующие ситуации:
- острая или недавно перенесенная инфекция, значимая для беременности;
- подъем специфических IgM-антител из-за нового интестинального контакта с токсоплазмой (локальная реинфекция?) или клинически значимое реактивирование;
- неспецифическая IgM-реакция (так называемые естественные IgM-антитела к токсоплазменным антигенам).
Нельзя оценивать позитивный IgM-тест при первом исследовании беременной без дальнейшего отбора признаков значимой для беременности инфекции. IgM-антитела персистируют, как правило, год, а часто даже 2-3 года. В каждом подобном случае необходимо исследование парных сывороток.
При сонографических данных, позволяющих предположить повреждение ребенка при токсоплазмозе в случае острой токсоплазменной инфекции у беременной, рекомендуется пренатальная диагностика. В большинстве случаев имеется относительное показание: при острой токсоплазменной инфекции у матери необходимо выяснить, не перешла ли инфекция на ребенка с нормальными данными сонографического исследования. При амниоцентезе исследуют околоплодные воды, при кордоцентезе - кровь.
Со времени инфицирования до момента исследования должно пройти не менее 4 нед (срок определяют по серологическим данным), потому что при более ранней пункции возбудитель, возможно, еще не достиг околоплодных вод и вероятен ложнонегативный результат. Пункцию делают не ранее 16 нед беременности. Нельзя до исследования проводить сочетанную терапию пириметамином и сульфадиазином, иначе возможны ложнонегативные результаты ПЦР. Если выявлена фетальная инфекция и одновременно имеются сонографические признаки повреждения у ребенка, с родителями следует обсудить возможность прерывания беременности. Если беременность без заметных отклонений со стороны плода не прервана, то проводят курсы терапии до родов и в течение первых 12 мес жизни ребенка (четырехнедельная комбинированная терапия пириметамином, сульфадиазином и фолиевой кислотой попеременно с четырехнедельной терапией ровамицином). После родов исследуют пуповинную кровь, плаценту методом ПЦР и сравнивают серологические пробы матери и ребенка.
Основные положения пренатальной диагностики токсоплазмоза следующие.
- Пренатальная диагностика необходима в следующих ситуациях:
- абсолютное показание: в случае острой токсоплазменной инфекции у беременной и данных УЗИ, позволяющих предположить повреждение плода;
- относительное показание: при острой токсоплазменной инфекции у беременной и "нормальных" данных УЗИ плода.
- со времени инфицирования до момента исследования должно пройти не менее 4 нед (для уменьшения количества ложноотрицательных результатов);
- амниоцентез проводят не ранее 16 нед беременности;
- нельзя до исследования проводить сочетанную терапию пириметамином и сульфадиазином (для уменьшения количества ложноотрицательных результатов).
Лечение Токсоплазмоза у беременных:
Лечение токсоплазмоза эффективно в периоды циркуляции в крови внецистных форм паразита, внутриклеточного деления тахизоитов с последующей паразитемией при остром и персистирующем процессе; на цистные формы (брадизоиты) препараты не действуют. В полной санации от паразита нет необходимости, так как цистные формы (носительство) обеспечивают нормальный нестерильный иммунитет.
Наиболее эффективны препараты пириметамина в комбинации с сульфаниламидами. Препараты блокируют функцию ферментов (редуктазы и синтетазы), участвующих в синтезе фолиевой кислоты паразита. Побочные действия всех антифолатов устраняют назначением фолиевой кислоты. На втором месте по эффективности стоят макролиды, тормозящие синтез белка на рибосомах возбудителя, учитывают также их меньшую токсичность и действие на внутриклеточные формы паразита.
При латентном токсоплазмозе (положительные результаты серологических проб в отсутствие клинических проявлений) лечение не проводят. Хотя при заражении в I триместре беременности риск врожденного токсоплазмоза невысок, в связи с возможностью тяжелого поражения плода показано прерывание беременности. Индивидуально решаются вопросы о прерывании беременности и предупреждении больной о потенциальной опасности химиотерапии, а также получения от нее письменного согласия на такое лечение.
В случае настойчивого желания женщины пролонгировать беременность в I триместре необходима терапия спирамицином. Начиная со II триместра при остром токсоплазмозе назначают пириметамин в сочетании с сульфаниламидами и чередуют их с курсами спирамицина. Терапию проводят до окончания беременности. В III триместре сульфаниламиды отменяют за 2 нед до предполагаемых родов во избежание конкурентозависимой гипербилирубинемии. Для устранения побочного действия пириметамина и сульфаниламидов (подавление функции костного мозга) назначают фолиевую кислоту до 5 мг/сут.
Схема лечения острого токсоплазмоза во время беременности следующая.
- С момента установления диагноза и до 15 нед: ровамицин 9 000000 ME в сутки.
- С 16 до 36 нед независимо от предшествующей терапии ровамицином проводят 4-недель-ную комбинированную терапию фолиевой кислоты: сульфаниламиды 4 г (по 1 г 4 раза в день), пириметамин - 1-й день 50 мг, затем 25 мг в день, лейковорин по 10-15 мг в день.
- С 36 нед и до конца беременности из-за опасности гемолиза и желтухи у новорожденного сульфадиазин заменяют ровамицином.
- Необходим еженедельный контроль клинического анализа крови и общего анализа мочи.
- Новорожденного обследуют (серология, клинические данные), при подтверждении врожденного токсоплазмоза проводят терапию чередующимися 4-недельными курсами под контролем неонатолога, офтальмолога, невропатолога, инфекциониста.
Профилактика Токсоплазмоза у беременных:
Профилактику внутриутробного токсоплазмоза следует проводить с учетом того факта, что только первичное заражение женщины во время беременности может привести к инфицированию плода. Методы профилактики подразделяют на санитарные и специальные методы. Первые включают информацию о соблюдении следующих правил: не пробовать сырой фарш, употреблять только термически хорошо обработанное мясо, тщательно вымытые фрукты, овощи, зелень, санировать кошачьи испражнения, следить за чистотой рук, работая в саду.
Специальные методы состоят в обследовании с использованием диагностического алгоритма всех женщин перед беременностью и во время беременности. При первом обращении беременной к врачу исследуют титр антител к Toxoplasma gondii. При положительном результате в том же образце сыворотки определяют содержание специфических IgM для исключения острой инфекции. При их обнаружении назначают лечение или рекомендуют прервать беременность. В отсутствие специфических антител обследование повторяют на 10-12-й неделе и 20-22-й неделе, так как серонегативные беременные будут составлять группу риска по острому токсоплазмозу.
За инфицированными, но "практически здоровыми детьми", родившимися от матерей с точно установленным первичным инфицированием во время беременности, необходимо диспансерное наблюдение до 10-летнего возраста, включающее регулярное клинико-лабораторное обследование для выявления возможной трансформации инфицирования в заболевание.
Основные положения профилактики врожденного токсоплазмоза следующие.
- Первичная профилактика - просвещение серонегативных по токсоплазмозу беременных:
- хорошая термическая обработка мяса и мясных изделий;
- тщательная обработка кипяченой водой салатов и фруктов;
- если у беременной дома есть кошка, необходимо применять консервированный или сухой корм, кошку держать в квартире, ящик для кала ежедневно чистить и ошпаривать кипятком;
- при припухании лимфатических узлов или жалобах, напоминающих грипп, для уточнения симптомов немедленно обратиться к врачу.
К каким докторам следует обращаться если у Вас Токсоплазмоз у беременных:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Токсоплазмоза у беременных, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
![Александров Павел Андреевич, инфекционист, гепатолог, паразитолог, детский инфекционист - Санкт-Петербург]()
Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
![Внутриутробное инфицирование токсоплазмами]()
Этиология
Таксономия:
Вид — Toxoplasma gondii
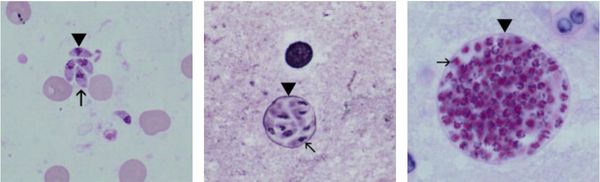
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
![Формы существования токсоплазмы]()
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
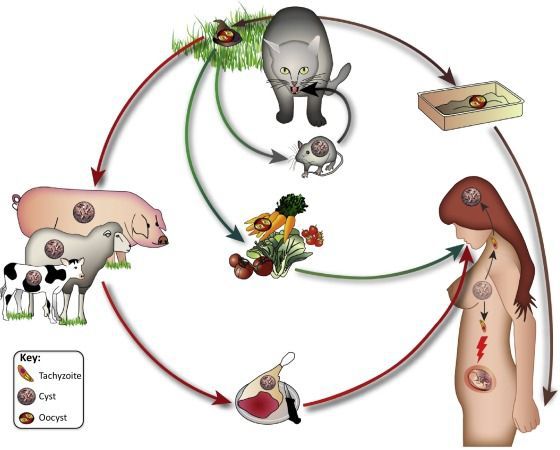
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
![Пути передачи токсоплазмоза]()
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
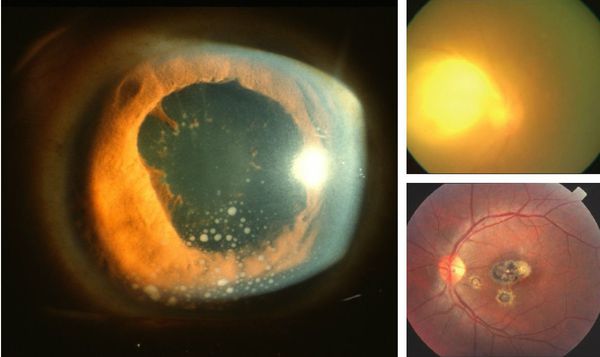
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
![Глазной токсоплазмоз]()
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
![Проникновение трофозоита в клетку]()
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым - 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода "двойной сэндвич" или "иммунозахват" IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
-
(ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови; — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
![Токсоплазмоз]()
Токсоплазмоз — это заболевание человека, вызванное микроскопическим одноклеточным паразитом Toxoplasma gondii. Отличается большим разнообразием клинических проявлений, в основном поражает:
- Нервную систему.
- Глаза.
- Скелетные и сердечную мышцы.
- Лимфатическую систему.
Возбудитель очень распространен в природе, его переносят несколько сотен видов животных и птиц, в том числе – домашних. Паразит легко проникает в организм, но часто не приводит к развитию острой инфекции. Заболевание обычно развивается у людей со сниженной иммунной реакцией – больных СПИДом и другими иммунодефицитными состояниями, при приеме иммуносупрессоров.
Возбудители заболевания, его источники
Наиболее опасным является внутриутробное инфицирование, которое нередко заканчивается выкидышем либо тяжелыми врожденными патологиями. По этой причине анализ на токсоплазмоз должен обязательно проводится при подготовке к беременности и вынашиванию ребенка.
По статистическим данным токсоплазма обнаруживается у 25-80% населения планеты. В отдельных регионах степень заражения достигает 95%.
![]()
Токсоплазма – внутриклеточный паразитический организм, который способен существовать в трех формах:
- Тахиозоиты. Имеют форму полумесяца и размер 2-4 мкм. Характерная особенность – при специальной окраске (по Романовскому-Гимзе) ядро приобретает красный цвет, а цитоплазма становится серо-голубой. В этой форме паразит проникает в клетки иммунной системы (макрофаги, фагоциты), в которых быстро размножается. После гибели клетки тахиозоиты высвобождаются и заражают здоровых макрофагов.
- Брадиозоиты (псевдоцисты). Это защитная форма токсоплазмы, в которой происходит большая часть жизнедеятельности возбудителя при нормальной иммунной реакции со стороны зараженного организма. Форма клетки брадиозоитов удлиненная, ядро смещено к одному из окончаний. Токсоплазмы в этой форме часто формируют тканевые псевдоцисты состоящие из множества клеток паразиты покрытых общей защитной оболочкой.
- Ооцисты. Эта форма токсоплазмы встречается только в эпителиальных клетках кишечника домашней кошки и ее диких родственников. Образуется в результате полового размножения паразита внутри клеток животного. Затем незрелые ооцисты выделяются в окружающую среду вместе с фекалиями. При достаточной температуре и притоке свежего кислорода ооцисты созревают в течение 2-7 дней. После завершения созревания ооцисты становятся способны заражать промежуточных хозяев токсоплазмы, в том числе – людей.
Основным источником заражения являются представители семейства кошачьих, в подавляющем большинстве – домашняя кошка. Механизм передачи паразита – фекально-оральный. Реализуется за счет:
- Употребления недостаточно термически обработанных мясных продуктов (особенно свинины и баранины).
- Через плохо вымытые овощи, зелень, фрукты.
- Несоблюдение правил личной гигиены (немытые руки).
Изредка возможно прямое заражение токсоплазмой через микроповреждения кожных покровов. От матери к ребенку паразит передается редко. В среднем одно заражение на 2-3,5 тыс. беременных. Наиболее вероятно инфицирование плода токсоплазмой если в процессе вынашивания организм беременной впервые столкнулся с паразитом.
Восприимчивость к токсоплазме крайне высока, для заражения достаточно единичных ооцист. Наиболее восприимчивы молодые люди, у пожилых (после 60 лет) паразит выявляется значительно реже.
![]()
Приобретенный токсоплазмоз, симптомы
![]()
Явные клинические симптомы у большей части заразившихся отсутствуют, болезнь сразу переходит в латентную фазу носительства. Инкубационный период составляет от 1 до 3 недель.
При проявлении выраженной клинической картины симптоматика нарастает медленно. Обычно болезнь начинается бессимптомно с увеличения региональных лимфатических узлов (паховых, подмышечных, шейных). Лимфоузлы эластичны, безболезненны, больные в этот период не предъявляют никаких жалоб.
После первой недели развития инфекционного процесса происходит увеличение селезенки и печени. Могут возникать ноющие боли в крупных мышечных группах нижних и верхних конечностей. У каждого пятого в этот период развивается хориоретинит проявляющийся в выпадении участков поля зрения.
Начиная со второй недели симптоматика поражения ЖКТ начинает затухать. Уменьшаются и быстро исчезают симптомы энтерита, снижается общая интоксикация организма. Одновременно развивается поражение:
- Опорно-двигательной системы. Усиливается болевой синдром в конечностях, суставах, возможно нарушение подвижности и мелкой моторики.
- Ретикулоэндотелиальной. Проявляется гепатолиенальным синдромом, мезаденитом.
- Сердечно-сосудистой. Нередко развиваются нарушения ритма сердечных сокращений, симптомы миокардита либо перикардита.
На 3-4 неделе заболевание завершается затуханием всех проявлений и переходом токсоплазмоза в бессимптомное носительство. При воздействии негативных факторов, ослабляющих иммунитет возможна манифестация заболевания с развитием вышеописанной клинической картины, которая снова переходит в латентную фазу.
Частые рецидивы острой формы токсоплазмоза, особенно на фоне иммуноподавляющих факторов, могут приводить к серьезным осложнениям. Чаще встречаются:
- Миокардиодистрофия.
- Психоневрологические патологии.
- Снижение интеллекта.
- Атрофия зрительного нерва вплоть до полной слепоты.
- Синдром хронической усталости.
Острый токсоплазмоз у женщин может приводит к нарушению менструального цикла, выкидышам и другим патологиям со стороны половой системы.
Хронический приобретенный токсоплазмоз – достаточно редкое явление, считается СПИД-ассоциированной формой заболевания. Протекает с периодическими обострениями, часто развиваются осложнения со стороны ЦНС в виде энцефалитов и поражения органов зрения.
Наиболее тяжелое следствие хронического токсоплазмоза – генерализованная инфекция в ходе которой быстро развивается полиорганная недостаточность, иногда данное осложнение завершается смертью больного.
Врожденный токсоплазмоз, возникающий при беременности
![]()
Возникает при проникновении паразита через плацентарный барьер и заражении плода. В большинстве случаев происходит при первичном заражении во время беременности, реже – при рецидиве токсоплазмоза связанном со снижением иммунитета. Основная группа риска – женщины, которые не были заражены токсоплазмой до наступления беременности. Если в результате контакта с возбудителем произойдет манифестация заболевания в процессе вынашивания плода – достаточно высока вероятность развития врожденного токсоплазмоза.
Процент выживаемости детей при внутриутробном инфицировании зависит от срока, на котором оно произошло:
- При инфицировании на первом триместре шанс на выживание плода – 15%
- На втором – 30%.
- На третьем – 60%
Даже если беременность успешно завершается, сохраняется крайне высокая степень развития врожденных патологий и врожденного токсоплазмоза. Болезнь протекает тяжело, особенно если инфицирование произошло на ранних сроках. Развивается характерная тетрада патологигй:
- Гидроцефалия.
- Двусторонний ретинохороидит.
- Задержка психофизического развития.
- Церебральные кальцификаты.
Прогноз в случае врожденного токсоплазмоза неблагоприятный, в большинстве случаев болезнь завершается смертью новорожденного либо тяжелой инвалидизацией. Даже если после внутриутробного заражения острая клиническая картина не возникла такие дети находятся в группе риска развития:
- Умственной недостаточности.
- Эпилепсии.
Возможно развития многих других патологий, которые проявляются спустя месяцы и годы после рождения. По этой причине острая форма токсоплазмоза, возникшая во время беременности – показание к проведению аборта даже на поздних сроках. При беременности необходимо сдавать массу анализов, которые помогают выявить наличие не только токсоплазмоза, но и ЦМВ-инфекции.
Показания к обследованию
Анализ чаще всего назначают в двух случаях:
- При планировании беременности в составе стандартного пакета лабораторной диагностики TORCH-инфекции.
- При подозрении на токсоплазмоз и определенных симптомах.
Также лабораторная диагностика используется при выявлении симптомов острого токсоплазмоза у взрослых либо детей.
В общей врачебной практике данный анализ назначают в случае проявления у пациентов специфических симптомов (нарушение зрения, судороги) а также ВИЧ-инфицированным.
Дифференциальная диагностика
Проводится с болезнями, симптомы которых схожи с острой и хронической формой токсоплазменной инфекции. В их число входят:
- Инфекционный мононуклеаз.
- Микоплазмоз.
- Хламидиоз.
- Цитомегалия.
- Туберкулез.
Также необходимо исключить онкологические патологии и системные заболевания (ревматизм, лимфогранулематоз). Окончательный диагноз устанавливается после получения результатов специфичных серологических исследований и ПЦР. Существует достаточно много лабораторных методик обнаружения специфических антител к токсоплазме. В их число входят:
- ИФА. Иммуноферментный анализ.
- РНИФ. Реакция непрямой иммунофлюоресценции. Становится позитивной с первой недели заболевания. Высокий титр антител может сохранятся до 15 лет.
- РСК. Реакция связывания комплемента. Становится положительной с 10-14 дня развития болезни, сохраняется на протяжении 2-3 лет.
Материал для исследования
![]()
Для обнаружения специфических антител к токсоплазме производится забор крови из вены, особой подготовки процедура не требует. Для проведения ПЦР-реакции подходит любой биологический материал – кровь, слюна, образцы тканей, другие биологические жидкости (ликвор, моча).
Если возникает потребность в диагностике токсоплазмоза у плода возможен забор крови из пупочного канатика. Процедура назначается редко потому что связана с высоким риском осложнений и преждевременного прерывания беременности. Более щадящая методика – взятие на анализ околоплодной жидкости путем пункции. Эти методики применяют в случае, когда результаты специфических анализов беременной с подозрением на токсоплазмоз не дают достаточной ясности диагноза.
Показания к применению различных лабораторных исследований и особенности интерпретации результатов у разных категорий обследуемых
В зависимости от категории пациента (возрастной группы, группы риска) показано применения различных наборов методик диагностики. Особенно важен правильный выбор диагностических методов в случае подозрений на токсоплазмоз у беременных женщин.
Обследование на токсоплазмоз при беременности
Если в процессе беременности у беременной выявлены симптомы которые могут свидетельствовать о развитии острого токсоплазмоза необходимо при помощи серологических методов установить уровень специфических иммуноглобулинов.
Для выявления острой стадии заболевания лучше всего подходит иммуноферментный метод (ИФА). Он наиболее точно показывает концентрацию IgM, повышение уровня которого свидетельствует о протекающем, либо недавно присутствовавшем остром токсоплазмозе.
![]()
Определение уровней IgG менее информативно так как эти антитела сохраняются долгое время после перенесенной инфекции и свидетельствуют скорее о носительстве, чем о недавнем заражении либо обострении. Женщины, перенесшие инфицирование токсоплазмой до беременности застрахованы от заражения плода и не входят в группу риска.
Также важно получение иммунологической картины в динамике, для чего специфические тесты проводятся не реже 1 раза в 2 недели. Изучение динамики изменений титров антител позволяют с большей точностью установить диагноз.
Нужно учитывать, что серологическая картина, свидетельствующая об инфицировании токсоплазмой не является 100% показанием для прерывания беременности. В этом случае потребуется проведение дополнительных анализов путем взятия крови плода из пупочного канатика и образцов амниотической жидкости пункционным методом.
Обследование новорожденных детей и детей раннего возраста
Направлено на раннее обнаружение возбудителя, до начала острой фазы врожденного токсоплазмоза и развития тяжелых осложнений. Назначается, когда есть подозрение на инфицирование токсоплазмой, включает в себя следующие тесты:
- Выделение паразита путем внесения материала из плаценты и пупочного канатика в живых мышей.
- Проведение ПЦР-анализа амниотической и люмбальной жидкостей.
- Компьютерная томография либо МРТ головы. Позволяет выявить на ранних стадиях специфические изменения в головном мозге, например, гидроцефалию.
Серологические методики также применяются, но они дают только дополнительную информацию. Иммунная система новорожденного недостаточно активна, часто неспособна выработать достаточно высокий титр специфических антител.
Обследование больных ВИЧ-инфекцией
Диагностика заключается в регулярном отслеживании титров иммуноглобулинов G серологическими методами. Титрование иммуноглобулинов M неинформативно так как у большинства ВИЧ-позитивных уровень антител этой группы крайне вариабелен.
В прямом выявлении возбудителя путем микроскопии образцов ткани либо заражения лабораторных животных как правило необходимости нет. Диагноз достаточно точно можно установить за счет серологической диагностики и наличия специфической клиники токсоплазмоза. У ВИЧ-позитивных больных она более выражена, что значительно упрощает постановку диагноза.
Обследование в Медарт
![]()
На базе медицинского центра Медарт выполняется полный комплекс серологических анализов для выявления токсоплазмы в организме пациента. Иммунологическое исследование с целью выявления специфических иммуноглобулинов входит в состав комплексных тестов ЗППП, предназначенных для пар, планирующих рождение ребенка. Возможно выполнения забора крови и других биологических жидкостей для установления наличия токсоплазмы и уточнения клинической картины протекания заболевания.
Высокоточное современное оборудование позволяет в кратчайшие сроки получить точные результаты исследований.
Преимущества медицинского центра Медарт:
- Квалифицированные специалисты.
- Возможность быстро получить точный результат исследования.
- Доступная стоимость.
На базе медцентра предоставляется полный комплекс услуг, от предварительного приема и консультаций до постановки и уточнения диагноза и назначения эффективных схем лечения и профилактики токсоплазмоза и других заболеваний.
Токсоплазмоз у детей является врожденным (при внутриутробном заражение) или приобретенным заболеванием, вызванным паразитами, для которого характерно хроническое течение, поражение ЦНС, миокарда, органов ретикулоэндотелиальной системы*, мышц, глаз.
*Ретикулоэндотелиальная система или система макрофагов — это вид клеток, рассеянных в разных отделах человеческого организма, несущих барьерную (защита от инфицирования) и фагоцитарную (уничтожение патогенных микроорганизмов) функцию и функцию обмена веществ. Больше всего таких клеток сконцентрировано в селезенке, лимфатических узлах и костном мозге.
Что провоцирует / Причины Токсоплазмоза у детей:
Возбудитель заболевания – простейший паразит Toxoplasma gondii семейства трипаносомид. Данный паразит существует в 3 формах: трофозоиты, цисты и ооцисты. Размножение трофозоитов происходит внутриклеточно во всех клетках животных, и обнаруживается в тканях на острой стадии инфекции. Цисты основываются в организме хозяина, создавая собственную оболочку. Они могут сохраняться долгие годы в организме. Большая часть их задерживается в миокарде, скелетных мышцах, ЦНС. Ооцисты поселяются в слизистой оболочке тонкой кишки кошек и выделяются с испражнениями. Ооцисты в благоприятной среде сохраняются до 1 года и более, именно они влияют на передачу инфекции.
![токсоплазмоз]()
Источниками заражения человека являются животные и птицы. Паразитируя в организме животного, через испражнения токсоплазма попадает во внешнюю среду, становясь причиной инфицирования других животных и людей. Инфицироваться можно через:
- зараженную землю – песочница, кошачий туалет, пикник в парке и прочее;
- грязные фрукты и овощи, находившиеся в непосредственном контакте с инфицированной средой;
- мясные и молочные продукты, содержащие цисты, не прошедшие термическую обработку;
- внутриутробное заражение. Паразит попадает через плаценту и поражает плод, провоцируя тяжелые заболевания мозга и глаз у ребенка. В случае заражения женщины в первом триместре беременности вероятность врожденного токсоплазмоза возрастает до 15-20 %. Беременность протекает в тяжелой форме. Заражение в третьем триместре отражается на детях в 65%. В случае инфицирования женщины до зачатия, за 6 месяцев и более, внутриутробного влияния на плод не будет, а если заражение произошло в период планирования ребенка, непосредственно перед наступлением беременности, появляется риск инфицирования ребенка;
- при переливании крови, если донор болен токсоплазмозом.
Патогенез (что происходит?) во время Токсоплазмоза у детей:
Токсоплазма проникает в организм, далее попадает в лимфоузлы, вызывая их гиперплазию и воспалительно-гранулематозный процесс. Для острой стадии главный симптом – увеличение лимфоузлов. Далее токсоплазмы перемещаются в кровь, которая разносит их по организму, после чего паразиты поселяются в органах и тканях – селезенка, скелетные мышцы, печень, ЦНС, сердце и т.д. В этих органах образуются воспалительные очаги паразитов – цисты, сохраняющиеся на протяжении длительного времени, иногда даже пожизненно, также образуются очаги некроза, приводящие к отложению соли кальция, таким образом, появляются кальцинаты. Для острой формы токсоплазмоза в организме характерно наличие тахизоиты, для случаев подострого и хронического течения – образование цист (наибольшее их количество находят в мышцах и головном мозге). Внутриутробное заражение при гематогенном инфицировании плода приводит к различным повреждениям зависимо от срока беременности и массивности инвазии. В случае инфицирования в первом триместре беременности возникает тяжелый генерализованный процесс, последствиями которого могут стать гибель плода, мертворождение, выкидыши или рождение ребенка с хроническим врожденным заболеванием. Если женщина заразилась на поздних сроках беременности, то у её ребенка наблюдается острая форма токсоплазмоза, поражающая, гепатолиенальную систему и поперечно-полосатую мускулатуру.
Различают нижеприведенные формы врожденного токсоплазмоза у детей:
- Острый врожденный токсоплазмоз. Проявляется симптомами: повышенная температура тела, увеличение печени и селезенки, желтуха, пневмония, миокардит; возможным осложнением является геморрагический синдром.
- Подострый врожденный токсоплазмоз: проявляется симптомом менингоэнцефалита.
- Хронический врожденный токсоплазмоз. Характерны крайне тяжелое течение, различные дефекты развития, выраженные дегенеративные изменения ЦНС с кальцификатами головного мозга. Осложнениями токсоплазмоза ЦНС являются задержка психомоторного развития, эпилептический синдром, глухота, слепота.
Симптомы Токсоплазмоза у детей:
Обе формы токсоплазмоза, как врожденная, так и приобретенная переходят в острое заболевание. У новорожденных наблюдается выраженная интоксикация, лихорадка, озноб, слабость, помутнение хрусталика, развитие косоглазия, пневмония, изменения формы и состояния внутренних органов, нервной системы, экзантема. У детей появляются элементы сыпи, которые состоят из небольших пятен розовой или красной окраски. Сыть обильно выражается на конечностях, внизу живота, её длительность до 2 недель, клонические и тонические судороги, паралич конечностей. Повышенный показатель давления ликвора указывает на токсоплазмоз. Заболевание развивается и прогрессирует, что может привести к летальному исходу в первые 2 недели жизни ребенка.
Диагностика Токсоплазмоза у детей:
В случае подозрения у новорожденного токсоплазмоза необходимо провести комплексное исследование слуховой, зрительной и нервной систем. Для диагностирования заболевания проводится микроскопия возбудителя (проверяется кровь, спинномозговая жидкость, плодные оболочки, пунктат лимфоузлов). Электронная микроскопия позволяет выявить возбудителя в тканях мозга.
Для диагностики также применяются следующие способы:
- Иммунофлюоресценция. Выявление титров IgM. Наличие IgM у новорожденного свидетельствует об инфицировании. IgM определяют через 2 недели после рождения или инфицирования.
- Проба Сэбина-Фельдмана на окрашивание токсоплазм. Решающий тест при обследовании новорожденных. Для его проведения используются парные сыворотки, 4-кратное увеличение титров указывает на наличие острой инфекции.
- Кожная проба с токсоплазмином.
- МРТ головного мозга.
- Биопсия мозга и наличие паразитов в пероксидазно-антипероксидазном тесте.
- Если на ультрасонографии размер латеральных желудочков увеличен, это косвенно указывает на наличие инфекции.
Лечение Токсоплазмоза у детей:
Лечебная терапия токсоплазмоза у детей должна быть комплексной. Лечение может проходить как при беременности – матери и ребенка, так и после рождения малыша, но есть исключения. Беременным с положительными результатами внутрикожной пробы и анализов, но при отсутствии симптомов заболевания лечение не назначается. Беременным женщинам с хроническим токсоплазмозом назначается профилактическая иммунотерапия. Самая большая опасность для беременной скрывается в свежем инфицировании. В таком случае проводится 1-2 курса химиотерапии. Но препараты химиотерапии не рекомендованы для применения в первом триместре, так как большинство из них имеют тератогенное действие на плод (развитие уродств).
Основными препаратами в лечение принято считать антибиотики первого ряда – сулъфадиазин (сульфазин) и пириметамин (хлоридин). К альтернативному препарату относится спирамицин 3 г/сут в течение 3 нед. (при беременности). Клиндамицин 900-1200 мг 3 раза в день внутривенно. Глюкокортикоиды – при токсоплазмозе ЦНС, антибактериальные препараты резерва – азитромицин, кларитромицин.
Острый токсоплазмоз новорожденных и беременных (после 16 недель). Сульфадиазин 100-200 мг/кг в сутки (2-6 г/сут – взрослым) с пириметамином (хлоридин) 2 мг/кг в сутки в течение 3 дней, затем 1 мг/кг в сутки до 25 мг в сутки в течение 4 нед. (взрослым 200 мг в 1-й день, затем 25-50 мг в сутки на 4 нед.).
Профилактика Токсоплазмоза у детей:
Основной профилактикой токсоплазмоза у детей есть скрупулезное соблюдение правил гигиены: мытье рук по возвращению с прогулки, после игр с животными, особенно с кошками, перед приемом пищи. Беременные женщины не должны контактировать с объектами, представляющими потенциальную угрозу, чистка кошачьего туалета должна проводиться только в перчатках. Домашние животные должны проходить проверку на наличие у них антител к токсоплазмам. Для профилактики хронического врожденного токсоплазмоза назначают сульфадиазин 100 мг/кг ежедневно, пириметамин 1 мг/кг каждые 2 дня и лейковорин 5 мг/кг каждые 2 дня. Профилактическое лечение продолжают до 1 года. Для токсических эффектов назначают лейковорин (кальция фолинат) по 5 мг в сутки через день (женщинам по 10 мг в сутки). Поддерживающая терапия проводится сочетанием этих препаратов в течение 3-4 мес.
К каким докторам следует обращаться если у Вас Токсоплазмоз у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Токсоплазмоза у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Читайте также: