Новые технологии с больными туберкулезом
Обновлено: 24.04.2024
Для цитирования: Мишин В.Ю., Степанян И.Э. Контролируемая химиотерапия туберкулеза органов дыхания в современных условиях. Проблема лекарственной устойчивости. РМЖ. 2000;12:496.
Центральный НИИ туберкулеза РАМН,
кафедра туберкулеза Московского государственного медико-стоматологического университета
Этиотропная химиотерапия играет приоритетную роль среди методов лечения туберкулеза, к которым относятся также лечебно-охранительный режим, рациональное питание, патогенетическая терапия, коллапсотерапия, оперативное и санаторно-курортное лечение. Лечебный эффект противотуберкулезных препаратов основан на их бактериостатическом или бактерицидном действии в отношении микобактерий туберкулеза (МБТ), которое приводит к уменьшению бактериальной популяции в организме больного.
Группа препаратов, применяемых для лечения туберкулеза, весьма немногочисленна и включает разнородные химические соединения – антибиотики и химиотерапевтические средства.
Основными противотуберкулезными средствами на сегодня являются изониазид, рифампицин, стрептомицин, пиразинамид, этамбутол, тиоацетазон. Первые два из перечисленных препаратов обладают бактерицидным действием и способны быстро убивать большое количество активно размножающихся МБТ [1].
Противотуберкулезные препараты “второго ряда” – канамицин, амикацин, капреомицин; этионамид (протионамид); офлоксацин, ципрофлоксацин; циклосерин (теризидон); ПАСК – назначают в случаях, когда по каким-либо причинам невозможно использовать основные средства [2].
Полвека назад, вскоре после появления первых противотуберкулезных препаратов, продолжительность лечения была сравнительно небольшой (1– 3 мес), химиотерапия оказывала фантастический эффект, что позволило необоснованно считать проблему лечения туберкулеза решенной. Однако опыт, накопленный фтизиатрией в последующие десятилетия, показал, что после того, как интенсивное размножение бактериальной популяции подавлено в результате химиотерапии, продолжается персистирование части микобактерий, которые сохраняются, главным образом, внутриклеточно (внутри фагоцитов). Подавить жизнедеятельность этой части МБТ очень трудно, так как большинство химиопрепаратов не действуют на внутриклеточно расположенные микобактерии. Оказалось также, что при монотерапии (лечение одним противотуберкулезным препаратом), нерегулярном приеме лекарств быстро формируется лекарственная устойчивость МБТ.
Таким образом, было обосновано одновременное назначение больным нескольких противотуберкулезных средств, созданы новые химиопрепараты, продолжительность лечения постепенно увеличивалась и достигла 12–18 мес, что не всегда было оправдано. Было установлено, что низкая эффективность лечения туберкулеза в большей степени обусловлена нерегулярным приемом препаратов, чем недостаточной длительностью его. В течение последнего десятилетия по рекомендации ВОЗ во многих странах внедрили методику контролируемой краткосрочной химиотерапии (ДОТС), которая оказалась эффективной и позволила сократить длительность лечения до 6–9 мес за счет использования рациональных режимов химиотерапии.
Режимы химиотерапии
Понятие “режим химиотерапии” включает определенную комбинацию химиопрепаратов, их дозировку, способ использования в виде однократной суточной дозы или разделенной на 2–3 приема, путь введения (внутрь, внутривенно, в виде аэрозолей, эндобронхиальных вливаний, ректально) и ритм приема (ежедневно или прерывисто).
Интенсивность и длительность химиотерапии больного туберкулезом определяется наличием или отсутствием бактериовыделения, тяжестью и распространенностью легочного процесса, сведениями о предшествующем лечении. Учет указанных факторов позволяет отнести каждый случай заболевания к определенной категории (табл. 1).
Курс противотуберкулезной химиотерапии состоит из двух фаз. Назначение первой фазы – интенсивной – подавить размножение бактериальной популяции, добиться ее количественного уменьшения. Главной задачей второй фазы является предупреждение размножения оставшихся микобактерий.
В первой фазе химиотерапии впервые выявленным бациллярным больным назначают 4 основных противотуберкулезных препарата. Интенсивную химиотерапию проводят 2 мес, а при сохранении бактериовыделения по данным микроскопии мазка – 3 мес. Во второй фазе химиотерапии у впервые выявленных больных используют 2 препарата в течение 4 мес ежедневно или через день.
Впервые выявленным больным, лечившимся нерегулярно или прервавшим лечение, а также больным с рецидивом туберкулеза, в интенсивной фазе рекомендуется назначение 5 химиопрепаратов в течение 2 мес, затем в течение еще 1 месяца применяют 4 химиопрепарата (отменяется стрептомицин). Вторую фазу химиотерапии у этой категории больных рекомендуется проводить 3 противотуберкулезными препаратами в течение последующих 5 мес ежедневно или через день.
Больным, у которых при первоначальном исследовании мокроты не были выявлены МБТ, интенсивную фазу химиотерапии проводят тремя основными противотуберкулезными препаратами, после чего переходят на прием двух препаратов в течение 4 мес (см. табл. 1).
Больные хроническими формами туберкулеза легких должны лечиться по индивидуальным схемам химиотерапии с учетом устойчивости микобактерий к химиопрепаратам (табл. 2).
Эффективность проводимой химиотерапии оценивают по динамике клинических проявлений, бактериовыделения, рентгенологически выявляемых изменений в легких (уменьшению инфильтративных изменений в легких и закрытию каверн).
Обеспечение регулярного приема больным назначенных химиопрепаратов является важной задачей в течение всего периода лечения. В стационаре прием назначенных химиопрепаратов осуществляется под контролем медицинского персонала с точным учетом принятых медикаментов. В амбулаторных условиях прием химиопрепаратов осуществляется под контролем медицинского персонала в противотуберкулезных диспансерах либо на дому у больного. Контроль облегчается при применении всей суточной дозы в один прием, при интермиттирующем лечении.
Удобство контролируемой химиотерапии обеспечивается также применением комбинированных таблетированных форм, содержащих 2–4 основных химиопрепарата. Майрин содержит этамбутол, изониазид и рифампицин, в майрин П дополнительно включен пиразинамид. Рифакомб плюс, рифатер и трикокс включают изониазид, пиразинамид и рифампицин; рифинаг и тибитекс - изониазид и рифампицин. Их применение значительно облегчает контроль за химиотерапией, особенно в амбулаторных условиях. Нерегулярный прием химиопрепаратов может привести к развитию лекарственной устойчивости МБТ и прогрессированию процесса.
Часть больных в процессе лечения нуждается в изменении режима химиотерапии вследствие возникновения неустранимых побочных реакций на препараты, либо обнаружения лекарственной устойчивости, либо отсутствия эффекта от проводимой терапии, что чаще всего выражается продолжающимся бактериовыделением и сохранением каверны в легком. Режим химиотерапии целесообразно менять не позже, чем через 2–3 мес после начала лечения, поскольку к концу 3-го месяца уже имеются результаты количественного исследования мокроты методом микроскопии до начала лечения и в процессе химиотерапии; результаты посева мокроты, сделанного до начала лечения, с данными о чувствительности МБТ к химиопрепаратам; динамика рентгенологических изменений в легких. Своевременная коррекция химиотерапии значительно повышает ее эффективность, способствует более быстрому заживлению деструктивных изменений в легких. Индивидуализация лечебной тактики осуществляется на основании информации, полученной на протяжении всего периода химиотерапии.
Причины неэффективности лечения
Положительных результатов лечения удается достичь не у всех больных. Среди важнейших причин неэффективности лечения больных туберкулезом можно назвать побочное действие противотуберкулезных препаратов; заметное увеличение частоты остропрогрессирующих форм туберкулеза, протекающих на фоне выраженного иммунодефицита с развитием необратимых изменений в легких; сопутствующие туберкулезу заболевания; плохое обеспечение противотуберкулезными химиопрепаратами, отсутствие контроля за приемом лекарств, недисциплинированность больных и др. Однако наиболее важной причиной недостаточной эффективности химиотерапии остается лекарственная резистентность МБТ.
Лекарственная резистентность МБТ
Больные туберкулезом, выделяющие лекарственно-устойчивые штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих лекарственно-резистентными возбудителями. Чем больше число больных, выделяющих лекарственно-устойчивые МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной лекарственной устойчивостью.
По определению экспертов ВОЗ [2], лекарственно-устойчивый туберкулез – это случай туберкулеза легких с выделением МБТ, устойчивых к одному и более противотуберкулезным препаратам. В последние годы в связи с ухудшением эпидемической ситуации существенно увеличилось число больных, выделяющих МБТ, устойчивые к основным противотуберкулезным препаратам. По данным ЦНИИ туберкулеза РАМН, у 50% впервые выявленных и ранее не леченных противотуберкулезными препаратами больных в мокроте определялись лекарственно-устойчивые МБТ, из них у 27,7% имелась устойчивость к 2 основным противотуберкулезным препаратам – изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота выявления лекарственно-уcтойчивых МБТ возрастает до 95,5% [3].
Феномен лекарственной устойчивости МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является лекарственная устойчивость. В активно размножающейся бактериальной популяции всегда имеется некоторое количество лекарственно-устойчивых мутантов, которые практического значения не имеют, но по мере сокращения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством лекарственно-чувствительных и устойчивых МБТ [4]. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. В клинической практике необходимо исследовать лекарственную чувствительность МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких [3].
Методы обнаружения лекарственной устойчивости МБТ
Повышение эффективности лечения туберкулеза, вызванного лекарственно-устойчивыми МБТ, возможно за счет использования ускоренных методов обнаружения лекарственной устойчивости МБТ, что позволяет своевременно изменять режим химиотерапии, отменив препараты, к которым выявлена устойчивость МБТ, и назначить противотуберкулезные средства, к которым чувствительность сохранена.
Исследование лекарственной устойчивости МБТ непрямым методом осуществляют после получения культуры МБТ, выделенных от больного, что требует от 30 до 45 сут. Коррекция химиотерапии в таком случае носит отсроченный характер и проводится, как правило, уже на конечном этапе интенсивной фазы химиотерапии.
Лекарственную устойчивость МБТ в настоящее время определяют методом абсолютных концентраций, который основан на добавлении в плотную питательную среду Левенштейна–Йенсена стандартных концентраций противотуберкулезных препаратов, которые принято называть предельными. Для изониазида она составляет 1 мкг/мл, рифампицина – 40 мкг/мл, стрептомицина – 10 мкг/мл, этамбутола – 2 мкг/мл, канамицина – 30 мкг/мл, амикацина – 8 мкг/мл, протионамида (этионамида) – 30 мкг/мл, офлоксацина (таривида) – 5 мкг/мл, циклосерина – 30 мкг/мл и пиразинамида – 100 мкг/мл. Определение лекарственной устойчивости МБТ к пиразинамиду проводят на специально приготовленной яичной среде с рН 5,5–5,6. Культура МБТ считается устойчивой, если в пробирке выросло более 20 колоний.
В последнее время для ускоренного определения лекарственной устойчивости применялся радиометрический метод с использованием автоматической системы BACTEC – 460 TB (Becton Dickinson Diagnostic Systems, Sparks, MD), который позволяет выявлять лекарственную устойчивость МБТ на жидкой среде Middlebrook 7H10 через 8–10 дней.
Другая не менее важная задача – правильное лечение впервые выявленных больных туберкулезом легких с использованием комбинации из 4–5 основных противотуберкулезных препаратов до получения данных лекарственной устойчивости МБТ [1]. В этих случаях существенно повышается вероятность того, что даже при наличии первичной лекарственной устойчивости МБТ бактериостатическое действие окажут 2 или 3 химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии при лечении впервые выявленных больных и назначение им в большинстве случаев только 3 химиопрепаратов является грубой врачебной ошибкой, что, в конечном счете, ведет к формированию вторичной лекарственной устойчивости МБТ.
Наличие у больного туберкулезом легких лекарственно-резистентных МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и к летальным исходам. Особенно тяжело протекают поражения легких, вызванные полирезистентными МБТ, которые устойчивы как минимум к изониазиду и рифампицину, т.е. к основным и самым активным противотуберкулезным препаратам [4]. Множественная лекарственная устойчивость МБТ является на сегодня наиболее тяжелой формой бактериальной устойчивости, а специфические поражения легких, вызванные такими микобактериями, называются полирезистентным туберкулезом легких [2]. Лекарственная устойчивость МБТ имеет не только клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных обходится намного дороже, чем больных с МБТ, чувствительными к основным химиопрепаратам. Разработка лечения лекарственно-резистентного туберкулеза легких является одним из приоритетных направлений современной фтизиатрии.
Возможные режимы химиотерапии при выявлении лекарственной устойчивости МБТ больных с впервые выявленным деструктивным туберкулезом легких представлены в табл. 2.
Для проведения эффективной химиотерапии больных хроническими формами туберкулеза легких с множественной лекарственной устойчивостью МБТ используют комбинации резервных противотуберкулезных препаратов, включающие пиразинамид и этамбутол, к которым медленно и довольно редко формируется вторичная лекарственная устойчивость [4]. В табл. 2 представлены схемы химиотерапии для больных с множественной лекарственной устойчивостью МБТ, ранее длительно получавших противотуберкулезную терапию.
Все резервные препараты обладают довольно низкой бактериостатической активностью, поэтому общая длительность химиотерапии у больных с хроническим фиброзно-кавернозным туберкулезом легких и множественной лекарственной устойчивостью МБТ должна составлять не менее 21 мес.
При отсутствии эффекта от проводимой химиотерапии резервными противотуберкулезными препаратами возможно применение хирургических методов лечения, наложение лечебного искусственного пневмоторакса или пневмоперитонеума. Оперировать следует после максимально возможного сокращения микобактериальной популяции, что определяется с помощью микроскопии или культурального исследования мокроты. После операции следует продолжать применять тот же режим химиотерапии минимум 18–20 мес. Лечебный искусственный пневмоторакс должен продолжаться у больных полирезистентным туберкулезом легких не менее 12 мес.
Повышение эффективности лечения больных с лекарственно-устойчивым туберкулезом легких в значительной степени зависит от своевременной коррекции химиотерапии и применения противотуберкулезных препаратов, к которым сохранена чувствительность. Для лечения больных лекарственно-устойчивым и, особенно, полирезистентным туберкулезом легких необходимо использовать резервные препараты: протионамид (этионамид), амикацин (канамицин), офлоксацин. Эти препараты в отличие от основных (изониазид, рифампицин, пиразинамид, этамбутол, стрептомицин) намного более дорогостоящие, менее эффективные и имеют много побочных эффектов. Они должны быть доступны только для специализированных противотуберкулезных учреждений.
Эффективное лечение больных туберкулезом достигается за счет подавления микобактериальной популяции путем применения современных режимов контролируемой химиотерапии основными противотуберкулезными препаратами: изониазидом, рифампицином, пиразинамидом, стрептомицином, этамбутолом. Важнейшими факторами, снижающими эффективность химиотерапии, следует признать резистентность МБТ к противотуберкулезным препаратам, характер специфического процесса и побочные реакции на химиопрепараты.
Повышение эффективности лечения больных с лекарственно-устойчивым туберкулезом легких в значительной степени зависит от своевременной коррекции химиотерапии и применения противотуберкулезных препаратов, к которым сохранена чувствительность. Для лечения больных лекарственно-устойчивым и, особенно, полирезистентным туберкулезом легких необходимо использовать резервные препараты: протионамид (этионамид), амикацин (канамицин), офлоксацин.
1. Лечение туберкулеза: рекомендации для национальных программ.- ВОЗ - Женева, 1998. - Пер. с англ. 77.
2. Рекомендации по лечению резистентных форм туберкулеза. - ВОЗ. - Женева, 1998. - Пер. с англ. 47.
3. Чуканов В.И. Основные принципы лечения больных туберкулезом легких. //Русс. мед. журн. 1998; 17: 1138–42.

Туберкулез – опасное инфекционное заболевание, вызываемое развитием различного рода бактерий, в том числе палочки Коха. До ХХ века лечение этой болезни было сложным и нерезультативным – она имела высокий уровень смертности. Каждый третий человек болел туберкулёзом. Откуда появилось это заболевание? Предположительно изначально оно существовало у животных ещё 245 миллионов лет назад. А первые симптомы туберкулёза у людей были отмечены в Вавилоне, в начале II тысячелетия до н.э. Долгие годы учёные-медики решали вопрос лечения туберкулёза у человека. Немецкий врач, микробиолог, гигиенист, учёный Роберт Кох в 1882 году разработал и сформировал определенный спектр процедур в лечении туберкулёза, которым занимается фтизиатрия. Это раздел клинической медицины, который направлен непосредственно на изучение и лечение туберкулёза. Врач-фтизиатр занимается причинно-следственным процессом, возникающим при развитии туберкулёзной инфекции в организме, её клинико-морфологическими проявлениями, а также лечением пациентов с диагнозом. Фтизиатр лечит легочные и внелегочные формы туберкулезной инфекции: верхних дыхательных путей, бронхолегочной системы, пищеварительной, мочеполовой, сердца, печени, почек, глазного и опорно-двигательного аппарата, кожи, ЦНС, лимфоузлов.
24 марта 1993 года по инициативе Всемирной организации здравоохранения было официально объявлено закрепить эту дату как Всемирный день борьбы против туберкулёза. Дата была выбрана в связи с открытием возбудителя туберкулёза Робертом Кохом (24 марта 1882 год – палочка Коха). Главная цель события – повышение уровня осведомленности о глобальной эпидемии туберкулёза и активных усилиях по ликвидации этой болезни. Врачи-фтизиатры выполняют широкий спектр работы при лечении больных туберкулёзом. Это диагностика и обследование пациентов с подозрением на инфицирование палочкой Коха, с виражом туберкулиновых проб; лечение больных туберкулёзом (составление индивидуальных схем терапии, корректировка доз лекарств, смена препаратов); диспансеризация и профосмотры, динамическое наблюдение за пациентами, прошедшими курс терапии, и лицами, контактировавшими с ними. Выполняется вакцинация и ревакцинация, проведение туберкулиновых проб по возрастам. Принимается реабилитационный комплекс мер: профилактические курсы терапии, социальная помощь (отдельная квартира, питание, трудоустройство).

Ольга Брониславовна Нечаева

Данные предоставлены Ольгой Брониславовной Нечаевой

Показатели по регионам среди заболевших туберкулёзом (ТБ)
Результаты предоставлены Ольгой Брониславовной Нечаевой
Как отмечает руководитель Центра мониторинга противодействия распространению туберкулёза, будет направлена помощь в работе главным специалистам – фтизиатрам, инфекционистам, пульмонологам, эпидемиологам и другим, при проведении анализа по оказанию медицинской помощи населению субъектов РФ по своему профилю.
24 марта 1882 года немецкий микробиолог Роберт Кох объявил об открытии возбудителя туберкулеза. В 2022 году с открытия палочки Коха прошло 140 лет, а 24 марта отмечается Всемирный день борьбы с туберкулёзом.
- Туберкулез пока не побежден, несмотря на то, что возбудитель заболевания открыли 140 лет назад. В разные годы смертность росла и падала, но болезнь все еще остается мировой проблемой. Как сегодня вы оцениваете эпидемиологическую ситуацию с туберкулезом?
- Открытие возбудителя туберкулеза стало большим прорывом в науке и медицинской практике.
С того момента прошло много времени. Был и период, когда мы действительно думали, что победим туберкулез – были открыты стрептомицин и рифампицин, которые стали достаточно эффективными препаратами для лечения туберкулеза. Но и микробактерия туберкулеза со временем изменилась: сегодня растет доля лекарственно-устойчивого заболевания. В клинической практике увеличивается число случаев, когда мы выявляем пациентов с туберкулезом, возбудитель которого устойчив ко всем известным противотуберкулезным препаратам. Это большая проблема и одна из причин, почему мы до сих пор не победили туберкулез.
Во времена Советского Союза в нашей стране была организована противотуберкулезная служба. Надо отметить, что врач-фтизиатр – это специальность, которая есть только на постсоветском пространстве. В зарубежных странах такой специальности нет, и пациентов с туберкулезом лечат пульмонологи. Я считаю, что фтизиатр — это специалист, который должен быть компетентным во всех проблемах, связанных с заболеваниями органов дыхания, так как широкий кругозор и глубокие знания патологии органов дыхания позволяют врачу построить дифференциально-диагностический ряд и своевременно поставить правильный диагноз.
В лечении туберкулеза применяется комплексный подход – сочетание этиотропного лечения (препараты, которые действуют непосредственно на возбудителя заболевания), патогенетической терапии (воздействие на различные звенья патогенеза туберкулеза) и хирургических методов лечения. Каждый пациент получает индивидуализированное лечение, с учетом лекарственной чувствительности возбудителя и лекарственной переносимости препаратов. Сегодня фтизиатрам мало знать, что у человека туберкулез – необходимы данные лекарственной чувствительности возбудителя, потому что без этого невозможно назначить адекватную терапию.
В настоящее время мы редко встречаем формы туберкулеза, которые описывали в начале ХХ века. Туберкулез изменился, изменилась и его диагностика. Например, если еще в 1980-х годах, выявляя в диагностическом материале кислотоустойчивые микроорганизмы, фтизиатры считали, что это равнозначно туберкулезу, то сейчас, обнаружив кислотоустойчивые микроорганизмы, грамотный врач должен выяснить, выявлены ли ДНК микобактерий туберкулезного комплекса. Если ДНК микобактерий туберкулезного комплекса не обнаружены, то не исключено, что у пациента нетуберкулезный микобактериоз.
В нашем институте успешно работает микробиологическая референс-лаборатория, в которой проводится весь спектр современных микробиологических исследований для диагностики туберкулеза и нетуберкулезного микобактериоза. Что очень важно, мы можем определить данные лекарственной чувствительности ко всем современным противотуберкулезным препаратам и контролировать эффективность лечения.
Да, мы не победили туберкулез за 140 лет. Изменился возбудитель заболевания, изменились люди. Но мы достигли огромного прогресса в диагностике, лечении и профилактике заболевания.
В нашей стране всегда работала тактика активного выявления туберкулеза – поиск больных в ходе обследований, проводимых независимо от наличия или отсутствия признаков заболевания туберкулёзом. Для этого проводят проверочные профилактические осмотры, флюорографию органов грудной клетки с определенной периодичностью, туберкулинодиагностику.

- Наверное, в области выявления туберкулеза его можно сравнить с онкологическими заболеваниями, где важно обнаружить рак на ранних стадиях.
- Безусловно. При раннем выявлении заболевания прогноз лечения наиболее благоприятный. При своевременной диагностике туберкулеза чаще диагностируются ограниченные формы заболевания, и если при этом установлена лекарственная чувствительность возбудителя, то это существенно сокращает сроки лечения и увеличивает его эффективность.
Туберкулез – это излечимая болезнь. Но надо вовремя его выявить и правильно лечить. Важна также приверженность пациентов к лечению. Надо понимать, что лечение туберкулеза нелегкое, это может быть и 4, и 6 основных препаратов, к которым добавляются препараты для предотвращения побочных эффектов. Некоторые пациенты негативно воспринимают именно количество препаратов – их действительно много.
- Обычно туберкулез лечат в амбулаторных условиях или пациенты находятся в стационаре?
- В России сочетаются оба вида лечения. Если пациент не бактериовыделитель, то при определенных формах туберкулеза диспансеры могут проводить лечение в амбулаторных условиях.
- Как выглядит современная диагностика туберкулеза?
- Диагностика туберкулеза – это сложный процесс. Так, при выявлении изменений в легких – неважно, это очаговые, инфильтративные изменения или полости распада – врач выстраивает дифференциально-диагностический ряд. Ведь рентгенологическая картина может соответствовать нескольким заболеваниям. Конечно, компьютерные томографы высокого разрешения, которые сегодня установлены в больницах, это серьезная помощь для врачей, но однозначно сказать, основываясь только на данных рентгенологического исследования, что человек болеет именно туберкулезом, мы не можем. Диагноз должен быть подтвержден этиологически – путем выявления возбудителя, или морфологически – по результатам исследования операционного материала или материала бронхобиопсий. Только после таких исследований мы можем сказать, что действительно у человека туберкулезное воспаление.
В институте применяется трехэтапная диагностическая программа, включающая комплексное клинико-рентгенологическое, микробиологическое исследование, бронхоскопию с комплексом биопсий, в том числе и инновационных, диагностические операции.
- С какого момента врачи начали не только опираться на снимки при постановке диагноза, но и проводить комплексные исследования?
- Наши учителя, которые заложили основы фтизиатрии, всегда стремились к тому, чтобы ставить диагноз, опираясь на совокупность всех данных. Но у них не было технической возможности.
Новые исследования появились вместе с технологическим прорывом. Большой прогресс – компьютерные томографы. Другой этап – виртуальная бронхоскопия. Следующий уровень – радиоизотопные методы, которые мы применяем и для диагностики, и для оценки эффективности лечения. Современная микробиологическая диагностика туберкулеза, расшифровка ДНК микобактерий туберкулеза, секвенирование – все это гармоничное развитие технологий, помогающих в диагностике туберкулеза. Однако мало получить результаты высокотехнологичных методов исследования, надо грамотно их интерпретировать, что позволяет поставить правильный диагноз.
- Туберкулез становится устойчивым к лекарствам. Какие работы ведутся, чтобы победить эту резистентность?
- Во фтизиатрию приходят новые, современные препараты. В том числе это препараты, которые раньше использовали для лечения других заболеваний, например, лепры, но они показали свою эффективность и при лечении туберкулеза. Некоторые антибиотики широкого спектра действия мы вообще перестали применять, так как к ним у возбудителя развилась тотальная лекарственная устойчивость.
Для борьбы с лекарственной устойчивостью необходимо синтезировать новые препараты, но это длительный процесс – от поиска новой молекулы до создания препарата и внедрения его в клиническую практику проходят годы.
- Какие альтернативы и дополнения к лекарственной терапии сегодня используются во фтизиатрии?
- Этиотропное лечение, то есть противотуберкулезная терапия, – это база, которая должна быть в обязательном порядке. Но бывают и крайне сложные случаи, когда мы определяем тотальную устойчивость возбудителя к противотуберкулезным препаратам. В таких ситуациях мы тоже научились подбирать схему лечения и применяем методы, которые повышают эффективность лечения.
В частности, мы применяем методы коллапсотерапии – искусственный пневмоперитонеум, искусственный пневматоракс. При применении таких методов лечения возникает коллапс легочной ткани, что уменьшает ее растяжение и создает благоприятные условия для заживления.
В последние годы мы применяем клапанную бронхоблокацию – врач-эндоскопист устанавливает при бронхоскопии клапан в бронх, дренирующий полость в легком, после чего полость спадается, и заживление проходит быстрее.
Подобные методы лечения – это индивидуальный подход к пациентам. Одного пациента можно успешно вылечить только препаратами, в другом случае дополнительно применяем клапанную бронхоблокацию и коллапсотерапию, отдельным пациентам требуется хирургическое вмешательство. Более того, есть пациенты с двусторонним деструктивным туберкулезом. В этих случаях проводят операцию на одном легком, а затем на другом.
Прорыв в хирургическом лечении заболеваний органов дыхания и в частности туберкулеза произошел, когда появилась возможность выполнять видеоторакоскопические операции. Мы отошли от больших кожных разрезов, которые делали еще в 90-х годах. Я застала этот период, когда начинала работать в хирургическом отделе института, например, для заднего доступа к легкому выполняли разрез длиной до 35 сантиметров. Сейчас выполняют видеоторакоскопические операции с небольшим разрезом. Дело не только в косметическом эффекте: при таком подходе минимизируется травма, и заживление проходит быстрее.
В настоящее время при хирургическом лечении деструктивного туберкулеза используется пломбировка силиконовым имплантом. Эта операция сопряжена с минимальной травматизацией и дает отличный лечебный эффект.
Сегодня пациенты могут вылечиться от туберкулеза, даже если заболевание поздно выявили или неэффективно лечили на ранних стадиях.
Чтобы победить туберкулез, Всемирная организация здравоохранения в 2015 году приняла стратегию End TB - ликвидация туберкулеза. Эта стратегия предполагала, что в течение каждого года заболеваемость туберкулезом в мире будет снижаться на 6-10%, а смертность – не менее чем на 10%. То есть к 2025 году заболеваемость туберкулезом должна снизиться на 35%, а смертность – на 50%.
- Это реально?
- Стратегию приняли в 2015 году, а в 2020 началась пандемия COVID-19. Во время локдауна доступ к медицинской помощи уменьшился, в результате и выявление туберкулеза в мире снизилось на 18%, а среди детей и подростков – на 24%. В России этот показатель составил 14%.
По данным ВОЗ, перспективные планы в борьбе с туберкулезом обратила вспять именно пандемия COVID-19. Мировые результаты по снижению заболеваемости и смертности от туберкулеза в 2020 году вернулись к результатам 2017 года. А по сравнению с 2019 годом в 2020 году смертность от туберкулеза в мире увеличилась на 100 000 человек. ВОЗ прогнозирует, что этот отсроченный эффект будет расти.
По показателям снижения заболеваемости и смертности от туберкулеза Россия идет опережающими темпами. В 2000 году заболеваемость туберкулезом была на уровне 90,4 на 100 000 населения, а в 2020 году - 32,4 на 100 000 населения, т.е. снижение заболеваемости практически в три раза. Смертность населения от туберкулеза в 2000 году составляла 20,6 на 100 000 населения, а в 2020 мы видим значительный прогресс – этот показатель составил 4,5 на 100 000 населения.
Как мы достигли таких результатов? Безусловно, этому способствовало положительное влияние государственной поддержки всех противотуберкулезных мероприятий, обеспечение противотуберкулезными препаратами и медицинским оборудованием. Кроме того, сама структура противотуберкулезной службы, ее способность работать как единый организм позволила достигать значимых результатов в борьбе с туберкулезом.
И именно противотуберкулезная служба оказалась наиболее готовой к пандемии COVID-19: для фтизиатра дистанцирование до полутора метров, изоляция заболевшего человека, использование средств индивидуальной защиты – само собой разумеющиеся профилактические меры.
Хочу сказать, что в 2021 году наш институт отметил 100-летие. Мы гордимся институтом и его историей, множество фтизиатрических достижений были получены именно в этих стенах. Это касается и хирургического лечения туберкулеза. Так, один из крупнейших советских хирургов, основоположник торакальной хирургии и выдающийся ученый – Лев Константинович Богуш – работал в нашем институте.
- Нарушения в маршрутизации пациентов, ограничение доступа к медицинской помощи во время пандемии могут в будущем вызвать взрывной рост запущенных случаев туберкулеза?
- Во время пандемии фтизиатрическая служба, в том числе в Москве, встала на борьбу с COVID-19, многие диспансеры в стране были перепрофилированы под лечение новой коронавирусной инфекции. Но фтизиатры смогли организовать работу так, чтобы не упустить профилактических мер, чтобы пациенты своевременно получали лечение. В 2021 году уровень охвата населения плановыми осмотрами повысился, и сегодня тот пробел, который появился в 2020 году, ликвидирован.
Для цитирования: Кучеров А.Л., Ильичева Е.Ю. Новые подходы к активному выявлению больных туберкулезом. РМЖ. 2000;12:492.
НИИ фтизиопульмонологии ММА им. И.М. Сеченова
Новомосковский городской противотуберкулезный диспансер
За последнее десятилетие в России сложилась крайне неблагополучная эпидемиологическая обстановка по туберкулезу. Заболеваемость населения туберкулезом с 1991 г. увеличилась на 150% и в 1999 г. составила 85,2 на 100 тыс. населения. Но статистический показатель заболеваемости не отражает ее истинной величины за отчетный год, так как не учитывает больных, оставшихся недовыявленными.
Прогрессивный рост заболеваемости связан с ухудшением социально-экономических условий и значительным сокращением охвата населения флюорографическими обследованиями, обусловленным радиофобией населения под влиянием многочисленных публикаций, направленных против флюорографии. Доля больных туберкулезом органов дыхания, выявленных при профилактических обследованиях, сократилась в среднем по России до 52%, что отрицательно сказалось на клинической структуре заболеваемости и эффективности лечения. Охват населения профосмотрами сократился до 56,9% против 75,3% в 1986 г., когда на туберкулез было обследовано 106,9 млн. человек. Это привело к значительному запаздыванию выявления больных туберкулезом. Об этом свидетельствует увеличение в структуре смертности от туберкулеза удельного веса больных, состоящих на диспансерном учете до 1 года, – с 8,6% в 1991 г. до 18,2% в 1999 г. Эффективность лечения впервые выявленных больных туберкулезом по критерию прекращения бактериовыделения снизилась с 81,4% в 1991 г. до 72,9% в 1999 г., а по критерию закрытия полостей распада - с 78,6% до 61,8% соответственно. Смертность от туберкулеза увеличилась почти в 3 раза.
Несмотря на то, что основными успехами в снижении заболеваемости туберкулезом и повышении эффективности лечения больных туберкулезом в прошлые годы мы обязаны массовой флюорографии, выполнять ее в прежнем объеме не удастся. И не потому, что велика радиофобия населения и ВОЗ настоятельно рекомендует заменить ее на бактериоскопию мазка мокроты с окраской по методу Циля-Нильсена, а по экономическим соображениям. Из-за недостаточного финансирования сократилась возможность приобретения новой флюорографической техники. В настоящее время около 85% флюорографических установок нуждается в замене из-за технического износа. В большинстве регионов прекращена работа с флюорокартотеками, вследствие чего флюорографически обследуются одни и те же контингенты. Статистические данные не отражают истинной величины охвата населения флюорографическими обследованиями из-за низкого их качества. По данным ретроспективной оценки флюорограмм, технический брак достигает 5-7%, пропуск патологии при двойном чтении флюорограмм - 15-40%, недовызов на дообследование - 15-20%. Эти погрешности суммарно составляют 30-50% всех исследований. Это подтверждается и медленным ростом выявляемости больных туберкулезом - с 0,3 в 1991 г. до 0,5 в 1999 г. на 1000 обследованных. При показателе заболеваемости 85,2 на 100 тыс. выявляемость должна быть более 0,8 на 1000 обследованных.
Система организации флюорографических обследований нуждается в реорганизации. Затраты при массовой профилактической флюорографии не адекватны получаемым результатам и обременительны для бюджета здравоохранения.
Тактика проведения профилактической флюорографии среди всего населения начинает заменяться тактикой проведения ее среди групп населения, подверженных повышенному риску заболевания туберкулезом, что уменьшает тенденции экстенсивного наращивания мощностей, позволяет в разумных пределах сокращать устаревшие материально-технические ресурсы и технологии, заменяя их на более совершенные и более экономичные. За последние годы получило признание выделение групп риска по туберкулезу, но отсутствие единой научно обоснованной концепции их формирования приводит к неоправданному их разрастанию.
Использование компьютерных технологий для индивидуального учета и формирования групп риска по специально разработанной программе позволило сократить объем флюорографических обследований на 50-55% и выявлять при этом 75-87,9% больных туберкулезом. В настоящей статье обобщен опыт работы Новомосковского городского противотуберкулезного диспансера Тульской области, где под руководством сотрудников НИИ фтизиопульмонологии ММА им. И.М. Сеченова в 1992 г. разработана и в 1993 г. внедрена система активного выявления туберкулеза на основе компьютерных технологий, включающая базу данных, программу экспресс-определения индивидуальной степени риска заболевания туберкулезом и методику выявления туберкулеза врачами общей лечебной сети по клиническим проявлениям заболевания 3. База данных заменила громоздкую бумажную картотеку на все взрослое население города и позволила контролировать объем всех видов обследования населения на туберкулез и другую легочную патологию, выделить традиционные группы риска, планировать объем флюорографических обследований, составлять отчет о профилактических обследованиях населения по возрасту, характеру выявленной патологии и видам обследования.
С целью определения индивидуальной степени риска заболевания туберкулезом и формирования групп риска применяется метод анкетного скрининга с последующей обработкой данных на компьютере по специальной программе, предназначенной для формирования групп риска на основе дискриминантного анализа. В результате ранжирования было отобрано 14 наиболее значимых факторов риска и для них получена дискриминантная функция, позволяющая распределить все взрослое население по степени риска на три группы: высокой, средней и низкой с условной априорной вероятностью заболевания туберкулезом для группы высокой степени риска свыше 0,5, средней - от 0,3 до 0,5, низкой - до 0,3 2.
База данных и программа экспресс-определения индивидуальной степени риска предназначена для использования на персональных компьютерах типа IВМ-РС. Вся работа выполняется штатом флюорокабинета и флюоротеки. Для сбора данных и ввода их в компьютер и получения ответа о степени риска опытному регистратору требуется 1-1,5 мин. Риск может со временем увеличиваться в связи с контактом с больными туберкулезом, перенесенными заболеваниями, ухудшением социально-экономических условий жизни и т.д. Поэтому при очередном флюорографическом обследовании вновь проводится тестирование и уточняется группа риска.
В базу данных были введены сведения о так называемых традиционных группах риска. К ним относятся: поликлиническая - 3,5% от взрослого населения; диспансерная, включающая IV и VII группы диспансерного учета, - 1,8%; декретированные контингенты - 10,6%; мигранты - 0,17%; освобожденные из УИН Минюста РФ - 0,5% от взрослого населения.
Общая численность традиционных групп риска по туберкулезу составила 17,2% от взрослого населения. Определение индивидуальной степени риска проводилось во время флюорографического обследования. За 5 лет произошло изменение численности групп риска. Группа высокой степени риска уменьшилась с 20,0% в 1995 г. до 11,9% - в 1999 г., средней - с 22,7% до 21,2% соответственно. Группа низкой степени риска за этот период увеличилась с 57,2% до 66,9%. Флюорографическое обследование населения из групп риска, сформированных методом анкетного скрининга, в 1999 г. дало следующие результаты. Заболеваемость в группе высокой степени риска была 226,0 на 100 тыс. (выявляемость - 2,6 на 1000 обследованных), в группе средней степени риска - 42,7 (выявляемость 0,4), низкой - 25,3 (выявляемость 0,25).
База данных и программа экспресс-определения индивидуальной степени риска позволяет исключить из числа традиционных групп риска неорганизованное население и лиц, не обследованных 2 года и более, так как при анкетном скрининге они автоматически распределяются по группам риска, от которых зависит кратность обследования.
Учитывая заболеваемость и выявляемость в группе высокой степени риска, обследование лиц из этой группы проводилось ежегодно, лиц, вошедших в группу средней степени риска, - 1 раз в 2 года. Что касается лиц из группы низкой степени риска, то они не включались в план флюорографических обследований, кроме лиц относящихся к декретированным контингентам. У части лиц этой группы (примерно 2%), возникает необходимость обследования на туберкулез при их обращении в поликлинику с жалобами или симптомами, подозрительными на туберкулез. В подобных случаях врачи общей лечебной сети направляют таких пациентов на флюорографическое обследование по клиническим показаниям.
Таким образом, флюорографическому обследованию 1 раз в год подлежат следующие группы: поликлиническая, диспансерная, декретированные контингенты, мигранты, прибывшие из мест лишения свободы в течение 3 лет после освобождения, высокой степени риска, что суммарно составляет 38,7% от взрослого населения района. Если прибавить сюда половину населения, входящего в группу средней степени риска (10,6%), непланируемые обследования (2,3%), то ежегодно должно обследоваться 43-45% взрослого населения. В 1999 г. в Новомосковском районе флюорографически обследовано 48,7% взрослого населения. В связи с тем, что в 1999 г. выявляемость в группе низкой степени риска увеличилась до 0,25 на 1000 обследованных (в 1995 г. - 0,18), было принято решение в порядке контроля обследовать эту группу для уточнения степени риска.
Большое практическое значение в настоящее время имеет стоимость выявления одного больного туберкулезом. На примере декретированных контингентов, которые являются традиционной группой риска и обследуются ежегодно, было установлено, что для выявления одного больного из декретированных контингентов необходимо обследовать 1855 человек. При стоимости одного флюорографического обследования, равной 15 руб., выявление одного больного в 1999 г. обошлось в 28350 руб. Анкетный скрининг декретированных контингентов позволил распределить их по группам риска, которые почти не отличаются от групп риска всего взрослого населения. В группу высокой степени риска вошло 10,6% декретированных контингентов и 11,9% всего взрослого населения, средней степени - 22,8% и 21,1%, низкой - 66,4% и 66,9% соответственно. Стоимость выявления одного больного туберкулезом из группы высокой степени риска составила 5235 руб., средней - 45985 руб., низкой - 66135 руб.
Внедрение методики активного выявления больных туберкулезом на основе компьютерных технологий позволило в 2 раза сократить расходы на флюорографию, снизить темпы роста заболеваемости и повысить эффективность лечения. Заболеваемость туберкулезом в районе в 1999 г. составила 69,2 на 100 тыс. (в целом по России - 85,2), эффективность лечения впервые выявленных больных: закрытие полостей распада - 81,8% (РФ - 61,8%), прекращение бактериовыделения - 91,0% (РФ - 72,9%).
Дополнительными методами выявления больных туберкулезом являются бактериологические методы: световая и люминесцентная микроскопия мазка мокроты и посев на МБТ. Применение этих методов в качестве скрининга оправдано у кашляющих и выделяющих мокроту, но считающих себя здоровыми.
У детей основным методом выявления является массовая туберкулинодиагностика, которая обеспечивает выявление преимущественно ограниченных форм туберкулеза. Из всех впервые взятых на учет детей не менее 80% выявляется с помощью туберкулиновых проб. Метод серологического скрининга, основанный на технологии иммуноферментного анализа (ИФА) для выявления туберкулеза не применяется из-за недостаточной специфичности.
В условиях, когда группа низкой степени риска в плановом порядке не обследуется, возрастает роль врачей общей лечебной сети в выявлении туберкулеза по клиническим проявлениям заболевания. Основным методом активного выявления больных туберкулезом до появления бактериовыделения является лучевой метод диагностики.
Для более эффективного и экономичного выявления туберкулеза интенсивно внедряются в практику методы цифровой беспленочной флюорографии. В Новомосковском районе в 2000 г. был приобретен беспленочный флюорограф на базе цифровой камеры КФЦ “Электрон”, на котором уже обследовано более 16 тыс. человек с целью выявления туберкулеза и других заболеваний легких и органов грудной клетки (рис.1). Преимущества цифровых беспленочных флюорографов перед пленочными заключаются в том, что они позволяют избежать расходов на пленку и химреактивы, снизить радиационную нагрузку на пациента более чем в 4 раза, получать рентгеновское изображение непосредственно по окончании экспозиции на экранах компьютерных мониторов, что исключает возможность брака изображения. Кроме того, беспленочный цифровой аппарат позволяет существенно повысить диагностическую ценность получаемого изображения за счет возможностей корректировать яркость и контрастность, выбирать интересующие области и масштабировать выбранные фрагменты изображения, получать как позитив, так и негатив.
Таким образом, внедрение новых технологий активного выявления туберкулеза и других заболеваний легких позволило заменить громоздкую бумажную флюорокартотеку на базу данных, на единой научной основе формировать группы риска и определять кратность их обследования, а беспленочный цифровой флюорограф избавил от необходимости приобретения расходных материалов для флюорографии, рентгенографического дообследования пациентов, двойного прочтения флюорограмм, технического брака и флюоротеки. Все это сократило расходы на выявление одного больного туберкулезом легких и другой легочной патологией примерно в 3 раза. Экономические расчеты показали, что затраты на приобретение отечественного беспленочного цифрового флюорографа окупаются за два года.
В настоящее время в России находится в эксплуатации более 100 отечественных беспленочных цифровых флюорографов различных моделей.
1. Кучеров А.Л., Ильичева Е.Ю. // Пробл. туб., 1998; 3: С.16-9.
2. Ильичева Е.Ю. // Туб. и экология, 1995; 3: С.11-3.
3. Ильичева Е.Ю. // Пробл. туб., 1996; 1: С.15-7.
4. Кучеров А.Л., Рыбкина Т.А., Матвеева Т.И. // Пробл. туб., 1990; 10: С.14-7.
с использованием цифровой беспленочной флюорографии сокращают расходы на выявление туберкулеза легких в 3 раза
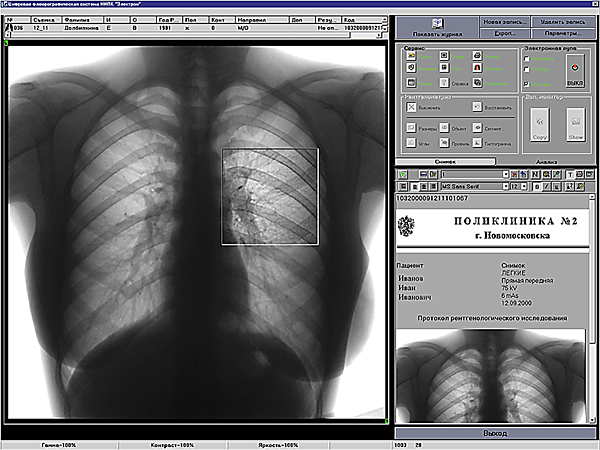
| Рис. 1. Цифровая флюорография (предоставлена НИПК "Электрон"). |
Читайте также:

