Объем жидкости при интоксикации у детей
Обновлено: 24.04.2024
Сайт предоставляет справочную информацию. Адекватная диагностика и лечение болезни возможны под наблюдением добросовестного врача. У любых препаратов есть противопоказания. Необходима консультация специалиста, а также подробное изучение инструкции!
Промывание желудка – метод очищения организма от токсинов и ядов, попавших в желудок, чаще применяется при острых отравлениях. Процедура улучшает состояние больного, способствует скорейшему выздоровлению, спасает жизнь.
В каких случаях следует промывать желудок?
Показания
- Острые отравления продуктами питания, грибами, медикаментами, алкоголем.
- Сужение выходного отдела желудка
- Снижение тонуса мышечной стенки желудка или 12-перстной кишки
- Непроходимость кишечника
- При выделении токсических веществ в просвет желудка. Например: выделение мочевины при хронической почечной недостаточности.
Противопоказания
- Органические сужения пищевода
- Острые кровотечения из пищевода или желудка
- Тяжелые ожоги гортани, пищевода, желудка кислотами и щелочами
- Нарушения мозгового кровообращения
- Инфаркт миокарда, нестабильная стенокардия, тяжелые нарушения сердечного ритма
- Бессознательное состояние (без предварительной интубации). Интубация – введение в гортань и трахею особой трубки для сохранения проходимости дыхательных путей и поддержания дыхательной деятельности.
- Отсутствие кашлевого или гортанного рефлекса
- Судороги, судорожное состояние
Способы промывания желудка
- Промывание без использования зонда
- Промывание с использованием толстого зонда
- Промывание с использованием тонкого зонда
- Если больной не может проглотить зонд, тогда он может самостоятельно выпить воду, а затем вызывать рвоту, таким образом, очищая желудок.
- Пить следует порциями до 500 мл за один раз. После чего ожидать рвоту или же её стимулировать. В общей сложности для эффективного промывания желудка требуется около 5-10 литров воды.
Подпишитесь на Здоровьесберегающий видеоканал


Что необходимо для промывания?
- Растворы для промывания:
- Чистая кипяченая вода (20-24°С).Вода для промывания не должна быть горячей, так как может расширить сосуды и усилить всасывание токсинов, ни холодной, что может вызвать спазм желудка.
- Солевой раствор (2 ст.л. на 5 л воды). Предупреждает продвижение токсинов и ядов дальше в кишечник, вызывая спазм выходного сфинктера желудка.
- Светлый раствор марганцовки (перманганат калия). Убедиться, что не осталось мелких кристаллов перманганата калия, для этого следует хорошо размешать раствор или же его профильтровать. Так как кристаллы могут попасть на слизистую пищевода, желудка и вызвать ожог. Перманганат калия связывает токсины, а так же оказывает антисептическое и противомикробное действие.
- Раствор соды (2 ст.л. на 5 л воды).
- Средства для сбора промывных вод (таз, ведро и т.п.). Промывные воды необходимо показать врачам скорой помощи, это поможет в диагностике заболевания.
- Средства защиты лицам помогающим больному (водонепроницаемый фартук, перчатки). Рвотные массы могут содержать вирусы, бактерии, яды и токсины, способные попасть в организм и вызвать различные заболевания (например: кишечную инфекцию или вирусный гепатит).
Как это сделать?
- Данная процедура не позволяет полностью очистить желудок и поэтому её лучше применять, только если промывание с помощью зонда невозможно!
- Нельзя вызывать рвоту! При отравлении сильными кислотами, щелочами, скипидаром, уксусной эссенцией, отбеливателями, средствами для чистки ванн и туалета, полиролью для мебели. В этих случаях следует использовать промывание желудка с помощью зонда.
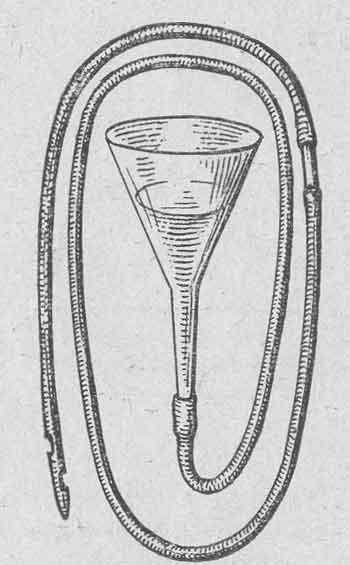
Промывание желудка с использованием толстого зонда
![]()
Что необходимо для промывания?
- Зонд для промывания желудка;
Сам зонд представляет собой трубку, изготовленную из резиновой смеси длинной 80-120 см, толстый зонд диаметром 10-13 мм, тонкий 5-9мм. Один конец срезан, а другой закруглен и имеет боковые отверстия. - Раствор для промывания (5-10 литров)
- Чистая кипяченая вода (20-24°С).Вода для промывания не должна быть горячей, так как может расширить сосуды и усилить всасывание токсинов, ни холодно, что может вызвать спазм желудка.
- Солевой раствор (2 ст.л. на 5 л воды). Предупреждает продвижение токсинов и ядов дальше в кишечник, вызывая спазм выходного сфинктера желудка.
- Светлый раствор марганцовки (перманганат калия). Убедиться, что не осталось мелких кристаллов перманганата калия, для этого следует хорошо размешать раствор или же его профильтровать. Так как кристаллы могут попасть на слизистую пищевода, желудка и вызвать ожог. Перманганат калия связывает токсины, а так же оказывает антисептическое и противомикробное действие.
- Раствор соды (2 ст.л. на 5 л воды).
- Важно! Правильно рассчитать однократную дозу вливаний (5-7 мл на 1 кг массы тела пациента). Одномоментное введение большого объема жидкости в желудок способствует её поступлению в кишечник.
- Воронка емкостью 500мл-1 л, кружка
- Полотенце, салфетки
- Емкость для промывных вод
- Перчатки, непромокаемый фартук
- Вазелиновое масло либо глицерин
Как это сделать?
- Убедиться, что больной в сознании и адекватно понимает происходящее.
- Придать правильное положение больному, сидя на стуле (ближе к спинке) или лежа на боку (без подушки под головой).
- Прикрыть грудь больного фартуком или пеленкой
- Определить необходимую длину зонда, для проведения процедуры. Для этого с помощью зонда измеряется расстояние, от губ до мочки уха, затем вниз по передней брюшной стенки, до нижнего края мечевидного отростка. Найденную точку следует отметить на зонде, что будет хорошим ориентиром при введении зонда и позволит довести его до нужного места.
- Объяснить больному, что при введении зонда он может чувствовать тошноту и позывы на рвоту, но если глубоко дышать через нос данные моменты можно подавить. Кроме того зонд нельзя сдавливать зубами и выдергивать.
- Вымыть руки, надеть перчатки
- Обильно полить закругленный конец зонда глицерином или вазелиновым маслом
- Встать справа от больного (если вы правша). Попросить пациента открыть рот и положить закругленный конец зонда на корень языка.
- При неадекватном поведении больного лучше проводить процедуру с помощником, который бы удерживал больного и фиксировал голову в правильном положении.
Промывание желудка с помощью тонкого желудочного зонда
Что необходимо для промывания?

- Тонкий желудочный зонд (диаметр 5-9 мм)
- Вазелиновое масло или глицерин
- Раствор для промывания (5- 10 литров)
- Чистая кипяченая вода (20-24°С).
- Солевой раствор (2 ст.л. на 5 л воды).
- Светлый раствор марганцовки (перманганат калия)
- Раствор соды (2 ст.л. на 5 л воды).
- Стаканчик с водой (50мл) и трубочкой для питья
- Шприц Жане
- Лейкопластырь
- Полотенце, салфетки
- Перчатки
- Емкость для промывных вод (таз, ведро и т.п.)
- 5-10 литров раствора для промывания
Как это сделать?
- Убедиться, что пациент понимает ход и цели предстоящей процедуры.
- Надеть фартук и перчатки.
- Ввести тонкий зонд через ротовое отверстие (см. промывание желудка с помощью толстого зонда) или через нос.
- Введение тонкого желудочного зонда через нос
- Определить наиболее проходимую ноздрю (продышать сначала одной ноздрей закрыв другую и наоборот).
- Определить расстояние необходимое для введения зонда. Для этого с помощью зонда измеряется расстояние, от кончика носа до мочки уха, затем вниз по передней брюшной стенки, до нижнего края мечевидного отростка. Найденную точку следует отметить на зонде, что будет хорошим ориентиром при введении зонда и позволит довести его до нужного места.
- Помочь пациенту принять нужное положение (высокое положение Фаулера).
- Прикрыть грудь больного полотенцем.
- Вымыть руки и надеть перчатки.
- Хорошо смазать слепой конец зонда вазелиновым маслом или глицерином.
- Слегка запрокинуть голову больного назад.
- Ввести зонд в носовой проход на 15-18 см, затем попросить его наклонить голову вперед.
- Продвигать зонд по задней стенке глотки, предлагая пациенту производить глотательные движения.
- Как только зонд будет проглочен, убедиться, что пациент может свободно дышать и говорить.
- Продолжать мягко продвигать зонд во время каждого глотательного движения до нужной отметки. При этом пациенту можно дать стакан с водой и трубочкой для питья, и попросить пить маленькими глотками немного наклонив голову вперед. Это поможет в продвижении зонда.
- В случае если возникает сильное сопротивление или же больной начинает кашлять, задыхаться, синеет лицо, значит, зонд попал в гортань, и следует немедленно его извлечь.
- Убедиться, что зонд попал в желудок.
- Используя шприц Жане ввести в желудок 20 мл воздуха, при этом выслушивая с помощью фонендоскопа или непосредственно прислонив ухо к брюшной стенке в области желудка характерные звуки.
- Набрать содержимое из желудка в шприц
- Набрать в шприц раствор для промывания, присоединить к зонду и ввести в желудок.
- Потянуть поршень шприца на себя, тем самым высасывая жидкость из желудка. Набранный шприц, отсоединить от зонда и вылить содержимое Набранную жидкость вылить в емкость для промывных вод.
- Повторять введение воды в желудок и её извлечение, пока не будет исчерпана вся запасенная вода (5-10 литров или 10-15% от массы тела).
В статье изложены современные подходы к регидратационной терапии при острых кишечных инфекциях у детей, в том числе с использованием комплексных методов, направленных на коррекцию не только синдрома обезвоживания, но и микроэкологических нарушений, ассоци
The article covers modern approaches to fluid therapy in acute intestinal infections in children, including use of complex methods directed not only to correction of dehydration syndrome, but also micro-ecological disorders associated with infectious affection of the intestine.
Дегидратационный синдром является ведущим патогенетическим фактором при ОКИ у детей, обуславливая тяжесть заболевания. Поэтому особую значимость для практического здравоохранения приобретает оперативность и правильность оценки степени дегидратации у ребенка, больного ОКИ [9]. Фундаментальные исследования Н. В. Воротынцевой, В. В. Малеева, В. И. Покровского по оценке выраженности обезвоживания на основе оценки острой потери массы тела пациента сохраняют свою актуальность до настоящего времени: эксикозу I степени соответствует потеря до 5% массы тела, что составляет до 50 мл/кг жидкости, эксикозу II степени — потеря 6–10% массы тела (60–100 мл/кг), эксикозу III степени — потеря более 10% массы тела (110–150 мл/кг). Обезвоживание с потерей массы тела более 20% не совместимо с жизнью [10]. Однако применительно к педиатрической практике определение дефицита массы тела ребенка на фоне болезни не всегда возможно ввиду интенсивного роста детей, поэтому оценка степени дегидратации проводится на основе клинических данных. В этой связи в настоящее время широкое распространение получили рекомендации Европейского общества педиатров, гастроэнтерологов и диетологов (European Society for Paediatric Gastroenterology Hepatology and Nutrition, ESPGHAN) от 2014 г. [11]. Однако в них предусмотрена клиническая оценка только внешнего вида, состояния глазных яблок и слизистых оболочек, а также наличие у ребенка слез. Более полная клиническая шкала M. H. Gorelick дополнительно включает определение времени капиллярной реперфузии (в норме не более 2 секунд), снижение диуреза, основные гемодинамические показатели (частота и наполнение пульса) и показатели нарушения дыхания [12]. Существуют и другие шкалы клинической оценки выраженности обезвоживания. Однако значимость каждого из симптомов обезвоживания в клинической практике может быть не всегда достаточно высокой, особенно при эксикозе I степени, что делает их наиболее применимыми при эксикозе II степени (табл. 1).
При ОКИ у детей преобладает изотонический тип обезвоживания, характеризующийся пропорциональной потерей жидкости и электролитов, в первую очередь натрия. При этом не отмечается изменения осмотического давления воды во внутриклеточном и внеклеточном пространствах, что затрудняет его определение лабораторными методами [15].
Объективизация диагностики степени выраженности обезвоживания у детей возможна с применением алгоритма, включающего клинические (увеличение времени капиллярной реперфузии, определяемая клинически сухость слизистых оболочек), анамнестические (выраженность диареи и рвоты), инструментальные (оценка влажности кожных покровов) и лабораторные (дефицит буферных оснований сыворотки крови) данные [16].
Также одним из важных аспектов патогенеза, являющегося закономерным для ОКИ любой этиологии, является развитие нарушений микрофлоры желудочно-кишечного тракта (ЖКТ). Ранее было показано, что при дизентерии Зонне у 67,8–85,1% пациентов, при сальмонеллезе — у 95,1%, иерсиниозе — у 94,9%, ротавирусной инфекции — у 37,2–62,8% нарушения со стороны микрофлоры ЖКТ носят выраженный характер [17–19].
Дестабилизация микробиоценоза ЖКТ на фоне течения инфекционного процесса приводит к снижению колонизационной резистентности микрофлоры, повышению выраженности воспалительных реакций со стороны слизистой оболочки кишки и снижению темпов репаративных процессов в кишечнике, что приводит к усугублению интоксикационного синдрома за счет высвобождения токсинов не только патогенных возбудителей, но и представителей условно-патогенной микрофлоры (УПФ), доля которых при ОКИ возрастает [20].
Основные патогенетические аспекты ОКИ обосновывают и терапевтические подходы — регидратационную и пробиотическую терапию, от своевременности и адекватности назначения которых зависят длительность заболевания и его исходы [10].
При развитии дегидратации основным принципом ведения таких больных является быстрое возмещение потерь жидкости и солей, а также увеличение буферной емкости крови. Общепризнано, что в педиатрической практике следует отдавать предпочтение оральной регидратации, как менее травматичной и более физиологичной для ребенка [21]. Международная практика применения оральной регидратации при ОКИ получила широкое применение с 70-х годов XX века, а ее включение в стандарты ведения больных позволило сократить число случаев госпитализации на 50–60% и значительно, на 40–50%, снизить летальность детей [22]. Однако первые рекомендации, которые можно отнести к регидратационной терапии и включающие в себя назначение рисового отвара, кокосового сока и морковного супа, относятся к периоду более 2500 лет назад и принадлежат древнеиндийскому врачу Sushruta [23]. В 1874 г. во Франции доктором Luton было обосновано назначение дополнительной воды для лечения детей, больных ОКИ. Впервые раствор, в состав которого вошли глюкоза, натрий и хлор, предложил использовать доктор Robert A. Phillips, после открытия механизма потенцирования глюкозой всасывания в кишечнике ионов натрия и калия [23]. В нашей стране в 30–50-х годах XX века проводилась разработка методов регидратационной терапии ОКИ М. С. Масловым (1928, 1945, 1955), В. И. Моревым (1937), В. Е. Балабан (1937). Основные принципы оральной регидратации, состав растворов и методы организации помощи больным ОКИ в нашей стране были разработаны Центральным научно-исследовательским институтом эпидемиологии под руководством В. И. Покровского [10].
Общий терапевтический подход к оральной регидратации предусматривает раннее назначение регидратационных растворов и проводится в два этапа:
- 1-й этап — восполнение потерь, произошедших до момента обращения за медицинской помощью. Назначается суммарное количество жидкости 50–80 мл/кг в течение 6 ч;
- 2-й этап — поддерживающая регидратация, задачей которой является восполнение текущих потерь жидкости при ОКИ. В сутки назначается 80–100 мл/кг жидкости. Длительность второго этапа оральной регидратации продолжается до момента выздоровления или появления показаний для парентеральной коррекции обезвоживания [24].
Согласно действующим современным подходам, для проведения оральной регидратации рекомендовано использование готовых форм растворов, сбалансированных по электролитному составу и осмолярности (75 мэкв/л натрия и 75 мэкв/л глюкозы и осмолярностью 245 мосм/л), при этом значению осмолярности растворов, рекомендуемых для педиатрического применения, уделяется огромное значение.
Также было показано, что данный тип растворов уменьшает потребность в инфузионной терапии, снижает выраженность диарейного синдрома и рвоты и позволяет уменьшить объемы растворов при проводимой оральной регидратации, что является важным преимуществом для педиатрии [16].
Необходимо учитывать, что коррекция обезвоживания должна проводиться с использованием и бессолевых растворов, среди которых предпочтение следует отдать питьевой воде (не минеральной!), возможно использование пектинсодержащих отваров (яблочный компот без сахара, морковно-рисовый отвар). Соотношение глюкозосолевых растворов и питьевой воды должно быть 1:1 при водянистой диарее, 2:1 при выраженной рвоте, 1:2 при инвазивных диареях [24].
Тяжелые формы ОКИ, отсутствие эффекта от оральной регидратации или наличие обильной рвоты, отеков, развитие функциональной (острой) почечной недостаточности являются показаниями для проведения парентеральной регидратации, которая может быть осуществлена с использованием одного из современных отечественных растворов — 1,5% раствора меглюмина натрия сукцината, доказавшего свою эффективность в интенсивной терапии данных состояний [30].
Патогенетическое обоснование необходимости применения пробиотических лекарственных средств при ОКИ не вызывает сомнения как в отечественной, так и в зарубежной литературе. Пробиотическую терапию рекомендовано назначать в составе комплексной стартовой терапии вне зависимости от этиологии заболевания и в как можно более ранние сроки. Данные препараты показаны также всем пациентам в периоде реконвалесценции с целью восстановления параметров микробиоценоза. Их применение при ОКИ у детей является не только патогенетически обоснованным, но и относится к самому высокому уровню доказательности — А — в соответствии с принципами доказательной медицины [31]. Данный факт был подтвержден в 2010 г. результатами метаанализа, включившего в себя результаты 63 рандомизированных контролируемых клинических исследований. В нем было показано, что использование пробиотиков достоверно уменьшает продолжительность диареи в среднем на 24,76 часа и сокращает частоту стула, при этом данные препараты характеризуются высоким профилем безопасности [32].
Одним из патогенетических механизмов, позволяющих рекомендовать пробиотики при ОКИ, является их положительное влияние на муциновый слой слизистой оболочки ЖКТ. На фоне течения инфекционного процесса наблюдается изменение физических характеристик данного барьера — снижение вязкости за счет разрушения дисульфидных связей между цистеиновыми мостиками суперструктуры данного геля, что может приводить к транслокации микроорганизмов из просвета кишечника в ткани. Данные процессы развиваются под действием патогенных микроорганизмов, имеющих соответствующие факторы патогенности в виде ферментов, разрушающих слизь (нейраминидаза, гиалуронидаза, муциназа). Длительное, в том числе в постинфекционном периоде, изменение физических свойств муцинового слоя приводит к риску развития воспалительных заболеваний кишечника [33]. Микроорганизмы, относящиеся к компонентам нормальной микрофлоры ЖКТ человека, а также продукты их обмена оказывают потенцирующее действие на состояние муцинового слоя посредством целого ряда механизмов, в том числе генетических [34, 35].
Современный взгляд на терапию пробиотиками подразумевает штамм-специфичный подход, который включает в себя установление в клинических исследованиях терапевтических эффектов, характерных для определенных генетически сертифицированных штаммов и дальнейшее их использование с учетом штамм-специфичных свойств пробиотиков в различных клинических ситуациях [36, 37].
Применительно к острым кишечным инфекциям у детей рабочая группа ESPGHAN в 2014 г. на основе анализа опубликованных систематических обзоров и результатов рандомизированных клинических исследований, в том числе плацебо-контролируемых, опубликовала меморандум, в котором разделила все пробиотические штаммы на пробиотики с положительной рекомендацией, с отрицательной рекомендацией и пробиотики с недостаточными доказательствами их эффективности. К рекомендованным штаммам (несмотря на низкий уровень доказательной базы по мнению экспертов) для терапии ОКИ у детей были отнесены Lactobacillus GG, Saccharomyces boulardii, Lactobacillus reuteri штамм DSM 17938 (исходный штамм ATCC 55730), а также термически инактивированный штамм Lactobacillus acidophilus LB, который формально к пробиотикам как живым микроорганизмам с заданными полезными свойствами отнесен быть не может, однако он показал свою эффективность при острых инфекционных гастроэнтеритах [38].
Штамм Lactobacillus reuteri DSM 17938 устойчив к следующим антимикробным средствам (возможен совместный прием пробиотиков Lactobacillus reuteri Protectis с этими средствами): амоксициллин, ампициллин, Аугментин, диклоксациллин, оксациллин, пенициллин G, феноксиметилпенициллин, цефуроксим, цефалотин, ванкомицин, доксициклин, тетрациклин, фузидовая кислота, ципрофлоксацин, энрофлоксацин, налидиксовая кислота, метронидазол. Lactobacillus reuteri DSM 17938 чувствительны к цефотаксиму, неомицину, стрептомицину, кларитромицину, эритромицину, рокситромицину, клиндамицину, хлорамфениколу, рифампицину, имипенему, линезолиду, виргиниамицину.
При этом Lactobacillus reuteri DSM 17938 характеризуется хорошим профилем безопасности, что подтверждено Продовольственной и сельскохозяйственной организацией ООН (Food and Agriculture Оrganization of the United Nations, FAO) и ВОЗ в 2002 г.
Клиническая эффективность Lactobacillus reuteri DSM 17938 показана при функциональных коликах у детей первого года жизни, в составе комплексной эрадикационной терапии H. рylori-инфекции, профилактики антибиотик-ассоциированной диареи, при метаболическом синдроме, в терапии аллергических заболеваний. Эффективность данного штамма подтверждена в 163 клинических исследованиях у 14 000 пациентов, из которых 114 — рандомизированные, двойные/слепые или слепые плацебо-контролируемые исследования, 47 — открытые исследования, 56 исследований проводились среди 7300 детей 0–3 лет жизни.
Однако наиболее хорошо изучены клинические эффекты данного штамма при ОКИ, что послужило причиной включения его в рекомендации ESPGHAN. Так, в многоцентровом рандомизированном простом слепом клиническом исследовании, проведенном среди госпитализированных с острым гастроэнтеритом детей, получавших традиционную терапию с или без 1 × 10 8 КОЕ Lactobacillus reuteri DSM 17938 на протяжении 5 дней, было показано, что назначение данного пробиотического штамма сокращает продолжительность диареи через 24 и 48 ч (50% в основной группе против 5% в группе сравнения, p < 0,001) и 72 ч (69% против 11%, р < 0,001), позволяет уменьшить сроки госпитализации (4,31 ± 1,3 дня против 5,46 ± 1,77 дня, р < 0,001) и снизить вероятность развития затяжного характера диареи (17% в группе сравнения и ни одного пациента в основной группе) [40]. Аналогичные данные были получены и в других исследованиях [41, 42].
Учитывая вышеизложенное, можно заключить, что в настоящее время в РФ единственным низкоосмолярным глюкозосолевым регидратационным раствором, содержащим Lactobacillus reuteri DSM 17938, является БиоГая ОРС (биологически активная добавка). Данный раствор оказывает терапевтическое действие по двум основным патогенетическим направлениям — корригировать и обезвоживание, и нарушения микробиоценоза при ОКИ у детей. Важно подчеркнуть, что, помимо глюкозы, солей и пробиотика, БиоГая ОРС содержит цинк, оказывающий положительное влияние на всасывание воды, который также потенцирует процессы иммунологической защиты и участвует в процессах регенерации.
По составу и осмолярности комбинация солей БиоГая ОРС соответствует рекомендациям Европейского общества педиатров, гастроэнтерологов и диетологов, а также ВОЗ и ЮНИСЕФ по оральной регидратации при легкой и средней степенях обезвоживания (табл. 2).
Эффективность данной комбинации — Lactobacillus reuteri DSM 17938 и растворов для оральной регидратации — была подтверждена в проспективном плацебо-контролируемом исследовании, где было показано снижение на 84% доли детей с обезвоживанием на вторые сутки приема данной комбинации [43].
Таким образом, комбинированная терапия пробиотиком и низкоосмолярным раствором для оральной регидратации (БиоГая ОРС) у детей без возрастных ограничений является не только патогенетически обоснованной, доказавшей свою несомненную эффективность и безопасность в контролируемых клинических исследованиях, но и наиболее перспективным направлением в лечении острых диарей любой этиологии, значительно уменьшающим полипрагмазию.
Литература
А. А. Плоскирева 1 , кандидат медицинских наук
А. В. Горелов, доктор медицинских наук, профессор, член-корреспондент РАН
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным механизмом заражения, вызываемых патогенными и условно-патогенными бактериями, вирусами или простейшими
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным (фекально-оральным) механизмом заражения, вызываемых патогенными (шигеллы, сальмонеллы и др.) и условно-патогенными бактериями (протеи, клебсиеллы, клостридии и др.), вирусами (рота-, астро-, адено-, калицивирусы) или простейшими (амеба дизентерийная, криптоспоридии, балантидия коли и др.).
Ведущим компонентом терапии ОКИ является рациональное лечебное питание, адаптированное к возрасту ребенка, характеру предшествующего заболевания и вскармливания.
Цель диетотерапии — уменьшение воспалительных изменений в желудочно-кишечном тракте, нормализация функциональной активности и процессов пищеварения, максимальное щажение слизистой оболочки кишечника.
Основные требования к диете при ОКИ:
включение в диеты низко- и безлактозных продуктов и кисломолочных продуктов, обогащенных бифидо- и лактобактериями;
снижение объема пищи в первые дни болезни на 15–20% (при тяжелых формах до 50%) от физиологической потребности;
Из диеты исключаются стимуляторы перистальтики кишечника, продукты и блюда, усиливающие процессы брожения и гниения в кишечнике: сырые, кислые ягоды и фрукты, соки, сырые овощи, сливочное и растительные масла (в чистом виде), сладости, свежая выпечка. Не следует давать бобовые, свеклу, огурцы, квашеную капусту, редис, апельсины, груши, мандарины, сливы, виноград. Не рекомендуется овсяная крупа, так как она усиливает бродильные процессы. Должны быть исключены из питания жирные сорта мясных и рыбных продуктов (свинина, баранина, гусь, утка, лосось и др.).
Цельное молоко в остром периоде кишечных инфекций назначать не следует, так как оно усиливает перистальтику кишечника и бродильные процессы в результате нарушения расщепления молочного сахара (лактозы), что сопровождается усилением водянистой диареи и вздутием живота.
В первые дни заболевания исключается также черный хлеб, способствующий усилению перистальтики кишечника и учащению стула.
При уменьшении проявлений интоксикации, прекращении рвоты и улучшении аппетита вводится творог, мясо (говядина, телятина, индейка, кролик в виде котлет, фрикаделек, кнелей), рыба нежирных сортов, яичный желток и паровой омлет. Разрешаются тонко нарезанные сухари из белого хлеба, каши на воде (кроме пшенной и перловой), супы слизистые, крупяные с разваренной вермишелью на слабом мясном бульоне.
В остром периоде заболевания рекомендуется использовать молочнокислые продукты (кефир, ацидофильные смеси и др.). Молочнокислые продукты за счет активного действия содержащихся в них лактобактерий, бифидобактерий, конечных продуктов протеолиза казеина (аминокислот и пептидов, глутаминовой кислоты, треонина и др.), увеличенного количества витаминов В, С и др. способствуют улучшению процессов пищеварения и усвоению пищи, оказывают стимулирующее влияние на секреторную и моторную функции кишечника, улучшают усвоение азота, солей кальция и жира. Кроме того, кефир обладает антитоксическим и бактерицидным действием на патогенную и условно-патогенную флору за счет наличия молочной кислоты и лактобактерий. Однако длительное применение только кефира или других молочнокислых смесей нецелесообразно, поскольку эти продукты бедны белками и жирами. Лечебным кисломолочным продуктом является Лактофидус — низколактозный продукт, обогащенный бифидобактериями.
При лечении детей с ОКИ в периоде выздоровления необходимо широко использовать плодово-овощные продукты (яблоки, морковь, картофель и др.), так как они содержат большое количество пектина. Пектин — коллоид, обладающий способностью связывать воду и набухать, образуя пенистую массу, которая, проходя по кишечному тракту, адсорбирует остатки пищевых веществ, бактерий, токсических продуктов. В кислой среде от пектина легко отщепляется кальций, оказывая противовоспалительное действие на слизистую оболочку кишечника. Фрукты и овощи содержат органические кислоты, обладающие бактерицидным действием, а также большое количество витаминов, глюкозу, фруктозу, каротин и др. Применение вареных овощей и печеных фруктов уже в остром периоде кишечных инфекций способствует более быстрому исчезновению интоксикации, нормализации стула и выздоровлению.
Питание детей грудного возраста
В последнее время в клинике кишечных инфекций предпочтение отдается назначению детям, находящимся на искусственном вскармливании, низко- и безлактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ, соевые смеси). При тяжелых формах ОКИ и развитии гипотрофии широко используются гидролизованные смеси (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил и др.), способствующие быстрому восстановлению процессов секреции и всасывания в кишечнике и усвоению белков, жиров и углеводов, что предупреждает развитие ферментопатии в исходе кишечной инфекции (табл).
По нашим данным, в результате клинико-лабораторной оценки влияния низколактозных смесей на клиническую картину и состояние микробиоценоза кишечника при вирусных диареях у детей раннего возраста был получен положительный эффект стимуляции функциональной активности нормальной и, в первую очередь, сахаролитической микрофлоры (по стабилизации показателей уксусной, масляной и пропионовой кислот), а также регулирующее влияние на процессы метаболизма углеводов и жиров в острый период заболевания. Клинический эффект заключался в быстром и стойком купировании основных проявлений болезни: рвоты, диареи, абдоминального синдрома и эксикоза, что наряду с хорошей переносимостью позволило рекомендовать низколактозные смеси для использования в качестве лечебного питания у детей раннего возраста в острый период кишечных инфекций вирусной этиологии.
При разгрузке в питании ежедневно объем пищи увеличивается на 20–30 мл на одно кормление и соответственно изменяется кратность кормлений, то есть увеличивается интервал между кормлениями. При положительной динамике заболеваний и улучшении аппетита необходимо довести суточный объем пищи до физиологической потребности не позднее 3–5 дня от начала лечения.
Детям 5–6 месяцев при улучшении состояния и положительной динамике со стороны желудочно-кишечного тракта назначается прикорм кашей, приготовленной из рисовой, манной, гречневой круп на половинном молоке (или воде при ротавирусной инфекции). Кашу назначают в количестве 50–100–150 г в зависимости от возраста ребенка и способа вскармливания до заболевания. Через несколько дней добавляют к этому прикорму 10–20 г творога, приготовленного из кипяченого молока, а затем — овощные пюре, ягодный или фруктовый кисель в количестве 50–100–150 мл, соки.
Питание детей 7–8 месяцев должно быть более разнообразным. При улучшении состояния им назначают не только каши, творог и кисели, но и овощные пюре, желток куриного яйца на 1/2 или 1/4 части, затем бульоны, овощной суп и мясной фарш. В каши и овощное пюре разрешается добавлять сливочное масло. Желток (яйцо должно быть сварено вкрутую) можно давать отдельно или добавлять его в кашу, овощное пюре, суп.
Питание детей старше года строится по такому же принципу, как и у детей грудного возраста. Увеличивается лишь разовый объем пищи и быстрее включаются в рацион продукты, рекомендуемые для питания здоровых детей этого возраста. В остром периоде болезни, особенно при наличии частой рвоты, следует провести разгрузку в питании. В первый день ребенку назначают кефир по 100–150–200 мл (в зависимости от возраста) через 3–3,5 часа. Затем переходят на питание, соответствующее возрасту, но с исключением запрещенных продуктов. В остром периоде заболевания всю пищу дают в протертом виде, применяется паровое приготовление вторых блюд. Крупу для приготовления каши и гарнира, овощи разваривают до мягкости. Набор продуктов должен быть разнообразным и содержать кисломолочные смеси, кефир, творог, сливки, сливочное масло, супы, мясо, рыбу, яйца, картофель, свежие овощи и фрукты. Можно пользоваться овощными и фруктовыми консервами для детского питания. Из рациона исключают продукты, богатые клетчаткой и вызывающие метеоризм (бобовые, свекла, репа, ржаной хлеб, огурцы и др.). Рекомендуются арбузы, черника, лимоны, кисели из различных ягод, желе, компоты, муссы, в которые желательно добавлять свежевыделенный сок из клюквы, лимона.
Правильно организованное питание ребенка с кишечной инфекцией с первых дней заболевания является одним из основных условий гладкого течения заболевания и быстрого выздоровления. Неадекватное питание и погрешности в диете могут ухудшить состояние ребенка, равно как и длительные ограничения в питании. Важно помнить, что на всех этапах лечения ОКИ необходимо стремиться к полноценному физиологическому питанию с учетом возраста и функционального состояния желудочно-кишечного тракта ребенка.
Значительные трудности в диетотерапии возникают у детей с развитием постинфекционной ферментопатии, которая развивается в разные сроки заболевания и характеризуется нарушением переваривания и всасывания пищи вследствие недостатка ферментов.
При ОКИ, особенно при сальмонеллезе, кампилобактериозе, протекающих с реактивным панкреатитом, наблюдается нарушение всасывания жира и появление стеатореи — стул обильный с блеском, светло-серый с неприятным запахом. Диетотерапия при стеаторее проводится с ограничением жира в рационе, но не более 3–4 мг/кг массы тела в сутки для детей первого года жизни. Это достигается путем замены части молочных продуктов специализированными низкожировыми продуктами (Ацидолакт) и смесями зарубежного производства, в состав которых в качестве жирового компонента входят среднецепочечные триглицериды, практически не нуждающиеся в панкреатической липазе для усвоения (Нутрилон Пепти ТСЦ, Хумана ЛП+СЦТ, Алфаре, Прегестимил, Фрисопеп и др.). При появлении признаков острого панкреатита из рациона исключают свежие фрукты, ягоды, овощи, концентрированные фруктовые соки на срок до 1 мес.
При лактазной недостаточности рекомендуется использование адаптированных низколактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ и др.) или соевых смесей (Нутрилон Соя, Фрисосой, Хумана СЛ, Симилак Изомил, Энфамил Соя и др.). При их отсутствии — 3-суточный кефир; детям первых трех месяцев жизни можно давать смесь типа В-кефир, состоящую из 1/3 рисового отвара и 2/3 3-суточного кефира с добавлением 5% сахара (глюкозы, фруктозы), 10% каши на воде, овощных отварах.
В качестве прикорма этим больным дают безмолочные каши и овощные пюре на воде с растительным или сливочным маслом, отмытый от сыворотки творог, мясное пюре, печеное яблоко. Схемы введения прикормов могут быть индивидуализированы, следует обратить внимание на раннее назначение мясного (суточная доза в 3–4 приема). Избегают применения сладких фруктовых соков, продуктов, повышающих газообразование в кишечнике и усиливающих перистальтику (ржаной хлеб, белокочанная капуста, свекла и другие овощи с грубой клетчаткой, кожура фруктов, чернослив, сухофрукты). Длительность соблюдения низколактозной диеты индивидуальна — от 1,5–2 до 6 месяцев.
После тяжелых кишечных инфекций может возникнуть непереносимость не только лактозы, но и других дисахаридов, реже — полная углеводная интолерантность (глюкозо-галактозная мальабсорбция), при которой у больных отмечается выраженная диарея, усиливающаяся при применении смесей и продуктов, содержащих дисахариды, моносахариды и крахмал (молочные и соевые смеси, крупы и практически все фрукты и овощи). Это чрезвычайно тяжелое состояние, приводящее к обезвоживанию и прогрессирующей дистрофии, требует строгого безуглеводного питания и парентерального введения глюкозы или полного парентерального питания. В отдельных случаях возможно пероральное введение фруктозы. При индивидуальной переносимости в диете сохраняются белок и жиросодержащие продукты: нежирное мясо — индейка, конина, говядина, кролик, растительное масло, ограниченный ассортимент овощей с низким содержанием сахарозы и глюкозы — цветная и брюссельская капуста, шпинат, стручковая фасоль, салат.
Дефицит белка возникает за счет нарушения утилизации, всасывания либо за счет потери эндогенного белка, особенно у детей с исходной гипотрофией. Коррекция потерь белка проводится путем назначения гидролизованных смесей (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил, Фрисопеп и др.).
При длительных постинфекционных диареях, особенно у детей, получавших повторные курсы антибактериальных препаратов, возможно развитие вторичной пищевой аллергии, сопровождающейся сенсибилизацией к белкам коровьего молока, реже — к яичному протеину, белкам злаковых культур. Такие нарушения могут возникать не только у детей с аллергическим диатезом, но и у больных без отягощенного преморбидного фона. Клинически постинфекционная пищевая аллергия проявляется гиперчувствительностью к ранее хорошо переносимым продуктам — молочным смесям, молочным кашам, творогу и др. У детей отмечаются боли в животе, вздутие после кормления, срыгивания, жидкий стул с мутной стекловидной слизью, иногда с прожилками крови, при копрологическом исследовании в кале обнаруживаются эозинофилы. Характерна остановка прибавки массы тела, вплоть до развития гипотрофии.
При выявлении аллергии к белкам коровьего молока в питании детей первого года жизни используются смеси на соевой основе (Нутрилак Соя, Нутрилон Соя, Фрисосой, Хумана СЛ, Энфамил Соя и др.) и на основе гидролизатов белка (Нутрилон Пепти ТСЦ, Нутримиген, Прегестимил, Фрисопеп и др.).
Отсутствие специализированных продуктов не является непреодолимым препятствием в организации безмолочного рациона. Элиминационная диета в этом случае составляется на основе безмолочных протертых каш (рисовой, гречневой, кукурузной), фруктовых и овощных пюре, картофеля, кабачков, цветной капусты, тыквы, из печеного яблока, банана, растительного и сливочного масла, мясного пюре. При этом необходимо учитывать физиологические потребности ребенка в основных пищевых веществах и энергии. Мясное пюре, как основной источник белка, при отсутствии специализированных смесей можно назначать с 2–3-месячного возраста. Предпочтительно использовать конину, мясо кролика, птицы, постную свинину, а также диетические мясные консервы — Конек-Горбунок, Чебурашка, Петушок, Пюре из свинины и др.
У детей старше года принцип составления рациона тот же. При назначении безмолочной диеты необходимо полностью компенсировать недостающее количество животного белка протеинами мяса, соевых смесей, а также исключить из диеты продукты, обладающие повышенной сенсибилизирующей активностью (шоколад, рыба, цитрусовые, морковь, свекла, красные яблоки, абрикосы и другие плоды оранжевой или красной окраски, орехи, мед). При постинфекционной пищевой аллергии срок соблюдения указанной диеты составляет не менее 3 месяцев, а чаще — от 6 до 12 месяцев. Эффект от элиминационной диеты оценивается по исчезновению симптомов заболевания, прибавке массы тела, нормализации стула.
Л. Н. Мазанкова, доктор медицинских наук, профессор Н. О. Ильина, кандидат медицинских наук Л. В. Бегиашвили РМАПО, Москва

Первоклассные специалисты инфекционных отделений детской больницы №9 им. Г.Н.Сперанского специально для мам и пап разработали методическое пособие по своевременному избавлению от кишечной инфекции до обращения к специалисту. Если вы с ребенком оказались на даче, в походе, на отдыхе за рубежом или там, где не сразу можно попасть на прием к врачу, врачи подскажут, как действовать, чтобы малыш или подросток как можно скорее выздоровел.
Не допустить обезвоживания!
При частой рвоте, повышенной температуре и жидком стуле и нужно немедленно начинать дробное выпаивание. Лучше использовать растворы солей, сухие порошки для приготовления, которые продаются в аптеках. Солевые растворы, например регидрон, необходимо чередовать с кипяченой водой. Если ребенок капризничает, тогда можно также предложить ребенку некрепкий чай, минеральную воду без газа в разумных количествах (воздержитесь от сульфатной или магниевой, чтобы не усилить жидкий стул).
Как правильно поить? Даже несколько крупных глотков из стакана могут спровоцировать рвоту. Единственный способ восполнить дефицит воды – давать жидкость очень маленькими порциями. Грудничку – по одной чайной ложке подростку – по одной столовой ложке воды или солевого раствора, чередуя их. Интересно, что если заменить стакан ложкой, в большинстве случаев рвота прекращается. Младенцев можно выпаивать, используя шприц на 2-5 мл, разумеется, без иглы. Маленькие порции воды или раствора нужно вливать в ребенка каждые пять минут – не реже, иначе ребенку не удастся выпить нужный объем, но и не чаще, иначе жидкость не успеет усвоиться и ребенка вырвет.
Что не нужно делать?
Выпаивать ребенка соками, морсами и молочными продуктами. Ориентироваться на его жажду. Если малыш или подросток не хочет пить, его все равно нужно дробно и часто поить. Если он просить жидкости больше, не давайте – большой объем вызовет рвоту.
Когда бить тревогу?
Необходимо обращать внимание на объем и частоту мочеиспусканий, характер стула. Если ребенок не мочится более 6-8 часов, необходим осмотр врача, так как при некоторых острых кишечных инфекциях возможно поражений почек. При появлении крови в стуле показано стационарное лечение.
Помните, что основная профилактика кишечных инфекций – личная гигиена, правильное приготовление и хранение пищи!
Читайте также: