Общий анализ крови при ротавирусе
Обновлено: 24.04.2024
В статье приведен обзор существующих подходов к оценке гематологических показателей у детей с острыми респираторными вирусными инфекциями и представлен инновационный метод их оценки, позволяющий наиболее точно определить степень тяжести заболевания у дете
Characteristics of hematological indices in acute respiratory diseases in children of different age groups
The article gives a review of the present approaches to the evaluation of hematological indices in children with acute respiratory viral infections. An innovative method of their evaluation which allows to define the level of severity of the disease in children of different age groups, was presented.
С целью оптимизация тактики лечения актуальными являются: стандартизация методик оценки клинико-лабораторных показателей при ОРИ; установление особенностей лабораторных показателей при ОРИ различной этиологии; оценка риска развития бактериальных осложнений и разработка прогностических критериев.
Традиционно в клинической практике проводится оценка гематологических показателей, в том числе в динамике. Особую значимость такая оценка приобретает при ведении пациентов с инфекционной патологией, учитывая выраженную реакцию гемограммы на инфекционный процесс и ее изменчивость в процессе лечения. В остром периоде заболевания, как правило, отмечаются существенные изменения показателей лейкоцитарной формулы, некоторых биохимических и серологических данных, при этом эти изменения могут носить разнонаправленный характер в зависимости от вида возбудителя, формы тяжести заболевания и возраста пациента.
Одним из наиболее перспективных направлений анализа гематологических показателей является приведение множества отдельных параметров к единому математическому значению, что позволяет стандартизировать и унифицировать клинико-лабораторные данные. Использование интегральных оценок гематологических показателей пациентов в динамике представляется перспективным для выявления клинико-лабораторных особенностей ОРИ различной этиологии, а также для определения формы тяжести, риска развития бактериальных осложнений. При этом статистически значимые отклонения в показателях гемограммы в динамике, как полученных рутинными методами, так и интегральных, позволят оценить эффективность и безопасность терапии при ОРИ у детей, что позволит создать алгоритмы динамического мониторинга качества проводимой терапии.
Применительно к оценке результатов клинических исследований одним из направлений интегральной оценки лабораторных данных является расчет лейкоцитарных индексов. Большой научно-практический потенциал использования подобных индексов подчеркивают многие авторы [3, 6], показывая их применимость в широком диапазоне нозологических форм, от инфекционных болезней до острой хирургической патологии. Наиболее изученными являются лейкоцитарные индексы интоксикации (ЛИИ) по Я. Я. Кальф-Калифу [5], по В. К. Островскому [8, 9], по Б. А. Рейсу [10], ядерный индекс по Г. Д. Даштаянц [1], индекс сдвига лейкоцитов крови [13], интегральный коэффициент ухудшения крови [11], энтропия лейкоцитарной формулы [12]. При их расчете используют относительные (выраженные в процентах) величины компонентов лейкоцитарной формулы, определение которых входит в рутинную клинико-лабораторную практику всех лечебно-профилактических учреждений. Использование интегральных показателей лейкоцитарной формулы крови позволяет повысить информативность традиционных диагностических тестов и качество оценки эффективности терапии, а в клинической практике — оптимизировать прогнозирование исходов заболевания и индивидуализировать схемы лечения и реабилитации. Применение оптимальных стандартизированных подходов к оценке гематологических показателей перспективно при компьютерной оценке результатов клинических исследований и разработке экспертных диагностических систем.
Однако эффективность использования лейкоцитарных индексов для оценки течения заболевания, эффективности и безопасности терапии у инфекционных больных до настоящего времени в достаточной степени изучена не была. Также существует необходимость разработки границ нормальных значений показателей лейкоцитарных индексов в педиатрической практике для различных возрастных групп.
Новыми перспективными комплексными способами анализа формы тяжести заболевания, риска развития бактериальных осложнений, эффективности и безопасности терапии при ОРИ, которые требуют дальнейшего изучения, являются методы оценки динамики относительных частот отклонений гематологических показателей, расчета их Z-оценок и комплексной Z-оценки.
Таким образом, разработка алгоритмов использования адекватных оценочных критериев и маркеров течения острого респираторного заболевания, применимых в широкой лечебной практике и не являющихся экономически обременительными для лечебно-профилактических учреждений, актуальна, так как позволит повысить точность оценки формы тяжести заболевания, риска развития бактериальных осложнений, эффективности и безопасности используемой терапии острых респираторных инфекций у детей.
Целью настоящего исследования было изучение особенностей изменения и клинической значимости рутинных показателей гемограммы, лейкоцитарных индексов и современных математических методов оценки гемограммы при острых респираторных вирусных инфекциях у детей разного возраста.
Пациенты и методы исследования
В исследовании были проанализированы клинико-лабораторные данные 44 пациентов в возрасте от 1 месяца до 14 лет с ОРВИ в остром периоде (на 1–3 сутки от начала заболевания). У всех пациентов собирался клинический и эпидемиологический анамнез, проводился клинический осмотр по общепринятым методам, осуществлялась термометрия, оценка жизненно важных показателей (ЧСС, ЧД, АД). Учитывая наличие возрастных особенностей гемограммы, в частности лейкоцитарной формулы, пациенты были разделены на три группы: 13 больных в возрасте до 1 года, 15 детей от 1 до 5 лет и 16 пациентов от 5 до 14 лет. У пациентов всех групп была проведена оценка показателей гемограммы, расчет лейкоцитарных индексов (табл. 1), а также Z-оценок основных показателей гемограммы. Оценка степени корреляции показателей гемограммы, лейкоцитарных индексов и Z-оценок основных показателей гемограммы осуществлялась с уровнем лихорадочной реакции, как одного из объективных маркеров тяжести острой респираторной вирусной инфекции, и формами тяжести основного заболевания путем расчета коэффициента корреляции Пирсона (ККП). Расчет Z-оценок компонентов лейкоцитарной формулы осуществлялся по формуле:
где Z — Z-оценка, X — значение показателя, m — среднее нормальное значение показателя, σ — среднеквадратичное отклонение данного показателя.
Установление этиологии острых респираторных инфекций осуществлялось методом ПЦР на базе ФБУН ЦНИИ эпидемиологии Роспотребнадзора.
Результаты исследования и обсуждение
В табл. 2 представлены формы тяжести в группах пациентов разного возраста. В этом отношении группы были сравнимы, лишь у детей старше 5 лет преобладало развитие ОРИ в легкой форме по сравнению с группой в возрасте от 1 до 5 лет.
Было проведено изучение корреляции между степенью лихорадочной реакции в °С (одного из основных объективных маркеров тяжести острой респираторной вирусной инфекции) и значением показателей гемограммы и лейкоцитарных индексов.
Анализ показал следующие результаты:
- суммарное содержание лейкоцитов в периферической крови, процентное содержание палочкоядерных и сегментоядерных нейтрофилов, эозинофилов, моноцитов — очень слабый (ККП от 0,1 до 0,3) и слабый (ККП от 0,3 до 0,38) уровень корреляции;
- лимфоциты — средний уровень корреляции (ККП 0,53) у пациентов до 1 года;
- базофилы — высокий уровень корреляции (ККП 0,7) у детей в возрасте от 1 года до 5 лет.
Эти данные свидетельствуют о низкой чувствительности прямой оценки показателей гемограммы при установлении степени тяжести острых респираторных вирусных инфекций.
Анализ средних значений лейкоцитарных индексов выявил для большинства из них зависимость от возраста: индекс соотношения лейкоцитов и СОЭ, индекс соотношения лимфоцитов и моноцитов, индекс соотношения лимфоцитов и эозинофилов, лейкоцитарные индексы интоксикации, индексы сдвига лейкоцитов крови, индекс Кребса, кровно-клеточный показатель, индекс соотношения нейтрофилов и моноцитов — прямая зависимость; индекс аллергизации, индекс эндотоксикоза, индекс Гаркави, индекс резистентности организма, лимфоцитарно-гранулоцитарный индекс, лейкоцитарный индекс — обратная зависимость (табл. 3).
Это объясняется тем, что все лейкоцитарные индексы не учитывают особенности лейкограммы детей — наличие перекреста между нейтрофилами и лимфоцитами, а также возрастную динамичность референсных значений моноцитов, палочкоядерных нейтрофилов и эозинофилов.
Оценка корреляции лейкоцитарных индексов с уровнем лихорадочной реакции продемонстрировала умеренную чувствительность этих показателей:
- ЛИИ по Я. Я. Кальф-Калифу — средний уровень корреляции (ККП 0,5) в группе пациентов от 1 года до 5 лет;
- индекс сдвига лейкоцитарной формулы по Н. И. Яблучанскому — отрицательная корреляция (ККП 0,5) в группе детей до 1 года;
- ядерный индекс степени эндотоксикоза по Г. Д. Даштаянц был связан с уровнем лихорадочной реакции у больных первого года жизни (ККП 0,8), у пациентов от 1 года до 5 лет (ККП 0,7).
Оценка доли пациентов с отклонениями от нормальных значений Z-оценок показателей гемограммы более 2SD (в %) у пациентов разного возраста показала наличие значимых отличий от других возрастных групп в отношении:
- лейкоцитов (у пациентов до 1 года);
- сегментоядерных нейтрофилов (у пациентов от 1 года до 5 лет);
- лимфоцитов (у пациентов старше 5 лет);
- СОЭ (у пациентов до 1 года) (табл. 4).
Проведенный анализ средних значений отклонений от нормальных значений Z-оценок показателей гемограммы более 2SD у пациентов разного возраста показал, что наиболее выраженные отклонения характерны для лимфоцитов у пациентов старше 5 лет и сегментоядерных нейтрофилов у пациентов до 1 года (табл. 5).
Проведенный ранговый корреляционный анализ продемонстрировал высокий уровень прямой корреляции между формой тяжести заболевания (легкая, средняя, тяжелая) и степенью отклонений от 2SD Z-оценок показателей гемограммы (табл. 6). Оценка производилась для всех возрастных групп, вместе взятых, что диктуется сутью метода Z-оценок.
Для оценки клинической эффективности метода Z-оценок был проведен анализ специфичности, чувствительности и точности данного метода при тяжелой форме острой респираторной инфекции.
Клиническая специфичность характеризуется числом клинически истинно отрицательно классифицированных пациентов, деленных на сумму клинически правильно отрицательно классифицированных плюс клинически ложноположительно классифицированных. Специфичность теста отражает вероятность отрицательного результата в отсутствие патологии, что при высокой специфичности позволяет адекватно отсеивать здоровых из популяции с предполагаемой патологией.
Клиническая чувствительность характеризуется числом клинически истинно положительно классифицированных пациентов, деленных на сумму клинически истинно положительно классифицированных плюс клинически ложноотрицательно классифицированных. Чувствительность теста отражает вероятность его положительного результата в присутствии патологии, что при высокой чувствительности теста позволяет с его помощью эффективно выявлять больных в общей популяции.
Комбинация клинической чувствительности и клинической специфичности теста характеризует клиническую эффективность теста [7].
Установление баланса между специфичностью и чувствительностью необходимо для определения прогностической значимости теста в установлении форм тяжести острой респираторной инфекции. Максимально специфичным явилось определение степени отклонения Z-оценок лейкоцитов и палочкоядерных нейтрофилов. Высокая чувствительность метода Z-оценок выявилась в отношении сегментоядерных нейтрофилов, моноцитов и лимфоцитов, что позволяет говорить о значимости данного метода в идентификации именно вирусных инфекций (рис. 1).
Показатель точности (диагностическая эффективность теста) Z-оценок показателей гемограммы отражает клиническую значимость данных показателей для выявления тяжелой формы заболевания (рис. 2). Применительно к острым респираторным инфекциям можно сказать, что оптимальная точность расчета отклонений Z-оценок отмечена для всех показателей гемограммы (0,7 и более).
Также было установлено, что проведение анализа распределения Z-оценок показателей гемограммы позволяет оценить норму реагирования гемограммы при воздействии определенных этиологических факторов.
Как видно из рис. 3, 4 и табл. 7, экстремумы парабол распределения Z-оценок лейкоцитов при этих инфекциях достоверно отличались: при гриппе он составлял 0,32 ± 0,02 ЕД, при респираторно-синцитиальной (РС) вирусной инфекции — 0,17 ± 0,01 ЕД (р < 0,01). При этом экстремумы отличались величиной изменений, которая имела более выраженный характер при гриппе.
При рино- и аденовирусных инфекциях экстремумы парабол распределения Z-оценок лейкоцитов также достоверно отличались между собой и находились, в отличие от аналогичного распределения при гриппе и РС-вирусной инфекции, в зоне отрицательных значений Z. Установление данных закономерностей реагирования гемограммы под воздействием различных этиологических факторов позволяет установить типичность отклонений в гемограмме для каждой из данных инфекций, что имеет большое дифференциально-диагностическое значение.
Достоверных различий в распределении Z-оценок лейкоцитов при гриппе и аденовирусной инфекции выявлено не было.
Таким образом, проведение анализа Z-оценок показателей гемограммы у детей с острыми респираторными инфекциями позволяет практическому врачу определять форму тяжести заболевания и оценивать соответствие гематологических показателей пациента этиогенным особенностям гемограммы.
Литература
М. Л. Абрамович
А. А. Плоскирева 1 , кандидат медицинских наук
ФБУН ЦНИИ эпидемиологии Роспотребнадзора, Москва
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Ротавирусная инфекция: причины появления, симптомы, диагностика и способы лечения.
Определение
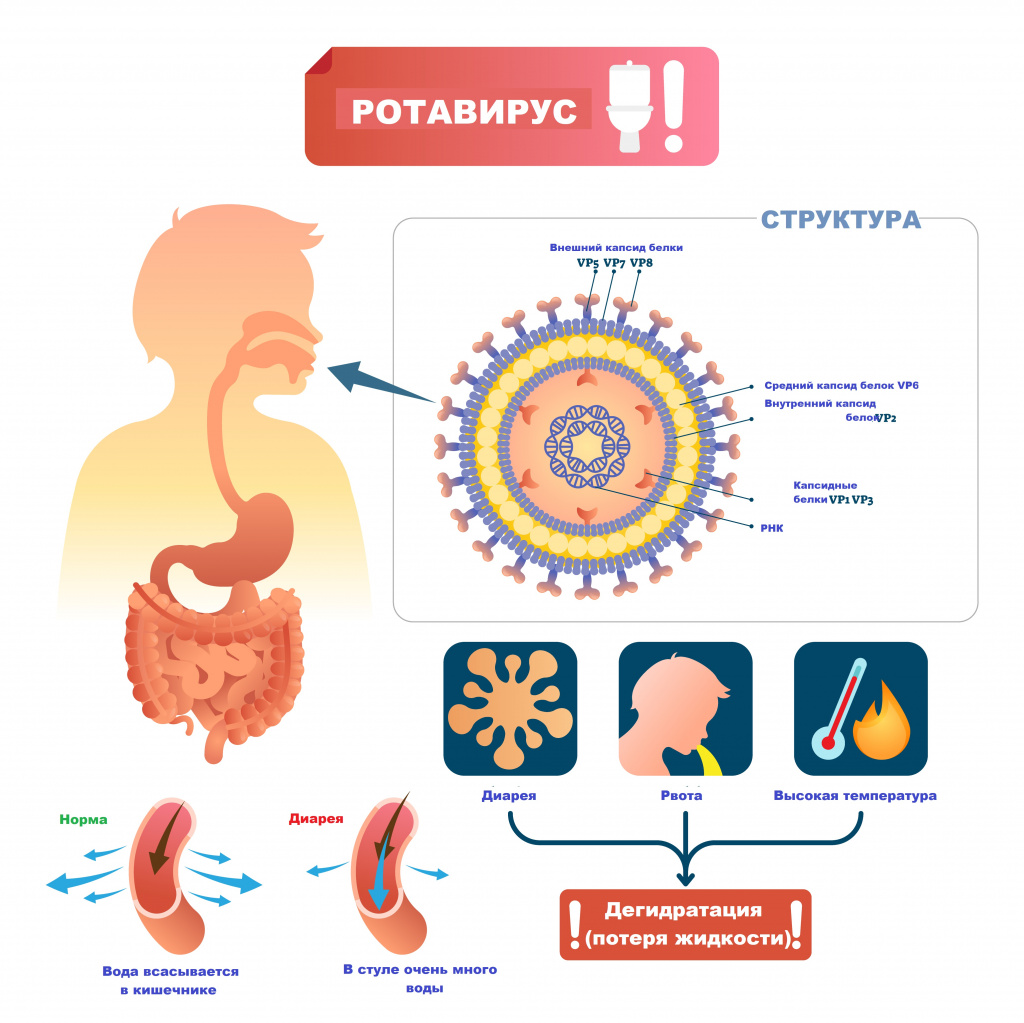
Ротавирусная инфекция (ротавирус) – это острое инфекционное заболевание, вызываемое ротавирусом и характеризующееся поражением желудочно-кишечного тракта по типу гастроэнтерита с развитием синдрома дегидратации (обезвоживания).
Причины появления ротавирусной инфекции
Возбудителем заболевания выступает вирус семейства Reoviridae, рода Rotavirus. Ротавирусы устойчивы к воздействию факторов окружающей среды, в питьевой воде, открытых водоемах и сточных водах они сохраняют жизнеспособность до нескольких месяцев, на овощах и фруктах – до 30 дней.
Основной источник и резервуар ротавирусной инфекции – больной человек в конце инкубационного периода и в первые дни болезни, выделяющий с фекалиями вирус, а также вирусоносители. Механизм передачи возбудителя – фекально-оральный.
- контактно-бытовой (через грязные руки и предметы обихода);
- водный (при употреблении воды, в которой присутствуют вирусы);
- пищевой (чаще всего при употреблении молока, молочных продуктов);
- реже – воздушно-капельный путь.
Ротавирусным гастроэнтеритом болеют люди любого возраста, но максимальная заболеваемость отмечается у детей первых двух лет жизни, людей пожилого возраста и лиц с нарушением функционирования иммунной системы.
Наблюдается зимне-весенняя сезонность, спорадические случаи заболевания регистрируются в течение всего года.
Ротавирусы проникают внутрь эпителия слизистой оболочки двенадцатиперстной кишки и верхних отделов тощей кишки. Размножение и накопление вируса приводит к гибели зрелых эпителиоцитов кишки и их отторжению. В результате нарушается абсорбция углеводов и простых сахаров, и они накапливаются в избыточном количестве. В просвете кишечника повышается осмотическое давление, нарушается всасывание воды и электролитов. Возникает водянистая диарея. Образование большого количество органических кислот, водорода, углекислого газа в процессе ферментации нерасщепленных дисахаридов кишечной микрофлорой ведет к повышению газообразования в кишечнике.
У детей с иммунными нарушениями ротавирус может стать причиной развития гепатита, нефрита, пневмонии, экзантемы, энцефалита с высоким риском летального исхода.
Классификация заболевания
Формы ротавирусной инфекции:
- типичная (гастрит, гастроэнтерит, энтерит);
- атипичная (стертая, бессимптомная);
- вирусоносительство.
- легкое;
- среднетяжелое;
- тяжелое.
- гладкое;
- негладкое (с обострениями и рецидивами).
- острое (до 1 месяца);
- затяжное (до 3 месяцев);
- хроническое (более 3 месяцев).
Инкубационный период ротавирусной инфекции составляет от 14 часов до 7 дней (в среднем 1-4 дня). Заболевание чаще всего начинается остро с повышения температуры тела от субфебрильных до фебрильных значений, появляются симптомы интоксикации (вялость, слабость, снижение аппетита), диарея и повторная рвота.
Кишечная дисфункция характеризуется жидким, водянистым, пенистым стулом желтого цвета без патологических примесей. При обильном жидком стуле развивается обезвоживание.
В тяжелых случаях возможно уменьшение количества мочи вплоть до полного ее отсутствия, снижение артериального давления.
В течение 3–6 дней могут присутствовать умеренные или сильные схваткообразные или постоянные боли в верхней половине живота. У детей младшего возраста в начале заболевания могут наблюдаться катаральные явления, которые предшествуют дисфункции кишечника: покашливание, насморк или заложенность носа, редко – конъюнктивит, катаральный отит. У детей раннего возраста на фоне высокой температуры могут развиться генерализованные судороги, сопровождающиеся потерей сознания.
Для легких форм ротавирусной инфекции характерны следующие симптомы:
- температура тела 37,1-38,0°C;
- умеренная интоксикация в течение 1–2 дней;
- нечастая рвота;
- стул жидкой кашицей до 5-10 раз в сутки.
- температура тела 38,0-39,0°C;
- выраженная интоксикация;
- повторная рвота в течение 1,5-2 дней;
- обильный водянистый стул от 10 до 20 раз в сутки;
- обезвоживание I–II степени.
- бурным началом;
- значительными потерями жидкости (обезвоживание II–III степени),
- многократной рвотой;
- водянистым стулом более 20 раз в сутки;
- снижением артериального давления.
Типичный ротавирусный гастроэнтерит характеризуется доброкачественным циклическим течением, наличием специфических признаков заболевания, а также обнаружением возбудителя в фекалиях.
К атипичным формам ротавирусного гастроэнтерита относятся:
- стертая и субклиническая формы со слабо выраженными и быстро проходящими симптомами;
- бессимптомная форма с отсутствием клинических признаков болезни, но с нарастанием титров специфических антител в крови;
- носительство ротавирусов после перенесенного острого ротавирусного гастроэнтерита, у здоровых лиц в очагах с инфекционной диареей;
- хроническая форма, сохраняющаяся более 3 месяцев.
Сочетание поражения желудочно-кишечного тракта и симптомов интоксикации, развитие обезвоживания, наличие ротавирусной инфекцией у лиц, контактирующих с больным, имеют большое значение в диагностике заболевания.
Окончательный диагноз ротавирусной инфекции ставится только на основании лабораторного подтверждения. Используют:
- методы, основанные на обнаружении ротавируса и его антигенов в фекалиях (электронная и иммуноэлектронная микроскопия, РЛА, ИФА);
- методы обнаружения вирусной РНК в копрофильтратах (метод молекулярных зондов – ПЦР и гибридизации, электрофорез РНК в полиакриламидном геле или агарозе);
- методы обнаружения специфических антител к ротавирусам в сыворотке крови (ИФА, РСК, РТГА, РНГА).
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо).
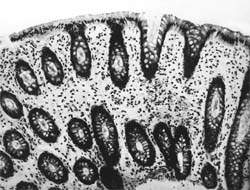 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
Методы диагностики ротавирусной инфекции
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
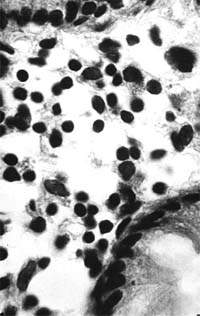 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
Основные методы диагностики и лечения ротавирусной инфекции. Что делать при появлении первых симптомов, чем лечить и как вылечить ротавирус у детей. Основные методы лечения: энтеросорбция, диетотерапия и оральная регидратация. Противовирусные препараты и энтеросорбенты для детей. Период восстановления и осложнения после ротавируса.

Для подтверждения ротавирусной инфекции используют молекулярно-генетические, серологические методы. Материалом для исследования служат фекалии. Исследования, направленные на обнаружение антигенов вируса или нуклеиновых кислот вирусов, желательно проводить в первые 4 дня болезни. Наиболее распространенный способ диагностики — обнаружение антигенов ротавируса в фекалиях с помощью иммуноферментного анализа (ИФА), реакции латекс-агглютинации (РЛА). В повседневной практике широко используется ПЦР-диагностика — полимеразная цепная реакция, которая относится к молекулярно-генетическим методам исследования. Существуют экспресс-тесты для выявления антигена ротавируса в фекалиях на основе иммунохроматографического метода (рота-тест).
Основа терапии и лечения острых кишечных инфекций — нормализация процессов, к нарушению которых привел возбудитель, микробные или вирусные токсины (воздействие на симптомы общей интоксикации, водно-электролитные нарушения, нарушение процессов пищеварения, изменения микробного пейзажа кишечника). Все это реализуется при комплексном подходе. Основой лечения является диетотерапия, возмещение потери жидкости (оральная регидратация (отпаивание) или инфузионная терапия), энтеросорбция.
Начать ее необходимо со снижения температуры (если она выше 38,5 °С): раздеть ребенка, обтереть прохладной водой, можно поставить жаропонижающую свечу (на основе парацетамола) в прямую кишку (ректально) или, при отсутствии многократных рвот, перорально (через рот) дать средства на основе парацетамола или ибупрофена в виде сиропа или таблетки (растереть в порошок) в возрастной дозе.
После оказания первой помощи необходимо приступить к оральной регидратации (отпаиванию или инфузионной терапии). Для оральной регидратации используются специальные глюкозо-солевые растворы (Хумана Электролит, Гидровит, ОРС-200, Супер-ОРС, Регидрон).
При отпаивании самым важным является дробность введения жидкости. Для этого родители должны набраться терпения и поить ребенка малыми порциями через 10–12 минут.
Ребенку в возрасте до года за раз можно давать до 5 мл (1 чайная ложка) жидкости, от 1 до 3 лет — до 10 мл (2 чайных или 1 десертная ложка), более старшим детям — до 15 мл (1 столовая ложка). Жидкость ребенку нужно давать из ложки, можно вливать за щеку из шприца (разумеется, без иголки) или отливать необходимый разовый объем жидкости в маленький рожок. Не следует давать ребенку чашку с большим объемом жидкости, т. к. у малыша имеется жажда, самостоятельно он может выпить много жидкости (80–150 мл) и этим спровоцировать рвоту.
Следует знать, что оральную регидратацию проводить нельзя при: неукротимой рвоте, общем тяжелом состоянии ребенка и обезвоживании II–III степени, резком снижении выделения мочи (олигоанурии), что может быть проявлением острой почечной недостаточности. В этих случаях она неэффективна, и драгоценное время на оказание адекватной медицинской помощи будет упущено.
Рациональное питание, или диетотерапия является важнейшей частью лечения детей, переносящих острые кишечные инфекции, т. к. при неадекватном питании возможно формирование длительной диареи, развитие гипотрофии (снижения массы тела), синдрома мальабсорбции (нарушения переваривания и всасывания пищевых веществ) и т. п. Основой диетотерапии является рациональный режим питания и коррекция диеты в зависимости от фазы заболевания. Адекватный подбор питания и специальная диета при ротавирусе способствует повышению сопротивляемости организма и благоприятному исходу ОКИ.
Доказано, что даже при тяжелых формах кишечных инфекций основные функции кишечника сохраняются, а длительное нахождение ребенка без пищи (так называемые водно-чайные паузы, которые раньше широко практиковали в лечении кишечных инфекций за неимением информации о том, чем кормить ребенка при ротавирусе) приводит к задержке восстановительных процессов в слизистой оболочке желудочно-кишечного тракта, способствует развитию белково-калорийной недостаточности и снижению массы тела.
Для детей первого года жизни, переносящих ОКИ, оптимальным видом пищи является грудное молоко, т. к. оно содержит огромное число защитных факторов (иммуноглобулин А, лизоцим, интерферон, лактоферрин, комплемент, бифидо- и лактобактерии и т. д.), чрезвычайно необходимых больному ребенку.
Ребенка необходимо чаще прикладывать к груди. Количество грудного молока, получаемого ребенком за одно кормление, можно контролировать, взвесив ребенка до начала кормления и после его завершения, высчитав разницу в массе тела, которая и будет являться количеством съеденного. В отдельных случаях ребенка можно кормить сцеженным грудным молоком.
Острые кишечные инфекции (ОКИ) у детей остаются ключевой проблемой во всем мире. По данным ВОЗ, они занимают второе место по заболеваемости после респираторных инфекций. Ежегодно выявляется около 1,7 миллиарда случаев острой диареи, связанной с ОКИ. В РФ у детей в возрасте от 0 до 17 лет число ежегодно регистрируемых случаев ОКИ составляет от 470 тыс. до 530 тыс., большая часть которых приходится на долю пациентов раннего возраста. Что нужно знать про кишечные инфекции – читайте в статье.

Почему возникают кишечные инфекционные заболевания у детей
Под термином острые кишечные инфекции принято понимать состояние, сопровождающееся диареей, и вызванное определенными микроорганизмами. Это могут быть бактерии, вирусы и простейшие.

Важно!
В последние годы доказано, что до 70% всех ОКИ вызываются вирусами, при этом ведущее место занимает ротавирус (до 35% среди всех инфекционных диарей). Рост заболеваемости вирусными ОКИ характерен для холодного времени года. В теплые месяцы растет вероятность заразиться бактериальными кишечными инфекциями.

Бактериальные ОКИ могут вызывать представители родов Salmonella, Shigella, патогенные штаммы Escherichia coli, Campylobacter, Staphylococcus, Klebsiella и пр. Возбудителями вирусных ОКИ, кроме ротавируса, могут быть норовирусы, астровирусы, аденовирусы F, коронавирусы и др.
Источником кишечной инфекции может быть больной человек или носитель. Передача микроорганизмов происходит различными путями:
Контактно-бытовой путь реализуется при попадании микроорганизмов на предметы обихода.
Пищевой путь возможен при заражении продуктов питания. Заражение происходит при употреблении пищи, обсемененной возбудителем. Например, заболеть дизентерией можно при употреблении некачественного молока, салатов и других продуктов, не подвергающихся тепловой обработке.
Водный путь характерен для многих кишечных инфекций. Возбудитель болезни передается через некипяченую воду.
Симптомы кишечной инфекции
Острая кишечная инфекция проявляется такими симптомами:
- диарея (понос) – стул становится жидким и частым;
- боль в животе;
- тошнота и рвота;
- повышение температуры тела.
Симптоматика может меняться в зависимости от возбудителя болезни. Например, при ротавирусной инфекции у ребенка бывает высокая температура тела и резкое обезвоживание. Дизентерия проявляется скудным частым стулом, выраженной болью в животе и лихорадкой. При сальмонеллезе наблюдается частая рвота, жидкий стул с примесью слизи.

Ротавирусная инфекция у ребенка: чем она опасна
Ротавирусная инфекция заслуживает особого внимания. По данным ВОЗ, ротавирусы инфицируют почти каждого ребенка в возрасте до 3-5 лет и являются основной причиной развития тяжелого обезвоживания.
Возбудитель инфекции относится к семейству Reoviridae. В 80% случаев наблюдаются вспышки заболевания в холодное время года – с ноября по апрель. Источником инфекции становится больной человек или вирусоноситель. Например, ребенок в 2 года ротавирусом может заразиться в детском саду или при контакте с другими детьми на детской площадке.
Антитела к ротавирусам вырабатываются после перенесенной инфекции, поэтому последующие эпизоды инфицирования могут протекать легче. Не все дети болеют тяжело. Нередко наблюдается бессимптомное течение заболевания. Такие дети переносят болезнь легко, но становятся источником инфекции для других людей.
Ротавирусная инфекция у ребенка в 2-3 года похожа на другие кишечные инфекции – и по одним только симптомам бывает сложно поставить диагноз. Поэтому обычно врач назначает обследование – предлагает сдать кал на анализ. Узнать, есть ли антитела к инфекции, можно по анализу крови – обычно это делают после выздоровления.
Рвота обычно возникает одновременно с поносом или предшествует ей , бывает повторной и длится 1-2 дня. Жидкий стул сохраняется до 3-7 дней, у грудничков – до двух недель. Чем младше ребенок, тем тяжелее он переносит заболевание.

Ротавирусная инфекция опасна обезвоживанием организма. Дегидратация чаще возникает в раннем возрасте. Поэтому если подозревается ротавирус у ребенка до года, сразу рекомендуется госпитализация . В более старшем возрасте лечение проводят дома – при стабильном состоянии пациента. Но это решение должен принять врач.
Дегидратация (обезвоживание) возникает в разгар болезни и сопровождается ухудшением самочувствия. Ребенок становится капризным и вялым, реже мочится, жалуется на жажду и сухость во рту. Груднички могут плакать без слез. Отмечается сухость кожи и слизистых оболочек, учащается дыхание и сердцебиение. Могут быть судороги, потеря сознания. При появлении таких симптомов медлить нельзя – нужно вызывать скорую помощь!
Лечением кишечной инфекции должен заниматься только врач!
Если вы подозреваете ротавирусную или другую инфекцию у ребенка – обратитесь к врачу. Он проведет обследование и подберет лечение с учетом вероятной причины заболевания.
Профилактика кишечных инфекционных заболеваний у детей
Чтобы кишечная инфекция не усложнила жизнь, рекомендуется:
Тщательно мыть руки после прогулки, посещения туалета.
Выбирать продукты с нормальным сроком годности, которые хранятся в подходящих для них условиях.
Пить только кипяченую воду или из проверенных источников.

Против некоторых кишечных инфекций разработаны вакцины, позволяющие предупредить опасное заболевание. Обсудите со своим педиатром, стоит ли привить вашего ребенка, чтобы защитить его от тяжелой инфекции.
- 1. Диагностика и лечение острых кишечных инфекций у детей. Л. Н. Мазанкова, С. Г. Горбунов. Методические рекомендации для врачей. Москва, 2012.
- 2. Ротавирусные вакцины. Документ по позиции ВОЗ. Эпидемиологический бюллетень, 2013.
- 3. Клинические рекомендации по диагностике и лечению ОКИ у детей в зависимости от типа диареи. А.А. Новокшонов, Л.Н. Мазанкова, В.Ф. Учайкин. Лечение и профилактика, 2013, №4 (8).
- 4. Острые кишечные инфекции у детей в практике педиатра: возможности диагностики и терапии. Д.В. Усенко, А.А. Плоскирева, А.В. Горелов. Вопросы современной педиатрии, 2014; 13 (3).

- Врач акушер-гинеколог (ЮУГМУ, педиатрический факультет, специализация на кафедре акушерства и гинекологии)
Пройдите тест и узнайте, находится ли ваш малыш в группе риска по развитию аллергии.

Цена от Клуба Baby&me

Цена от Клуба Baby&me

Цена от Клуба Baby&me

Цена от Клуба Baby&me

Статья неполная: начало есть, а конец смазан. Что по данной теме можно в конце написать? Только одно: срочно обращайтесь к врачу. Это опасно.
Статья неполная: начало есть, а конец смазан. Что по данной теме можно в конце написать? Только одно: срочно обращайтесь к врачу. Это опасно. И еще одно, ДЕЛАЙТЕ ПРИВИВКУ, которая в национальный календарь не входит, а от этого ужаса спасает.

Как вспомню ротовирус, так вздрогну. В Турции переболели со старшим (ему тогда 4 года почти было) и беременная младшим сыном переболела
Как вспомню ротовирус, так вздрогну. В Турции переболели со старшим (ему тогда 4 года почти было) и беременная младшим сыном переболела
Очень часто слышу от знакомых про данную инфекцию, но специально не интересовалась что это такое. Хорошая статья
Очень часто слышу от знакомых про данную инфекцию, но специально не интересовалась что это такое. Хорошая статья

Ротавирусная инфекция — одна из самых частых причин инфекционных диарей у детей.

Для профилактики ротавирусной инфекции проводится комплекс мероприятий, цель которых — предупредить инфекционные заболевания, имеющие фекально-оральный.

Основные методы диагностики и лечения ротавирусной инфекции. Что делать при появлении первых симптомов, чем лечить и как вылечить ротавирус у детей.
Мы контролируем ситуацию и продолжаем поставки детского питания в магазины. Если у вас есть вопросы, обращайтесь на нашу горячую линию.
Мы считаем, что грудное вскармливание является идеальным питанием для младенцев, и всецело поддерживаем рекомендацию Всемирной организации здравоохранения об исключительно грудном вскармливании в течение первых шести месяцев жизни ребенка. Также мы признаем, что грудное вскармливание не всегда может быть доступно для родителей. Какой бы вариант кормления вы ни выбрали, клуб Nestlé Baby&me всегда готов предоставить новейшую научно обоснованную информацию, чтобы вы чувствовали поддержку и были уверены в том, что даете своему ребенку лучшее питание.
с помощью электронной почты или телефона
Войдите в систему, чтобы продолжить узнавать больше о правильном питании на каждом этапе развития вашего малыша!
Введите электронную почту или телефон.
Ссылка для авторизации выслана на e-mail.
ВАЖНОЕ ЗАМЕЧАНИЕ. Мы считаем, что грудное вскармливание является идеальным началом питания для младенцев и полностью поддерживаем рекомендацию Всемирной организации здравоохранения об исключительно грудном вскармливании в течение первых шести месяцев жизни с последующим введением адекватного питательного прикорма вместе с продолжением грудного вскармливания до двухлетнего возраста.
Мы также понимаем, что грудное вскармливание не всегда возможно для родителей, поэтому рекомендуем вам поговорить со своим лечащим врачом о том, как кормить ребенка, и получить совет о том, когда вводить прикорм. Если вы решите не кормить грудью, помните, что такое решение может быть трудно отменить и оно имеет социальные и финансовые последствия. Введение частичного кормления из бутылочки сократит количество грудного молока. Детскую смесь всегда следует готовить, использовать и хранить как указано на этикетке, чтобы избежать риска для здоровья ребенка.
Читайте также:

