Обязательно исследовать трихинеллез лошадей
Обновлено: 22.04.2024
Для цитирования:
Скворцова Ф.К., Успенский А.В. Диагностика трихинеллеза на ранних стадиях развития личинок. // Российский паразитологический журнал. – М., 2016. – Т.35. – Вып. 1 . – С.
For citation:
Skvortsova F. K., Uspensky A.V. Diagnostics of trichinosis in the early stages of larval development. RussianJournalofParasitology, 2016, V.35, Iss.1, pp.
ДИАГНОСТИКА ТРИХИНЕЛЛЕЗА НА РАННИХ СТАДИЯХ РАЗВИТИЯ ЛИЧИНОК
Основой профилактики трихинеллеза является обязательная ветеринарно-санитарная экспертиза мяса всех используемых в пищу туш свиней, кабанов, барсуков, медведей, других всеядных и плотоядных животных методами компрессорной трихинеллоскопии и пептолиза мышечной ткани зрелых личинок трихинелл. Подтверждение диагноза на трихинеллез зависит от многих факторов, в числе которых значится отбор образцов мышечной ткани от определенных наиболее инвазированных частей туши, метода исследования и используемого оборудования.
В число таких факторов также входит стадия развития паразита в течение биологического цикла до заражения нового хозяина. Единичные ювенильные личинки трихинелл появляются в миофибриллах мышечной ткани уже на 5-7-й дни после заражения, то есть с начала миграции по крови. Развитие личинок до инвазионной стадии возможно только в поперечно-полосатой мускулатуре, где они проходят сложный органогенез и увеличиваются в длину более чем в 10 раз. (Геллер Э.Р., Тимонов Е.В.,1969). Длительная миграция личинок ведет к накоплению их в мышцах к 25-30 суткам в зависимости от интенсивности инвазии.
Вопросу об инвазионности личинок трихинел всегда уделялось большое внимание. Трихинеллы становятся нвазионными на 16-17-й день после заражения, когда у большинства личинок заканчивается органогенез (Лемишко П.М.,1947,1948, 1949).
По данным Richels (1955) на 17-19 день после заражения кутикула личинок становится непроницаемой и стойкой в отношении влияния химических веществ. Устойчивость мышечных трихинелл к действию желудочного сока объясняется своеобразным строением кутикулы. Геллер Э.Р. и Е.В.Тимонов (1969)) считают, что личинки трихинелл приобретают устойчивость к перевариванию с 17-го дня после заражения и с этого возраста становятся инвазионными.
По Березанцеву Ю.А. (1969) только с 19-го дня единичные личинки бывают заметными в мышцах при трихинеллоскопии.
Некоторые разногласия авторов в сроках достижения инвазионности и образования начальной капсулы объясняются использованием для заражения различных изолятов и даже видов трихинелл или их хозяев.
Отсутствие четко различимой капсулы у инвазионных личинок в раннем возрасте (16-24 сутки после заражения) затрудняет постановку диагноза. Так на практике при исследовании мяса на трихинеллез компрессорным методом трихинеллоскописты ищут инкапсулированных трихинелл, то есть трихинелл, спирально свернутых и окруженных капсулой. Это объясняется тем, что существующие руководства и методические положения по диагностике трихинеллеза направлены на выявление в основном инкапсулированных личинок (у капсулообразующих трихинелл) и редко упоминают свернутых в виде скрепки личинок бескапсульных трихинелл T. pseudospiralis или личинок на ранних стадиях развития.
Таким образом, часть инвазионных неинкапсулированных личинок или личинок с формирующейся капсулой на ранних стадиях развития могут оказаться невыявленными. Особенно это актуально при спонтанном заражении промысловых животных и обычной при этом невысокой интенсивности инвазии.
Следовательно, в ранние сроки после заражения (16-24 сутки) затруднительно обнаружить в мышечной ткани мигрирующие личинки трихинелл без капсул или с формирующейся капсулой компрессорным методом, который чаще всего применяется в повседневной практике.
Целью нашей работы являлась диагностика неинкапсулированных личинок трихинелл на ранних стадиях развития компрессорным методом и методом пептолиза на аппаратах для выделения личинок. Метод пептолиза широко внедрен в производство и становится незаменимым в спорных случаях для подтверждения диагноза трихинеллеза.
Материалы и методы
Материалом для исследования служили образцы мышечной ткани от экспериментально зараженных Trichinella spiralis крыс. Всего было заражено 18 беспородных белых крыс весом 90-100г в дозе 10 л/г. Для проведения ранней диагностики при трихинеллезе крыс убивали с 6 по 24 день после заражения.
В первую очередь исследовали компрессорным методом наиболее поражаемые и доступные мышцы: диафрагму, массетер и грудные мышцы при увеличении (х 25, 50, 100). На каждый срок сделаны микрофотографии личинок на срезах.
Диагностика неинкапсулированных личинок трихинелл компрессорным методом
В период формирования в мышечных волокнах инвазионной личинки в ней происходят сложные преобразования. Личинка увеличивается в длину, при этом начинается формирование внутренних органов и вырабатываются защитные приспособления на реакцию хозяина для существования на мышечной стадии. Выявление в мышечной ткани личинок трихинелл юных мигрирующих личинок при обычном увеличении трихинеллоскопа (х50) или МБС микроскопа (х25-50) затруднительно, так как в начале развития личинки располагаются по длине мышечных волокон и имеют лишь незначительные изгибы, легко маскируясь мышечной тканью. Срезы мышечной ткани для изучения должны быть предельно тонкими.
При компрессорном исследовании установили, что небольшое количество новорожденных личинок появляется в мышечных волокнах уже на 6-й день после заражения, куда заносятся по капиллярам с током крови. В мышечном волокне юная личинка располагается вдоль его. Однако, увидеть личинки на срезе крайне сложно даже при увеличении х100, но около среза в выделившейся жидкости наблюдали светлые юные личинки даже при увеличении х25.
Рис. 1. Личинки T. spiralis в жидкости возле среза на 10-е сутки после заражения
В мышечных волокнах личинки располагались вдоль оси волокна, заметить их возможно только при увеличении не менее х 100 на очень тонком срезе и при высокой интенсивности инвазии исходного образца.
Через 11-12 дней в жидкости возле среза возрастало число выделившихся личинок разных размеров и с разной степенью дифференциации органов (Рис.2).
Рис. 2. Личинки T. spiralis в жидкости возле среза на 13-е сутки после заражения
Вокруг пораженных волокон иногда видны воспалительные клеточные инфильтраты (х100).
Через 13-14 дней личинки разных размеров хорошо видны в жидкости возле срезов в разных стадиях органогенеза, часть из них со сформированной пищеварительной системой и зачатками половых гонад (х 50).
На мышечном срезе прямые ровные личинки трихинелл длиной около 0,3 ммв единичных случаях можно обнаружить под сарколеммой мышечного волокна по его длине при увеличении х 100.
Через 15 суток в жидкости возле среза видно большое количество разновозрастных личинок на разных стадиях органогенеза. Выделяются единичные личинки темного цвета, согнутые в дугу или в полукольцо. Длина отдельных личинок достигает 0,5 мм (Рис. 3).
Рис. 3. Личинки T. spiralis в жидкости возле среза на 15-е сутки после заражения
На срезе ткани прямые личинки, расположенные по длине мышечного волокна, плохо просматриваются даже при х 100. Первые попавшие в волокна единичные трихинеллы начинают скручиваться, изгибаться дугообразно или в виде петли.
Через 16 суток множество личинок разных размеров видны в жидкости возле среза. Наряду со светлыми и почти прозрачными юными личинками встречаются единичные темные личинки с оформленной пищеварительной и половой системами длиной до 0,6-0,7 мм.
В мышечной ткани встречались личинки с изогнутыми концами, свернутые дугообразно, в виде овала или петли, редко – свернутые спиралью (х100).
Через 17 и 18 суток. Личинки трихинелл разных размеров в большом количестве видны в жидкости возле срезов, среди них увеличилось число темных подвижных личинок длиной до 0,8 мм (Рис. 4)
Рис. 4. Личинки T. spiralis в жидкости возле среза на 17-е сутки после заражения
В мышечной ткани накопилось значительное количество как вытянутых по длине волокон личинок, так и изогнутых дугообразно в виде восьмерок, скрепок или свернутых спирально, которые хорошо видны на тонких срезах при увеличении х 50 и 100.
Через 19 и 20 дней личинки трихинелл разных размеров в большом количестве видны в жидкости возле срезов, среди них выделяются темные подвижные личинки размером до 0,9 мм, свернутые в спираль.
На срезе ткани у значительной части личинок изогнуты оба конца или они различно свернуты в виде скрепок, дуг, восьмерок, спирали, при внимательном изучении их можно заметить при увеличении х 25-50.
Через 21 и 22 дня. Личинки разных размеров видны в жидкости возле среза, но количество светлых юных форм значительно уменьшилось. Большинство выделившихся личинок - темные подвижные размером до 0,9 мм (Рис. 5).
Рис. 5. Личинки T. spiralis в жидкости возле среза на 22-е сутки после заражения
В мышечной ткани преимущественно встречались изогнутые с двух концов или спирально свернутые личинки. Капсулы у таких личинок не просматривались даже при высоком увеличении (х 100).
Через 24 дня в жидкости возле среза видны единичные светлые личинки и полностью сформированные темные подвижные трихинеллы в большом количестве длиной до 1 мм.
В мышечной ткани вокруг некоторых личинок с трудом различали тонкие капсулы, которые видны при х 50 и 100. Большинство личинок изогнуты дугообразно или скручены в спираль без заметных границ капсулы и хорошо видны при трихинеллоскопии.
Таким образом, выявление неинкапсулированных трихинелл на ранних стадиях развития требует дополнительного внимательного просмотра жидкости вокруг среза ткани при максимальном увеличении. Появление в выделившейся жидкости личинок на разных стадиях органогенеза говорит о заражении трихинеллами. Личинки с малопроницаемой темной кутикулой с полностью сформированной пищеварительной и половой системами появляются через 16 полных суток после заражения.
Тонкая соединительная капсула у личинок просматривается у единичных личинок обычно на 23-24сутки после заражения.
При исследовании на трихинеллез необходимо тщательно исследовать срезы и жидкость, выделяемую возле них, так как нельзя быть уверенными в пригодности мяса вследствие всегда невысокой инвазии трихинеллами при спонтанном заражении.
Диагностика неинкапсулированных трихинелл методом автоматизированного пептолиза
При пептолизе мышечной ткани 6 инвазированных трихинеллами крыс в дозе 10 л/г, с 10 по 15 сутки после заражения при микроскопировании в осадке личинок не обнаружили.
Через 16 суток после заражения крыс в образцах мышечной ткани от 2 крыс после пептолиза обнаружили 17 и 38 подвижных трихинелл (0,34 и 0,76 л/г). Личинки имели плотную слабопроницаемую кутикулу и сформированную пищеварительную и половую системы. Длина личинок не превышала 0,7 мм.
Выделенными личинками заразили две белые мыши. Через 36 дней после пептолиза мышечной ткани мышей обнаружили в небольшом количестве живые трихинеллы.
Через 17 суток в образце мышечной ткани после пептолиза обнаружили 176 подвижных трихинелл (30,5 л/г). Длина личинок составляла 0,8 мм. У личинок была хорошо выражена пищеварительная и половая системы и отчетливо заметен ректум. Личинками были заражены две мыши. После пептолиза мышечной ткани через 35 дней выявили высокую зараженность мышей трихинеллами.
Через 19 суток в образце обнаружили 877 личинок трихинелл длиной до 1.2 мм с законченным органогенезом (170,5 л/г). По длине ректума легко можно было различить половую принадлежность трихинелл (самцов и самок). Личинками заразили 10 мышей в дозе 10 л/г. Зараженность мышей через 32 дня оказалась очень высокой.
Через 21 сутки в образце обнаружили 920 личинок трихинелл (180,4 л/г).
Через 24 сутки – 985 личинок (190,7 л/г).
Таким образом, при пептолизе автоматизированным методом мышечной ткани крыс, инвазированных личинками T.spiralis, установили, что личинки в возрасте с 10 по 15 сутки после заражения данным методом не выявляются. Единичные трихинеллы, начиная с 16-дневного возраста, выявляются при микроскопировании, несмотря на недостаточные размеры личинок. Массовое выделение трихинелл начинается с 17-го дня после заражения, когда большая часть личинок достигает инвазионности.
Неинкапсулированные трихинеллы 16-дневного возраста становятся инвазионными, что показало успешное заражение белых мышей личинками, выделенными после пептолиза. По результатам биопробы основная масса личинок становится инвазионными к 19-20 дням после заражения.
Таким образом, автоматизированным методом пептолиза мышечной ткани легко диагностировать заражение животных неинкапсулированными личинками трихинелл, что затруднительно или иногда невозможно при компрессорном исследовании. Диагностика трихинеллеза автоматизированным методом наиболее эффективна при достижении личинками инвазионности.
2. Геллер Э.Р., Переверзева Э.В. // Мат. научн. конф. ВОГ- Ч.4.- М.-1965.-С.42-46.
4. Лемишко П.М. //Ветеринария.-1947.-№ 5.-С.37.
5. Лемишко П.М. // Ветеринврия.-М.-1948.-№ 11.-С.36-37.
7. Силакова Л.Н. // Мат. докл. Всесоюз. конф. по проблемам трихинеллеза человека и животных.- Вильнюс.- 1972,- С.63-66.
Что такое тениоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Тениоз (Taeniosis) — паразитарное заболевание человека, вызываемое половозрелой стадией ленточного гельминта (свиного цепня), который проникает в организм человека при употреблении плохо приготовленного мяса, паразитирует в тонком кишечнике и вызывает расстройства пищеварения. В некоторых случаях может осложняться цистицеркозом — паразитированием в тканях организма личинок свиного цепня, что приводит к серьёзным последствиям и даже смерти.
Возбудитель
- домен — эукариоты;
- царство — животные;
- тип — плоские черви;
- класс — ленточные черви;
- отряд — циклофиллиды;
- семейство — тенииды;
- род — Taenia;
- вид — свиной цепень (Taenia solium).
Свиной цепень (устаревшее название "cолитёр") — это плоский (ленточный) паразитический червь, длина которого в кишечнике человека достигает 3 метров, а по данным Ц ентра по контролю и профилактике заболеваний США (CDC) его длина может достигать 7 метров. Как правило, паразитирует только 1 червь. Паразит имеет головку, шейку и тело. Тело червя (стробила) состоит из члеников (п роглоттидов), их число может достигать 1000 . Головка (сколекс) размерами до 2 мм в диаметре имеет хоботок и 4 мышечные присоски (органы прикрепления), расположенные крестообразно. На хоботке есть крючья в количестве от 22 до 32, из-за этого есть второе название паразита — вооружённый цепень.
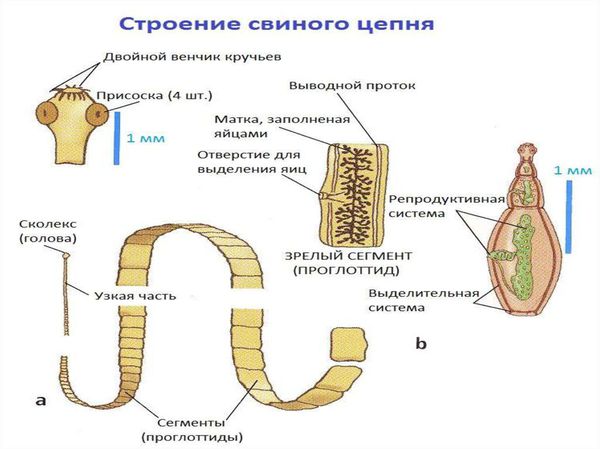
Яйца паразита попадают с калом человека в окружающую среду. Животные (свиньи, собаки, кошки и даже человек при несоблюдении гигиены) поедают яйца, зародыши проходят через кишечную стенку и разносятся кровью по всему организму, после чего оседают в тканях (в основном в соединительной ткани между мышцами). Через пару месяцев яйца превращаются в финны (цистицерки), которые живут до 5 лет, после чего они погибают и обызвествляются (накапливают минеральные вещества, соли кальция). Цистицерки имеют вид полупрозрачных беловатых пузырьков диаметром до 1,5 см, внутри видна мелкая сформированная головка.
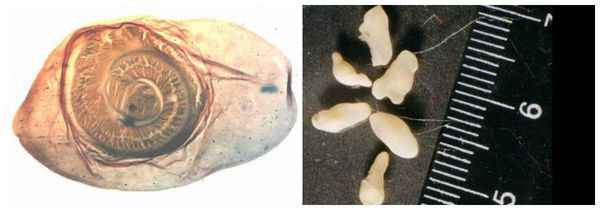
Для полноценного развития свиного цепня необходима смена хозяев за его жизнь. Человек является окончательным хозяином. В его кишечнике паразитирует взрослый гельминт, который развивается за 2 месяца из финны (личинки червя в тканях), съеденной с мясом. Паразит прикрепляется к стенке тонкого кишечника и растёт, поглощая пищу и постепенно наращивая членики (от шейки), которые по мере созревания отрываются и выходят в окружающую среду при дефекации. Паразит может жить в кишечнике десятки лет.
Человек может стать и промежуточным хозяином (при поедании яиц). В этом случае для паразита наступит "экологический тупик" — он не сможет развиться до половозрелой стадии и продолжить свой род, потому что мясо человека с финнами никто не ест.
Яйца выживают в окружающей среде в течение нескольких месяцев в зависимости от условий. Высыхание могут выдерживать в течение 10 месяцев, способны зимовать под снегом, в воде живут до 4 месяцев. При кипячении погибают практически мгновенно, при 65 °С сохраняют жизнеспособность в течение 3 минут, при 20-25 °С под воздействием прямых солнечных лучей сохраняются до 2 дней, если они закрыты травой — до полутора месяцев. Раствор хлорной извести 10-20 % убивает яйца за 5-6 часов. Цистицерки в мясе погибают при его замораживании при температуре -12 °С и поддержании в толще мяса температуры не ниже -10 °С в течение 10 дней [1] [2] [9] [10] .
Эпидемиология
Тениоз является одним из древнейших известных заболеваний. Первые упоминания встречаются ещё в 16 веке до нашей эры (Древний Египет), имеются записи Аристотеля и Гиппократа (финноз свиней). В настоящее время ВОЗ относит тениоз и цистицеркоз к группе забытых ("пренебрегаемых") болезней, т. е. тех, о которых мало говорят и обращают внимание развитые страны.
Распространение повсеместное, но наиболее поражены отдельные регионы: Индия, Африка, Южная Америка, Азия, Северный Китай, Восточная Европа, Белоруссия, Украина. Это регионы, где уровень дохода низкий или ниже среднего, где люди едят много плохо приготовленной свинины и недостаточно соблюдается гигиена. Здесь цистицеркоз является причиной эпилепсии в 30 % случаев, а в некоторых областях, где свиньи и люди живут вместе — до 70 %, по данным ВОЗ [3] . В РФ в среднем выявляется до 500 случаев в год [11] . Есть тенденция к повышенной заболеваемости сельских жителей и работников свиноводческих хозяйств.
Механизм передачи фекально-оральный, путь заражения пищевой. Источник инфекции и окончательный хозяин — заражённый человек, выделяющий с фекалиями яйца гельминта. Промежуточные хозяева — иногда человек, но чаще животные, которые поедают корм, загрязнённый фекалиями человека: свиньи (отсюда происходит название вида), кабаны, обезьяны, собаки, кошки.
Факторы передачи:
- При тениозе — недостаточно термически обработанное мясо свиней или диких кабанов. Наиболее опасно мясо, не прошедшее ветеринарный контроль. В этом случае человек заражается, поедая финны, т. е. зародыши червя, с инфицированным мясом.

- При цистицеркозе — загрязнённые яйцами пища и объекты внешней среды при несоблюдении людьми правил гигиены. Фактором передачи также может быть аутоинвазия, когда у человека с паразитом в кишечнике из-за нарушения перистальтики ЖКТ яйца из кишечника попадают в желудок. Т. е. яйца свиного цепня заразны и опасны для человека сразу, как только покидают организм с каловыми массами. Поэтому риск заражения цистицеркозом есть для любого человека, особенно если пренебрегать правилами гигиены и правилами обработки пищевых продуктов (тщательное мытьё) [1][3][5][7][11] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тениоза
Множество случаев заражения и болезни проходит бессимптомно или малосимптомно. Жалобы таких больных обычно незначительны и связаны в основном с расстройствами пищеварения. Примерно через 1-1,5 месяца от момента заражения (а может и раньше) может наблюдаться лёгкое недомогание, головокружение, слабость, нарушения сна, умеренные головные боли, раздражительность, сниженный или повышенный аппетит, тошнота, дискомфорт и несильные боли в разных отделах живота. Развиваются запоры, чередующиеся с диареей, возможен анальный зуд, больной может умеренно худеть.
Характерной особенностью является периодическое (раз в несколько месяцев) выделение с калом оторвавшихся члеников паразита начиная с 2-3 месяцев паразитирования и так десятки лет. Их хорошо видно невооружённым глазом. Могут быть симптомы гипохромной анемии (недостатка железа): бледность кожи и слизистых, быстрая утомляемость при физической нагрузке, шум в ушах, обмороки, чувство мурашек по коже. Развивается гиповитаминоз В1 (тёмно-красный сухой язык со сглаженными сосочками). В результате отравления организма продуктами жизнедеятельности паразита, а также из-за расстройства пищеварения повышается склонность к необъяснимым высыпаниям токсико-аллергического характера на коже.

Тениоз у беременных
У беременных заболевание может протекать более тяжело, что обусловлено характерными физиологическими процессами в организме женщины этого периода. Наиболее часто наблюдаются расстройства пищеварения (запоры, диарея), тошнота, рвота, снижение гемоглобина, зуд кожи, перианальный зуд. Может быть плохой набор веса у плода. Вследствие более частого нарушения желудочно-кишечной перистальтики (моторики) повышается риск заброса яиц паразита в желудок и развития цистицеркоза [1] [4] [6] [10] .
Патогенез тениоза
Во время паразитирования свиной цепень повреждает слизистую при помощи крючьев и присосок, что вызывает расстройство пищеварения и нарушает моторику кишечника. Кроме того, гельминт потребляет много важных для человека питательных веществ, микроэлементов и отравляет организм продуктами своей жизнедеятельности, что приводит к токсико-аллергическому отравлению.
При заглатывании яиц паразита извне или при рефлюксной болезни, когда нарушается моторика кишечника и яйца из кишки попадают в желудок, развивается цистицеркоз. В различных органах и тканях развиваются соединительнотканные капсулы, содержащие зародыш — цистицерк. Вокруг наблюдаются воспалительные изменения в виде аллергической реакции и дистрофически-атрофические изменения из-за механического давления на окружающую ткань.
При локализации в головном мозге вокруг капсулы наблюдается воспаление мелких сосудов и инфильтрация окружающей ткани плазматическими клетками, что вызывает расстройство движения спинномозговой жидкости (ликвора), отёк мозговой ткани, развитие менингита и энцефалита. При паразитировании в оболочках мозга у его основания возможно развитие рацемозной (ветвистой) формы цистицеркоза до 25 см в длину.
С течением времени (до 5 лет) цистицерк претерпевает дегенеративные изменения — происходит его набухание и разложение (расплавление), что сопровождается усилением токсического и местного воспалительного воздействия. Исходом гибели личиночной формы паразита является кальцификация и местное рубцевание. Специфичных симптомов при этом процессе нет, после полной гибели цистицерков болезнь заканчивается, если, они не находятся в жизненно важных органах [1] [5] [6] [9] .
Классификация и стадии развития тениоза
По Международной классификации болезней 10-го пересмотра (МКБ 10):
- Тениоз:
- B68.0 Инвазия, вызванная Taenia solium.
- B68.9 Тениоз неуточнённый (при подозрении на болезнь, но отсутствии лабораторного подтверждения).
- Цистицеркоз:
- B69.0 Цистицеркоз центральной нервной системы (судороги, эпилепсия, необъяснимая рвота).
- B69.1 Цистицеркоз глаза (нарушения зрения, слепота).
- B69.8 Цистицеркоз других локализаций.
- B69.9 Цистицеркоз неуточнённый [1][2] .
Осложнения тениоза
Острый аппендицит. В правой половине живота снизу постепенно нарастают боли, появляется тошнота, характерен субфебрилитет (температура тела от 37,1 до 38,0 °С). В анализе крови наблюдается нейтрофильный лейкоцитоз со сдвигом влево — повышенный уровень нейтрофилов с преобладанием незрелых форм, которые не могут в полной мере осуществлять защитную функцию.
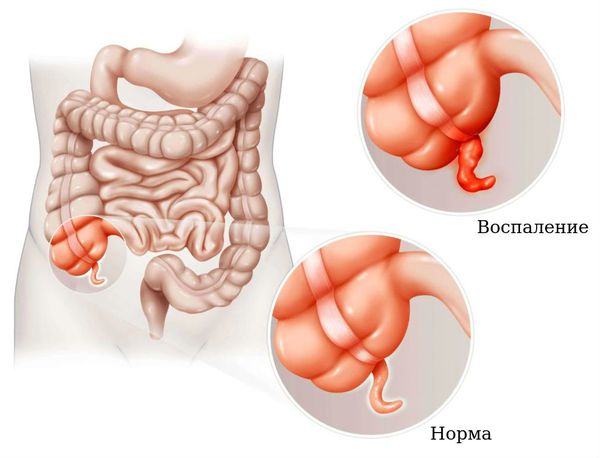
Панкреатит ( воспаление поджелудочной железы) . Характеризуется тошнотой, рвотой, опоясывающими болями в животе.
Кишечная непроходимость. Симптомы — с хваткообразные боли в животе без связи с приёмом пищи, запоры, метеоризм, вздутый живот, учащение пульса, рвота, бледность кожи.
Холангит ( воспаление жёлчных протоков) . Субфебрильная или фебрильная лихорадка, выраженные боли в правом подреберье, озноб, повышенная потливость, тошнота и рвота, желтуха и кожный зуд.
Гипохромная анемия. Бледность кожи и слизистых оболочек, повышенная утомляемость, чувство мурашек и покалывания, головокружения, шум в ушах, обмороки.
Цистицеркоз. Может быть осложнением тениоза, а может быть отдельным заболеванием. В основном симптоматика проявляется при поражении центральной нервной системы (ЦНС) — головного и спинного мозга и глаз. В зависимости от локализации возникают головные боли различной интенсивности, рвота, эпилептические припадки, нарушения речи, расстройства личности, бред и галлюцинации, деменция. При поражении глаз могут наблюдаться воспалительно-дистрофические процессы в различных отделах глаз — рецидивирующие конъюнктивиты, увеиты, отслоение сетчатки, атрофия глазного яблока, что может привести к слепоте. При поражении сердца могут возникать нарушения ритма. При поражении мышц и подкожной клетчатки иногда может наблюдаться некоторая болезненность при ощупывании и приподнятость этого участка в виде подкожного плотного опухолевидного бугорка [1] [5] [5] [8] .
Диагностика тениоза
Тениоз или цистицеркоз может быть заподозрен на основании следующих признаков:
- эпиданамнез — проживание на территории развитого свиноводства, употребление плохо приготовленной свинины, низкий социально-экономический уровень страны или региона;
- расстройства пищеварения;
- астено-невротические проявления — слабость, повышенная утомляемость, эмоциональная нестабильность, раздражительность, повышенная потливость;
- выход с калом неподвижных члеников паразита;
- развитие неврологической симптоматики (эпилепсия), патологии органов зрения.
Дифференциальная диагностика
Основывается на данных анамнеза, типичном виде члеников паразита и их микроскопическом исследовании.
Лабораторная диагностика
Клинический анализ крови — изменений может не быть, иногда наблюдаются гипохромная анемия, умеренное повышение эозинофилов, повышение скорости оседания эритроцитов (СОЭ), редко выявляется небольшое повышение лейкоцитов за счёт сегментоядерных клеток (наиболее большой группы иммунных клеток).
Общий анализ мочи — как правило, без отклонений.
Биохимический анализ крови — возможны отклонения при развитии осложнений:
- При холангитах — повышение маркеров нарушения выработки или оттока желчи: АСТ, ГГТ, ЩФ, общего билирубина.
- При панкреатитах — повышение амилазы.
- При поражении сердца — повышение ЛГД и КФК-МВ.
Серологические специфические исследования:
- Иммуноферментный анализ (ИФА) антител IgG — в основном применяются с целью диагностики внекишечного поражения — цистицеркоза, результаты могут быть ложноположительными;
- Иммунный блоттинг — более точный метод лабораторного исследования сыворотки крови на присутствие антител , который применяют для подтверждения результатов ИФА. Этот метод позволяет снизить число ложных результатов, но в РФ он недоступен.
ПЦР кала — выявление антигенов свиного цепня. Это достаточно чувствительный метод, однако может дать ложноотрицательный результат ввиду ограниченного количества материала в кале.
Копроовоскопия — микроскопическое изучение кала с целью обнаружения яиц и зрелых члеников паразита. По яйцам невозможно установить точный диагноз, т. к. они очень похожи на яйца других представителей этого рода, проводится не менее трёх раз в разные дни. Для определения вида паразита необходимо исследование члеников.
Инструментальная диагностика
Компьютерная (КТ) и магнитно-резонансная томография (МРТ), ультразвуковое исследование (УЗИ), прямая офтальмоскопия — применяются для выявления цистицеркоза. КТ лучше выявляет кальцификаты цистицерков (особенно небольшие). МРТ больше подходит для обнаружения цистицерков в некоторых трудновизуализируемых местах мозга, также МРТ указывает на местные окружающие изменения (отёк) и возможную гибель паразита.
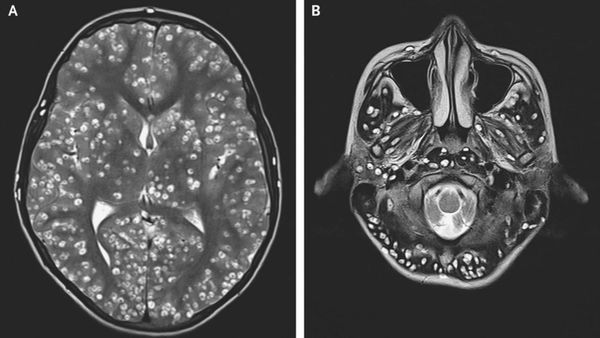
Исследования спинномозговой жидкости при поражении цистицерками ЦНС (лимфоцитарный плеоцитоз, увеличение уровня эозинофилов, белка).
Биопсия — морфологическое исследование биоптатов при оперативном вмешательстве [1] [3] [6] [10] .
Лечение тениоза
Госпитализации подлежат больные с тяжёлыми сопутствующими заболеваниями, а также больные с цистицеркозом ЦНС и глаз. Остальные больные могут лечиться амбулаторно.
В качестве этиотропной терапии (направленной на уничтожение возбудителя) применяется Празиквантел и Никлозамид. Есть данные об эффективности Альбеназола, но они ограничены. Продолжительность лечения — 3 дня.
При лечении цистицеркоза выбор способа уничтожения паразита зависит от его локализации и количества. При локализации под кожей и в тканях (кроме ЦНС и глаз) лечение, как правило, не проводят, так как риск последствий от приёма препарата выше пользы от лечения. Однако, если наличие паразита ведёт к каким-то физическим и эстетическим недостаткам, лечение назначается.
При локализации цистицерков в ЦНС и глазах лечение проводят только в условиях неврологического стационара, применяются Празиквантел и Альбендазол в сочетании с глюкокортикостероидами (т. к. есть риск местного воспаления и повреждения нервной системы и глаз).
В качестве мер патогенетической и симптоматической терапии при тениозе могут назначаться средства нормализации моторики кишечника (прокинетики) и микрофлоры кишечника (пре- и пробиотики).
При цистицеркозе головного мозга применяют противосудорожные препараты.
Возможно хирургическое лечение (удаление цистицерков при поражении головного и спинного мозга).
Контроль излеченности тениоза:
- визуальный — осмотры кала (о выздоровлении говорит отсутствие периодического отделения члеников червя);
- 4 отрицательных анализа кала на яйца гельминтов с интервалом в 1 месяц [2][4][5][8] .
Прогноз. Профилактика
При изолированном тениозе прогноз благоприятный. При развитии осложнений, особенно цистицеркозе ЦНС и глаз, прогноз серьёзный: возможно развитие тяжёлых стойких поражений (эпилепсия, слепота) и летальный исход.
Дается обзор отечественных и зарубежных работ по проблеме трихинеллеза. Трихинеллез - паразитарная болезнь человека и животных, вызываемая паразитированием трихинелл, кишечных нематод, личинки которых мигрируют в поперечнополосатые мышцы и там инкапсулируются. Трихинеллез имеет глобальное распространение, хотя уровень заболеваемости человека существенно различается по регионам мира. Заражение человека происходит в результате употребления мяса, содержащего личинки паразита. Клинические проявления болезни варьируют от бессимптомной инфекции до фульминантного заболевания с летальным исходом. Кардинальными признаками трихинеллеза являются отеки век и лица, миалгии, лихорадка, эозинофилия. При тяжелом течении развиваются токсико-аллергический миокардит и менингоэнцефалит. Химиотерапия проводится препаратами группы карбаматбензимидазолов.
The paper revews trichinosis studies conducted by Russian and foreign investigatos. Trichinosis is a parasitic disease of man and animals, which is caused by Trichinella, intestinal nematodes, whose larvae migrate into the cross-striated muscules where they encyst. Trichinosis is found worldwide, although its morbidity rates greatly differ in the world`s regions. It is contracted by ingestion of meat containing the larvae of the parasite. The clinical manifestations vary from asymptomatic infection to fulminant disease leading to death. The essential signs of trichinosis are facial and periorbital edema, myalgia, fever, eosinophilia. Toxic and allergic myocarditis and meningoencephalitis occur with its severe type. Chemotherapy is performed by using drugs from a group of benzimidazole carbamates.
А.М. Бронштейн, МД.
Доктор мед. наук, зав. клиническим отделом Института медицинской паразитологии и тропической медицины им. Е. И. Марциновского МЗ РФ, Москва; проф. кафедры инфекционных болезней и тропической медицины с курсом эпидемиологии Российского медицинского университета. Москва.
В.И. Лучшев.
Доктор мед. наук, зав. кафедрой инфекционных болезней и тропической медицины с курсом эпидемиологии Российского медицинского университета. Москва.
Pr. A.M. Bronshtein, MD.
Head of Clinical Department, Ye.I. Martsinovsky Institute of Medical Parasitology & Tropical Medicine RF Ministry of Health; proffessor of the Department of Infectious Diseases & Tropical Medicine, Russian Medical University, Moscow.
Prof. V.I. Luchshev.
Head, Department of Infectious Diseases & Tropical Medicine, Russian Medical University.
Correspondence to: A.M.Bronstein, Clinical Department, Martsinovsky Institute of Medical Parasitology & Tropical Medicine, Hospital N 24, Pistsovaya St. 10, Moscow 103287, Tel. (095) 285-2669.
Паразит-возбудитель
Таксономия. Возбудители трихинеллеза - нематоды семейства Trichinellidae. В настоящее время описано пять видов трихинелл [1]:
- Trichinella spiralis - распространен повсеместно, паразитирует у домашних свиней, высокопатогенен для человека.
- Trichinella nativa - распространен в Северном полушарии, паразитирует у диких млекопитающих, чрезвычайно устойчив к холоду, патогенен для человека.
- Trichinella britovi - распространен на севере Евразии, паразитирует у диких млекопитающих, малопатогенен для человека.
- Trichinella nelsoni - распространен в Экваториальной Африке, паразитирует у диких млекопитающих, малопатогенен для человека.
- Trichinella pseudospiralis - распространен повсеместно, паразитирует у птиц и диких млекопитающих, не образует капсулы вокруг личинок в мышцах. Патогенность для человека не доказана.
Кроме перечисленных видов генетическим анализом выделено еще три варианта возбудителя, таксономический статус которых не определен [1].
Морфология. Трихинеллы - одни из наиболее мелких из известных нематод - имеют типичное для круглых гельминтов строение длиной от 1 до 4 мм. Только что отродившиеся юные трихинеллы имеют палочковидную форму, длиной 0,1 мм. Ко времени попадания в поперечнополосатую мускулатуру личинки увеличиваются до 0,7 - 1 мм и приобретают форму спирали, вокруг которой начинает образовываться капсула. У человека капсула лимонообразной формы. Размер капсулы 0,3 - 0,6 мм [1, 2].
Биология. При трихинеллезе одно и то же животное сначала выступает в качестве окончательного (кишечные трихинеллы), а затем - промежуточного (мышечные трихинеллы ) хозяина паразита. Заражение происходит при поедании мяса, содержащего живые инкапсулированные личинки трихинелл. В желудке под воздействием пищеварительного сока капсула растворяется, личинки выходят в просвет кишечника и через час активно внедряются в слизистую оболочку кишки. На 4 - 7 сутки после заражения самки начинают отрождать живых личинок. Длительность отрождения личинок может продолжаться 10 - 30 дней. За это время одна самка производит от 1000 до 2000 личинок. Активно проникшие в кровеносную систему личинки током крови могут быть занесены в любой орган. Однако только в поперечнополосатых мышцах возможно дальнейшее развитие паразита. На 3-й неделе после заражения личинки становятся инвазионными и принимают типичную спиралевидную форму. К началу 2-го месяца после заражения в мышцах вокруг личинок формируется соединительнотканная фиброзная капсула, которая через 6 мес начинает обызвествляться [1, 2 ].
Экология. Известно более 100 видов млекопитающих, являющихся хозяевами трихинелл. Заражение происходит при поедании инвазированных животных или их трупов. В качестве хозяев выступают не только хищники и всеядные, но и отдельные виды травоядных животных, например лошади [1, 2 ].
Традиционно разделяют природные и антропоургические очаги трихинеллеза. Однако резкой границы между этими типами очагов не существует, и на многих территориях происходит активный обмен возбудителями между дикими и домашними животными [2].
В окружении человека циркуляция трихинелл происходит преимущественно по цепи: домашняя свинья - крыса - домашняя свинья. Часто свиньи заражаются не только при поедании живых или павших инвазированных крыс, но и трупов собак, кошек, а также сырых или плохо проваренных боенских конфискатов и кухонных отходов. Видимо, таким же путем заражаются собаки и лошади. Описаны вспышки трихинеллеза у лиц, употреблявших в пищу мясо собак и лошадей, а также мясо диких животных: медведей, енотов, лис, барсуков, моржей и др. [3 - 7].
В СССР в начале 80- х годов причиной заболевания людей трихинеллезом служило преимущественно употребление в пищу мяса диких животных, что определялось высоким уровнем пораженности этим гельминтозом диких млекопитающих (до 25 % кабанов и до 70% бурых медведей). В последние годы в России резко увеличилось число заболеваний, связанных с употреблением в пищу мяса домашних свиней. Эта тенденция является отражением увеличения производства свинины индивидуальными производителями. Последние, как правило, незнакомы с необходимыми мерами предупреждения заражения свиней трихинеллезом и грубо нарушают санитарно-ветеринарное законодательство. В результате пораженность поголовья свиней индивидуальных производителей многократно превышает пораженность трихинеллезом общественного поголовья свиней [ 8 ].
Устойчивость возбудителя к воздействию физических факторов
Инкапсулированные личинки трихинелл проявляют жизнеспособность и заразительность в течение 4 мес при сохранении во влажном субстрате после полного разложения трупа инвазированного животного и более 300 дней в условиях, препятствующих полному разложению трупа. Личинки устойчивы к таким видам кулинарной обработки, как соление, копчение, замораживание. В экспериментальных условиях инактивация личинок достигалась нагреванием до 80 ° С и выше. Однако в практических условиях нагревание мяса, содержащего инкапсулированные личинки трихинелл, в микроволновой печи до температуры 81 ° С не обеспечивало инактивации, равно как и обжаривание мяса в масле при температуре 167 ° С в течение 6 мин. Мясо белого медведя после вымораживания при температуре -15 ° С в течение 35 дней сохраняло заразительность для лабораторных животных [2, 9].
Трихинеллез у человека

1. Зименков В.А., Сивкова Т.Н., Доронин-Доргелинский Е.А. Распространение трихинеллеза диких животных в Российской Федерации // Пермский аграрный вестник. 2016. № 4 (16). С. 98–103.
2. Цибезов В.В., Баландина М.В., Черных О.Ю., Шевкопляс В.Н., Алипер Т.И., Верховский О.А. Оценка эффективности иммуноферментного метода диагностики трихинеллеза свиней // Ветеринария Кубани. 2013. № 1. С. 3–5.
3. Мезенцев С.В. Эпизоотология трихинеллеза в Алтайском крае // Бюллетень науки и практики. 2018. Т. 4. № 9. С. 127–134.
4. Саркисян Н.Э. Трихинеллез // Бюллетень медицинских интернет-конференций. 2017. Т. 7. № 6. С. 1081.
7. Гребенкин А.А. Оптимизация ветеринарно-санитарной экспертизы на трихинеллез: дис. … канд. вет. наук: 03.00.19. Москва, 2004. 118 с.
8. Файнфельд И.А., Крылов А.В. Трихинеллез на Дальнем Востоке: распространение, патогенез, клиника, лечение, профилактика // Бюллетень физиологии и патологии дыхания. 2014. № 54. С. 111–115.
9. Шипкова Л.Н., Пескова Т.Ю. Трихинеллез- нематодоз краснодарского края // Международный журнал прикладных и фундаментальных исследований. 2015. № 11–5. С. 771–772.
10. Макарова Т.Е., Бельды В.Н., Отводникова Н.И., Стафеева Т.Н. Трихинеллез. Клиника. Диагностика. Лечение // Здравоохранение Дальнего Востока. 2008. № 2 (34). С. 36–40.
Трихинеллез – зоонозная болезнь, которой подвержены различные виды млекопитающих, птиц и амфибий. Впервые трихинеллез описал немецкий врач Фридрих Зенкер в 1860 г. Заболевание представляет значительную угрозу сельскохозяйственным животным, главным образом – свиньям. Большое значение данный паразитоз имеет и для человека.
Ценкер доказал, что трихинелла – биологическая причина острого, подчас смертельного заболевания. Это открытие считается важнейшим событием XIX века в гельминтологии.
Достоверно известно, что им болели и тысячи лет назад: личинки трихинелл обнаружены в мышечной ткани мумии молодого ткача, жившего на берегах Нила около 1200 года до н.э. Современникам египтянина была известна опасная болезнь, связанная с употреблением свиного мяса . С момента открытия возбудителя по настоящее время проблема трихинеллеза не теряет своей актуальности. Заболевание широко распространено среди диких животных в различных регионах мира, а также в России, что подтверждается многочисленными исследованиями [1].
Трихинеллез относится к природно-очаговым заболеваниям, так как основными носителями и источниками трихинелл являются дикие животные (медведь, барсук, кабан). Свиньи заражаются трихинеллезом при поедании термически не обработанных отбросов и остатков пищи, а также крыс, зараженных трихинеллами. Трихинеллез чрезвычайно широко распространен во всем мире, практически нет ни одного государства, благополучного по данному гельминтозу. Бесконтрольный выпас свиней, торговля свининой, не подвергавшейся ветеринарно – санитарной экспертизе, использование в пищу промысловых животных – всё это создаёт угрозу групповой заболеваемости трихинеллезом людей. В научной среде существуют различные точки зрения на причины возникновения и ареал энзоотий трихинеллеза 2 .
Выделяются синантропные и природные очаги. В первых паpазитаpная система включает в себя в классическом варианте T. spiralis, домашнюю свинью и крысу; другие синантропные животные, такие, как собаки, кошки и пр., хотя и бывают поpажены трихинеллезом, большой pоли в поддержании циркуляции паразита не играют. В пpиpодных очагах паpазитаpная система состоит из T. nativa или T. nelsoni и pазличных диких животных, всеядных и гpызунов. Очаги двух типов могут взаимодействовать между собой: напpимеp, инвазия может заноситься из пpиpоды в поселки и там циpкулиpовать, поскольку свинья воспpиимчива ко всем видам тpихинелл. И наобоpот, показано, что T. spiralis может пеpеходить от свиней на диких животных пpиpодного окpужения синантpопного очага [5].
Развитие тpихинелл pазных видов и у pазличных животных пpоисходит однотипно и включает фазы: кишечную, мигpационную и мышечную. Трихинеллы вызывают инвазии (заболевания) – трихинеллезы. Заражение происходит через мясо, содержащее инкапсулиpованные личинки тpихинелл. В процессе пищеваpения в желудке и двенадцатипеpстной кишке капсулы pазpушаются, что занимает пpимеpно 1 час. Личиночные стадии трихинелл живут в поперечно – полосатой мускулатуре плотоядных и всеядных животных: свиней (домашних и диких), медведей, барсуков, собак, кошек, крыс, мышей и других грызунов, лисиц, норок, волков, шакалов, гиен, а также морских теплокровных животных: моржей, нерп, тюленей, китов. При употреблении в пищу здоровым животным или человеком мяса, содержащего жизнеспособные личинки трихинелл, эти личинки выходят из капсулы и в течение 1–2 суток превращаются в зрелых особей. Взрослые особи дифференцируются на самцов и самок и расселяются по всему тонкому кишечнику, а личинки активно внедряются в поперечно – полосатую мускулатуру [5].
Установлено, что трихинеллезом в России болеют все виды из семейства Felidae и Canidae: волки, шакалы, лисицы, песцы, енотовидная собака, енот-полоскун, куницы, харза, собаки, собственно все виды из семейства псовых; норки, горностаи, ласки, ежи, колонки, хорьки, росомахи, барсуки, рыси, кошки, медведи, свиньи и кабаны, мыши и крысы, сони, белки, сурки, бурундуки, суслики, дикобразы, ондатры, бобры, лемминги, землеройки, куторы, моржи и тюлени [1].
В Российской Федерации ежегодно регистрируется от 30 до 200 случаев заболевания трихинеллезом. За период с 1992 по 2001 годы, трихинеллез свиней постоянно регистрировался на 13 административных территориях.
Наиболее часто инвазия отмечалась в регионах с развитым свиноводством – Краснодарском крае, Северной Осетии, Московской области и в меньшей степени Калининградской, Ростовской, Вологодской и Ленинградской областях и Таймырском автономном округе. В Алтайском и Приморском краях, Камчатской области и других территориях – отмечали единичные случаи инвазии [6].
Повсеместно распространённым является вид возбудителя T. spiralis (Owen, 1835). Объект, обеспечивающий ее существование – домашняя свинья, к котоpой этот вид хоpошо адаптиpован. У свиньи может быть до 12 000 личинок этого вида в 1 г мышц, пpичём они остаются жизнеспособными годами. Жизнеспособность личинок зависит от условий хранения и переработки мяса. Обсемененность мяса может быть большой, но последствия легкими, если жизнеспособность личинок по тем или иным причинам снижена. Хотя личинки трихинелл устойчивы к низким температурам, они все же постепенно отмирают при хранении в замороженном состоянии. Человек заpажается обычно чеpез свинину, котоpая может являться источником инвазии в pазных видах: ваpеная, жаpеная, сыpой фаpш, шашлык, окоpок, сало (с пpослойкой мышечной ткани), колбаса, особенно сыpокопченая, но даже и ливеpная. Опасность мясных продуктов (колбасы и т.п.) домашнего приготовления обычно выше, чем продуктов промышленного производства ввиду того, что при изготовлении последних перемешивается мясо из многих источников, и при попадании одной зараженной туши среди многих заразное начало разбавляется и концентрация личинок в конечном продукте бывает очень низка [5].
Многочисленными исследованиями последних лет конкретизирована не только эпидемиологическая и эпизоотическая обстановка по трихинеллезу в различных регионах нашей страны, но и особенности локализации личинок трихинелл у разных видов хозяев, что имеет большое значение для проведения ветеринарно-санитарной экспертизы туш. Однако, современные научные данные не отражены в действующих ветеринарно-санитарных нормативно-правовых актах. Так, по Н.Е. Косминкову и по Ю.А. Березанцеву (1961) установлено: в свиных тушах наибольшее количество личинок трихинелл содержится в мышцах языка, массетерах, ножек диафрагмы, мышце пищевода, мышцах шеи и в межреберных мышцах [1].
Несмотря на пристальное внимание паразитологов к проблеме эпидемиологии и эпизоотологии трихинеллеза, ситуация по распространению данной инвазии в Российской Федерации остается неблагополучной [1].
Для того, чтобы добиться сокращения численности популяции трихинелл, необходимо помнить, что самым уязвимым местом в биологическом цикле паразита является переход его личинок от одного хозяина к другому, этот переход осуществляется только вследствие трофической цепи. Поэтому все усилия должны быть направлены на разрыв различных трофических уровней, искусственно возникающих в результате хозяйственной деятельности человека и охоты. В синантропных и антропоургических очагах это достигается неукоснительным соблюдением ветеринарно–санитарных правил по разведению, содержанию, уходу, убою и переработке туш домашних свиней – основного источника трихинелл для людей; в природных – соблюдением правил охоты, с обязательным уничтожением туш промысловых животных [3].
Трихинеллез опасен для здоровья и жизни людей, причиняет ощутимый экономический урон свиноводству, в связи с этим необходимо усилить работу ветеринарно-санитарных учреждений по оздоровлению природно-синантропных очагов трихинеллеза. Сложность борьбы с этой инвазией обуславливается ее широким распространением в природном биоценозе, наличием тесных контактов между дикими и домашними животными. Согласно ветеринарному законодательству, в России туши свиней подлежат обязательному исследованию на трихинеллез. Продажа мяса, не прошедшего ветеринарно-санитарный контроль, а также приготовление и реализация мясных блюд из него являются уголовно наказуемым деянием.
Для профилактики необходимо гигиеническое воспитание населения, широкое распространение информации о трихинеллезе через все средства массовой информации. Запрещается убой свиней на дому без ветеринарной экспертизы и трихинеллоскопии. Большое значение имеет проведение дератизации в свиноводческих хозяйствах [8, 1, 10, 4].
Читайте также:

