Очаги хронической инфекции в лор-органах
Обновлено: 25.04.2024
Для цитирования: Зверева Н.Н. Инфекционно-воспалительные заболевания носоглотки и придаточных пазух носа при ОРЗ. РМЖ. 2014;25:1854.
Острые респираторные заболевания (ОРЗ) продолжают занимать значительное место в структуре заболеваемости в различных странах мира, а среди заболеваний инфекционной природы стойко удерживают первое место [1]. ОРЗ – это этиологически разнородная группа острых инфекционно-воспалительных болезней дыхательных путей, сходных по клиническим проявлениям и эпидемиологическим характеристикам, но отличающихся особенностями патогенеза и морфологии, в основе которых лежит воспаление слизистых оболочек (СО) верхних (ринит, назофарингит, фарингит, тонзиллит, эпиглоттит) и/или нижних дыхательных путей (ларингит, трахеит, бронхит, бронхиолит, пневмония) с развитием дистрофии и некроза эпителия и нарушением мукоцилиарного клиренса [2]. В структуре ОРЗ доминирующими заболеваниями являются острые вирусные респираторные инфекции (ОРВИ), на долю которых приходится 90–95% [2]. Причиной ОРВИ могут быть более 200 различных вирусов, представителей 5-ти семейств РНК-содержащих вирусов и 1-го – ДНК:
По данным Роспотребнадзора [3], в прошедшем сезоне длительность эпидемического подъема заболеваемости ОРВИ и гриппом составила 17 нед. При этом превышение эпидемических порогов заболеваемости от 10 до 40% было отмечено в 31 субъекте РФ. Лабораторный мониторинг за гриппом и ОРВИ в структуре идентифицированных за сезон (2009) вирусов гриппа показал, что в европейской части страны преобладали вирусы гриппа А (H3N2), на Дальнем Востоке и в Сибири – вирусы гриппа А (H1N1). На протяжении всего эпидемического сезона в России сравнительно активно выделялись и другие респираторные вирусы: парагриппа 1, 2, 3 типов, аденовирусы, РС-вирусы [3]. На эпидемический сезон 2014–2015 гг. для стран Северного полушария ВОЗ рекомендовала тот же штаммовый состав противогриппозных вакцин, что и в эпидсезон 2013–2014 гг., а именно: А/California/7/2009 (H1N1); А/Texas/50/2012 (H3N2); B/Massachusetts/2/2012 [4].
Согласно рекомендациям ВОЗ, к числу приоритетных групп, подлежащих вакцинации против гриппа, относятся дети в возрасте от 6 мес. до 5 лет [4]. В прошедшем сезоне в РФ эпидемический подъем заболеваемости гриппом и ОРВИ более активно из всех возрастных групп отмечался среди детей в возрасте до 6 лет [3]. Дети первых месяцев жизни болеют ОРВИ и гриппом редко, поскольку находятся в относительной изоляции от источников инфекции. Кроме того, многие из них сохраняют в течение первого полугодия жизни пассивный иммунитет, полученный от матери трансплацентарно с иммуноглобулинами класса G. Наибольшая заболеваемость ОРВИ и гриппом приходится на детей второго полугодия и первых 3 лет жизни, что, как правило, связано со значительным увеличением числа контактов, посещением детских дошкольных учреждений. Ребенок, посещающий детский сад, в течение первого года может болеть ОРВИ до 10–15 раз, на втором году – 5–7 раз, в последующие годы – 3–5 р./год. Снижение заболеваемости объясняется приобретением специфического иммунитета в результате перенесенных ОРВИ [2].
Столь частая заболеваемость ОРВИ в детском возрасте выдвигает эту проблему в число наиболее актуальных в педиатрии. Повторные заболевания существенно влияют на развитие ребенка. Они приводят к ослаблению защитных сил организма, способствуют формированию хронических очагов инфекции, вызывают аллергизацию организма, препятствуют проведению профилактических прививок, отягощают преморбидный фон и задерживают физическое и психомоторное развитие детей. Во многих случаях частые ОРВИ патогенетически связаны с астматическим бронхитом, бронхиальной астмой, хроническим пиелонефритом, полиартритом, хроническими заболеваниями носоглотки и многими другими заболеваниями [2].
Острый ринит и ринофарингит – наиболее часто встречающиеся проявления инфекционно-воспалительного процесса при ОРВИ. Частота ринитов и ринофарингитов у детей составляет около 70% от всех заболеваний верхних дыхательных путей [1]. Ринит (от греч. rhis, род. падеж rhinos – нос) и фарингит (от греч. pharynx – глотка) характеризуются преимущественным поражением слизистых носоглотки. Как правило, острый ринит имеет 3 стадии. Во время 1-й стадии (она длится от 1–2 ч до 1–2 дней) больные испытывают зуд и сухость в полости носа, сопровождающиеся частым чиханием; кроме того, у них возникают головная боль, недомогание, снижается обоняние, слезятся глаза, повышается температура тела. Во время 2-й стадии у больных появляются (как правило, в больших количествах) прозрачные выделения из носа, гнусавость и затрудненность дыхания. Во время 3-й стадии выделения становятся слизисто-гнойными и постепенно проходят, дыхание улучшается. Как правило, при остром рините больные выздоравливают в течение 7–10 дней [6]. Для клинической картины ринофарингита характерны: гиперемия, отечность, зернистость слизистой задней стенки глотки, болезненность при глотании, затруднение носового дыхания, ринорея, чихание, повышение температуры тела от субфебрильных значений до гипертермии. Может появиться кашель, который возникает за счет раздражения при стекании слизи по задней стенке глотки, а также за счет сухости СО глотки при дыхании через рот [7]. Отмечаются симптомы интоксикации в виде слабости, вялости, снижения аппетита.
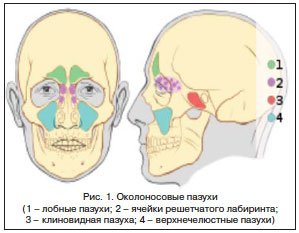
При развитии воспалительного процесса СО полости носа поражается также СО околоносовых пазух (ОНП) [7]. Синусит (от лат. sinus – пазуха) – острое или хроническое воспаление придаточных пазух носа (ППН). Наиболее часто регистрируется воспаление СО верхнечелюстной (гайморовой) пазухи – гайморит, на 2-м месте по частоте встречаемости стоит этмоидит – воспаление решетчатого лабиринта, затем фронтит – воспаление лобной пазухи и сфеноидит – воспаление клиновидной пазухи (рис. 1). Заболевание может быть 1- или 2-сторонним, с вовлечением в процесс одной пазухи или поражением всех ППН с одной (гемисинусит) или обеих (пансинусит) сторон [9, 10].
Ведущая роль в развитии воспалительного процесса в ОНП принадлежит состоянию остиомеатального комплекса (боковой стенки носа, где располагаются соустья пазух носа и узкие ходы между структурами, формирующими эту стенку) и инфекции (вирусной или бактериальной). Вирусная инфекция приводит к повышению продукции секрета слизистых желез и развитию отека СО полости носа, в т. ч. в остиомеатальном комплексе. Естественные соустья ОНП блокируются отечной СО и патологическим секретом. Нарушается вентиляция, давление в ОНП становится ниже атмосферного, усиливается транссудация, а эвакуация слизи нарушается в связи с угнетением мукоцилиарного транспорта вплоть до его полной остановки. Застой секрета, нарушение вентиляции формируют благоприятные условия для присоединения бактериальной инфекции. Микробная флора начинает активно размножаться, процесс из асептического переходит в септический гнойный, и в клинической картине начинают доминировать симптомы инфекционного воспаления ОНП [9, 10].
В случаях внебольничного инфицирования острый синусит чаще всего вызывают Streptococcus pneumoniae и Haemophilus influenzae, которые определяются более чем в 75% случаев заболеваний у взрослых и детей. Cреди других микроорганизмов у взрослых преобладают анаэробные бактерии, стрептококки и Staphylococcus aureus, у детей – Moraxella catarrhalis. При госпитальных синуситах определяются, как правило, грамотрицательные бактерии или стафилококки, а также их сочетания. Вирусы выявляются примерно в 30% случаев острого синусита. Среди них наиболее частыми патогенами являются риновирусы, вирусы гриппа и парагриппа [11].
Согласно европейским рекомендациям, клинический диагноз риносинусита ставится при наличии затруднения носового дыхания и выделений из полости носа или по задней стенке глотки. К дополнительным симптомам относятся ощущение давления или боль в лицевой области, а также снижение обоняния [7]. Острый риносинусит подразделяют на поствирусный, который характеризуется усилением симптомов после 5 дней или сохранением симптомов после 10 дней заболевания ОРВИ, но с общей продолжительностью менее 12 нед., и бактериальный, который характеризуется более тяжелым течением: лихорадкой >38°С, выраженной болью в области лица, гнойным секретом в полости носа [7].
В настоящее время важное место в лечении острых ринофарингитов и риносинуситов отводится грамотно назначенной симптоматической терапии.
Промывание полости носа солевыми растворами способствует лучшему очищению СО носа и элиминации вируса. Изотонические растворы для промывания носа, содержащие такие микроэлементы, как Са, Fе, К, Мg, Сu, способствуют повышению двигательной активности ресничек, активизации репаративных процессов в клетках СО носа и нормализации функции ее желез. Данные средства способствуют разжижению слизи и облегчают ее удаление из носа, усиливают резистентность СО носа к болезнетворным бактериям и вирусам [13].
При применении сосудосуживающих препаратов следует помнить об опасности формирования медикаментозного ринита. В связи с этим сроки использования местных деконгестантов у детей примерно в 2 раза меньше, чем у взрослых, и составляют 3–5 дней. Детям младшего возраста желательно применять препараты короткого действия по причине опасности длительной ишемии не только СО полости носа, но и мозга, что может провоцировать общие судороги [13].
В стадии серозной экссудации рекомендуется применять местные вяжущие средства, содержащие серебра протеинат. Серебра протеинат – это серебросодержащее белковое соединение, обладающее вяжущим, антисептическим и противовоспалительным действием. В аптечные прописи протеинат серебра вошел с 1964 г. – в форме 2% раствора под названием протаргол. Протаргол представляет собой коричнево-желтый или коричневый порошок без запаха, хорошо растворяется в воде, имеет слабогорький вяжущий вкус. Содержание серебра в нем составляет 7,8–8,3% [13]. Из порошка в аптеках готовят 2% растворы, которые используют для наружного применения.
На сегодняшний день существует многолетний опыт успешного применения протаргола при ринофарингитах и риносинуситах. В отличие от сосудосуживающих капель коллоидное серебро воздействует на причину инфекционно-воспалительного процесса ЛОР-органов, подавляя жизнедеятельность возбудителей инфекции и уменьшая воспалительный процесс. Протаргол оказывает бактериостатический и бактерицидный эффекты на штаммы бактерий, вызывающие ОРЗ, такие как Staphylococcus spp., Streptococcus spp., Moraxella spp. и др. [13]. При этом протеинат серебра обладает не только антимикробными, но и противовирусными и иммуностимулирующими свойствами. Так, рядом исследователей было установлено, что ионы серебра имеют выраженную способность инактивировать вирусы гриппа [13], некоторые энтеро- и аденовирусы [14]. Сосудосуживающее действие у данного лекарственного средства достаточно мягкое, что позволяет применять его в течение длительного времени [13].
Протаргол обладает выраженным профилактическим действием, т. к. образует защитную пленку на поверхности поврежденной слизистой, тем самым предотвращая проникновение микроорганизмов в кожу и слизистые.
В отличие от системных АБП протаргол действует селективно, не приводит к развитию дисбактериоза.
При остром рините детям младше 6 лет протаргол назначают по 1–2 капли 3 р./сут, взрослым и детям старше 6 лет – по 2–3 капли 3 р./сут. У детей старше 6 лет и взрослых допустимо использование спрея (по 1 впрыску 3 р./сут). Длительность применения при остром процессе обычно составляет 1 нед., при хроническом рините – 14 и более дней. В этом случае протаргол мягко воздействует на кровеносные сосуды полости носа, суживает их, что уменьшает поступление к СО крови. Отсутствие дополнительного питания способствует тому, что разрастание СО уменьшается или совсем приостанавливается [13].
Более чем 50-летний опыт применения 2% раствора серебра протеината свидетельствует о его хорошей эффективности и высоком профиле безопасности в лечении инфекционно-воспалительных заболеваний носоглотки и придаточных пазух носа при осложнениях ОРЗ.
Очаговая инфекция в практике оториноларинголога
Журнал: Вестник оториноларингологии. 2014;(4): 4‑6
Пальчун В.Т. Очаговая инфекция в практике оториноларинголога. Вестник оториноларингологии. 2014;(4):4‑6.
Pal'chun VT. The focal infection encountered in the practical work of an otorhinolaryngologist. Vestnik Oto-Rino-Laringologii. 2014;(4):4‑6. (In Russ.).
Таким образом формируется острая стадия очага инфекции. Она продолжает прогрессировать, микробы становятся все более защищенными, и в течение 3-4 нед завершается хронизация острого воспаления. Главной характеристикой хронической стадии является то, что иммунные возможности и антибактериальное лечение оказываются недостаточными для полной элиминации инфекции. Консервативное лечение уже не может полностью подавить хронический очаг инфекции в ЛОР-органах, оно может лишь снять обострение процесса.
Элиминация очаговой инфекции (выздоровление) в полостях околоносовых пазух и среднего уха, в небных миндалинах, в гортани может произойти самостоятельно или в результате лечения лишь в острой стадии очаговой инфекции, когда механизмы устойчивости микробов в очаге инфекции еще не полностью сформировались. Эффективность консервативного лечения по этой причине тем выше, чем раньше оно начато, и проводится соответствующими препаратами в адекватной дозировке до завершения воспаления. В противном случае имеется большая вероятность хронизации и возникновения осложнений. Достоверным признаком хронизации наряду с местными симптомами являются последующие обострения воспалительного процесса.
Закономерности развития очаговой инфекции верхних дыхательных путей и уха во многом раскрывает и объясняет взаимосвязь и единство ЛОР-органов с другими органами и системами.
В структуре общей патологии большой удельный вес имеют заболевания ЛОР-органов, представленные в значительной мере острой и хронической очаговой инфекцией. В одних случаях эта инфекция осложняется распространением инфекции и формированием новых заболеваний, сопровождающихся нарушением функционального состояния организма и отрицательным влиянием на течение уже имеющихся болезней, в других - частым переходом инфекции по контакту на соседние или отдаленные органы с формированием тяжелых осложнений.
Кроме этого, осложнения очаговой инфекции верхних дыхательных путей и уха часто сопровождаются отеком (гипертрофией) слизистой оболочки в области очага инфекции, что соответственно суживает (и даже закрывает) выводные протоки полостей (околоносовых пазух, среднего уха) и нарушает их дренаж. Последнее ведет, как правило, к активизации воспалительной реакции окружающих тканей в виде нарастания отека, инфильтрации, образования гнойного экссудата, нарастанию интоксикации организма. При этом возрастает вероятность генерализации инфекции.
Клиническая значимость очаговой инфекции в оториноларингологии, как и во всей медицине, оценивается по характеру развития местного процесса, участию инфекции (или возможности участия) в патогенезе многочисленных местных и общих заболеваний (осложнений).
Практически все острые и хронические воспалительные процессы в оториноларингологии являются очагами инфекции и представляют опасность распространения инфекции по продолжению и контактным путем.
Отмеченные характеристики очаговой инфекции ЛОР-органов хорошо известны, так же как и особенности выбора эффективной (адекватной) лечебной тактики. Тем не менее многие врачи с завидной настойчивостью (и не только оториноларингологи) игнорируют научно обоснованную тактику лечения в этих случаях. При этом в острой стадии очаговой инфекции без учета закономерностей патогенеза нарушается адекватность консервативного лечения, а после хронизации процесса вместо хирургической элиминации инфекции продолжают в течение длительного времени применять консервативное лечение. Результатом является высокий уровень распространенности очаговой инфекции и ее осложнений.
Среди многочисленных очагов инфекции к числу наиболее клинически значимых и распространенных относится хроническая инфекция небных миндалин. Высокая агрессивность этой инфекции обусловлена рядом следующих факторов. В лимфатической ткани (в том числе и в миндалинах) при воспалении не формируется воспалительный защитный вал (выполняющий так называемую барьер-фиксирующую функцию). Эпителиальный покров стенок крипт миндалин в норме имеет множество разрывов, где эпителий отсутствует, а микробы свободно проникают из крипт в лимфаденоидную ткань миндалины и, не размножаясь, погибают, являясь в норме антигеном для выработки иммунитета.
В отличие от нормы при токсико-аллергической форме хронического тонзиллита живые и размножающиеся микробы обнаруживаются не только в лимфаденоидной ткани, но и внутри лимфоцитов, кровеносных и лимфатических сосудов небных миндалин.
Таким образом, иммунопатологическими антигенами в тонзиллярном очаге хронической инфекции являются живые размножающиеся и погибшие микроорганизмы, их токсины и альтерированные клетки миндалин. Эти особенности патогенеза токсико-аллергической формы хронического тонзиллита объясняют активное формирование в миндалинах большого количества иммунопатологических антител и, тем самым, высокую и постоянную интоксикацию и тенденцию к распространению инфекции из небных миндалин, возникновение различных осложнений.
Основным доводом против тонзиллэктомии при хроническом тонзиллите является наличие защитной (иммунной) роли у хронически воспаленных небных миндалин, которую нужно сохранить. Так ли это на самом деле? Следует отметить, что главное в данном случае заключается в том, что в иммунном процессе при хроническом тонзиллите появляется новый фактор - формирование в очаге инфекции, охватывающей всю паренхиму миндалин, иммунопатологических (агрессивных) антител, которые обусловливают токсико-аллергическую реакцию с соответствующей симптоматикой. Ведущим патогеном при хроническом тонзиллите является β-гемолитический стрептококк группы А (БГСА). Клинически диагностируемая без особых затруднений интоксикация при токсико-аллергической форме хронического тонзиллита достоверно свидетельствует о наличии в организме этиологических и иммунопатологических факторов, участвующих в возникновении грозных осложнений. Среди них - острая ревматическая лихорадка (ОРЛ) с необратимыми поражениями сердца, нефрит, поражение суставов и др. Удаление очага инфекции (тонзиллэктомия) в этот период уже не излечит наступившую патологию, оно лишь поможет уменьшить дальнейшее развитие перечисленных осложнений.
Соотношение защитных иммунных процессов в организме и агрессивных иммунопатологических антител в небных миндалинах лежит в основе тяжести патогенеза хронического тонзиллита. Классификация хронического тонзиллита, разделяющая его на простую и токсико-аллергическую формы, предусматривает диагностическую оценку иммуннопатологических (токсико-аллергических) реакций у больных. Наличие и значимость таких реакций является прямым показанием к хирургической элиминации очага инфекции (тонзиллэктомии).
Следует отметить, что небные миндалины в течение первых десятилетий жизни человека выполняют уникальную и, с точки зрения физиологии, парадоксальную функцию формирования в организме ограниченного очага инфекции, который дает антигены для становления иммунитета. Происходит это следующим образом. В лимфаденоидной ткани небных миндалин имеется по 16-18 глубоких древовидно разветвленных щелей (крипт) с общей поверхностью стенок более 250 см 2 . Микрофлора из полостей рта и глотки свободно проникает в крипты и вегетирует в них в оптимальных условиях. Стенки крипт легко проницаемы для микробов, поскольку покрыты слоем эпителия с часто встречающимися изъязвлениями. Таким образом, анатомическое устройство небных миндалин приспособлено для инкубации микрофлоры и поступления ее в паренхиму миндалин, где она является антигеном для выработки иммунитета. В ткани миндалин в норме (при отсутствии клинических признаков воспаления) обнаруживаются лишь тела погибших микробов и только в паренхиме. В то же время при токсико-аллергической форме хронического тонзиллита обнаруживаются и микробный детрит, и живые размножающиеся микробы в паренхиме, внутри сосудов и внутри лимфоцитов. В первом случае интоксикации нет, во втором - подтверждается токсико-аллергическая форма заболевания.
Таким образом, в небных миндалинах действует биологический механизм становления иммунитета посредством очаговой инфекции, уровень активности которой поддерживается общим иммунитетом и должен быть ниже интоксикационного для организма. Достоверным показателем перехода этого механизма в патологическое состояние являются клинические признаки интоксикации.
Наиболее частые местные и общие осложнения очаговой инфекции и связанное с ней ухудшение состояния организма могут быть представлены следующим образом.
В ревматическую группу осложнений, обусловленных в основном острым и хроническим тонзиллитом и фарингитом, входят такие заболевания, как уже упоминавшиеся выше ревматические поражения сердца, суставов, почек, острая ревматическая лихорадка. Часто при хроническом тонзиллите встречается хроническая субклиническая интоксикация организма с разной выраженности нарушениями (или угнетением) функционального состояния организма, практически всегда наступает ухудшение течения имеющихся заболеваний, качества жизни пациента.
К ринологическим осложнениям очаговой инфекции (гайморит, этмоидит, сфеноидит, фронтит) относятся воспалительный инфильтрат и абсцедирование в области щеки, лба, орбиты (флегмона орбиты с поражением зрения). Со стороны глотки и гортани - паратонзиллярный и заглоточный абсцессы, парафарингеальная флегмона, медиастинит, стеноз гортани, евстахиит.
Внутричерепные абсцессы и менингит могут быть рино- и отогенными, так же как и сепсис. Тромбоз сигмовидного синуса и сопутствующий ему сепсис, паралич лицевого нерва, вестибуло-кохлеарные осложнения обычно обусловлены очагом инфекции в среднем ухе.
Теоретические и практические вопросы очаговой инфекции ЛОР-органов, в частности этиология, патогенез, диагностика, лечебная тактика, во многом решены. Во всяком случае настолько, что при правильном их использовании в практической оториноларингологии была бы существенно снижена относительно высокая в настоящее время распространенность очаговой инфекции. Однако на практике крайне неудовлетворительно проводится лечение этой патологии: с большими отступлениями от научно обоснованной и хорошо известной адекватной и эффективной лечебной тактики. Обычно это выражается в том, что назначение лечения часто не соотносится с этапами развития патогенеза очага инфекции и его осложнений: не корректно подобрана, несвоевременно и не ритмично применяется (преждевременно или наоборот - излишне долго проводится стартовая и последующая терапия).
Нарушается режим лекарственной терапии и в острой стадии, а после хронизации - необоснованно длительно продолжается консервативное лечение, в то время как в этот период необходима (без всякого промедления) хирургическая элиминация хронического очага инфекции.
Таким образом, высокая заболеваемость, разнообразие и тяжесть очаговой инфекции и ее осложнений в оториноларингологии широко представлены и связаны со всеми областями медицины. Инфекционная природа локального воспаления в полостях верхних дыхательных путей и среднего уха, ее агрессивный характер, вызывающий патологию иммунной системы с образованием иммунопатологических антител, многообразие форм развития осложнений обусловливают общемедицинскую значимость этой патологии.
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022;
кафедра инфекционных заболеваний у детей ФП и ДПО Санкт-Петербургского государственного педиатрического медицинского университета Минздрава России, Санкт-Петербург, Россия, 194100
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022;
кафедра инфекционных заболеваний у детей ФП и ДПО Санкт-Петербургского государственного педиатрического медицинского университета Минздрава России, Санкт-Петербург, Россия, 194100
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022
Персистирующие инфекции у детей с хроническими заболеваниями ЛОР-органов: возможности этиотропной терапии
Журнал: Вестник оториноларингологии. 2015;80(5): 46‑50
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022;
кафедра инфекционных заболеваний у детей ФП и ДПО Санкт-Петербургского государственного педиатрического медицинского университета Минздрава России, Санкт-Петербург, Россия, 194100
Цель работы — этиологическая диагностика и этиотропная терапия 176 детей в возрасте от 2 до 12 лет с хронической патологией ЛОР-органов в зависимости от длительности заболевания: до 1 года (n=72), от 1 года до 2 лет (n=54) и более 2 лет (n=50). Использовались бактериологический метод для определения характера микрофлоры верхних дыхательных путей и молекулярно-биологический методы для выявления ДНК вируса Эпштейна—Барр, цитомегаловируса и вируса герпеса человека 6-го типа в крови и слюне. В терапии всех детей использовались препараты рекомбинантного интерферона курсом 1—1,5 мес, в 41% случаев в сочетании с антибактериальной терапией, с последующей иммунокорригирующей терапией индукторами интерферона (79,4% пациентов) или бактериальными лизатами (20,6%). Показана доминирующая роль герпесвирусов 4, 5 и 6-го типов в формировании хронической ЛОР-патологии у детей, постепенное снижение активности герпесвирусных инфекций у детей с длительностью процесса более 2 лет. Наиболее частыми бактериальными агентами, определяемыми из носо- и ротоглотки детей с хронической ЛОР-патологией, были Staphylococcus aureus и Streptococcus pyogenes, а также грибы рода Candida, частота выявления которых не зависела от длительности патологического процесса. Эффективность этиотропной терапии снижалась с течением времени с 78% на 1-м году заболевания до 30% при длительности процесса более 2 лет.
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022;
кафедра инфекционных заболеваний у детей ФП и ДПО Санкт-Петербургского государственного педиатрического медицинского университета Минздрава России, Санкт-Петербург, Россия, 194100
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022;
кафедра инфекционных заболеваний у детей ФП и ДПО Санкт-Петербургского государственного педиатрического медицинского университета Минздрава России, Санкт-Петербург, Россия, 194100
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022
Отдел респираторных инфекций Научно-исследовательского института детских инфекций ФМБА России, Санкт-Петербург, Россия, 195022
Формирование хронической патологии ЛОР-органов, распространенность которой у детей в России составляет от 181,9 до 465,0 на 1000 [1], тесно связано с частым и затяжным течением респираторных заболеваний. Доля часто и длительно болеющих (ЧДБ) в детской популяции остается стабильно высокой и составляет от 20 до 65% в разных возрастных группах. В 40% случаев к 7—8 годам у ЧДБ детей формируется хроническая патология, при этом риск хронизации прямо пропорционален увеличению кратности эпизодов острых респираторных инфекций (ОРИ) в течение года [2].
С персистенцией вирусных и бактериальных возбудителей, возникающей на фоне иммуносупрессии и усугубляющей ее, в последние годы связывают рецидивирующее течение респираторных заболеваний. По нашим данным, у ЧДБ детей в подавляющем большинстве случаев выявляются маркеры активной Эпштейна—Барр (ВЭБ), цитомегаловирусной (ЦМВ) и/или герпес-6-го типа вирусной (ВГЧ-6) инфекции. При бактериологическом исследовании из носо- и ротоглотки патогенная и условно-патогенная микрофлора в этиологически значимом количестве (>10 4 КОЕ/мл) определяется у половины ЧДБ детей [3, 4].
Наиболее часто у детей формируется хроническая аденотонзиллярная патология. Острый аденоидит является реакцией лимфоидного органа на антигенную стимуляцию (чаще вирусами) [5]. При персистенции инфекционного агента аденоидит приобретает затяжное и хроническое течение. Доля детей, больных хроническим аденоидитом и тонзиллитом, колеблется от 20 до 50% [6, 7]. Эпштейна—Барр вирусная инфекция является одной из наиболее частых причин хронического воспалительного процесса в носоглотке с выраженной гипертрофией глоточной миндалины, что приводит к формированию стойкой обструкции верхних дыхательных путей и нарушению носового дыхания [8—10].
Помимо ВЭБ, в ткани глоточной миндалины персистируют и другие вирусы. По данным S. Herberhold и соавт. [11], методом полимеразной цепной реакции (1ТДР) в образцах ткани глоточной миндалины людей, не болевших ОРВИ, в 97% случаев были обнаружены вирусы респираторной группы, при этом в 83% образцов выявлено более двух вирусов. Наиболее часто из образцов глоточной миндалины выделяли аденовирус (80%), вирус герпеса 7-го типа (51%), вирус герпеса 4-го типа (ВЭБ) (43%), энтеровирус (31%) [12].
В этиологии хронического аденоидита большую роль играет также хроническая бактериальная инфекция. При этом микроорганизмы формируют биопленку (сообщество бактериальных клеток, покрытых экзополисахаридным матриксом), которая является своеобразной защитой как от факторов неспецифического и специфического иммунитета, так и от антибактериальной активности лекарственных препаратов [13, 14].
Наиболее актуальными при хроническом воспалении в носоглотке считают S. pneumoniae и H. influenzae. У детей с хроническим аденоидитом пневмококк обнаружен в 50% случаев, гемофильная палочка — в 66,7% [15]. С поверхности глоточной миндалины наиболее часто выделяли Н. influenzae (64,4%), М. catarrhalis (35,6%) и S. aureus (33,3%). По данным отечественных авторов, основным возбудителем при хроническом аденоидите является S. aureus, высеваемый почти у 50% пациентов [17].
Цель исследования — определить частоту персистирующих инфекций у детей с хронической патологией ЛОР-органов и оценить возможности этиотропной терапии с учетом длительности заболевания.
Пациенты и методы
Под наблюдением находились 176 детей от 2 до 12 лет, обратившихся по поводу рекуррентного течения респираторных заболеваний с поражением верхних дыхательных путей в амбулаторно-поликлиническое отделение и отделение респираторных (капельных) инфекций ФГБУ НИИДИ ФМБА России. У всех детей, включенных в данное исследование, диагностировали гипертрофию аденоидов II—III степени, у 87 детей (49%) — сочетанную с гипертрофией небных миндалин II—III степени. Клиническое обследование и анализ медицинской документации показали, что в наблюдаемой группе ЧДБ детей хронический аденоидит был диагностирован у 142 (80,7%), рецидивирующий синусит — у 41 (23,3%), хронический тонзиллит — у 37 (21,0%), рецидивирующий отит у 28 (15,9%) детей.
Помимо клинико-лабораторного обследования, включавшего клинический анализ крови, общий анализ мочи, биохимический анализ крови с определением уровня аланинаминотрансферазы и антистрептолизина-О (АСЛ-О), пациентам проводили исследование крови и слюны с использованием ПЦР для выявления ДНК герпесвирусов 4-го типа — ВЭБ, 5-го типа — ЦМВ и герпеса 6-го типа (тест-системы производства ФГУН ЦНИИЭ Роспотребнадзора, Москва).
Полуколичественным бактериологическим (культуральным) методом оценивали качественный состав аэробной и факультативно анаэробной микрофлоры слизистой носо- и ротоглотки.
Дети были объединены в три группы в зависимости от длительности заболевания (табл. 1).

Таблица 1. Распределение детей с хронической ЛОР-патологией в зависимости от длительности заболевания
Высокая частота определения молекулярно-генетических маркеров герпесвирусной инфекции у детей с хронической ЛОР-патологией явилась обоснованием для назначения данной категории детей препаратов интерферона и индукторов интерферона с противовирусной, иммуномодулирующей, а также антилимфопролиферативной целью, что важно для пациентов с гиперплазией лимфоидной ткани в носо- и ротоглотке.
Терапия включала в себя поэтапное применение препаратов интерферона (ректальные или оральные формы) в течение 30—40 дней и индукторов интерферона в течение 20—50 дней. Виферон получали 56,2% детей, генферон — 11,9%, кипферон — 10,8%, реаферон-ЕС-липинт — 21,1%. При наличии гнойного процесса в носо- и/или ротоглотке или высеве β-гемолитического стрептококка группы, А противовирусная терапия интерфероном сочеталась с антибактериальной в 41,0% случаев (антибиотики и местные антисептики). В случае диагностированной стрептококковой инфекции (высев β-гемолитического стрептококка группы, А или повышение АСЛ-О) после 10—14-дневного курса антибиотика дети получали бициллинотерапию в течение полугода (15,9% пациентов). В качестве индуктора интерферона у 38,6% пациентов использовали изопринозин, у 14,7%) — амиксин, у 11,9% — циклоферон и у 14,2% — анаферон детский. 20,6% детей с диагностированной бактериальной носоглоточной инфекцией после курса интерферона получали системные лизаты (рибомунил — 13,6%), бронхомунал — 7,0% пациентов).
Эффект терапии оценивали по частоте обострений в течение года после лечения, сохранению жалоб в межрецидивный период (преимущественно на затруднение носового дыхания и храп во сне), наличию и характеру отделяемого из носа вне периода обострения, степени гипертрофии миндалин и аденоидов после лечения и через год.
Статистическая обработка материала проведена с помощью пакета программ Stat Soft Statistica for Windows XP v.7.0. Для случаев нормального распределения признака оценку значимости и достоверности различий средних значений проводили с помощью параметрического t-критерия Стьюдента.
Результаты и обсуждение
ДНК герпесвирусов 4, 5 и 6-го типов на первом году хронического заболевания ЛОР-органов выделяли у подавляющего большинства пациентов, причем как в слюне (95,8±2,3%), так и в крови (83,3±4,4%) (рис. 1). После 2 лет течения патологического процесса в носо- и ротоглотке частота выделения ДНК герпесвирусов 4, 5 и 6-го типов уменьшилась до 70,0±6,4% (p<0,001), причем в половине случаев ДНК удавалось выделить только в слюне, что свидетельствует о снижении активности вирусной инфекции.

Рис. 1. Частота выделения ДНК герпесвирусов 4, 5 и 6-го типов методом ПЦР из крови и слюны детей с хронической ЛОР-патологией в зависимости от длительности заболевания.
ДНК ВЭБ у детей с хронической ЛОР-патологией на первом году заболевания определяли в 63,9% случаев, в более поздние сроки — у 48,1±6,7%. ДНК ЦМВ выявляли на первом году заболевания у 48,6±5,9% детей, а после двух лет — только у 18,0±5,4% (p<0,001). Частота выделения ДНК герпеса 6-го типа также снижалась с 66,7±5,5% у пациентов на первом году хронического заболевания ЛОР-органов до 34,0±6,7% у детей с длительностью заболевания более двух лет (p<0,001).
Обращает на себя внимание снижение частоты выявления смешанных герпесвирусных инфекций (ГВИ). Если у детей 1-й группы смешанную ГВИ диагностировали у 70,8±5,4% пациентов, а моноинфекцию у 25,0±5,1%, то у детей с длительностью заболевания более 2 лет — смешанную ГВИ выявляли только в 24,0±6,0% случаев, а моноинфекцию — у 46,0±7,1% детей (p<0,001). Частота выделения ДНК ВЭБ, ЦМВ и ВГЧ-6 у детей с хронической патологией ЛОР-органов в зависимости от длительности заболевания представлена в табл. 2.

Таблица 2. Частота подтверждения моно- и микст-герпесвирусных инфекций (ВЭБ, ЦМВ и ВГЧ-6) методом ПЦР у детей с хронической ЛОР-патологией в зависимости от длительности заболевани, p±m% Примечание. * — достоверное отличие между показателями 1-й и 3-й групп; ** — достоверные отличия показателей 1-й и 2-й групп по сравнению с показателем 3-й группы.
При бактериологическом исследовании мазков из носо- и ротоглотки частота выделения патогенной и условно-патогенной микрофлоры в диагностически значимом количестве достоверно не отличалась в группах и отмечалась у 56,9±5,8% пациентов из 1-й группы, у 53,7±6,8% во 2-й и у 44,0±7,0% — в 3-й. Чаще других выделяли Staph. aureus, грибы рода Candida и β-гемолитический стрептококк группы, А (табл. 3).

Таблица 3. Частота выделения патогенной и условно-патогенной микрофлоры в диагностическом титре из носо- и ротоглотки ЧДБ детей с хронической патологией ЛОР-органов в зависимости от длительности заболевания, p±m% Примечание. * — достоверное отличие от частоты выделения остальных микроорганизмов, p
Анализ эффективности проведенной консервативной этиотропной и иммунотропной терапии детей с хроническими заболеваниями ЛОР-органов в зависимости от их длительности у ЧДБ детей представлен в табл. 4. Несмотря на то, что консервативная терапия во всех группах достоверно снижала частоту обострений в год, более значимый эффект был получен в группе с длительностью процесса до 1 года, в которой отмечено уменьшение гиперплазии глоточной миндалины как после курса терапии, так и через год после лечения (рис. 2).

Таблица 4. Частота обострений в год у детей с хронической патологией ЛОР-органов до и через 1 год после начала комплексной терапии в зависимости от длительности заболевания, p±m% Примечание. * — достоверное отличие от показателя до лечения, p

Рис. 2. Частота выявления гипертрофии аденоидов III степени у детей с хронической ЛОР-патологией до и после комплексной терапии в зависимости от длительности заболевания.
Нормализация носового дыхания и купирование воспалительного процесса в носо- и ротоглотке (отсутствие патологического отделяемого из носа в межрецидивный период) отмечалась у 77,8±4,9% пациентов с длительностью заболевания до 1 года, в 55,6±6,8% случаев при длительности от 1 года до 2 лет и только в 30,0±6,5% случаев при длительности более 2 лет.
Выводы
1. У ЧДБ детей с хроническими заболеваниями ЛОР-органов в 96% случаев выявлены молекулярно-генетические маркеры активной персистенции герпесвирусов 4, 5 и 6-го типов (ВЭБ, ЦМВ и ВГЧ-6), у половины пациентов — в ассоциации с бактериальными возбудителями.
2. Частота выделения ДНК герпесвирусов 4, 5 и 6-го типов из крови ЧДБ детей с хронической патологией ЛОР-органов снижается с 83% у больных с длительностью заболевания до 1 года до 34% при длительности процесса более 2 лет, однако выделение из слюны сохраняется у 70% таких пациентов.
3. Частота выделения патогенных и условно-патогенных бактериальных возбудителей в диагностически значимом количестве из носо- и ротоглотки детей с хронической патологией ЛОР-органов не зависит от длительности заболевания.
4. Эффективность консервативной этиотропной терапии детей с хронической ЛОР-патологией, сопряженной с гиперплазией аденоидов и миндалин, зависит от длительности патологического процесса и составляет 78% на первом году заболевания и 30% при длительности заболевания более 2 лет.

Наличие очага хронической инфекции в организме не позволяет считать человека абсолютно здоровым до его полной санации, независимо от того, проявляется этот очаг как-либо или нет. Чаще всего этими очагами бывают кариозные зубы, хронический тонзиллит и холецистит. Однако также очагами хронической инфекции также могут выступать придаточные пазухи носа (хронический гайморит, фронтит), уши (хронический средний отит, тубоотит) или даже полость носа (все формы хронических ринитов). Даже если эти очаги никак себя не проявляют, они могут быть причиной самых разнообразных, зачастую весьма тяжелых заболеваний.
Если клинические проявления присутствуют, то ими чаще всего являются симптомы общей интоксикации. Чаще всего они выражены не сильно, имеют непостоянный и перемежающийся характер. Субфебрильная температура без четко выраженной причины, ухудшение аппетита, нарушение сна, повышенная утомляемость, снижение работоспособности — вот наиболее частые жалобы, встречающиеся у носителей хронической инфекции. Весьма часто наблюдаются различные нарушения сердечной деятельности — нарушения ритма, перебои, экстрасистолы, снижение аэробной выносливости. Иногда наблюдаются также тонзиллогенные токсические изменения в миокарде и коронарных сосудах, приводящих к болям по типу ишемических и даже сердечной недостаточности.
Необходимо также помнить, что очаги хронической инфекции зачастую сочетаются и даже связаны друг с другом. Сочетание различных очагов усиливает их неблагоприятное влияние на организм, угнетает иммунную систему и ухудшает общее состояние.
Следует заметить, что особую опасность представляют очаги хронической инфекции, расположенные в небных миндалинах. Именно они являются причиной таких грозных осложнений, как ревматизм и ревматический эндокардит и эндоваскулит, приводящие в дальнейшем к поражению клапанного аппарата сердца и сердечной мышцы с последующей инвалидизацией.
Заметное отрицательное влияние интоксикация из хронических очагов инфекции оказывает также на опорно-двигательный аппарат, в частности, суставы.
Встречаются также упорные головные боли, невротические и психические нарушения, вызванные присутствием в организме очагов хронической инфекции.
Длительное присутствие в организме очагов хронической инфекции неизбежно приводит к отрицательному влиянию инфекционной интоксикации, функциональным, а впоследствии и органическим изменениям в органах, особенно если они своевременно не диагностируются и не лечатся.
Отзывы
Виды санации
С целью санации ЛОР-органов проводятся следующие процедуры:
- промывание;
- ультразвуковое воздействие;
- лазеротерапевтическое воздействие;
- виброакустическое воздействие;
- ультрафиолетовое облучение.
Показания
Показаниями к санации верхних дыхательных путей являются следующие симптомы:
- повышенная температура;
- затруднение дыхания;
- снижение обоняния;
- снижение слуха и болезненные ощущения в области ушей;
- першение, жжение и боль в горле.
При наличии гнойных пробок в гландах осуществляется промывание миндалин. Показаниями к санации полости носа являются скопления секреторных или послеоперационных масс в носу при невозможности их самостоятельного удаления.
Противопоказания
Санация носовых пазух и носовых ходов — такая же обязательная и необходимая процедура, как умывание по утрам, ежедневный приём душа или чистка зубов. Ведь носовая полость выполняет массу важных функций: от согревания и очищения вдыхаемого воздуха до участия в формировании тембра голоса. Каждая околоносовая пазуха и каждый носовой ход — это место скопления гнойных масс и выделяемого слизистого секрета, которые необходимо удалять для поддержания полноценной работы носовой полости и пазух носа. Инфекции поджидают нас везде: на работе, в школе, в детском саду, в транспорте… А путь, по которому попадают в организм бактерии и вирусы, ведёт через слизистую оболочку носовой полости. Именно слизистая выступает как своеобразный фильтр, на котором задерживаются болезнетворные микроорганизмы, инородные частицы и аллергены. По статистике на слизистой оседает до 80% патогенной микрофлоры, содержащейся во вдыхаемом воздухе. Необязательно проводить промывание каждого носового хода или пазухи ежедневно. Достаточно проводить санацию полости носа на регулярной основе, не забывая, насколько важны для организма здоровые пазуха и слизистая носа.
Также санация носового хода и около-носовых пазух проводится при таких заболеваниях и состояниях, как: острый и хронический гаймориты; острый и хронический риниты; различные виды синуситов; выделения гнойных масс из носовых ходов; затруднённость носового дыхания; болевые ощущения в области носа.
Санация наружного слухового канала (НСК) — гигиеническая процедура, преследующая несколько целей:
- Удаление из слухового канала биологических загрязнений (ушная сера).
- Обработка слухового канала антимикробными, противовоспалительными, обезболивающими лекарственными средствами.
Небные миндалины — это скопления лимфоидной ткани, которые расположены в углублении между языком и мягким небом.
В том случае, если у человека диагностирован тонзиллит в хронической форме, врач осматривает всю слизистую оболочку ротовой полости пациента. Цель терапии — это восстановление структуры миндалин и обязательная стабилизация иммунитета.
Методики промывания лакун миндалин
Промывание лакун небных миндалин — простая процедура, однако ее должен проводить только врач-отоларинголог. Специалисты не рекомендуют выполнять ее самостоятельно в домашних условиях. Существует вероятность того, что болезнь начнет прогрессировать и возникнут осложнения. Также в ходе манипуляции велика вероятность травмировать миндалины или небо.
Наиболее распространенные способы промывания миндалин с помощью:
Подготовка к процедуре
Перед манипуляцией ЛОР-врач изучает историю болезни пациента с целью исключения возможных противопоказаний. При необходимости назначает дополнительные лабораторно-инструментальные исследования: общеклинический анализ крови и анализ мочи, рентгенографию грудной клетки и электрокардиографию.
Непосредственно перед промыванием необходимо отказаться от приема пищи. В период лечения не рекомендуется употреблять твердую пищу, которая может поранить внутреннюю оболочку небных миндалин.
Стоимость услуг
Читайте также:

