Омепразол или нольпаза хеликобактер
Обновлено: 18.04.2024
В этой статье продолжаем разговор о заболеваниях различных отделов желудочно-кишечного тракта, возникающих в ходе лечения препаратами группы нестероидных противовоспалительных средств (НПВП). Лекарственные поражения тонкой и толстой кишок — тема настоящей статьи.
При длительном приеме НПВП, особенно в возрасте старше 65 лет, у 60-70 % больных развивается бессимптомное поражение слизистой оболочки тонкой кишки (энтеропатия), которое сопровождается кровопотерей и потерей белка, что в свою очередь приводит к снижению гемоглобина крови (железодефицитной анемии) и альбумина.
Хотя известно, что тонкая кишка является органом, где проходят последние этапы пищеварения и всасывание пищевых ингредиентов, но она является и областью хронической кровопотери у больных, принимающих НПВП. Потеря крови может быть от 1 до 10 мл в сутки, что нарушает обмен железа и приводит к развитию анемии. Не менее часто такие осложнения возникают при приеме малых доз аспирина, назначаемых с целью профилактики сердечно-сосудистых и церебральных заболеваний.
Ранее было показано, что аспирин-индуцированные энтеропатии могут развиться при краткосрочном приема аспирина в течение 1-2 недель, в том числе и в кишечнорастворимой форме его и в виде свечей. Такие повреждения слизистой как петехии (точечные кровоизлияния), эрозии встречаются в 20-60% случаев и более серьезные – язвы до 10%.
Причины повреждения
В настоящее время предложена теория многофакторного повреждения слизистой тонкой и толстой кишки (энтероколопатии).
Первым повреждающим фактором являются сами препараты НПВП и аспирина и их метаболитов, которые могут непосредственно действовать на клетки слизистой тонкой и толстой кишок (энтероциты и колоноциты) и нарушать барьерную функцию слизистой и повышать ее проницаемость для бактерий и токсинов. Считается, что развитие анемии является маркером повышенной проницаемости слизистой и воспаления тонкой кишки у больных, длительно принимающих НПВП.
Токсины являются вторым повреждающим фактором, вызывающим местный воспалительный процесс, который усугубляется агрессивным действием желчи и ферментов, пищей и бактериями, находящимися в просвете кишечника. Местное воспаление способствует повышению кишечной проницаемости для желчных кислот и метаболитов НПВП, что повреждает клетки слизистой оболочки кишечника.
Важным фактором повреждения слизистой является изменения микробиоты (микрофлоры) кишечника. Показано, что грамм-отрицательные микроорганизмы усиливают неблагоприятное эффект НПВП на слизистую, а пробиотики (лактобациллы и бифидобактерии) защищают слизистую. Кроме того, некоторые микроорганизмы в процессе своей жизнедеятельности выделяют фермент глюкуронидазу, под воздействием которой разрушаются НПВП и их метаболиты и, всасываясь, увеличивают неблагоприятный эффект воздействия на слизистую кишечника.
Важным является тот факт, что применение антисекреторных препаратов, снижающих кислотность желудочного сока (ИПП, Н2блокаторы гистамина), которые назначаются часто одновременно с НПВП, способствуют избыточному росту, изменению состава и качества микроорганизмов в просвете кишечника. Применение этих препаратов при поражении нижних отделов желудочно-кишечного тракта не только не предотвращают, но поддерживают неблагоприятное воздействие НПВП на слизистую кишечника.
У людей старше 65 лет поражение кишечника при приеме НПВП увеличивается в 4 раза, при приеме Н2 блокаторов гистамина – в 4 раза, ИПП – в 5 раз, избыточный рост в кишечнике грамм-отрицательной флоры увеличивает риск в 6.5 раз.
В развитии энтеропатии могут иметь значение снижение защиты слизистой тонкой кишки и прежде всего простагландинов (о которых мы подробно говорили в статье «Лекарственные поражения желудка«), а также сосудистые поражения тонкой кишки.
Клинические проявления
Длительный приём НПВП и аспирина или их сочетание может сопровождаться диареей (поносами), снижением массы тела, слабостью, недомоганием, болями в животе, снижением аппетита, связанными с нарушениями всасывания железа, низким гемоглобином и недостатком витамина В12. Но чаще случаи энтеропатий протекают бессимптомно или невыраженными клиническими проявлениями (в 60-70 % случаев).
Несколько слов о причинах развитии дефицита железа при НПВП-энтеропатиях. Известно, что часто при назначении НПВП как защита слизистой назначаются антисекреторные препараты (чаще ингибиторы протонной помпы — ИПП), которые снижают кислотность желудочного сока и тем самым затрудняют переход 3-валентного железа, содержащегося в пище в 2-валентное, которое во много раз быстрее всасывается в тонкой кишке. Возникает недостаток всасывания железа в кишечнике при его дефиците. У пациентов с энтеропатиями снижается аппетит вследствие активного воспаления в слизистой тонкой кишки или нарушений в желудке и как результат уменьшение приема пищи.
Диагностика НПВП и аспирин-индуцированной энтеропатии
Общий алгоритм
- Анамнез пациента – прием НПВП или аспирина более 2 недель.
- Исключение лечения антибиотиками.
- Клинические проявления.
- Результаты лабораторно-инструментального обследования:
- анализ крови клинический (на выявление железа — и В12-дефицитной анемии) — гемоглобин, эритроциты, железо, ферритин, В12, гомоцистеин),
- белки и белковые фракции (альбумин!),
- анализ кала на скрытую кровь,
- кальпротектин в кале, повышение которого может быть выявлено уже через 7 суток после приема НПВП и аспирина,
- водородный тест с глюкозой для исключения синдрома избыточного бактериального роста в тонкой кишке,
- микробиологический анализ кала.
- Рентгеноскопия желудочно-кишечного тракта – продвижение (пассаж) бария по тонкой кишке.
- Видеокапсульная эндоскопия (выявление петехий, эрозий, язв, источника кровотечения, спаек) в кишечном тракте.
Проведение обычных гастродуоденоскопии и колоноскопии выявляет источник кровотечения около 5% случаев.
Видеокапсульная эндоскопия
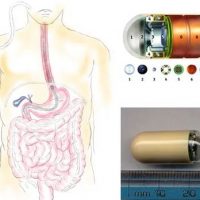
Это обследование имеет большую информативность, оно сделало максимально доступной диагностику повреждений кишечного тракта. Видеокапсульная эндоскопия позволила уточнить частоту лекарственного поражения кишечного тракта.
Согласно современным данным при лечении НПВП и аспирином наблюдаются повреждения кишечного тракта в виде изъязвлений у 30-40% случаев, кровотечения и анемия – у 1/3 больных и воспалительные повреждения слизистой оболочки кишки более чем у 2/3 пациентов. У пациентов, принимавших НПВП на протяжении 3 месяцев, повреждение слизистой оболочки кишечника наблюдается более чем в 50% случаев (по данным капсульной эндоскопии).
На сегодняшний день число кровотечений из верхних отделов желудочно-кишечного тракта за последнее десятилетие уменьшилось в два раза, но количество кишечных кровотечений возросло в два раза. До 40% кровотечений в желудочно-кишечном тракте приходится на кишечник, к которым приводят даже короткие курсы приема НПВП и малые дозы аспирина. При сочетании приема НПВП и ацетилсалициловой кислоты (аспирина) чаще возникают кишечные кровотечения, чем желудочные.
Профилактика и лечение НПВП/аспирин – энтероколопатий
В настоящее время обсуждаются различные подходы к профилактике НПВП поражений слизистой кишечника. Испытываются препараты различных групп:
- антибактериальные средства (Метринидазол, Трихопол, Рифаксимин), которые уменьшают количество грамм-отрицательных бактерий в кишечнике,
- 5-аминосалициловой кислоты (сульфасалазина, салафалька),
- противовирусные препараты (алиспоривир),
- блокаторы бактериальной глюкуронидазы,
- пробиотики и др.
Ребамипид (Ребагит)
Одним из немногих препаратов, доказавших свою клиническую эффективность в предупреждении НПВП поражения как верхних отделов желудочно-кишечного тракта, так и нижних отделов, является Ребамипид (Ребагит) – индуктор синтеза эндогенных простагландинов, стимулятор функции защиты слизистой желудочно-кишечного тракта (ЖКТ).
Свойства Ребагита
Клинические и собственные результаты использования этого препарата позволяют еще раз обратить внимание на положительные свойства его для предупреждения и лечения НПВП/аспирин индуцированных поражений слизистой кишечника (энтеро- и колопатий):
- повышает синтез простагландинов в слизистой желудочно-кишечного тракта, что сопровождается повышением синтеза защитной слизи и бикарбонатов, стимуляцией кровообращения,
- под воздействием его увеличивается число грамм-положительных лактобацилл и уменьшается количество грамм-отрицательных бактероидов и клостридий в кишечнике,
- уменьшается выраженность воспаления в поврежденной слизистой оболочке ЖКТ, восстанавливает поврежденную слизистую кишечника (цитопротективный эффект).
С помощью капсульной видеоэндоскопии доказана способность в 4 раза уменьшить риск развития повреждений слизистой тонкой кишки у добровольцев, принимающих Диклофенак (Вольтарен) + ИПП.
Исследования подтвердили способность препарата предупреждать повреждения кишечника при проведении монотерапии НПВП, при частом использовании в клинической практике НПВП+ ИПП, НПВП/аспирин+ИПП.
Результаты исследований по данным капсульной эндоскопии показали, что препарат достоверно способствует заживлению повреждений при НПВП-индуцированной энтеропатии, профилактизирует появление новых повреждений, улучшает обменные (метаболические) процессы в слизистой оболочке кишечника, повышая уровень белка.
Результаты исследований
Интересны исследования, проведенные зарубежными учеными в последние годы. Не была доказана способность ИПП (в частности, лансопразола) профилактизировать НПВП-индуцированные поражения кишечника.
В 2013 году было установлено, что омепразол (ИПП) не оказывает протективного действия на слизистую оболочку тонкой кишки при приеме НПВП.

Обнадеживающие результаты были получены при изучении эффективности Ребамипида, который показал заживляющий и защищающий эффект при аспирин-индуцированных поражениях слизистой кишечника. Результаты исследования показали негативное воздействие аспирина 100 мг в сутки у всех исследуемых больных. Достоверно меньшее количество петехий (кровоизлияний) и эрозий было отмечено в группах больных, принимающих Ребамипид – 15,5 в сравнении без него – 48,4%. Т.е. достоверно доказано, что препарат обладает профилактическим и лечебным действием аспирин-индуцированных поражений кишечника.
Еще одно исследование: изучалось профилактическое действие Ребамипида при одновременном назначении его с НПВП. Группа А – Диклофенак 75мг/сутки +Омепразол 20 мг+ плацебо (пустышка), Группа Б – Диклофенак 75 мг/сутки+ омепразол 20мг + Ребамипид 100 мгХ3 раза/сутки. Курс 14 дней. Оценка повреждений слизистой кишечника проводилась капсульной эндоскопией до и после 2-х недель приема лекарств. Результаты исследования показали, что в группе с пустышкой среднее количество повреждений на одного человека составило 25, а в группе принимающих Ребамипид – 8,9, т.е. добавление к лечению Ребамипида способствовало трехкратному снижению количества повреждений слизистой оболочки кишечника.
Закофальк
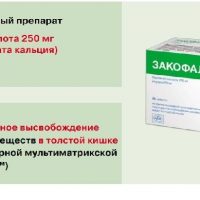
В последнее время представляет интерес комбинированный пребиотик Закофальк, в состав которого входит инулин и масляная кислота. Инулин содержится в клубнях и корнях артишока, одуванчика, топинамбура, злаковых, фруктах, цикории и др., действие его — стимуляция нормальной собственной флоры человек, улучшение всасывания кальция и магния в тонкой кишке, участие в липидном и углеводном обмене.
Масляная кислота – основной продукт бактериального обмена и важнейший энергетический источник для клеток толстой кишки (колоноцитов), регулятор моторной функции кишечника, снижающий воспаление, улучшающий защитный барьер и уменьшающий проницаемость слизистой оболочки толстой кишки. Причем основными продуцентами масляной кислоты являются не бифидобактерии и лактобациллы, а другие группы бактерий, например, эубактерии, фузобактерии, непатогенные клостридии и др.
Закофальк, принимаемый перед едой 3-4 раза в день, обеспечивает постепенное высвобождение компонентов на протяжении всей кишки в течение 24 часов. Курс лечения 30 дней.
Лекарственные поражения тонкой и толстой кишок. Заключение
Любые НПВП и низкие дозы аспирина у большинства больных вызывают повреждения слизистой оболочки кишечника.
Назначения антисекреторных препаратов (ИПП, Н2блокаторов гистамина) в клинической практике не только не защищают, но и усиливают повреждение кишечника, в отличие от верхних отделов ЖКТ.
Единственным доступным препаратом, способным не только предупреждать, но и лечить НПВП-энтероколопатии и НПВП-гастропатии, является Ребамипид.
О фитотерапии лекарственного поражения желудочно-кишечного тракта см. в разделе фитотерапия.
Еще каких‑то 30–40 лет назад диагноз язвенной болезни желудка выбивал почву из‑под ног. Пожизненная диета и бесконечное лечение язвы, которая, несмотря на все ухищрения врачей, прекрасно себя чувствовала в желудке и не собиралась заживать. Сегодня решение найдено. Триумфальное открытие, ставшее ключом к разгадке язвенной болезни, до сих пор придает уверенности ученым. А главное, вселяет надежду тысячам людей, которые ждут новых лекарств от рака, СПИДа и множества других тяжелых заболеваний.

Провизор первой категории и заведующая аптекой. Автор многочисленных работ по фармакологии и фармакотерапии
Язвенная болезнь в мире больших цифр
С каждым годом диагностируется все больше новых случаев заболевания. Медики связывают такую неутешительную тенденцию с широким использованием нестероидных противовоспалительных препаратов, значительно повышающих уязвимость стенки желудка. Однако достижения современной медицины позволяют давать очень благоприятный прогноз при язвенной болезни. А ведь еще в конце прошлого века все было не так однозначно.
Схемы эрадикационной терапии
| Препарат | Доза | Кратность применения |
| Эрадикационная терапия 1 линии (7–10 дней) | ||
| ИПП | стандартная доза | 2 раза в день |
| кларитромицин | 500 мг | |
| амоксициллин | 1г | |
| Терапия 2 линии (10–14 дней) — при неэффективности или непереносимости терапии первой линии | ||
| ИПП | стандартная доза | 2 раза в день |
| метронидазол или амоксициллин | 500 мг (амоксициллин — 1 г) | 3 раза в день (амоксициллин 2 раза в день) |
| тетрациклин | 500 мг | 4 раза в день |
| висмута препарат | 120 мг | |
Методом проб и ошибок
Долгие годы происхождение язвенной болезни трактовалось неверно. Ложные теории становились крепким основанием для ошибочного лечения, не приносившего ожидаемых результатов. В начале XX века врачи склонялись к мнению, что язвенной болезнью желудка человек расплачивается за нервные потрясения. Основой терапии были диета, исключающая все жареное, острое и пряное, и, разумеется, успокоительные препараты. Неудивительно, что на фоне такого лечения выздоровление было весьма сомнительным исходом.
Чуть позже в возникновении язвенной болезни начинают обвинять злосчастную соляную кислоту. Она и только она объявляется первопричиной заболевания. В привычную схему лечения вносятся соответствующие коррективы: основой противоязвенной терапии становятся антациды. Эти препараты, несомненно, облегчали течение язвенной болезни, однако полного излечения гарантировать не могли. Временная ремиссия, наступавшая после курса эрадикационной терапии антацидами, как правило, заканчивалась рецидивом. И только в начале 80‑х годов забрезжила долгожданная и выстраданная миллионами больных истина.
ОткрытиеHelicobacter pylori
После неудачной попытки заразить хеликобактерной инфекцией поросят Маршалл решился на эксперимент, достойный великих исследователей. Он выпил содержимое чашки Петри, в которой культивировались H. pylori, и приготовился к ожиданию. Ученый надеялся, что через год или чуть больше у него смогут диагностировать язвенную болезнь желудка, и он наконец докажет очевидную причинно-следственную связь. Однако события не заставили себя долго ждать.
Спустя три дня после начала эксперимента мать Маршалла заметила, что у сына стало дурно пахнуть изо рта. Вскоре к симптомам присоединилась тошнота и рвота, а всего лишь спустя восемь дней после отчаянного поступка эндоскопическое исследование подтвердило: в желудке врача начался острый гастрит, а из мазка со слизистой была культивирована H. pylori. На 14‑й день эксперимента Маршалл начал принимать антибиотики. После курса лечения было зафиксировано полное выздоровление.
В 1985 году подробности эксперимента появились на страницах Медицинского журнала Австралии. Кстати, вскоре эта статья приобрела всемирную известность и стала самой цитируемой за всю историю издания. Казалось бы, доказательства очевидны и дело — за малым. Однако до полного признания оставалось еще почти десятилетие.
Препараты для эрадикационной терапии(международные и торговые названия)
| Группа | Международное название | Торговое название |
| антибиотики пенициллины | амоксициллин | Оспамокс, Флемоксин Солютаб, Хиконцил |
| антибиотики макролиды | кларитромицин | лабакс, Клабакс ОД, Кларитромицин-Зентива, Кларитромицин Пфайзер, Клацид, Клацид СР, Фромилид, Фромилид Уно |
| антибиотики тетрациклины | тетрациклин | Тетрациклин |
| ингибиторы протонной помпы | омепразол | Зероцид, Лосек, Омез, Омизак, Ортанол, Ромесек, Улкозол, Ультоп, Хелицид, Цисагаст |
| лансопразол | Ланзабел, Ланзап, Ланзоптол, Ланцид, Лоэнзар-сановель, Эпикур | |
| рабепразол | Берета, Золиспан, Зульбекс, Нофлюкс, Онтайм, Париет, Рабелок, Хайрабезол | |
| пантопразол | Зипантола, Контролок, Кросацид, Нольпаза, Пантаз, Панум, Пептазол, Пиженум-сановель, Пулореф, Санпраз, Ультера | |
| эзомепразол | Нексиум, Нео-зекст, Эманера | |
| противомикробные и противопротозойные средства | метронидазол | Клион, Метрогил, Метронидазол, Трихопол, Флагил, Эфлоран |
| гастропротекторы | висмута трикалия дицитрат | Де-Нол, Новобисмол |
Борьба за признание
Только в 1994 году Национальные институты здравоохранения США документально подтвердили тесную связь между H. pylori и язвенной болезнью и рекомендовали лечить ее с помощью антибиотиков. Тем не менее в 1995 году большинство больных язвой желудка по‑прежнему получали антисекреторную терапию, и лишь 5 % счастливчиков встречали врачей, которые назначали антибиотики.
В том же 95‑м Американский фонд здравоохранения провел крупный опрос среди людей, страдающих язвенной болезнью. Результаты были впечатляющими. Спустя более чем 10 лет после открытия H. pylori 90 % пациентов не имели понятия о том, что истинной причиной их заболевания была инфекция, и винили во всем стрессы и слабые нервы.
В 1996 году Американское агентство по контролю за лекарственными препаратами (FDA) впервые в мире одобрило применение антибиотика для лечения язвенной болезни. Еще через год, в тех же Соединенных Штатах, запускается национальная кампания, цель которой — информировать врачей и фармацевтов о связи между язвенной болезнью желудка и H. pylori. Вскоре весть об абсолютной излечимости прежде довольно тяжелого заболевания разлетелась по странам, городам и весям, и началась новая эпоха в терапии язвенной болезни.
Комбинированные препараты для эрадикационной терапии
| Международное название | Торговое название |
| омепразол+амоксициллин+кларитромицин | Пилобакт АМ |
| лансопразол+амоксициллин+кларитромицин | Ланцид Кит, Хелитрикс |
Препараты для эрадикации Helicobacter pylori
Сегодня разработано несколько схем эрадикационной терапии хеликобактер пилори, которые подбираются индивидуально. Традиционный антихеликобактерный комплекс включает:
антибиотик (амоксициллин, кларитромицин или тетрациклин);
ингибитор протонной помпы;
метронидазол;
препараты висмута.
Амоксициллин
Антибиотик пенициллинового ряда, амоксициллин, и структурно, и по спектру активности очень близок к ампициллину. Амоксициллин стабилен в кислой среде. Препарат ингибирует синтез клеточной стенки бактерий, действует и местно, и системно после абсорбции в кровоток и последующего проникновения в просвет желудка. H. pylori демонстрирует хорошую чувствительность к амоксициллину in vitro, однако для эрадикации бактерии требуется комплексная терапия.
Кларитромицин
Кларитромицин, 14‑членный макролид, представляет собой производное эритромицина с аналогичным спектром активности и показаниями к применению. Однако в отличие от эритромицина он более устойчив к воздействию кислот и имеет более длительный период полувыведения. Результаты исследований, доказывающих, что схема тройной антихеликобактерной терапии с использованием кларитромицина дает положительный результат в 90 % случаев, привели к широкому использованию антибиотика. В связи с этим в последние годы было зафиксировано увеличение распространенности устойчивых к кларитромицину штаммов H. pylori.
Тетрациклины
Точкой приложения тетрациклинов является бактериальная рибосома. Антибиотик прерывает биосинтез белка и специфически связывается с 30S-субъединицей рибосомы, исключая добавление аминокислот к растущей пептидной цепи. Тетрациклин доказал in vitro эффективность против H. pylori и сохраняет активность при низком pH.
Ингибиторы протонной помпы (ИПП)
Терапия ИПП доказала свою эффективность в различных клинических исследованиях. Предполагается, что антисекреторные препараты группы ИПП могут способствовать повышению концентрации антимикробных средств, в частности, метронидазола и кларитромицина, в просвете желудка. ИПП уменьшают объем желудочного сока, вследствие чего вымывание антибиотиков с поверхности слизистой уменьшается и концентрация, соответственно, увеличивается. Кроме того, снижение объема соляной кислоты поддерживает стабильность антимикробных препаратов. Различные ИПП не отличаются по эффективности.
Метронидазол
H. pylori, как правило, очень чувствительны к метронидазолу, эффективность которого не зависит от pH среды. После перорального или инфузионного применения в желудочном соке достигаются высокие концентрации препарата, что позволяет достичь максимального терапевтического эффекта. Метронидазол приводит к потере спиральной структуры ДНК H. pylori, в результате чего происходит поломка в ДНК и бактерия погибает.
Препараты висмута
Висмут стал одним из первых препаратов для эрадикации H. pylori. Существуют доказательства, что висмут оказывает непосредственное бактерицидное действие, хотя его минимальная ингибирующая концентрация (МИК — наименьшее количество препарата, ингибирующее рост возбудителя) в отношении H. pylori слишком высока. Как и другие тяжелые металлы, такие как цинк и никель, соединения висмута снижают активность фермента уреазы, который принимает участие в жизненном цикле H. pylori. Кроме того, препараты висмута обладают местной антимикробной активностью, действуя непосредственно на клеточную стенку бактерий и нарушая ее целостность.
Гарантии эффективности — в руках фармацевта?
Эффективность эрадикационной терапии подсчитана и разложена по полочкам. Терапия первой линии успешна более чем в 75 % случаев, а лечение по альтернативной схеме (второй линии) приносит выздоровление 93 % больных. Неудовлетворительный результат лечения объясняется просто: бактерии быстро приспосабливаются к антибиотикам и появляются новые, устойчивые штаммы. Чтобы победить H. pylori, нужно строго соблюдать схему лечения. И недисциплинированный пациент, пытающийся заменить, отменить или отложить прием одного или даже нескольких компонентов эрадикационной терапии, должен знать о поджидающей его опасности.
Ингибиторы протонной помпы (ИПП) — одни из самых востребованных препаратов, без которых не обходится лечение язвенной болезни и других заболеваний пищеварительного тракта, связанных с повышенным образованием соляной кислоты. В эту группу входит всего несколько лекарственных средств, имеющих один механизм действия, сходные показания и побочные эффекты. Но действительно ли их свойства полностью сопоставимы? Мы решили пристально рассмотреть два ингибитора протонной помпы, являющихся препаратами выбора при лечении большинства распространённых заболеваний желудка: омепразол и пантопразол.
Общая информация
Омепразол — первый представитель ИПП, синтезированный ещё в 1978 году и поступивший в клиническую практику спустя 10 лет. Через 40 лет он вошёл в число самых продаваемых лекарств в мире: только в США в 2018 году было выписано 58 миллионов рецептов на это ЛС. Реальные объёмы продаж препарата намного выше, так как одна из его форм принадлежит к ОТС-группе, причём как в РФ, так и во многих других странах мира [1].
Механизм действия
И омепразол, и пантопразол являются производными бензимидазола, что обусловливает схожесть физико-химических свойств и фармакологического действия. Оба препарата относятся к пролекарствам: они образуют активную форму в секреторных канальцах париетальных клеток. Именно в просвет последних выступают участки молекул фермента, ответственного за основной этап выработки соляной кислоты — Н + /К + -АТФ-азы.
Активация омепразола и пантопразола протекает с последовательным присоединением атома водорода к пиридиновому и бензимидазольному кольцам. Главное условие активации — сильнокислая среда, соответствующая таковой в секреторных канальцах париетальных клеток.
После ионизации омепразол и пантопразол уже не могут проникать через клеточную мембрану и накапливаются внутри канальцев. Концентрация препаратов в просвете секреторных канальцев в 1000 раз выше, чем концентрация в крови и в париетальной клетке. Примечательно, что пантопразол концентрируется в просвете канальцев медленнее, чем омепразол: время, необходимое для 50 % блокады Н + /К + АТФ-азы омепразолом и пантопразолом составляет 400 и 1100 секунд, соответственно. Таким образом, омепразол активируется быстрее, чем пантопразол, и связывается с протонным насосом в более краткие сроки [2, 3].
Результаты исследования in vitro показали, что омепразол достигает максимального ингибирования протонного насоса через 20 минут после приёма, а пантопразол — через 30 минут.
Фармакокинетические и фармакодинамические свойства
Омепразол и пантопразол отличаются друг от друга, как минимум, по двум фармакокинетическим показателям.
Биодоступность омепразола составляет 35 % при однократном применении и 60 % — при приёме курсом, в то время как биодоступность пантопразола при курсовой дозе достигает 77 %. Следует отметить, что, несмотря на существенную разницу в биодоступности препаратов, их клиническая эффективность в равных дозах не сопоставима. По результатам исследований, кислотоблокирующий эффект 20 мг омепразола сопоставим с эффективностью пантопразола в дозе 40 мг [4].
Время до достижения максимальной концентрации в плазме крови для омепразола составляет 0,5–3,5 часа. Пантопразол достигает максимальной концентрации через 2–3 часа после приёма. Очевидно, что разница между верхней и нижней границами достижения этого показателя не позволяет корректно сравнивать препараты и сделать определённый вывод.
Эффективность
За последние десятилетия был проведён ряд исследований, в которых изучалась сравнительная эффективность разных доз омепразола и пантопразола у различных категорий пациентов.
- Два слепых рандомизированных исследования подтвердили сопоставимую клиническую эффективность омепразола 20 мг в сутки и пантопразола 40 мг в сутки при язвенной болезни двенадцатиперстной кишки за 2, 4 и 8 недель лечения [5, 6].
- Результаты мультицентрового двойного слепого исследования показали сопоставимую эффективность омепразола 20 мг в сутки и пантопразола 40 мг в сутки при рефлюкс-эзофагита через 8 недель терапии [7].
- По результатам метаанализа при лечении омепразолом 20 мг в сутки и пантопразолом 40 мг в сутки эффективность заживление эрозий пищевода через 8 недель терапии была сопоставима [8].
Таким образом, результаты исследований демонстрируют сопоставимый клинический эффект омепразола в дозировке 20 мг в сутки и пантопразола в дозе 40 мг в сутки при язвенной болезни, рефлюкс-эзофагите.
Межлекарственные взаимодействия
ИПП подвергаются биотрансформации в печени с помощью изоферментов системы цитохрома Р450, прежде всего CYP2C9 и CYP3A4. При этом блокаторы Н+/К+-АТФазы ингибируют изоферменты цитохрома Р-450, что имеет большое значение в разрезе лекарственных взаимодействий. Разница в выраженности ингибирования разных изоферментов обусловливает способность ИПП вступать во взаимодействие с препаратами, которые являются субстратами для соответствующих ферментов [4].
Исследования доказывают, что пантопразол более выраженно блокирует и CYP2C9, и CYP3A4, чем омепразол. Следовательно, возможность лекарственных взаимодействий первого в отношении препаратов, которые являются субстратами для соответствующего фермента, выше по сравнению со вторым.
- Субстраты для CYP2C9: варфарин, лозартан, нестероидные противовоспалительные препараты, в том числе ибупрофен и диклофенак, ирбесартан, карведилол [9–11].
- Субстраты для CYP3A4: амиодарон, амлодипин, буспирон, верапамил, карбамазепин, итраконазол, кетоконазол, кларитромицин, ловастатин, прогестерон, флуконазол, эритромицин и другие.
- Субстратами для обеих форм являются глибенкламид, амитриптилин и имипрамин.
Данные об ингибирующей активности омепразола и пантопразола дают основания утверждать, что именно омепразол имеет минимальный риск межлекарственного взаимодействия с НПВП [11]. Напомним, последние нередко комбинируют с ИПП для снижения риска гастропатии.
Важное значение имеет и способность вступать в лекарственное взаимодействие с клопидогрелем. Известно, что ИПП могут назначаться в комбинации с этим антиагрегантом с целью предупреждения повреждения слизистой оболочки пищеварительного тракта и развития желудочно-кишечного кровотечения. Клопидогрель — пролекарство, активные метаболиты которого образуются при помощи ряда изоферментов цитохрома Р450. Все ИПП, являясь ингибиторами изоферментов системы цитохрома, вступают во взаимодействие с клопидогрелем, замедляя его активацию и снижая его антиагрегантную способность [12, 13].
Особенную роль играет способность ИПП ингибировать фермент CYP2C19 — основной изофермент, участвующий в активации клопидогреля. Более мощным ингибитором CYP2C19 является омепразол: его способность ингибировать этот изофермент в несколько раз выше, чем пантопразола. Таким образом, пантопразол имеет преимущество при совместном применении с клопидогрелем по сравнению с омепразолом [4].
Схожая ситуация возникает и при совместном приёме пантопразола или омепразола с антидепрессантом циталопрамом [4].
Нежелательные реакции
Оба ИПП — и омепразол, и пантопразол — проявляют ряд идентичных побочных эффектов. Так, при их приёме может развиваться головокружение, головная боль, крапивница, боль в животе, запоры или диарея, метеоризм, другие диспепсические симптомы, в частности, тошнота и рвота. Характерным для обоих препаратов редким неблагоприятным явлением является перелом шейки бедра и рабдомиолиз [4].
Наряду с общими, омепразол и пантопразол проявляют и индивидуальные побочные эффекты. Так, на фоне применения омепразола может развиваться поражение печени, почек, панкреатит, лихорадка. У пациентов, получающих пантопразол, регистрировались угрожающие жизни осложнения — синдром Стивенса-Джонсона (тяжёлая реакция гиперчувствительности с поражением кожи и слизистых оболочек), синдром Лайелла (очень тяжёлая форма аллергического буллезного дерматита), а также изменение картины крови — тромбоцитопения. С вероятностью более 1 % при применении пантопразола могу возникать острый гастроэнтерит, боли в суставах, спине, а также диспноэ, инфекции верхних дыхательных и мочеполовых путей, гриппоподобное состояние [4].
Вывод
Омепразол и пантопразол обладают сопоставимой антисекреторной активностью (в дозах 20 мг в сутки и 40 мг в сутки соответственно) и профилем безопасности. Основные отличия препаратов заключаются в их способности к ингибированию изоферментов системы цитохрома Р450 и связанных с ними межлекарственных взаимодействиях. Пациентам, которым необходимо принимать ИПП в комбинации с клопидогрилем и циталопралом, целесообразнее делать выбор в пользу пантопразола, как препарата с более низкой ингибирующей активностью в отношении изофермента, участвующего в активации соответствующего антиагреганта или антидепрессанта.
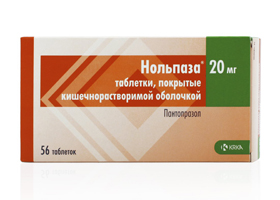
Фото препарата
- Латинское название: Nolpaza
- Код АТХ: A02BC02
- Действующее вещество: Пантопразол (Pantoprazole)
- Производитель: Valdepharm (Франция), КРКА (Словения), КРКА-Рус (Россия)
Состав
В состав 1 таблетки Нольпаза входит 20 или 40 мг действующего вещества пантопразола натрия в пересчете на пантопразол, а также вспомогательные компоненты: сорбитол, маннитол, кросповидон, кальция стеарат, натрия карбонат безводный.
Форма выпуска
Выпускается в виде овальных, немного двояковыпуклых таблеток, которые покрывает светлая коричнево-желтая пленочная оболочка. На изломе таблетка шероховатая, имеет цвет от белого до светло-желтого. Выпускается в контурной ячейковой упаковке по 14 штук, реализуется в картонных коробках по 1, 2 или 4 упаковки в каждой.
Фармакологическое действие
Нольпаза является гипоацидным препаратом, входящим в группу ингибиторов протонной помпы. В его составе есть действующее вещество — пантопразол, являющееся производным бензимидазола. Это вещество угнетает активность H+/K+АТФазы. Попадая в кислую среду, активный компонент Нольпазы превращается в фармакологически активную форму и обеспечивает блокировку последнего этапа гидрофильной секреции HCl в желудке. Базальная и стимулированная продукция соляной кислоты угнетается препаратом одинаково активно. Применение лекарства ведет к увеличению секреции гастрина, однако, это явление обратимое.
Фармакодинамика и фармакокинетика
Препарат применяется перорально, после чего его активный компонент быстро абсорбируется в кровоток. Биодоступность активного вещества — 77%, от приема пищи она не зависит. Наибольшая концентрация в плазме отмечается через 2-2.5 часа после употребления Нольпазы внутрь.
Характерной особенностью препарата является высокий уровень связи с белками крови – примерно 98%. Препарат метаболизируется в печени, его выведение происходит в виде метаболитов с мочой, незначительная часть – с калом. Время полувыведения пантопразола — 1 час, его метаболит выводится через 1,5 часа.
Больным, страдающим нарушениями функционирования печени, необходимо корректировать дозу лекарственного средства. Пожилым пациентам, а также больным, страдающим нарушениями почек, доза не корректируется.
Показания к применению
Прежде чем начинать лечение, необходимо четко знать от чего таблетки применяются. Показания к применению Нольпазы следующие:
-
легкой степени;
- рефлюкс-эзофагит различной степени (лечение и профилактика);
- пептическая язва желудка и двенадцатиперстной кишки;
- состояния, провоцирующие гиперсекрецию (синдром Золлингера-Эллисона и др.);
- эрадикация Helicobacter pylori (назначается в комбинации с антибиотиками).
Кроме того, показания к применению лекарства есть, если необходимо профилактическое средство для защиты от развития язвенных поражений людей, проходящих длительное лечение нестероидными противовоспалительными препаратами.
Противопоказания
Противопоказания для приема Нольпазы следующие:
- Высокая чувствительность к составляющим препарата (непереносимость фруктозы и др.).
- Нольпаза 40 мг не применяется вместе с противомикробными средствами для лечения пациентов с тяжелыми заболеваниями почек и/или печени.
- Нельзя принимать препарат людям с невротической диспепсией.
Препарат назначается с осторожностью:
- Людям, страдающим болезнями печени. Если лечение проводится на протяжении длительного времени, следует обязательно контролировать у пациентов уровень печеночных ферментов.
- Тем, у кого существует высокий риск развития язвы, кишечных, желудочных кровотечений.
- Пациентам с высоким риском развития гиповитаминоза В12.
Побочные действия
Как правило, прием препарата не провоцирует проявления нежелательных эффектов. Однако иногда возникают следующие побочные действия:
- В функциях ЖКТ: нарушение стула, гастралгия, метеоризм, тошнота, повышение уровня печеночных ферментов. Редко отмечается гепатотоксическое влияние, желтуха, иногда – желтуха, которая сопровождается печеночной недостаточностью.
- В функциях ЦНС: головокружение, головная боль, эмоциональная лабильность, нарушения зрения.
- В функциях мочевыделительной системы: появление отеков, интерстициальный нефрит.
- Возможно проявление аллергических реакций: зуда, сыпи на коже, крапивницы, светочувствительности. Редко развивается отек Квинке.
- В некоторых случаях отмечается боль в мышцах, повышается температура тела, отмечается гипертриглицеридемия.
Инструкция по применению Нольпазы (Способ и дозировка)
Лекарственное средство применяется перорально. Инструкция на Нольпазу 40 мг и 20 мг следующая: глотать лекарство нужно целиком, не разжевывая, запивать обильным количеством жидкости. Препарат оптимально принимать перед едой. Если врач назначил прием Нольпазы по 1 таблетке в сутки, то лучше принять ее утром. Детальная инструкция по применению Нольпазы, а также дозировка определяется врачом в индивидуальном порядке.
Людям с легкой формой гастроэзофагеальной рефлюксной болезни, как правило, назначается Нольпаза 20 мг, не более одной таблетки в сутки. Лечение продолжается от 14 дней до 1 месяца, иногда врач принимает решение о продлении терапии на 2 месяца.
При лечении обострения рефлюкс-эзофагита, а также в целях профилактики назначается по 20 мг лекарственного средства один раз в день. Если существует высокая вероятность развития рецидива болезни, дозу увеличивают до 40 мг 1 раз в день. Когда состояние улучшается, дозу снова снижают до 20 мг. Взрослые, которые получают нестероидные противовоспалительные лекарства, принимают Нольпазу с целью профилактики язвенных поражений (20 мг 1 раз в сутки).
В схемах эрадикации Helicobacter pylori Нольпаза назначается по 40 мг дважды в сутки, при этом прием препарата нужно комбинировать с приемом противомикробных препаратов. Пить таблетки нужно утром и вечером.
Те больные, которые страдают синдромом Золлингера-Эллисона и другими болезнями, которые сопровождаются усиленной секрецией, назначается изначально по 40 мг дважды в день, если есть необходимость, доза может быть увеличена до 80 мг ежедневно.
Если у человека есть нарушения в работе печени, то ежедневно ему можно принимать не более 20 мг пантопразола. Перед тем, как начинать лечение препаратом, нужно обязательно пройти исследования и исключить наличие злокачественной опухоли в пищеводе и в желудке.
Передозировка
Информации о передозировке не поступало. Препарат хорошо переносится даже в больших дозах. Если человек чувствует себя плохо, необходимо провести промывание желудка, принять энтеросорбенты, провести симптоматическое лечение.
Взаимодействие
Если сочетать прием препарата и Кетоконазол и другие средства с рН-зависимой абсорбцией, биодоступность последних снижается.
Если Нольпаза принимается с антикоагулянтами кумаринового ряда, то эффективность последних может меняться.
При сочетании приема Нольпазы с антацидными препаратами, фармакокинетика этих средств не меняется.
Условия продажи
Реализуется в аптеках по рецепту врача.
Условия хранения
Хранить лекарственное средство нужно в сухом месте, беречь от попадания света. Температура хранения должна составлять от 15 до 30 °С.
Срок годности
Хранить препарат можно 2 года.
Особые указания
Перед началом лечения нужно обязательно исключить у пациента наличие онкологического новообразования, так как в процессе лечения могут маскироваться симптомы, в связи с чем постановка диагноза не будет сделана своевременно. Если через месяц у пациента будут отсутствовать результаты лечения препаратом, ему нужно пройти еще одно обследование. При продолжительном лечении необходимо обязательное регулярное наблюдение у врача. На быстроту реакции, работу с механизмами и управление автотранспорта Нольпаза не влияет.
Александр Сергеевич Трухманов, профессор:
– Спасибо большое, Игорь Вениаминович.
Почему же мы останавливаемся на вопросе эквивалентной дозировки?
Дело в том, что в последнее время участились ситуации, в которых для преодоления резистентности к проводимой терапии, для преодоления рефрактерности (например, при лечении пациентов с гастроэзофагеальной рефлюксной болезнью) применяются дозировки в 2, иногда даже в 3 раза больше стандартных.
Разрешите предоставить вашему вниманию некоторые определения (они четкие и официальные), чтобы нам в итоге понять, каким образом оценить различные антисекреторные препараты, различные ИПП. Это в связи с тем, что их исходные дозировки отличаются.
Давайте рассмотрим эти определения.
Фармацевтическая эквивалентность содержит в себе два понятия.
Фармацевтические эквиваленты – это лекарственные препараты, которые содержат одинаковый ингредиент, действующее вещество. Причем именно в той дозировке и способе применения, которые для данного препарата указаны. Фармацевтические эквиваленты могут отличаться по виду лекарственной формы, виду таблетки, окраске, названию.
Это, например, те препараты аспирина, которые имеют разные названия, но содержат ацетилсалициловую кислоту в одинаковой дозе.
Фармацевтическая альтернатива – это препараты, которые содержат одинаковый компонент. Однако, например, эти одинаковые компоненты могут присутствовать в виде разных солей или в разных формах лекарственного препарата.
Здесь, вы видите, приводится пример гидрохлорида тетрациклина и фосфата тетрациклина. Или хинидина сульфат, который может содержаться в дозе 200 мг как в таблетках, так и в капсулах.
Таким образом, фармацевтические эквиваленты и фармацевтическая альтернатива – это препараты, содержащие одинаковый активный ингредиент.
Что такое биоэквивалентность?
Это очень важное понятие, которое мы должны понимать. Биоэквивалентные препараты – это фармацевтические препараты, которые сопоставимы в своей эффективности в плане биодоступности при одинаковом способе применения.
Я напомню, что биодоступность – это та часть лекарственного препарата, которая достигает конечной точки приложения после прохождения всасывания и метаболизма в печени.
При приеме оригинальных и генерических препаратов они могут демонстрировать одинаковую биоэквивалентность. Она может отличаться где-то по разным нормам до 15%. Это степень всасывания, распределения, биодоступности.
Как правило, биоэквивалентность определяется в эксперименте. Этот эксперимент позволяет нам сказать, что генерический лекарственный препарат сопоставим по своей эффективности с оригинальным препаратом.
Безусловно, идентичные параметры, которые получаются в эксперименте с участием добровольцев, позволяют говорить, что какой-то конкретный генерик сопоставим по своей эффективности с оригинальным препаратом.
Вернемся к сопоставлению разных ИПП. Мы можем увидеть, что такие показатели, как биодоступность, связывание с белками плазмы, период полувыведения у всех ИПП, которые в настоящее время присутствуют у нас, примерно сопоставимы.
Вы видите внизу ссылки, которые позволяют нам, получая тот или иной препарат в пользование, проверить показания биодоступности, путей метаболизма и так далее.
Теперь мы переходим к понятию – терапевтическая эквивалентность.
Терапевтические эквиваленты – это лекарственные препараты, обладающие одинаковым клиническим эффектом и профилем безопасности. Причем подчеркивается, что этот анализ проводится в условиях, отвечающих инструкции по применению.
Дело в том, что клинический эффект может оцениваться по разным показателям. Это влияние на симптоматику, на какие-то функциональные показатели.
Однако нам очень важно понимать, отдавать себе отчет в том, что сравнения различных лекарственных препаратов (в частности, одной группы) должно проводиться в условиях, обозначенных в инструкции по применению. Это имеет отношение, прежде всего, к дозировкам лекарственных препаратов.
Давайте ознакомимся с теми данными, которые публикует Администрация по лекарствам и пищевым продуктам США. Они свидетельствуют, что каждый из ИПП очень подробно проанализирован.
20 мг – это половинная дозировка, которая применяется в определенных случаях. Все эти случаи чрезвычайно строго прописаны, обозначены в инструкции по применению.
Насколько это имеет значение?
Давайте обратимся к стандартам лечения эрозивного эзофагита, то есть, больных с гастроэзофагеальной рефлюксной болезнью, и очень внимательно посмотрим на дозы, которые рекомендованы при лечении эрозивного эзофагита.
Естественно, каждый из нас имеет полное право назначить ту дозу лекарственного препарата, которая, на наш взгляд, окажет максимальное эффективное воздействие и будет наиболее полезна для нашего пациента.
Но мы должны в то же время отдавать себе отчет в том, что когда мы назначаем препарат в двойной дозировке, мы выходим за рамки инструкции по применению. Если мы назначаем эту двойную дозировку, мы обязательно должны обосновать необходимость назначения двойной дозировки того или иного лекарственного препарата.
Подчеркивается, что данная классификация не является основанием для пересмотра стандартов лечения. Не является основанием для сравнения эффективности лекарственных препаратов. Является исключительно справочными данными, которые основаны на проведении сопоставительных исследований в плане фармакокинетических свойств того или иного ИПП.
Можем ли мы говорить о наличии эквивалентных дозировок при анализе антисекреторного влияния ИПП?
Если мы зададимся такой задачей и проведем эксперимент, в котором будет оцениваться антисекреторная активность (например, по повышению уровня pH желудочного сока) при назначении препаратов ИПП в различных дозах, мы можем в итоге сказать, какая эффективность у какого ИПП по показателю повышения pH, например, до 4-х.
Повышение pH само по себе – это, безусловно, важный показатель. Он функционален. Мы можем сопоставлять препараты, но нас интересует клиническая эффективность.
• при лечении пациентов с гастроэзофагеальной рефлюксной болезнью,
• при лечении язвенной болезни (заживлении язвенного дефекта),
• в отношении действия в плане эрадикации инфекции H.pylori.
Давайте посмотрим на данную таблицу.
Теперь мы рассмотрим с вами результаты рандомизированных клинических исследований, посвященных заживлению язвы в течение 4-х недель.
Наконец, сравнение схем эрадикации (то, о чем говорилось в первых двух лекциях) с использованием одинаковых схем – то есть, с использованием одинаковых антибактериальных средств и разных ИПП также продемонстрировало результат, который ожидаем.
При сравнительном анализе эффективности различных препаратов следует, прежде всего, руководствоваться инструкцией по применению. Сравнить те дозировки, которые указаны как стандартные.
Тогда мы можем добиться объективизации результатов. В итоге улучшить качество лечения.
Читайте также:

