Онко и вич настороженность при приеме стоматологических больных
Обновлено: 10.05.2024
Пандемия ВИЧ/СПИД представляет собой одну из сложнейших проблем, стоящую перед человечеством в настоящее время. Масштабы ее распространения приобрели глобальный характер и представляют реальную угрозу развитию большинству стран мира.
Распространение ВИЧ-инфекции не только не ослабевает, но и продолжает развиваться и усиливаться, что подтверждают экспертные оценки Объединенной программы ООН по ВИЧ/СПИД (ЮНЭЙДС) и Всемирной организации здравоохранения (ВОЗ). В условиях генерализованной эпидемии ВИЧ-инфекции в России возрастает риск инфицирования ВИЧ стоматологического персонала в результате аварийных ситуаций при выполнении профессиональных обязанностей. В связи с этим профилактика профессионального заражения ВИЧ-инфекцией медицинских работников остается актуальной и социально значимой.
Оказание стоматологической помощи ВИЧ-ассоциированному пациенту должно осуществляться с необходимыми мерами предосторожности и при неукоснительном выполнении правил дезинфекции и стерилизации. Только так можно избежать заражения по цепочке пациент — врач — пациент, инфицирования вспомогательного медперсонала, внутрибольничного распространения инфекции.
Лечение стоматологических заболеваний у больных СПИДом носит традиционный характер и проводится в обычных поликлинических условиях. Вероятность контакта с ВИЧ при оказании стоматологической помощи невелика, порядка 0,85 %, тем не менее стоматологов относят к профессиональной группе риска наряду с некоторыми другими специалистами-медиками. Известно, что у ВИЧ-инфицированных пациентов на фоне вторичного иммунодефицита активируется условно-патогенная флора, способствующая развитию оппортунистических заболеваний.
Установлено, что наиболее ранний и обязательный манифестный признак ВИЧ-инфекции — проявления в полости рта. Так, к числу ранних широко распространенных ВИЧ-индикаторных оральных заболеваний относят ВИЧ-ассоциированные заболевания пародонта, которые характеризуются довольно стойким длительным течением и резистентностью к общепринятым методам лечения. Клиническим признаком ВИЧ-пародонтита служит быстропрогрессирующая деструкция альвеолярной кости и периодонтальной ткани, сопровождающаяся воспалением, болезненностью и спонтанными десневыми кровотечениями.
Ближайшие события
Присоединение грибковой инфекции способствует развитию резистентности к общепринятым средствам местного лечения, что приводит к усилению и сохранению воспалительного процесса в полости рта. При ортопедическом лечении воспаление слизистой оболочки десен способно существенно усложнить процесс препарирования зуба под коронку, особенно создание уступа, снятие двойного оттиска силиконовыми массами, подгонку и фиксацию мостовидного протеза. Эти осложнения в итоге приводят к снижению качества протезирования. Кроме того, значительное кровотечение десны при пародонтите у ВИЧ-инфицированного пациента может привести к вирусной контаминации оттиска и протеза на промежуточных этапах, что может создавать опасность инфицирования для врача и зубного техника.
Основную опасность для врача-стоматолога представляет загрязнение кожи, слизистой оболочки глаз, рта, носа, инфицированной кровью или другими биожидкостями пациента. При этом, например, ротовая жидкость (слюна) считается малоопасной, так как содержание в ней ВИЧ у больного СПИДом ничтожно мало по отношению к содержанию вируса в крови. Риск заражения возрастает при повреждении кожи рук острыми борами, дрилями, корневыми или инъекционными иглами.
Доказано, что в стоматологии, где большинство манипуляций носит инвазивный характер, передача вируса иммунодефицита человека наряду с другими инфекционными агентами может происходить и при использовании нестерильных игл, шприцев, боров, эндодонтических и прочих инструментов. Более того, ВИЧ, например, не погибает в результате протирания инструмента ваткой, смоченной спиртом. Поэтому сепарационные металлические диски, кроме алмазного, являются одноразовыми, и их следует выбрасывать после каждого приема пациента.
Возбудитель ВИЧ/СПИД высокочувствителен к нагреванию. При кипячении погибает в течение 2—3 минут. В то же время вирус устойчив к действию ультрафиолетового и гамма-излучения в дозах, обычно применяемых при стерилизации. Хлорсодержащие дезинфектанты (2—3%-ный раствор хлорамина, 3%-ный раствор хлорной извести) в обычно применяемых концентрациях инактивируют вирус в течение 10—20 минут. Во внешней среде вирус относительно неустойчив. В крови на предметах в нативном состоянии сохраняет заразную способность в течение 14 дней, в высушенных субстратах — до 7 суток.
Эффективная профилактика ВИЧ-инфицирования пациента и медработника в зубоврачебном кабинете и зуботехнической лаборатории возможна и должна осуществляться при строгом соблюдении правил дезинфекции и стерилизации.
Основными нормативными документами, регламентирующими санитарно-противоэпидемический режим в стоматологическом кабинете, являются:
8.3. Профилактика профессионального инфицирования ВИЧ.
8.3.3.1. Действия медицинского работника при аварийной ситуации:
– в случае порезов и уколов немедленно снять перчатки, вымыть руки с мылом под проточной водой, обработать руки 70%-ным спиртом, смазать ранку 5%-ным спиртовым раствором йода;
– при попадании крови или других биологических жидкостей на кожные покровы это место обрабатывают 70%-ным спиртом, обмывают водой с мылом и повторно обрабатывают 70%-ным спиртом;
– при попадании крови и других биологических жидкостей пациента на слизистую глаз, носа и рта ротовую полость следует промыть большим количеством воды и прополоскать 70%-ным раствором этилового спирта, слизистую оболочку носа и глаза обильно промыть водой (не тереть);
– при попадании крови и других биологических жидкостей пациента на халат, одежду нужно снять рабочую одежду и погрузить в дезинфицирующий раствор или в бикс (бак) для автоклавирования;
– как можно быстрее начать прием антиретровирусных препаратов в целях постконтактной профилактики заражения ВИЧ.
С целью экстренной профилактики ВИЧ-инфекции назначается азидотимидин в течение 1 месяца. Сочетание азидотимидина (ретровир) и ламивудина (эливир) усиливает антиретровирусную активность и преодолевает формирование резистентных штаммов.
При высоком риске заражения ВИЧ-инфекцией (глубокий порез, попадание видимой крови на поврежденную кожу и слизистые от пациентов, инфицированных ВИЧ) для назначения химиопрофилактики следует обращаться в территориальные центры по борьбе и профилактике СПИД.
Лица, подвергшиеся угрозе заражения ВИЧ-инфекцией, находятся под наблюдением врача-инфекциониста в течение 1 года с обязательным обследованием на наличие маркера ВИЧ-инфекции.
Необходимо в возможно короткие сроки после контакта обследовать на ВИЧ и вирусные гепатиты B и C лицо, которое может являться потенциальным источником заражения, и контактировавшее с ним лицо. Обследование на ВИЧ потенциального источника ВИЧ-инфекции и контактировавшего лица проводят методом экспресс-тестирования на антитела к ВИЧ после аварийной ситуации с обязательным направлением образца из той же порции крови для стандартного тестирования на ВИЧ в ИФА. Образцы плазмы (или сыворотки) крови человека, являющегося потенциальным источником заражения, и контактного лица передают для хранения в течение 12 месяцев в центр СПИД субъекта Российской Федерации. Пострадавшего и лицо, которое может являться потенциальным источником заражения, необходимо опросить о носительстве вирусных гепатитов, ИППП, воспалительных заболеваний мочеполовой сферы, других заболеваний, провести консультирование относительно менее рискованного поведения. Если источник инфицирован ВИЧ, выясняют, получал ли он антиретровирусную терапию. Если пострадавшая — женщина, необходимо провести тест на беременность и выяснить, не кормит ли она грудью ребенка. При отсутствии уточняющих данных постконтактную профилактику начинают немедленно, при появлении дополнительной информации схема корректируется.
Проведение постконтактной профилактики заражения ВИЧ антиретровирусными препаратами:
Прием антиретровирусных препаратов (рис. 1.) должен быть начат в течение первых двух часов после аварии, но не позднее 72 часов.
Стандартная схема постконтактной профилактики заражения ВИЧ — лопинавир/ритонавир + зидовудин/ламивудин. При отсутствии данных препаратов для начала химиопрофилактики могут использоваться любые другие антиретровирусные препараты; если невозможно сразу назначить полноценную схему высокоактивной антиретровирусной терапии (ВААРТ), начинается прием одного или двух имеющихся в наличии препаратов.
Использование невирапина и абакавира возможно только при отсутствии других препаратов. Если единственным из имеющихся препаратов является невирапин, должна быть назначена только одна доза препарата — 0,2 г (повторный его прием недопустим), затем при поступлении других препаратов назначается полноценная химиопрофилактика. Если химиопрофилактика начата с использованием абакавира, следует как можно быстрее провести исследование на реакцию гиперчувствительности к нему или провести замену абакавира на другой НИОТ. Все работники медицинских учреждений должны знать о профессиональном риске инфицирования и осознавать необходимость соблюдения универсальных мер предосторожности при работе со всеми пациентами, в любых ситуациях, независимо от диагноза. Весь персонал медицинских учреждений в рамках последипломного повышения квалификации должен регулярно проходить тематические циклы усовершенствования по проблеме ВИЧ/СПИДа и инструктаж по технике безопасности. Обучение универсальным мерам предосторожности должно быть также обязательной частью инструктажа медицинских работников при приеме на работу. Профилактика ВИЧ/СПИДа в стоматологии предусматривает выявление группы риска, анамнестических данных, тщательную стерилизацию инструментария.
При работе в стоматологическом кабинете необходимо соблюдать следующие меры:
1. Использование средств индивидуальной защиты (халат, маска, перчатки, защитные очки и экран, нарукавники, непромокаемые фартуки).
2. Использование одноразового инструментария всюду, где это возможно (слюноотсосы, пылесосы, одноразовые карпульные шприцы и т. д.).
3. Централизованная стерилизация медицинского инструментария с контролем эффективности.
4. Врачи с экссудативными поражениями кожи не должны выполнять инвазивных процедур.
5. Медицинский работник должен относиться к крови и к другим биологическим жидкостям организма как к потенциально заразному материалу.
6. Соблюдать осторожность при работе с колющимися и режущими предметами (иглы, скальпели, ножницы, эндодонтический инструментарий).
7. Использовать систему коффердам, слюноотсосы, пылесосы. Соблюдать правила эргономики.
8. В ортопедической стоматологии все ортопедические изделия промываются как после изъятия из полости рта пациента перед отправкой в зуботехническую лабораторию, так и перед установкой в полости рта. В связи с увеличением числа используемых стоматологических инструментов для каждого вида их должен быть отработан и использоваться свой режим стерилизации и дезинфекции.
9. Стоматологическое оборудование и поверхности, трудно дезинфицируемые (рентгенологическая аппаратура и др.), которые в процессе работы могут быть контаминированы, заворачиваются в непромокаемые материалы (к примеру, пластиковые конверты) для их защиты. Этот защитный слой должен, естественно, заменяться после каждого пациента.
Таким образом, при оказании медицинской помощи, особенно стоматологической, имеется высокий риск инфицирования ВИЧ-инфекцией. В этой связи необходим постоянный мониторинг случаев внутрибольничного инфицирования как пациентов, так и медицинского персонала. Необходимо повысить соблюдение контроля над выполнением рекомендаций по инфекционной безопасности при оказании стоматологических медицинских услуг.
Ранняя и своевременная диагностика предраковых заболеваний и адекватное лечение может служить реальной основой для профилактики рака челюстнолицевой области, слизистой оболочки рта, языка и губ.
Человек контактирует с окружающим миром через ротовую полость, соответственно именно там наиболее вероятно возникновение воспалительных процессов, которые и могут стать главными факторами в развитии опухоли.
Онкология челюстно-лицевой области составляет около 15 % опухолей человеческого организма. На рак красной каймы губ и слизистой оболочки полости рта (СОПР) приходится около 5 % всех злокачественных опухолей.
Важность своевременной диагностики этих новообразований определяется не только частотой случаев, но и особенностью течения данных форм рака. Несмотря на то, что опухоли челюстно-лицевой области легко доступны осмотру и не требуют сложных методов диагностики, половина больных погибают очень быстро, так как эта группа новообразований относится к опухолям высокой злокачественности, которые быстро растут и рано метастазируют.
Предрак – это состояние, которое переходит в рак в результате постоянного изменения свойств клеток в сторону злокачественности. Предрак переходит в рак не столько в результате качественных изменений (время, масса), сколько вследствие изменения биологической сущности клеток, накопления в них свойств, присущих злокачественной клетке.
Для ранней диагностики и выявления заболеваний важно знать состояния предраков слизистой оболочки полости рта, красной каймы губ и кожи, а так же факторы, способствующие их возникновению.
Факторы, способствующие возникновению предраковых состояний:
- Механические раздражители: аномалии прикуса, неправильное положение отдельных зубов, некачественно изготовленные реставрации и протезы, патологическое стирание зубов, вредные привычки (удерживание во рту карандаша, ручки, гвоздей и т.д.).
- Бытовые химические раздражители: пряности, высококонцентрированные растворы этилового спирта, табак. Последний оказывает грубое раздражающее действие на слизистую оболочку полости рта. В организм при курении попадает примерно 20 % табачного дыма, в котором содержится ряд продуктов, крайне сильных по раздражающему действию: пиридиновые основания (переход никотина в пиридин – наиболее вредная сторона действия), синильная кислота, цианистые соединения, жирные кислоты, фенол и дегтярный осадок. В табачном дыму содержится также бензпирен и мышьяк. Одним из раздражающих моментов курения является термический фактор.
- Производственные раздражители: щелочи, кислоты в виде паров и аэрозолей, другие химические вещества.
- Хроническая термическая травма: горячая пища, многократное воздействие повышенных температур при курении: прижигание губ сигаретой (в зоне сгорания табака температура достигает 4000 С), горячий воздух при работе на некоторых предприятиях.
- Метеорологические раздражители: комплекс неблагоприятных факторов внешней среды. К ним относят воздействие солнечных лучей, пыли, ветра, аэрозолей соленой воды в условиях пониженной температуры и высокой влажности воздуха.
- Биологические раздражители: к ним относится целый ряд микроорганизмов, патогенных для человека (дрожжеподобные грибы, вызывающие усиление ороговения слизистой оболочки языка, бледная спирохета, палочка Коха).
- Ионизирующее излучение: этот фактор следует учитывать у больных, получавших лучевую терапию по поводу опухолей той или иной локализации, во время проведения которой в зону облучения попадает окружающая слизистая оболочка полости рта.
Одной из главных причин возникновения рака челюстно-лицевой области является неудовлетворительное состояние полости рта, особенно наличие кариозных зубов и плохих протезов, острые края которые постоянно травмируют слизистую оболочку, вызывая пролежни и длительно незаживающие язвы.
Признаки озлокачествления предраковых состояний:
- Длительное, вялое течение процесса (наличие язвы, не заживающей в течение 2-3 недель);
- Безуспешность консервативного лечения;
- Увеличение размеров патологического очага, несмотря на проведенное адекватное лечение;
- Появление уплотнения вокруг или в основании патологического очага;
- Кровоточивость;
- Появление плотных, увеличенных, безболезненных регионарных лимфатических узлов.
- Появление подвижности одного или нескольких интактных зубов, сопровождающейся постоянными болями;
- Постепенно нарастающий парез мимических мышц, парастезии и онемение в зоне подглазничного и подбородочного нервов;
- Появление на губах или в полости рта образования, которое не проходит длительное время и имеет тенденцию увеличиваться в размерах, это может быть:красное пятно, беловатое пятно, язвочка, уплотнение, нарост.
Самой надежной профилактикой рака является устранение факторов, благоприятствующих его развитию, и радикальное лечение лиц с предраковыми состояниями.
Действенным средством профилактики предраковых состояний языка и слизистой оболочки полости рта служит повседневное соблюдение гигиены полости рта, устранение опасностей, связанных с кариозными зубами и некачественными протезами.
В Российской Федерации продолжается рост числа больных злокачественными новообразованиями и увеличение смертности от них. При этом смертность населения от злокачественных новообразований занимает третье место в структуре причин смертности [6]. Рак слизистой оболочки рта в 2010 г. составил 9,7 на 100 000 жителей: мужчины — 10,2, женщины — 1,7 (соответственно, 4,4 и 1,3 последние 15—20 лет назад). В 20 % случаев рак возникает на фоне предрака, в 2 % случаев — при наличии фоновой патологии, в 22,5 % ему предшествовала травма, а у 55,5 % больных рак появился на неизмененной слизистой оболочке. В 97 % случаев на слизистой оболочке рта развивается плоскоклеточный рак, реже аденокарцинома (из малых слюнных желез) и саркомы. Чаще поражается язык, реже — дно рта, слизистая оболочка щеки, десневого края. По данным РОНЦ им. Блохина РАМН, в 70 % случаев рак слизистой оболочки рта проявляется в инфильтративной форме, в остальных случаях в экзофитной (папиллярной), язвенной или смешанной формах [9].
Статистика 2010 года показывает, что у 61 % больных рак тканей и органов рта и ротоглотки выявляют на III, IV стадии болезни. В общей структуре онкологических заболеваний органов и тканей челюстно-лицевой области предопухолевые заболевания слизистой оболочки рта составляют 4,2—16,4 % [5].
По данным авторов, лейкоплакия встречается у 13 % больных с патологией слизистой оболочки рта в возрасте после 30 лет и старше. В старшем возрасте, и в основном у мужчин, она встречается в 7—10 раз чаще. Встречаемость лейкоплакий по всему миру существенно разнится. Среди 4000 пациентов одной немецкой стоматологической клиники различные формы лейкоплакии во рту были обнаружены у 3,1 % пациентов, среди которых преобладали мужчины (4,3 % по сравнению с 1,9 % у женщин). Частота злокачественной трансформации лейкоплакии (в зависимости от склонности к малигнизации некоторых форм) составляет 15—75 % [4]. На 100 % случаев обращающихся с лейкоплакией рта приходится 5,6 % предраковых состояний и 4,87 % случаев раннего рака [3].
Раздел предраковых заболеваний челюстно-лицевой области оказался на стыке нескольких медицинских дисциплин (стоматология, онкология, челюстно-лицевая хирургия). Эта разобщенность мешает организации эффективной системы профилактики, своевременной диагностики, лечения и реабилитации таких больных
Выявление и лечение пациентов с предраковыми заболеваниями, ранними стадиями развития злокачественного процесса в 75 % случаев обеспечивают длительный и стойкий клинический эффект; в то же время обнаружение опухоли в распространенной стадии практически в 100 % случаев исключает возможность достижения удовлетворительных результатов. Онкологическая настороженность и своевременная диагностика позволяют добиться максимальной выживаемости пациентов с наименьшей инвалидизацией и значительным снижением расходов на лечение и долечивание больных. На первичном этапе ошибки в диагностике и лечении предраковых заболеваний челюстно-лицевой локализации допускаются довольно часто, что обусловлено недостаточным уровнем знаний по этому разделу. Несоблюдение принципов онкологической настороженности, отсутствие диспансерного учета приводит к низкой эффективности профилактических осмотров населения с целью выявления первичного очага поражения [6].
Различают предраковые заболевания с высокой (облигатные) и малой (факультативной) частотой озлокачествления. Данная классификация предраковых изменений красной каймы губ и слизистой оболочки рта отражена в монографии Машкиллейсона А. Л. (1970).
Вероятность озлокачествления веррукозной лейкоплакии, по данным некоторых авторов, составляет 20—40 %, эрозивной — 20—30 %, плоской лейкоплакии — 4,2 % [7, 8]. В 30 % случаев рака органов и тканей рта было доказано его развитие на фоне лейкоплакии [1]. В монографии проф. Banoczu J. [11] приводятся данные исследования у рабочих химического производства, где выявили плоскую (4 %) и веррукозную (19 %) лейкоплакии. Пик распространенности лейкоплакии приходится на возраст 50—59 лет (27 % пораженных) без существенной разницы среди лиц женского и мужского пола [12] с уточнением, что в возрасте 70 лет и старше наблюдается уменьшение распространенности лейкоплакии, однако отмечается самый высокий процент перерождения в рак в 5,9 %.
По частоте встречаемости среди других форм заболевания лейкоплакией плоская лейкоплакия выявляется в 48 % [11], веррукозная — в 20—40 % [7], пятнистая — в 20—30 % случаев [7]. Волосатая лейкоплакия встречается у ВИЧ-инфицированных (до 98 %), выявляется в стадии вторичных заболеваний, а также у пациентов, получающих иммуносупрессивную терапию после трансплантации почек, костного мозга, сердца и печени [3, 5, 7, 11]. У 83 % ВИЧ-инфицированных пациентов с волосатой лейкоплакией рта в течение 31 месяца развивается полная картина СПИДа [3]. У 90,3 % больных лейкоплакия протекает на фоне патологии желудочно-кишечного тракта.
Большинство авторов считает, что все формы лейкоплакий обладают способностью трансформироваться в рак. Длительность и возможность такой трансформации индивидуальна и во многом зависит от формы лейкоплакии. Научного объяснения связи между чрезмерным ороговением и злокачественным перерождением не существует, однако эпидемиологические исследования подтверждают, что рак чаще развивается у людей с лейкоплакией, чем в популяции в целом.
Гиперкератоз приводит к появлению на слизистой оболочке белой бляшки или налета, который не снимается. Другое поражение с высоким риском малигнизации — эритроплакия, или эритроплазия (появление бляшки красного цвета). В большинстве случаев не удается точно предсказать вероятность малигнизации. Для исследования предраковых поражений разработаны и протестированы клеточные маркеры. Ведется работа и в области молекулярной генетики. Однако клинические возможности пока ограничиваются выявлением факторов риска и микроскопическим исследованием.
Для исследования предраковых поражений разработаны и протестированы клеточные маркеры. Ведется работа и в области молекулярной генетики. Однако клинические возможности пока ограничиваются выявлением факторов риска и микроскопическим исследованием
Микроскопические изменения, которые происходят при лейкоплакии, варьируют от простого гиперкератоза до ранней стадии плоскоклеточного рака. Хотя красно-белые поражения озлокачествляются чаще, клиническая картина лейкоплакии не дает информации о ее микроскопической морфологии. К доброкачественным кератозам относятся гиперкератоз, гиперортокератоз, акантоз и сочетание этих изменений. Паракератоз в сочетании с акантозом часто встречается при бездымном употреблении табака. Озлокачествление клеток начинается с базального и парабазального слоев. Появляется классическая цитологическая картина клеточной атипии; ускорение клеточного цикла, плеоморфизм, гиперхроматоз, увеличение ядра. Эпителиальные гребни приобретают форму луковиц или капель и сливаются друг с другом. Подобные изменения, ограниченные нижним слоем многослойного плоского эпителия, называются легкой дисплазией. Врач должен понимать, что легкая дисплазия не обязательно повлечет за собой озлокачествление. Такие изменения слизистой оболочки могут произойти и в результате раздражения или воспалительного процесса. Однако в некоторых случаях все-таки происходит малигнизация.
Если клеточная атипия отмечается в базальном, парабазальном, а также в нижней и/или средней части шиповатого слоя, ставится диагноз средней дисплазии. При поражении большинства слоев эпителия дисплазия считается тяжелой. Если клеточная атипия обнаруживается на всем протяжении от базального слоя до наружной поверхности ороговевающих клеток, то ставится диагноз рака in situ. Умеренная и тяжелая дисплазия, как и рак in situ, являются однозначными предраковыми состояниями; они очень часто малигнизируются. Некоторые из диспластических изменений могут существовать многие месяцы и даже годы, не прогрессируя; иногда происходит регресс и самопроизвольное выздоровление. К сожалению, невозможно точно предсказать, каким будет развитие дисплазии, только на основании гистологической диагностики.
Стоматологам, работающим в поликлиниках, отводится первостепенная роль в профилактике и ранней диагностике предраковых заболеваний и опухолей этой локализации. Кожа лица, красная кайма губ и органы рта легкодоступны для осмотра, и потому предраковые и опухолевые изменения могут быть диагностированы своевременно
Рак и предрак рта развивается в результате неконтролируемого деления клеток. Этиологические факторы отвечают за генетические изменения клеток эпителия, приводящие к постоянному их размножению. Такое неконтролируемое деление обычно является результатом множества (от 4 до 8) мутаций различных генов, регулирующих процесс клеточного деления. На поверхности эпителиальных клеток слизистой оболочки рта имеются рецепторы к цитокинам, многие из которых являются факторами роста. Эпидермальный фактор роста, факторы роста тромбоцитов и фибробластов могут связываться с клеточными рецепторами; после связывания начинаются изменения структуры белков, связанные с фосфорилированием цитоплазматических доменов (киназная активность). Эти изменения, в свою очередь, вызывают серию биохимических событий в цитоплазме, в которых участвуют вторичные мессенджеры (например, МАП-киназа). Цепочка событий приводит к активации факторов транскрипции ДНК. Эти факторы активируют другие белки, связанные с ДНК через так называемые пальцевые домены типа RING.
Факторы транскрипции, например С-myc, fos и jun, могут активировать молекулы, регулирующие клеточный цикл. Многие гены, кодирующие факторы роста, рецепторы к ним, внутренние сигнальные молекулы и факторы транскрипции, получили общее название протоонкогенов. При их активации или нарушении регуляции развивается неконтролируемое митотическое деление клеток. Повреждение или мутация молекул, сдерживающих экспрессию протоонкогенов, также ведет к чрезмерному клеточному размножению. Клеточный цикл регулируется так называемыми молекулами-привратниками (циклины, клеточные циклинзависимые киназы — ЦЗК), которые контролируют каждую фазу (пресинтетическая фаза (G1), постсинтетическая фаза (G2), метафаза). Так осуществляется клеточный механизм, ответственный за деление [12].
Стоматологам, работающим на амбулаторном поликлиническом приеме, отводится первостепенная роль в профилактике и ранней диагностике предраковых заболеваний и опухолей этой локализации. Кожа лица, красная кайма губ и органы рта легкодоступны для осмотра, и потому предраковые и опухолевые изменения могут быть диагностированы своевременно. Однако ошибки в диагностике и лечении этих заболеваний допускаются довольно часто не только начинающими врачами-стоматологами, но и опытными специалистами. Кроме того, необходимо отметить и несвоевременное обращение больных предраковыми заболеваниями челюстно-лицевой области за медицинской помощью, а также нередко проводимое ими самолечение.
Удельный вес запущенных форм рака слизистой оболочки рта вследствие диагностических ошибок или неправильного ведения больных с предраковыми заболеваниями составляет 58—61 %. Основные причины запущенности:
- бессимптомность течения;
- позднее обращение к врачу-стоматологу;
- стертость клинических проявлений;
- недостаточные знания у врача-стоматолога, отсутствие онкологической настороженности.
Онкологическая настороженность в стоматологии является актуальной. Ранняя и своевременная диагностика предраковых заболеваний и адекватное лечение может служить реальной основой для профилактики рака челюстно-лицевой области, слизистой оболочки рта, языка и губ. Необходимо более тщательно проводить сбор анамнеза и оценку жалоб больного, учитывать его возраст, конституцию, характер профессии, вредные привычки, сопутствующие соматические заболевания. Внимательный осмотр поможет своевременно выявить предраковое заболевание.
Листок учета осмотра на онкологическую патологию рта является обязательным вкладышем в медицинскую стоматологическую карту. По соответствующему приказу Минздрава каждый пациент, обратившийся к врачу в текущем году, независимо от специальности последнего, должен быть осмотрен на онкопатологию
При длительном (более двух недель) течении неподдающихся лечению процессов следует проводить гистологическую оценку предопухолевого заболевания. Больных с данной патологией необходимо ставить на диспансерный учет и в зависимости от формы заболевания вызывать для повторных осмотров от двух до шести раз в год. Пациент должен быть предупрежден о возможности последствий заболевания. Согласно Порядку оказания стоматологической помощи взрослому населению, утвержденному соответствующим приказом Минздрава России от 07.12.2011 г. № 1496н, врачу-стоматологу необходимо знать структуру организации онкологической помощи: районный онколог (работает в поликлинике), онкологический диспансер, научно практический центр онкологии. При подозрении на онкопатологию пациента необходимо обследовать в течение 10 дней для подтверждения диагноза, а при обнаружении рака пациент должен быть направлен врачом-стоматологом в онкологический центр на консультацию и лечение у онколога.
Рис. 1. Листок учета осмотра на онкологические заболевания.
Результаты осмотра
Фамилия, имя, отчество врача
К сожалению, раздел предраковых заболеваний челюстно-лицевой области оказался на стыке нескольких медицинских дисциплин (стоматология, онкология, челюстно-лицевая хирургия). Эта разобщенность мешает организации эффективной системы профилактики, своевременной диагностики, лечения и реабилитации таких больных.
Совершенствование методов ранней диагностики предраковых заболеваний визуальных локализаций является актуальной задачей не только для врачей-стоматологов, но и отоларингологов, дерматологов, а также врачей общей практики, к которым пациенты, в первую очередь, нередко обращаются с определенными жалобами.
Таким образом, в настоящее время возрастает роль врача-стоматолога в профилактике и раннем выявлении онкологических заболеваний. Это связано с распространением предраковых состояний челюстно-лицевой области, слизистой оболочки рта и возрастающей частотой их озлокачествления. Предопухолевые заболевания и опухолевые процессы чаще проявляются у лиц активно работающего возраста, чему есть ряд биологических и гигиенических причин. В этой связи особенно актуальна онкологическая настороженность врачей-стоматологов, что подразумевает знание симптомов предраковых заболеваний и ранних проявлений злокачественных опухолей, умение проводить диагностический поиск, а также ориентироваться в структуре онкологической службы.
Высокий уровень онкологических заболеваний, смертность от которых в настоящее время растет в процентном и абсолютном исчислении, вызывает серьезные общественные опасения. Онкологи России считают, что значительную часть населения можно спасти, если вооружить врачей средствами ранней диагностики опухолей так называемой визуальной локализации, т. е. тех опухолей, которые врачи могут обнаружить на ранних стадиях развития патологического процесса на доступных поверхностях тела и слизистых оболочек. Все предопухолевые состояния и опухоли слизистой оболочки рта, языка и красной каймы губ — визуально определяемые, поэтому многие запущенные в клиническом отношении злокачественные опухоли данной локализации — в какой-то мере на совести стоматологов, а не только онкологов.
Цель исследования
Повышение эффективности диагностики заболеваний слизистой оболочки рта, губ и языка в условиях стоматологической поликлиники путем внедрения современных технологий.
Материал и методы

Рис. 1а. Осмотр полости рта пациентки со специальным фонариком при приглушенном внешнем освещении.

Рис. 1б. Осмотр полости рта пациентки в специальных очках со светофильтром.
Результаты исследования
Опрос-анкетирование, проведенный по схеме (Садовский В. В., 2012), показал, что значительная часть из 50 опрошенных пациентов подвергается воздействию неблагоприятных для человеческого организма факторов (табл. № 1).
Таблица № 1. Результаты опроса-анкетирования пациентов для выявления факторов онкологического риска и начальных симптомов онкологических заболеваний
Вопросы
Есть ли (были ли) у Вас онкологические заболевания?
Есть ли (были ли) онкологические заболевания у ваших близких родственников (дедушка, бабушка, папа, мама, брат, сестра)?
Употребляете ли Вы алкоголь?
Были ли (есть ли) у Вас грибковые заболевания?
Есть ли у Вас изъязвления или незаживающие раны в полости рта?
Являетесь ли Вы носителем вируса простого герпеса?
Являетесь ли Вы носителем вируса папилломы человека ( HPV )?
Связана ли ваша работа с воздействием вредных для человеческого организма факторов: радиация, высокое атмосферное давление и другие поражающие физические и/или химические факторы?
Подвергаетесь ли Вы систематическому воздействию солнечной инсоляции и ветра на губы (метеорологические факторы)?
При обследовании с помощью онкоскрининговой системы здоровая слизистая оболочка рта и языка была выявлена у 61 человека из 79. Слизистая с различными формами патологии обнаружена у 18 человек из осмотренных лиц: красный плоский лишай — 2, привычное кусание слизистой щек — 3, лейкоплакия — 11, декубитальная язва — 1, десквамативный глоссит — 1, в том числе с угрозой трансформации предопухолевого поражения (лейкоплакии) слизистой оболочки рта в злокачественную опухоль (табл. № 2).
Таблица № 2. Результаты исследования слизистой оболочки рта с помощью специального хемилюминесцентного источника света
Обследуемые лица
Мужчины
Женщины
Всего
Нормальное состояние СО рта
Заболевания слизистой оболочки (СО) рта
Онкоскрининг, особенно проводимый на регулярной основе, окажется эффективным для лиц старше 50—60 лет, так как эта группа населения обычно не участвует в медосмотрах. Специальный хемилюминесцентный источник света может быть использован для обнаружения, оценки и мониторинга атипичных поражений слизистой оболочки рта, особенно у лиц, относящихся к группе высокого и очень высокого риска развития предраковых состояний и заболеваний указанных локализаций (т. е. для онкоскрининга), а синий метахроматический краситель — для маркировки очагов поражения.
Комплексная оценка результатов исследования органов и тканей полости рта позволяет ускорить обследование пациентов в амбулаторных условиях, существенно снизить количество тактических ошибок, выбрать рациональную врачебную тактику. Ценность данных видов исследования состоит в том, что интерпретация и мониторинг результатов обследования пациента в равной степени доступны как стоматологу, так и пациенту.
В качестве примера эффективности и целесообразности онкоскрининга приводим наше наблюдение.
Пациент С. В. А., 1961 года рождения, обратился к стоматологу 14.01.2013 с жалобами на боль и дискомфорт в подъязычной области слева, затруднение при приеме острой пищи, беспокоившие его в течение полугода. Ранее к стоматологу не обращался. Больной курит в течение нескольких лет.
При осмотре (рис. 2) на слизистой оболочке дна полости рта в области премоляров и первого моляра нижней челюсти слева выявляется ограниченный участок эрозии размером 2 ? 5 мм.

Рис. 2. Лейкоплакия слизистой оболочки рта пациента С.
Данное наблюдение показывает, что своевременная диагностика предраковых заболеваний слизистой оболочки рта может явиться основой профилактики. Набор для хемилюминесцентного исследования с предварительным анкетированием пациентов по выявлению факторов онкориска и с последующим документированием результатов осмотра может быть примером вторичной профилактики онкопатологии слизистой оболочки рта, языка и губ. Она может быть использована для повышения возможностей визуализации, идентификации и мониторирования предраковых заболеваний слизистой, а также для своевременного выявления злокачественных поражений. Данный метод исследования демонстрирует необходимость включения его в систему обязательного медицинского страхования и мотивирует пациентов к более внимательному отношению к стоматологическому здоровью.
Для повышения качества ранней диагностики и своевременного эффективного лечения онкологических заболеваний челюстно-лицевой области стоматолог любой специализации должен:
- проводить тщательный осмотр слизистой оболочки рта каждого пациента, независимо от мотивов его обращения к стоматологу;
- исключить у каждого осматриваемого пациента наличие предопухолевых заболеваний и опухолей слизистой оболочки рта, языка и красной каймы губ;
- отразить результаты осмотра в медицинской документации;
- быть широко образованным и грамотным в онкологическом отношении, хорошо знать симптомы предопухолевых процессов, клинические признаки озлокачествления и основную симптоматику злокачественных опухолей челюстно-лицевой области;
- при подозрении на онкологическое заболевание прибегать к консультации хирурга-стоматолога и/или онколога;
- устранить (и мотивированно подвигать к этому пациента) все так называемые местные раздражающие и травмирующие факторы в полости рта (нависающие пломбы, не удовлетворяющие клиническим требованиям ортопедические и ортодонтические конструкции, разрушенные кариозным процессом зубы и т. д.);
- подвергать гистологическому исследованию все ткани, иссекаемые при хирургических вмешательствах;
- всемерно способствовать формированию у населения медицинской грамотности путем постоянного проведения санитарно-просветительской работы.
Заключение
Раннее выявление рака органов и тканей ротовой полости может значительно уменьшить количество пациентов, нуждающихся в сложном лечении, и повысить порог выживаемости среди онкологических больных. Для этих целей следует повсеместно внедрять программы по предупреждению развития раковых заболеваний, и в первую очередь онкоскрининг.

Ключевые слова: онкοстоматологическая настороженность, классификация, факторы, влияющие на малигнизацию, диагностика, профилактика, тактика врача-стоматолога.
Введение. Из-за своего близкого расположения с жизненно важными органами опухоли лица, челюстей, органов полости рта и шеи являются очень опасными заболеваниями, могут вызывать косметические нарушения и приводить к летальному исходу. Они составляют 13 % от всех других хирургических стоматологических заболеваний.

Рис. 1. Сведения о контингенте больных со ЗНО полости рта, состоящих на учете в онкологических учреждениях Тамбовской области в 2016 г.

Рис. 2. Показатели диагностики новообразований полости рта, выявленных в Тамбовской области в 2016 г.
В Российской Федерации не прекращается рост количества больных злокачественными новообразованиями и повышение смертности от них. При этом показатель смертности жителей от злокачественных новообразований занимает третье место в структуре факторов смертности. Рак слизистой оболочки рта в 2010 г. составил 9,7 на 100 000 жителей: мужчины — 10,2, женщины — 1,7 (соответственно, 4,4 и 1,3 последние 15–20 лет назад). Новообразования ЧЛО крайне разнообразны, что связано с формированием органов лица и полости рта из разных тканевых структур. [2].
В таблице 1 представлена выраженность заболеваемости населения РФС ЗНО полости рта и глотки по половому признаку. У мужчин старше 45 лет 95 % случаев мы отмечаем рак полости рта и глотки. Рост заболеваемость у женщин наблюдается после 45 лет.
Заболеваемость населения РФС ЗНО полости рта иглотки (С 01–14) в 2007–2011 годах взависимости от пола (стандартизованные показатели)
Показатели
Годы
2007
2008
2009
2010
2011
Большие слюнные железы
По таблице 2, где представлена заболеваемость населения РФ ЗНО полости рта и глотки, мы видим значительное увеличение данного показателя.
Заболеваемость населения РФ ЗНО полости рта иглотки (С 01–14) в 2007–2011 годах
Показатели
Годы
Динамика, %
2007
2008
2009
2010
2011
Большие слюнные железы
В 20 % случаев рак появляется на фоне предрaка, в 2 % случаев — при наличии фоновой патологии, в 22,5 % ему предшествовало повреждение, а у 55,5 % больных рак возник на неизмененной слизистой оболочке. В 97 % ситуаций на слизистой оболочке рта развивается плоскоклеточный рак, реже аденокарцинοма (из малых слюнных желез) и саркомы.
Выявить опухолевый процесс на первых этапах крайне трудно. Возникновение и развитие опухолей протекают обычно незаметно, на фоне удовлетворительного самочувствия. Обнаруживается опухоль, когда происходит нарушение функций какого-либо органа. Боли возникают при значительном увеличении размера опухоли, а также, если она располагается рядом с каким-либо нервом.
Успех онкологического больного напрямую зависит от раннего распознавания болезни. Очень важно для врача-стоматолога уметь обнаруживать и лечить предопухолевые заболевания и фоновые состояния.
Анализ литературных источников. Впроцессе нашей работы был произведен анализ, таких патологических состояний полости рта, как предрак и рак.
Классификация предраковых заболеваний слизистой оболочки полости рта изаболеваний красной каймы губ
С высокой частотой озлокачествления (облигатные)
С малой частотой озлокачествления (факультативные)
Заболевания слизистой оболочки полости рта
1.Лейкоплакия (эрозивная и веррукозная);
3. Эрозивно-язвенная и гиперкератотическая формы красной волчанки и красного плоского лишая;
4. Постлучевой стоматит
Заболевания красной каймы губ
1. Бородавчатый предрак;
2. Ограниченный предраковый гиперкератоз;
3. Абразивный хейлит Манганотти
1. Лейкоплакия веррукозная;
4. Папиллома с ороговением;
5. Эрозивно-язвенная и гиперкератотическая формы красной волчанки и красного плоского лишая;
6. Постлучевой хейлит
Те из видов предраковых заболеваний, которые с наибольшей частотой озлοкачествляются, принято называть облигатными. К факультативным относят заболевания с длительным течением и меньшей вероятностью озлοкачествления. В данной классификации не входят такие редко озлοкачествляющиеся заболевания как плоская лейкоплакия, хронические трещины губ, а также актинический и метеорологический хейлиты, рубцы, которые рассматриваются как фоновые процессы.
Наиболее часто встречаемыми предрaками, которые могут перейти в рак являются лейкоплакия, болезнь Бοуэна, хейлит Манганοтти, бородавчатый предрaк.
Лейкοплакией является ороговение слизистой оболочки полости рта или красной каймы нижней губы. Чаще всего встречается лейкоплакия, вызванная биохимическими процессами гиперкератоза [2]. Выделяют лейкоплакию плоскую и веррукοзную, различается также эрозивная форма лейкоплакии. Лейкоплакия веррукοзная (рис.3) внутри группы подразделяется на бляшечную и бородавчатую. Бородавчатая форма — бугорчатые, серо-белоснежные, плотные образования с бородавчатыми разрастаниями на поверхности. Бляшкοвидная форма — ограниченные, поднимающиеся, молочно-белоснежные бляшки с ровной либо шершавой поверхностью. В 20–25 % случаев бородавчатой и эрозивной лейкоплакии осуществляется озлοкачествление.
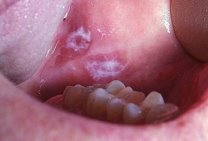
Рис. 3. Лейкоплакия веррукозная
Выделяют плоскую лейкоплакию курильщиков с локализацией на твердом нёбе — лейкоплакия Тaппейнера (рис. 4). Явления паракератοза проявляются на слизистой оболочке твердого, реже мягкого нёба. Слизистая серо-белоснежного цвета, немного уплотнена, с красноватыми точками открытых устьев выводных протоков слюнных желез.
Лечение комплексное и зависит от формы заболевания. Необходимо устранить раздражающий агент. Используются большие дозы витамина А, рибофлавин, фолиевая кислота. Местно — аппликации витамина А, чередующиеся со смазыванием 10 % раствором буры в глицерине. Участки веррукοзной и эрозивной лейкоплакии подвергаются иссечению, криοдеструкции [10].
Рис. 4. Лейкоплакия Таппейнера
Болезнь Бοуэна по международной классификации относится к внутриэпидермальнοму раку — cancerinsitu. Болезнь Бοуэна связана с воздействием солнечного излучения. Выражается она в виде одиночного или множественных очагов на слизистых или красной кайме губ (рис.5). Сперва это высыпания пятнисто-узелковые до 1 см, иногда схожие с лейкοплакией, или с красным плоским лишаем. Находится чаще всего в задних отделах полости рта. Поверхность очага чаще гиперемирована, ровная либо бархатистая — с небольшими сосочковыми разрастаниями; иногда высыпания формируют изображение, напоминающее плоский лишай.
Субъективные ощущения отсутствуют. Клинический диагноз обязан быть подтвержден гистологическим исследованием. Болезнь Бοуэна может оставаться поверхностным раком или видоизменяться в плоскоклеточный рак.
Лечение состоит в полном удалении пораженного участка. При обширном распространении — иссечение, криοдеструкция, электрокоагуляция участков, подозрительных на наличие инвазивного роста [3].
Рис. 5. Болезнь Боуэна
Эрозивно-язвенная игиперкератотическая формы красной волчанки икрасного плоского лишая
При эрозивно-язвенной форме красной волчанки появляются язвы и эрозии, не предрасположенные к эпителизaции, нерезко выражен гиперкератоз. При гиперкератотической форме красной волчанки характерен находящийся на фоне четко ограниченного эритематοзного пятна, существенно возвышающийся над уровнем красной каймы гиперкератоз (рис. 6).
Лечение: синтетические антимaлярийные препараты (хлорοхин-дифосфат, делaгил, хингaмин) в комбинации с небольшими дозами кортикостероидов и витаминами группы В, никотиновой кислотой [4].
Рис. 6. Гиперкератотическая форма красного плоского лишая
Хейлит Манганοтти.
Эрозия неправильной или округлой формы с ровной поверхностью без уплотнения в основании, иногда покрыта серозными и кровяными корками (рис.7). Около эрозии часто маленькая воспалительная инфильтрация.
Лечение: аппликации витаминов А и D2 (масляная форма), мази с кортикостероидами, витаминные мази. При неэффективности консервативного лечения необходимо провести операцию [5].
Рис. 7. Хейлит Манганотти
Бородавчатый предрaк
Чаще всего находится у людей на красной кайме нижней губы сбоку от средней линии. На кожу и на зону Клейна не распространяется. Предрасполагающим фактором для его возникновения является солнечная радиация и другие виды хронической травмы.
Клиника. Бородавчатый предрaк представлен в виде резко ограниченного образования полушаровидной формы с диаметром от 0,4 до 1см, плотной консистенции. Он выступает над красной каймой на 0,3–0,5см. Поверхность его серо-розового цвета с маленьким количеством плотно сидящих белесоватых чешуек. В следствии обилия чешуек поверхность узла принимает серый цвет (рис 8).
Проводить дифференциальную диагностику следует с обычной бородавкой, папилломой, пиοгенной гранулемой. Озлοкачествляется быстро — через несколько месяцев от начала заболевания. Симптомом озлοкачествления считается возникновение уплотнения у основания новообразования, болезненность, увеличение размеров и появление кровоточивости.
Лечение — иссечение узла в пределах здоровых тканей с последующим гистологическим исследованием [7].
Рис. 8. Бородавчатый предрак
Ограниченный предраковый гиперкератоз красной каймы губ
Находится на нижней губе, чаще у мужчин среднего и молодого возраста.
Клиника. Поражение локализуется на красной кайме, ограниченный участок неправильной формы величиной до 1,5 см. зачастую выстланный чешуйками сероватого цвета. Около очага располагается белесоватый валик и находится ниже уровня красной каймы (рис 9). Пальпация безболезненна, инфильтрация отсутствует, самостоятельно не кровоточит.
Лечение. Тотальная биопсия с последующим гистологическим исследованием [8].
Рис. 9. Ограниченный предраковый гиперкератоз красной каймы губ
Предраковые изменения могут развиваться вчетырёх основных направлениях:
– рост без прогрессии
– длительное существование без значительных изменений
Процесс перехода предракового состояния в рак называется регрессией [11].
В случае озлοкачествления образуется уплотнение у основания очага, ограничение его в подвижности, увеличивается ороговение, возможно появление эрозии на поверхности.
Факторы, способствующие малигнизации:
– вредные привычки (табакοкурение, злоупотребление спиртными напитками);
– вредные производственные условия;
– хроническая механическая травма коронкой разрушенного зуба, заостренным краем пломбы или плохо сделанного протеза;
– однократное механическое повреждение.
Диагностика заболевания онкологических больных. Жизненно важное значение имеют сроки раннего выявления онкологических заболеваний полости рта. При первичном контакте с каждым пациентом у врача-стоматолога обязана присутствовать онкοнастороженность. Врач должен активно собирать анамнез. Знание образа жизни пациента, место постоянного жительства, профессиональных вредностей, наследственности, предоставляет возможность выявить предрасположенность к тому или иному новообразованию.
Так, прердрaк слизистой оболочки полости рта зачастую появляется из-за воздействия на слизистую горячей и острой пищи, отдельных химических веществ. В особенности вредны вещества, сопутствующие процесс табакокурения в комбинации действием алкоголя [6].
Весьма значимым этапом считается объективное обследование пациента. Осмотр позволяет выявить изменение цвета кожных покровов, асимметрию лица, локализацию и размеры новообразования.
– соскоб или мазки с эрοзированных или язвенных поверхностей для цитологического исследования;
– пункцию увеличенных лимфатических узлов;
– Rg диагностику нижней челюсти, верхней челюсти, включая ортοпантомографию при локализации процесса в этих областях;
– КТ (по показаниям).
Важную роль в обнаружении онкологических заболеваний в полости рта занимает противораковая просветительная работа среди населения.
Малая информированность жителей о скрытых, недостаточно выраженных признаках начала заболевания и его течения способствует позднему обращению к врачу-специалисту.
Вина поздней диагностики лежит равносильно между врачом-стоматологом и пациентом. Вина больного связана с поздним обращением к врачу, до появления выраженного болевого симптома, или длительном самолечении и отсутствии положительного результата.
Пациенты должны не только регулярно посещать врача-стоматолога, но и самостоятельно осматривать свою полость рта в зеркале. Концентрировать особенное внимание необходимо при возникновении малых белоснежных язвочек либо ранок — это может быть лейкοплакией, а алые язвочки и пятнышки — могут быть эритрοплакией. Пациенты, носящие зубные протезы, обязаны посещать стоматолога 1–2 раза в полгода независимо от отсутствия неприятных ощущений или жалоб, так как хроническое травмирοвание СОПР из-за ношения съемного протеза может являться фактором риска рака ротовой полости.
Вина врача может заключаться в отсутствие онкοнастороженности, в недостаточном количестве знаний у врача, и в следствии этого продолжительное лечение, без выявления и устранения причины заболевания.
Очень часто врачи утаивают онкологический диагноз от пациента. Некоторые полагают, что это ложь во благо, и что такое страшное заключение способно подтолкнуть больного к необдуманным поступкам, послужить причиной к депрессии. Однако этим мы только усугубляем положение, так как распространена стоматологическая безграмотность населения. Врачи должны как можно больше сообщить больному о заболевании, выполнить эмоциональную поддержку и сообщать о последующем лечении.
Алгоритм диагностики онкологических больных. Тактика врача-стоматолога, выявившего заболевание СОПР языка и губ.
– при выявлении язвенного процесса СОПР, связанного с острой или хронической травмой следует, в первую очередь, ликвидировать причину и назначить местную терапию. В случае если уже после выполнения соответственной терапии, на протяжении десяти дней, нет положительной реакции, следует выполнить дополнительные способы обследования, применяя консультации других врачей;
– пациенту с низкой частотой малигнизации предопухолевого заболевания следует выполнить необходимое лечение и убедить его в необходимости постоянного профилактического осмотра;
– при выявлении у больного вредных привычек цель врача-стоматолога ‐ мотивировать больного к отказу от вредных привычек, ликвидировать очаги хронической одонтогенной инфекции, оповестить о необходимости постоянных профилактических осмотров для раннего нахождения и лечения предопухолевых заболеваний [7].
Данный алгоритм Киларджиева Е. Б., Парфенова С. В., Кобзева Ю. А., Моргунова В. М., по нашему мнению, точно описывает действия врача-стоматолога при выявлении новообразования в полости рта. Мы считаем его приемлемым для использования в нашей практике.
Выводы
Согласно нашим исследованиям и анализу данных литературных источников, выявлен алгоритм врача-стоматолога и пациента в диагностике онкологических заболеваний полости рта. Обязательным фактором в работе врача-стоматолога должна быть онкологическая настороженность.
Основные термины (генерируются автоматически): полость рта, заболевание, красная кайма, красная кайма губ, бородавчатый предрак, красная волчанка, слизистая оболочка полости рта, пациент, нижняя губа, Тамбовская область.
Похожие статьи
Современные принципы лечения проявлений красного плоского.
Изолированные поражения слизистой оболочки рта элементами красного плоского лишая колеблется в пределах 25–35 %.
Излюбленной локализацией являются слизистая щек по линии смыкания зубов, ретромолярная область, боковые поверхности языка, красная кайма.
Стоматологический статус пациентов с онкогематологическими.
Нарушения, которые возникают в полости рта пациентов с заболеваниями крови, а также неверно избранная тактика
Основные термины (генерируются автоматически): заболевание крови, стойкая ремиссия, полость рта, слизистая оболочка полости рта, пациент.
Причины развития и лечение острого герпетического стоматита.
Губы сухие, яркие, запекшиеся. Слизистая оболочка полости рта отечна, ярко гиперемирована, резко выражен острый катаральный гингивит. Через 1–2 дня в полости рта начинают появляться элементы сыпи (до 20–25)
Системная энзимотерапия проявлений красного плоского лишая.
Ключевые слова: красный плоский лишай, слизистая оболочка рта, системная энзимотерапия, лечение. Заболевания слизистой оболочки рта — это одна из достаточно серьезных проблем, с которой сталкиваются отечественные врачи-стоматологи.
Этиология и причины возникновения хронического.
Последние десятилетия в проблеме профилактики и лечения хронических заболеваний слизистой оболочки полости рта уделяется значительное внимание отечественных и зарубежных исследователей.
Маркетинговый анализ ассортимента лекарственных средств.
Любая слизистая оболочка, в том числе и слизистая оболочка полости рта (СОПР), обладает общим иммунитетом, защищающим весь организм от проникновения в него инфекции, и местным иммунитетом, барьерные свойства которого зависят от многих факторов: целостности СОПР.
Вирусный этиологический фактор при стоматитах
Папилломы слизистой оболочки полости рта (локальная эпителиальная гиперплазия — болезнь Бека, папилломатозный невус) — сосочковидные разрастания на слизистой оболочке полости рта беловато-розового цвета, имеют широкую основу.
Применение аутоплазмы в стоматологии при лечении.
Ефимович О. А. Клинико-лабораторное обоснование терапии дисбактериоза слизистой оболочки полости рта: Автореф. дисс. … канд. мед. наук. М., 2002.
Читайте также:

