Опасность вич заключается в том что он генетически наследуется
Обновлено: 01.05.2024
ВИЧ (вирус клеточного иммунодефицита) – ретровирус, вызывающий синдром приобретенного иммунодефицита – СПИД. Один из путей передачи – половым путем и, следовательно, относится к заболеваниям, передающимся половым путем.
- H – человек, так как вызывает заболевание после попадания в организм человека;
- I – иммунодефицит, так как вирус вызывает нарушение системы иммунитета, то есть неспособность организма защищаться от инфекций;
- V – вирус, так как причиной заболевания является вирус, микроорганизм, неспособный воспроизводиться сам по себе, то есть он использует материал и энергию клетки для воспроизводства.
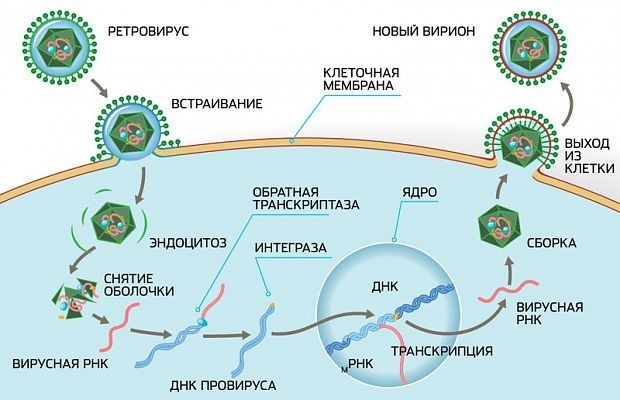
Для ретровирусов характерно то, что они медленные вирусы. Это означает, что они остаются в организме хозяина в течение длительного времени и приводят к медленному прогрессированию болезни до смерти. Вирус имеет сферическую форму и содержит геном двойной РНК. Когда он попадает в клетку хозяина, вирус использует фермент обратной транскриптазы, чтобы преобразовать свой геном РНК в ДНК, которая затем встраивается в геном хозяина.
Попадая в организм человека, ВИЧ атакует определенный тип белых кровяных клеток, Т-лимфоциты, размножается в них, уничтожает их и постепенно приводит к ослаблению иммунитета . В соответствии с конкретными молекулами, обнаруженными на поверхности этих клеток, их также называют клетками CD4.
Существует два типа (серотипов) вируса ВИЧ:
ВИЧ1 более опасен. Пока что ВИЧ-подобные вирусы были обнаружены у многих приматов, что привело к гипотезе о том, что они природные хранилища вируса.
Эпидемиология ВИЧ
По оценкам, в настоящее время в мире насчитывается более 34 миллионов человек, живущих с ВИЧ, из них более 97% – в менее развитых странах (страны Африки к югу от Сахары).
Наибольшее количество инфицированных приходится на возрастную группу от 25 до 39 лет.
Путь передачи и группы риска
ВИЧ передается несколькими путями:
- Незащищенный половой акт – люди (гетеросексуалы и гомосексуалисты) имеют высокий риск частой смены половых партнеров и практики незащищенного полового акта. Анальный секс является наиболее рискованным из-за наиболее чувствительной слизистой оболочки, за ним следует вагинальный и, реже, оральный.
- Через кровь и ее производные – многократное получение донорской крови и других продуктов крови при переливании. Сегодня встречается редко из-за введения обязательного тестирования продуктов крови.
- Вторичное использование шприцев для инъекций наркоманами – люди, делящиеся наркотиками и употребляющие наборы для инъекций после других, подвергаются высокому риску.
- Через инфицированную мать ребенку – при беременности, родах и грудном вскармливании.
Пути, по которым ВИЧ НЕ передается:
- воздух;
- общие контакты – рукопожатие, объятия, поцелуи в щеку;
- интимный контакт без полового акта – поцелуи, ласки;
- контакт с объектами – в автобусе, поезде, школе;
- использование общественных туалетов, саун, бассейнов, душевых;
- кашель, чихание, контакт кожи со слезами или слюной;
- лечение в больницах, медицинских и стоматологических клиниках при соблюдении стандартных гигиенических мер;
- оказание первой помощи при соблюдении стандартных мер гигиены;
- массаж, физиотерапия, прокалывание ушей, пирсинг при соблюдении стандартных гигиенических мер;
- царапины и укусы домашних животных (собаки, кошки);
- укусы насекомых;
- уход за людьми, живущими с ВИЧ и СПИДом, при условии соблюдения стандартных мер гигиены.
Течение ВИЧ-инфекции
ВИЧ-инфекция протекает хронически. Начинается она с попадания вируса в кровоток и длится всю жизнь. Инфекция проникает в организм через слизистые оболочки или при прямом поступлении через кровь, атакует конкретную клетку иммунной системы – Т-лимфоцит.
Когда внутри Т-лимфоцитов образуется большое количество новых вирусов, они лопаются, выделяют множество вирусов в кровоток и распадаются. Вирусы попадают в новые Т-лимфоциты, и процесс повторяется. Таким образом, ВИЧ постепенно разрушает Т-лимфоциты, что приводит к ослаблению иммунитета и возникновению оппортунистических инфекций и некоторых злокачественных заболеваний.
Хотя ВИЧ в первую очередь атакует определенные клетки иммунной системы, Т-лимфоциты, он также может напрямую повредить некоторые другие клетки организма, например, нервные клетки, клетки слизистой оболочки пищеварительного тракта.
Прогрессирование ВИЧ-инфекции делится на 3 этапа:
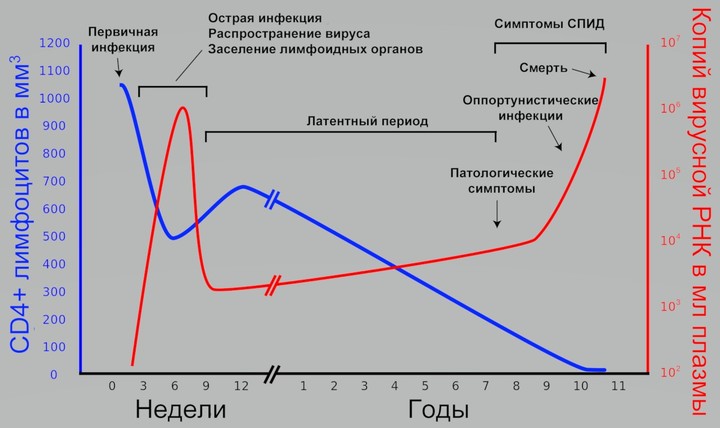
Развивается через 3-6 недель после заражения. Чаще всего проявляется легким вирусным заболеванием (лихорадка, головная боль, боль в горле, боли в мышцах и суставах, сыпь, увеличение лимфатических узлов) и остается незамеченным. Обычно это длится от 1 до 3 недель.
Во время этой фазы в кровотоке циркулирует большое количество вируса, и человек очень заразен. ВИЧ в больших количествах присутствует в половом секрете. Вирус активно размножается, атакует и убивает клетки иммунной системы, что лучше всего видно по уменьшению количества лимфоцитов CD4.
Очень часто у ВИЧ-положительных людей отсутствуют какие-либо симптомы поражения иммунной системы. Это не показатель того, что иммунная система не повреждена.
Уровень вируса в крови может упасть очень низко, но человек до сих пор заражен и антитела могут быть обнаружены в крови. Недавние исследования показали, что на этой стадии ВИЧ не отдыхает, а очень активен в лимфатических узлах.
Большое количество клеток CD4 инфицируется и умирает, производя большое количество вируса. Эти факторы могут быть подтверждены путем измерения уровня клеток CD4 и количества вируса в крови. Длится от 7 до 10 лет .
а) Ранняя — количество лимфоцитов CD4 резко падает, пока не достигнет 200, когда он переходит во вторую фазу.
Проявляется такими общими симптомами, как:
- лихорадка и потливость;
- потеря аппетита и массы тела – более 4,5 кг за 2 месяца;
- сильная утомляемость – продолжающаяся несколько недель без видимых причин;
- длительный понос;
- увеличение лимфатических узлов, особенно на шее и подмышках;
- грибковые инфекции ротовой полости;
- одышка и сухой кашель;
- розовые или пурпурные пятна на коже, обычно твердые и напоминающие синяки.
б) Продвинутая — количество лимфоцитов CD4 менее 200 , наблюдается развитие и поддержание этих общих симптомов с развитием характерных оппортунистических инфекций, заболеваний, опухолей, синдрома распада и деменции.
в) Поздняя — количество лимфоцитов CD4 менее 50 / мл. Эта стадия заболевания опасна для жизни, у нелеченных пациентов приводит к смерти.
Важно помнить, что вирус ВИЧ может передаваться от инфицированного человека не инфицированному на любой стадии инфекции.
Синдром приобретенного иммунодефицита (СПИД)
- A – приобретенный, так как заболевание возникает у человека после заражения ВИЧ, то есть приобретается в течение жизни, а не передаётся по наследству (генетически).
- I – иммунный, так как влияет на иммунную систему, то есть на специализированные клетки, находящиеся в крови и борющиеся с различными инородными телами и микроорганизмами (бактериями, грибами, вирусами).
- D – дефицит, так как возникает слабость иммунной системы, и защитные силы теряют способность эффективно бороться с различными инородными телами и микроорганизмами.
- S – синдром, так как обозначает набор состояний и признаков заболевания, характерных для конкретного заболевания; больной СПИДом может страдать от целого ряда различных заболеваний и оппортунистических инфекций.
СПИД представляет собой последнюю и наиболее тяжелую стадию ВИЧ-инфекции, вызванную серьезным повреждением иммунной системы. СПИД – это фактически название группы заболеваний, возникающие в результате ослабленной иммунной системы человека, инфицированного ВИЧ.
Многочисленные микроорганизмы окружающие людей постоянно, но иммунная система здорового человека справляется с ними без видимых симптомов. У больных СПИДом обычные микроорганизмы приводят к широкому спектру воспалительных заболеваний. И пациент, в конечном итоге умирает, от инфекций, вызванных бактериями, вирусами, грибами, простейшими, не представляющих значительной опасности для здоровья людей.
ВИЧ также напрямую повреждает клетки нервной системы, вызывая тяжелые неврологические заболевания (ВИЧ-энцефалопатию).
Вирус иммунодефицита человека (ВИЧ) – это инфекционное заболевание, в основе которого лежат значительные деструктивные изменения иммунной, нервной и других систем организма. Болезнь характеризуется хроническим, многолетним течением, которое сопровождается вторичными инфекционными процессами и формированием новообразований.
К отдельной форме заболевание отнесли в конце прошлого века, после выявления значительного количества больных, страдающих иммунодефицитом, проявлениями пневмоцистной пневмонии и саркомы Капоши. Этому симптомокомплексу дали название СПИД – синдром приобретенного иммунодефицита человека. СПИД развивается после малосимптомного и бессимптомного периода инфицирования, длящегося несколько лет и постепенно разрушающего иммунную систему человека. Признаки СПИДа более выражены, чем на стадии ВИЧ (вирус иммунодефицита человека).
Классификация
Классификация ВИЧ включает разные группы болезни, которые вызваны вирусом и имеют различные проявления:
- инфекционные и паразитарные болезни (микозы, кандидозы, цитомегаловирус и др.);
- злокачественные новообразования (саркома Капоши, лимфома Беркитта, неходжкинские лимфомы, недоброкачественные новообразования кроветворной, лимфатической систем и родственных к ним тканей, множественные и неуточненные новообразования);
- иные уточненные болезни и состояния (энцефалопатии, лимфатический интерстициальный пневмонит, изнуряющий синдром, генерализованная лимфоаденопатия, иммунологические и гематологические нарушения, острый ВИЧ-инфекционный синдром и др.);
- неуточненные патологии.
Этиология
Вирус иммунодефицита человека – возбудитель заболевания, который был выделен в 1984 году и отнесен к ретровирусам. Вирион имеет сферическую форму, геном ВИЧ образован двухнитевой РНК. В пораженных клетках вирус формирует ДНК.
Выделяют вирусы 2 типов:
- ВИЧ-1 – широко распространен, это - главный возбудитель ВИЧ-инфекции и СПИДа в Америке, Европе и Азии;
- ВИЧ-2 – возбудитель распространен меньше, имеет много общего с ВИЧ-1, чаще всего его выделяют в Западной Африке.
Вирус иммунодефицита отличается высокой антигенной изменчивостью. Он очень быстро проходит весь свой жизненный цикл, всего за 1-2 дня. При этом, в день образуется до 1 миллиарда вирионов.
Вирус иммунодефицита человека очень чувствителен к внешним воздействиям и быстро гибнет под действием всех дезинфектантов. Заразность вируса резко снижает нагревание до 55 градусов, а при повышении температуры до 70-80 градусов возбудитель погибает уже через 10 минут.
ВИЧ устойчив к воздействию ультрафиолета и ионизирующей радиации, хорошо переносит низкие температуры. Также, он способен годами сохранять жизнеспособность в крови, предназначенной для переливания.
Пути заражения
Основной источник заболевания – инфицированный ВИЧ человек. Опасность заражения сохраняется на всех стадиях инфекции, пожизненно. В большом количестве возбудитель содержится в крови (в том числе и в менструальной), сперме, вагинальных выделениях. Возбудитель можно обнаружить в слюне, женском молоке, слезной, спинномозговой жидкостях. Наибольшую опасность представляют кровь, сперма и вагинальный секрет.
Пути передачи ВИЧ:
- половой (гомо- и гетеросексуальный) – риск инфицирования вирусом иммунодефицита повышается при увеличении количества половых партнеров, при инфекциях, которые передаются при сексе (герпес, сифилис, хламидиоз, трихомониаз и гонорея), бактериальных вагинозах;
- парентеральный (трансфузионный – переливание крови, трансплацентарный – через плаценту от матери ребенку, инъекционный – инъекции наркотиков);
- вертикальный – от матери к плоду во время беременности, а также заражение ребенка при родоразрешении и грудном вскармливании;
- трансплантационный.
Риск профессионального инфицирования медицинского работника на рабочем месте повышается при: порезе или уколе предметом с видимыми следами крови, глубоком повреждении тканей, порезе вены или артерии зараженного пациента, высоком уровне у пациента вирусной нагрузки.
Риск развития заболевания при любом пути передачи во многом определяется вирусной нагрузкой. При этом низкий уровень содержания РНК возбудителя в крови не исключает возможности заражения ВИЧ-инфекцией.
Пути заражения ВИЧ неразрывно связаны с рискованным сексуальным поведением, обусловленным употреблением спиртных напитков и наркотических веществ. Алкоголь и наркотики усиливают сексуальное влечение, делают поведение менее самокритичным, что подталкивает человека к необдуманным поступкам.
Индивидуальные (поведенческие) факторы риска включают:
- беспорядочные сексуальные контакты;
- занятия коммерческим сексом;
- употребление инъекционных наркотических средств;
- неиспользование средств профилактики заболеваний, которые передаются при сексуальном контакте;
- сексуальное насилие;
- раннее начало половой жизни и др.
Вероятность передачи ВИЧ-инфекции повышает наличие очагов воспаления, повреждения слизистой половых органов.
Бытовая передача вируса не доказана.
Группы риска:
- лица, занятые в сфере коммерческого секса и их клиенты;
- медицинские работники (особенно, медики, работающие в инфекционных отделениях);
- мужчины-гомосексуалисты;
- лица, находящиеся в заключении;
- наркоманы, употребляющие инъекционные наркотики;
- мигранты;
- бездомные;
- подростки, состоящие на учете в инспекциях по делам несовершеннолетних.
Патогенез
После присоединения ВИЧ к оболочке клетки-хозяина его РНК с некоторыми вирусными ферментами проникает в цитоплазму клетки, где с помощью вирусного фермента происходит обратная транскриптаза на РНК возбудителя с образованием ДНК.
ДНК вируса иммунодефицита проникает в ядро клетки и встраивается в ДНК клетки-хозяина, после чего клетки человека начинают самостоятельно производить новые вирусные частицы. Новые вирусные частицы проникают в новые клетки, имеющие рецептор CD4, что приводит к:
- нарушению межклеточных взаимодействий внутри иммунной системы;
- функциональной иммунной несостоятельности;
- постепенному истощению клеток крови лимфоцитов CD4;
- прогрессирующему иммунодефициту.
Период от момента инфицирования до смерти у каждого различный, без необходимого лечения он составляет 10-12 лет.
Клинические проявления и осложнения
При ВИЧ-инфекции выделяют несколько периодов заболевания:
- инкубационный – длится с момента инфицирования до развития острой стадии заболевания;
- асимптомная (бессимптомная, латентная) стадия – включает острый период, бессимптомную инфекцию (сероконверсия) и персистирующую генерализованную лимфаденопатию (ПГЛ);
- стадия выраженных клинических проявлений, которые характеризуются появлением вторичных заболеваний (СПИД-ассоциированный комплекс, или пре-СПИД);
- терминальная стадия (стадия СПИД).
С момента заражения до появления первых симптомов ВИЧ может пройти от 2-3 недель до 3 месяцев. Изредка инкубационный период затягивается до 1 года. При заражении у больных развивается острый ретровирусный синдром с первичными признаками ВИЧ, напоминающими ОРВИ или грипп: лимфаденопатия, лихорадка, артралгия, миалгия, сильная головная боль, ангина, иногда – появляется пятнисто-папулезная сыпь, диспепсические расстройства (тошнота, рвота или диарея), увеличивается печень и селезенка.
В бессимптомный период ВИЧ-инфекция клинически себя никак не проявляет. Человек чувствует себя вполне здоровым, но при этом в его крови есть вирус иммунодефицита и он несет опасность заражения для окружающих. Бессимптомная стадия может длится от 3-6 месяцев до 3-5 лет.
Стадия ПГЛ длится несколько лет. Основной признак ВИЧ – увеличение лимфатических узлов (подчелюстных, заднешейных, подмышечных). Узлы безболезненные, плотно-эластичные до 1-3 см в диаметре. Возможно незначительное повышение температуры, увеличение печени и селезенки.
СПИД-ассоциированный комплекс характеризуется появлением инфекционных, оппортунистических заболеваний, свойственных пациентам с иммунодефицитом. Инфекции могут вызывать простейшие, грибы, бактерии и вирусы.
Осложнения ВИЧ-инфекции на стадии пре-СПИДа:
- Бактериальная пневмония
- Пневмоцистная пневмония
- Внелегочный криптококкоз
- Кандидоз трахеи, легких, бронхов, пищевода
- Криптоспоридиоз с продолжительной диареей
- Инвазивный рак шейки матки
- Цитомегаловирусная инфекция
- Гистоплазмоз
- Лейкоэнцефалопатия
- Герпес
- Саркома Капоши
- Диссеминированная инфекция, вызванная атипичными микобактериями
- Лимфома (иммунобластная, Беркитта, В-клеточные формы)
- Энцефалопатия, сопровождающаяся слабоумием
- Токсоплазмоз головного мозга, глаз, легких
- Хронический кишечный изоспориаз и др.
СПИД-ассоциированный комплекс длится несколько лет с периодами относительного улучшения состояния.
Симптомы ВИЧ прогрессирования:
- генерализованная лимфаденопатия;
- необъяснимая потеря веса (более 10%);
- повышенная утомляемость;
- хроническая диарея (более 3 недель);
- одышка;
- сухой кашель;
- ночная потливость;
- лихорадка, длящаяся более двух недель (иногда до 3 недель и более);
- дерматиты.
ВИЧ-инфекция, терминальная стадия которой носит необратимый характер и заканчивается смертью, характеризуется активным развитием инфекционных заболеваний и новообразований. Клинические проявления очень разнообразны, что обусловлено многочисленными инфекционными агентами, множественным поражением систем и органов.
Симптомы СПИДа терминальной стадии условно подразделяют на разные типы болезней:
- легочной тип – развитие инфильтративной пневмонии;
- желудочно-кишечный тип – тяжелая хроническая диарея;
- церебральный тип – атрофия коры головного мозга, поражения сосудов мозга, слабоумие;
- диссеминированный тип – стойкая лихорадка, падение массы тела, нарастающая слабость, поражение разных органов.
Наиболее ярким опухолевидным проявлением является саркома Капоши (опухоль кровеносных сосудов головы, конечностей, туловища, слизистой оболочки рта, органов желудочно-кишечного тракта, легких).
Диагностика
Стандартной диагностикой ВИЧ являются лабораторные методы исследования:
- обнаружение антител в иммуноферментном анализе (ИФА);
- реакции иммунного блоттинга (окончательно подтверждают инфицирование ВИЧ);
- экспресс-тесты на ВИЧ;
- радиоиммунопреципитация;
- реакция непрямой иммунофлюоресценции (РНИФ); .
В подавляющем большинстве выявить антитела к ВИЧ можно в течение первых 3 месяцев после инфицирования. При получении положительного результата инфекционист назначает повторный анализ на вирус иммунодефицита.
Лабораторная диагностика ВИЧ, ее дополнительные методы, направлены на выявление в иммунной системе нарушений, вызванных иммунодефицитом: определение общего количества лимфоцитов и Т-хелперов (CD4), вычисление соотношения Т-хелперов и Т-супрессоров (CD8).
Лечение
Лица с диагностированной ВИЧ-инфекцией госпитализируются в инфекционные отделения. Больных в стадии СПИДа помещают в специальные боксовые отделения для предупреждения заражения другими инфекциями.
Лечение ВИЧ основные направления:
- этиотропное лечение – антиретровирусная терапия;
- иммуномодулирующая терапия;
- лечение инфекционных заболеваний, антибиотикотерапия;
- лечение новообразований.
Иммуномодулирующая терапия является одним из основных лечебных направлений и включает заместительное и иммуностимулирующее лечение.
Иммунозаместительная терапия предусматривает пересадку костного мозга и переливание лимфоцитарной массы.
Иммуностимулирующая терапия проводится медикаментозными препаратами.
Противоопухолевое лечение ВИЧ заключается в лучевой и специальной фармакотерапии.
Пациенты с вирусом иммунодефицита находятся под диспансерным наблюдением пожизненно, независимо от стадии болезни.
При этом проводится регулярное лабораторное обследование, анализ клинических проявлений заболевания для наблюдения за течением инфекционного процесса и функциональным состоянием системы иммунитета.
Профилактика ВИЧ-инфекции
Первостепенное значение в предупреждении распространения ВИЧ имеет пропаганда здорового образа жизни (отказ от употребления алкоголя и приема наркотиков) и правильного сексуального поведения (использование презервативов, ограничение половых партнеров).
Специфическая профилактика ВИЧ с применением вакцинации находится только на стадии разработки.
При нахождении ВИЧ-инфицированного больного в условиях дома члены семьи должны соблюдать необходимый санитарно-гигиенический режим:
- регулярная влажная уборка помещений;
- туалет и ванную комнату необходимо обрабатывать обязательно с дезинфектантами;
- белье должно подвергаться кипячению;
- режущие предметы и ножницы по возможности обрабатывать спиртом и т.д.
Статья носит информационно-ознакомительный характер. Пожалуйста, помните: самолечение может вредить вашему здоровью.
Испытания лекарств от ВИЧ часто включает в себя аналитическое прерывание лечения, когда пациенты с ВИЧ прекращают прием антиретровирусной терапии (АРТ), чтобы ученые могли понаблюдать, как неконтролируемый вирус реагирует на исследуемые препараты.
Участие в такого рода клинических испытаниях может вызвать страх у человека с ВИЧ, который привык поддерживать неопределяемую вирусную нагрузку. Кроме того, предыдущее исследование, проведенное доктором Лау, показало, что многие люди с ВИЧ не были уверены в том, как работают эти испытания, и многие из них не были готовы к длительным периодам определяемой вирусной нагрузки.
Ученые работают над различными стратегиями излечения ВИЧ-инфекции. Некоторые методы нацелены на сокращение латентных резервуаров ВИЧ — инфицированных иммунных клеток, которые не производят новые вирионы в течение многих месяцев или лет. Другие виды терапии пытаются повысить способность иммунной системы контролировать вирус.
Существуют два типа исследований, основанных на прерывании лечения, которые используются для оценки потенциальной терапии: изучение времени до восстановления вирусной активности (TVR) и изучение контрольных точек. В исследованиях TVR после того, как участники прекращают АРТ, ученые измеряют время, необходимое, чтобы вирусная нагрузка сначала достигла обнаруживаемого уровня (50 копий/мл), а затем время, необходимое для достижения более высокого порога (часто 10 000 копий/мл), после чего участники возобновляют прием АРТ. Если тем, кто получает лечение, требуется больше времени для достижения этих пороговых значений по сравнению с контрольной группой, это указывает на то, что терапия замедляет восстановление вирусной активности. Исследования TVR часто используются для оценки методов терапии, нацеленной на резервуары, обычно они длятся всего несколько недель.
Исследования контрольных точек демонстрируют, насколько эффективно иммунная система участников контролирует ВИЧ самостоятельно. В этих гораздо более длительных исследованиях (до нескольких месяцев) исследователи позволяют вирусным нагрузкам участников достигать высоких уровней, имитируя острую фазу ВИЧ, чтобы проследить, сможет ли их иммунная система в дальнейшем снизить эту нагрузку. Порог для возобновления АРТ обычно устанавливается на высоком уровне (часто 100 000 копий/мл). Когда участники, получающие лечение, способны контролировать ВИЧ при более низких уровнях вирусной нагрузки и в течение более длительного времени, чем участники контрольной группы, это говорит о том, что терапия повышает их иммунитет против вируса.
Несмотря на то, что нет конкретных рекомендаций, определяющих, как планировать исследования с прерыванием лечения, группа ученых, занимающихся исследованием ВИЧ, встретилась в 2018 году, чтобы обсудить этические стороны и выработать методы для снижения риска. Прекращение АРТ во время этих исследований не просто подвергает участников риску длительных периодов определяемой, а в некоторых случаях и высокой вирусной нагрузки. Более высокие вирусные нагрузки также могут подвергать опасности и ВИЧ-отрицательных половых партнеров участников.
До сих пор в большинстве исследований риск снижался за счет небольшого числа участников и отсутствия контрольной группы, которая вместо лечения принимала неактивное плацебо. Включение контрольной группы важно, потому что это позволяет ученым сравнивать тех, кто принимает лекарства, с теми, кто находится на плацебо. Тем не менее научное сообщество обсуждало этичность использования контрольных групп в подобных испытаниях лекарств, потому что они подвергаются длительным периодам повышенной вирусной нагрузки в отсутствие каких-либо препаратов, даже экспериментальных.
Исследование
Доктор Лау и ее коллеги использовали данные предыдущих клинических испытаний для создания математических моделей, позволяющих оценить, как различные их параметры влияют на статистическую мощность испытания.
Статистическая мощность аналогична чувствительности. Например, тест на ВИЧ с чувствительностью 80% успешно идентифицирует вирус у 80% людей, которые на самом деле ВИЧ-положительны, но не выявит у остальных 20% ВИЧ-положительных людей. Когда клиническое испытание, оценивающее лечебную терапию, должно достигнуть статистической мощности в 80% (при условии, что терапия имеет реальную пользу для тех, кто ее принимает), в испытании будет 80-процентная вероятность обнаружить пользу и 20-процентная вероятность ее упустить.
Проще говоря, чем больше данных задействовано в испытании, тем большей статистической мощностью оно будет обладать. Такие факторы, как количество участников, число контрольных параметров, продолжительность испытания и частота анализов крови, влияют на статистическую мощность испытания.
Результаты пробного моделирования TVR
В отношении недавнего исследования TVR с участием 13 человек такая модель показала, что при мощности 80% исследование выявило бы только лечение со значительным снижением реактивации (от 70 до 80%). Чтобы исследование TVR выявило снижение реактивации на 30%, потребуется уже по 120 участников в группе терапии и в контрольной группе. Поскольку в большинстве исследований TVR задействовано малое число участников, они, вероятно, не устанавливают умеренных результатов терапии.
Может показаться нелогичным планирование исследования для выявления меньшего эффекта от лечения, когда конечной целью является поиск максимальной пользы (т. е. терапия, приводящая к 100% снижению реактивации). Тем не менее на начальных этапах поиска лекарства необходимо фиксировать даже умеренные результаты, чтобы решить, требует ли этот метод дальнейшего изучения.
Помимо рекомендации увеличить количество участников, команда предлагает использовать ретроспективные контрольные данные в дополнение к контрольным группам. Данные из предыдущих испытаний, в которых люди прерывали АРТ, могли бы повысить потенциал выявления умеренной пользы от лечения. Они смоделировали гипотетическое исследование TVR, в которое вошли 50 участников и 50 человек из контрольной группы. При мощности 80% эта конструкция может обнаруживать снижение реактивации до 43%. Добавление ретроспективных данных еще 150 участников позволило бы в том же испытании выявить снижение до 36%.
Такое моделирование также не показало практически никакого улучшения способности обнаруживать снижение реактивации при увеличении продолжительности испытаний TVR свыше пяти недель. После этого срока модель предсказала улучшение обнаружения не более чем на 1%. Точно так же они не обнаружили практически никакой пользы от проведения лабораторного мониторинга чаще, чем раз в неделю. Наблюдение за людьми два раза в неделю почти не помогло обнаружить снижение реактивации.
Ученые провели отдельный анализ для оценки максимального риска передачи ВИЧ во время исследований TVR на основе предыдущих данных. Они оценили максимальный риск передачи, предполагая, что участники занимались незащищенным сексом и что доконтактная или другие методы профилактики не использовались. Кроме того, если во время еженедельного мониторинга не сообщать пациенту показатель вирусной нагрузки сразу же, то участник, которому необходимо возобновить АРТ (если его вирусная нагрузка превысила 1000), скорее всего, отложит это до следующего еженедельного визита.
Было подсчитано, что в этом случае во время пятинедельного исследования TVR с порогом вирусной нагрузки 1000 для повторного начала АРТ максимальный риск передачи ВИЧ составил 3,6 на 1000 участников, занимающихся вагинальным сексом. При анальном сексе для вводящих партнеров максимальный риск составлял около 7 на 1000, а для принимающих партнеров — около 70 из 1000. Изменение схемы исследования, включающее экспресс-тестирование на вирусную нагрузку и возобновление АРТ в тот же день, снижает предполагаемый максимальный риск до 0,9, 1,8 и 18 на 1000 соответственно.
Результаты моделирования исследования по контрольным величинам
Исследования контрольных точек должны иметь достаточную статистическую мощность, чтобы отделять преимущества предлагаемой лечебной терапии от контроля после лечения. Используя результаты исследования CHAMP, ученые предположили, что исходный уровень контроллеров после лечения ниже 4%. Если целью исследования было определить увеличение количества контролеров до 20% (это означает, что терапия помогла людям, которые не являются естественными контроллерами, подавить вирус), их модель показала, что 24-недельное исследование со статистической мощностью 80% потребует участия 60 пациентов.
Из-за чрезвычайно высоких вирусных нагрузок в типичных исследованиях контрольных величин (до 100 000) авторы сравнили, как использование более консервативного порогового значения (1000) для возобновления АРТ повлияет на способность этих исследований обнаруживать увеличение числа контроллеров после лечения. CHAMP показало, что у 55% контроллеров после лечения первоначальные всплески вирусной нагрузки не превышали 1000 копий/мл, и в дальнейшем они сохраняли вирусную нагрузку ниже этого порога.
Используя эти данные, Лау и Кромер предположили, что использование порога в 1000 копий маскирует 45% естественных контроллеров после лечения, что может помешать обнаружить, когда терапия усиливает иммунный контроль участников над ВИЧ. Чтобы восстановить статистическую мощность, потребуется больше участников. Как и в приведенном выше примере, при мощности 80% и цели выявления 20-процентного повышение числа контроллеров после лечения свыше базового уровня 4%, более низкий порог вирусной нагрузки потребует увеличить количество участников с 60 до 120 как в лечебных, так и контрольных группах.
Как и в случае исследований TVR, ученые также оценили максимальный риск передачи ВИЧ во время определения контрольных величин, используя те же предположения, что и описанные выше (отсутствие стратегий профилактики и экспресс-тестирования на вирусную нагрузку, незащищенный секс, недельная задержка перед возобновлением АРТ). Из-за гораздо большей продолжительности испытаний и высоких пороговых значений вирусной нагрузки (для этого они сослались на исследование контрольных величин, в котором использовали данные 50 000 человек) они оценили максимальный риск передачи ВИЧ как 13 случаев на 1000 при вагинальных половых контактах, около 25 на 1000 — для вводящего партнера при анальном сексе, 214 на 1000 — крайне высокий — для принимающего партнера при анальном сексе.
Предлагаемая гибридная схема испытаний
Основываясь на собственном моделировании и оценках максимального риска передачи, ученые предлагают использовать гибридную модель для анализа прерывания лечения. В озвученной ими схеме прерывания будут начинаться с пятинедельного исследования TVR. Хотя оно, как правило, применяется, когда терапия нацелена на резервуары ВИЧ, у людей, отвечающих на терапию, направленную на усиление иммунитета, также будет наблюдаться более медленное восстановление вируса (если лечение было эффективным).
Начало испытания для оценки потенциального лечения с помощью исследования TVR подвергнет участников гораздо более коротким перерывам в лечении, что позволит исследователям определить, имела ли эта терапия достаточную эффективность, чтобы перейти к более длительному изучению заданных значений. Если медики согласятся с необходимостью дальнейшего исследования, а пациенты с вирусной нагрузкой ниже 1000 согласятся перейти к следующей фазе, они продолжат тщательное наблюдение в течение 24 недель или до тех пор, пока вирусная нагрузка участников не превысит 1000 копий/мл, после чего они возобновят АРТ.
Ученые рекомендуют провести экспресс-тестирование на вирусную нагрузку и возобновить АРТ в тот же день, чтобы свести к минимуму риск передачи инфекции. По их оценке, ограничение контрольной точки теми, кто уже демонстрирует контроль за вирусом, до вирусной нагрузки ниже 1000, снижение порога вирусной нагрузки для возобновления АРТ до 1000, ограничение продолжительности до 24 недель, а также включение тестирования по месту оказания медицинской помощи и возобновление АРТ в тот же день снижают максимальный риск передачи до 0,2 на 1000 при вагинальном сексе, до 0,35 на 1000 — для вводящего партнера при анальном сексе и до 3,1 на 1000 — для принимающего партнера при анальном сексе. И это значительное улучшение показателей по сравнению с оценкой, полученной в ходе традиционных исследований контрольных величин.
Если первоначальное исследование TVR показывает, что лечение не требует дальнейшего изучения (например, если не обнаружено позитивного эффекта), то ученые смогут избежать затрат на проведение длительного исследования контрольных величин.
Выводы
Ученые пришли к выводу, что в испытаниях лекарств недостаточно участников для обеспечения знаковой статистической мощности при умеренных результатах лечения. Поскольку чаще всего при испытаниях терапии также не используются контрольные группы, количественная оценка пользы лечения чрезвычайно сложна. Специалисты рекомендуют сотрудничать всем заинтересованным структурам для создания ретроспективной контрольной базы данных, которая позволила бы разработать схему испытаний, не полностью полагающуюся на контрольные группы плацебо. Тем не менее они отмечают, что задействование ретроспективных контрольных данных означает включение людей, которые с большей вероятностью начали АРТ во время хронической ВИЧ-инфекции, и тех, кто использует более старые схемы АРТ, которые могут действовать как искажающие факторы.
Тем не менее сокращение числа участников, получающих плацебо, снижение пороговых значений вирусной нагрузки, продолжительности испытаний и рисков передачи ВИЧ могут побудить большее число людей с ВИЧ участвовать в исследованиях с прерыванием лечения.
ВИЧ-инфекция — это медленно прогрессирующее инфекционное заболевание, вызываемое вирусом иммунодефицита человека (ВИЧ).
Размножаясь, ВИЧ поражает клетки иммунной системы — так называемые CD4+ Т-лимфоциты. В результате чего количество их постепенно уменьшается.
Что это за клетки?
Они отвечают за уничтожение тех вирусов, которые попали в организм человека и смогли преодолеть гуморальный барьер.
Т-лимфоциты действуют не против возбудителей, циркулирующих в крови, а распознают измененную, то есть зараженную вирусом, клетку и разрушают ее. Клетки CD4 регулируют весь этот процесс, выполняя функцию иммунной памяти.
Именно поэтому против ВИЧ иммунная система не может сработать так, как это было бы с любым другим вирусом.
Стоит сразу отметить, что ВИЧ — вирус нестойкий, он погибает вне среды человеческого организма при высыхании содержащих его жидкостей и практически моментально погибает при температуре выше 56ºС.
ВИЧ содержится во всех биологических жидкостях человеческого организма. Однако достаточное для инфицирования количество ВИЧ может содержаться только в крови, сперме, предэякуляте, вагинальном секрете и грудном молоке.
Слюна, пот и моча не содержат достаточного для инфицирования количества вируса.
Пути инфицирования ВИЧ
Вероятность инфицирования при незащищенном контакте такого типа наиболее велика.
Некоторые другие практики, например оральный секс, могут подразумевать меньшую опасность инфицирования.
Несмотря на то, что в справочниках обычно для орального секса отмечается процент вероятности, отличный от нуля, за всю историю эпидемии пока достоверно не зафиксировано ни одного случая инфицирования таким образом — даже в том случае, если принимающий партнер проглатывает сперму после эякуляции.
Таким образом, получить ВИЧ может каждый независимо от пола, возраста, национальности, сексуальной ориентации, материального достатка или принадлежности к какой-либо социальной группе.
Часто люди могут знать, как необходимо поступать, чтобы избежать инфицирования, однако в силу социальных, культурных или экономических условий, в которых им приходится находиться, они могут воздерживаться от правильных действий.
Что такое СПИД?
ВИЧ-инфекция течет медленно и почти бессимптомно. В течение многих лет она может никак не тревожить человека.
СПИД — синдром приобретенного иммунодефицита — тяжелое состояние, которое вызывается у человека длительным течением ВИЧ-инфекции.
Считается, что с момента проникновения вируса в организм до достижения стадии СПИДа проходит в среднем 10 лет (от 5 до 15 лет). Но только в том случае, если пациент, получив вирус, не начал лечение.
Антиретровирусная терапия является единственным средством для лечения ВИЧ-инфекции с доказанной эффективностью.
Если антиретровирусная терапия не начата вовремя и количество CD4+ Т-лимфоцитов снизилось ниже критического уровня 200 кл/мкл, у человека появляется вероятность развития СПИДа.
Но СПИДа можно избежать!
Что для этого нужно сделать? Необходимо как можно скорее после обнаружения в организме следов вируса начать так называемую антиретровирусную терапию (сокращенно АРВТ или АРТ).
Антиретровирусная терапия — это комбинация из 3-4 препаратов, которые блокируют размножение ВИЧ на разных этапах. Вследствие ее применения вирус иммунодефицита человека перестает размножаться.
Пока АРТ неспособна элиминировать вирус, то есть полностью вылечить ВИЧ-инфекцию, однако в состоянии не просто продлить жизнь ВИЧ-инфицированного человека, но и повысить ее качество.
Пациенты, которые получают АРТ, не болеют СПИДом!
Предполагаемая продолжительность жизни человека с ВИЧ-инфекцией, получающего АРТ, не отличается от таковой в общей популяции людей. Более того, человек, принимающий препараты АРТ и достигший неопределяемого уровня вирусной нагрузки, безопасен для своего сексуального партнера, даже в том случае, если занимается с ним сексом без презерватива.
Считается, что, если у человека с ВИЧ показатель вирусной нагрузки менее 200 копий, риск передачи отсутствует. Если этот показатель выше — риск безусловно есть. В этом случае ВИЧ-отрицательному партнеру советуется начать доконтактную профилактику (PrEP, ДКП).
Почему важно регулярно проходить тестирование на ВИЧ?
Зная результат обследования, вы избавитесь от неопределенности, связанной с тревожными размышлениями о том, что у вас может быть ВИЧ-инфекция, но вы не знаете об этом.
Плюсы тестирования:
Если результат теста показал, что у вас нет ВИЧ-инфекции, но при этом вы знаете, что ваше поведение связано с риском инфицирования, вы можете узнать, как быть осторожнее, дабы избежать инфицирования в будущем.
Впрочем, о тестировании не стоит забывать даже тем, кто состоит в моногамных отношениях: вы не можете знать наверняка, верен ли ваш партнер. Более того, испытывая чувство вины, он может стыдиться рассказывать вам о тех случайных связях, которые были у него на стороне.
Большинство тестов определяют не сам ВИЧ, а антитела к нему: иммунная система начинает вырабатывать их после того, как вирус попадает в организм. У 97 % людей антитела к ВИЧ выявляют в срок от 3 до 12 недель после инфицирования. В течение этого срока проверку можно проходить как в лабораторных условиях (ИФА-диагностика), так и при помощи домашней тест-системы — по крови или слюне.
Более чувствительные тесты (ИФА четвертого поколения) выявляют антигены, которые являются частью самого вируса и появляются в достаточном для определения количестве, пока антитела еще не появились. Подобные тест-системы показывают результат на сроке в 2—6 недель после инфицирования.
ПЦР-диагностика выявляет не антитела или антигены, а генетический материал вируса. Из-за высокой стоимости и сложности этот метод используется реже других. Он способен показать точный результат в срок от 1 до 4 недель.
Более подробно о том, каким бывает тестирование, вы можете узнать, вернувшись к оглавлению данного раздела.
ВИЧ-положительными называют людей, чей тест на ВИЧ показал положительный результат. То есть вирус в организме этого человека есть.
ВИЧ-отрицательными — людей, чей тест не обнаружил следов вируса в организме.
Знайте: тот факт, что у кого-то из вас обнаружена ВИЧ-инфекция, вовсе не означает, что вы должны отказываться от секса и/или отношений.
Но это значит, что как можно скорее вам нужно начать антиретровирусную терапию. От этого зависит ваше здоровье и здоровье вашего партнера.
Не бойтесь АРВ-терапии: несмотря на то, что в прошлом многие препараты от ВИЧ были весьма токсичны, сегодня они ничуть не опаснее других лекарств. Свои побочные эффекты есть и у них, но всех их можно избежать, если правильно подобрать схему лечения.
Запомните: схема подбирается врачом! Именно он обладает всеми необходимыми знаниями, чтобы определить, какие именно таблетки и по какому графику вам необходимо принимать. Не занимайтесь самолечением!
Если вы столкнулись с побочными эффектами, сообщите об этом вашему лечащему врачу в центре СПИД и попросите его подобрать для вас альтернативную схему терапии.
Как оценивают эффективность АРВТ и от чего она зависит?
Для оценки эффективности и неэффективности лечения используются разные критерии: вирусологические, иммунологические и клинические.
Вирусологическая эффективность — это уменьшение вирусной нагрузки до неопределяемой (менее 20 копий/мкл). Чем быстрее и значительнее упадет вирусная нагрузка, тем дольше терапия будет эффективной. Если через 6 месяцев после начала терапии вирусная нагрузка сохраняется выше порога определения — это вирусологическая неэффективность.
Причинами вирусологической неэффективности лечения могут быть:
низкая приверженность пациента лечению, то есть пропуск приема препаратов; несоблюдение других условий приема лекарств, например, таких как сочетание с пищей, межлекарственные взаимодействия; резистентность вируса к проводимой АРТ.
Иммунологическая эффективность — это увеличение количества CD4+ T- клеток. В разных исследованиях критерием иммунологического ответа служит прирост количества CD4+ T-клеток на 50 в микролитре, на 100 в мкл или на 200 в мкл. Или превышение CD4+ T-клетками порога в 200 кл/мкл или 500 кл/мкл. Под иммунологической неэффективностью подразумевается отсутствие прироста CD4+ T-клеток.
Стадия СПИДа наступает только в том случае, если количество CD4+ ниже 200 кл/мкл.
Клиническая эффективность
Клинический успех лечения оценивается как отсутствие СПИД- индикаторных заболеваний. Уменьшение выраженности общих симптомов.
Клинический успех лечения напрямую связан с вирусологическим и иммунологическим ответом на лечение.
Как рассказать партнеру, с которым я встречаюсь, что у меня ВИЧ?
Многие люди с ВИЧ-инфекцией сталкивались с отказом в отношениях, когда рассказывали о ВИЧ партнерам, с которыми встречались, из-за чего им было тяжело в дальнейшем принимать решение о раскрытии своего статуса.
Рассказать о себе партнеру будет проще, если вы предварительно обсудите это с другими ВИЧ-позитивными людьми или с профессионалом, работающим в этой сфере.
Однако помните, что ваш диагноз касается в первую очередь вас — это ваш личный мир, очень глубокая и интимная часть вас и вашей жизни.
От того, как и при каких обстоятельствах вы это преподнесете, будет зависеть реакция вашего партнера. Лучше всего рассказывать о том, что у вас ВИЧ-инфекция, тогда, когда вы сами приняли свой диагноз, а значит, перестал испытывать чувства вины и стыда, связанные с диагнозом.
Потому что состояние, находясь в котором, мы делимся чем-то сокровенным, отражается на собеседнике.
Теперь меня бросят, и я останусь один?
Нет. Не обязательно. Конечно, такая новость может огорчить и даже напугать вашего любимого человека, но это вовсе не означает, что он обязательно должен вас из-за этого бросить.
В мире много пар, в которых один из партнеров имеет положительный ВИЧ-статус, и эти пары остаются вместе, несмотря на ВИЧ.
Общение и честность являются ключевыми факторами укрепления и успешного развития отношений. Вы оба должны четко говорить о том, как вы чувствуете себя и что вы хотите друг от друга. Вам обоим нужно уметь внимательно слушать и слышать друг друга.
Вместо послесловия
В течение всех последних лет количество людей с ВИЧ в России растет, количество инфицированных от общего их числа равняется примерно одному проценту, то есть с ВИЧ живет практически каждый сотый россиянин. Это очень много.
Значительная часть из них — совсем не представители уязвимых групп, а гетеросексуальные мужчины и женщины, никогда не употреблявшие наркотиков.
Один из ста — совсем немного? Но это закон статистики: тем самым сотым может стать каждый. Вне зависимости от образа жизни, вероисповедания и социального статуса.
Более того, среди российских геев или мужчин, практикующих секс с мужчинами, носителем вируса по разным оценкам является каждый десятый или даже каждый пятый.
Это очень много. Именно поэтому Фонд помощи людям, живущим с ВИЧ, как и многие другие ВИЧ-сервисные организации, регулярно проводит анонимное бесплатное тестирование на ВИЧ.
В любое время пройти абсолютно анонимный тест (для этого не нужны ни прописка, ни паспорт) можно в открытом пространстве фонда СПИД.ЦЕНТР по адресу:
Москва, ул. Нижняя Сыромятническая, д. 11, с.1, офис 313.
Читайте также:

