Описторхоз клонорхоз фасциолез дикроцелиоз
Обновлено: 18.04.2024

Паразитарные болезни (от греч. parasitos — нахлебник; синоним инвазионные болезни) — группа заболеваний, вызываемых животными паразитами (паразитическими червями, простейшими, членистоногими) и характеризующихся цикличностью, часто длительностью течения, развитием постинвазионного, обычно непродолжительного, иммунитета. Среди паразитарных болезней выделяют гельминтозы, протозоозы, энтомозы и акариазы.
Гельминтозы вызываются паразитическими червями — гельминтами. Всего существует более 200 видов гельминтов. Среди гельминтозов наиболее распространены аскаридоз, шистосоматоз, энтеробиоз. Протозоозы вызываются простейшими. Известны более 20 видов простейших, вызывающих болезни у человека. Наиболее распространены амебиаз, лейшманиозы, лямблиоз, малярия, токсоплазмоз, трипаносомозы.
Энтомозы и акариазы вызываются паразитическими членистоногими, насекомыми и клещами. К энтомозам относятся миазы (заболевания, обусловленные паразитированием личинок некоторых видов мух) и дерматозоонозы (дерматиты от укусов насекомых), к акариазам — чесотка. Паразитами называют организмы, которые живут за счет других организмов, используя их как среду обитания и источник питательных веществ. В свою очередь, организм, который служит местом обитания и источником питания для паразита, является его хозяином.
Описторхоз
Описторхоз — гельминтоз, вызываемый паразитическими червями из класса сосальщиков, характеризующийся преимущественным поражением гепатобилиарной системы и поджелудочной железы. Возбудитель — двуустка кошачья. Развитие паразита происходит в пресных водоемах. Промежуточным его хозяином является моллюск; через два и более месяцев паразиты покидают моллюск и внедряются в тело дополнительного хозяина — в мышцы карповых рыб (язь, линь, плотва, лещ, сазан, чебак, красноперка). Окончательными хозяевами являются человек, кошка, собака, лисица, ондатра, норка. Описторхисы паразитируют в желчных протоках, желчном пузыре, реже — в протоках поджелудочной железы окончательного хозяина. Заражение человека происходит при употреблении в пищу сырой (строганина) или недостаточно проваренной (прожаренной, просоленной) пораженной рыбы. В России известны два больших очага описторхоза — в Западной Сибири (в бассейнах рек Оби и Иртыша), в Пермской области (бассейн реки Камы). Групповые и единичные случаи заражения людей наблюдаются в районе побережья Черного и Каспийского морей, Ладожского озера, бассейнах Волги, Дона, Донца, Северной Двины, Немана. Болезнь регистрируется также в Европе — Австрии, Венгрии, Голландии, Франции. Источником инвазии являются зараженные описторхисами люди и животные.
Эхинококкоз
Эхинококкоз распространен практически повсеместно. В России данный гельминтоз чаще регистрируется в Новосибирской, Томской и Омской областях, Якутии (республика Саха) и Бурятии. Человек является промежуточным хозяином эхинококка, окончательным служит домашняя собака, имеющая наибольшее эпидемиологическое значение, а также волк, шакал, лиса, гиена, койот и некоторые другие хищные животные.
Заражение человека происходит при тесном контакте с инвазированными собаками, а также при употреблении в пищу загрязненных яйцами эхинококка зелени и овощей, с водой, при снятии и разделке шкур зараженных хищников.
Клиника инвазии у человека зависит от количества, размеров и локализации эхинококковых пузырей. Чаще всего встречается эхинококкоз печени (60—80 %). В начальных стадиях клинические проявления скудные: тяжесть и умеренные непостоянные боли в правом подреберье, возможна крапивница как проявление аллергизации, эозинофилия. Далее определяются медленно прогрессирующее увеличение печени, асцит, отеки, желтуха. В случаях эхинококкоза легких появляются упорный сухой кашель, кровохарканье, боли в грудной клетке. Физикальные данные при исследовании легких неспецифичны. Эхинококкоз других органов встречается редко, симптоматика в этих случаях сходна с проявлениями новообразования. При клиническом обследовании пациента следует иметь в виду, что во время грубой пальпации стенки развитого паразитарного пузыря могут разорваться, что может привести к непредсказуемым последствиям. Пунктирование эхинококкового пузыря возможно только после лапаротомии. Диагностика эхинококкоза сложна и базируется на учете комплекса данных: изучения анамнеза, в том числе эпидемиологического, клиники, рентгенологических исследований, сканирования печени и селезенки, ультразвуковой и иммунодиагностики (реакция энзим-меченых антител — РЭМА).
Трихинеллез
Трихинеллез встречается повсеместно, в России чаще регистрируется в Магаданской области, Хабаровском, Красноярском и Краснодарском краях.
Человек заражается при употреблении в пищу пораженной личинками трихинеллы свинины, реже — мяса бурых медведей, кабана и других животных. Личинки трихинелл с током крови заносятся в различные органы и ткани, прежде всего в мышцы.
Инкубационный период составляет 5—45 дней.
Заболевание протекает остро, повышается температура тела, появляются тошнота, понос, характерны выраженный отек век, одутловатость лица. Отмечаются отечность и гиперемия конъюнктивы. Позже появляются боли в мышцах, нередко интенсивные. Чаще поражаются мышцы шеи, поясницы, икроножные. На коже появляется разнообразная сыпь. Осложнения инвазии разнообразны: тромбозы, пневмонии, нефриты, миокардиты, менингоэнцефалиты.
Диагностика трихинеллеза комплексная, включает эпидемиологический анамнез, анализ клинических проявлений, иммунологические тесты (РНГА — реакция непрямой агглютинации, РСК — реакция связывания комплемента, кожная аллергическая проба), исследование мышц животного и кусочка мышц больного (трапециевидной, дельтовидной или икроножной) с последующей микроскопией.
Аскаридоз
Аскаридоз является самым распространенным из всех гельминтозов человека. Единственным источником инвазии служит человек. Заражение происходит при проглатывании с водой или пищей яиц гельминта. Далее личинки аскарид мигрируют с током крови через воротную систему печени и нижнюю полую вену, правое сердце, заносятся в легкие, где находятся от нескольких дней до полутора недель. Из легких личинки продвигаются к трахее и глотке и с заглатываемой слюной и пищей повторно попадают в кишечник, где и превращаются в половозрелых гельминтов. Яйца аскарид устойчивы во внешней среде и могут сохраняться в почве на глубине 20 см в средней полосе России до 7 лет, в южных районах — более 10 лет.
Паразитируют аскариды в кишечнике, однако могут проникать из него в печень и поджелудочную железу, а иногда способны проникать в дыхательные пути или придаточные пазухи носа. Клинические проявления гельминтоза зависят от локализации и численности паразитов. В миграционной фазе инвазии клинические проявления могут отсутствовать, в других случаях (при массивном заражении) возможно развитие бронхитов, реже пневмоний, появление на коже полиморфной сыпи, повышение температуры. В кишечной фазе аскаридоза характерны симптомы со стороны пищеварительного тракта и нервные расстройства в различных сочетаниях.
Осложнения аскаридоза могут быть грозными, вплоть до кишечной непроходимости и перитонита. Диагноз устанавливают на основании обнаружения в кале яиц аскарид или самих паразитов.
Токсокароз - гельминтное заболевание, вызываемое несвойственным человеку паразитом – токсокарой, очень схожей с аскаридой человеческой – нематодой семейства Anisakidae рода Тохосаrа. Диаметр ее личинки составляет 0,02 мм.
Известны два вида токсокар:
- Toxocara canis – гельминт, поражающий представителей семейства псовых (собак, волков, лисиц, песцов);
- Тохосаrа mystax (cati) – гельминт семейства кошачьих.
Источником инвазии для людей являются собаки, выделяющие яйца токсокар с фекалиями, а также загрязненная яйцами шерсть животного. В США 20% взрослых собак и 95% щенков заражено этими гельминтами, а яйца токсокар обнаруживаются в 10-30% проб почв парков и дворов.
Инвазированные люди не являются источником заражения, так как человек для токсокары – несвойственный хозяин, и возбудители в организме человека не достигают половозрелого состояния.
Среди животных механизм передачи возбудителя бывает:
- прямой (заражение яйцами из окружающей среды);
- внутриутробный (заражение плода личинками через плаценту);
- трансмаммарный (передача личинок с молоком).
Для людей основными предпосылками передачи возбудителя токсокароза является загрязненность почвы яйцами токсокар и контакт с ней. Другими факторами передачи могут быть:
- шерсть животных;
- загрязненные продукты питания;
- зараженная вода;
- немытые руки.
Заражение человека происходит при попадании инвазионных яиц токсокар в кишечник. В проксимальном отделе тонкого кишечника из яиц выходят личинки, которые через слизистую оболочку проникают в кровоток, затем заносятся в печень и правую половину сердца.
Попав в легочную артерию, личинки продолжают миграцию и переходят из капилляров в легочную вену, достигают левой половины сердца и затем разносятся кровью по разным органам и тканям. Мигрируя, они достигают места, где диаметр сосуда не пропускает их, и здесь личинки покидают кровяное русло, оседая в печени, легких, сердце, почках, поджелудочной железе, головном мозге, глазах и других органах и тканях.
Токсокароз характеризуется тяжелым, длительным и рецидивирующим течением (от нескольких месяцев до нескольких лет), что связано с периодическим возобновлением миграции личинок токсокар. Клинические проявления зависят от интенсивности заражения, распространения личинок в тех или иных органах, степени иммунного ответа хозяина.
- лейкокории;
- абсцесса в стекловидном теле;
- неврита зрительного нерва;
- кератита.
Практически всегда токсокарозом поражается только один глаз.
Последствия паразитирования в организме:
Мигрируя в организме человека, личинки травмируют ткани, оставляя геморрагии, некрозы, воспалительные изменения. Паразит гибнет, успев нанести человеку вред. Поражение зрительного нерва личинкой токсокары может привести к односторонней слепоте. При висцеральном токсокарозе известны случаи развития тяжелых пневмоний, которые протекали с осложнениями и заканчивались летальными исходами. Описаны случаи токсокароза, связанные с миграцией личинок в миокард и важные в функциональном отношении участки центральной нервной системы. При токсокарозе часто образуются многочисленные гранулемы в любом органе и ткани (в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге), в центре которой появляется зона некроза, разрушающая данный орган.
Обнаружить мигрирующие личинки токсокары трудно, а идентифицировать их в гистологических срезах удается редко. Поэтому главными методами в диагностике токсокароза являются иммунологические, ведь антитела к токсокаре могут определяться и при личиночной стадии их паразитирования.
Диагноз устанавливают также на основе клинических проявлений заболевания, титрами специфических антитоксокарозных антител. Указание на содержание в семье собаки или на тесный контакт с собаками свидетельствует об относительно высоком риске заражения токсокарозом.
Наличие аллергии на шерсть животных также часто встречается при токсокарной инвазии.
Профиль включает в себя выявление антител в крови к ряду паразитов и яиц кишечных паразитов в кале:
- токсокары (антитела класса IgG)
- трихинеллы (антитела класса IgG)
- описторхисы (антитела IgG, специфические ЦИК, содержащие антигены описторхисов)
- эхинококки (антитела класса IgG)
- аскариды (антитела класса IgG)
- лямблии (суммарные антитела)
- соскоб на энтеробиоз
- определение яиц кишечных паразитов в кале (гименолепидоз, описторхоз, клонорхоз, фасциолез, дикроцелиоз, метагонимоз, нанофиетоз, дифиллоботриоз, аскаридоз, трихоцефалез, анкилостомидоз, стронгилоидоз, трихостронгилез, некатороз, шистосомоз, лямблиоз)
Стоимость профиля: 3706 руб.
Срок исполнения: 1-3 дня
Забор крови для проведения исследования оплачивается дополнительно. Стоимость взятия крови - 100 рублей.
Фасциолез – это паразитарная инвазия, вызываемая печеночной или гигантской двуусткой и характеризующаяся преимущественным поражением гепатобилиарной системы. Течение фасциолеза сопровождается недомоганием, лихорадкой, крапивницей, тошнотой, болями в правом подреберье, увеличением размеров печени, желтухой. В диагностике фасциолеза информативны серологические методы (ИФА, РИФ, РИГА), исследование дуоденального содержимого и фекалий на яйца гельминтов, УЗИ печени и желчевыводящих путей. В комплексную терапию фасциолеза включают диету, прием антигельминтных средств (триклабендазол, празиквантел), желчегонных, антигистаминных препаратов.
МКБ-10
Общие сведения
Фасциолез - внекишечный гельминтоз, обусловленный паразитированием в паренхиме печени и желчных путях печеночной или гигантской фасциолы (сосальщика). Наряду с описторхозом, клонорхозом, парагонимозом, шистосомозами фасциолез относится к наиболее распространенным трематодозам человека. Фасциолез, вызываемый печеночным сосальщиком, распространен в Австралии, странах Европы и Южной Америки. Фасциолез, связанный с гигантским сосальщиком, встречается в Африке, Восточной Азии, районах Средней Азии и Закавказья. Описаны, как спорадические, так и массовые вспышки заболевания, охватывавшие сотни человек. Согласно имеющимся данным, фасциолезом поражено от 2,5 до 17 млн. населения планеты.

Причины фасциолеза
Характеристика возбудителя
Механизм передачи
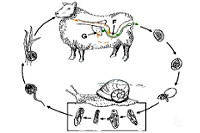
Окончательными хозяевами сосальщиков служат травоядные сельскохозяйственные животные, реже – человек. Паразитируя в желчевыводящей системе, гельминты откладывают яйца, которые с испражнениями попадают в окружающую среду и свое дальнейшее развитие проходят в пресной воде. Там вышедшие из яиц личиночные стадии (мирацидии) внедряются в тело брюхоногих моллюсков, являющихся промежуточными хозяевами возбудителя фасциолеза.
Во внутренних органах моллюсков мирацидии превращаются сначала в спороцисты, а затем в хвостатые церкарии. Через 1-2 месяца церкарии снова выходят в воду, инцистируются, превращаясь в адолескарий, и прикрепляются к поверхности водных растений или водной пленке. В этой стадии личинки становятся инвазионными, т. е способными вызывать фасциолез у животных и человека.
Заражение животных фасциолезом происходит при поедании травы на выпасе, загрязненной личинками двуустки; инфицирование человека возможно при употреблении в пищу дикорастущих или огородных растений, полив которых осуществлялся водой из пресных водоемов; питье некипяченой воды; во время купания и т. д. В желудочно-кишечном тракте личинки фасциолы высвобождаются из оболочек, через стенку кишечника выходят в брюшную полость, где через капсулу внедряются в паренхиму печени и таким образом попадают в желчные протоки. Возможен гематогенный путь миграции – через кишечные и воротную вены в печеночные протоки.
Через 3-4 месяца паразитирования в организме окончательного хозяина фасциолы достигают половозрелой стадии и начинают откладывать яйца. В гепатобилиарной системе человека возбудители фасциолеза способны паразитировать 5-10 и более лет.
Патогенез
Развивающиеся в миграционную фазу инвазии токсико-аллергические реакции связаны с сенсибилизацией организма антигенами личинок, а также механическим травмированием тканей на пути их продвижения. В хронической стадии фасциолеза патологические эффекты обусловлены паразитированием гельминтов в желчных протоках. Половозрелые гельминты вызывают повреждение печеночной паренхимы с развитием микроабсцессов и фиброзных изменений печени.
Скапливаясь в желчных ходах, фасциолы могут способствовать их обструкции и нарушению оттока желчи, развитию пролиферативного (а в случае присоединения вторичной инфекции – гнойного) холангита. Общетоксическое воздействие на организм при фасциолезе обусловлено поступлением в кровь продуктов жизнедеятельности гельминтов и распада печеночной ткани. В исходе длительного течения фасциолеза может развиваться цирроз печени и портальная гипертензия.
Симптомы фасциолеза
В развитии фасциолеза выделяют инкубационный период, острую (миграционную) и хроническую (связанную с паразитированием взрослых гельминтов) стадии. В зависимости от инвазирующей дозы, инкубационный период может длиться от 1 до 8 недель.
В миграционную фазу главным образом выражены общетоксические и аллергические симптомы. Больные фасциолезом жалуются на подъемы температуры, слабость, недомогание, головную боль. Лихорадка может быть субфебрильной или высокой (до 39-40°С), носить ремитирующий или волнообразный характер. На этом фоне появляется крапивница и кожный зуд, отек Квинке, высокая (до 80-85%) эозинофилия в крови. Развиваются диспепсические расстройства: тошнота, рвота, боли в эпигастрии и правом подреберье; происходит увеличение размеров печени, сопровождающееся желтухой. В раннем периоде часто развивается аллергический миокардит, характеризующийся загрудинными болями, артериальной гипертензией, тахикардией. Через несколько недель клинические проявления острого фасциолеза значительно или полностью стихают.
Спустя 3-6 месяцев заболевание вступает в хроническую стадию, симптомы которой обусловлены непосредственным поражением печени и желчных путей. Течение хронического фасциолеза сопровождается гепатомегалией, приступообразными болями в правом боку; в периоды обострения – желтухой. Длительная инвазия приводит к развитию диспепсического синдрома, анемии, гепатита, цирроза печени.
Вторичное инфицирование чревато возникновением гнойного холецистита и холангита, абсцессов печени, стриктуры желчных путей. В литературе описаны казуистические случаи фасциолеза с нетипичной локализацией сосальщиков в головном мозге, легких, молочных железах, евстахиевых трубах, гортани, подкожных абсцессах.
Диагностика
Чаще всего фасциолез диагностируется уже в хронической стадии, когда с беспокоящими жалобами больные обращаются к терапевту или гастроэнтерологу. Предположительный диагноз основывается на совокупности эпидемиологических данных и клинических данных. В пользу фасциолеза свидетельствует наличие ранее зафиксированных случаев инвазии на данной территории, групповая заболеваемость, употребление в пищу салатных растений, питье воды из открытых источников или использование ее для мытья посуды, фруктов, овощей и пр.
- Методы выявления возбудителя. В раннем периоде фасциолеза диагноз подтверждается серологическими методами (РИФ, ИФА, РИГА, РСК). В хронической стадии информативно обнаружение яиц фасциол в фекалиях или дуоденальном содержимом. Паразиты могут быть обнаружены с помощью ультразвукового исследования печени и желчного пузыря, КТ печени.
- Биохимия крови. В биохимических пробах печени отмечается повышение активности трансаминаз и щелочной фосфатазы, гипопротеинемия, гипоальбуминемия.
Фасциолез необходимо отличать от описторхоза, клонорхоза, вирусных гепатитов, панкреатита, холангита, холецистита другой этиологии.
Лечение фасциолеза
Лечение фасциолеза проводится стационарно. В острую фазу назначается щадящая диета, десенсибилизирующие препараты; при развитии миокардита и гепатита показаны глюкокортикостероиды. К противопаразитарной терапии переходят только после стихания острых явлений. В качестве этиотропных препаратов при фасциолезе используются триклабендазол, гексахлорпараксилол, празиквантел. С целью изгнания погибших фасциол из желчных протоков назначаются желчегонные средства.
Контрольное паразитологическое обследование (анализ кала на яйца гельминтов, дуоденальное зондирование с исследованием порций желчи) проводится спустя 3 и 6 месяцев. В случае развития гнойных осложнений требуется назначение антибиотиков и проведение хирургического вмешательства (дренирования абсцесса печени, дренирования желчных протоков и др.).
Прогноз и профилактика
Ранняя диагностика фасциолеза позволяет провести своевременную терапию и добиться выздоровления. При высокоинтенсивной инвазии или вторичной бактериальной инфекции прогноз может быть серьезным, вплоть до летального исхода. Индивидуальная профилактика фасциолеза заключается в недопущении употребления сырой воды из водоемов, плохо промытой огородной зелени. Меры общественного контроля включают очистку водоемов, их защиту от фекального загрязнения, ликвидацию промежуточных хозяев фасциолеза – моллюсков, ветеринарное обследование и дегельминтизацию скота, санитарно-просветительскую работу.
Описторхоз – гельминтное заболевание, вызываемое плоскими паразитическими червями класса сосальщиков и протекающее с поражением гепатопанкреатобилиарной системы. Течение описторхоза характеризуется лихорадкой, болями в животе, нарушением аппетита, кожными высыпаниями, желтухой, гепатоспленомегалией, диспепсией, астматическим бронхитом, астеновегетативным синдромом. Диагностика описторхоза основывается на обнаружении яиц описторхисов в дуоденальном содержимом и в кале, результатах серологических реакций, данных биохимического анализа крови, инструментальных исследований (УЗИ, холецистохолангиографии, КТ). Для терапии описторхоза используются противогельминтные (празиквантел, азинокс), желчегонные и ферментные препараты.
МКБ-10
Общие сведения
Описторхоз – внекишечный гельминтоз из группы трематодозов, возбудители которого паразитируют в желчных протоках печени и поджелудочной железе, вызывая полиморфные клинические проявления. Наиболее напряженный очаг описторхоза расположен на территории Западной Сибири, в низовьях р. Иртыш и среднем течении Оби, где инвазированность местного населения приближается к 80-90%. Кроме этого, эндемичными по описторхозу районами служат бассейны рек Волга, Кама, Днепр, Дон, Енисей и др., главным образом, связанные с рыбным промыслом и рыбопереработкой. Наибольшая заболеваемость регистрируется среди лиц в возрасте от 15 до 50 лет, преимущественно мужчин. Опасность описторхоза заключается в том, что при длительном течении он повышает риск развития рака печени и рака поджелудочной железы.

Причины описторхоза
Описторхоз вызывают два вида гельминтов-сосальщиков: Opisthorchis felineus и Opisthorchis viverrini. На территории России распространен возбудитель О. felineus – сибирская или кошачья двуустка. Это плоский гельминт длиной 4–20 мм, шириной 1–4 мм, имеющий ланцетовидное тело, снабженное ротовой и брюшной присосками. Описторхоз, вызываемый O. viverrini встречается в странах Юго-Восточной Азии.
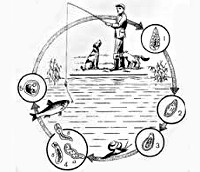
Развитие описторхисов происходит с трехкратной сменой хозяев: первым промежуточным хозяином выступают моллюски, вторым промежуточным - пресноводные рыбы семейства карповых (лещ, сазан, линь, елец, язь, плотва и др.) и окончательным - млекопитающие (кошка, собака, лисица, выдра, песец, соболь, человек), питающиеся рыбой. Окончательные хозяева выделяют яйца с личинками во внешнюю среду вместе с фекалиями. Попав в водоем, яйца заглатываются пресноводными моллюсками рода Codiella, в организме которых претерпевают изменения: сначала из яйца выходит мирацидий, который последовательно превращается в спороцисту, редию и церкария. Хвостатая личинка (церкарий) выходит из тела моллюска и в водоеме прикрепляется к телу карповых рыб, внедряется в соединительную и мышечную ткань, где инцистируется, превращаясь в метацеркарий. Находясь в теле рыб, через 6 недель личинки становятся инвазионными, т. е. приобретают способность вызывать описторхоз у окончательных хозяев.
Заражение человека и животных происходит при употреблении инвазированной, плохо обработанной (сырой, малосольной) рыбы. В ЖКТ окончательного хозяина под действием дуоденального сока капсула и оболочки личинок растворяются, в результате чего метацеркарии мигрируют в общий желчный проток, внутрипеченочные желчные протоки, а также в протоки поджелудочной железы. В гепатопанкреатобилиарной системе через 3–4 недели метацеркарий превращается в зрелого описторхиса, способного продуцировать яйца. Полный цикл развития гельминта от стадии яйца до половозрелой особи длится 4–4,5 месяца. Инвазированность человека описторхисами может варьировать от нескольких единиц до десятков тысяч. В организме окончательного хозяина кошачья двуустка может паразитировать 20-25 лет.
Патогенез описторхоза
Характер и выраженность патологических процессов, характеризующих течение описторхоза, зависят от массивности и длительности инвазии, состояния иммунной системы. В зависимости от этих факторов течение описторхоза может быть стертым или манифестным; легким, среднетяжелым и тяжелым. В патогенезе описторхоза выделяют раннюю (острую) и позднюю (хроническую) стадии.
В острой стадии гельминтоза доминируют токсико-аллергические реакции, развивающиеся в ответ на действие метаболитов паразитов на организм хозяина. Они сопровождаются повышением проницаемости сосудистой стенки, периваскулярным отеком и эозинофильной инфильтрацией стромы различных органов, образованием некротических очагов в паренхиме печени. Повреждение сосальщиками эпителия желчных протоков вызывает гиперплазию бокаловидных клеток, кистозное расширение мелких желчных ходов. При хроническом описторхозе в стенках желчных протоков развивается вялотекущее воспаление, выявляется разрастание соединительной ткани, нередко возникает закупорка гельминтами мелких желчных протоков. Данные процессы приводят к развитию вторичного бактериального холангита, дискинезии желчевыводящих путей, образованию желчных камней, в тяжелых случаях – к циррозу печени и портальной гипертензии. Поражения поджелудочной железы при описторхозе определяются, главным образом, отеком железы и нарушением оттока панкреатического секрета, что сопровождается кистевидным расширением канальцев, пролиферативным каналикулитом и фиброзом органа.
Симптомы описторхоза
Острая фаза описторхоза манифестирует через 2-4 недели после заражения. Легкая форма гельминтоза начинается с внезапного скачка температуры тела до 38°С и последующего сохранения субфебрилитета в течение в течение 1-2-х недель. В это время пациенты испытывают слабость, боли в животе, отмечают неустойчивый характер стула. В периферической крови при легком течении описторхоза выявляется умеренный лейкоцитоз и эозинофилия до 15 - 20%.
Среднетяжелая форма описторхоза протекает с лихорадкой (до 39°С и выше), которая длится около 3-х недель. Характерны миалгии и артралгии, уртикарные кожные высыпания, катар верхних дыхательных путей, увеличение печени и селезенки, рвота, диарея, астматический бронхит. Нарастают лейкоцитоз, эозинофилия до 25 - 60%, повышается СОЭ.
Тяжелые формы острого описторхоза развиваются у 10 - 20% больных и могут протекать по тифоподобному, гастроэнтероколитическому, гепатохолангитическому и респираторному вариантам. Симптоматика тифоподобного варианта описторхоза включает высокую лихорадку, озноб, лимфаденит, полиморфную кожную сыпь, диспепсию. В клинике преобладают явления интоксикации и аллергизации; возможно токсико-аллергическое поражение ЦНС или миокарда. При гастроэнтероколитической форме описторхоза развивается клиническая и патоморфологическая картина гастрита (катарального, эрозивного), гастродуоденита, язвы желудка и двенадцатиперстной кишки, энтероколита. Данные состояния сопровождаются снижением аппетита, тошнотой, болями в эпигастрии и правом подреберье, диареей. В течении гепатохолангитического варианта острого описторхоза превалируют желтуха, гепатоспленомегалия, абдоминальный синдром по типу печеночной колики или опоясывающего характера. Патологические синдромы могут включать в себя гепатит, холангит, холецистит, панкреатит. При вовлечении органов дыхания (респираторном варианте описторхоза) развивается трахеит, астмоидный бронхит, пневмония, плеврит, лихорадка.
Хронический описторхоз чаще всего протекает по типу дискинезии желчных путей, холангиогепатита, холангиохолецистита, желчнокаменной болезни, хронического панкреатита, гастрита, дуоденита. Имеют место признаки астеновегетативного синдрома: слабость, утомляемость, раздражительность, эмоциональная неустойчивость, головная боль, нарушение сна, повышенное потоотделение. Могут развиваться дистрофические изменения миокарда, проявляющиеся болями за грудиной, тахикардией, артериальной гипотонией. Длительное течение хронического описторхоза может осложниться циррозом печени, гнойным холангитом, флегмоной желчного пузыря, желчным перитонитом, первичным раком печени и поджелудочной железы.
Диагностика описторхоза
При проведении диагностики описторхоза учитываются эпидемиологические сведения, указывающие на пребывание пациента в эндемичных очагах, употребление в пищу свежезамороженной, малосоленой, недостаточно термически обработанной рыбы. Характерно изменение биохимических проб печени и ферментов поджелудочной железы - повышение билирубина, трансаминаз, амилазы и липазы. Данные инструментальных исследований (ФГДС, УЗИ гепатодуоденальной зоны и поджелудочной железы, холецистография, КТ, МРТ печени и желчевыводящих путей) обнаруживают признаки гастродуоденита, дискинезии желчевыводящих путей, холецистита, холангита, гепатита, панкреатита.
В целях паразитологического подтверждения описторхоза проводится микроскопическое исследование дуоденального содержимого и кала, в которых обнаруживаются яйца кошачьей двуустки. Для повышения вероятности обнаружения яиц гельминта перед проведением дуоденального зондирования и копроовоскопии целесообразно назначать пациенту тюбажи по Демьянову и желчегонные препараты. Выявить противоописторхозные антитела в сыворотке крови позволяет иммуноферментный анализ. Ввиду полиморфизма клинических симптомов течение острого описторхоза может напоминать вирусный гепатит, пищевую токсикоинфекцию, заболевания тифопаратифозной группы, миграционную фазу аскаридоза и анкилостомидоза.
Лечение описторхоза
Лечение описторхоза осуществляется поэтапно. На первом этапе назначается подготовительная терапия, включающая желчегонные и спазмолитические препараты, блокаторы Н1-гистаминовых рецепторов; по показаниям – короткие курсы антибиотиков. Кроме медикаментозной терапии, проводится физиотерапевтическое лечение (электрофорез сернокислой магнезии, магнитотерапия, микроволновая терапия). Целью подготовительного этапа служит нормализация желчевыделения и оттока желчи, купирование воспалительного процесса в ЖКТ и желчевыводящих путях.
В рамках основного этапа лечения описторхоза назначается противогельминтная химиотерапия. Наибольшую эффективность в уничтожении паразитов доказали празиквантел и его аналоги. После проведения дегельминтизации для эвакуации описторхисов с желчью проводится слепое зондирование, импульсная магнитотерапия, электростимуляция диафрагмального нерва. В случае выраженного токсико-аллергического синдрома требуется назначение антигистаминных препаратов, глюкокортикоидов, инфузионной терапии. Контроль эффективности противопаразитарного лечения предполагает проведение трехкратного исследования фекалий и дуоденального содержимого.
Заключительный этап курса лечения описторхоза направлен на выведение продуктов распада паразитов и восстановления биоценоза кишечника. С этой целью проводятся тюбажи с ксилитом, сорбитом, минеральной водой; назначаются желчегонные и ферментные препараты, гепатопротекторы, сорбенты, пре- и пробиотики.
Прогноз и профилактика описторхоза
При легких и среднетяжелых формах описторхоза прогноз обычно благоприятный, хотя возможны случаи повторной гельминтной инвазии. При возникновении гнойного холецистита и перитонита исход зависит от полноты и скорости оказания хирургической помощи. Прогностически неблагоприятно развитие острой печеночной недостаточности, рака печени, поджелудочной железы или холангиокарциномы.
Действия по предотвращению заражения описторхозом включают лечебно-профилактическую работу (выявление и дегельминтизацию инвазированных), эпидемиологические мероприятия (защиту водоемов от загрязнения фекалиями человека и животных, соблюдение технологии обработки и приготовления рыбы, уничтожение моллюсков), санитарно-просветительную работу (информирование населения).
Клонорхоз – это хронически протекающая гельминтная инвазия. Основные симптомы связаны с вовлечением печени и поджелудочной железы; при значительной длительности заболевания возможно появление цирротических изменений, острого панкреатита, увеличивается вероятность возникновения злокачественных новообразований гепатобилиарной системы. Характерны аллергические реакции, обусловленные наличием паразита в организме, лимфаденопатия. Диагностика патологии связана с обнаружением возбудителя в каловых массах. Лечение – противогельминтная, десенсибилизирующая, противовоспалительная и симптоматическая терапия.
МКБ-10
Общие сведения
Клонорхоз – трематодоз, то есть инфекция, вызываемая сосальщиками. Первое описание гельминта было сделано английским исследователем Макконелом в 1874 году, в дальнейшем возбудитель подробно изучался японским ученым Кобаяши. Наибольшая распространенность клонорхоза отмечается в Юго-Восточной Азии (большинство случаев зафиксировано в Китае, Корее и Японии), Приамурье, Приморском крае. На сегодняшний день ввиду трудовой миграции, экономического сотрудничества, глобализации гельминтоз становится проблемой общемировой инфектологии. Чаще инфицируются мужчины старше 35 лет, четкой сезонности не прослеживается.

Причины клонорхоза
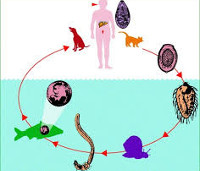
Возбудитель гельминтоза – трематода Clonorchis sinensis, двуустка китайская. Источниками инфекции служат люди и млекопитающие, путь передачи алиментарный. Взрослые черви C. sinensis обычно живут в желчных протоках окончательных хозяев, яйца выделяются с фекалиями. Пресноводные улитки могут служить первыми промежуточными хозяевами. Яйца в воде развиваются в мирацидии, а после проглатывания улитками – в спороцисты, редии и церкарии. Зрелые церкарии свободно плавают в воде, вторгаются во вторых промежуточных хозяев (пресноводных рыб) через кожу, а затем образуют метацеркарии в мускулатуре рыбы.
Основными факторами риска клонорхоза являются работа в учреждениях общественного питания, рыболовном промысле и фермерских хозяйствах, низкая организованность социально-бытовых условий, малый размер доходов населения. Пораженность рыб метацеркариями в разных регионах варьируется от 7 до 102 пресноводных видов. Одним из свойств гельминта является длительное (до 40 лет) персистирование в организме без лечения, а также связь с формированием фиброза и злокачественных перерождений гепатоцитов, ткани билиарных протоков. Частота инвалидности после перенесенной нозологии коррелирует с выраженностью симптомов.
Патогенез
Механизмы патологического воздействия клонорхов до конца не изучены. Гельминт вызывает перидуктальную фиброплазию, начиная с 7-го дня болезни, активирует перекисное окисление липидов, что сопровождается повреждением ДНК клеток гепатобилиарного аппарата. Гепатоциты подвергаются гидропической дегенерации, подавляется апоптоз аномальных клеток, что способствует опухолевому росту. Поддержание хронического воспаления приводит к фиброзным изменениям тканей, образованию карцином.
У многих больных с симптомами данного гельминтоза выявляется высокий уровень содержания IL-33/ST2 – мощного индуктора пролиферации и фиброза эпителиоцитов. Индуцируемое паразитом производство IL-13 и IL-10 позволяет избегать воздействия иммунной системы ввиду их выраженного противовоспалительного эффекта; другим эффектом указанных интерлейкинов является индукция образования коллагена в тканях. В клетках желчепузырного эпителия отмечается избыточное производство ФНО-альфа и гамма-интерферонов, поддерживающих хроническое воспаление.
Симптомы клонорхоза
Период инкубации длительный – от 2-4 недель до десятилетий. Начало болезни имеет клинические проявления только у 10-40% пациентов, в остальных случаях симптомы не обнаруживаются или мало влияют на самочувствие больных, что приводит к отсутствию этиотропного лечения. Гельминтоз может начинаться с появления слабости, повышения температуры тела от 37,5 до более 40° C, дискомфорта в животе, жидкого стула, тошноты, желтушности склер. Через 14-30 дней симптомы исчезают самостоятельно или на фоне лечения, пациент долгое время ощущает себя здоровым.
Проявления клонорхоза преимущественно связаны с поражением желчевыделительной системы, симптомы дисфункции которой включают в себя ноющие боли в правом подреберье, изжогу, периодическую тошноту и вздутие живота, метеоризм, жидкий стул после жирной и жареной пищи. Иногда пациенты замечают темный цвет мочи (наподобие крепкой заварки). При развитии цирроза больные теряют массу тела, появляются отеки, нарушения сна, снижение памяти и другие симптомы печеночной недостаточности. Чаще всего осложнения и тяжелое течение клонорхоза регистрируются у лиц 40-60 лет.
Осложнения
Наиболее распространенными считаются гнойные осложнения, связанные с присоединением симптомов бактериального воспаления стенок желчного пузыря и внутрипеченочных протоков, абсцессы. Реже возникают хронические поражения пищеварительного тракта: язвенная болезнь 12-перстной кишки, дуоденит, панкреатит, холецистит, гепатит. Печеночные циррозы встречаются в 0,06% случаев клонорхоза. Самая частая онкологическая патология, связанная с длительной инвазией, отсутствием лечения паразитоза – холангиокарцинома.
Диагностика
Подтверждение диагноза проводится инфекционистом, необходим тщательный сбор эпидемиологического анамнеза за прошедшие десятилетия. Другие специалисты – хирурги, гастроэнтерологи – привлекаются для консультации при наличии показаний. Основными диагностическими лабораторно-инструментальными признаками инфекции являются:
- Физикальные данные. Объективный осмотр при клонорхозе нередко не выявляет патологических изменений. В ряде ситуаций при пальпации живота обнаруживается значимая гепатомегалия, болезненность в области желчного пузыря, вздутие, метеоризм, реже спленомегалия, субиктеричность склер. Обязательным является изучение мочи и кала (изменение оттенка, запаха, консистенции физиологических выделений).
- Лабораторные исследования. В анализе крови определяется лейкоцитоз, эозинофилия до 80%, ускорение СОЭ. Обнаруживается повышение активности печеночных трансаминаз, ГГТП, щелочной фосфатазы, общего и прямого билирубина, триглицеридов; гипоальбуминемия. В анализе мочи выявляется изменение цвета, увеличение плотности, появление билиарных пигментов, уробилиногена, единичных лейкоцитов.
- Выявление инфекционных агентов. Обязательно проведение копроовоскопии по методу Като либо формалин-эфирного обогащения с учетом того, что яйца клонорха имеют схожесть с яйцами описторха и других трематод. Серологическая диагностика является высокочувствительным методом с высокой вероятностью перекрестных реакций с антителами к иным сосальщикам. Современная методика LAMP (изотермальная петлевая амплификация) считается менее дорогостоящей, чем ПЦР-исследование.
- Инструментальные методы. Малоинформативны при симптомах клонорхоза, но помогают в проведении дифференциального диагноза с опухолевыми процессами, холангитами иного происхождения. Рекомендуется УЗИ органов брюшной полости, предпочтительно – с контрастированием (CEUS), МРТ. В некоторых случаях выполняется тонкоигольная биопсия печеночной ткани, диагностическая лапароскопия.
Дифференциальный диагноз осуществляется с описторхозом – клинически эти патологии неотличимы, необходимо лабораторное подтверждение. При остром начале симптомы клонорхоза схожи с другими гельминтными поражениями (аскаридозом, трихинеллезом, токсокарозом), поскольку на первый план выходит аллергический компонент заболевания. Вирусные гепатиты чаще протекают с выраженной желтухой, относительно коротким инкубационным периодом, характерным анамнезом.
Лечение клонорхоза
Госпитализация пациентов с симптомами хронического клонорхоза осуществляется по клиническим и эпидемиологическим показаниям, при остром течении производится в обязательном порядке. При выраженных аллергических, холестатических симптомах, тяжелом преморбидном фоне назначается постельный режим. Диетические рекомендации связаны с нарушениями функции желчевыводящей системы, печеночной ткани. Показано частое дробное щадящее питание, исключается жирное, жареное, маринады, кофе, алкоголь, газированные напитки. Питьевой режим желательно увеличить в пользу кипяченой воды, зеленых сортов чая, несладких компотов, отвара шиповника.
Консервативная терапия
Установленный диагноз клонорхоза позволяет начать лечение после предварительного этапа, заключающегося в подготовке организма к дегельминтизации в течение 10-14 дней. Необходимо соблюдение щадящей диеты, уточнение варианта дискинезии желчевыводящих протоков (гипер-, гипокинетический) для адекватного определения путей элиминации паразитов, прием патогенетических средств. Затем пациенты получают этиотропную терапию, в дальнейшем необходимо восстановление функций гепатобилиарной системы.
Однократный курс антигельминтных препаратов продолжительностью 7-21 день эффективен в 90-94% случаев инфекции, при длительном (более 10 лет) существовании паразита в организме курсовое лечение рекомендуется повторить. Перспективные препараты, такие как трибендимидин, обладают минимальными побочными действиями по сравнению с празиквантелем. Применяются следующие виды лечения:
- Этиотропная терапия. Используются антигельминтные средства с доказанной активностью в отношении клонорхов – празиквантел и трибендимидин, назначаемые курсом перорально. Пациентов информируют о преходящих симптомах диспепсии, головных болях и головокружении, связанных с действием лекарственных форм и не требующих медикаментозной коррекции. В качестве альтернативы перечисленным средствам иногда выбирают гексахлорпараксилол.
- Патогенетическое лечение. Показаны желчегонные препараты из группы холекинетиков, спазмолитики (дротаверин), средства инфузионной дезинтоксикации – глюкозо-солевые растворы, хлосоль, сукцинат-содержащие медикаменты. Широко применяются такие десенсибилизирующие средства, как препараты кальция, при выраженном аллергозе показаны антигистаминные и глюкокортикостероиды.
- Симптоматическая терапия. Включает ферменты, энтеросорбенты, тюбажи с сульфатом магния, боржоми, сорбитом 1-2 раза в неделю. При симптомах присоединения вторичной флоры проводится бактериологическое исследование желчи и дуоденального содержимого, в схему лечения добавляют антибиотики. Для восстановления эвакуаторной функции кишечника рекомендуются пробиотики.
Экспериментальное лечение
Современные исследователи предлагают использовать для элиминации паразита средства с доказанным положительным клиническим эффектом на животных. К таковым относятся артеметер, артесунат, OZ78 и мебендазол. Последний показал хорошие терапевтические результаты при ко-инфекциях с другими гельминтозами. Изучается влияние преднизолона на активность паразитарного воспаления – в экспериментальном лечении препарат уменьшал агрегацию воспалительных клеток, но увеличивал размеры гельминта, его репродуктивную функцию.
Прогноз и профилактика
При отсутствии осложнений прогноз благоприятный, данные о летальных исходах клонорхоза отсутствуют. Согласно рекомендациям ВОЗ, в районах, где поражено более 20% населения, следует проводить ежегодное профилактическое лечение жителей. Вакцина не разработана, некоторые исследования свидетельствуют о положительном иммунологическом эффекте при введении облученных метацеркариев мышам. К неспецифическим защитным мерам относят отказ от употребления сырых и недостаточно термически обработанных пресноводных рыб и моллюсков, раннее начало лечения больных, контроль над системами водоснабжения, водоотведения.
3. Current status and perspectives of Clonorchissinensis and clonorchiasis: epidemiology, pathogenesis, omics, prevention and control/ Ze-Li Tang, Yan Huang, and Xin-Bing Yu// Infect Dis Poverty – 2016 - №5.
Читайте также:

