Определить при вскрытии рак или туберкулез
Обновлено: 22.04.2024
Московский городской научно-практический центр борьбы с туберкулезом Департамента здравоохранения, Москва, Россия, 107014
Основные принципы построения патологоанатомического диагноза и кодирования причин смерти при туберкулезе
Московский городской научно-практический центр борьбы с туберкулезом Департамента здравоохранения, Москва, Россия, 107014
Правильное установление причины наступления смерти человека является одной из важнейших задач, постоянно решаемых патологоанатомами и судебно-медицинскими экспертами при исследовании тел умерших. На практике далеко не всегда однозначно удается определить этапы и механизм танатогенеза (последовательность патологических процессов, ведущих к смерти) и правильно сформулировать судебно-медицинский или патологоанатомический диагноз (ПАД). Это в первую очередь относится к случаям сочетания различных видов насильственной смерти с различными заболеваниями, в том числе с туберкулезом. Судебно-медицинским экспертам приходится все чаще встречаться c не диагностированными при жизни различными формами туберкулеза, которые могут выступать в роли основной причины смерти, а также фонового или сопутствующего заболевания [1, 2].
Встречаемость данной патологии в повседневной экспертной практике танатологических подразделений некоторых ГСМЭУ Российской Федерации часто влечет соответствующие дефекты секционных и лабораторных исследований, сложности при формулировании диагноза и, как следствие, ошибочные экспертные выводы [3]. Таким образом, неправильно полученная статистическая информация от ГСМЭУ о причинах смерти становится основой ошибочного демографического анализа, что неблагоприятно сказывается на эффективности планирования, управления и организации как регионального здравоохранения, так и на федеральном уровне [4, 5].
Цель исследования — унификация ПАД и кодировок причин смерти от туберкулеза, а также больных туберкулезом от прочих причин.
Для корректного построения ПАД необходимо руководствоваться двумя основными принципами: подходить к формулировке диагноза с нозологических позиций согласно требованиям Международной статистической классификации болезней и проблем, связанных со здоровьем, МКБ-10 и соблюдать рубрификацию.
Общепринятые разделы ПАД:
Морфологическими проявлениями прогрессирования патологического процесса соответствуют клинические фазы инфильтрации, распада и обсеменения. Этап заживления или организации отражают клинические фазы рассасывания, уплотнения, рубцевания и обызвествления.
Наружным бактериовыделением считается прижизненное обнаружение МБТ в выделяемых больным во внешнюю среду жидкостях и экскретах: мокроте, смывах бронхов, моче, кале, раневом отделяемом, в том числе из наружных свищей, выделениях из половых путей. Как правило, эти данные отражены в медицинской документации (медицинская карта стационарного или амбулаторного больного). Данные об обнаружении МБТ в ПАД представляют с указанием их вида, номера и даты исследования.
К наружному бактериовыделению не относится посмертное выявление возбудителя при цитологическом исследовании в мазках-отпечатках внутренних органов, плевральной или асцитической жидкости (с окраской препарата по методу Циля—Нильсена или при люминесцентной микроскопии), а также гистобактериоскопическом исследовании гистологических препаратов, иммуногистохимических исследованиях — реакции с антителом МБТ или выявление в нативных тканях ДНК возбудителя методом полимеразной цепной реакции (ПЦР). Обнаружение перечисленными методами этиологического фактора процесса (МБТ или кислотоустойчивые бактерии) подтверждает факт наличия туберкулеза, но не является доказательством наружного бактериовыделения.
Кодирование нозологических форм в Свидетельствах необходимо проводить в строгом соответствии с указаниями МКБ-10. Например, фиброзно-кавернозному туберкулезу легких, казеозной пневмонии, цирротическому туберкулезу легких, очаговому туберкулезу легких, туберкулеме, инфильтративному туберкулезу легких присваивается код А15 — туберкулез органов дыхания, подтвержденный бактериологически и гистологически или код А15.2 — туберкулез легких, подтвержденный гистологически. Туберкулезная эмпиема плевральной полости (туберкулезный плеврит, подтвержденный бактериологически и гистологически) имеет код А15.6, туберкулезный спондилит (туберкулез костей и суставов) — А18.0, туберкулез почек (туберкулез мочеполовой системы) — А18.1, диссеминированный туберкулез (острый милиарный туберкулез одной уточненной локализации) — А19.0, генерализованный туберкулез (острый милиарный туберкулез множественной локализации) — А19.1. Остаточные туберкулезные изменения в зависимости от их локализации имеют код В90 [9—12].
Приводим примеры правильного формулирования ПАД и заполнения I и II разделов п. 19 Свидетельства при различных формах туберкулеза.
Осложнения: отек легких, анемия (указать данные общего анализа крови), кахексия, хроническое легочное сердце (масса сердца 340 г, дилатация полостей правых отделов сердца, гипертрофия миокарда правого желудочка 0,7 см, желудочковый индекс 0,8).
Заключение: смерть больного З., 58 лет, последовала от фиброзно-кавернозного туберкулеза легких. Непосредственная причина смерти — прогрессирование туберкулеза.
Медицинское свидетельство о смерти (п. 19. I):
а) прогрессирование туберкулеза;
б) фиброзно-кавернозный туберкулез легких (код А15.2).
При исходной макроскопической картине в случае обнаружения при гистологическом исследовании хронической туберкулезной каверны типичного трехслойного строения с признаками прогрессирования цирротического туберкулеза легких патологический процесс следует расценивать как фиброзно-кавернозный туберкулез на фоне выраженных цирротических изменений легкого.
Осложнения: хроническое легочное сердце (масса сердца 380 г, дилатация правых отделов сердца, гипертрофия миокарда правого желудочка 0,9 см, желудочковый индекс 1,1), общее хроническое венозное полнокровие (мускатная печень, цианотическая индурация почек, селезенки), анасарка, двусторонний гидроторакс (справа 800 мл транссудата, слева 1000 мл), гидроперикард (120 мл), отек легких.
В данном случае смерть пациента последовала от диссеминированного туберкулеза легких подострого течения, что привело к формированию хронического легочного сердца с декомпенсацией в финале патологического процесса.
Медицинское свидетельство о смерти (п. 19. I):
а) легочно-сердечная недостаточность;
б) хроническое легочное сердце;
в) диссеминированный туберкулез легких (код А19.0).
В ПАД и Свидетельстве может быть указана только одна форма туберкулеза, при этом приоритет отдается хронической, деструктивной форме (например, фиброзно-кавернозному туберкулезу легких перед казеозной пневмонией и диссеминированным туберкулезом легких) или более тяжелому распространенному процессу (например, казеозной пневмонии перед диссеминированным туберкулезом легких).
Не следует писать: фиброзно-кавернозный туберкулез правого легкого, диссеминированный туберкулез левого легкого.
Следует записать: фиброзно-кавернозный туберкулез легких в фазе прогрессирования — хроническая большая туберкулезная каверна верхней доли правого легкого с бронхогенной диссеминацией в нижнюю долю и в контралатеральном легком.
Не следует писать: казеозная пневмония нижней доли правого легкого, фиброзно-кавернозный туберкулез верхней доли правого легкого.
Следует записать: фиброзно-кавернозный туберкулез легких в фазе прогрессирования — хронические туберкулезные каверны верхней доли правого легкого, сливающиеся ацинозные и лобулярные очаги диссеминации в нижней доле с формированием обширных фокусов по типу казеозной пневмонии.
Не следует писать: казеозная пневмония правого легкого, диссеминированный туберкулез левого легкого.
Следует записать: казеозная пневмония правого легкого с бронхогенной диссеминацией в левом легком.
Осложнения: отек легких, печеночная недостаточность (иктеричность кожного покрова, слизистых и серозных оболочек; указать данные печеночных проб и биохимического анализа крови); анемия (указать данные общего анализа крови); кахексия.
Медицинское свидетельство о смерти:
п. 19. I. а) раковая кахексия;
б) рак легкого с метастазами (код С34);
II. Туберкулема легкого (код А15.2).
Фоновое заболевание: очаговый туберкулез верхней доли правого легкого в фазе организации после противотуберкулезной полихимиотерапии.
Осложнения: паренхиматозная желтуха (иктеричность кожного покрова, слизистых и серозных оболочек, билирубин общий 295 мкмоль/л, билирубин прямой 162,1 мкмоль/л); асцит (2000 мл); реактивный плеврит (слева 800 мл, справа 500 мл); отек легких; набухание и отек головного мозга.
Медицинское свидетельство о смерти:
п. 19. I. а) печеночно-почечная недостаточность;
б) острая токсическая дистрофия печени (код К71);
II. Очаговый туберкулез легких (код А15.2).
1) острый трансмуральный инфаркт миокарда задней стенки левого желудочка; атеросклероз коронарных артерий с поражением 50% поверхности интимы и стенозом до 70%;
2) диссеминированный туберкулез легких в фазе прогрессирования — ацинозные, сливные ацинозные, лобулярные очаги казеозного некроза; малые и средние острые каверны во всех долях легких, наличие в мокроте МБТ (люминесцентная бактериоскопия №, дата).
Осложнения: пустые полости сердца и крупных сосудов; выраженный отек легких.
Медицинское свидетельство о смерти:
п. 19. I. а) острая левожелудочковая недостаточность;
б) острый инфаркт миокарда (код I21);
II. Диссеминированный туберкулез легких (код А19.0).
В случае смерти от прогрессирующего туберкулеза, развившегося на фоне гормональной терапии, проводимой по поводу какой-либо другой болезни (бронхиальная астма, системная красная волчанка, склеродермия, идиопатический фиброзирующий альвеолит, псориаз и пр.), туберкулез выставляют на первое место. Если для лечения использовались гормоны, то болезни будут относиться к фоновым заболеваниям (с указанием дозировок препаратов и сроков лечения гормонами), которые также фиксируются во II разделе п. 19 Свидетельства. Если наступление смерти происходит от прогрессирующего туберкулеза, развившегося на фоне противоопухолевой терапии, такой случай расценивается аналогично.
Фоновое заболевание: системная красная волчанка, леченная стероидными гормонами (гормональный препарат, доза, длительность получения препарата).
Осложнения: отек легких, отек головного мозга.
Медицинское свидетельство о смерти:
п. 19. I. а) прогрессирование туберкулеза;
б) туберкулез множественной локализации (код А19.1);
II. Системная красная волчанка (код М32).
Заключение
Формулировка ПАД при туберкулезе в каждом случае требует индивидуального подхода с сопоставлением клинических данных и результатов патологоанатомического исследования. Необходимым условием является правильная оценка активности и распространенности туберкулезного процесса с определением роли туберкулеза в танатогенезе. Глубокий анализ каждого секционного случая способствует правильной трактовке данной патологии, верному определению места туберкулеза в структуре ПАД, что позволяет обеспечить корректной информацией подразделения медицинской статистики, эпидемиологическую и фтизиатрическую службы.
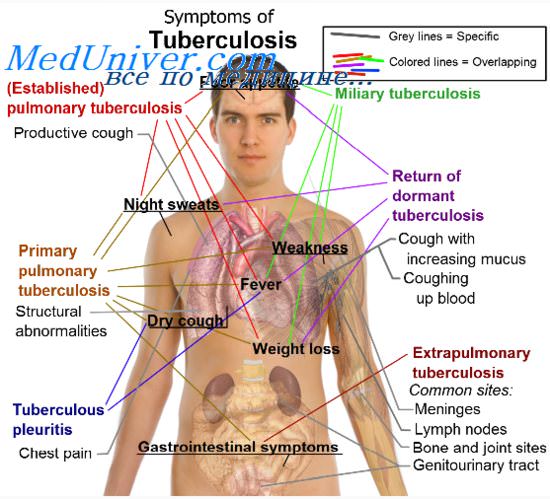
Типы рентгенологической картины туберкулеза и рака легкого. Примеры сочетания рака и туберкулеза.
Таким образом, можно выделить следующие основные типы рентгенологических проявлений сочетанного поражения легких туберкулезом и раком.
Тип I: появление в зоне стационарных или регрессирующих туберкулезных изменений новой одиночной изолированной круппоочаговой или фокусной тени, особенно неправильно округлой формы с волнистыми контурами и с относительно однородной структурой.
Иллюстрацией может служить следующее наблюдение.
Больной Ц., 77 лет, страдает двусторонним очаговым туберкулезом легких с 1960 г. После длительного курса химиотерапии очаги частично рассосались и приобрели фиброзный характер. В 1963 г. в верхушке левого легкого на фоне этих изменений без клинико-рентгенологических признаков их обострения появилась одиночная изолированная отчетливо отграниченная овальной формы тень диаметром 1—1,5 см. Несмотря на возобновление противотуберкулезной терапии, объем этого образования увеличивался. В конце 1964 г. появились кровохарканье, боли в боку, усилился кашель, а в вернхем отделе легкого возник сегментарный ателектаз. Общее состояние больного постепенно ухудшалось, и при явлениях легочно-сердечной недостаточности он умер в 1965 г. На секции был подтвержден диагноз рака верхушечного сегментарного бронха левого легкого, развившегося в зоне фиброзных изменений и казеозных очагов.
Тип II: возникновение на фоне активных туберкулезных изменений или вне их зоны новой, подобно I типу, тени, которая, несмотря на специфическую химиотерапию, увеличивается в размерах, хотя туберкулезные изменения при этом регрессируют.
Примером может служить следующее наблюдение.
Больной Б., 66 лет, страдает очаговым туберкулезом легких с 1942 г. До 1968 г. туберкулезный процесс был неактивным. В начале этого года наступило ухудшение общего состояния, усилился кашель, появились боли в правом боку. Рентгенологически выявлена инфильтрация вокруг старых очагов в верхушках легких и округлая фокусная тень в прикорневом отделе переднего сегмента правого легкого. Через 3 мес после начатой туберкулостатической терапии общее состояние больного улучшилось, инфильтративные изменения вокруг старых очагов частично рассосались, но фокус в прикорневом отделе переднего сегмента правого легкого увеличился в объеме, приобрел бугристые очертания, что дало основание заподозрить развитие периферического рака при наличии туберкулеза. В дальнейшем опухоль достигла еще больших размеров, между тем как туберкулезные изменения почти полностью рассосались.
Тип III: присоединение к заглохшему или активному туберкулезу: а) гиповентиляции, эмфиземы, пневмонита, ателектаза сегмента, доли или всего легкого; б) нарастающих перибронхиальных, интерстициальных или стелющихся по междолевой плевре уплотнений, исходящих из корня легкого; в) одностороннего увеличения и уплотнения корня легкого, особенно за счет внутрйтрудных лимфатических узлов.
Больной П., 57 лет. Ограниченный туберкулез легких и туберкулез гортани впервые были выявлены у него в 1955 г. После длительной специфической терапии наступило клиническое излечение. В 1960 г. отмечено обострение туберкулеза легких с бацилловыделением. В дальнейшем процесс протекал волнообразно, по к 1964 г. он стабилизировался и бацилловыделение прекратилось. В 1965 г. без каких-либо клинико-рентгенологических признаков обострения остаточных туберкулезных изменений в верхушках легких усилилась одышка, появились боли в левой половине грудной клетки и надсадный кашель. К концу 1965 г. эти симптомы нарастали, участилось кровохарканье, появились лейкоцитоз (11 600), палочкоядерный сдвиг нейтрофилов (до 29%), ускорилась РОЭ (40—50 мм/ч), увеличился уровень фибриногена в сыворотке крови (1030 мг%). Тогда же рентгенологически выявлены сначала гиповентиляция нижней доли левого легкого, а затем пневмонит в ней с уплотнением и увеличением корня, но без признаков обострения туберкулезного процесса. Под влиянием неспецифической терапии пневмонит ликвидировался, но сменился локальной эмфиземой нижней доли с увеличением объема и уплотнением корня легкого. Несмотря на продолжающееся лечение, общее состояние больного ухудшилось, появились резкая слабость и кахексия, развился ателектаз нижней доли левого легкого и левосторонний плеврит. В конце 1966 г. больной умер. На секции подтвердился диагноз рака левого нижнедолевого бронха при наличии двусторонних фиброзноочаговых изменений в легких.
Тип IV: появление выраженного асимметричного утолщения стенки старой туберкулезной каверны с полипообразными бугристыми разрастаниями в просвете или вокруг нее при отсутствии перифокального воспаления и бронхогенной диссеминации.
Следующее наблюдение иллюстрирует такой тип процесса.
Больной Б., 58 лет, страдает диссеминированным туберкулезом легких с 1950 г. В 1956 г. наступило обострение процесса с образованием деструкции в верхней доле левого легкого. К концу 1963 г. туберкулез стабилизировался, бацилловыделение прекратилось, но каверна в левом легком сохранялась. В 1964 г. при отсутствии явных клинико-рентгенологических признаков обострения туберкулеза состояние больного ухудшилось, появились боли в левой половине грудной клетки, слабость, периодические кровохарканья, усилился кашель, ускорилась РОЭ (30—40 мм/ч); увеличилось содержание глобулинов в сыворотке крови, преимущественно за счет фрвкцин, а рентгенологически было обнаружено выраженное асимметричное утолщение стенки каверны и уплотнение прилежащих к ней отделов легкого и корня. Одновременно в мокроте были обнаружены клетки плоскоклеточного рака. В последующем опухоль увеличилась в объеме, образовался ателектаз сначала верхушечно-заднего сегмента, а затем всей верхней доли левого легкого. В июне 1966 г. больной умер. На секции был подтвержден диагноз рака, развившегося на фоне туберкулеза и исходившего из стенки каверны (рис. 109).
С целью выяснения уровня диагностики, клинико-рентгенологических проявлений и путей распознавания сочетанных форм туберкулеза и рака мы изучили, в частности, ретроспективно материалы о 139 больных, находившихся в последние годы в нашей клинике, у которых диагноз первичного бронхогепного рака, сочетающегося с туберкулезом легких, был тем или иным способом верифицирован. Из них у 76 он был подтвержден результатами операции или секции, у 50 — гистологическим изучением биоп-сированных тканей или цитологическим исследованием мокроты, у 13 — после длительного клинико-рентгенологического наблюдения.
Из приведенных данных становится очевидным, что к моменту поступления в клинику у подавляющего большинства больных уже отмечались различные клинические симптомы и сдвиги в лабораторных показателях, которые могут встречаться как при туберкулезе, так и при раке легких. Однако при совокупной их оценке и степепи выраженности они лишь в 24,4% случаев не вызывали подозрения на сосуществование туберкулеза и рака легкого. В 18% комплекс этих показателей указывал либо на присоединение рака, либо на обострение или рецидив туберкулеза. В остальных 57,6% клиническая симптоматология и результаты лабораторного исследования не укладывались в проявления только туберкулеза и были в большей мере характерны для присоединившегося рака легкого. В этих случаях среди клинических симптомов и лабораторных показателей наибольшее диагностическое значение имели: обнаружение опухолевых клеток в мокроте, резко выраженные патологические сдвиги в биохимических показателях и повторяющиеся кровохарканья.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Различия рака и туберкуломы. Диагностические особенности рака и туберкуломы.
По мере прогрессирования размеры периферического рака достигают значительной величины (6—8—10 см). Подрастая к корню легкого, он нередко теряет шаровидную форму и принимает характер центрально расположенной опухоли. При этом он сравнительно редко распространяется в соседнюю долю легкого, хотя край тени опухоли может образовать прогибающуюся книзу линию (симптом Ленка).
У 20—30% больных в раковом узле отмечаются мелкие полости распада. У 10—13% образуются более крупные полости, характерные для так называемого кавернозного рака. В этих случаях мелкие или щелевидные полости постепенно объединяются и превращаются в единую обширную полость, иногда достигающую 6—8 см в диаметре. Она имеет неправильные ландкартообразные очертания и содержит обычно небольшое количество жидкости. Наружные контуры распавшегося периферического рака сохраняют характерные для него признаки, а стенка остается довольно толстой (более 5 мм). При этом в окружающей легочной ткапи отсутствуют очаги обсеменения. К важным диагностическим признакам прогрессирования раковой опухоли относятся появление ее метастазов в лимфатических узлах корня легкого и средостения, развитие плеврита, прорастание тканей грудной стенки, диафрагмы и т. д.
Определенное значение приобретают результаты бронхографии, при которой удается установить симптомы, характерные для рака: признак культи (ампутации) бронха в зоне опухоли, деструкцию и перавномерное сужение мелких бронхов. При опухолях больших размеров, кроме того, может наблюдаться оттеснение и смещение соседних бронхов. При ангиопульмонографии определяются характерные изменения в виде обеднения сосудов вокруг опухоли или симптом культи на границе с нею. Скиалогическая картина периферического рака легкого, таким образом, заметно отличается от таковой при туберкуломе.
При бронхоскопии у большинства больных периферическим раком легкого не удается обнаружить патологические изменения из-за недоступности непосредственному осмотру субсегментарных и мелких бронхов. Только в части случаев можно отметить гиперемию и отечность слизистой оболочки сегментарных, долевых и главных бронхов или косвенные признаки бластоматозного процесса. У больных туберкулезом нередко выявляется специфический эндобронхит в виде инфильтрации или язвенного поражения слизистой оболочки сегментарных и более крупных бронхов.
Важную роль в дифференциальной диагностике рака и туберкуломы играют лабораторные методы исследования. Более чем у 1/2 больных периферическим раком легких в мокроте или в промывных водах бронхов при цитологическом исследовании находят опухолевые клетки, а у 3/4 — эритроциты. Обнаруживаемые иногда при этом бациллы являются кислотоустойчивыми сапрофитами, реже микобактериями туберкулеза. В последнем случае их обнаруживают в мокроте однократно, и выделяются они обычно в результате обострения и распада латентного туберкулезного очага в зоне опухоли.
Такой же случайной находкой становятся в свою очередь атипичные клетки цилиндрического эпителия у больных туберкулезом легких, страдающих одновременно хроническим бронхитом, пневмосклерозом.
Обращают на себя внимание некоторые отличия в гемограмме: тенденция к лейкоцитозу и лимфопении при раке и к лимфоцитозу при туберкулезе. При раке в большей мере снижено содержание в сыворотке крови альбуминов и повышен уровень глобулинов, главным образом за счет фракций. При туберкул омах состав белков в этих случаях обычно мало изменен.
После впрыскивания под кожу туберкулина у части больных туберкулезом (у 43% —по данным И. П. Жингеля, 1974) уменьшается содержание альбуминов и увеличивается уровень глобулиновых фракций. При раке таких сдвигов не наблюдается. Этот феномен является отображением более высокой чувствительности организма больных туберкулезом к данному аллергену, чем у страдающих раком. Среди последних у 1/3 мы отмечали отрицательные реакции на 1 ТЕ, а среди больных туберкуломой легких—у 19%.
Однако даже с помощью всех указанных методов исследования не всегда удается дифференцировать периферический рак и туберкулому легких. В таких случаях производят катетеризацию периферических бронхов с аспирационной биопсией и цитологическим исследованием извлеченного аспирата. С помощью этого метода удается верифицировать диагноз в среднем у 60—70% больных раком. Однако при расположении опухоли в кортикальных отделах легкого разрешающая диагностическая способность данного способа исследования уменьшается. Более эффективной в этих случаях может оказаться игловая биопсия леткого, посредством которой удается не только установить наличие опухоли, но и определить ее гистологический характер. При отрицательных результатах всех этих методов исследования или невозможности применить их по каким-либо причинам следует прибегать к торакотомии, если для этого нет противопоказаний.
Необходимо подчеркнуть, что весь объем диагностических приемов должен выполняться по определенному плану и по возможности в ограниченные сроки. В связи с этим нельзя считать оправданным длительное применение туберкулостатических средств как метода дифференциальной диагностики ex juvantibus. При такой тактике могут быть упущены возможности для эффективного хирургического вмешательства при периферическом раке легкого.
Среди опухолевых процессов, которые могут походить на туберкулому, следует иметь в виду узловатую форму бронхиоло-альвеолярного ракач или аденоматоза. В отличие от первичного рака бронхов адсноматоз сравнительно часто встречается у людей более молодого возраста и нередко у женщин. Так, из 29 таких больных, которых наблюдали на протяжении 1947 — 1970 гг. Galy и Marcq (1973), было 12 женщин и 17 мужчин. Их средний возраст составлял 50 лет, а некоторым было 25—30 лет Клинико-рентгенологическая картина болезни, по данным указанных авторов, протекает в виде 3 типов. У части больных в одной из долей легких, преимущественно нижней, появляется крупнофокусное образование, напоминающее туберкулезный инфильтрат или туберкулому.
В этих случаях обычно нет признаков метастазирования в плевру и лимфатические узлы. В других случаях в пределах доли обнаруживают несколько изолированных или сливающихся между собой очагов, причем у части больных при этом выявляется поражение внутригрудных лимфатических узлов и плевры. Третью группу составляют больные с более распространенными очаговыми и сливными фокусными изменениями в одном или обоих легких обычно уже с признаками метастазирования.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Впервые выявленные очаговые образования легких малого размера (до 2 см в диаметре). Динамическое наблюдение или операция?
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2016;(10): 57‑60
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Введение. Патологические образования легких малого размера (до 2 см) в подавляющем большинстве случаев выявляются при проведении компьютерной томографии грудной клетки, выполняемой по различным причинам. Обнаруженные при таком обследовании очаговые образования в легочной ткани нередко остаются без внимания специалистов, что порой влечет за собой неутешительные результаты лечения данной категории больных. Угрожающим фактором в диагностике опухолей легких малого диаметра является их бессимптомность. Цель. Разработать алгоритм лечения у больных с выявленными образованиями легких до 2 см в диаметре. Материал и методы. Работа основана на результатах обследования и лечения 110 больных с патологическими образованиями легких малого диаметра, находившихся в Клинике факультетской хирургии им. Н.Н. Бурденко с 1997 по 2013 г. Всем пациентам были выполнены операции удаления участков легочной ткани из различных операционных доступов: 44 видеоторакоскопические резекции легкого, 43 миниторакотомии с видео сопровождением, 23 миниторакотомии. Результаты. У 25 пациентов был выявлен рак легкого, у 38 - доброкачественные опухоли (гамартомы и туберкуломы), у 10 больных - диссеминированный туберкулез, что потребовало незамедлительного лечения в специализированных стационарах. Вывод. При малых размерах образований (от 0,5 до 2 см) показано удаление их без морфологического подтверждения диагноза до операции. Оптимальный оперативный доступ для хирургического лечения пациентов с опухолями легких малого размера следует выбирать в зависимости от диаметра и количества патологических образований. При единичной опухоли легкого размером менее 0,5 см, впервые выявленной при компьютерной томографии, наиболее целесообразной тактикой будет динамическое наблюдение больного и проведение контрольной компьютерной томографии через 3-6-12 мес.
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Одиночный очаг в легких (ООЛ) определяют как локальный участок уплотнения легочной ткани округлой или близкой к ней формы диаметром до 3 см [15]. Это международное определение отличается от традиционного отечественного представления о легочных очагах, источником которого является фтизиатрическая практика (в классификации туберкулеза легких размер очагов не превышает 1 см, а уплотнения большего размера определяются как инфильтраты, туберкуломы и другие виды изменений) [14, 15].
Патологические образования легких малого размера (до 2 см) в большинстве случаев выявляются при проведении компьютерной томографии грудной клетки, выполняемой по различным причинам [10, 11, 14, 16-18].
Некоторые характеристики объемных образований при КТ позволяют судить об их характере - доброкачественное или злокачественное, однако они не являются определяющими при постановке диагноза [19]. Также о характере образования можно судить по скорости его роста [20].
Между тем по результатам одного КТ-исследования часто трудно провести дифференциальную диагностику, требуются повторные исследования в динамике. При воспалительном процессе очаги исчезают через 1-2 мес. В случае атипичной железистой гиперплазии очаги не изменяются в течение нескольких лет. При аденокарциноме можно заметить увеличение размера и/или усиление плотности, а также сосудистую конвергенцию [11, 12].
Обнаруженные при таком обследовании очаговые образования в легочной ткани нередко остаются без внимания специалистов, что порой влечет за собой неутешительные результаты лечения этой категории больных.
Трудности точной диагностики очаговых образований легких хорошо известны - дифференциальную диагностику чаще всего приходится проводить между периферическим раком, доброкачественной опухолью (гамартохондрома и др.), туберкуломой, саркоидозом, метастатическими поражениями легкого [1-4, 6, 7, 10, 12].
По мнению С.В. Миллер и соавт. [8], диагностическая торакотомия является завершающим методом комплексного обследования больных с округлыми образованиями легких небольшого размера и обеспечивает действительно раннюю диагностику и своевременное хирургическое лечение. Следовательно, радикальное хирургическое вмешательство, предпринятое при округлом образовании в легком, генез которого неясен, является методом, позволяющим провести морфологическую верификацию ранней стадии злокачественной опухоли и выполнить органосохраняющую операцию.
Другие авторы считают, что в настоящее время не существует единого подхода к определению характера очаговых образований легких. Очевидно, что при высоком риске злокачественной опухоли оптимальный подход заключается в возможно более ранней морфологической верификации диагноза. В случае низкого риска злокачественного процесса более рационально проводить динамическое наблюдение [11].
Второй возможный результат - обнаружение признаков злокачественного процесса (очаг диаметром более 1 см с лучистыми неровными контурами, очаги по типу матового стекла и смешанного солидного типа, которые должны расцениваться как потенциально злокачественные), при которых необходима морфологическая верификация в условиях специализированного лечебного учреждения [12].
Ежегодно в России раком легкого заболевают свыше 63 тыс. человек, в том числе свыше 53 тыс. мужчин. У более 20 тыс. пациентов (34,2%) рак легкого выявляется в IV стадии, поэтому задача обнаружения злокачественных опухолей легких на ранних стадиях их развития чрезвычайно актуальна [2, 7, 8].
Угрожающим фактором при диагностике опухолей легких малого диаметра является их бессимптомность. Отсутствие жалоб, скудная клиническая картина заболевания, сложности с профилактикой и первичным выявлением очагов делают проблему образований легких до 2 см в диаметре актуальной для научных изысканий и практически значимой для сохранения здоровья и нередко жизни пациентов.
Материал и методы
Работа основана на результатах обследования и лечения 110 больных с патологическими образованиями легких малого диаметра, находившихся в Клинике факультетской хирургии им. Н.Н. Бурденко с 1997 по 2013 г. Мужчин было 63, женщин - 47. Возраст больных находился в пределах 19-74 лет.
У всех больных при рентгенологическом исследовании, включая компьютерную томографию, были впервые выявлены очаговые образования в легких размером от 0,5 до 2 см. Всем пациентам были выполнены операции удаления участков легочной ткани с опухолью из различных доступов: 44 видеоторакоскопические резекции легкого, 43 миниторакотомии с видеосопровождением, 23 миниторакотомии. Окончательный диагноз формулировали после планового гистологического исследования удаленного патологического образования легкого. Летальных исходов не было.
Все больные были разделены на группы в зависимости от размера очагового образования: 1-ю группу (диаметр ООЛ 0,5-1; рис. 1) составили 9 мужчин и 14 женщин, 2-ю группу (диаметр ООЛ 1-2 см; рис. 2) - 30 мужчин и 13 женщин, 3-ю группу (множественные ООЛ; рис. 3) - 27 мужчин и 17 женщин.

Рис. 1. Компьютерная томограмма груди пациента 1-й группы

Рис. 2. Компьютерная томограмма груди пациента 2-й группы.

Рис. 3. Компьютерная томограмма груди пациента 3-й группы.
Результаты и обсуждение
Больные 1-й группыбыли оперированы из миниторакотомного доступа, 2-й - из миниторакотомного доступа с видеоподдержкой, 3-й - из видеоторакоскопического доступа. Результаты гистологического исследования удаленных патологических образований представлены в таблице.

Данные гистологического исследования удаленных патологических образований
Очевидно, что в настоящее время остается нерешенным вопрос о показаниях и противопоказаниях к оперативному удалению одиночных образований легких размером от 0,5 до 1 см, диагностические алгоритмы у подобных пациентов также сформулированы нечетко. По нашим данным, злокачественное поражение легких и плевры в этой группе было диагностировано у 3 (13%) пациентов, доброкачественные опухоли - у 5 (21,7%).
Во 2-й группе у 13 пациентов был выявлен рак легкого. Доброкачественные опухоли (гамартомы) легкого имелись у 18 больных, у 7 пациентов была диагностирована туберкулома. Таким образом, в этой группе частота злокачественных и доброкачественных опухолей вместе с туберкуломами составила 88,4%.
У 9 (20,4%) пациентов 3-й группы были выявлены злокачественные поражения легких, у 10 (22,7%) - диссеминированный туберкулез, у 20 (45,5%) - саркоидоз, что потребовало незамедлительного лечения в специализированных стационарах.
Таким образом, диагностический алгоритм исследований у больных с впервые выявленными периферическими образованиями легких определяют данные мультиспиральной компьютерной томографии. При малом размере образований (от 0,5 до 2 см) показано их удаление без морфологического подтверждения диагноза до операции. Оптимальный оперативный доступ для хирургического лечения пациентов с опухолями легких малого размера следует выбирать в зависимости от диаметра и количества патологических образований. При единичной опухоли легкого размером менее 0,5 см, впервые выявленной при компьютерной томографии, наиболее целесообразной тактикой будет динамическое наблюдение больного и проведение контрольной компьютерной томографии через 3, 6, 12 мес.
Читайте также:

