Опыты по заражению сифилисом
Обновлено: 26.04.2024
Из донорской крови производится целый ряд препаратов крови, среди которых только альбумины во время технологического цикла подвергаются термической обработке, достаточной для уничтожения бледной трепонемы [1, 3, 5, 6]. Помимо альбуминов, изготавливается большое количество препаратов, не подвергающихся такой обработке:
- криопреципитат;
- иммуноглобулины - антистафилококковый, антивирусный, противостолбнячный;
- иммуноглобулин против гепатита В, иммуноглобулин человека нормальный;
- сыворотки - антистафилококковая, антипротейная, антисинегнойная, антидифтерийная, антиэндотоксиновая;
- тромбин;
- интерферон внутривенного и интраназального применения;
- фибринолизин;
- фибриноген;
- биологический антисептический тампон и другие (S).
Технологический процесс производства названных препаратов крови предусматривает хранение консервированной плазмы в течение 30 суток при t = +4+/-2 о С, а также воздействие 8 о и 25 о этиловым спиртом в течение 24 часов. Обработка происходит в кислой среде (используется уксусная кислота при рН=5,2). Предусматривается также 3-4 кратное замораживание (-20 о С) и последующее оттаивание (до +8 о С) материала, которое приводит к разрушению клеточных оболочек. Возможно, многие из этих факторов губительно влияют на бледную трепонему [4].
Проведено экспериментальное исследование, целью которого было установить влияние ряда технологических факторов, используемых при производстве препаратов крови, на жизнеспособность возбудителя сифилиса.
Подвижность и патогенность бледных трепонем штамма Никольса изучалась в условиях, максимально приближенных к производственным: в консервированной плазме, в спиртовом и уксусном растворах плазмы крови, а также при замораживании и оттаивании. Во все растворы добавляли взвесь бледных трепонем до содержания в каждом поле зрения 25-30 микроорганизмов.
Консервированную плазму (консервант "Глюгицир"), содержащую бледные трепонемы, хранили при t = +4+/-2 о С в течение 30 суток.
Плазму крови с добавлением этилового спирта (8 о ) хранили 24 часа при t = -2 о С. Кислый раствор плазмы крови (рН уксусной кислоты = 5,2) в течение 18 часов хранили при t = 0 о С. Консервированную плазму с бледными трепонемами трижды замораживали (t = -20 о С) и оттаивали.
Подвижность бледных трепонем в препаратах, приготовленных из вышеуказанных растворов, изучали в темном поле зрения микроскопа.
В результате микроскопического исследования установлено, что консервированная плазма крови к 5-му дню хранения при t = +4+/-2 о С не содержит подвижных бледных трепонем, а на 22-е сутки в ней отсутствуют уже и неподвижные микроорганизмы (таблица 1). Хранение плазмы крови, содержащей бледные трепонемы с добавлением этилового спирта, приводит через полчаса к резкому снижению числа подвижных бледных трепонем (таблица 2). В препарате менее половины микроорганизмов подвижны, преобладают трепонемы с ротаторными движениями. К концу первого часа в каждом поле зрения микроскопа было до 3-4 вялоподвижных микроорганизмов, контрактильные движения отсутствовали. Отмечалось снижение числа бледных трепонем до 4-17 в каждом поле зрения. Микроорганизмы были утолщены и укорочены. Еще через час только единичные бледные трепонемы были вяло подвижны и, в основном, за счет ротаторных движений. Продолжалось снижение числа бледных трепонем до 11 в поле зрения микроскопа. Морфологические изменения были значительно выражены: укорочение, утолщение и разволокнение микроорганизмов. А через 2 часа 30 минут с момента начала эксперимента, подвижные бледные трепонемы отсутствовали в исследуемых препаратах и число микроорганизмов было снижено до 6-10 в поле зрения.
Таблица 1. Влияние сроков хранения плазмы консервированной крови на подвижность бледных трепонем.
| Дни наблюдения | Число трепонем | |
| подвижные | неподвижные | |
| 1 | 30 | - |
| 2 | 22 | 3 |
| 5 | - | 12 |
| 7 | - | 10 |
| 12 | - | 10 |
| 15 | - | 6 |
| 22 | - | - |
| 30 | - | - |
Таблица 2. Влияние 8 о спиртового раствора на подвижность бледных трепонем.
| Время | Бледные трепонемы | |
| подвижные | неподвижные | |
| 10 30 | 25 | - |
| 11 00 | 8 | 16 |
| 11 30 | 3 | 1 |
| 12 30 | 1 | 10 |
| 13 00 | - | 10 |
| 23 00 | - | - |
Морфологические изменения представлены значительным укорочением, утолщением и разволокнением бледных трепонем.
Исследуемая кислая среда приводит к обездвиживанию бледных трепонем в течение 40 минут, а восемнадцатичасовое хранение в ней - к полному лизису трепонем (таблица 3). Из таблицы видно, что к началу исследования все бледные трепонемы были подвижны, преобладали ротаторные и сгибательные движения. Через 20 минут появилось до 16 неподвижных микроорганизмов, а количество подвижных уменьшилось до 9. Бледные трепонемы с контрактильными движениями отсутствовали, наблюдались микроорганизмы с ротаторными и сгибательными движениями. Еще через 20 минут во всех полях зрения микроскопа подвижные микроорганизмы отсутствовали, число неподвижных возросло. Та же микроскопическая картина сохранилась в течение следующих 20 минут. А к концу второго часа отмечалось снижение бледных трепонем до 12 в каждом поле зрения. Наблюдались морфологически измененные, укороченные и утолщенные микроорганизмы. Через 18 часов хранения в плазме бледные трепонемы отсутствовали. Данное наблюдение позволяет сделать вывод, что консервирование с уксусной кислотой (рН = 5,2) вызывает такие морфологические изменения бледных трепонем, которые приводят к их разрушению.
Таблица 3. Влияние уксусной кислоты на подвижность бледных трепонем, содержащихся в консервированной плазме крови.
| Время | Бледные трепонемы | |
| подвижные | неподвижные | |
| 12 30 | 25 | - |
| через 20 минут | 9 | 16 |
| через 40 минут | - | 23 |
| через 1 час | - | 23 |
| через 2 часа | - | 12 |
| через 18 часов | - | - |
При двукратном замораживании (-20 о С) и оттаивании консервированной плазмы крови, содержащиеся в ней бледные трепонемы теряют подвижность, при трехкратном - полностью разрушаются (таблица 4).
Таблица 4. Изменение подвижности бледных трепонем в плазме консервированной крови при трехкратном замораживании и оттаивании.
| Бледные трепонемы | Дни оттаивания | |||
| 1 | 7 | 14 | 21 | |
| подвижные | 30 | 4 | - | - |
| неподвижные | - | 9 | 3 | - |
При микроскопическом исследовании препарата из крови, хранившейся 7 суток при температуре -20 о С, оказалось, что большинство бледных трепонем неподвижны, причем они укорочены и утолщены. До 4-х микроорганизмов в поле зрения микроскопа умеренно подвижны, в основном, за счет ротаторных движений. Отмечалось значительное уменьшение числа бледных трепонем относительно первоначальной концентрации.
При повторном оттаивании плазмы консервированной крови, хранившейся 14 суток при температуре -20 о С, подвижные бледные трепонемы в ней отсутствовали. Отмечалось снижение числа бледных трепонем до 3 в каждом поле зрения. Морфологические изменения были значительно выражены: наблюдалось укорочение, утолщение и разволокнение микроорганизмов.
На 21-й день хранения содержимое колбы оттаивали в третий раз и готовили препарат для микроскопического исследования хранившихся замороженными в плазме бледных трепонем. Ни в одном поле зрения микроскопа микроорганизмы не обнаружены.
Учитывая теоретическую возможность сохранения измененных бледных трепонем (зерна, гранулы), было проведено изучение риска заражения полученных полуфабрикатов и готовых препаратов крови на 73 кроликах - самцах массой 2,5-3 кг, у которых серологические реакции на сифилис (КСР, РИТ и РИФ-200) были отрицательными. Каждому кролику вводили по 0,75 мл препарата внутрикожно с каждой стороны мошонки.
В течение 6 месяцев после инъекций кролики находились на клинико-серологическом контроле. Животных осматривали каждые 2 недели в течение первых 2 месяцев, затем - раз в месяц; кровь для исследования в КСР брали из краевой вены уха раз в месяц, в РИТ и РИФ-200 - раз в 3 месяца. После окончания наблюдения у кроликов удаляли подколенные лимфатические узлы и перевивали их здоровым кроликам 1-го пассажа, а от них через 6 месяцев наблюдения - кроликам 2-го пассажа. За пассажными кроликами проводили клинико-серологическое наблюдение; исходных кроликов и животных 1-го пассажа после удаления лимфатических узлов, а кроликов 2-го пассажа через 4-6 месяцев наблюдения заражали внутрикожно на мошонке взвесью патогенных бледных трепонем штамма Никольса с тем, чтобы убедиться в отсутствии у них скрытого сифилиса.
Все кролики удовлетворительно перенесли их введение. У одного животного, зараженного консервированной плазмой с патогенными бледными трепонемами, отмечалась отечность правого яичка, а на коже мошонки справа образовалась кровянисто-гнойная корка диаметром 0,5 см. На 2-м месяце отек регрессировал, корка отпала, на коже мошонки остался рубец диаметром 0,2 см. В последующие 4 месяца клинико-серологического наблюдения кролик оставался серологически здоров. Вышеописанная корка на коже мошонки была расценена как результат случайной травмы кожи во время заражения. У одного кролика на первом месяце наблюдения были положительные результаты КСР (реакция Вассермана с трепонемным антигеном - 2+, неспецифическим - 4+, кардиолипиновым - 4+). Однако повторное серологическое исследование через 7 дней и в последующие месяцы наблюдения дали отрицательные результаты.
Клинико-серологическое наблюдение за другими животными не выявило у них признаков сифилитической инфекции. Они оставались клинически здоровыми, а КСР, РИТ и РИФ-200 были отрицательными.
От 69 оставшихся в живых кроликов через 6 месяцев наблюдения произведен пассаж лимфатических узлов здоровым кроликам 1-го пассажа и затем через 6 месяцев от 62 кроликов 1-го пассажа кроликам 2-го пассажа. При наблюдении за этими кроликами также не выявлено клинических проявлений сифилиса, серологические реакции сохранились отрицательными в течение всего эксперимента. Все кролики после окончания наблюдения были реинфицированы взвесью бледных трепонем штамма Никольса, что привело к развитию твердых шанкров у всех животных, а результаты серологических реакций, исследованных через 1,5 месяца, были резко положительными.
Таким образом, в эксперименте in vitro и на кроликах in vivo показана высокая эффективность производственных факторов при обеззараживании сырья, содержащего патогенные бледные трепонемы штамма Никольса.
Литература.
1. Гаврилов O.K. Развитие трансфузиологии и основные достижения службы крови СССР.// Проблемы гематологии и трансфузиологии: Юбилейный сб. науч. работ к 50-летию ЦНИИГПК. - М., 1976. - T.1. - С. 24-42.
2. Жибург Б.Б., Сидоркевич С.В., Бондарчук Ю.В. Вирусы и сепсис: широкий спектр взаимоотношений.// Сепсис. Актуальные вопросы клиники и эксперимента; Сб. науч. тр. - Махачкала, 1997. - С. 20-23.
3. Русанов Б.М., Розенберг Г.Я. Типовой комплексный регламент производства белковых препаратов плазмы донорской крови. - М. 1979. - 303 с.
4. Профилактика трансфузионного сифилиса: заключит. отчет о НИР/ Исп. Ротанов С.В., Сергеева Э.В. М.: - ЦКВИ, 1984. - 21 с.
5. Фром А.А., Скобелев Л.И., Русанов В.М. Белки плазмы и их фракционирование в производстве препаратов крови. - М.: Медицина, 1974. - 251 с.
6. Jamieson G.A. The development of plasma perivatives for clinical use.// Proc. of the American Real Cross Symposium. - Washington, D.C., October 1971. "Vox Song".
Сифилис (syphilis) - хроническое инфекционное заболевание, возникающее при заражении бледной трепонемой. Инфицирование происходит преимущественно половым путем, но возможна передача трансплацентарно (врожденный сифилис) при бытовых контактах (бытовой сифилис) и при переливании крови (гемотрансфузионный путь).
Этиология
С помощью электронного микроскопа установлено, что бледная трепонема в очагах поражения чаще располагается в межклеточных щелях, периэндотелиальном пространстве, кровеносных сосудах, нервных волокнах, особенно при ранних формах сифилиса. Нахождение бледных трепонем в периэпиневрии еще не является доказательством поражения нервной системы. Чаще подобное обилие трепонем имеет место при явлениях септицемии. В процессе фагоцитоза часто возникает состояние эндоцитобиоза, при котором трепонемы в лейкоцитах заключаются в полимембранную фагосому. Факт заключения трепонем в полимембранных фагосомах - явление весьма неблагоприятное, так как, находясь в состоянии эндоцитобиоза, бледные трепонемы длительно сохраняются, защищенные от воздействия антител и антибиотиков. В то же время клетка, в которой образовалась такая фагосома, как бы защищает организм от распространения инфекции и прогрессирования болезни. Это зыбкое равновесие может сохраняться длительно, характеризуя латентное (скрытое) течение сифилитической инфекции.
Для получения культуры бледных трепонем необходимы сложные условия (специальные среды, анаэробные условия и др.). Вместе с тем культуральные трепонемы быстро теряют морфологические и патогенные свойства. Кроме указанных выше форм трепонем, предполагалось существование зернистых и невидимых фильтрующихся форм бледных трепонем.
Вне организма бледная трепонема весьма чувствительна к внешним воздействиям, химическим веществам, высыханию, нагреванию, влиянию солнечных лучей. На предметах домашнего обихода бледная трепонема сохраняет свою вирулентность до высыхания. Температура 40-42°С сначала повышает активность трепонем, а затем приводит к их гибели; нагревание до 60°С убивает их в течение 15 мин., а до 100°С - моментально. Низкие температуры не оказывают губительного влияния на бледную трепонему, и в настоящее время хранение трепонем в бескислородной среде при температуре от -20 до -70°С или высушенных из замороженного состояния является общепринятым методом сохранения патогенных штаммов.
Условия и пути заражения сифилисом
В настоящее время основным путем заражения сифилисом следует признать половой контакт больного со здоровым; случаи бытового заражения (при пользовании общими посудой, сигаретами, трубками и т. д.) встречаются редко. Внеполовое заражение может происходить, если во рту больного находятся эрозированные сифилитические элементы. Значительно реже наблюдаются случаи, когда трепонемы, находящиеся в отделяемом сифилитических элементов, попадают на предметы домашнего обихода, которые становятся посредником в передаче инфекции (во влажной среде трепонемы долго сохраняют жизнеспособность вне организма человека). Врачи и другой медицинский персонал могут заразиться при осмотре больного сифилисом или при проведении лечебных процедур. Такие случаи наблюдали среди акушерок, врачей-хирургов, акушеров-гинекологов, стоматологов, венерологов, лабораторных работников, проводивших исследование на бледную трепонему. Во избежание подобного заражения надо работать с больным в перчатках, следить за целостью кожи кистей, а после обследования больного (особенно с заразной стадией сифилиса) протирать руки дезинфецирующим раствором и мыть их с мылом.
Весьма редки случаи заражения сифилисом при прямом переливании (трансфузии) крови от больного сифилисом донора. Считают, что слюна больного заразительна вследствие наличия в ней бледных трепонем только в том случае, если у больного в полости рта имеются сифилитические элементы. Высказывается предположение о заразительности молока кормящей женщины, больной сифилисом, даже если в области грудного соска нет видимых сифилитических изменений.
Так же трактуют вопрос о заразительности спермы, несмотря на отсутствие проявлений болезни на половых органах больного активным сифилисом. Вместе с тем считают, что моча и пот больных сифилисом не заразительны. Одним из возможных путей передачи сифилитической инфекции является плацентарный: от больной матери плоду через плаценту. В результате может развиться врожденный сифилис.
Экспериментально установлено, что для развития сифилитической инфекции играет роль и количество возбудителя, вводимого в организм подопытного животного. Можно предположить, что и у людей это имеет определенное значение (поэтому у лиц, неоднократно находившихся в половом контакте с больным активной формой сифилиса, возможность заражения намного возрастает по сравнению с теми, кто имел однократную и кратковременную половую связь). Вместе с тем отсутствие критериев зараженности заставляет венерологов проводить превентивное лечение всем лицам, имевшим половой контакт с больным заразной формой сифилиса, а также тем лицам (особенно детям), которые были в тесном бытовом контакте.
Экспериментальный сифилис
Попытки заразить сифилисом различных животных с целью создания экспериментальной модели инфекции (для изучения вопросов этиологии, патогенеза, терапии и др.) предпринимались еще в прошлом столетии. Однако первые опыты по экспериментальному заражению сифилисом животных, которые получили всеобщее признание, произведены И.И. Мечниковым и Ру в 1903 г. Авторы не только удачно заразили двух шимпанзе сифилисом, но и наблюдали у них развитие проявлений вторичного периода болезни (папулы на животе и конечностях).
Патогенез
Реакция организма больного на внедрение бледной трепонемы сложна, многообразна и недостаточно изучена. Заражение происходит в результате проникновения бледной трепонемы через кожу или слизистую оболочку, целость которых обычно нарушена. Однако ряд авторов допускают возможность внедрения трепонемы через неповрежденную слизистую оболочку. В то же время известно, что в сыворотке крови здоровых лиц имеются факторы, обладающие иммобилизующей активностью по отношению к бледным трепонемам. Наряду с другими факторами они дают возможность объяснить, почему при контакте с больным человеком не всегда отмечается инфицирование.

40 лет подряд правительство США ставило грандиозный эксперимент. 600 зараженных сифилисом черных крестьян из Алабамы получали плацебо и мышьяк, хотя нормальные лекарства уже существовали. Целью эксперимента было не вылечить больных, а наблюдать за тем, как именно они умирают. Никакой научной пользы — только безумие, которое длилось с 30-х по 70-е.

Таскиги был нищей неприветливой дырой в Алабаме, так что местные жители ухватились за возможность бесплатной медицинской помощи. Вот только лечить их никто особо и не собирался. Правительство использовало здешнее население как материал для экспериментов. Город стал секретным полигоном для исследования сифилиса. Врачи не только не излечивали больных, но даже способствовали распространению эпидемии.
Хуже всего то, что горожане оставались подопытными крысами, зараженными сифилисом, даже когда в остальном мире уже появилось лекарство от него. Их намеренно изолировали так, чтобы они не смогли получить помощь от других врачей.
Цель исследования была в том, чтобы позволить пациентам умереть от сифилиса. Лечить их в планы не входило.
Звучит как обычная теория заговора. Однако правительство США официально признало существование этого опыта и извинилось перед жителями Таскиги, а Билл Клинтон, в бытность президента, лично принес им извинение от лица нации.
Но случилось это лишь в 1997 году. А пока на дворе 1932 год — сифилис бушует в южных штатах, особенно среди нищих и чернокожих, и всем на них наплевать. Причины — банальные: расизм (большинство жителей Таскиги — черные) и невежество. Причем невежество как пациентов, так и врачей. С бедняками понятно — они понятия не имели о природе сифилиса, но доктора были немногим лучше.

Доктора под предводительством Кларка Талиаферро пообещали всем, кто хочет принять участие в эксперименте, бесплатный проезд, бесплатное лечение и (а вот здесь уже стоило задуматься) бесплатное место на кладбище и похороны. Сейчас трудно понять, насколько чисты были помыслы Кларка Талиаферро. Выглядит все так, словно он действительно хотел помочь и был полон решимости найти лекарство от сифилиса.
Вот только альтруизм исследователей не выдержал столкновения с реальностью. Великая депрессия все испортила: проект лишили финансирования и должны были закрыть. Талиаферро фактически выдавили с руководящего поста, и его место занял Оливер Венгер — помощник, оказавшийся гораздо циничнее и, в плохом смысле, дальновиднее.

Оливер Венгер
Благодаря его усилиям эксперимент продолжили, причем на долгие 40 лет. Только вся суть работы была поставлена с ног на голову. Амбициозный Венгер продал душу дьяволу и с готовностью променял роль врача на роль эдакого полубога, который распоряжается человеческими жизнями так, словно это подопытные животные.
В распоряжении Венгера оказались 600 человек из местных чернокожих батраков. 399 из них были больны сифилисом, 201 — без этого заболевания, это была контрольная группа. До 40-х годов еще можно было сказать, что подопытных действительно лечили: им давали разные препараты, но почти все они были неэффективны. Причем на тот момент это и так, в общем-то, было известно — никакого практического смысла в таком лечении не было.
Больным давали токсичные препараты на основе ртути, висмута и мышьяка. Некоторым, вроде как, даже помогало. Некоторых убивало. Большинству делало только хуже. Подход, как вы понимаете, устаревший даже в 30-е. В 40-х годах случилось нечто, что окончательно дает право называть эксперимент преступным:
Лекарство от сифилиса было найдено. Но подопытным об этом не сказали.
Эксперимент в Таскиги продлился до 1972 года. 30 лет местных жителей держали в неведении о том, что весь мир уже лечит их недуг с помощью пенициллина. Им же давали плацебо в ожидании того, как они станут материалом для вскрытия.

Экспериментаторы просто хотели выяснить, умирают ли черные от сифилиса так же, как белые (этих-то уже исследовали). Оказалось, что да, симптомы и страдания — те же самые. Поразительное открытие, для которого понадобилось 40 лет и сотни человеческих жизней.
Но как исследователям удавалось водить за нос столько людей на протяжении почти полувека? Неужели никто не удосужился съездить в другой город или обратиться к иным врачам? Добиться этого, что неудивительно в таком эксперименте, удалось благодаря подлости.

Юнис Ривер — медсестра, которая поднялась до координатора проекта
Зачем она это делала, неужели ей было не жаль своих черных братьев, умирающих в муках? Ответ до ужаса прост: благодаря эксперименту она сумела стать фактическим руководителем проекта. Ее власть была настолько велика, что со временем она оказалась самой влиятельной персоной во всем городе Таскиги.

Все изменилось только в 1972 году, когда стараниями Бакстана история стала всенародным достоянием. О Таскиги написали Washington Star и New York Times. Сенатор Эдвард Кеннеди созвал слушания в конгрессе США. По стране прошла волна протестов. Специально назначенная конгрессом комиссия постановила, что эксперимент является бесполезным и антигуманным, и он был прикрыт.
В ходе эксперимента 40 жен заразились от своих мужей, и еще 19 детей родились с врожденным сифилисом.

Тем, кому любопытна эта история, советуем прочитать статьи в самих Washington Post и New York Times, которые в свое время помогли рассказать правду о Таскиги.
Прямые методы диагностики служат для выявления бледной трепонемы (Т. pallidum) или генетического материала этого возбудителя в образцах, взятых из очагов поражения. Прямое выявление возбудителя сифилиса является абсолютным доказательством наличия заболевания. Найденный генетический материал (ДНК/РНК) может свидетельствовать как об активном, так и о ранее леченном сифилисе.
На ранней стадии болезни, возбудитель сифилиса активно размножается в очаге инфицирования, при этом антитела к антигенам бледной трепонемы (Treponema pallidum) начинают появляться только со второй недели после инфицирования. Бледная трепонема располагается в тканевых щелях, между волокнами соединительной ткани, вокруг лимфатических и кровеносных сосудов, в стенках и даже просветах лимфатических капилляров.
При медицинском обследовании, у пациентов с подозрением на сифилис, все высыпания на коже или слизистых оболочках следует считать сифилитическими. Исследованию на бледную трепонему подлежат все эрозивные и язвенные шанкры, мокнущие и эрозивные папулы, широкие кондиломы на коже и слизистых оболочках рта, половых органов и анальной области.
Материалом, который необходим для бактериологического исследования на бледную трепонему, является тканевая жидкость (серум). Если нет возможности исследовать высыпания (например, в случаях раннего сифилиса), то рекомендуется проводить пункцию увеличенного регионарного лимфатического узла с соблюдением всех правил асептики, то есть стерильными инструментами и соблюдая правила, направленные на предотвращение распространения микроорганизмов. Кроме того, образцы могут быть получены путем взятия спинномозговой жидкости (ликвора) или плодной жидкости.
Важным условием для обнаружения бледной трепонемы в пат. материалах является правильное взятие проб из сифилитических элементов. Затем содержимое полученных проб изучают в лаборатории.
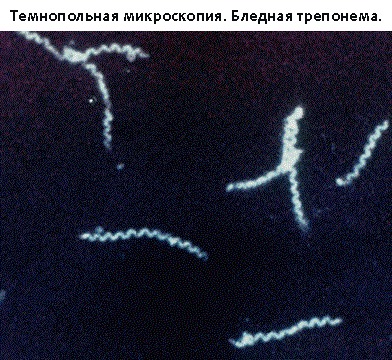
Обнаружение бледной трепонемы методом темнопольной микроскопии (ТПМ).
В России в качестве рутинного метода прямой визуализации T. pallidum традиционно используется метод темнопольной микроскопии (ТПМ, dark field microscopy, DFM).
1. Конденсор темного поля
Исследование на бледную трепонему в темном поле зрения проводится с помощью стандартного микроскопа, снабженного конденсором темного поля.
Конденсор представляет собой двояковыпуклую линзу, прикрепляемую снизу предметного столика с таким расчетом, чтобы линза конденсора располагалась под отверстием предметного столика. Конденсор служит для собирания (конденсации) пучка световых лучей, что обеспечивает наибольшее освещение исследуемого предмета.
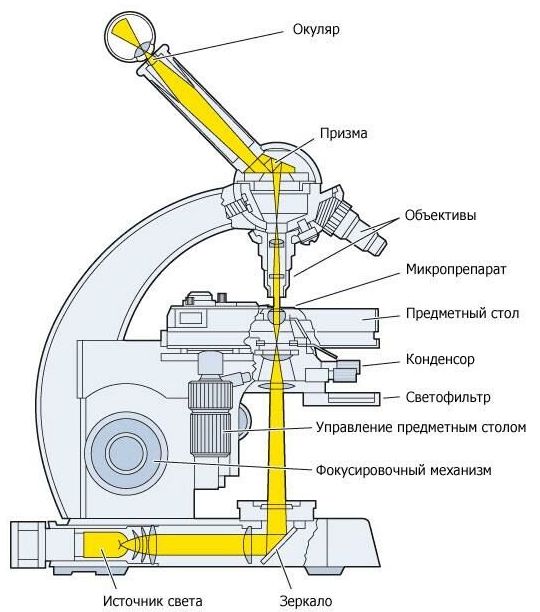
Неокрашенные живые бледные трепонемы не видны в световой микроскоп при обычном освещении препарата. Необходимые условия создаются путем замены обычного конденсора микроскопа особым конденсором, в котором центральная часть затемнена и проникновение лучей света происходит через узкую щель.
Вследствие получающегося при этом бокового освещения достигается отраженное свечение всех твердых частиц на темном поле (это называется "эффектом Тиндаля"), в том числе бледной трепонемы. Для получения темного поля необходим сильный источник света.
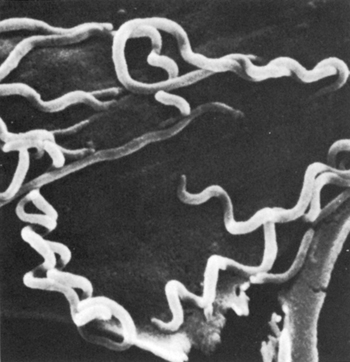
2. Бледная трепонема, характерные особенности при темнопольной микроскопии
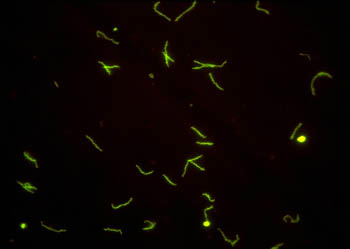
Исследование в темном поле микроскопа позволяет изучать бледную трепонему (БТ) в живом виде, а также достоверно отличать её от других трепонем как по морфологическим признакам, так и по характерным особенностям движения.
Чтобы отличать бледную трепонему от морфологически сходных типов сапрофитных трепонем, бледные трепонемы при исследовании должны быть живыми. Темнопольное исследование взятого материала должно быть проведено немедленно, сразу после получения образца, поэтому оборудование должно быть подготовлено заранее.
В затемненном поле зрения бледная трепонема выглядит, как движущаяся тонкая спираль или тонкий нежный пунктир с серебристым оттенком, слабо преломляющие свет. Помимо этих бактерий, в препарате все поле зрения усеяно массой мельчайших светящихся точек, находящихся в хаотичном броуновском движении.
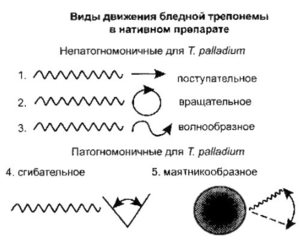
Бледные трепонемы движутся характерным образом: вращаются вокруг своей продольной оси, перемещаются в одном направлении, качаются наподобие маятника или совершают волнообразные, сократительные или сгибательные движения ("шагающая трепонема"). Бледная трепонема движется плавно, что является важной особенностью этого микроогранизма.

T. phagedenis, электронная микроскопия
В полости рта и на половых органах встречаются сапрофитные трепонемы: T . refringens и T. phagedenis (reiteri) в урогенитальном тракте и T. denticola в полости рта.
Непатогенные трепонемы морфологически сходны с T. pallidum. От них бледную трепонему отличает толщина, характер движения и форма завитков.
T.refringens колонизирует наружные половые органы. Эта бактерия движется быстро и неравномерно, отличается большей толщиной, отсутствием сгибательных движений, и более пологими и широкими завитками. T.denticola является представителем нормальной микрофлоры полости рта, ее завитки короче и направлены под более острым углом. В нормальной флоре наружных половых органов человека встречается также T. phagedenis.
Наличие непатогенных трепонем затрудняет исследования материала, взятого из поражений в полости рта или прямой кишке. При дифференциации трепонем может ошибиться даже опытный исследователь, поэтому присутствие этих микроорганизмов делает малодостоверным проведение исследования с данным материалом. Если необходимо провести тестирование материала, полученного из одного из указанных выше мест, то предпочтительнее выполнить DFA или NAAT (лучше отдать предпочтение методу ПИФ или молекулярно-биологическим методам).
Методом темнопольной микроскопии невозможно отличить бледную трепонему от патогенных возбудителей других трепонематозов — T. pallidum carateum (пинта), T. pallidum pertenue (фрамбезия), T. pallidum endemicum (беджель).
3. Применение темнопольной микроскопии для диагностики сифилиса
Микроскопию в темном поле можно применять для диагностики первичных и вторичных поражений кожи при сифилисе в результате заражения половым путем. В редких случаях этот метод можно использовать при третичном сифилисе (в последнем случае — если материал взят из глубины инфильтрата или со дна язвы).
Также с помощью этого метода исследуют поражения при раннем врожденном сифилисе, когда заражение плода бледной трепонемой произошло в утробе матери. Чтобы подтвердить диагноз "врожденный сифилис", для приготовления препарата для микроскопии можно использовать ткань пуповины, органы плода, выжатый сок плаценты, амниотическую (плодную) жидкость, отделяемое слизистой оболочки носа, содержимое пузырей (при ладонно-подошвенной сифилитической пузырчатке), тканевой жидкости (серума) с раздраженных папул.
Метод темнопольной микроскопии, используемый для диагностики сифилиса, отличается простотой, дешевизной, быстротой и достаточно высокой чувствительностью. Однако у него есть известные недостатки – невозможность диагностики скрытых и поздних форм сифилиса и непригодность для контроля излеченности. Даже многократный отрицательный результат микроскопического исследования на бледную трепонему не может исключить сифилис.
Кроме того, для проведения исследования методом ТПМ микроорганизмы T. pallidum должны быть подвижными. В условиях применения пациентами различных антибактериальных препаратов, в том числе для лечения других заболеваний, диагностическая чувствительность ТПМ снижается. В подобных случаях необходимо исследование методом прямой иммунофлюоресценции (ПИФ) или проведение серологического обследования на сифилис.
Для повышения информативности лабораторной диагностики разрабатываются более чувствительные и специфичные прямые тесты на основе молекулярно-биологических технологий, например различные модификации метода ПЦР.
Метод прямой иммунофлюоресценции (ПИФ)
При необходимости микроскопия возбудителя в темном поле может быть дополнена прямой реакцией иммунофлюоресценции (ПИФ, direct fluorescent antibody test, DFA).
Прямой метод иммунофлюоресценции (по Кунсу) основан на взаимодействии антител, меченых флюорохромом, с антигеном, который находится на клетке, в клетке или в тканях. В качестве флюорохрома используют флюоресцеинизотиоционат (ФИТЦ).
Метод прямой иммунофлюоресценции предусматривает прямое выявление T. pallidum в образце при обработке материала специфическими моноклональными антителами. При этом на запарафинированные мазки или биопсийный материал накладываются противотрепонемные антитела, меченные флюоресцирующим красителем. Затем, образующиеся комплексы антиген—антитело исследуют под люминесцентным микроскопом.
В результате взаимодействия анти- T.pallidum антител, меченных ФИТЦ, и бледной трепонемы при люминесцентной микроскопии наблюдается специфическое ярко-зеленое свечение: бледная трепонема флюоресцирует ярко-зеленым цветом, сохраняя все морфологические признаки спирохеты.
Забор образцов производится таким же образом, как и для темнопольной микроскопии, при этом сам метод ПИФ является более точным, чувствительным и специфичным, чем ТПМ.
Метод ПИФ имеет преимущества перед темнопольной микроскопией для выявления бледной трепонемы. Флюоресцирующие микроорганизмы проще детектировать, вероятность спутать их с другими видами трепонем снижена. При этом возможна дифференцировка патогенных трепонем от непатогенных при исследовании материала со слизистых полости рта и прямой кишки, фиксация препаратов перед транспортировкой в лабораторию. Для исследования может быть использован материал, полученный при биопсии или аутопсии.
Кроме того, применение ПИФ ограничено из-за отсутствия промышленного производства и сертификации соответствующих ингредиентов в ряде стран, в частности, ФИТЦ-меченых моноклональных антител к патогенной бледной трепонеме.
Метод полимеразной цепной реакции (ПЦР)

Для диагностики сифилиса применяется прямой метод определения ДНК бледной трепонемы — метод ПЦР; это один из методов амплификации нуклеиновых кислот (МАНК, nucleic acid amplification test, NAAT).
Метод полимеразной цепной реакции (ПЦР) позволяет исследовать различные образцы (отделяемое сифилидов, биопсийный материал, биологические жидкости) в свежем, замороженном, фиксированном и парафинированном виде. В качестве объекта исследования методом ПЦР могут быть использованы соскобы шанкров и других высыпаний (папул, широких кондилом и т.д.), спинномозговая, амниотическая жидкость, сыворотка крови.
ПЦР–тесты для выявления ДНК бледной трепонемы были разработаны в 1991 году одновременно в нескольких лабораториях. Этот метод позволяет выявить и идентифицировать единственную молекулу ДНК бледной трепонемы среди сотен тысяч других молекул, что делает потенциально возможной диагностику нейросифилиса, третичного, врожденного сифилиса при наличии единичных трепонем в исследуемом материале.
Метод ПЦР высокоспецифичен, чувствителен и воспроизводим при правильном проведении и подготовке образцов. Однако, применительно к диагностике сифилиса, методы МАНК пока используется в исследовательских целях.
- PCR в режиме реального времени (PCR-RT). Учет полученных результатов происходит автоматически в режиме реального времени по уровню свечения флюорохромных меток;
- методика PCR-анализа с помощью обратной транскриптазы (PCR-ОТ);
- мультиплексная PCR (PCR-М, М-ПЦР), которая позволяет в биологической пробе одновременно определять наличие возбудителей нескольких заболеваний.
Основными достоинствами метода ПЦР и его модификаций является универсальность (возможность обнаружить любые нуклеиновые кислоты), весьма высокая чувствительность (80 – 94,7 %) и высокая специфичность (до 100 %). Результат получается быстро, для анализа необходима проба малого объема (несколько микролитров). Современные методы ПЦР позволяют одновременно исследовать нескольких возбудителей заболеваний, а также получать документальный ответ в виде фотографий и вносить результаты диагностики на компьютерные информационные носители. К недостаткам метода ПЦР-анализа следует отнести высочайшие требования к оснащению лаборатории, качеству тест–наборов и регламенту исследования.
Метод ПЦР является дополнительным и может быть рекомендован, главным образом, для исследования отделяемого эрозивных и язвенных высыпаний при подозрении на первичный сифилис, особенно при их локализации на слизистой оболочке рта; при применении пациентами местных и системных антибактериальных средств накануне обращения к врачу; при отрицательных результатах серологических тестов в начале первичного периода, когда ошибка метода ТПМ особенно значима.
Развитие высокочувствительного метода ПЦР и разработка его модификаций, оценивается как весьма перспективное. Особую важность этот метод приобретает при диагностике первичного серонегативного сифилиса (при котором серологические исследования дают отрицательный результат), раннего скрытого, врожденного сифилиса и нейросифилиса.
Препятствием к широкому внедрению метода ПЦР для диагностики сифилиса является отсутствие в массовой доступности тест-систем, разрешенных к медицинскому применению. В США применение ПЦР рекомендовано лабораториям, располагающим соответствующими тест-системами (в том числе созданными в самих лабораториях, in house). В России и странах Восточной Европы широкое использование метода лимитируется небольшим количеством наборов реагентов, прошедших валидацию и разрешенных к медицинскому применению на территории соответствующих государст
NASBA
NASBA - Nucleic Acid Sequence-Based Amplification, амплификация, основанная на последовательности нуклеиновых кислот (другие переводы - реакция амплификации на основе нуклеотидной последовательности нуклеиновых кислот, реакция транскрипционной амплификации). Методика NASBA основана на выделении РНК микроорганизма (в отличие от полимеразной цепной реакции, где используется ДНК). Этот метод тестирования считается одним из самых перспективных и многообещающих направлений молекулярной диагностики.
Использование в качестве мишени для NASBA видоспецифических участков рибосомальной РНК обеспечивает методу высокую специфичность. Так как РНК — менее стабильный по сравнению с ДНК тип генетического материала, который быстрее деградирует при разрушении клеток, то на основании результатов выявления РНК можно судить о наличии в образце жизнеспособных микроорганизмов, например, после проведенного лечения. С практической точки зрения важно, что для проведения NASBA в лабораторных условиях используется то же оборудование, что и для проведения ПЦР в реальном времени (PCR-RT). Кроме того, исходный биоматериал после ПЦР может исследоваться методом NASBA. В результате этого существует возможность интегрирования указанного метода в протокол лабораторного обследования, что позволит верифицировать возбудителя
Отдельные исследовательские коллективы уже получают достаточно перспективные результаты при изучении сифилитической инфекции методом NASBA и NASBA-RT, используя в качестве качестве мишени фрагмент гена 16s рРНК бледной трепонемы. Полученные данные позволяют отнести метод NASBA к диагностически перспективным в изучении сифилитической инфекции наряду с имеющимися методами диагностики.
Заражение сифилисом лабораторных животных
Задолго до открытия бледной трепонемы многие ученые стали проводить эксперименты по заражению сифилисом разнообразных животных. В естественных условиях животные сифилисом не болеют, но возможно искусственное заражение некоторых их видов. Первые успешные опыты были проведены на шимпанзе в начале 20-го века. Дальнейшие опыты на обезьянах привели к ряду блестящих научных открытий, но ввиду трудностей содержания и дороговизны обезьян, основными лабораторными животными стали кролики. Опыты с другими животными (холоднокровными, птицами, различными млекопитающими) давали отрицательный или недостаточный для практического применения результат. Некоторое значение имели только данные, полученные на морских свинках и мышах.
Заражение сифилисом кроликов является старейшим методом прямого выявления бледной трепонемы, т.к. кролик является наиболее чувствительным и удобным лабораторным животным для привития сифилиса. Заражение кроликов производят инокуляцией (введением микроорганизмов в ткани, от латинского inoculatio - "прививка") инфекционного материала в яичко. Чувствительность кроликов к инфекции Treponema pallidum практически 100%, если во взятом для прививки материале содержится достаточное количество бледных трепонем.
Реакции иммунной системы организма при заражении сифилисом

Сифилис - это инфекционное заболевание, вызываемое бледной трепонемой (бактерией Treponema pallidum). Организм человека, заболевшего сифилисом, защищается от возбудителя заболевания с помощью механизмов иммунитета. Проникновение, длительное сохранение в организме (персистенция) и размножение возбудителя заболевания в организме хозяина приводят к выраженным изменениям со стороны иммунной системы.
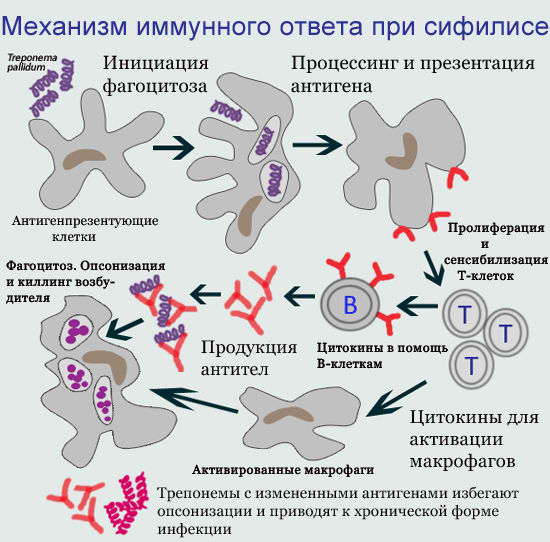
После попадания бледных трепонем в организм и при их дальнейшем размножении, в организме больного человека происходят иммунные сдвиги. Механизм иммунного ответа при сифилисе исследован не полностью, однако имеются достаточно убедительные данные о том, что в этом процессе участвуют все звенья иммунной системы.
Активируются механизмы как врожденного неспецифического иммунитета, свойственного человеку как биологическуому виду, так и адаптивного, антиген-опосредованного иммунного ответа, вызванного контактом с антигеном. В иммунном ответе организма принимают участие как клеточные (макрофаги, Т-лимфоциты), так и гуморальные механизмы (синтез специфических иммуноглобулинов — антител).
Иммунную реакцию вызывают белки, входящие в состав структур бледной трепонемы; они являются чужеродными веществами для организма человека и относятся к антигенам. Все антигены трепонемы способны стимулировать организм больного вырабатывать антитела соответствующих классов. Вследствие этого, в сыворотке крови больных сифилисом отмечается множественность антител: протеиновых, комплементсвязывающих, полисахаридных реагинов, иммобилизинов, агглютининов.
Классы вырабатываемых антител меняются на разных этапах течения сифилиса — в различных стадиях болезни преобладают то одни, то другие антитела, относящиеся к разным классам иммуноглобулинов. Сила иммунного ответа и спектр антител, выявляемых на разных стадиях развития инфекции, зависит от особенностей организма у данного человека.
Во многих случаях иммунологический ответ не предотвращает поэтапного развития инфекции. Организм хозяина неспособен уничтожить сифилитическую инфекцию, что приводит к дальнейшей эволюции патологического процесса. Болезнь, начавшись с местного процесса, распространяется на весь организм и продолжается много лет.
Клеточный и гуморальный иммунный ответ на внедрение бледной трепонемы в организм
В иммунном ответе организма на заражение принимают участие клеточные и гуморальные механизмы иммунитета.
1. Клеточный иммунитет при заражении сифилисом
На клеточном уровне бледной трепонеме противодействуют высокоспециализированные клетки иммунной системы — макрофаги, T-лимфоциты, B-лимфоциты. Происходит изоляция и частичное уничтожение трепонем фагоцитами, в основном макрофагами. Фагоцитоз носит преимущественно незавершенный характер — при поглощении фагоцитом возбудитель не погибает, а остается в клетке, сохраняя свою структуру и способность к размножению. Более того, фагоцит оберегает от антител и воздействия антибиотиков бледную трепонему, которая становится недоступной для защитных сил организма.
Ранний сифилис характеризуется частичным угнетением клеточного иммунитета и развитием состояния иммуносупрессии, постепенно нарастающей активизацией гуморального иммунитета. Клеточное звено страдает в первую очередь, так как Т-лимфоциты более чувствительны к воздействию бактерий T. pallidum.
У больных вторичным, латентным и третичным сифилисом формируется клеточный иммунитет, признаки которого выявляются в реакциях in vivo (кожные пробы) и in vitro (стимуляция Т-лимфоцитов трепонемными антигенами).
2. Гуморальный иммунитет при заражении сифилисе
Гуморальный иммунный ответ заключается в продукции широкого спектра противосифилитических антител. В структуре бледной трепонемы выявлено большое количество соединений, имеющих выраженные антигенные свойства для иммунной системы человека. На начальных этапах развития сифилиса происходит более выраженный синтез антител к антигенам, имеющим высокое содержание в клетке T. pallidum и локализующимся в структуре мембран наружной клеточной стенки или протоплазматического комплекса.
3. Уклонение бледных трепонем от иммунного ответа
Клеточное и гуморальное звенья иммунитета не в состоянии обеспечить полное уничтожение и элиминацию бледных трепонем. Благодаря своему необычному молекулярному строению, T. pallidum обладает замечательной способностью уклоняться от защитной реакции макроорганизма.
Электронно-микроскопические исследования показали, что при сифилисе преобладает незавершенный фагоцитоз трепонем (захват и поглощение трепонем лейкоцитами, макрофагами и другими клетками). При этом трепонемы не погибают, а получают защиту от антибиотиков и антител, и могут даже размножаться в фагоцитирующей клетке. В течение всего инкубационного периода, а также в конце первичного и в начале вторичного периодов сифилиса, возбудители активно размножаются и распространяются по всему организму.
Гуморальный иммунный ответ. Противосифилитические антитела.
1. Неспецифические антитела при сифилисе
Реагиновые антитела у больного сифилисом — это иммуноглобулины класса IgG и IgM. Они являются комплексным ответом на высвобождение липоидных молекулярных фрагментов из поврежденных клеток хозяина, а также на появление липопротеиноподобных структур, сходных с кардиолипином, входящих в состав бактериальной клетки бледной трепонемы.
Липидные антигены cоставляют значительную часть бактериальной клетки T. pallidum. Помимо других антигенов, в клеточной стенке бледной трепонемы содержится фосфолипид кардиолипин; на его долю приходится около 30% сухого вещества клетки спирохеты. В организме человека, больного сифилисом, могут присутствовать липиды, имеющие сходное строение с липоидными структурами клеточной стенки бледной трепонемы. Это аутоантигены, образующиеся в результате разрушения органов и тканей, в основном липиды митохондриальных мембран.
Аутоантигены - это компоненты клеток и тканей собственного организма, которые распознаются при определённых условиях как частично чужеродные. Аутоантитела к кардиолипину – это антитела, направленные организмом против собственного кардиолипина.
Клетки человека, больного сифилисом выделяют в большом количестве липоидный и липопротеиноподобный материал, сходный с кардиолипином. Бледная трепонема приводит к поражению внутренних органов, в частности, к повреждению печени и сердца, освобождая некоторые фрагменты тканей. При интенсивном размножении спирохет в организме больного происходит распад тканей, в результате чего из поврежденных клеток высвобождаются липоидные молекулярные фрагменты.
Иммунная система пациента реагирует, вырабатывая реагиновые антитела на эти фрагменты. Продукты распада клеток — липоидные белки — поступают в кровяное русло. Эти белки являются чужеродными для организма человека, поэтому реакция организма проявляется в виде выработки неспецифических антител (иммуноглобулинов) класса IgM и IgG к липоидному и липопротеиноподобному материалу. Именно эти антитела исторически называются реагинами.
Следует иметь в виду, что реагины с помощью кардиолипиновых тестов могут обнаруживаться в организме людей, никогда не болевших сифилисом, т.к. их количество повышается при различных физиологических и патологических состояниях, не связанных с сифилисом, например у пациентов с аутоиммунными, воспалительными и гематологическими заболеваниями. Эти реагины могут быть причиной так называемых биологических ложноположительных серологических реакций на сифилис.
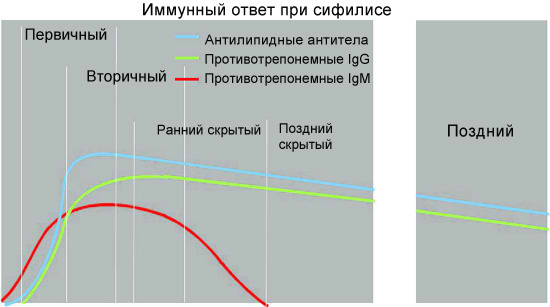
Антилипидные (неспецифические) антитела появляются в организме человека со стадии первичного сифилиса —примерно через 7-14 дней после образования твердого шанкра, через 4-5 недель после заражения.
Антитела против кардиолипина выявляют посредством нетрепонемных серологических тестов. При нетрепонемных методах анализа на сифилис не различают тип антител (IgG, IgM или др.), а определяют суммарный ответ.
2. Специфические антитела при сифилисе
Специфические антитрепонемные антитела направлены против бледной трепонемы. Плазматические клетки организма вырабатывают специфические антитела, направленные против соответствующих антигенов возбудителя заболевания.
На ранних этапах развития сифилиса, как бактериальной инфекции, у заболевшего человека осуществляется выработка специфических антител, относящихся преимущественно к иммуноглобулинам класса M (первичный иммунный ответ). Трепонемоспецифические Ig класса M у больных сифилисом могут регистрироваться даже в период инкубации. Позднее происходит переключение на синтез IgG (вторичный иммунный ответ).
Параметры иммунного ответа могут изменяться в результате проводимого лечения. Адекватное лечение раннего сифилиса приводит к быстрому снижению титров неспецифических антител и специфических IgM.
По мере развития патологического процесса постепенно включаются механизмы образования антител классов G и А. Ведущая роль в гуморальном ответе переходит к специфическим антителам IgG и IgА. При этом специфические IgG обычно сохраняются в сыворотке крови в течение длительного периода времени,а иногда и всю жизнь
Динамика образования специфических антител у больного при сифилисе
По данным современных исследований, гуморальный ответ при сифилисе происходит в соответствии с общими закономерностями для бактериальных инфекций. Вначале вырабатываются иммуноглобулины класса M против наиболее иммуногенных и специфичных антигенов возбудителя. Специфические антитела класса M способны выявляться в крови пациентов, инфицированных T. pallidum, на самых ранних этапах развития инфекции, уже через 1,5-2 недели после заражения, что клинически соответствует скрытому инкубационному периоду заболевания. При первичном и вторичном сифилисе содержание указанных антител в крови больных быстро нарастает и сохраняется на высоком уровне; максимальное их содержание у больных сифилисом приходится на 6—9-ю неделю заболевания.
После успешного лечения антибактериальными препаратами специфические IgM у больных относительно быстро элиминируют из кровотока (через 3—12 месяцев). При лечении раннего сифилиса IgM исчезают через 3-6 месяцев, позднего – через 1 год. Большое диагностическое значение приобретает выявление антитрепонемных антител IgM в крови новорожденных. Так как IgM не проходит через плаценту, выявление антитрепонемных IgM-антител у новорожденного указывает на врожденный сифилис. Точно так же IgM-антитела не проникают через гематоэнцефалический барьер, и их появление в спиномозговой жидкости говорит о нейросифилисе.
Многие лабораторные методики диагностики сифилиса основаны именно на выявлении трепонемоспецифических IgM. Например, иммуноферментный анализ (ИФА) на твердой фазе и линейный иммуноблоттинг (ИБ) на микропористых стрипах с использованием антивидовых конъюгатов на основе моноклональных антител к тяжелой мю-цепи в структуре IgМ человека, а также реакция непрямой иммунофлюоресценции (РИФ) с исследованием 19S-фракции сыворотки крови, содержащей тяжелые IgМ.
Раннее определение специфических IgM также может быть применено для своевременного выявления случаев раннего врождённого сифилиса (определение специфических IgM в крови новорожденных) или случаев реинфекции у пациентов, ранее перенесших сифилис.
Без лечения, по мере развития болезни и разрешения клинических проявлений вторичного периода, уровень специфических IgМ в крови больных сифилисом постепенно понижается и начинает преобладать синтез IgG. Развитие иммунного ответа на антигенную стимуляцию в организме больного сифилисом сопровождается постепенным переключением с синтеза антител класса M на продукцию более мелких молекул иммуноглобулинов класса G.
Специфические иммуноглобулины класса G в кровотоке больных сифилисом появляются более поздно, в конце 3-й или на 4-й неделе после заражения и, как правило, достигают более высоких титров, чем IgM. Уже на 6 неделе после инфицирования уровень IgG преобладает над уровнем IgM и может сохраняться в таком состоянии годы.
Содержание специфических IgG, постепенно увеличиваясь, достигает максимальной выраженности через 1—1,5 года, после чего несколько снижается, подвергаясь волнообразным колебаниям в зависимости от активности инфекционного процесса. Количество специфических IgG в циркулирующей крови после адекватно проведенного лечения снижается медленно. Антитела этого класса могут сохраняться даже после клинического излечения пациента в течение десятков лет или пожизненно.
Кроме перечисленных видов антител, в гуморальном иммунитете при сифилисе принимают участие иммуноглобулины класса А. Антитела IgA вырабатываются в сравнительно небольших количествах. Вопрос о синтезе IgE и IgD в настоящее время изучен недостаточно.
Читайте также:

