Организм сам справляется с вич
Обновлено: 26.04.2024
Перед тем как говорить о вакцине против ВИЧ, стоит начать с более общего вопроса: что мы понимаем под прививками и вакцинами с научной точки зрения?
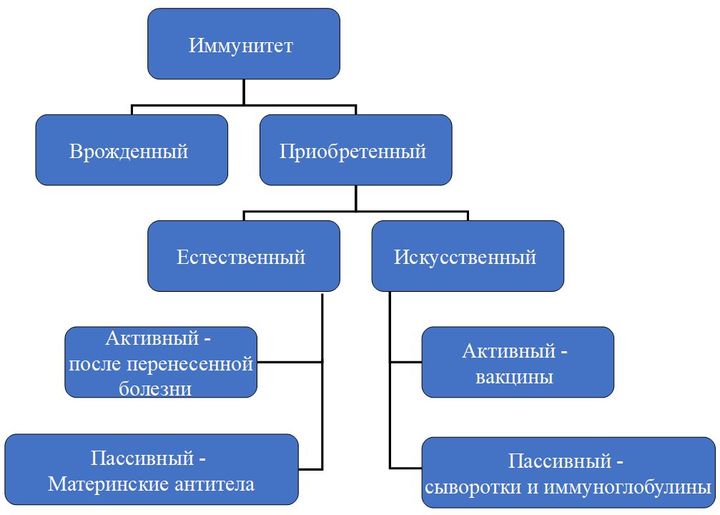
По механизму возникновения иммунитет делится на два вида: врожденный и приобретенный. Первый есть у каждого человека с рождения, он выработан эволюционно. Благодаря нему человек не болеет многими болезнями, которыми, например, страдают животные.
Второй возникает в течение жизни и у каждого может отличаться в зависимости от того, с какими возбудителями человеку довелось встретиться.
Приобретенный иммунитет может быть активным (он возникает вследствие реакции организма на перенесенную болезнь, присутствие возбудителя в организме), а может быть пассивным, когда антитела, например, передаются от матери ребенку во время беременности.
Именно по этим антителам, как правило, и ставится диагноз, если мы пользуемся экспресс-тестами. В случае с ВИЧ существует и пассивный иммунитет. Но при передаче вируса от матери ребенку, к сожалению, он не обладает достаточным защитным эффектом.
Еще одно направление — это искусственный иммунитет. Он тоже бывает активным и пассивным. Пассивный — это иммуноглобулины, выработанные либо у лабораторных животных, либо у других иммунизированных лиц, и сыворотки. Активный же достигается собственно путем вакцинации.
Какие бывают вакцины?
Вакцины бывают профилактические (защитные) и лечебные. Они различаются по типу воздействия на организм и по своим результатам.
Пассивный иммунитет возникает быстрее, сразу после того, как в организм ввели чужие антитела. Однако он бывает совсем недолговременным. Активный иммунитет держится долго, чаще — пожизненно, но и возникает не сразу.
Иммунный ответ: как это все работает?
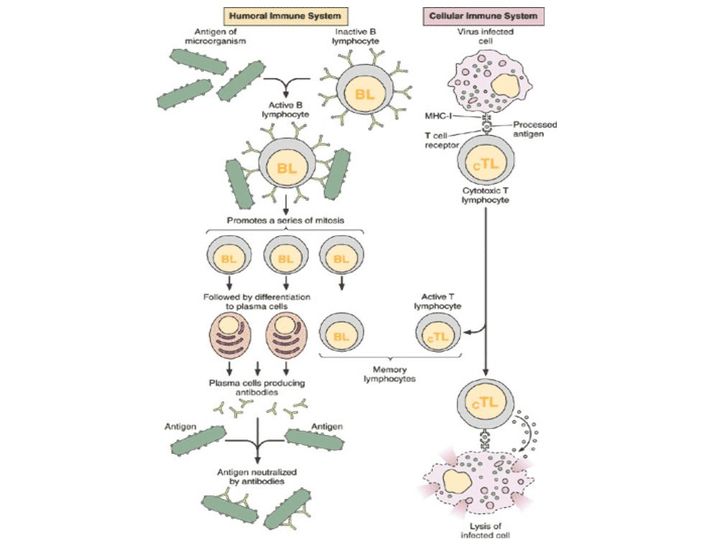
Ученые обычно говорят о гуморальном и клеточном иммунитете. Принцип работы гуморального заключается в следующем: в нашем организме есть специальные клетки — лимфоциты. Они постоянно циркулируют в крови и проверяют все, что попадается им на пути, по принципу свой/чужой.
Например, антитела к ВИЧ-инфекции появляются где-то через месяц после заражения, соответственно, все это время вирус может циркулировать в организме. Почему они неэффективны? Во-первых, потому что появляются слишком поздно.
Во-вторых, потому что вирус, с которым мы имеем дело, очень изменчив. Если даже В-клетки обнаружили его антиген, выработали к нему антитела, способные нейтрализовать заразу, то за время, которое ушло на все это, сам вирус успевает мутировать и оказаться неуязвимым для выработанного организмом оружия.
Когда мы говорим о клеточном иммунитете, речь идет об уничтожении тех вирусов, которые преодолели гуморальный барьер и успели забраться в саму клетку.
Клетки CD4 частично регулируют весь процесс и выполняют функцию клеток памяти. Их принято называть хелперами. CD8 — собственно занимаются уничтожением, за это их зовут киллерами.
ВИЧ — единственный вирус, который поражает не просто клетки организма, а собственно клетки иммунной системы. Той самой, которая с вирусом должна, по идее, бороться.
Именно поэтому против ВИЧ-инфекции иммунитет не может сработать так, как это было бы с любым другим вирусом.
Какие возникают трудности при создании вакцины против ВИЧ?
На данный момент в рамках более ста испытаний уже протестировано более сорока видов вакцин с участием тысяч добровольцев, и есть целая система, в которой регистрируются все исследования по вакцинации от ВИЧ.
Последнее время в разного рода СМИ регулярно появляется информация, что той или иной компанией разрабатывается новая вакцина против ВИЧ. Однако обнадеживающих результатов не так уж и много. Почему?
Лучшая из существующих вакцин, которая дошла до третьей фазы исследований, показала свою защитную эффективность только в 60 % случаев в течение одного года, а в течение уже трех лет — только в 30 %. Это очень мало для вакцины. Она должна давать до 90 % эффективности.
И связано это с тем, что существует ряд препятствий для создания вакцины от ВИЧ-инфекции. Во-первых, такая вакцина не может состоять из ослабленного или живого вируса, как многие другие. Если ввести даже одну-две частицы ВИЧ в организм, это вызовет не иммунный ответ, а инфицирование организма.
Во-вторых, и мы об этом уже сказали, вирус находится внутри CD4-лимфоцитов. Мы пока не научились извлекать вирус из клетки, не повреждая ее саму. И на данный момент до конца не понимаем, какие именно механизмы могли бы обеспечить полную защиту от ВИЧ-инфекции.
В-третьих, многие вакцины пока разрабатываются, испытываются на подопытных животных: мышах, свиньях. В случае с ВИЧ кроме обезьян, на которых можно было бы воспроизвести инфекцию, у нас нет подходящих подопытных животных, результаты работы с которыми можно было бы легко перенести на человека.
Исследования на людях дороги и имеют ряд этических ограничений. Можно было бы привить группу здоровых добровольцев, но инфицировать их, чтобы проверить, как работает вакцина, врачи не могут. Ни один подопытный на такое не согласится. А вдруг вакцина не сработает?
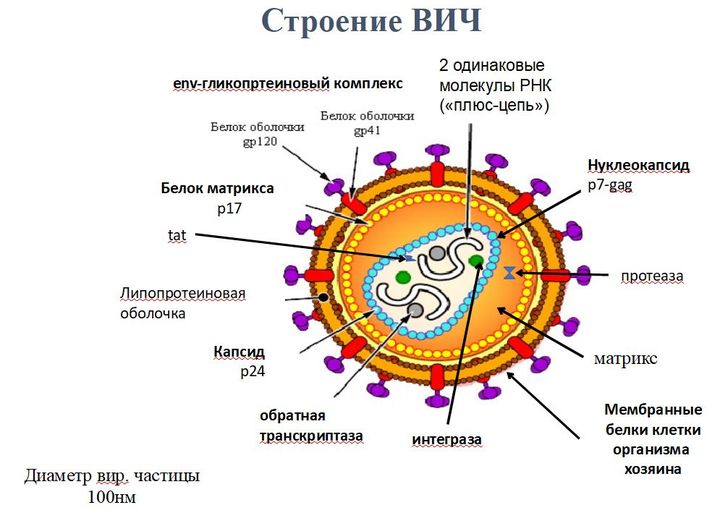
Разработки вакцины. Дорожная карта
Тем не менее ученым уже удалось выработать основные направления в иммунотерапии ВИЧ-инфекции. С одной стороны — это попытка активации специфического иммунитета, который не срабатывает при естественном течении ВИЧ-инфекции. С другой стороны — профилактическая пассивная иммунизация.
Что значит пассивная? Мы подозреваем, что существуют люди, которые не инфицируются ВИЧ даже при достаточно частом контакте с вирусом. Видимо, у них возникает хороший иммунный ответ, и иммунная система справляется с вирусом самостоятельно. А значит, мы можем попытаться либо взять у уже иммунизированных лиц готовые антитела, либо создать их генно-инженерным путем, чтобы потом ввести в организм.
Клинические исследования в области ВИЧ-инфекции по пассивной иммунизации начались еще в начале 80-х годов, то есть одновременно с обнаружением самого вируса.
Они встречаются как раз у того типа пациентов, который мы только что назвали. В эксперименте на животных было показано: если у организма есть эти антитела, даже в случае нарочного введения вируса заражения не происходит.
Интересно, что эти антитела не убивают вирус, но они могут с ним соединяться, блокируя его рецепторы, как бы окружая и покрывая вирус, не давая ему обычным способом проникнуть в клетку. Через какое-то время вирус, не найдя клетки, где он может размножиться, погибает.
Суть этой экспериментальной вакцины заключается в том, что состоит она из двух разных антигенов, синтезированных искусственно, но идентичных белкам настоящего вируса.
Искусственная комбинация белков не может сама по себе вызвать развитие инфекции, но, по идее, должна вызвать развитие антител — такое, каким бы оно было в норме при попадании вируса в организм.
В течение первых 12 месяцев исследования каждая из женщин, участвующих в нем, получит шесть инъекций: три инъекции — в течение первого месяца и по одной — каждый последующий.
Первые результаты ожидаются где-то к 2021 году. Однако здесь есть нюансы: белки, с которыми работают ученые в рамках указанного исследования, аналогичны для субтипа ВИЧ, распространенного в Африке, но редко встречающегося у нас, в России.
Итоги: ДКП, ПКП, АРВТ
В настоящее время есть некоторые инфекции, которые человечество эффективно научилась контролировать с помощью вакцинации, а некоторые и вовсе победить, как оспу. Но рассчитывать на скорый результат в случае с ВИЧ пока не приходится.
Возможно, комбинация всех перечисленных подходов, пассивного и активного иммунитета, одновременно сможет стать эффективной, чтобы оказывать профилактическое воздействие.
Однако пока в контексте ВИЧ-инфекции действовать нам придется на популяционном уровне — традиционными способами профилактики распространения заболевания. В первую очередь это: практики более безопасного сексуального поведения, использование стерильных инструментов во всех медицинских сферах, доконтактная профилактика, постконтактная профилактика и эффективная антиретровирусная терапия.
Исцеление – не то слово, которое часто используется в связи с термином "ВИЧ-инфекция". 35 лет прошло с момента обнаружения вируса и большую часть времени врачи рассматривали полное выздоровление скорее как фантазию, а не возможную перспективу. Всю потому, что ВИЧ не похож ни на один другой вирус. Он уничтожает те самые иммунные клетки, которые предназначены для того, чтобы с ним бороться. Он разрушает иммунную защиту месяцами, а иногда – годами.
На сегодняшний день с заболеванием живут 37 млн человек по всему миру. Однако сегодня ученые больше понимают о том, как вирус "скрывается" в клетках организма и почему наша бдительная иммунная система "не замечает" его.
Национальные институты здравоохранения (NIH) США финансируют усилия по лечению ВИЧ, а фонды – например AmfAR – ищут ресурсы, которые позволят полностью искоренить эпидемию.
"Абсолютно точно, что ВИЧ можно излечить, – говорит Ровена Джонстон, вице-президент и директор по исследованиям AmfAR. – Вопрос на миллиард долларов: "Как это сделать?".
Профессор медицины из Медшколы при Университете Джона Хопкинса Роберт Силичано одним из первых идентифицировал резервуары ВИЧ.
"Проблема в том, что такая форма ВИЧ не видна иммунной системе и на нее не влияют лекарственные препараты", – говорит Силичано. По словам доктора, вирус покидает свою укреплённую башню и идёт на штурм лишь тогда, когда человек перестаёт принимать лекарства.
В одном из докладов, которые представили на конференции по ретровирусам и оппортунистическим инфекциям 2018 года в Бостоне, исследователи обнаружили убедительные доказательства того, что резервуары могут быть активированы и устранены, по крайней мере – у животных. Дэн Барух и его коллеги из Медицинского центра Beth Israel Deaconess и Гарвардской медицинской школы показали, что препарат, который стимулирует иммунную систему и активирует резервуары, в сочетании с мощным антителом может нейтрализовать ВИЧ у инфицированных обезьян на полгода.
"Я думаю, что наши данные повышают вероятность получить препарат для полного вызоровления. Это возможно", – заявил Барух.
Такой метод в научной среде называют shock and kill: он основан на "выталкивании" спящего вируса из резеруаров и последующем уничтожении. Это шаг к избавлению людей от пожизненной зависимости от АРВ-препаратов.
Этот метод еще не был протестирован на людях и вопрос полного выздоровления еще в процессе изучения. Исследователи напоминают, что на сегодняшний день единственным полностью излечившимся от ВИЧ человеком является "берлинский" пациент, которому пересадили костный мозг от донора с особой мутацией, которая не позволяет вирусу иммунодефицита "прикрепляться" к клеткам. Браун прекратил прием АРВ-препаратов после пересадки. Прошло уже больше 10 лет и его тест на ВИЧ остаётся отрицательным.
[Подробнее об излечении Тимоти Рэя Брауна – в материале СПИД.ЦЕНТРа]
Случай Брауна доказывает, что полное выздоровление возможно, но врачи дожны добраться до "каждого закутка" организма, где может прятаться вирус, говорит доктор Стивен Дикс, профессор медицины Калифорнийского университета в Сан-Франциско.
Сейчас некоторые исследователи даже полагают, что возможно полностью реконструировать иммунную систему человека, чтобы она была способна успешно устранить любой вирус. Этим уже пользуются онкологи в борьбе с опухолями: иммунную систему программируют таким образом, что та сама атаковала злокачественные клетки.
"Я настроен оптимистично, поскольку параллели в терапии ВИЧ-инфекции и онкологии настолько тесны, что мы сможем применять товые технологии и в терапии ВИЧ", – говорит Дикс.
Никто из специалистов не ожидает, что ВИЧ будет побежден в следующем году или ближайшие пару лет. Но они более чем уверены, что в будущем мы победим эпидемию.
Перед тем как говорить о вакцине против ВИЧ, стоит начать с более общего вопроса: что мы понимаем под прививками и вакцинами с научной точки зрения?
По механизму возникновения иммунитет делится на два вида: врожденный и приобретенный. Первый есть у каждого человека с рождения, он выработан эволюционно. Благодаря нему человек не болеет многими болезнями, которыми, например, страдают животные.
Второй возникает в течение жизни и у каждого может отличаться в зависимости от того, с какими возбудителями человеку довелось встретиться.
по теме
Лечение
Как устроен иммунитет: Объясняем по пунктам
Приобретенный иммунитет может быть активным (он возникает вследствие реакции организма на перенесенную болезнь, присутствие возбудителя в организме), а может быть пассивным, когда антитела, например, передаются от матери ребенку во время беременности.
Именно по этим антителам, как правило, и ставится диагноз, если мы пользуемся экспресс-тестами. В случае с ВИЧ существует и пассивный иммунитет. Но при передаче вируса от матери ребенку, к сожалению, он не обладает достаточным защитным эффектом.
Еще одно направление — это искусственный иммунитет. Он тоже бывает активным и пассивным. Пассивный — это иммуноглобулины, выработанные либо у лабораторных животных, либо у других иммунизированных лиц, и сыворотки. Активный же достигается собственно путем вакцинации.
Вакцины бывают профилактические (защитные) и лечебные. Они различаются по типу воздействия на организм и по своим результатам.
Пассивный иммунитет возникает быстрее, сразу после того, как в организм ввели чужие антитела. Однако он бывает совсем недолговременным. Активный иммунитет держится долго, чаще — пожизненно, но и возникает не сразу.

Иммунный ответ: как это все работает?
Ученые обычно говорят о гуморальном и клеточном иммунитете. Принцип работы гуморального заключается в следующем: в нашем организме есть специальные клетки — лимфоциты. Они постоянно циркулируют в крови и проверяют все, что попадается им на пути, по принципу свой/чужой.
по теме

Лечение
Гид по вакцинам. Когда и какую прививку сделать? А главное: надо ли вообще прививаться? (Спойлер: конечно, надо)
Например, антитела к ВИЧ-инфекции появляются где-то через месяц после заражения, соответственно, все это время вирус может циркулировать в организме. Почему они неэффективны? Во-первых, потому что появляются слишком поздно.
Во-вторых, потому что вирус, с которым мы имеем дело, очень изменчив. Если даже В-клетки обнаружили его антиген, выработали к нему антитела, способные нейтрализовать заразу, то за время, которое ушло на все это, сам вирус успевает мутировать и оказаться неуязвимым для выработанного организмом оружия.
Когда мы говорим о клеточном иммунитете, речь идет об уничтожении тех вирусов, которые преодолели гуморальный барьер и успели забраться в саму клетку.
Клетки CD4 частично регулируют весь процесс и выполняют функцию клеток памяти. Их принято называть хелперами. CD8 — собственно занимаются уничтожением, за это их зовут киллерами.
ВИЧ — единственный вирус, который поражает не просто клетки организма, а собственно клетки иммунной системы. Той самой, которая с вирусом должна, по идее, бороться.

Именно поэтому против ВИЧ-инфекции иммунитет не может сработать так, как это было бы с любым другим вирусом.
Какие возникают трудности при создании вакцины против ВИЧ?
На данный момент в рамках более ста испытаний уже протестировано более сорока видов вакцин с участием тысяч добровольцев, и есть целая система, в которой регистрируются все исследования по вакцинации от ВИЧ.
Последнее время в разного рода СМИ регулярно появляется информация, что той или иной компанией разрабатывается новая вакцина против ВИЧ. Однако обнадеживающих результатов не так уж и много. Почему?

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
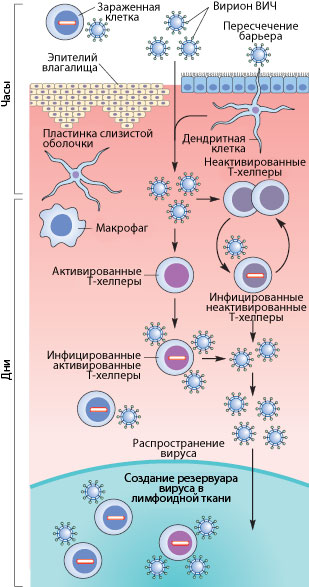
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.

Возможно ли полное выздоровление от ВИЧ-инфекции, как, например, это происходит при лечении гепатита С?
Чтобы снизить риск развития негативных последствий, пациенту дают иммуносупрессивные (подавляющие действие клеток трансплантата) препараты. В этот период человек становится крайне уязвим к инфекциям, его помещают в специальный стерильный бокс; также нередко требуются переливания крови и тромбоцитарной массы.
Каким образом трансплантация способствовала излечению от ВИЧ-инфекции
После трансплантации мужчина перестал принимать антиретровирусную терапию (АРВТ), и вирус в организме больше не выявлялся. К сожалению, в сентябре 2020 года Тимоти Рэй Браун скончался в возрасте 54 лет: смерть была вызвана рецидивом лейкоза.
Другие случаи выздоровления от иммунодефицита
К сожалению, данная манипуляция является слишком сложной, опасной и дорогостоящей для того, чтобы таким образом лечить всех пациентов с ВИЧ. Выздоровление может наступить, но польза от операции существенно меньше рисков, которые возникают при трансплантации костного мозга. Это тем более актуально сегодня, когда мы имеем большое количество высокоэффективных и безопасных антиретровирусных препаратов. Однако сам факт выздоровления пациентов дает надежду на то, что в будущем излечение от ВИЧ-инфекции возможно.
Несколько лет к случаям выздоровления ВИЧ-инфицированного человека относили ситуацию пациента из Сан-Паулу, который, согласно протоколу клинического исследования, получал интенсифицированный режим АРВТ (5 препаратов и никотинамид). После прерывания терапии у него длительное время сохранялась неопределяемая вирусная нагрузка и не определялась ДНК вируса в мононуклеарах крови (один из резервуаров ВИЧ в организме). Но в ноябре 2020 года (через 6 лет после прерывания терапии) исследование крови на вирусную нагрузку ВИЧ вновь показало положительный результат — 6300 коп/мл.
По сравнению с вирусом, который выявлялся у пациента на момент начала терапии, выявленные копии имеют генетические отличия в структуре РНК ВИЧ. Было ли выздоровление у пациента из Бразилии? Отличия в геноме могут быть связаны с эволюцией вируса внутри организма или с тем, что изначально произошло инфицирование несколькими штаммами, с последующей активацией другого субтипа вируса (в обоих случаях мы говорим о рецидиве инфекции). Кроме того, могла иметь место реинфекция (повторное проникновение вируса в организм).
В настоящее время активно ведутся разработки, которые помогут достичь полного излечения от ВИЧ-инфекции. Но мы узнаем лишь в будущем, какие из них окажутся действительно эффективными.
Автор: врач-инфекционист Университетской клиники H-Clinic Светлана Юрьевна Дегтярева
Медицинский редактор: руководитель Университетской клиники H-Clinic, к.м.н., врач-инфекционист Коннов Данила Сергеевич.
Читайте также:

