Осложненные инфекции мочевыводящих путей включая пиелонефрит
Обновлено: 25.04.2024
Категории МКБ: Интерстициальный цистит (хронический) (N30.1), Инфекция мочевыводящих путей без установленной локализации (N39.0), Острый тубулоинтерстициальный нефрит (N10), Острый цистит (N30.0), Пионефроз (N13.6), Хронический тубулоинтерстициальный нефрит (N11)
Общая информация
Краткое описание
Союз педиатров России
Клинические рекомендации: Инфекция мочевыводящих путей у детей
N10/ N11/ N13.6/ N30.0/ N30.1/ N39.0
Бактериурия – присутствие бактерий в моче (более 105 колоний-образующих единиц (КОЕ) в 1 мл мочи), выделенной из мочевого пузыря.
Асимптоматической бактериурией называют бактериурию, обнаруженную при диспансерном или целенаправленном обследовании у ребенка без каких- либо жалоб и клинических симптомов заболевания мочевой системы.
Острый пиелонефрит – воспалительное заболевание почечной паренхимы и лоханки, возникшее вследствие бактериальной инфекции.
Хронический пиелонефрит – повреждение почек, проявляющееся фиброзом и деформацией чашечно-лоханочной системы, в результате повторных атак инфекции МВП. Как правило, возникает на фоне анатомических аномалий мочевыводящего тракта или обструкции.
Рефлюкс-нефропатия - фокальный или диффузный склероз почечной паренхимы, первопричиной которого является пузырно-мочеточниковый рефлюкс, приводящий к внутрипочечному рефлюксу, повторным атакам пиелонефрита и склерозированию почечной ткани.
Уросепсис - генерализованное неспецифическое инфекционное заболевание, развивающееся в результате проникновения из органов мочевой системы в кровеносное русло различных микроорганизмов и их токсинов.
Классификация
Этиология и патогенез
Среди возбудителей инфекций мочевыводящих путей у детей преобладает грам-отрицательная флора, при этом около 90% приходится на инфицирование бактериями Escherichia coli. Грамположительные микроорганизмы представлены, в основном, энтерококками и стафилококками (5-7%). Кроме того, выделяют внутрибольничные инфекции штаммами Klebsiella, Serratia и Pseudomonas spp. У новорождённых детей относительно частой причиной инфекций мочевыводящих путей являются стрептококки групп А и В. В последнее время отмечен рост выявления Staphylococcus saprophyticus, хотя его роль остается спорной.
В настоящее время более половины штаммов E. coli при ИМВП у детей приобрели устойчивость к амоксициллину, однако сохраняют умеренную чувствительность к амоксициллину/клавуланату.
Среди многочисленных факторов, обуславливающих развитие инфекции МВП, приоритетное значение имеют биологические свойства микроорганизмов, колонизирующих почечную ткань, и нарушения уродинамики (пузырно-мочеточниковый рефлюкс, обструктивная уропатия, нейрогенная дисфункция мочевого пузыря).
Наиболее частым путем распространения инфекции считается восходящий. Резервуаром уропатогенных бактерий являются прямая кишка, промежность, нижние отделы мочевыводящих путей.
Анатомические особенности женских мочевыводящих путей (короткая широкая уретра, близость аноректальной области) обуславливают большую частоту встречаемости и рецидивирования ИМВП у девочек и девушек.
При восходящем пути распространения инфекции МВП после преодоления бактериями везикоуретерального барьера происходит их быстрое размножение с выделением эндотоксинов. В ответ происходит активация местного иммунитета макроорганизма: активация макрофагов, лимфоцитов, клеток эндотелия, приводящая к выработке воспалительных цитокинов (ИЛ 1, ИЛ 2, ИЛ 6, фактора некроза опухоли), лизосомальных ферментов, медиаторов воспаления; происходит активация перекисного окисления липидов, что приводит к повреждению почечной ткани, в первую очередь, канальцев.
Гематогенный путь развития инфекции мочевых путей встречается редко, характерен преимущественно для периода новорожденности при развитии септицемии и у детей грудного возраста, особенно при наличии иммунных дефектов. Этот путь также встречается при инфицировании Actinomyces species, Brucella spp., Mycobacterium tuberculosis.
Эпидемиология
Распространенность ИМВП в детском возрасте составляет около 18 случаев на 1000 детского населения. Частота развития ИМВП зависит от возраста и пола, при этом чаще страдают дети первого года жизни. У детей грудного и раннего возраста ИМВП – самая частая тяжелая бактериальная инфекция, она наблюдаются у 10-15% госпитализируемых лихорадящих больных этого возраста. До 3-х месячного возраста ИМВП чаще встречается у мальчиков, в более старшем возрасте – у девочек. В младшем школьном возрасте: 7.8% у девочек и 1.6% у мальчиков. С возрастом после первого перенесенного эпизода ИМВП возрастает относительный риск развития рецидива.

Мы уже поговорили о внебольничных инфекциях мочевыводящих путей, сегодня пришла очередь поговорить о нозокомиальных и так называемых осложненных (хотя нозокомиальные являются их частным случаем).
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Мы уже поговорили о внебольничных инфекциях мочевыводящих путей, сегодня пришла очередь поговорить о нозокомиальных и так называемых осложненных (хотя нозокомиальные являются их частным случаем). Конечно, лечение всех этих состояний находится в ведении профильных специалистов (коим эта статья, скорее всего, неактуальна), но, увы, не в каждой больнице они есть, да и предварительный диагноз ставить все равно нужно нам. Актуальность темы также вызвана и тем, что сейчас лето, и оно на редкость жаркое на европейской территории нашей страны, а потому все это безобразие попало в максимально комфортные для себя условия, когда тепло, темно и сыро.
Для начала определимся в терминологии, чтобы в дальнейшем не запутаться.
Вспомним, что внебольничные инфекции мы разобрали тут. Они, как мы помним, относятся к довольно быстро, при должном навыке, излечимым состояниям. Лечить их относительно несложно, так как флора дикая и непуганая, а схемы антибактериальной терапии относятся к справочному материалу.
Другое дело осложненные инфекции мочевыводящих путей и их частный случай – нозокомиальные. Тут все сразу все сложно, начиная с возбудителей, заканчивая методами лечения. Начнем традиционно с микробиологических аспектов.
Если вы помните, то основными возбудителями внебольничных уроинфекций были кишечные палочки. Назначаешь практически не глядя антибиотик, к которому данная палка чувствительна, пара-тройка дней – и пациент практически здоров, но тут начинается война за длительность обязательного приема препарата. И вот эта самая война, в случае проигрыша врача и некоторых обстоятельств со стороны пациента, доводит последнего до осложнений. Но обо всем по порядку.
Итак, главными возбудителями осложненных уроинфекций являются:
- Семейство Enterobacteriaceae (Proteus spp., Klebsiella spp., Morganella spp., Serratia spp.)
- Pseudomonasaeruginosa, она же синегнойная палочка
- Семейство Acinetobacter
На вторых ролях находятся:
- Метициллин-резистентные стафилококки (MRSA), хотя в случае развития карбункула почки он играет главнейшую роль
- Семейство Enterococcus (включая ванкомицин-резистентные)
- Семейство Candida
Но главное, что необходимо помнить, – чаще всего случаи осложненных инфекций, и особенно нозокомиальных, носят полимикробный характер, особенно когда пациенту установлен постоянный мочевой катетер.
Клинические аспекты
Что влияет на возможность развития осложнений? Все как везде – особенности со стороны пациента, особенности со стороны оказания медицинской помощи, особенности окружающей пациента среды.
Особенностями со стороны пациента являются:
- Возраст – чем старше пациент, тем риск осложнений выше.
- Пол – у мужчин все сильно сложнее в виду анатомии мочевыводящих путей, а также с возрастом и с развитием аденомы простаты.
- Наличие сопутствующих заболеваний – сахарный диабет, ВИЧ, онкозаболевание или аутоиммунное заболевание с применением иммуносупрессивной терапии.
- Наличие конкрементов, стриктур и т. п. в мочевыводящих путях, ведущее к трудностям в консервативной терапии и требующее хирургического лечения.
- Наличие заболеваний, которые поддерживают персистирование возбудителей, но не могут быть полностью удалены, – постоянный мочевой катетер, аномалии почки и т. п.
Со стороны окружающей среды – тепло, темно и сыро, то есть подгузники, прокладки, одноразовые пеленки и тому подобные предметы ухода, не меняющиеся в нормативные интервалы времени. И вот тут-то и выходят на первый план представители семейства Enterobacteriaceae, хотя синегнойка это все тоже очень любит. Кроме того, надо обязательно запомнить, что имеют место локальные факторы. Возбудители осложненных, особенно внутрибольничных, уроинфекций будут разными даже в разных корпусах одного и того же стационара (если, конечно, между ними не ходит один и тот же сотрудник, выполняющий одни и те же манипуляции, но тут отловить и победить, точнее, убедить руки мыть, станет намного проще), не говоря уж о разных больницах одного города и уж тем более разных городов, областей и тому подобных административных образований. А потому нужно что? Правильно, проводить локальный микробиологический мониторинг, тем более что сейчас, не прошло и 15 лет, появились автоматизированные, в том числе и облачные системы, упрощающие эту деятельность – и не надо ничего самим придумывать, например, Excel’евские таблички размером километр на километр рисовать. Частным примером является продукт, который представили на прошлом, еще осеннем, МАКМАХ 2020 – AMRCloud, оно же AntiMicrobial Resistance Cloud. Подробности можно прочитать здесь.
Как проявляются осложненные уроинфекции:
- Острый осложненный цистит как следствие установки катетера, в том числе постоянного, или диагностический исследований (то есть как результат нарушений правил асептики и антисептики при выполнении манипуляций).
- Осложненный пиелонефрит как следствие мочекаменной болезни (камни всегда являются инфицированными, более того, носителями биопленок), аденомы простаты и опухолей. Выше мы уже говорили, что данные обстоятельства затрудняют отток мочи, и особенно сей факт актуален для мужчин и лиц пожилого возраста. Основным возбудителем будет наша любимая E.coli, правда, уже вооруженная некоторыми факторами резистентности, и в дальнейшем все будет зависеть от длительности проводимой терапии, ее успешности и устранения факторов, препятствующих оттоку мочи.
- Хронический пиелонефрит является логическим продолжением осложненного, у него даже возбудитель тот же самый – E.coli, которая в этой ситуации уже вооружена до зубов всеми возможными факторами резистентности, так как пациент прошел не два и даже не пять курсов антимикробной терапии. Плохо то, что помимо возникающих обострений хронический пиелонефрит умеет переходить в уросепсис, и чаще всего такой переход бывает у лежачих или ограниченных в движении больных. Этот больной либо не в состоянии чувствовать происходящие с ним изменения, либо не в состоянии об этом сказать, и тогда на выручку придут невербальные признаки боли, например, развитие сгибательных контрактур нижних конечностей. Так что как только вы заметили, что пациент изменил положение в кровати, причем настолько длительно, что ноги разогнуть практически невозможно, необходимо взять полный набор анализов, хотя бы ради подстраховки, тем более что чаще всего данное состояние развивается очень медленно, а развернутая картина может появиться за дни, если не часы до летального исхода.
- Инфекции, связанные с медицинским вмешательством (они же нозокомиальные, они же внутрибольничные, они же госпитальные)– всегда связаны с нарушением правил асептики и антисептики при проведении процедур или манипуляций, а также с использованием открытых дренажных систем для отвода мочи. Возбудители могут быть самыми разными – что на руках принесем, то и будет, но впереди планеты всей, конечно, синегнойка и Enterobacteriaceaespp. Про руки написали уже два раза, повторяться не будем, а про катетеры все же упомянем. Использование открытой системы почти гарантированно приведет к развитию инфекции максимум через неделю после ее установки (минимальные сроки – это 3-4 дня), все придется удалять, лечить, снова устанавливать, что ужасно неудобно как больному, так и его родственникам, поэтому в общих интересах использовать закрытые системы, а в случае длительной их установки крайне тщательно обучать родственников уходу за оными.
Что делать, если все же такой пациент появился? Чтобы не инфицировать всех остальных, потребуется изоляция, которая в первую очередь нас будет мотивировать более тщательно соблюдать меры по асептике и антисептике.
Диагностические аспекты
- Локальный микробиологический мониторинг. Учитывая довольно высокий уровень смертности от уросепсиса, особенно нозокомиального, его проще предупредить, чем с ним бороться, а для этого надо знать врагов в лицо и на старте предполагать, кто это может быть.
- Лабораторная диагностика – ищем признаки воспаления, либо его усиления всеми доступными и возможными методами – общие анализы, C-реактивный белок, прокальцитонин, и т. д. и т. п., всем, чем владеете, то и надо использовать.
- Микробиологическая диагностика должна проводиться в идеале автоматизированными методами, так как чем дольше пациент получает не тот препарат, тем хуже для него и его микрофлоры. А чтобы эмпирику назначить верно, смотрим пункт первый – локальный мониторинг.
Терапевтические аспекты
- Если есть факторы, усложняющие эвакуацию мочи, и они устранимы – обязательно устраняем, иначе все пойдет на второй и третий круг, далее хронизация процесса, а потом… Но не будем повторяться.
- Препаратами выбора остаются фторхинолоны, цефалоспорины четвертого поколения и карбопенемы. В случае панрезистентности включаем тяжелую артиллерию в виде препаратов глубочайшего резерва, таких как цефтазидим/авибактам и тому подобных монстров, хотя самостоятельно этого делать не советуем, сразу зовите клин. фарма.
- В случае развития обструкции мочевых путей переводим пациента в хирургическое отделение для решения вопроса об оперативном лечении.
Подводя итоги, повторим, что в случае развития внутрибольничных инфекций мы всегда обязаны опираться на данные локального мониторинга, мероприятия по асептике и антисептике удваивать, а то и утраивать, но вообще-то призывать уполномоченных разбираться со всем этим лиц в лице эпидемиолога и клинического фармаколога, а самим не забывать мыть руки и максимально четко исполнять требования СанПина, так как все эти правила написаны кровью.

Мы уже поговорили о внебольничных инфекциях мочевыводящих путей, сегодня пришла очередь поговорить о нозокомиальных и так называемых осложненных (хотя нозокомиальные являются их частным случаем).
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Мы уже поговорили о внебольничных инфекциях мочевыводящих путей, сегодня пришла очередь поговорить о нозокомиальных и так называемых осложненных (хотя нозокомиальные являются их частным случаем). Конечно, лечение всех этих состояний находится в ведении профильных специалистов (коим эта статья, скорее всего, неактуальна), но, увы, не в каждой больнице они есть, да и предварительный диагноз ставить все равно нужно нам. Актуальность темы также вызвана и тем, что сейчас лето, и оно на редкость жаркое на европейской территории нашей страны, а потому все это безобразие попало в максимально комфортные для себя условия, когда тепло, темно и сыро.
Для начала определимся в терминологии, чтобы в дальнейшем не запутаться.
Вспомним, что внебольничные инфекции мы разобрали тут. Они, как мы помним, относятся к довольно быстро, при должном навыке, излечимым состояниям. Лечить их относительно несложно, так как флора дикая и непуганая, а схемы антибактериальной терапии относятся к справочному материалу.
Другое дело осложненные инфекции мочевыводящих путей и их частный случай – нозокомиальные. Тут все сразу все сложно, начиная с возбудителей, заканчивая методами лечения. Начнем традиционно с микробиологических аспектов.
Если вы помните, то основными возбудителями внебольничных уроинфекций были кишечные палочки. Назначаешь практически не глядя антибиотик, к которому данная палка чувствительна, пара-тройка дней – и пациент практически здоров, но тут начинается война за длительность обязательного приема препарата. И вот эта самая война, в случае проигрыша врача и некоторых обстоятельств со стороны пациента, доводит последнего до осложнений. Но обо всем по порядку.
Итак, главными возбудителями осложненных уроинфекций являются:
- Семейство Enterobacteriaceae (Proteus spp., Klebsiella spp., Morganella spp., Serratia spp.)
- Pseudomonasaeruginosa, она же синегнойная палочка
- Семейство Acinetobacter
На вторых ролях находятся:
- Метициллин-резистентные стафилококки (MRSA), хотя в случае развития карбункула почки он играет главнейшую роль
- Семейство Enterococcus (включая ванкомицин-резистентные)
- Семейство Candida
Но главное, что необходимо помнить, – чаще всего случаи осложненных инфекций, и особенно нозокомиальных, носят полимикробный характер, особенно когда пациенту установлен постоянный мочевой катетер.
Клинические аспекты
Что влияет на возможность развития осложнений? Все как везде – особенности со стороны пациента, особенности со стороны оказания медицинской помощи, особенности окружающей пациента среды.
Особенностями со стороны пациента являются:
- Возраст – чем старше пациент, тем риск осложнений выше.
- Пол – у мужчин все сильно сложнее в виду анатомии мочевыводящих путей, а также с возрастом и с развитием аденомы простаты.
- Наличие сопутствующих заболеваний – сахарный диабет, ВИЧ, онкозаболевание или аутоиммунное заболевание с применением иммуносупрессивной терапии.
- Наличие конкрементов, стриктур и т. п. в мочевыводящих путях, ведущее к трудностям в консервативной терапии и требующее хирургического лечения.
- Наличие заболеваний, которые поддерживают персистирование возбудителей, но не могут быть полностью удалены, – постоянный мочевой катетер, аномалии почки и т. п.
Со стороны окружающей среды – тепло, темно и сыро, то есть подгузники, прокладки, одноразовые пеленки и тому подобные предметы ухода, не меняющиеся в нормативные интервалы времени. И вот тут-то и выходят на первый план представители семейства Enterobacteriaceae, хотя синегнойка это все тоже очень любит. Кроме того, надо обязательно запомнить, что имеют место локальные факторы. Возбудители осложненных, особенно внутрибольничных, уроинфекций будут разными даже в разных корпусах одного и того же стационара (если, конечно, между ними не ходит один и тот же сотрудник, выполняющий одни и те же манипуляции, но тут отловить и победить, точнее, убедить руки мыть, станет намного проще), не говоря уж о разных больницах одного города и уж тем более разных городов, областей и тому подобных административных образований. А потому нужно что? Правильно, проводить локальный микробиологический мониторинг, тем более что сейчас, не прошло и 15 лет, появились автоматизированные, в том числе и облачные системы, упрощающие эту деятельность – и не надо ничего самим придумывать, например, Excel’евские таблички размером километр на километр рисовать. Частным примером является продукт, который представили на прошлом, еще осеннем, МАКМАХ 2020 – AMRCloud, оно же AntiMicrobial Resistance Cloud. Подробности можно прочитать здесь.
Как проявляются осложненные уроинфекции:
- Острый осложненный цистит как следствие установки катетера, в том числе постоянного, или диагностический исследований (то есть как результат нарушений правил асептики и антисептики при выполнении манипуляций).
- Осложненный пиелонефрит как следствие мочекаменной болезни (камни всегда являются инфицированными, более того, носителями биопленок), аденомы простаты и опухолей. Выше мы уже говорили, что данные обстоятельства затрудняют отток мочи, и особенно сей факт актуален для мужчин и лиц пожилого возраста. Основным возбудителем будет наша любимая E.coli, правда, уже вооруженная некоторыми факторами резистентности, и в дальнейшем все будет зависеть от длительности проводимой терапии, ее успешности и устранения факторов, препятствующих оттоку мочи.
- Хронический пиелонефрит является логическим продолжением осложненного, у него даже возбудитель тот же самый – E.coli, которая в этой ситуации уже вооружена до зубов всеми возможными факторами резистентности, так как пациент прошел не два и даже не пять курсов антимикробной терапии. Плохо то, что помимо возникающих обострений хронический пиелонефрит умеет переходить в уросепсис, и чаще всего такой переход бывает у лежачих или ограниченных в движении больных. Этот больной либо не в состоянии чувствовать происходящие с ним изменения, либо не в состоянии об этом сказать, и тогда на выручку придут невербальные признаки боли, например, развитие сгибательных контрактур нижних конечностей. Так что как только вы заметили, что пациент изменил положение в кровати, причем настолько длительно, что ноги разогнуть практически невозможно, необходимо взять полный набор анализов, хотя бы ради подстраховки, тем более что чаще всего данное состояние развивается очень медленно, а развернутая картина может появиться за дни, если не часы до летального исхода.
- Инфекции, связанные с медицинским вмешательством (они же нозокомиальные, они же внутрибольничные, они же госпитальные)– всегда связаны с нарушением правил асептики и антисептики при проведении процедур или манипуляций, а также с использованием открытых дренажных систем для отвода мочи. Возбудители могут быть самыми разными – что на руках принесем, то и будет, но впереди планеты всей, конечно, синегнойка и Enterobacteriaceaespp. Про руки написали уже два раза, повторяться не будем, а про катетеры все же упомянем. Использование открытой системы почти гарантированно приведет к развитию инфекции максимум через неделю после ее установки (минимальные сроки – это 3-4 дня), все придется удалять, лечить, снова устанавливать, что ужасно неудобно как больному, так и его родственникам, поэтому в общих интересах использовать закрытые системы, а в случае длительной их установки крайне тщательно обучать родственников уходу за оными.
Что делать, если все же такой пациент появился? Чтобы не инфицировать всех остальных, потребуется изоляция, которая в первую очередь нас будет мотивировать более тщательно соблюдать меры по асептике и антисептике.
Диагностические аспекты
- Локальный микробиологический мониторинг. Учитывая довольно высокий уровень смертности от уросепсиса, особенно нозокомиального, его проще предупредить, чем с ним бороться, а для этого надо знать врагов в лицо и на старте предполагать, кто это может быть.
- Лабораторная диагностика – ищем признаки воспаления, либо его усиления всеми доступными и возможными методами – общие анализы, C-реактивный белок, прокальцитонин, и т. д. и т. п., всем, чем владеете, то и надо использовать.
- Микробиологическая диагностика должна проводиться в идеале автоматизированными методами, так как чем дольше пациент получает не тот препарат, тем хуже для него и его микрофлоры. А чтобы эмпирику назначить верно, смотрим пункт первый – локальный мониторинг.
Терапевтические аспекты
- Если есть факторы, усложняющие эвакуацию мочи, и они устранимы – обязательно устраняем, иначе все пойдет на второй и третий круг, далее хронизация процесса, а потом… Но не будем повторяться.
- Препаратами выбора остаются фторхинолоны, цефалоспорины четвертого поколения и карбопенемы. В случае панрезистентности включаем тяжелую артиллерию в виде препаратов глубочайшего резерва, таких как цефтазидим/авибактам и тому подобных монстров, хотя самостоятельно этого делать не советуем, сразу зовите клин. фарма.
- В случае развития обструкции мочевых путей переводим пациента в хирургическое отделение для решения вопроса об оперативном лечении.
Подводя итоги, повторим, что в случае развития внутрибольничных инфекций мы всегда обязаны опираться на данные локального мониторинга, мероприятия по асептике и антисептике удваивать, а то и утраивать, но вообще-то призывать уполномоченных разбираться со всем этим лиц в лице эпидемиолога и клинического фармаколога, а самим не забывать мыть руки и максимально четко исполнять требования СанПина, так как все эти правила написаны кровью.
Инфекции мочевыводящих путей (ИМП) в большинстве стран мира — одна из наиболее актуальных проблем. Так, в США ИМП становятся причиной обращения к врачу 7 миллионов пациентов в год, а для миллиона пациентов являются причиной госпитализации [9]. Особую категорию ИМП составляют осложненные инфекции. Согласно современной классификации, к осложненным инфекциям мочевыводящих путей (ОИМП) относятся заболевания, объединенные наличием функциональных или анатомических аномалий верхних или нижних мочевых путей или протекающие на фоне заболеваний, снижающих общий иммунный статус.
Необходимо отметить, что группа ОИМП представлена крайне разнородными заболеваниями: от тяжелого пиелонефрита с явлениями обструкции и угрозой развития уросепсиса до катетер-ассоциированных инфекций МВП, которые могут исчезнуть самостоятельно после извлечения катетера.
Причины возникновения осложненных ИМП
Наиболее часто встречающиеся причины возникновения ОИМП приведены в табл. 1 [5].
Нарушения уродинамики вследствие обструкции МВП
На основании данных можно сделать вывод, что в большинстве случаев причиной осложненного течения ИМП становятся нарушения уродинамики по обструктивному типу при камнях различной локализации, стриктурах мочеточника и лоханочно-мочеточникового сегмента, инфравезикальной обструкции. Восстановление нормальной уродинамики является краеугольным камнем лечения любой мочевой инфекции. В тех случаях, когда причина возникновения обструкции не может быть ликвидирована немедленно, следует прибегать к дренированию верхних мочевых путей нефростомическим дренажем, а в случае инфравезикальной обструкции — к дренированию мочевого пузыря цистостомическим дренажем. Обе операции предпочтительно выполнять чрезкожно под ультразвуковым контролем.
Инородные тела МВП
Часто причиной осложнений при ИМП становятся инородные тела в мочевыводящих путях: конкременты почек и мочевого пузыря, различные дренажи. Лечение подобных инфекций длительное и подчас малоэффективное. Причина кроется в образовании на поверхности инородных тел микробной пленки, которая состоит из связанных между собой и с какой-либо поверхностью микроорганизмов, находящихся в различных фазах роста, их внеклеточных продуктов, соматических клеток, органического и неорганического материала [1].
Биопленка может быть ассоциирована не только с поверхностью дренажных трубок и конкрементов, но и с рубцово-измененными и некротизированными тканями, присутствующими в просвете мочевыводящих путей после предшествующих оперативных вмешательств. Так или иначе, но большинство осложняющих факторов благоприятствуют образованию биопленок. Бактерии, формирующие биопленку, значительно отличаются от планктонных свободно плавающих микробных клеток, не говоря уже о культуре микроорганизмов, использующейся для лабораторных тестов. Доза антибиотика, бактерицидная в отношении возбудителя в лабораторных условиях, зачастую не оказывает на биопленку никакого воздействия; кроме того, бактерии в биопленке более устойчивы к факторам окружающей среды. Вышесказанное свидетельствует о том, что именно биопленка в итоге является основной причиной возникновения трудностей, которые часто сопровождают лечение осложненной хронической персистирующей инфекции мочевыводящих путей.
Нейрогенные нарушения мочеиспускания
К заболеваниям, нарушающим нормальную уродинамику и осложняющим течение ИМП, относятся и нейрогенные нарушения мочеиспускания. Рассчитывать на успех лечения ИМП можно только после коррекции нейрогенных нарушений и восстановления нормальной уродинамики.
Сопутствующие заболевания
Особую группу составляют осложняющие факторы, связанные с наличием сопутствующих тяжелых заболеваний. Список этих заболеваний является предметом обсуждения, однако некоторые нозологии могут быть внесены в него без колебаний. Это заболевания, обусловливающие общее снижение иммунологической реактивности организма: сахарный диабет, иммунодефицитные состояния. К фоновым заболеваниям, значительно осложняющим течение ИМП, относятся также серповидно-клеточная анемия, почечная и печеночно-почечная недостаточность.
Катетер-ассоциированные ИМП
Факторы риска развития ОИМП
Помимо причин, обусловливающих возникновение ОИМП, существует ряд факторов риска развития этого состояния (табл. 3) [5].
Серьезную проблему для выбора эффективной терапии представляет сочетание ОИМП с хроническим простатитом. Хронический простатит — одно из самых трудных для диагностики и лечения заболеваний в урологии. Любое повышение внутриуретрального давления приводит к рефлюксу мочи и содержащихся в ней микроорганизмов в протоки периферической зоны в обход протоков центральной зоны предстательной железы, соустье которых с уретрой по своей природе почти клапанное. При несостоятельности внутреннего сфинктера нейрогенного происхождения или резекции шейки мочевого пузыря ткань простаты подвергается постоянному риску инфицирования и реинфицирования. Хронический бактериальный простатит характеризуется персистированием преимущественно грамотрицательных бактерий в секрете простаты и рецидивирующими ИМП [1, 3].
Этиология ОИМП
В табл. 2 приведены возбудители, наиболее часто являющиеся причиной возникновения ИМП [7]. Обращает на себя внимание, что на втором и третьем местах после наиболее распространенного возбудителя ИМП — кишечной палочки — при осложненных ИМП находятся Enterococcus spp. и Pseudomonas spp., а при катетер-ассоциированных инфекциях — дрожжевые грибки, отсутствующие при неосложненных ИМП.
Микробиологические особенности осложненных ИМП учитываются при выборе препарата для их лечения.
Лечение ОИМП
Лечение инфекции мочевых путей подразумевает проведение эффективной антибактериальной терапии при условии восстановления нормальной уродинамики и направлено на профилактику уросепсиса и возникновения рецидивов. Исключения составляют катетер-ассоциированные инфекции, в большинстве случаев исчезающие после удаления катетера. Открытым остается вопрос о необходимости антибактериальной терапии у пациентов с асимптоматической бактериурией. Большинство урологов считают, что лечение в подобных ситуациях не показано.
Дополнительной проблемой, значительно усложняющей лечение ОИМП, является высокая устойчивость микроорганизмов к большинству антибактериальных препаратов, длительно применяющихся в урологической практике. Госпитализация, неадекватные по длительности курсы лечения и некорректное назначение лекарственных препаратов приводят зачастую к возникновению антибиотико-устойчивых штаммов.
В нашей клинике в случае тяжелых инфекций мочевыводящих путей, а также в послеоперационном периоде после масштабных оперативных вмешательств мы в последнее время применяем новый антимикробный препарат группы фторхинолонов — L-изомер офлоксацина — левофлоксацин (таваник). Подобный выбор при назначении антибактериальной терапии объясняется доказанной способностью препаратов этой группы лучше проникать в биопленку [2, 9].
Поскольку на левофлоксацин приходится практически вся противомикробная активность в рацемической смеси изомеров, его активность in vitro в два раза превышает активность офлоксацина. Биодоступность препарата равняется 99 %, а особенности его фармакокинетики таковы, что 87 % препарата экскретируется с мочой в неизмененном виде [4]. Несмотря на наличие перекрестной устойчивости между левофлоксацином и другими фторхинолонами, некоторые микроорганизмы, устойчивые к хинолонам, могут проявлять чувствительность к левофлоксацину.
В исследованиях in vitro левофлоксацин доказал свою эффективность в отношении E.coli, Enterobacter, Klebsiella, Proteus Mirabilis, Pseudomonas aurugenosa, являющихся наиболее частыми возбудителями осложненной и неосложеннной форм урогенитальной инфекции (табл. 2).
Курс лечения таваником в дозе 250 мг однократно в течение суток на протяжении 10 дней проведен нами у 20 больных. Согласно полученным данным, эффективность и безопасность лечения были признаны хорошими и очень хорошими у 95% пациентов. Сходные результаты приводят в своих работах G. Richard, C. DeAbate et al., применявшие препарат по аналогичной схеме и добившиеся клинического эффекта у 98,1% пациентов [8]. Столь высокие показатели объясняются непродолжительностью применения левофлоксацина в урологической практике, чем и обусловлено отсутствие устойчивых к его действию штаммов микроорганизмов. Надо отметить, что устойчивость к препаратам этой фармакологической группы, связанная со спонтанными мутациями in vitro, встречается крайне редко [9].
Наряду с фторхинолонами в лечении ИМП широко применяются цефалоспорины II поколения (цефуроксим) и особенно III поколения (цефотаксим, цефтазидим и др.), а также карбапенемные антибиотики (имипенем/циластатин, меропенем).
При осложненных инфекциях МВП иногда назначают полусинтетические пенициллины (ампициллин, пиперациллин) и их комбинации с ингибиторами b-лактамаз (ампициллин/сульбактам, пиперациллин/тазобактам), ко-тримоксазол, аминогликозиды (обычно в комбинации с b-лактамами). Однако эффективность этих препаратов при ОИМП прогнозировать достаточно сложно из-за существенных различий в чувствительности возбудителей в зависимости от региона, стационара и источника развития инфекции (внебольничные или госпитальные). Таким образом, при назначении указанных препаратов в ходе терапии ОИМП следует опираться на данные бактериологического исследования мочи и учитывать чувствительность выделенных микроорганизмов.
Препараты нитрофуранового ряда — нефторированные хинолоны (налидиксовая кислота), оксихинолины (5-НОК) — не должны применяться для терапии ОИМП, так как они являются уроантисептиками, то есть создают терапевтическую концентрацию в моче, но не в паренхиме почек.
Длительность курса антибактериальной терапии ОИМП должна составлять не менее 14 дней. Более короткие курсы (7-10 дней) допустимы при назначении фторхинолоновых антибиотиков, выделении высокочувствительного возбудителя и устранении факторов, осложняющих течение ИМП [5].
В заключение хочется подчеркнуть, что лечение инфекций мочевыводящих путей — процесс сложный, длительный и зачастую малоэффективный, поскольку из всего многообразия существующих на сегодня антибактериальных препаратов ни один не обладает достаточно высокой эффективностью в отношении биопленок. Поэтому усилия врачей должны быть направлены преимущественно на профилактику возникновения подобных инфекций.

Количество людей, страдающих заболеваниями мочевыделительной системы, постоянно увеличивается. Сегодня в России примерно 4% населения страдают от подобных болезней, при этом женщины болеют гораздо чаще мужчин. Особенности анатомического строения женской мочевыделительной системы позволяют инфекции практически беспрепятственно проникать в мочевой пузырь.
Пиелонефрит – это неспецифическое воспалительное заболевание почек с поражением канальцевой системы органа, почечной паренхимы и чашечно-лоханочной области. Представляет собой инфекционный процесс, проявляется болью в области поясницы и высокой температурой тела. При остром течении требует срочной госпитализации, без должного лечения приводит к серьезным осложнениям.
Диагностикой и лечением заболевания занимается уролог или нефролог.
Пиелонефрит – что это за болезнь?
Инфекция поражает самый верхний отдел мочевыделительной системы – почки.
С учетом этиологии, течения болезни и площади охвата пиелонефрит может быть:
- первичным или вторичным – самостоятельным или возникшим на фоне предшествующих патологий (аномалий развития, инфекций, травм);
- острым или хроническим – ярко выраженным ил вяло текущим;
- односторонним или двусторонним – с поражением одной или обеих почек.
В 80% случаев острая форма переходит в хроническую, которая в 70% случаев протекает бессимптомно. Очаг инфекции может сохраняться на протяжение всей жизни, даже если пациент не испытывает выраженных симптомов почечной патологии. При этом достаточно незначительного сбоя в работе иммунной системе или ее ослабления, чтобы спровоцировать обострение болезни.
Симптомы пиелонефрита

Острая форма имеет характерную клиническую картину:
При хронической форме признаки пиелонефрита несколько смазаны, симптоматика видоизменена:
- периодические слабо выраженные приступы боли в пояснице;
- частые позывы к мочеиспусканию;
- повышение артериального давления.
При отсутствии лечения хроническая форма приводит к перерождению почечной ткани в соединительную, что приводит к почечной недостаточности.
Причины заболевания
Основная причина – агрессия патогенной или условно-патогенной флоры (протей, кишечная палочка, энтерококки, стафилококки, синегнойная палочка и др.). В абсолютно здоровом организме их активность автоматически подавляет иммунная система. При ее нарушении защитные силы слабеют, и болезнь активизируется.
Факторы развития инфекционного процесса:
У женщин заболевание диагностируют в 3-5 раз чаще, нежели у мужчин.
На заметку! Инфекция может попадать в организм по восходящему пути (через уретру и мочевой пузырь) или используя гематогенный и лимфогенный пути распространения – мигрируя в почки из других очагов инфекции в организме.
Диагностика
Острый пиелонефрит почек требует срочной госпитализации, поэтому основная диагностика проходит в условиях стационара. Помимо общего осмотра с измерением температуры, простукиванием поясничной зоны и пальпацией брюшины, врач назначает инструментальные методы обследования и лабораторные анализы.
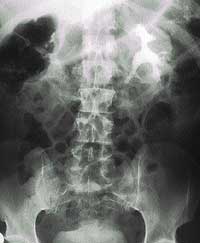
- рентген с контрастом — делают в виде нескольких последовательных снимков – это позволяет оценить форму почечных чашечек и лоханок, выявить характер движения мочи, наличие обструкций в мочеточниках, присутствие камней;
- УЗИ почек – открывает вид на состояние органа в динамике (на мониторе он увеличен в объеме, расширена область лоханок, паренхима имеет повышенную плотность);
- КТ и МРТ дают возможность с высокой точностью изучить не только строение самих почек, но и их сосудистой системы, включая мельчайшие аномалии и обструкции, которые не покажет УЗИ или рентген.
Список лабораторных анализов:
- общий анализ крови – СОЭ, уровень лейкоцитов;
- биохимический анализ крови – уровень креатинина, мочевины, калия;
- серологические анализы на специфические антитела к возбудителю;
- ПЦР-диагностика с выявлением генного материала возбудителей;
- бактериологическое исследование мочи;
- общий анализ мочи с определением физико-химических показателей;
- анализы мочи по Нечипоренко (утренний), Аддис-Каковскому (суточный) Амбурже (трехчасовой) – дают более четкие значения показателей;
- проба по Зимницкому позволяет оценить способность почек фильтровать кровь по концентрации мочи, взятой через каждые 3 часа
Внимание! Любые отклонения уровня калия от естественной фиксированной нормы являются поводом для назначения гемодиализа.
Читайте также:

