Основную долю среди возбудителей внутрибольничных инфекций составляют
Обновлено: 19.04.2024
Ежегодно в США регистрируют около 1,7 млн случаев внутрибольничных инфекций, вызванных микроорганизмами, при этом 99 тыс. из них заканчиваются летально. В развитых странах Европы смертность от внутрибольничных инфекций составляет 25 тыс. случаев в год, из них две трети обусловлены грамотрицательными бактериями. В нашей стране внутрибольничные инфекции в два раза повышают риск летального исхода
Внутрибольничные инфекции
Изучение внутрибольничных инфекций (ВБИ) началось более 150 лет назад, но по-прежнему они остаются серьезной проблемой, приводя к удлинению сроков лечения, хронизации процесса, инвалидности, а в наиболее тяжелых случаях — к смерти больных. Согласно определению ВОЗ, внутрибольничными инфекциями считаются любые клинически выраженные заболевания микробного происхождения, поражающие больного в результате его госпитализации или посещения лечебного учреждения либо возникающие в течение 30 дней после выписки из больницы.
К внутрибольничным инфекциям также относятся инфицирование сотрудников больницы, связанное с их профессиональной деятельностью. Эти болезни отличаются механизмами и факторами передачи, особенностями течения эпидемиологического и инфекционного процессов, а также особой ролью медицинского персонала в возникновении, поддержании и распространении инфекции. Подобные инфекции могут быть обусловлены широким внедрением в практику инструментальных, эндоскопических, биохимических и других методов диагностики, которые сопряжены с нарушением целости покровов тела человека. Проблема в том, что конструкция некоторых медицинских приборов не позволяет произвести их полную стерилизацию после каждой процедуры, оставляя лазейку для проникновения нежелательных микробов во внутреннюю среду организма человека.
Агенты ВБИ
Всего насчитывается более 200 агентов, которые могут быть причиной внутрибольничных инфекций. До появления антибиотиков основными из них были стрептококки и анаэробные палочки. Однако после начала клинического применения антибиотиков возбудителями основных внутрибольничных инфекций стали ранее непатогенные или условно-патогенные микроорганизмы. К ним относятся стафилококки (Staphylococcus aureus, St. epidermidis, St. saprophiticus), стрептококки (Streptococcus spp.), энтерококки (Enterococcus faecalis, Enterococcus durans), эшерихия (Escherichia coli), клебсиелла (Klebsiella spp.), энтеробактер (Enterobacter spp.), протей (Proteus mirabilis), серрация (Serratia marcescens), псевдомонада (Pseudomonas aeruginosa). Нередко встречаются ВБИ, вызываемые Providencia spp., Stenotrophomona smaltophilia, Acinetobacter baumannii, Citrobacter spp., Clostridium difficile и другими микроорганизмами.
Всего насчитывается более 200 агентов, которые могут быть причиной внутрибольничных инфекций
Роль облигатно-патогенных микроорганизмов в развитии внутрибольничных инфекций невелика. В неинфекционных стационарах регистрируют несколько нозологических форм инфекций, вызванных возбудителями этой группы. К ним относятся вирусы гепатитов В, С, D, ВИЧ, гриппа и других ОРВИ, острых кишечных вирусных инфекций, герпеса, цитомегаловирусной инфекции, а также анаэробные клостридии и хламидии.
ВОЗ предупреждает
Эксперты ВОЗ совместно с отделом инфекционных заболеваний при Тюбингенском университете (Германия) назвали 12 бактерий, которые представляют наибольшую опасность для здоровья человека.
В первую критическую группу вошли Acinetobacter baumannii, Pseudomona saeruginosa и Enterobacteriaceae, которые часто выявляют в больницах и домах престарелых, причем заражение ими может привести к развитию смертельных инфекций, например пневмонии и заболеваний крови. Эти бактерии устойчивы к большинству антибиотиков, в том числе карбапенемам и цефалоспоринам.
Основные пути приспособления больничных штаммов — это устойчивость к одному или нескольким антибиотикам широкого спектра действия и снижение чувствительности к антисептикам
Во вторую группу списка ВОЗ включены Enterococcus faecium, Staphylococcus aureus, Helicobacter pylori, Campylobacter spp., Salmonellae и Neisseria gonorrhoeae. К третьей категории отнесены Streptococcus pneumoniae, Haemophilus influenzae и Shigella spp.
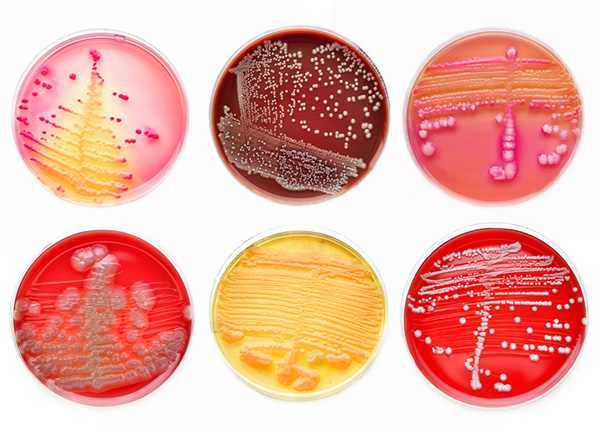
Госпитальные штаммы
Основные пути приспособления больничных штаммов — это устойчивость к одному или нескольким антибиотикам широкого спектра действия и снижение чувствительности к антисептикам. Госпитальные штаммы очень разнообразны, в каждой больнице или отделении возможно появление своего характерного штамма со свойственным только ему набором биологических свойств. При этом популяции возбудителей внутрибольничных инфекций отличаются не только гетерогенностью, но и динамичностью во времени.
Из больниц антибиотикорезистентные штаммы, особенно это касается грамотрицательных бактерий, постепенно начинают распространяться во внебольничную среду.
Эковары
Эковары — это варианты одного вида микроорганизма, которые приспособились к обитанию в определенной экосистеме. В данном случае выделяют больничные и внебольничные эковары. Больничными эковарами люди заражаются в основном во время инъекций, операций, переливания крови, гемосорбции, гемодиализа, мануальных и эндоскопических исследований и др.
Госпитальные инфекции, обусловленные внебольничными эковарами, часто возникают при нарушении целости покровов тела на фоне общего снижения иммунитета. Возбудители инфекций проникают во внутреннюю среду организма при повреждении слизистых оболочек, через ожоги, травматические раны, открытые гнойно-воспалительные очаги.
Устойчивые к большинству антибиотиков штаммы золотистого стафилококка (methicillinresistant Staphylococcus aureus — MRSA) стали настоящим бичом больниц. Несмотря на все усилия, ликвидировать инфекцию не удается
Больничные эковары способны вызывать госпитальную инфекцию не только при снижении функции иммунной системы, но и при нормальном иммунном ответе после инъекций или операций. Причем инфицирующая доза больничного эковара может быть относительно небольшой. Для появления инфекции, вызванной внебольничным эковаром, кроме снижения иммунитета, необходимо еще два условия: пассивное проникновение возбудителя во внешнюю среду организма и массивная инфицирующая доза.
Генетическая стабильность больничных инфекций Pseudomonas aeruginosa
Прежде считалось, что в больничной среде бактерии изменяются ускоренными темпами, увеличивая таким образом генетическое разнообразие внутрибольничной микрофлоры. Для изучения этого вопроса датские ученые проследили генетические изменения бактерии Pseudomonas aeruginosa, которые произошли с 70-х годов прошлого века в пределах одной из больниц Копенгагена. Для этого они использовали бактериальные штаммы, выделенные в анализах больных муковисцидозом, поскольку Pseudomonas aeruginosa является источником инфекций дыхательных путей, осложняя течение этой болезни.
Хирург и специалист по инфекционным заболеваниям Марк Шпигельман из Университетского колледжа в Лондоне считает, что повышенные требования к гигиене в хирургических клиниках парадоксальным образом способствуют распространению внутрибольничных инфекций
Один вариант штамма в течение 35 лет дал около 200 000 поколений, переходя от одного пациента к другому. В связи с высокой неоднородностью условий и длительным временем можно было бы ожидать широкой генетической диверсификации исходного штамма, но оказалось, что внутрибольничные инфекционные возбудители после периода быстрых адаптаций изменяются относительно мало, скорость мутирования у них низкая и расщепления на отдельные линии не происходит.
Эти наблюдения на первый взгляд кажутся противоречивыми, так как долгая эволюция в нестабильных условиях могла бы способствовать повышению генетического разнообразия. Тем не менее выяснилось, что, несмотря на то что внутренняя среда больного весьма неустойчива и разнородна из-за инфекций и постоянного лечения всевозможными препаратами, эта разнородность не способствует быстрому увеличению генетического разнообразия.
Clostridium difficile
Спорообразующая бактерия Clostridium difficile относится к стойким и трудноискоренимым возбудителям больничных инфекций. Заражение происходит через руки медицинского персонала, например, при измерении ректальной температуры, причем не помогает даже использование индивидуальных чехлов для датчиков.

У получавших антибиотики больных (даже однократно перед операцией) под влиянием токсинов Clostridium difficile возможно развитие псевдомембранозного колита, основным проявлением которого является диарея. У некоторых больных профузная диарея сопровождается интоксикацией, высокой лихорадкой, лейкоцитозом. Если пациент продолжает получать антибиотики вплоть до выписки, то псевдомембранозный колит может начаться дома.
MRSA — повод для изменений правил больничной гигиены
Устойчивые к большинству антибиотиков штаммы золотистого стафилококка (methicillinresistant Staphylococcus aureus — MRSA) стали настоящим бичом больниц. Несмотря на все усилия, ликвидировать инфекцию не удается. Вне больниц бактерия, как правило, теряет активность. Однако в последнее время все чаще отмечают случаи, когда инфекция выходит за пределы медицинских учреждений.
Хирург и специалист по инфекционным заболеваниям Марк Шпигельман из Университетского колледжа в Лондоне считает, что повышенные требования к гигиене в хирургических клиниках парадоксальным образом способствуют распространению внутрибольничных инфекций. При этом он указывает на два принципиальных факта, которые должны объяснить неэффективность борьбы с инфекцией в больницах. Во-первых, избыточные меры гигиены, применяемые в больницах, особенно в хирургических отделениях, уничтожают безвредные бактерии, создавая тем самым среду для заселения бактериями MRSA. Во-вторых, применение антибиотиков с гигиенической целью, в частности использование антибактериального мыла, не только приводит к появлению устойчивых к антибиотикам штаммов, но и активизирует защитные механизмы у бактерий, которые в менее агрессивной среде не действуют.
Как специалист по истории и развитию инфекционных заболеваний в древних человеческих популяциях Марк Шпигельман предлагает предпринять ряд мер по борьбе с инфекцией. Прежде всего надо строго разделить больницы, где используют антибиотики, от тех, где их не применяют (прежде всего это касается хирургических отделений). Разделение должно быть очень жестким. Персонал не должен совмещать работу в больницах разного типа.
В случае необходимости использовать антибиотики в клинике, где они запрещены, больного следует перевести в другое медицинское учреждение. Кроме того, выдвинуто неожиданное предложение по изменению гигиенических процедур. Предлагается вместо антибиотиков при подготовке к операции использовать пробиотики, которые помогут противостоять болезнетворным бактериям.
Внутрибольничные инфекции – различные инфекционные заболевания, заражение которыми произошло в условиях лечебного учреждения. В зависимости от степени распространения различают генерализованные (бактериемию, септицемию, септикопиемию, бактериальный шок) и локализованные формы внутрибольничных инфекций (с поражением кожи и подкожной клетчатки, дыхательной, сердечно-сосудистой, урогенитальной системы, костей и суставов, ЦНС и т. д.). Выявление возбудителей внутрибольничных инфекций проводится с помощью методов лабораторной диагностики (микроскопических, микробиологических, серологических, молекулярно-биологических). При лечении внутрибольничных инфекций используются антибиотики, антисептики, иммуностимуляторы, физиотерапия, экстракорпоральная гемокоррекция и т. д.

Общие сведения
Внутрибольничные (госпитальные, нозокомиальные) инфекции - инфекционные заболевания различной этиологии, возникшие у пациента или медицинского сотрудника в связи с пребыванием в лечебно-профилактическом учреждении. Инфекция считается внутрибольничной, если она развилась не ранее 48 часов после поступления больного в стационар. Распространенность внутрибольничных инфекций (ВБИ) в медицинских учреждениях различного профиля составляет 5-12%. Наибольший удельный вес внутрибольничных инфекций приходится на акушерские и хирургические стационары (отделения реанимации, абдоминальной хирургии, травматологии, ожоговой травмы, урологии, гинекологии, отоларингологии, стоматологии, онкологии и др.). Внутрибольничные инфекции представляют собой большую медико-социальную проблему, поскольку утяжеляют течение основного заболевания, увеличивают длительность лечения в 1,5 раза, а количество летальных исходов - в 5 раз.

Этиология и эпидемиология внутрибольничных инфекций
Основными возбудителями внутрибольничных инфекций (85% от общего числа) выступают условно-патогенные микроорганизмы: грамположительные кокки (эпидермальный и золотистый стафилококк, бета-гемолитический стрептококк, пневмококк, энтерококк) и грамотрицательные палочковидные бактерии (клебсиеллы, эшерихии, энтеробактер, протей, псевдомонады и др.). Кроме этого, в этиологии внутрибольничных инфекций велика удельная роль вирусных возбудителей простого герпеса, аденовирусной инфекции, гриппа, парагриппа, цитомегалии, вирусных гепатитов, респираторно-синцитиальной инфекции, а также риновирусов, ротавирусов, энтеровирусов и пр. Также внутрибольничные инфекции могут быть вызваны условно-патогенными и патогенными грибами (дрожжеподобными, плесневыми, лучистыми). Особенностью внутригоспитальных штаммов условно-патогенных микроорганизмов служит их высокая изменчивость, лекарственная резистентность и устойчивость к воздействию факторов среды (ультрафиолета, дезинфектантов и пр.).
Источниками внутрибольничных инфекций в большинстве случаев выступают пациенты или медицинский персонал, являющиеся бактерионосителями или больными стертыми и манифестными формами патологии. Как показывают исследования, роль третьих лиц (в частности, посетителей стационаров) в распространении ВБИ невелика. Передача различных форм госпитальной инфекции реализуется с помощью воздушно-капельного, фекально-орального, контактного, трансмиссивного механизма. Кроме этого, возможен парентеральный путь передачи внутрибольничной инфекции при проведении различных инвазивных медицинских манипуляций: забора крови, инъекций, вакцинации, инструментальных манипуляций, операций, ИВЛ, гемодиализа и пр. Таким образом в медучреждении возможно заразиться гепатитами В, С и D, гнойно-воспалительными заболеваниями, сифилисом, ВИЧ-инфекцией. Известны случаи внутрибольничных вспышек легионеллеза при приеме больными лечебного душа и вихревых ванн.
Факторами, участвующими в распространении внутрибольничной инфекции, могут выступать контаминированные предметы ухода и обстановки, медицинский инструментарий и аппаратура, растворы для инфузионной терапии, спецодежда и руки медперсонала, изделия медицинского назначения многоразового использования (зонды, катетеры, эндоскопы), питьевая вода, постельные принадлежности, шовный и перевязочный материал и мн. др.
Значимость тех или иных видов внутрибольничной инфекции во многом зависит от профиля лечебного учреждения. Так, в ожоговых отделениях преобладает синегнойная инфекция, которая в основном передается через предметы ухода и руки персонала, а главным источником внутрибольничной инфекции являются сами пациенты. В учреждениях родовспоможения основную проблему представляет стафилококковая инфекция, распространяемая медицинским персоналом-носителем золотистого стафилококка. В урологических отделениях доминирует инфекция, вызываемая грамотрицательной флорой: кишечной, синегнойной палочкой и др. В педиатрических стационарах особую значимость имеет проблема распространения детских инфекций – ветряной оспы, эпидемического паротита, краснухи, кори. Возникновению и распространению внутрибольничной инфекции способствуют нарушение санитарно-эпидемиологического режима ЛПУ (несоблюдение личной гигиены, асептики и антисептики, режима дезинфекции и стерилизации, несвоевременное выявление и изоляция лиц-источников инфекции и т. д.).
К группе риска, в наибольшей степени подверженной развитию внутрибольничной инфекции, относятся новорожденные (особенно недоношенные) и дети раннего возраста; пожилые и ослабленные пациенты; лица, страдающие хроническими заболеваниями (сахарным диабетом, болезнями крови, почечной недостаточностью), иммунодефицитом, онкопатологией. Восприимчивость человека к внутрибольничным инфекциям увеличивается при наличии у него открытых ран, полостных дренажей, внутрисосудистых и мочевых катетеров, трахеостомы и других инвазивных устройств. На частоту возникновения и тяжесть течения внутрибольничной инфекции влияет долгое нахождение пациента в стационаре, длительная антибиотикотерапия, иммуносупрессивная терапия.
Классификация внутрибольничных инфекций
По длительности течения внутрибольничные инфекции делятся на острые, подострые и хронические; по тяжести клинических проявлений – на легкие, среднетяжелые и тяжелые формы. В зависимости от степени распространенности инфекционного процесса различают генерализованные и локализованные формы внутрибольничной инфекции. Генерализованные инфекции представлены бактериемией, септицемией, бактериальным шоком. В свою очередь, среди локализованных форм выделяют:
- инфекции кожи, слизистых и подкожной клетчатки, в т. ч. послеоперационных, ожоговых, травматических ран. В частности, к их числу относятся омфалит, абсцессы и флегмоны, пиодермия, рожа, мастит, парапроктит, грибковые инфекции кожи и др.
- инфекции полости рта (стоматит) и ЛОР-органов (ангина, фарингит, ларингит, эпиглоттит, ринит, синусит, отит, мастоидит)
- инфекции бронхолегочной системы (бронхит, пневмония, плеврит, абсцесс легкого, гангрена легкого, эмпиема плевры, медиастинит)
- инфекции пищеварительной системы (гастрит, энтерит, колит, вирусные гепатиты)
- глазные инфекции (блефарит, конъюнктивит, кератит)
- инфекции урогенитального тракта (бактериурия, уретрит, цистит, пиелонефрит, эндометрит, аднексит)
- инфекции костно-суставной системы (бурсит, артрит, остеомиелит)
- инфекции сердца и сосудов (перикардит, миокардит, эндокардит, тромбофлебиты).
- инфекции ЦНС (абсцесс мозга, менингит, миелит и др.).
Диагностика внутрибольничных инфекций
Критериями, позволяющими думать о развитии внутрибольничной инфекции, служат: возникновение клинических признаков заболевания не ранее чем через 48 часов после поступления в стационар; связь с проведением инвазивного вмешательства; установление источника инфекции и фактора передачи. Окончательное суждение о характере инфекционного процесса получают после идентификации штамма возбудителя с помощью лабораторных методов диагностики.
Для исключения или подтверждения бактериемии проводится бактериологический посев крови на стерильность, желательно не менее 2-3-х раз. При локализованных формах внутрибольничной инфекции микробиологическое выделение возбудителя может быть произведено из других биологических сред, в связи с чем выполняется посев мочи, кала, мокроты, отделяемого ран, материала из зева, мазка с конъюнктивы, из половых путей на микрофлору. Дополнительно к культуральному методу выявления возбудителей внутрибольничных инфекций используются микроскопия, серологические реакции (РСК, РА, ИФА, РИА), вирусологический, молекулярно-биологический (ПЦР) методы.
Лечение внутрибольничных инфекций
Сложности лечения внутрибольничной инфекции обусловлены ее развитием в ослабленном организме, на фоне основной патологии, а также резистентностью госпитальных штаммов к традиционной фармакотерапии. Больные с диагностированными инфекционными процессами подлежат изоляции; в отделении проводится тщательная текущая и заключительная дезинфекция. Выбор противомикробного препарата основывается на особенностях антибиотикограммы: при внутрибольничной инфекции, вызванной грамположительной флорой наиболее эффективен ванкомицин; грамотрицательными микроорганизмами – карбапенемы, цефалоспорины IV поколения, аминогликозиды. Возможно дополнительное применение специфических бактериофагов, иммуностимуляторов, интерферона, лейкоцитарной массы, витаминотерапии.
При необходимости проводится чрескожное облучение крови (ВЛОК, УФОК), экстракорпоральная гемокоррекция (гемосорбция, лимфосорбция). Симптоматическая терапия осуществляется с учетом клинической формы внутрибольничной инфекции с участием специалистов соответствующего профиля: хирургов, травматологов, пульмонологов, урологов, гинекологов и др.
Профилактика внутрибольничных инфекций
Основные меры профилактики внутрибольничных инфекций сводятся к соблюдению санитарно-гигиенических и противоэпидемических требований. В первую очередь, это касается режима дезинфекции помещений и предметов ухода, применения современных высокоэффективных антисептиков, проведения качественной предстерилизационной обработки и стерилизации инструментария, безукоснительного следования правилам асептики и антисептики.
Медицинский персонал должен соблюдать меры индивидуальной защиты при проведении инвазивных процедур: работать в резиновых перчатках, защитных очках и маске; осторожно обращаться с медицинским инструментарием. Большое значение в профилактике внутрибольничных инфекций имеет вакцинация медработников от гепатита В, краснухи, гриппа, дифтерии, столбняка и других инфекций. Все сотрудники ЛПУ подлежат регулярному плановому диспансерному обследованию, направленному на выявление носительства патогенов. Предупредить возникновение и распространение внутрибольничных инфекций позволит сокращение сроков госпитализации пациентов, рациональная антибиотикотерапия, обоснованность проведения инвазивных диагностических и лечебных процедур, эпидемиологический контроль в ЛПУ.
Ежегодно в США регистрируют около 1,7 млн случаев внутрибольничных инфекций, вызванных микроорганизмами, при этом 99 тыс. из них заканчиваются летально. В развитых странах Европы смертность от внутрибольничных инфекций составляет 25 тыс. случаев в год, из них две трети обусловлены грамотрицательными бактериями. В нашей стране внутрибольничные инфекции в два раза повышают риск летального исхода
Внутрибольничные инфекции
Изучение внутрибольничных инфекций (ВБИ) началось более 150 лет назад, но по-прежнему они остаются серьезной проблемой, приводя к удлинению сроков лечения, хронизации процесса, инвалидности, а в наиболее тяжелых случаях — к смерти больных. Согласно определению ВОЗ, внутрибольничными инфекциями считаются любые клинически выраженные заболевания микробного происхождения, поражающие больного в результате его госпитализации или посещения лечебного учреждения либо возникающие в течение 30 дней после выписки из больницы.
К внутрибольничным инфекциям также относятся инфицирование сотрудников больницы, связанное с их профессиональной деятельностью. Эти болезни отличаются механизмами и факторами передачи, особенностями течения эпидемиологического и инфекционного процессов, а также особой ролью медицинского персонала в возникновении, поддержании и распространении инфекции. Подобные инфекции могут быть обусловлены широким внедрением в практику инструментальных, эндоскопических, биохимических и других методов диагностики, которые сопряжены с нарушением целости покровов тела человека. Проблема в том, что конструкция некоторых медицинских приборов не позволяет произвести их полную стерилизацию после каждой процедуры, оставляя лазейку для проникновения нежелательных микробов во внутреннюю среду организма человека.
Агенты ВБИ
Всего насчитывается более 200 агентов, которые могут быть причиной внутрибольничных инфекций. До появления антибиотиков основными из них были стрептококки и анаэробные палочки. Однако после начала клинического применения антибиотиков возбудителями основных внутрибольничных инфекций стали ранее непатогенные или условно-патогенные микроорганизмы. К ним относятся стафилококки (Staphylococcus aureus, St. epidermidis, St. saprophiticus), стрептококки (Streptococcus spp.), энтерококки (Enterococcus faecalis, Enterococcus durans), эшерихия (Escherichia coli), клебсиелла (Klebsiella spp.), энтеробактер (Enterobacter spp.), протей (Proteus mirabilis), серрация (Serratia marcescens), псевдомонада (Pseudomonas aeruginosa). Нередко встречаются ВБИ, вызываемые Providencia spp., Stenotrophomona smaltophilia, Acinetobacter baumannii, Citrobacter spp., Clostridium difficile и другими микроорганизмами.
Всего насчитывается более 200 агентов, которые могут быть причиной внутрибольничных инфекций
Роль облигатно-патогенных микроорганизмов в развитии внутрибольничных инфекций невелика. В неинфекционных стационарах регистрируют несколько нозологических форм инфекций, вызванных возбудителями этой группы. К ним относятся вирусы гепатитов В, С, D, ВИЧ, гриппа и других ОРВИ, острых кишечных вирусных инфекций, герпеса, цитомегаловирусной инфекции, а также анаэробные клостридии и хламидии.
ВОЗ предупреждает
Эксперты ВОЗ совместно с отделом инфекционных заболеваний при Тюбингенском университете (Германия) назвали 12 бактерий, которые представляют наибольшую опасность для здоровья человека.
В первую критическую группу вошли Acinetobacter baumannii, Pseudomona saeruginosa и Enterobacteriaceae, которые часто выявляют в больницах и домах престарелых, причем заражение ими может привести к развитию смертельных инфекций, например пневмонии и заболеваний крови. Эти бактерии устойчивы к большинству антибиотиков, в том числе карбапенемам и цефалоспоринам.
Основные пути приспособления больничных штаммов — это устойчивость к одному или нескольким антибиотикам широкого спектра действия и снижение чувствительности к антисептикам
Во вторую группу списка ВОЗ включены Enterococcus faecium, Staphylococcus aureus, Helicobacter pylori, Campylobacter spp., Salmonellae и Neisseria gonorrhoeae. К третьей категории отнесены Streptococcus pneumoniae, Haemophilus influenzae и Shigella spp.

Госпитальные штаммы
Основные пути приспособления больничных штаммов — это устойчивость к одному или нескольким антибиотикам широкого спектра действия и снижение чувствительности к антисептикам. Госпитальные штаммы очень разнообразны, в каждой больнице или отделении возможно появление своего характерного штамма со свойственным только ему набором биологических свойств. При этом популяции возбудителей внутрибольничных инфекций отличаются не только гетерогенностью, но и динамичностью во времени.
Из больниц антибиотикорезистентные штаммы, особенно это касается грамотрицательных бактерий, постепенно начинают распространяться во внебольничную среду.
Эковары
Эковары — это варианты одного вида микроорганизма, которые приспособились к обитанию в определенной экосистеме. В данном случае выделяют больничные и внебольничные эковары. Больничными эковарами люди заражаются в основном во время инъекций, операций, переливания крови, гемосорбции, гемодиализа, мануальных и эндоскопических исследований и др.
Госпитальные инфекции, обусловленные внебольничными эковарами, часто возникают при нарушении целости покровов тела на фоне общего снижения иммунитета. Возбудители инфекций проникают во внутреннюю среду организма при повреждении слизистых оболочек, через ожоги, травматические раны, открытые гнойно-воспалительные очаги.
Устойчивые к большинству антибиотиков штаммы золотистого стафилококка (methicillinresistant Staphylococcus aureus — MRSA) стали настоящим бичом больниц. Несмотря на все усилия, ликвидировать инфекцию не удается
Больничные эковары способны вызывать госпитальную инфекцию не только при снижении функции иммунной системы, но и при нормальном иммунном ответе после инъекций или операций. Причем инфицирующая доза больничного эковара может быть относительно небольшой. Для появления инфекции, вызванной внебольничным эковаром, кроме снижения иммунитета, необходимо еще два условия: пассивное проникновение возбудителя во внешнюю среду организма и массивная инфицирующая доза.
Генетическая стабильность больничных инфекций Pseudomonas aeruginosa
Прежде считалось, что в больничной среде бактерии изменяются ускоренными темпами, увеличивая таким образом генетическое разнообразие внутрибольничной микрофлоры. Для изучения этого вопроса датские ученые проследили генетические изменения бактерии Pseudomonas aeruginosa, которые произошли с 70-х годов прошлого века в пределах одной из больниц Копенгагена. Для этого они использовали бактериальные штаммы, выделенные в анализах больных муковисцидозом, поскольку Pseudomonas aeruginosa является источником инфекций дыхательных путей, осложняя течение этой болезни.
Хирург и специалист по инфекционным заболеваниям Марк Шпигельман из Университетского колледжа в Лондоне считает, что повышенные требования к гигиене в хирургических клиниках парадоксальным образом способствуют распространению внутрибольничных инфекций
Один вариант штамма в течение 35 лет дал около 200 000 поколений, переходя от одного пациента к другому. В связи с высокой неоднородностью условий и длительным временем можно было бы ожидать широкой генетической диверсификации исходного штамма, но оказалось, что внутрибольничные инфекционные возбудители после периода быстрых адаптаций изменяются относительно мало, скорость мутирования у них низкая и расщепления на отдельные линии не происходит.
Эти наблюдения на первый взгляд кажутся противоречивыми, так как долгая эволюция в нестабильных условиях могла бы способствовать повышению генетического разнообразия. Тем не менее выяснилось, что, несмотря на то что внутренняя среда больного весьма неустойчива и разнородна из-за инфекций и постоянного лечения всевозможными препаратами, эта разнородность не способствует быстрому увеличению генетического разнообразия.
Clostridium difficile
Спорообразующая бактерия Clostridium difficile относится к стойким и трудноискоренимым возбудителям больничных инфекций. Заражение происходит через руки медицинского персонала, например, при измерении ректальной температуры, причем не помогает даже использование индивидуальных чехлов для датчиков.

У получавших антибиотики больных (даже однократно перед операцией) под влиянием токсинов Clostridium difficile возможно развитие псевдомембранозного колита, основным проявлением которого является диарея. У некоторых больных профузная диарея сопровождается интоксикацией, высокой лихорадкой, лейкоцитозом. Если пациент продолжает получать антибиотики вплоть до выписки, то псевдомембранозный колит может начаться дома.
MRSA — повод для изменений правил больничной гигиены
Устойчивые к большинству антибиотиков штаммы золотистого стафилококка (methicillinresistant Staphylococcus aureus — MRSA) стали настоящим бичом больниц. Несмотря на все усилия, ликвидировать инфекцию не удается. Вне больниц бактерия, как правило, теряет активность. Однако в последнее время все чаще отмечают случаи, когда инфекция выходит за пределы медицинских учреждений.
Хирург и специалист по инфекционным заболеваниям Марк Шпигельман из Университетского колледжа в Лондоне считает, что повышенные требования к гигиене в хирургических клиниках парадоксальным образом способствуют распространению внутрибольничных инфекций. При этом он указывает на два принципиальных факта, которые должны объяснить неэффективность борьбы с инфекцией в больницах. Во-первых, избыточные меры гигиены, применяемые в больницах, особенно в хирургических отделениях, уничтожают безвредные бактерии, создавая тем самым среду для заселения бактериями MRSA. Во-вторых, применение антибиотиков с гигиенической целью, в частности использование антибактериального мыла, не только приводит к появлению устойчивых к антибиотикам штаммов, но и активизирует защитные механизмы у бактерий, которые в менее агрессивной среде не действуют.
Как специалист по истории и развитию инфекционных заболеваний в древних человеческих популяциях Марк Шпигельман предлагает предпринять ряд мер по борьбе с инфекцией. Прежде всего надо строго разделить больницы, где используют антибиотики, от тех, где их не применяют (прежде всего это касается хирургических отделений). Разделение должно быть очень жестким. Персонал не должен совмещать работу в больницах разного типа.
В случае необходимости использовать антибиотики в клинике, где они запрещены, больного следует перевести в другое медицинское учреждение. Кроме того, выдвинуто неожиданное предложение по изменению гигиенических процедур. Предлагается вместо антибиотиков при подготовке к операции использовать пробиотики, которые помогут противостоять болезнетворным бактериям.
Важнейшая тема – как для нас, врачей, так и для наших пациентов – внутрибольничное инфицирование, точнее, методы его профилактики. Поговорим об этом более подробно.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: врач – клинический фармаколог Трубачева Е.С.

Давайте посмотрим на проблему более конкретно, тем более, что от нее напрямую зависит жизнь самых тяжелых и сложных пациентов. Предупредим сразу, теоретическую часть вопроса вы можете прочитать в огромном количестве публикаций научного и научно-популярного характера. Мы поговорим как врачи-практики, что и откуда берется, и как от этого избавиться.
Итак, первое и основное, что уже неоднократно сказано, но что необходимо запомнить, – МИКРОБЫ, ВЫЗЫВАЮЩИЕ ВБИ, НЕ УМЕЮТ НИ ЛЕТАТЬ, НИ ХОДИТЬ, НИ ПОЛЗАТЬ, и оказываются в организме пациента только с нашей медицинской помощью, потому эти состоянии и названы – инфекции, связанные с медицинским вмешательством. А под вмешательством может рассматриваться вообще любое действие с пациентом – перевязка, установка зонда или дренажа, отсасывание мокроты, эндоскопические манипуляции и т.д. и т.п.
Кто более других подвержен рискам ВБИ?
- Соматически тяжелые пациенты
- Пациенты с сопутствующими заболеваниями
- Дети и пожилые пациенты
- Все, вне зависимости от возраста, ранее получавшие антибиотики или находившиеся по любому поводу в ОРИТ, ПИТ или просто в стационаре (если это только не ваше отделение, и вы точно знаете, что с ним происходило)
- Пациенты, переведенные из других ЛПУ (на них обычно просто лютый зоопарк всего, и они опасны не только сами для себя, но еще и для всех остальных пациентов не только отделения, но и вообще больницы)
Какие ЛПУ и отделения наиболее рискованны по ВБИ?
- Стационары, выстроенные в виде единого здания, либо имеющие общие переходы. В больницах, выстроенных в виде отдельных, несообщающихся корпусов, поддерживать cанэпидрежим и режим нераспространения ВБИ несопоставимо проще.
- Стационары, в которых гнойные отделения находятся в одном здании с чистыми, – тут можно убиться вусмерть, но синегнойку с ацинеткой вывести будет невозможно в принципе, если только не обстраивать классический санпропускник на входе и выходе из гнойных в чистые.
- Стационары, чьи отделения не имеют палат-изоляторов. Можно опять же расшибиться в лепешку, но если вы не можете изолировать пациента с устойчивой микрофлорой от остальных, эти самые все остальные и полягут.
- Самыми опасными же являются отделения реанимации и ПИТЫ, ввиду высочайшего процента использования антибиотиков, кроме того, онкологические и онкогематологические отделения, гнойные же отделения скорее опасны для чистых, чем сами для себя.
- Вообще, любой стационар с отсутствующим микробиологическим мониторингом, без собственной бак. лаборатории и службы эпиднадзора в виде эпидемиологов и натасканного на тему клинического фармаколога, – это не самое лучшее место для того, чтобы там оказаться в качестве пациента, тем более врачу (вы же помните, что в каждом из нас свой зоопарк?)
Что делать?
1. Мыть руки. Нет, даже вот так – МЫТЬ РУКИ – и делать это правильно. Методику мытья вы все прекрасно знаете. Если не знаете – берите СанПин и внимательно его изучайте по всем пунктам:
12.4. Гигиеническая обработка рук
12.4.1. Гигиеническую обработку рук следует проводить в следующих случаях:
- перед непосредственным контактом с пациентом;
- после контакта с неповрежденной кожей пациента (например, при измерении пульса или артериального давления);
- после контакта с секретами или экскретами организма, слизистыми оболочками, повязками;
- перед выполнением различных манипуляций по уходу за пациентом;
- после контакта с медицинским оборудованием и другими объектами, находящимися в непосредственной близости от пациента;
- после лечения пациентов с гнойными воспалительными процессами, после каждого контакта с загрязненными поверхностями и оборудованием.
12.4.2. Гигиеническая обработка рук проводится двумя способами:
- гигиеническое мытье рук мылом и водой для удаления загрязнений и снижения количества микроорганизмов;
- обработка рук кожным антисептиком для снижения количества микроорганизмов до безопасного уровня.
12.4.3. Для мытья рук применяют жидкое мыло с помощью дозатора (диспенсера). Вытирают руки индивидуальным полотенцем (салфеткой), предпочтительно одноразовым.
12.4.4. Гигиеническую обработку рук спиртосодержащим или другим разрешенным к применению антисептиком (без их предварительного мытья) проводят путем втирания его в кожу кистей рук в количестве, рекомендуемом инструкцией по применению, обращая особое внимание на обработку кончиков пальцев, кожи вокруг ногтей, между пальцами. Непременным условием эффективного обеззараживания рук является поддержание их во влажном состоянии в течение рекомендуемого времени обработки.
12.4.5. При использовании дозатора новую порцию антисептика (или мыла) наливают в дозатор после его дезинфекции, промывания водой и высушивания. Предпочтение следует отдавать локтевым дозаторам и дозаторам на фотоэлементах.
12.4.6. Кожные антисептики для обработки рук должны быть легко доступны на всех этапах лечебно-диагностического процесса. В подразделениях с высокой интенсивностью ухода за пациентами и с высокой нагрузкой на персонал (отделения реанимации и интенсивной терапии и т.п.) дозаторы с кожными антисептиками для обработки рук должны размещаться в удобных для применения персоналом местах (у входа в палату, у постели больного и др.). Следует также предусматривать возможность обеспечения медицинских работников индивидуальными емкостями (флаконами) небольших объемов (до 200 мл) с кожным антисептиком.
12.4.7. Использование перчаток.
12.4.7.1. Перчатки необходимо надевать во всех случаях, когда возможен контакт с кровью или другими биологическими субстратами, потенциально или явно контаминированными микроорганизмами, слизистыми оболочками, поврежденной кожей.
12.4.7.2. Не допускается использование одной и той же пары перчаток при контакте (для ухода) с двумя и более пациентами, при переходе от одного пациента к другому или от контаминированного микроорганизмами участка тела к чистому. После снятия перчаток проводят гигиеническую обработку рук.
12.4.7.3. При загрязнении перчаток выделениями, кровью и т.п. во избежание загрязнения рук в процессе их снятия следует тампоном (салфеткой), смоченным раствором дезинфицирующего средства (или антисептика), убрать видимые загрязнения. Снять перчатки, погрузить их в раствор средства, затем утилизировать. Руки обработать антисептиком.
Руки под перчатки надо мыть! Ибо они имеют свойство рваться, причем в самый неподходящий момент. Потом будете следователю долго объяснять, как вы торопились и вообще никогда такого не было, а тут… Лучше все-таки до автоматизма отработать навык, чем потом расхлебывать его отсутствие.
3. Регулярно терзать эпидемиологическую службу на предмет результатов мониторингов или служебок по расходникам и т. п. Не все же им вас терзать. Приставать лучше всего письменно, чтобы следы этих приставаний оставались, они могут очень сильно пригодиться в будущем.
4. Ну и учиться, учиться и еще раз учиться. Или менять специальность, так как к огромному сожалению все, что связано с медициной, особенно критических состояний, стало слишком опасным.
Но несмотря на такой невеселый разговор, автор и редакция Видаль от всей души хотела бы поздравить Вас с наступающим 2020 годом и выражает надежду, что наш цикл стал полезной частичкой уходящего 2019 года.
Внутрибольничные инфекции – различные инфекционные заболевания, заражение которыми произошло в условиях лечебного учреждения. В зависимости от степени распространения различают генерализованные (бактериемию, септицемию, септикопиемию, бактериальный шок) и локализованные формы внутрибольничных инфекций (с поражением кожи и подкожной клетчатки, дыхательной, сердечно-сосудистой, урогенитальной системы, костей и суставов, ЦНС и т. д.). Выявление возбудителей внутрибольничных инфекций проводится с помощью методов лабораторной диагностики (микроскопических, микробиологических, серологических, молекулярно-биологических). При лечении внутрибольничных инфекций используются антибиотики, антисептики, иммуностимуляторы, физиотерапия, экстракорпоральная гемокоррекция и т. д.

Общие сведения
Внутрибольничные (госпитальные, нозокомиальные) инфекции - инфекционные заболевания различной этиологии, возникшие у пациента или медицинского сотрудника в связи с пребыванием в лечебно-профилактическом учреждении. Инфекция считается внутрибольничной, если она развилась не ранее 48 часов после поступления больного в стационар. Распространенность внутрибольничных инфекций (ВБИ) в медицинских учреждениях различного профиля составляет 5-12%. Наибольший удельный вес внутрибольничных инфекций приходится на акушерские и хирургические стационары (отделения реанимации, абдоминальной хирургии, травматологии, ожоговой травмы, урологии, гинекологии, отоларингологии, стоматологии, онкологии и др.). Внутрибольничные инфекции представляют собой большую медико-социальную проблему, поскольку утяжеляют течение основного заболевания, увеличивают длительность лечения в 1,5 раза, а количество летальных исходов - в 5 раз.

Этиология и эпидемиология внутрибольничных инфекций
Основными возбудителями внутрибольничных инфекций (85% от общего числа) выступают условно-патогенные микроорганизмы: грамположительные кокки (эпидермальный и золотистый стафилококк, бета-гемолитический стрептококк, пневмококк, энтерококк) и грамотрицательные палочковидные бактерии (клебсиеллы, эшерихии, энтеробактер, протей, псевдомонады и др.). Кроме этого, в этиологии внутрибольничных инфекций велика удельная роль вирусных возбудителей простого герпеса, аденовирусной инфекции, гриппа, парагриппа, цитомегалии, вирусных гепатитов, респираторно-синцитиальной инфекции, а также риновирусов, ротавирусов, энтеровирусов и пр. Также внутрибольничные инфекции могут быть вызваны условно-патогенными и патогенными грибами (дрожжеподобными, плесневыми, лучистыми). Особенностью внутригоспитальных штаммов условно-патогенных микроорганизмов служит их высокая изменчивость, лекарственная резистентность и устойчивость к воздействию факторов среды (ультрафиолета, дезинфектантов и пр.).
Источниками внутрибольничных инфекций в большинстве случаев выступают пациенты или медицинский персонал, являющиеся бактерионосителями или больными стертыми и манифестными формами патологии. Как показывают исследования, роль третьих лиц (в частности, посетителей стационаров) в распространении ВБИ невелика. Передача различных форм госпитальной инфекции реализуется с помощью воздушно-капельного, фекально-орального, контактного, трансмиссивного механизма. Кроме этого, возможен парентеральный путь передачи внутрибольничной инфекции при проведении различных инвазивных медицинских манипуляций: забора крови, инъекций, вакцинации, инструментальных манипуляций, операций, ИВЛ, гемодиализа и пр. Таким образом в медучреждении возможно заразиться гепатитами В, С и D, гнойно-воспалительными заболеваниями, сифилисом, ВИЧ-инфекцией. Известны случаи внутрибольничных вспышек легионеллеза при приеме больными лечебного душа и вихревых ванн.
Факторами, участвующими в распространении внутрибольничной инфекции, могут выступать контаминированные предметы ухода и обстановки, медицинский инструментарий и аппаратура, растворы для инфузионной терапии, спецодежда и руки медперсонала, изделия медицинского назначения многоразового использования (зонды, катетеры, эндоскопы), питьевая вода, постельные принадлежности, шовный и перевязочный материал и мн. др.
Значимость тех или иных видов внутрибольничной инфекции во многом зависит от профиля лечебного учреждения. Так, в ожоговых отделениях преобладает синегнойная инфекция, которая в основном передается через предметы ухода и руки персонала, а главным источником внутрибольничной инфекции являются сами пациенты. В учреждениях родовспоможения основную проблему представляет стафилококковая инфекция, распространяемая медицинским персоналом-носителем золотистого стафилококка. В урологических отделениях доминирует инфекция, вызываемая грамотрицательной флорой: кишечной, синегнойной палочкой и др. В педиатрических стационарах особую значимость имеет проблема распространения детских инфекций – ветряной оспы, эпидемического паротита, краснухи, кори. Возникновению и распространению внутрибольничной инфекции способствуют нарушение санитарно-эпидемиологического режима ЛПУ (несоблюдение личной гигиены, асептики и антисептики, режима дезинфекции и стерилизации, несвоевременное выявление и изоляция лиц-источников инфекции и т. д.).
К группе риска, в наибольшей степени подверженной развитию внутрибольничной инфекции, относятся новорожденные (особенно недоношенные) и дети раннего возраста; пожилые и ослабленные пациенты; лица, страдающие хроническими заболеваниями (сахарным диабетом, болезнями крови, почечной недостаточностью), иммунодефицитом, онкопатологией. Восприимчивость человека к внутрибольничным инфекциям увеличивается при наличии у него открытых ран, полостных дренажей, внутрисосудистых и мочевых катетеров, трахеостомы и других инвазивных устройств. На частоту возникновения и тяжесть течения внутрибольничной инфекции влияет долгое нахождение пациента в стационаре, длительная антибиотикотерапия, иммуносупрессивная терапия.
Классификация внутрибольничных инфекций
По длительности течения внутрибольничные инфекции делятся на острые, подострые и хронические; по тяжести клинических проявлений – на легкие, среднетяжелые и тяжелые формы. В зависимости от степени распространенности инфекционного процесса различают генерализованные и локализованные формы внутрибольничной инфекции. Генерализованные инфекции представлены бактериемией, септицемией, бактериальным шоком. В свою очередь, среди локализованных форм выделяют:
- инфекции кожи, слизистых и подкожной клетчатки, в т. ч. послеоперационных, ожоговых, травматических ран. В частности, к их числу относятся омфалит, абсцессы и флегмоны, пиодермия, рожа, мастит, парапроктит, грибковые инфекции кожи и др.
- инфекции полости рта (стоматит) и ЛОР-органов (ангина, фарингит, ларингит, эпиглоттит, ринит, синусит, отит, мастоидит)
- инфекции бронхолегочной системы (бронхит, пневмония, плеврит, абсцесс легкого, гангрена легкого, эмпиема плевры, медиастинит)
- инфекции пищеварительной системы (гастрит, энтерит, колит, вирусные гепатиты)
- глазные инфекции (блефарит, конъюнктивит, кератит)
- инфекции урогенитального тракта (бактериурия, уретрит, цистит, пиелонефрит, эндометрит, аднексит)
- инфекции костно-суставной системы (бурсит, артрит, остеомиелит)
- инфекции сердца и сосудов (перикардит, миокардит, эндокардит, тромбофлебиты).
- инфекции ЦНС (абсцесс мозга, менингит, миелит и др.).
Диагностика внутрибольничных инфекций
Критериями, позволяющими думать о развитии внутрибольничной инфекции, служат: возникновение клинических признаков заболевания не ранее чем через 48 часов после поступления в стационар; связь с проведением инвазивного вмешательства; установление источника инфекции и фактора передачи. Окончательное суждение о характере инфекционного процесса получают после идентификации штамма возбудителя с помощью лабораторных методов диагностики.
Для исключения или подтверждения бактериемии проводится бактериологический посев крови на стерильность, желательно не менее 2-3-х раз. При локализованных формах внутрибольничной инфекции микробиологическое выделение возбудителя может быть произведено из других биологических сред, в связи с чем выполняется посев мочи, кала, мокроты, отделяемого ран, материала из зева, мазка с конъюнктивы, из половых путей на микрофлору. Дополнительно к культуральному методу выявления возбудителей внутрибольничных инфекций используются микроскопия, серологические реакции (РСК, РА, ИФА, РИА), вирусологический, молекулярно-биологический (ПЦР) методы.
Лечение внутрибольничных инфекций
Сложности лечения внутрибольничной инфекции обусловлены ее развитием в ослабленном организме, на фоне основной патологии, а также резистентностью госпитальных штаммов к традиционной фармакотерапии. Больные с диагностированными инфекционными процессами подлежат изоляции; в отделении проводится тщательная текущая и заключительная дезинфекция. Выбор противомикробного препарата основывается на особенностях антибиотикограммы: при внутрибольничной инфекции, вызванной грамположительной флорой наиболее эффективен ванкомицин; грамотрицательными микроорганизмами – карбапенемы, цефалоспорины IV поколения, аминогликозиды. Возможно дополнительное применение специфических бактериофагов, иммуностимуляторов, интерферона, лейкоцитарной массы, витаминотерапии.
При необходимости проводится чрескожное облучение крови (ВЛОК, УФОК), экстракорпоральная гемокоррекция (гемосорбция, лимфосорбция). Симптоматическая терапия осуществляется с учетом клинической формы внутрибольничной инфекции с участием специалистов соответствующего профиля: хирургов, травматологов, пульмонологов, урологов, гинекологов и др.
Профилактика внутрибольничных инфекций
Основные меры профилактики внутрибольничных инфекций сводятся к соблюдению санитарно-гигиенических и противоэпидемических требований. В первую очередь, это касается режима дезинфекции помещений и предметов ухода, применения современных высокоэффективных антисептиков, проведения качественной предстерилизационной обработки и стерилизации инструментария, безукоснительного следования правилам асептики и антисептики.
Медицинский персонал должен соблюдать меры индивидуальной защиты при проведении инвазивных процедур: работать в резиновых перчатках, защитных очках и маске; осторожно обращаться с медицинским инструментарием. Большое значение в профилактике внутрибольничных инфекций имеет вакцинация медработников от гепатита В, краснухи, гриппа, дифтерии, столбняка и других инфекций. Все сотрудники ЛПУ подлежат регулярному плановому диспансерному обследованию, направленному на выявление носительства патогенов. Предупредить возникновение и распространение внутрибольничных инфекций позволит сокращение сроков госпитализации пациентов, рациональная антибиотикотерапия, обоснованность проведения инвазивных диагностических и лечебных процедур, эпидемиологический контроль в ЛПУ.
Читайте также:

