Особенности патогенеза кишечных бактериальных инфекций
Обновлено: 18.04.2024
Роза Исмаиловна Ягудина, д. фарм. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
С наступившим летом тема нашей статьи приобрела особую актуальность. Кишечные инфекции — это целая группа инфекционных заболеваний, поражающих в основном желудочно-кишечный тракт. Острые кишечные инфекции по своей распространенности уступают только острым респираторным заболеваниям. Пик заболеваемости обычно приходится на лето, но и в холодное время года часто встречаются кишечные инфекции, вызываемые преимущественно вирусами. Однако наиболее частая причина возникновения этих заболеваний — попадание возбудителей инфекции с загрязненными продуктами и водой в желудочно-кишечный тракт.
Всего в настоящее время известно около 30 инфекционных кишечных заболеваний. К наиболее распространенным относятся:
- пищевая токсикоинфекция (в основном стафилококковой этиологии)
- сальмонеллез
- дизентерия
- энтеровирусная и ротавирусная инфекция
- холера
Осложнения кишечных инфекций:
- бактериальные инфекции органов дыхания и среднего уха
- дисбактериоз кишечника
- кишечное кровотечение
- перфорация стенки кишки
- инвагинация кишечника
- бактериально-токсический шок
Возбудители кишечной инфекции
Помимо инфекционных агентов из естественной среды источником заражения может стать уже заболевший человек. Выделяя большое количество патогенных микроорганизмов (микробы выделяются с испражнениями, рвотными массами, иногда с мочой), больной заражает предметы, находящиеся вокруг, и, если не соблюдать меры предосторожности, может возникнуть цепная реакция в распространении инфекции.
Практически все возбудители кишечных инфекций чрезвычайно живучи. Они способы подолгу существовать в почве, воде и на различных предметах (ложках, тарелках, дверных ручках и мебели). Инфекционные микроорганизмы во внешней среде не только не погибают, но и сохраняют способность к размножению, а размножаются они наиболее активно в теплых и влажных условиях. Однако самая благоприятная среда для развития бактерий — это кисломолочные и мясные продукты.
Установлена связь отдельных форм острых кишечных инфекций с видами пищи. Так, дизентерия чаще возникает при употреблении молока и молочных продуктов, а кишечные инфекции, вызванные стафилококком, — при употреблении молочных продуктов и кондитерских изделий с кремом. Иерсиниозы обычно развиваются при употреблении сырых овощей, салатов и другой растительной пищи.
Возбудителями кишечных инфекций могут быть как бактерии (сальмонеллы, шигеллы, иерсинии, энтеропатогенные кишечные палочки, стафилококки), так и их токсины (пищевые токсикоинфекции). Вирусы (ротавирусы, энтеровирусы, астровирусы, парвовирусы) пока на втором месте по частоте встречаемости, однако в последнее время вирусные инфекции получают всё более широкое распространение. И на последнем месте — простейшие (лямблии, амебы, бластоцисты).
После попадания патогенов в организм человека, как правило, проходит бессимптомный инкубационный период, который продолжается от 6 до 48 часов — от попадания микроорганизмов в ротовую полость до момента поступления их в кишечник, где происходит их бурное размножение. После того как патогенные микроорганизмы размножились, начинается стадия клинических проявлений.
N. B.! При появлении симптомов, напоминающих острую кишечную инфекцию, необходимо срочно обратиться к инфекционисту для правильного подбора терапии и профилактики осложнений.
Наступает острый период — от 1 до 14 дней, в это время клинические проявления со стороны ЖКТ выражены максимально. Как правило, период заканчивается, когда нормализуется температура и прекращается ведущий симптом (понос или рвота).
Период реконвалесценции — не менее 2 недель, а в некоторых случаях при отсутствии лечения до нескольких лет. В этот период функция желудочно-кишечного тракта, как правило, восстанавливается не полностью — может быть неустойчивый стул.
В основном все кишечные инфекции протекают с достаточно похожими симптомами. Они всегда начинаются внезапно. В самом начале заболевания появляется резкая слабость, вялость, снижение аппетита, головная боль, повышение температуры — неспецифические симптомы, которые могут напоминать симптомы респираторных вирусных инфекций. Однако вскоре возникают тошнота, рвота, схваткообразные боли в животе, понос с примесью слизи, гноя или крови (например, при дизентерии), также могут беспокоить жажда и озноб. Среди клинических проявлений со стороны желудочно-кишечного тракта, как правило, сильнее всего выражены симптомы, связанные с пораженным органом:
- тошнота, рвота и боли в эпигастральной области (при гастрите);
- понос (при энтерите);
- рвота и понос (при гастроэнтерите);
- кровь в стуле и его нарушения (при колите);
- поражения всего кишечника (при энтероколите).
Одно из самых неблагоприятных последствий кишечной инфекции — это дегидратация организма из‑за рвоты и/или поноса и, как следствие, нарушение водно-электролитного обмена. Результатом резкой дегидратации может стать даже шок.
Однако иногда кишечные инфекции могут не иметь видимых симптомов, но сопровождаются выделением возбудителей. В плане распространения инфекции такое носительство наиболее опасно: ничего не подозревающий человек становится постоянным источником инфекции, заражая окружающих.
Врачу важно провести дифференциальную диагностику между кишечной инфекцией и соматическими заболеваниями со сходными симптомами: диареей, связанной с приемом лекарственных препаратов, острым аппендицитом, инфарктом миокарда, пневмонией, внематочной беременностью и т. д.
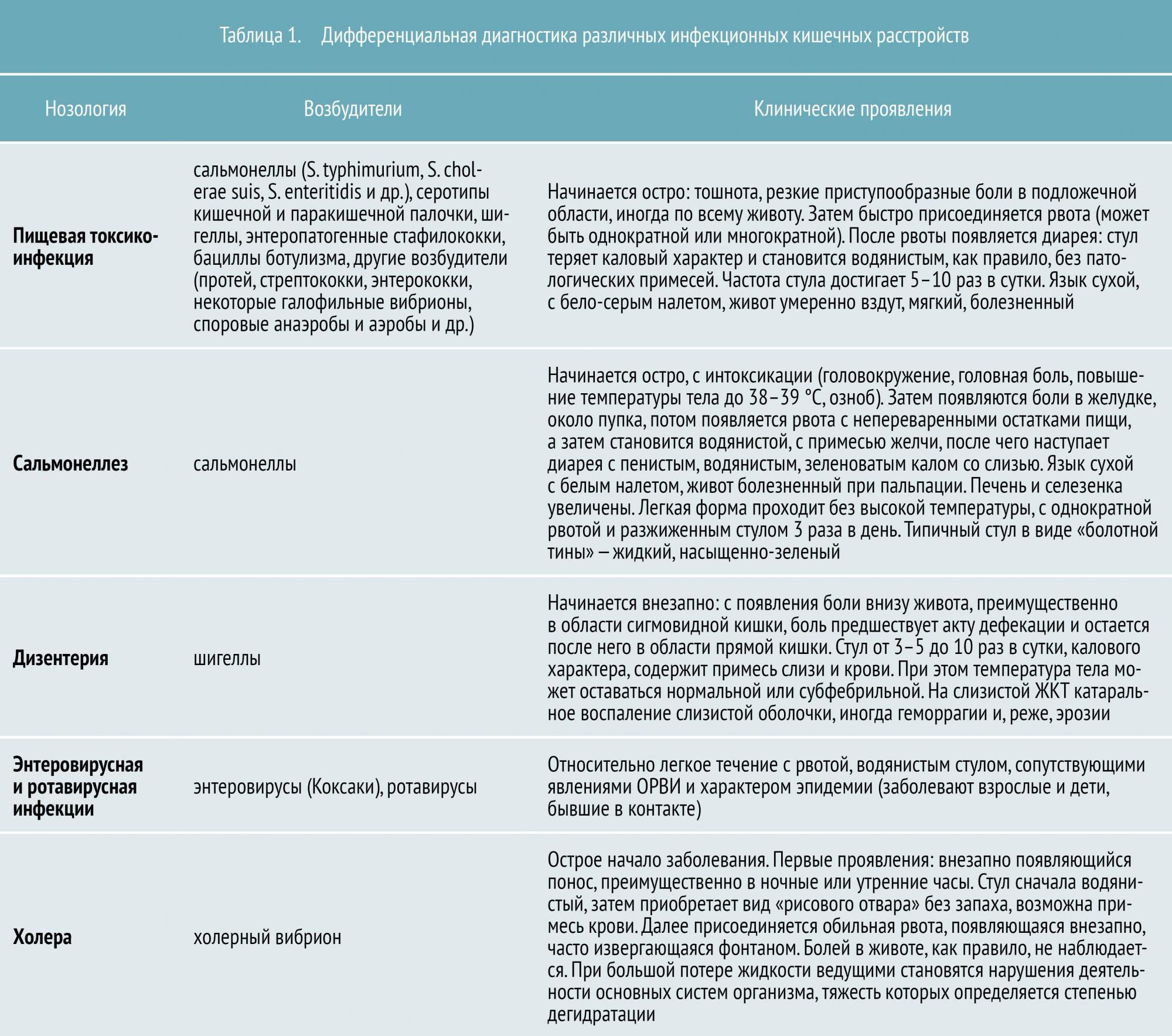
Диагностика и лечение кишечной инфекции
- Выделение из крови возбудителя и его антигенов (токсинов)
- Бактериологическое исследование: выделение и типирование возбудителя в посевах кала, других биологических секретов и экскретов организма больного
- Вирусологическое исследование: выделение вируса из кала в посевах на культуре клеток или при электронной микроскопии
- Микроскопическое исследование: обнаружение паразитов в мазках нативного кала после обработки специальными красителями
- Выявление сывороточных антител к антигенам возбудителя и роста их титра: серологическое обследование с использованием специальных диагностикумов в реакциях (РПГА, РИГА, ИФА и т. п.); прирост титра в 4 раза.
Основные принципы терапии кишечных инфекций:
- борьба с возбудителем (антибактериальная терапия);
- борьба с обезвоживанием (как правило, для устранения недостатка жидкости пациентам назначают солевые растворы);
- устранение диареи (энтеросорбенты);
- соблюдение щадящей диеты (исключение свежих овощей и фруктов, молочных продуктов, сладкого).
Во время болезни необходимо соблюдать диету, помогающую замедлить перистальтику кишечника. Рекомендуются продукты с высоким содержанием танина (черника, черемуха, крепкий чай); вещества вязкой консистенции (слизистые супы, протертые каши, кисели); сухари; индифферентные вещества — паровые блюда из нежирного мяса и рыбы. Важный этап в лечении кишечных инфекций — исключение из рациона жареных и жирных блюд, сырых овощей и фруктов.
Главное направление лечебной тактики — нейтрализация экзотоксинов в кишечнике (энтеросорбенты) и регидратация — компенсация патологических потерь жидкости и электролитов специально разработанными глюкозо-солевыми растворами. Объем вводимых растворов зависит от степени обезвоживания и массы тела больного, а скорость введения составляет 1–1,5 л/ч. Дезинтоксикационная и регидратационная терапия в 85–95 % случаев может осуществляться перорально.
Антибиотики может назначить только инфекционист с учетом проведенных лабораторных тестов и выявленного возбудителя инфекции. Однако при выраженной диарее для ускоренной санации обоснованным является назначение антибактериальных ЛС, которые не всасываются или плохо всасываются из кишечника и обладают широким спектром действия (например, энтерофурил или ко-тримоксазол). Эффективными средствами альтернативной этиотропной терапии, в качестве препаратов от острой кишечной инфекции, являются энтеросорбенты и пробиотики. Этиотропное действие пробиотиков связано с выраженной антагонистической активностью в отношении всех возбудителей острых кишечных инфекций (ОКИ) бактериальной этиологии и опосредованным иммуномодулирующим действием на местное звено иммунитета.
Обзор лекарств для лечения кишечных инфекций
Нифуроксазид (энтерофурил)
Безрецептурное противомикробное средство широкого спектра действия, производное 5‑нитрофурана. Антимикробная активность нифуроксазида вызвана наличием в его составе NO2‑группы, которая угнетает активность дегидрогеназы и нарушает синтез белков в патогенных бактериях.
Нифуроксазид не оказывает действия на сапрофитную флору, не нарушает равновесия нормальной кишечной флоры. При острой бактериальной диарее восстанавливает эубиоз кишечника. При инфицировании энтеротропными вирусами препятствует развитию бактериальной суперинфекции. Этот препарат для лечения кишечной инфекции можно назначать беременным и кормящим женщинам, детям начиная с одного месяца. Терапия нифуроксазидом не должна превышать 7 дней, при этом запрещено употреблять алкоголь.
Безрецептурный препарат в форме вагинальных и ректальных суппозиториев. Обладает иммуномодулирующим, противовирусным, антихламидийным действием. Кипферон — комплексная лекарственная форма, содержащая человеческий рекомбинантный интерферон-α2 и комплексный иммуноглобулиновый препарат (КИП). Разрешен к применению у детей на первом году жизни.
Ко-тримоксазол (сульфаметоксазол + триметоприм)
Механизм действия ко-тримоксазол а обусловлен двойным блокированием метаболизма микроорганизмов. Триметоприм обратимо ингибирует дигидрофолатредуктазу микроорганизмов, нарушает образование из дигидрофолиевой кислоты тетрагидрофолиевой, продукцию нуклеиновых кислот, пиримидиновых и пуриновых оснований; подавляет размножение и рост бактерий. Сульфаметоксазол, который по строению схож с парааминобензойной кислотой, захватывается бактерией и препятствует включению парааминобензойной кислоты в дигидрофолиевую кислоту. В связи с тем что ко-тримоксазол угнетает жизнедеятельность кишечной палочки, снижается образование в кишечнике никотиновой кислоты, рибофлавина, тиамина и прочих витаминов B-комплекса. Это лекарство, помогающее от кишечной инфекции, отпускается по рецепту, применяется с 2‑месячного возраста.
Бактисубтил — споры бактерий Bacillus cereus IP. Рецептурный препарат от кишечной инфекции бактисубтил сохраняет и корригирует физиологическое равновесие кишечной флоры. Споры бактерий, содержащиеся в препарате, устойчивы к действию желудочного сока. Прорастание бактерий в вегетативные формы происходит в кишечнике, затем они высвобождают энзимы, которые расщепляют углеводы, жиры, белки. В результате образуется кислая среда, предотвращающая процессы гниения. Препарат препятствует нарушению синтеза витаминов группы В и Р в кишечнике, его нельзя запивать горячим, а также сочетать с алкоголем. Детям его назначают с семилетнего возраста. Бактисубтил резистентен к действию различных антибиотиков и сульфаниламидных препаратов, поэтому может быть назначен одновременно с ними.
Декстроза + калия хлорид + натрия хлорид + натрия цитрат (регидрон)
Регидратирующее средство для перорального приема восстанавливает водно-электролитное равновесие, нарушенное при обезвоживании организма; корректирует ацидоз. Содержимое одного пакетика растворяют в литре свежепрокипяченной охлажденной питьевой воды. Приготовленный раствор нужно хранить в холодильнике и использовать в течение 24 часов. В раствор нельзя добавлять никакие другие компоненты, чтобы не нарушить действие препарата. Отпускается без рецепта.
Безрецептурное лекарственное средство природного происхождения, обладающее протективным действием в отношении слизистой оболочки кишечника и выраженными адсорбирующими свойствами. Являясь стабилизатором слизистого барьера, образует поливалентные связи с гликопротеинами слизи и увеличивает продолжительность ее жизни, образуя физический барьер, который защищает слизистую оболочку пищеварительного тракта от отрицательного действия ионов Н+, соляной кислоты, желчных солей, микроорганизмов, их токсинов и других раздражителей. Обладает селективными сорбционными свойствами, защищает слизистую оболочку пищеварительного тракта от отрицательного воздействия. В терапевтических дозах не влияет на моторику кишечника.
Профилактика кишечных инфекций, в том числе и острых
Для профилактики кишечных инфекций важно регулярно мыть руки и проводить влажную уборку в квартире. Лучше сразу же выкидывать продукты с истекшим сроком годности, не покупать их в местах с непонятными условиями хранения — как бы ни были привлекательны, скажем, грибочки у бабушки возле метро — а фрукты и овощи есть только тщательно вымытыми.
Избежать распространения болезни поможет ранняя диагностика и изоляция больного с кишечной инфекцией. В очаге инфекции нужно обработать поверхности дезинфицирующими растворами, прокипятить посуду. Выписку пациентов проводят только после отрицательного результата контрольного обследования кала. Всем, кто перенес кишечную инфекцию, в течение месяца необходимо регулярно проходить диспансерное наблюдение в поликлинике.
Патогенетические механизмы ОКИсвязаны с особенностями возбудителей, которые посредством нескольких механизмов преодолевают противомикробную защиту организма хозяина. Такими механизмами являются: •адгезия(адгезины – лектиноподобные молекулы – обеспечивают адгезию бактерий к микроворсинкам слизистой оболочки кишечника; агглютинины различной природы и др.); •инвазия(инвазины – белки бактериального происхождения, обеспечивающие инвазию путем изменения функций цитоскелета эпителиальных клеток; жгутики, энтеробактины (различные сидероформные системы, связывающие ионы Fe 2+ ); интегрины и т. д.); •продукцияэнтеротоксинов (действующих на механизмы ионного обмена в энтероцитах); • продукция цитотоксинов(вызывающих гибель клеток хозяина).
С помощью адгезии микроорганизмы колонизируют кишечник и способны находиться и размножаться в нем, несмотря на наличие перистальтики и механизмов антимикробной резистентности. При адгезии микроорганизмов происходит продукция энтеротоксина, который достигает своей цели – клеток кишечника. У некоторых возбудителей (энтеротоксигенная E. coli) механизм адгезии реализуется с помощью поверхностных структурных белков, у других (энтеропатогенная E. coli) – с помощью фактора адгезии. Продукция энтеротоксинов характерна для V. cholerae. Она облегчает прикрепление возбудителя к клеткам слизистой оболочки кишечника. Энтеротоксин стимулирует внутриклеточную систему аденилатциклазы, что приводит к активной секреции электролитов и интерстициальной жидкости в просвет кишечника. Стенка кишечника остается морфологически интактной, однако в связи со значительным объемом секретируемой жидкости в течение нескольких часов может развиваться выраженное, угрожающее жизни обезвоживание. В ходе реализации механизма инвазии вначале происходит адгезия, а затем – инвазия возбудителей ОКИ в слизистую оболочку кишечника, развивается воспалительная реакция, результатом которой может быть гибель клеток эпителия, а клиническим проявлением – лихорадка, спастические сокращения кишечника, боли в животе, наличие слизи и/или крови в кале. Механизм инвазии характерен для шигелл, сальмонелл, кампилобактерий. Некоторые бактерии способны продуцировать цитотоксины. Шигеллы (S. dysenteriae) обладают способностью выделять классический тип цитотоксина (токсин Шига). Энтерогеморрагические E. coli серотипа О157, энтеропатогенные E. coli и Vibrio parahaemoliticus также способны продуцировать подобный токсин. Таким образом, ОКИ существенно различаются структурой возбудителей, их способностью к инвазии, механизмами патогенеза.
174. Возбудители кампилобактериоза. Биологические свойства, факторы вирулентности. Механизм и пути передачи. Источники инфекции. Принципы мб диагностики. Препараты для лечения.
Кампилобактериоз (лат.campylobacteriosis) — острое инфекционноезоонозноезаболевание, характеризуется синдромом общейинтоксикации, поражениемжелудочно-кишечного трактаи возможностью генерализации патологического процесса. На сегодняшний день профилактика кампилобактериоза пока не разработана
Возбудителем кампилобактериоза являются различные серотипы Campylobacter fetus jejuni. В последнее время большое внимание уделяют болезням, обусловленным С. pylori, который в настоящее время получил название Helicobacter pylori, а болезни, им обусловленные, - геликобактериоаз. Он проявляется в виде острого гастрита, хронического антрального гастрита, язвенной болезни желудка и двенадцатиперстной кишки, реже в виде эзофагита, энтерита и др. Другие подвиды кампилобактеров, циркулирующие среди животных, в патологии человека значения не имеют. С. fetus jejuni представляет собой подвижную грамотрицательную палочку, изогнутую в форме запятой (вибриона) длиной 1,5-2 мкм, толщиной 0,3-0,5 мкм, имеет жгутик. Может образовывать и нитевидные формы. Растет на агаровых средах с добавлением 1% глицерина; колонии мелкие. Оптимум роста 37оС, рН 7,0, спирты и сахара не ферментирует, гемолиза на средах с кровью не вызывает, не выделяет индола и аммиака, не разжижает желатины, не свертывает молока, образует сероводород, дает положительную реакцию на каталазу. Имеет термостабильные О-антигены и термолабильные Н-антигены. Отмечена антигенная связь с бруцеллами. Подразделяется на серотипы (их более 50), однако 10 наиболее распространенных серотипов обусловливают около 70% всех заболеваний.
При нагревании кампилобактеры быстро инактивируются, при комнатной температуре сохраняются до 2 нед, в сене, воде, навозе - до 3 нед, а в замороженных тушах животных - несколько месяцев. Они патогенны для морских свинок, хомяков; чувствительны к эритромицину, левомицетину, стрептомицину, канамицину, тетрациклинам, гентамицину, малочувствительны к пенициллину, нечувствительны к сульфаниламидным препаратам, триметаприму.
Кампилобактериоз широко распространен во всех странах. Кампилобактеры обусловливают от 5 до 10% всех острых диарейных болезней. В США наблюдались эпидемические вспышки кампилобактериоза, связанные с употреблением зараженной воды или молока. При вспышках, связанных с употреблением сырого молока, заболеваемость достигала 60%. Резервуаром и источником инфекции являются многие виды животных, преимущественно домашние. Носительство С. fetus jejuni особенно часто наблюдается у кроликов (11-13%), кошек (30-45%) и уток (более 80%). Источниками возбудителя могут быть мышевидные грызуны. В нашей стране кампилобактериоз животных выявлялся на северо-западе Европейской части страны, в Поволжье, Западной Сибири и других районах. Человек заражается в основном через загрязненные выделениями животных воду и продукты. Нельзя исключить возможность заражения от человека, например при инфицировании новорожденных детей. У здоровых людей встречается бактерионосительство (около 1%). Наблюдаются профессиональные заболевания лиц, постоянно контактирующих с животными. Заболевания могут возникать при прямом контакте с больными животными, особенно при уходе за животными во время отелов и ягнения. Инфицирование наступает при употреблении недостаточно прогретого мяса, зараженного прижизненно или постмортально. Описаны случаи заболеваний после употребления непастеризованного молока. Чаще заболевают дети (новорожденные и дошкольного возраста), беременные, ослабленные лица, пожилые. В странах с умеренным климатом отмечается сезонность - заболеваемость повышается в летние месяцы.
Возбудитель попадает в организм преимущественно через желудочно-кишечный тракт при алиментарном заражении. Инфицирующая доза зависит от индивидуальной чувствительности. Кампилобактер вначале прикрепляется к поверхности энтероцитов, затем при помощи жгутика повреждает клеточную мембрану и оказывается внутри клетки. Довольно быстро проникает в кровь. Бактериемия наблюдается не только при острой форме, но и при хронически протекающих заболеваниях желудка. На месте ворот инфекции развиваются воспалительные изменения. При проникновении микробов в кровь высвобождается токсин, который обусловливает развитие общей интоксикации. Гематогенно обсеменяются многие органы и ткани. У ослабленных людей заболевание принимает септическое течение с формированием вторичных очагов в различных органах (эндокардиты, менингиты, энцефалиты, перитонит и др.). Подобное течение кампилобактериоза наблюдается на фоне цирроза печени, алкоголизма, при кахексии, а также у новорожденных и престарелых. Обильная рвота и понос могут приводить к дегидратации, гиповолемическому шоку. У лиц с хорошо функционирующей иммунной системой заражение не сопровождается клинически выраженными проявлениями (субклиническая форма, здоровое бактерионосительство).
Инкубационный период продолжается от 1 до 6 дней (чаще 1-2 дня). По клиническому течению выделяют следующие формы кампилобактериоза: 1) гастроинтестинальную; 2) генерализованную (септическую); 3) субклиническую; 4) хроническую.
Осложнения: инфекционно-токсический шок, тромбогеморрагический синдром, дегидратация.
Диагноз подтверждают выделением возбудителя из испражнений, крови, цереброспинальной жидкости, ткани абортированного плода. Посевы делают на специальные селективные твердые питательные среды с бриллиантовым зеленым, с тиогликолятом или триптиказосоевый бульон с 5% бараньей или лошадиной кровью и антибиотиками. Для ретроспективной диагностики используют серологические методы. Исследуют парные сыворотки, взятые с интервалом 10-14 дней. Для выявления антител используют различные реакции (РСК, РПГА, микроагглютинации, иммунофлюоресцентный метод).
Препаратами выбора при лечении являются трихопол (метронидазол) 0,25–0,5 г 3 раза в день или эритромицин 0,25–0,5 г 4 раза в день или другие макролиды (мидекамицин, рокситромицин, кларитромицин, азитромицин и др.), а также фторхинолоны. В тяжелых случаях кампилобактериоза, в том числе при распространенных формах заболевания, используют сочетание препаратов: макролиды (ровамицин), аминогликозиды (нетромицин) и метрогил.
Продолжительность терапии зависит от формы кампилобактериоза. При локализованных она составляет 7–14 дней, при распространенных – не менее 14 дней.
Подавляющее число бактерий может вызвать у человека инфекционный процесс, причем практически во всех его органах. Кишечные бактериальные инфекции отличают присущие только им сугубо специфические особенности. Эти особенности начинаются с пути заражения — алиментарного, когда микроорганизмы с водой и пищей попадают в просвет пищеварительного тракта, и сразу же начинается бурное размножение и возбудителей и, естественно, выделение их токсинов: экзо- или энтеротоксинов (истинных токсинов) и эндотоксинов.
Именно токсины определяют все разнообразие клинической симптоматики и патогенез острых кишечных инфекций.
Энтеротоксины выделяют не только холерные вибрионы (о холере см. лекцию 25 "Карантинные инфекции"), но сальмонеллы, кишечные палочки, шигеллы, иерсинии, клебсиеллы, кампи-лобактеры. При этом выделены две разновидности энтеротокси-на: термолабильный (у всех вышеперечисленных бакте-
рий) и термостабильный (эшерихии). Механизм связывания энтеротоксина с энтероцитами следующий: возбудители выделяют муциназу и нейраминазу — ферменты, расщепляющие сиаловую кислоту гликопротеинов гликокаликса и позволяющие связаться микроорганизму с рецептором клеточной мембраны энтероцита. При некоторых инфекциях (шигиллез) подобные рецепторы уже удалось выделить. Токсическое действие энтеротоксина — активация аденилатциклазной системы, накопление цАМФ, перфузия (флюкс) жидкости и ионов натрия из клетки. Так реализуется действие термолабильного энтеротоксина. Механизм действия термостабильного энтеротоксина отличается участием другой циклазной системы — цГМФ. Однако эффект тот же: если термолабильный энтеротоксин стимулирует накопление и экскрецию жидкости в канал кишки, то термостабильный энтеротоксин ингибирует абсорбцию жидкости и электролитов энтероцитами и стимулирует экскрецию ионов хлора. Результирующая обоих механизмов — водная диарея.
Благодаря феномену адгезии возбудителя к гликоликали-ксу клетки хозяина токсин оказывает свое действие без проникновения микроорганизма в клетку.
При диарейных инфекциях, вызываемых грамотрицательной микрофлорой, ведущую роль в патогенезе играют эндотоксины, токсичным компонентом которых является липополисахарид (липид А — главная его часть, ответственная за токсический эффект). Он накапливается в зоне адгезии, а затем, всасываясь в эн-тероциты, вызывает активацию простагландинов Е и F с последующим накоплением цАМФ и развитие водной диареи. Как известно, липополисахарид обладает способностью воздействовать на механизм свертывания крови, приводя к тромбозу и кровоизлияниям, т.е. по сути играет ведущую роль в развитии эндотокси-ческого (септического) шока, который иногда развивается при острых кишечных инфекциях, вызываемых грамотрицательны-ми микроорганизмами (сальмонеллезы).
Следует учесть, что при некоторых диарейных болезнях возможно выделение как экзо-, так и эндотоксинов (сальмонеллезы). Некоторые авторы предлагают все бактериальные кишечные инфекции различать по токсинам, продуцируемым бактериями, и по клиническим проявлениям, которые оказываются преобладающими. Американские авторы разделяют диарейные болезни на 2 группы: вызываемые инвазивными и неинвазивными возбудителями. Инвазивные, как ясно из названия, проникают в эпителий, разрушая его; типичным представителем их являются шигеллы. Прототипом неинвазивных является холерный вибрион.
Классификация бактериальных кишечных инфекций с учетом их возбудителя
I. Грамотрицательные палочки семейства Enterobacteriaceae:
1. Escherichiae
- Сальмонеллы Брюшной тиф
Шигеллезы (дизентерия) - Эшерихии Эшерихиозы:
Yersinieae Кишечный иерсиниоз
II. Грамотрицательные палочки семейства Vibrionaceae
Вибрион Коха Холера 1
Грамотрицательные палочки семейства Legionellaceae Legionella pneumophila Легионеллез
Грамотрицательные палочки семейства Spirillaceae
Helicobacter pylori Хеликобактериоз
1 См. лекцию 25 "Карантинные инфекции".
Брюшной тиф
• Брюшной тиф — острое кишечное инфекционное заболевание, вызываемое S.typhi abdominalis. Возбудитель относится к роду сальмонелл, который в настоящее время включает более 2500 различных серотипов. Исторически сложилось выделять брюшной тиф из всех заболеваний, вызываемых сальмонеллами, считать его основным представителем этой группы заболеваний, хотя к нему и не применяется термин "сальмонеллез". В последние годы он утратил свое значение. Заболеваемость неуклонно снижается, а смертность невелика и колеблется от долей процента в развитых странах до 2,3 % в Мексике, Индии. Сезонных колебаний при нем не бывает, но в странах, эндемичных по брюшному тифу, заболеваемость возрастает в летние месяцы.
Брюшной тиф — строгий антропоноз, единственным источником заболевания является больной человек или бактерионоситель.
Патогенез. Заражение происходит алиментарным путем. Возбудитель при заглатывании попадает в тонкую кишку и раэмяо жается там, выделяя эндотоксин. Затем сальмонелла проникает в слизистую оболочку (при этом электронно-микроскопически отчетливо виден интерэпителиальный путь проникновения, с мини-
мальными повреждениями энтероцитов), через одиночные и групповые фолликулы, в лимфатические сосуды, регионарные лимфатические узлы и дальше в кровоток. Эта первичная бактериемия возникает через 24—72 ч после заражения, клинически не документируется, транзиторная, быстро прекращается в связи с фагоцитозом возбудителя макрофагами. Однако часть сальмонелл сохраняется и после внутриклеточного размножения вновь попадает в кровоток, вызывая продолжающуюся в течение нескольких дней и даже недель повторную бактериемию. Именно бактериемией манифестирует брюшной тиф, и диагноз можно поставить, выделив сальмонеллу из крови (гемокультура). Таким образом, инкубационный период составляет 10—14 дней.
С бактериемией связаны генерализация инфекта и начало становления иммунитета. Начиная со 2-й недели заболевания, с помощью реакции агглютинации в крови определяют антитела к возбудителю. Бактериемия приводит к началу элиминации возбудителя — сальмонеллы с током крови попадают в печень, а далее — в желчные пути, где находят облигатную среду для своего существования. Не вызывая клинически выраженного холецистита, брюшнотифозные палочки в большом количестве размножаются в желчи (бактериохолия), с которой и выделяются в просвет тонкой кишки. С этого момента сальмонеллы обнаруживают во всех экскретах больных (фекалии, моча, пот, молоко лак-тирующих женщин). Посевы фекалий (копрокультура) становятся положительными на 3-й, иногда на 4-й неделе, когда выделение возбудителей с желчью достигает пика.
Попадая с желчью естественным путем в тонкую кишку, бактерии в групповых и солитарных лимфоидных фолликулах вызывают гиперергическую реакцию в связи с сенсибилизацией их при заражении (первая встреча) и бактериемии (вторая встреча). Эта реакция выражается некрозом лимфатического аппарата тонкой (иногда и толстой) кишки, подобным таковому при феномене Артюса.
Патологическая анатомия. Изменения при брюшном тифе делят на местные и общие.
Местные изменения при брюшном тифе наблюдаются прежде всего в тонкой кишке, при этом процесс локализуется преимущественно в терминальном отделе подвздошной кишки на протяжении 1—1,5 м и достигает максимума у самого илеоцекального клапана (илеотиф). Нередко изменения развиваются и в толстой кишке (колотиф), но чаще поражаются и тонкая, и толстая кишка (илеоколотиф), хотя в толстой кишке изменения выражены значительно слабее. Процесс развивается в слизистой оболочке и в лимфоидном аппарате кишечника. Брюшной тиф — классическое циклическое заболевание, и изменения в кишечнике укладываются в следующие 5 стадий, или периодов, заболевания: моз-
говидного набухания, некроза, образования язв, чистых язв и заживления. Каждая стадия продолжается примерно неделю.
Встадии мозговидного набухания групповые фолликулы увеличиваются в размерах настолько, что становятся видимыми глазом, выступая над поверхностью слизистой оболочки в виде плоских мягко-эластических бляшек серого цвета с неровной поверхностью в виде борозд и извилин, напоминающих мозг ребенка. На разрезе они сочные, розовато-серые. При гистологическом исследовании групповых фолликулов лимфоциты видны в небольшом количестве, они вытеснены моноцитами и очень крупными одноядерными клетками со светлой цитоплазмой и бледным ядром — макрофагами, которые принято называть тифозными (брюшнотифозные) клетками, так как эти клетки фагоцитируют брюшнотифозные палочки. Тифозные клетки образуют очаговые скопления, или брюшнотифозные гранулемы ("тифомы"). Помимо тифозных клеток, в гранулемах видны в небольшом количестве моноциты, гистиоциты и ретикулярные клетки. Таким образом, морфологическим выражением мозговидного набухания является острое продуктивное воспаление с образованием макрофагальных гранулем, отражающих реакцию гиперчувствительности замедленного типа в ответ на инфекционный агент. Источником макрофагов являются пролиферирую-щие моноциты. Гранулемы сливаются между собой, полностью вытесняя лимфоидную ткань. Слизистая оболочка подвздошной кишки полнокровна, в просвете кишки полужидкие и кашицеобразные массы с примесью слизи (картина катарального воспаления), регионарные лимфатические узлы заметно увеличиваются, становятся сочными, мягкими, красноватого цвета.
Встадии некроза групповых фолликулов брюшнотифозные гранулемы подвергаются некрозу, который начинается с поверхностных отделов и постепенно углубляется, достигая мышечной и даже серозной оболочки. Некротические массы грязно-серые, а затем имбибируются желчью и приобретают зеленовато-желтую или коричневатую окраску. На третьей неделе заболевания происходит отторжение некротических масс (стадия образования язв)и возникают изъязвления ("грязные язвы"), очертания которых повторяют форму фолликулов. Они появляются первоначально в терминальной части подвздошной кишки, затем — в вышележащих отделах. Края свежих язв имеют форму валика и нависают над дном. Дно неровное, на нем видны остатки некротизированной ткани. При отторжении некротических масс возможны обнажение и разрушение стенок сосудов с последующим кровотечением.
На четвертой неделе изъязвления становятся неглубокими, с низкими закругленными краями и гладким, свободным от некроза дном (стадия чистых язв); они имеют правильную
овальную форму и вытянуты вдоль кишки. В этой стадии иногда происходит перфорация язвы с последующим развитием перитонита.
Пятая неделя заболевания характеризуется выраженными процессами регенерации: в дне язвы разрастается грануляционная ткань, затем с краев наплывает регенерирующий эпителий и образуется нежный рубчик — стадия заживления язв. При гистологическом исследовании стенка кишки обычного строения, отмечается лишь отсутствие лимфоидной ткани в этом месте.
Влимфатических узлах брыжейки, прежде всего области илеоцекального угла, отмечаются изменения, развивающиеся в той же последовательности, что и в лимфоидном аппарате кишки. Сначала они увеличиваются за счет полнокровия, пролиферации моноцитарных фагоцитов и ретикулярных клеток, вытесняющих лимфоциты. Затем появляются тифозные клетки и формируются брюшнотифозные гранулемы, которые некроти-зируются, а затем происходит их организация или петрификация. Иногда о перенесенном брюшном тифе удается судить только по этим петрифицированным лимфатическим узлам.
Приведенное выше классическое стадийное течение брюшного тифа является общепризнанным, однако оно, как оказалось, является достаточно условным. В разных участках тонкой кишки одного больного можно одновременно увидеть структурные изменения, характерные для двух, иногда трех стадий брюшного тифа. Чем проксимальнее расположены изменения, тем они "моложе", чем дистальнее, ближе к илеоцекальному углу, тем они "старее". Судить на основании патологоанатомических данных о стадии брюшного тифа следует по наиболее "старым изменениям", наблюдаемым в терминальном отрезке подвздошной кишки.
Общие изменения обусловлены распространением брюшнотифозных палочек в период персистирующей бактериемии, которая длится несколько дней (а иногда несколько недель). Брюшнотифозные палочки неоднократно попадают в кожу и во все внутренние органы, вызывая в них типичные изменения. Характерным признаком брюшного тифа является розеолезная сыпь, которая появляется на 8—10-й день заболевания на коже живота, боковых поверхностей груди и на спине в виде мелких, слегка приподнятых над поверхностью кожи розовато-красных пятнышек, исчезающих при надавливании. Гистологически в со-сочковом слое дермы находят гиперемию сосудов, отек и воспалительные инфильтраты из лимфоцитов, плазмоцитов, гистиоцитов и лаброцитов. Эпидермис разрыхлен, с явлениями гиперкератоза. В элементах сыпи выявляются сальмонеллы. У ослабленных больных, особенно на фоне авитаминоза С, сыпь приобретает геморрагический характер.
В печени, селезенке, костном мозге, лимфатических узлах, легких, желчном пузыре появляются брюшнотифозные гранулемы. В редких случаях местные (кишечные) изменения при брюшном тифе уступают общим, причем из внекишеч-ных очагов гранулематозного поражения высеваются сальмонеллы. Ведущими клиническими проявлениями заболевания становятся поражение легких (пневмотиф), гортани (ларинготиф) или желчных путей (холангиотиф).
Помимо типичных, при брюшном тифе находят изменения, характерные для любого инфекционного заболевания: гиперпластические процессы в органах лимфатической системы и дистрофические — в паренхиматозных. Селезенка, как правило, увеличена в 3—4 раза, капсула ее напряжена, на разрезе пульпа вишневого цвета, дает обильный соскоб, иногда образуются инфаркты. Выражены гиперплазия красной пульпы, пролиферация моноцитарных элементов и ретикулярных клеток, а также характерные брюшнотифозные гранулемы. В миокарде, печени, почках находят дистрофические изменения. Изредка развивается холецистит.
Осложнения. Среди кишечных осложнений наиболее часты и опасны кровотечения и прободение язвы. Кровотечение возникает обычно на 3-й неделе и может быть смертельным. Очень опасна 4-я неделя болезни, когда в процессе очищения от некротических масс язва углубляется. Обычно основные изменения развиваются в слизистой оболочке, в области групповых фолликулов, но гранулемы по ходу лимфатических сосудов проникают до серозной оболочки и именно в области гранулем развивается некроз и перфорация язвы. Вторая причина прободения связана с тем, что на 4-й неделе заболевания симптомы общей интоксикации исчезают, температура тела нормализуется, субъективное состояние больного становится вполное удовлетворительным, и в это время на фоне нарушения диеты возможна перфорация язв с развитием перитонита. Неоднократно описывали перитонит на фоне "амбулаторного брюшного тифа", переносимого больными на ногах. В этих случаях причиной перитонита может быть попадание в брюшную полость распадающихся ме-зентериальных лимфатических узлов при их некрозе или пульпы селезенки при надрыве ее капсулы (последнее возникает при суб-капсулярном расположении брюшнотифозных гранулем.
К внекишечным осложнениям брюшного тифа относят гнойный перихондрит гортани, восковидные (ценкеровские) некрозы прямых мышц живота, периоститы большеберцовой кости, ребер и межпозвоночных дисков, остеомиелиты, артриты, цистит, простатит. Большинство этих осложнений отмечали в до-антибиотический период, сейчас они представляют лишь исторический интерес. В настоящее время описывают множество ос-
ложнений, которые возникают у больных в связи с присоединением вторичной инфекции, прежде всего стафилококков, пневмококков, стрептококков. В этих случаях развиваются очаговая пневмония с поражением нижних долей, внутримышечные абсцессы.
Брюшнотифозный сепсис встречается крайне редко, при этом местные (кишечные) изменения могут отсутствовать (typhus sine typho), но ярко выражен "тифозный статус" больного: бред, потеря сознания, нарушение слуха, гектическая температура. В настоящее время при брюшном тифе "тифозный статус" встречается крайне редко (не более 2,8 %).
Прогноз. До применения антибиотиков летальность при брюшном тифе достигала 20 %. В настоящее время прогноз благоприятный, смерть наступает в 1—3 % случаев обычно от осложнений (внутрикишечное кровотечение, перитонит, пневмония, сепсис). Фатальным чаще всего оказывается перитонит, который имеет вялое течение, и при нем погибают до 50 % больных. Брюшной тиф — инфекция, редкая хотя бы потому, что уже много лет поддается левомицетиновой терапии, и при которой в отличие от большинства бактериальных инфекций не образуются антибиотикоустойчивые штаммы. Однако возможно развитие осложнений в связи с передозировкой антибиотиков, когда одномоментная гибель большого числа сальмонелл приводит к коллапсу, парезу сосудистой стенки, развитию ДВС-синдрома. После перенесенного заболевания возможно развитие бактерионосительства, которое проходит спонтанно в течение года, однако 3 % больных остаются бактерионосителями пожизненно (хроническое носительство) с локализацией возбудителя в желчных путях.
Эшерихиозы — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечной палочки, протекающих с симптомами общей интоксикации и поражением ЖКТ.
Классификация
Этиология и патогенез
Эшерихии — подвижные грамотрицательные палочки, аэробы, относящиеся к виду Escherichia coli, роду Escherichia, семейству Enterobacteriaceae. Растут на обычных питательных средах, выделяют бактерицидные вещества-колицины. Морфологически серотипы не отличаются друг от друга. Эшерихии содержат соматические (О-Аг — 173 серотипа), капсульные (К-Аг — 80 серотипов) и жгутиковые (Н-Аг — 56 серотипов) антигены. Диареегенные кишечные палочки подразделяются на пять типов:
Факторы патогенности ЭТКП (пили, или фимбриальные факторы) определяют склонность к адгезии и колонизации нижних отделов тонкой кишки, а также к токсинообразованию. Термолабильный и термостабильный энтеротоксины ответственны за повышенную экскрецию жидкости в просвет кишки. Патогенность ЭПКП обусловлена способностью к адгезии. ЭИКП способны, имея плазмиды, проникать в клетки кишечного эпителия и размножаться в них. ЭГКП выделяют цитотоксин, шигоподобные токсины 1-го и 2-го типов, содержат плазмиды, которые облегчают адгезию к энтероцитам. Факторы патогенности энтероадгезивных кишечных палочек изучены недостаточно.
Эшерихии устойчивы в окружающей среде, могут месяцами сохраняться в воде, почве, испражнениях. Сохраняют жизнеспособность в молоке до 34 дней, в детских питательных смесях — до 92 дней, на игрушках — до 3-5 мес. Хорошо переносят высушивание. Обладают способностью размножаться в пищевых продуктах, особенно в молоке. Быстро погибают при воздействии дезинфицирующих средств и при кипячении. У многих штаммов Е. coli отмечают полирезистентность к антибиотикам.
Эшерихии проникают через рот, минуя желудочный барьер, и в зависимости от типовой принадлежности оказывают патогенное действие.
Энтеротоксигенные штаммы способны вырабатывать энтеротоксины и фактор колонизации, посредством которого осуществляются прикрепление к энтероцитам и колонизация тонкой кишки.
Энтеротоксины — термолабильные или термостабильные белки, которые воздействуют на биохимические функции эпителия крипт, не вызывая видимых морфологических изменений. Энтеротоксины усиливают активность аденилатциклазы и гуанилатциклазы. При их участии и в результате стимулирующего действия простагландинов увеличивается образование цАМФ, вследствие чего в просвет кишки секретируется большое количество воды и электролитов, которые не успевают реабсорбироваться в толстой кишке, — развивается водянистая диарея с последующими нарушениями водно-электролитного баланса. Инфицирующая доза ЭТКП — 10х10 10 микробных клеток.
ЭИКП обладают свойством внедряться в клетки эпителия толстой кишки. Проникая в слизистую оболочку, они вызывают развитие воспалительной реакции и образование эрозий кишечной стенки. Из-за повреждения эпителия усиливается всасывание в кровь эндотоксинов. У больных в испражнениях появляются слизь, кровь и полиморфно-ядерные лейкоциты. Инфицирующая доза ЭИКП — 5х10 5 микробных клеток.
Механизм патогенности ЭПКП изучен недостаточно. У штаммов (055,086,0111 и др.) выявлен фактор адгезии к клеткам Нер-2, за счёт которого происходит колонизация тонкого кишечника. У других штаммов (018, 044, 0112 и др.) этот фактор не обнаружен. Инфицирующая доза ЭПКП — 10х10 10 микробных клеток.
ЭГКП выделяют цитотоксин (SLT — shiga-like toxin), который разрушает клетки эндотелия, выстилающего мелкие кровеносные сосуды кишечной стенки проксимальных отделов толстой кишки. Сгустки крови и фибрин препятствуют кровоснабжению кишки — в кале появляется кровь. Развивается ишемия кишечной стенки, вплоть до некроза. У некоторых больных наблюдают осложнения с развитием синдрома диссеминированного внутрисосудистого свёртывания (ДВС), ИТШ и ОПН.
ЭАКП способны к колонизации эпителия тонкой кишки. Вызванные ими заболевания взрослых и детей протекают длительно, но легко. Это связано с тем, что бактерии прочно закрепляются на поверхности эпителиальных клеток.
Эпидемиология
Основной источник эшерихиозов — больные со стёртыми формами заболевания, меньшую роль играют реконвалесценты и носители. Значимость последних возрастает, если они работают на предприятиях по приготовлению и реализации пищевых продуктов. По некоторым данным, источник возбудителя при энтерогеморрагических эшерихиозах (0157) — крупный рогатый скот. Инфицирование людей происходит при употреблении продуктов, которые были недостаточно термически обработаны. Механизм передачи — фекально-оральный, который осуществляется пищевым, реже — водным и бытовым путём. По данным ВОЗ, для энтеротоксигенных и энтероинвазивных эшерихии характерен пищевой, а для энтеропатогенных — бытовой путь.
Из пищевых продуктов чаще фактором передачи служат молочные изделия, готовые мясные продукты, напитки (квас, компот и др.).
В детских коллективах инфекция может распространяться через игрушки, загрязнённые предметы обихода, руки больных матерей и персонала. Реже регистрируют водный путь передачи эшерихиозов. Наиболее опасно загрязнение открытых водоёмов, которое происходит в результате сброса необезвреженных хозяйственно-бытовых сточных вод, особенно из детских учреждений и инфекционных больниц.
Основу профилактики эшерихиозов составляют меры по пресечению путей передачи возбудителя. Особенно важно соблюдать санитарно-гигиенические требования на объектах общественного питания, водоснабжения; предупреждать контактно-бытовой путь заражения в детских учреждениях, родильных домах, стационарах (использование индивидуальных стерильных пелёнок, обработка рук дезинфицирующими растворами после работы с каждым ребёнком, дезинфекция посуды, пастеризация, кипячение молока, молочных смесей). Продукты, готовые к употреблению, и сырые, нужно разделывать на разных досках отдельными ножами. Посуду, в которой транспортируют пищу, необходимо обрабатывать кипятком.
При подозрении на эшерихиоз необходимо обследовать беременных до родов, рожениц, родильниц и новорождённых.
Контактных в очаге заболевания наблюдают 7 дней. Детей, контактных с больным эшерихиозом по месту жительства, допускают в детские учреждения после разобщения с больным и трёхкратных отрицательных результатов бактериологического исследования кала.
При выявлении больных эшерихиозом в детских учреждениях и родильных домах прекращают приём поступающих детей и рожениц. Персонал, матери, дети, бывшие в контакте с больным, а также дети, выписанные домой незадолго до заболевания, обследуются трёхкратно (проводят бактериологическое исследование кала). При выявлении лиц с положительными результатами обследования их изолируют. Больных, перенёсших эшерихиоз, наблюдают в течение 3 мес с ежемесячным клиническим и бактериологическим обследованием в КИЗ. Перед снятием с учёта — двукратное бактериологическое исследование кала с интервалом в 1 день.
Клиническая картина
Cимптомы, течение
Клинические проявления эшерихиозов зависят от типа возбудителя, возраста больного, иммунного статуса.
Заболевание начинается остро, больных беспокоят слабость, головокружение. Температура тела нормальная или субфебрильная. Появляются тошнота, повторная рвота, разлитые схваткообразные боли в животе. Стул частый (до 10-15 раз в сутки), жидкий, обильный, водянистый, нередко напоминающий рисовый отвар. Живот вздут, при пальпации определяют урчание, небольшую разлитую болезненность. Тяжесть течения определяется степенью дегидратации. Возможна молниеносная форма заболевания с быстрым развитием эксикоза. Длительность болезни 5-10 дней.
Особенности эшерихиоза, вызванного энтероадгезивными штаммами, изучены мало. Заболевание регистрируют у пациентов с ослабленной иммунной системой. Чаще выявляют внекишечные формы — поражение мочевыводящих (пиелонефрит, цистит) и желчевыводящих (холецистит, холангит) путей. Возможны септические формы (коли-сепсис, менингит).
Диагностика
Клиническая картина эшерихиозов сходна с клинической картиной других диарейных инфекций. Поэтому диагноз подтверждают на основании бактериологического метода исследования. Материал (испражнения, рвотные массы, промывные воды желудка, кровь, моча, ликвор, жёлчь) следует брать в первые дни болезни до назначения больным этиотропной терапии. Посевы производят на среды Эндо, Левина, Плоскирева, а также на среду обогащения Мюллера.
Используют иммунологические методы исследования РА, РИГА в парных сыворотках, но они не убедительны, так как возможны ложноположительные результаты из-за антигенного сходства с другими энтеробактериями. Эти методы используют для ретроспективной диагностики, особенно во время вспышки.
Перспективным методом диагностики служит ПЦР. Инструментальные методы исследования (ректороманоскопия, колоноскопия) при эшерихиозах малоинформативны.
Дифференциальный диагноз
Дифференциальную диагностику эшерихиозов проводят с другими острыми диарейными инфекциями: холерой, шигеллёзом, сальмонеллёзом, кампилобактериозом, ПТИ стафилококковой этиологии и вирусными диареями: ротавирусной, энтеровирусной, Норволк-вирусной инфекцией и др.
В отличие от эшерихиозов, холера характеризуется отсутствием интоксикации, лихорадки, болевого синдрома, наличием многократной рвоты, быстрым развитием дегидратации III-IV степени. Помогает в постановке диагноза эпидемиологический анамнез — пребывание в эндемичных для холеры регионах.
Сальмонеллёз, в отличие от эшерихиозов, характеризуется более выраженной интоксикацией, разлитыми болями в животе, болезненностью при пальпации в эпигастральной и околопупочной областях, урчанием. Характерен зловонный стул зеленоватого цвета.
Для ПТИ стафилококковой этиологии, в отличие от эшерихиозов, характерны острое, бурное начало заболевания, короткий инкубационный период (30-60 мин), более выражены симптомы интоксикации, рвота неукротимая. Боли в животе режущего характера, с локализацией в эпигастральной и околопупочной областях. Характерны групповой характер заболевания, связь заболевания с пищевым фактором, быстрый регресс болезни.
Осложнения
Чаще эшерихиозы протекают доброкачественно, но возможны осложнения: ИТШ, гиповолемический шок с дегидратацией III-IV степени, ОПН, сепсис, пневмония, пиелоцистит, пиелонефрит, холецистит, холангит, менингит, менингоэнцефалит. Летальный исход в результате ОПН (синдром Гассера) регистрируют у детей до 5 лет в 3-7% случаев. В Москве за последние 10 лет летальных исходов не было.
Лечение
В остром периоде болезни больным рекомендуют щадящую терапию (стол № 4, при нормализации стула — № 2, в период реконвалесценции — № 13).
В лёгких случаях заболевания достаточно назначения оральной регидратационной терапии (регидрон и другие растворы, количество которых должно в 1,5 раза превышать потери воды с испражнениями).
Показаны ферменты (панзинорм-форте, мезим-форте), энтеросорбенты (полисорб, энтеросгель, энтеродез в течение 1-3 дней). При лёгком течении болезни целесообразно использование кишечных антисептиков (интетрикс по две капсулы три раза в день, неоинтестопан после каждого акта дефекации по две таблетки, до 14 в сутки, энтерол по две капсулы два раза в день) в течение 5-7 дней. Лёгкие и стёртые формы эшерихиозов не требуют назначения этиотропных препаратов.
При лечении больных в условиях стационара показан постельный режим в первые 2-3 дня. Назначают этиотропную терапию. С этой целью при среднетяжёлых формах используют один из следующих препаратов: ко-тримоксазол по две таблетки два раза в день или препараты фторхинолонового ряда (ципрофлоксацин по 500 мг два раза в сутки перорально, пефлоксацин по 400 мг два раза в сутки, офлоксацин по 200 мг два раза в сутки), длительность терапии 5-7 дней.
В тяжёлых случаях фторхинолоны применяют вместе с цефалоспоринами 2-го (цефуроксим по 750 мг четыре раза в сутки внутривенно или внутримышечно; цефаклор по 750 мг три раза в сутки внутримышечно; цефтриаксон 1,0 г один раз в сутки внутривенно) и 3-го поколения (цефоперазон по 1,0 г два раза в сутки внутривенно или внутримышечно; цефтазидим по 2,0 г два раза в сутки внутривенно или внутримышечно).
При дегидратации II-III степени назначают регидратационную терапию внутривенно кристаллоидными растворами (хлосоль, ацесоль и пр.), которую проводят по общим правилам.
При выраженных симптомах интоксикации используют коллоидные растворы (декстран и др.) в объёме 400-800 мл/сут.
После приёма антибактериальных препаратов при продолжающейся диарее используют эубиотики для коррекции дисбактериозов (бифидумбактерин-форте, хилак-форте и др.) в течение 7-10 дней. Больных выписывают после полного клинического выздоровления, нормализации стула и температуры тела, а также однократного бактериологического исследования кала, которое проводят не ранее чем через 2 дня после окончания лечения.
При лёгкой форме заболевания 5-7 дней, при среднетяжёлой 12-14 дней, при тяжёлой — 3-4 нед. Диспансеризация не регламентирована.
Госпитализация
Госпитализацию больных с эшерихиозами проводят по клиническим и эпидемиологическим показаниям. Больных при среднетяжёлом и тяжёлом течении заболевания госпитализируют в инфекционные больницы. В лёгких случаях больные могут лечиться амбулаторно при наличии благоприятных бытовых, санитарно-гигиенических условий.
По эпидемиологическим показаниям госпитализации подлежат лица из декретированных групп, больные из организованных коллективов, а также пациенты, проживающие в коммунальных квартирах, общежитиях.
Читайте также:

