Оспа имеет клеточное строение
Обновлено: 18.04.2024
Натуральная оспа представляет собой инфекционное заболевание человека, относящееся к особо опасным инфекциям, вызываемое вирусом Orthopoxvirus variola, характеризующееся лихорадкой, интоксикацией и специфическими высыпаниями на коже и слизистых оболочках. Распространение натуральной оспы происходит аэрозольным путем, при этом возбудитель настолько устойчив в воздушной среде, что может вызывать заражение людей, находящихся не только в одной комнате с больным, но и в соседних помещениях. В середине 70-х годов ХХ века полная ликвидация натуральной оспы в развитых странах привела к отмене профилактической вакцинации против этого заболевания.
Общие сведения
Натуральная оспа представляет собой инфекционное заболевание человека, относящееся к особо опасным инфекциям, вызываемое вирусом Orthopoxvirus variola, характеризующееся лихорадкой, интоксикацией и специфическими высыпаниями на коже и слизистых оболочках.
Характеристика возбудителя
Вирус Orthopoxvirus variola входит в группу вирусов оспы животных и человека, устойчив в окружающей среде, легко переносит понижение температуры и высыхание, может сохранять жизнеспособность при замораживании в течение нескольких лет. При комнатной температуре сохраняется в оспенных корочках до года, в мокроте и слизи – до трех месяцев. При нагревании до 100° С вирус в высушенном виде погибает только через 5-10 минут.
Натуральная оспа передается по аэрозольному механизму преимущественно воздушно-капельным и воздушно-пылевым путями. Аэрозоль с возбудителем способен перемещаться с током воздуха на значительное расстояние, поражая людей, располагающихся в одной комнате с больным, и проникая в соседние помещения. Оспа имеет тенденцию к распространению в многоэтажных многоквартирных помещениях, лечебных учреждениях, скученных коллективах.
Естественная восприимчивость человека – высокая. Неиммунизированные лица заражаются в подавляющем большинстве случаев, процент невосприимчивых лиц составляет не более 12 из 100 непривитых (в среднем 5-7%). После перенесения заболевания формируется стойкий длительный (более 10 лет) иммунитет.
Симптомы натуральной оспы
Инкубационный период натуральной оспы обычно составляет 9-14 дней, может увеличиваться до 22 дней. Выделяют периоды заболевания: продромальный (или период предвестников), высыпаний, нагноения и реконвалесценции. Продромальный период длится от двух до четырех дней, отмечается лихорадка, симптомы интоксикации (головная боль, озноб, слабость, боли в мышцах, пояснице). В это же время на бедрах и груди может обнаруживаться сыпь, напоминающая экзантему при кори или скарлатине.
К концу продромального периода лихорадка, обычно, спадает. На 4-5 сутки появляется оспенная сыпь (период высыпания), первоначально представляющая собой мелкие розеолы, прогрессирующие в папулы, а через 2-3 дня – в везикулы. Везикулы имеют вид многокамерных мелких пузырьков, окруженных гиперемированной кожей и имеющих небольшое пупковидное углубление в центре. Сыпь локализуется на лице, туловище, конечностях, не исключая ладони и подошвы, в отличие от ветряной оспы элементы сыпи в одной зоне мономорфны. С прогрессированием сыпи снова нарастает лихорадка и интоксикация.
К концу первой недели заболевания, в начале второй, начинается период нагноения: температура резко поднимается, состояние ухудшается, сыпные элементы нагнаиваются. Оспины теряют свою многокамерность, сливаясь в единую гнойную пустулу, становятся болезненными. Спустя неделю пустулы вскрываются, образуя черные некротические корочки. Кожа начинает сильно зудеть. На 20-30 сутки наступает период реконвалесценции. Температура тела больного постепенно нормализуется с 4-5 неделе заболевания, оспины заживают, оставляя после себя выраженное шелушение, а в дальнейшем - рубцы, иногда весьма глубокие.
Выделяют тяжелые клинические формы оспы: папулезно-геморрагическую (черная оспа), сливную и оспенную пурпуру. Среднетяжелое течение имеет оспа рассеянная, легкое – оспа без сыпи и температуры: вариолоид. В такой форме оспа протекает обычно у привитых лиц. Характерны редкие высыпания, не оставляющие после себя рубцов, интоксикационные симптомы отсутствуют.
Осложнения натуральной оспы
Чаще всего натуральная оспа осложняется инфекционно-токсическим шоком. Отмечают осложнения воспалительного характера со стороны нервной системы: миелиты, энцефалиты, невриты. Есть вероятность присоединения вторичной инфекции и развития гнойных осложнений: абсцессов, флегмон, лимфаденитов, пневмонии и плеврита, отитов, остеомиелита. Может развиться сепсис. После перенесения оспы могут остаться последствия в виде слепоты или глухоты.
Диагностика и лечение натуральной оспы
Диагностика натуральной оспы производится с помощью вирусоскопического исследования с использованием электронного микроскопа, а так же вирусологическими и серологическими методами: микропреципитация в агаре, ИФА. Исследованию подлежит отделяемое оспенных пустул и корочки. С 5-8 дня заболевание возможно определение специфических антител с помощью РН, РСК, РТГА, ИФА.
Лечение натуральной оспы заключается в назначении противовирусных препаратов (метисазон), введении иммуноглобулинов. Кожу, пораженную оспенной сыпью, обрабатывают антисептическими средствами. Дополнительно (ввиду гнойного характера инфекции) назначается антибиотикотерапия: применяют антибиотики групп полусинтетических пенициллинов, макролидов и цефалоспорины. Симптоматическая терапия заключается в активной дезинтоксикации с помощью внутривенной инфузии растворов глюкозы, водно-солевых растворов. Иногда в терапию включают глюкокортикоиды.
Прогноз и профилактика натуральной оспы
Прогноз зависит от тяжести течения и состояния организма больного. Привитые лица, как правило, переносят оспу в легкой форме. Тяжело протекающая оспа с геморрагическим компонентом может закончиться смертью.
В настоящее время специфическая профилактика оспы производится с целью не допустить ее завоза из эпидемически опасных регионов. Ликвидация оспы в развитых странах достигнута благодаря массовой вакцинации и ревакцинации населения на протяжении нескольких поколений, в настоящее время плановая всеобщая вакцинация нецелесообразна. В случае выявления больного натуральной оспой, осуществляют его изоляцию, а так же производят карантинные мероприятия в отношении всех, имевших контакт с больным. В очаге инфекции производят тщательную дезинфекцию, контактных лиц вакцинируют в течение первых трех дней с момента контакта.
Вирусы оспы. Виды вирусов оспы. Строение вирусов оспы.
Вирусы оспы (ВО) — самые крупные вирусы, содержащие ДНК, молекулярная масса которой больше, чем у любого другого вируса животных. Они широко распространены в природе, вызывают заболевания позвоночных и беспозвоночных с летальным исходом или в виде легко протекающей продолжительной инфекции с образованием доброкачественных опухолей. ВО передаются членистоногими при прямом контакте, аэрозольно или механически. ВО обычно имеют узкий круг хозяев, хотя некоторые из них представляют исключения, в том числе вирусы вакцины и оспы птиц. Вирусы оспы позвоночных включают восемь родов (орто-, пара-, ави-, капри-, лепори-, суи-, моллюсци- и ятапоксвирусы).
Разделение вирусов оспы позвоночных на роды проведено с учетом массы и структуры генома, размера и формы вириона, способности к генетической рекомбинации, антигенной связи и спектра патогенности.
Ортопоксвирусы. Типичный представитель - вирус осповакцины (ВОВ). Спектр естественных хозяев узкий, обычно ограничен одним видом животных: вирусы агглютинируют эритроциты цыплят; варьируют по вирулентности для естественных хозяев и лабораторных животных. Другие виды: вирусы оспы буйволов, верблюдов, крупного рогатого скота, мышей, обезьян и вирус натуральной оспы.
Парапоксвирусы. Типичный представитель — вирус контагиозного пустулёзного дерматита (эктимы) овец и коз (вирус орф). Представители рода серологически связаны между собой, но отличаются от представителей других родов; гемагглютинин не образуют. Другие виды: вирусы пустулёзного стоматита крупного рогатого скота, контагиозной эктимы серн и сыпи доярок.
Авипоксвирусы. Естественные хозяева — птицы; типичный представитель — вирус оспы кур. Члены рода серологически связаны между собой. Другие виды: вирусы оспы канареек, голубей, перепелов, воробьев, скворцов, индеек и оспы Юнко. Передаются членистоногими.
Каприпоксвирусы. Естественные хозяева — парнокопытные; типичный представитель — ВО мелких жвачных (овец и коз). В данный род входит также вирус кожной бугорчатки крупного рогатого скота.
Лепорипоксвирусы. Типичный представитель — вирус миксомы кроликов. Передается механически членистоногими. Другие виды: вирусы фибромы зайцев, кроликов (вирус Шоупа) и белок. Вирус злокачественной фибромы кроликов — летальный туморогенный поксвирус, возникший, по-видимому, вследствие рекомбинации между вирусами фибромы и миксомы кроликов.
Суипоксвирусы. Типичный представитель — вирус оспы свиней. В инфицированных клетках образуются несколько типов цитоплазматических включений и наблюдается вакуолизация ядра. Другие члены рода не определены.
Моллюсципоксвирусы. Типичный представитель — вирус контагиозного моллюска. Возможные члены рода — вирусы однокопытных и обезьян.
Ятапоксвирусы включают вирус опухолей обезьян Яба и вирус оспы Тана.
Вирусы оспы — наиболее крупные из всех вирусов животных. Под электронным микроскопом они выглядят как большие овальные (кирпичеобразные) частицы размером около 250-350x200-270 нм.
Орто-, ави-, лепорипоксвирусы более вытянуты, а вирус оспы свиней шире, чем другие ВО. Парапоксвирусы имеют овальную (коконообразную) форму и размер 260x160 нм.
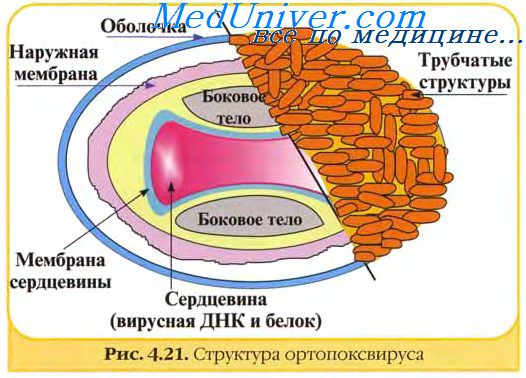
В структуре вирусов оспы различают три основных компонента: двояковогнутую сердцевину, овальные боковые тела и оболочку вириона. Сердцевину вириона составляют ДНК и связанные с нею белки. Сердцевина окружена гладкой мембраной (толщиной около 5 нм), снаружи покрытой слоем вертикально уложенных и плотно прилегающих друг к другу цилиндрических субъединиц (5x10 нм). Вогнутость сердцевины с обеих сторон занята овальными образованиями (неизвестной природы), называемыми боковыми телами. Они как бы сдавливают сердцевину, придавая ей форму двояковогнутого диска, имеющего на разрезе вид гантели.
Вирионы заключены в липопротеиновую супероболочку, которая имеет толщину 20—30 нм и содержит липиды клетки и вирусспецифические белки.
Вирионы большинства вирусов оспы окружены слоем беспорядочно расположенных трубчатых структур, придающих им характерный вид. Эти структуры состоят из сферических субъединиц диаметром около 5 нм. Субъединицы построены из молекул протеина или гликопротеина. В состав ворсинок длиной 20 нм покрывающих поверхность вируса осповакцины (ВОВ), входит белок с молекулярной массой 58 кД, относящийся к главным полипептидам вириона. Поверхность парапоксвирусов покрыта длинными нитеподобными трубочками, уложенными крест-накрест, напоминающими клубок пряжи.
Вирус осповакцины содержит белки, липиды и ДНК, которые соответственно составляют 90, 5 и 3,2% массы вириона (5х10~15 г). В вирусе оспы птиц около 1/3 массы составляют липиды.
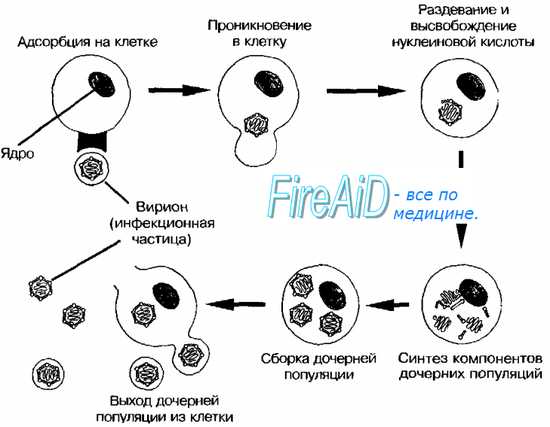
Вирион образуется включением ДНК внутрь незрелых вирусоподобных частиц, которые затем созревают, покрываясь дополнительно наружными оболочками. Репликация и сборка вирионов происходят в разных местах цитоплазмы (в виропластах или вирусных фабриках), и вирионы освобождаются почкованием или при лизисе клеток.
Вирионы, освободившиеся из клетки почкованием до ее разрушения, покрыты оболочкой, которая содержит клеточные липиды и несколько вирусспецифических белков.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
В заражённых вирусом клетках возможны патологические проявления разностороннего характера.
Морфология патологических эффектов. Зараженные вирусом клетки. Основные реакции зараженных вирусом клеток.
Характерные проявления взаимодействий между вирусом и чувствительными клетками-видимые поражения заражённых клеток вплоть до их гибели, а также присутствие возбудителей в исследуемом материале.
Альтерация и воспаление зараженных вирусом тканей. При вирусных инфекциях на первый план выступает картина повреждения клеток и воспалительных изменений тканей, при различных инфекциях их соотношение и выраженность варьируют. В противоположность бактериальным инфекциям (где доминируют полиморфноядерные лейкоциты), при вирусных поражениях среди клеточных элементов воспалительных реакций доминируют мононуклеары (лимфо- и моноциты). На этапах, предшествующих разрушению клеток, можно визуально наблюдать их дегенеративные и некротические изменения.
Тельца включений зараженных вирусом клеток. Микроскопия заражённых клеток часто позволяет выявить тельца включений — характерный, но не абсолютный признак вирусных поражений. Тельца значительно крупнее, чем отдельные вирионы, и часто окрашиваются кислыми красителями (например, эозином).
• При заражении клеток ДНК-содержащими вирусами тельца включений располагаются в ядре; исключение — тельца включений поксвирусов (тельца Гварнери).
• При заражении клеток РНК-содержашими вирусами тельца включений располагаются в цитоплазме (например, тельца Бабеша-Нёгри, выявляемые в цитоплазме клеток головного мозга при бешенстве).
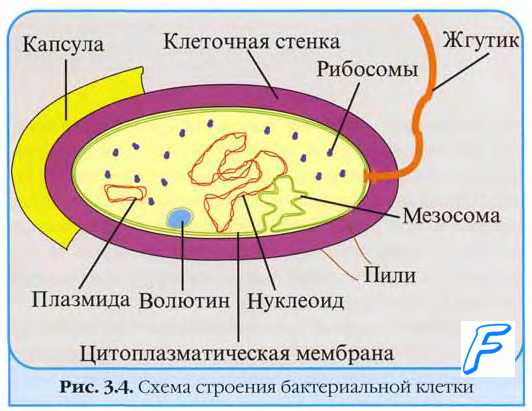
Причины гибели зараженных вирусом клеток. Размножаясь в клетке, вирусы индуцируют синтез вирусспецифических белков, в той или иной степени подавляющих метаболизм клетки. Нарушение синтеза макромолекул вызвано нарушением трансляции клеточной мРНК. Среди РНК-геномных вирусов наиболее быстрое и глубокое подавление макромолекулярных синтезов в клетке вызывают пикорнавирусы, среди ДНК-геномных — покс- и герпесвирусы. Действие указанных вирусов реализуется на ранних этапах (до появления морфологических признаков цитопатического эффекта). Ингибирование синтеза РНК и ДНК обычно вторично по отношению к воздействию на белки, контролирующие экспрессию генов и пролиферацию клетки. Значительно реже нарушения вызывают вирусные белки, напрямую ингибирующие синтез нуклеиновых кислот. Среди РНК-геномных вирусов наиболее быстрое и глубокое подавление синтезов нуклеиновых кислот вызывают пикорнавирусы, среди ДНК-геномных — покс- и герпесвирусы.
Во время репродукции вируса в клетке накапливаются вирусные компоненты, оказывающие токсическое и повреждающее действие на клеточные структуры. Например, цитотоксические свойства проявляют капсомеры некоторых аденовирусов, гликопротеины парамиксовирусов. В процессе вирусной инфекции также происходит повреждение мембран лизосом, содержимое которых высвобождается и осуществляет аутолиз клетки. Таким образом, гибель клеток наступает в результате сочетания раннего подавления синтеза клеточных компонентов, накопления токсических вирусных продуктов и повреждения лизосом.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
Читайте также:

