Острые инфекционные заболевания обострение хронических заболеваний
Обновлено: 24.04.2024
Для эффективного лечения хронических инфекционнных заболеваний предлагаются инновационные подходы, включающие: диагностику - оценку аутоиммунитета, комплексную терапию, направленную на элиминацию возбудителей, восстановление иммунитета, в том числе иммуни
For effective treatment of chronic infectious diseases some innovative approaches were suggested that include: diagnostic, autoimmunity assessment, complex therapy targeted to eliminate the agents, immunity restoration including intestine immunity and further rehabilitation.
Нерешенные проблемы патогенеза, лечения хронических заболеваний встают все острее. В настоящее время показано, что при большинстве хронических заболеваний, ранее считавшихся неинфекционными, выявляются латентные или активные бактериально-вирусные процессы [1, 2].
Хронические инфекционные заболевания, как правило, являются сочетанными (микст-инфекции). Вcе чаще они трудно поддаются лечению, носят рецидивирующий характер, в ряде случаев отмечается их непрерывное течение.
Многократно проводимая антибактериальная терапия оказывается не всегда эффективной, часто имеет место иммуносупрессивное, выраженнное побочное действие антибиотиков. То есть иммуносупрессивная терапия при хронических инфекционных процессах и хронических заболеваниях патогенетически не всегда обоснована. Есть ли альтернатива?
При проведении вакцинации также могут отмечаться побочные эффекты, в том числе выраженные. Введение вакцин в ряде случаев вызывает развитие слабого специфического иммунного ответа, или, наоборот, выявляется гиперреактивность, при этом могут активироваться очаги хронической инфекции, нарушаться механизмы иммунорегуляции, приводящие к развитию аутоиммунных процессов [3].
К решению данных вопросов можно подойти с позиций современных знаний в области иммунофизиологии и иммунопатологии [1–3, 5–7].
Все болезни являются инфекционными, если не доказано другого [1]
Колонизация микроорганизмами слизистых начинается еще внутриутробно (во время беременности, от матери). После рождения микроорганизмы поступают во внутреннюю среду через дыхательные пути, пищеварительный тракт с пищей, по мере взросления этот процесс ассимиляции увеличивается.
Факторами, усиливающими поступление микроорганизмов, являются вредные привычки (например, курение), поездки в различные страны, заболевания желудочно-кишечного тракта.
Один из механизмов воздействия генов микроорганизмов на геном человека следующий. Гены микроорганизмов участвуют в активации ключевого ядерного фактора транскрипции NF-каппа-би, который запускает продукцию ряда белков, поддерживающих воспалительные процессы (ферменты, медиаторы, цитокины).
T. Marshall в своих исследованиях показал, что при аутоиммунных заболеваниях в клетках различных органов, в крови выявляются геномы вируса Эпштейна–Барр, цитомегаловируса, вируса гепатита С, Chlamydia trachomatis, грибов.
То есть геном микроорганизмов (в настоящее время обнаружено более 1 миллиона генов микроорганизмов по сравнению с 25 тысячами генов человека) при большинстве хронических заболеваний выявляется во многих клетках организма.
Феномен антигенной молекулярной мимикрии
При частых обострениях хронических инфекционных процессов, определенном генотипе (особенности HLA-системы), нарушениях в регуляции иммунного ответа может возникнуть аутоиммуный процесс.
Комплексная оценка аутоиммунитета — инновационный подход к диагностике при хронических заболеваниях
В настоящее время хорошо известно, что все основные события, связанные с воспалительными процессами, развиваются в органах, т. е. местно. Изменения в периферической крови указывают на системность, распространенность, наличие выраженной активности воспалительного процесса.
В течение 20 последних лет активно развивается инновационный подход к диагностике различных заболеваний: появился иммунологический метод, позволяющий оценивать наличие и степень выраженности воспалительного процесса в основных органах и системах [5, 6].
Новые подходы к лечению хронических инфекционных процессов
В клетках человека, в лимфоцитах присутствует ядерный рецептор (VDR-рецептор), который участвует в синтезе Toll-подобных рецепторов, распознающих общие детерминанты многих микроорганизмов. Этот механизм участвует в подавлении активности различных патогенов (бактерий, вирусов).
При хронических инфекционных процессах VDR-рецептор заблокирован, инактивирован микроорганизмами.
В настоящее время обнаружено [1], что препарат олмесартана медоксомил (Кардосал) обладает высокой противовоспалительной активностью при различных заболеваниях, в том числе аутоиммунных, он способен восстанавливать активность VDR-рецептора. При этом прием данного препарата должен осуществляться длительно, практически постоянно. Этот препарат относится к группе сартанов (антагонисты рецепторов ангиотензина II) (Диован, Лозап и др.), которые применяются для лечения артериальной гипертензии.
Противовоспалительным эффектом, основанным на новом механизме действия, обладают экстракты босвеллиевой кислоты (из ладанного дерева), экстракты семян сибирской кедровой сосны. При применении данных препаратов происходит блокада активности ядерного фактора NF-каппа-би [4], при этом подавляется синтез провоспалительных цитокинов и др. (интерлейкина-1, фактор некроза опухолей альфа, бета, ряда металлопротеиназ).
В комплексную терапию включается специфическое лечение активной, преобладающей в данный момент бактериально-вирусной инфекции с последующей длительной реабилитацией, которая может осуществляться в течение нескольких месяцев. При этом показали свою высокую эффективность препараты — Глицирам 2 табл. 3 раза в день, производные бетулина — Суперантитокс 50 мг 1 раз в день, экстракты из босвеллиевой кислоты 10 мг 1 раз в день.
В комплексном лечении и реабилитации пациентов с хроническими инфекционными (воспалительными) процессами нами обязательно применяется коррекция состояния кишечника (важнейшего органа иммунитета) и органов желудочно-кишечного тракта, билиарной системы. В частности, пробиотики рекомендуется применять длительно: 2 и более месяцев.
Немного фактов: более 60% всех иммунокомпетентных клеток находится в кишечнике, площадь которого в 10 раз больше площади кожных покровов и составляет более 300 м 2 , кишечник имеет большую метаболическую активность, чем печень, он синтезирует три четверти всех нейротрансмиттеров, в кишечнике находится клеток в 10 раз больше, чем во всем остальном организме.
Состояние иммунитета кишечника ослабляется наличием дисбиоза (синдрома избыточного бактериального роста, повышенной проницаемости, пищевой непереносимости).
Нарушенное состояние кишечника невозможно восстановить без нормализации работы вышележащих органов — желудка, печени, желчного пузыря, поджелудочной железы. Поэтому в комплексную терапию хронических инфекционных заболеваний входит лечение патологий желудочно-кишечного тракта (ЖКТ).
Вакцинация. Спорные вопросы. Предлагаемые решения
Известные иммунологи (академик РАН Черешнев В. А., Shoenfeld Y., 2012) указывают, что введение комплексных вакцин не всегда согласовывается с основными законами функционирования иммунитета: силы, конкуренции антигенов, интервалов, суммации раздражений.
При использовании вакцин описана еще одна достаточно новая проблема — синдром ASIA [3]. Адъюванты, используемые в вакцинах для усиления действия антигенов, могут вызывать у лиц с особенностями генотипа (HLA) повышенную предрасположенность к развитию аутоиммунных процессов. Подобный эффект могут оказывать латекс, силикон.
В наших работах [8, 9] убедительно показано, что у детей с увеличенной вилочковой железой, регистрируемой в момент вакцинации, или имевших гиперплазию тимуса в анамнезе у 60% не вырабатывался защитный титр антител к дифтерийному компоненту вакцин АКДС и АДС (независимо от фирмы-производителя вакцин и лабораторий, в которых контролировался уровень антител). После проведения иммунотропной терапии содержание специфических антител достигало защитного уровня.
В связи с этим мы рекомендуем перед вакцинациями, прежде всего у детей первых месяцев и первых лет жизни, определять величину тимуса (по УЗИ).
Можно ли избежать осложнений при проведении вакцинаций?
Заключение
Рекомендуется перед проведением первой вакцинации детям первых месяцев жизни проводить УЗИ тимуса (диагностика тимомегалии или гипоплазии тимуса) для определения дальнейшей тактики ведения ребенка.
Литература
А. В. Симонова*, доктор медицинских наук, профессор
Л. Г. Кузьменко**, доктор медицинских наук, профессор
И. С. Лебедева*
И. Д. Баранова*, кандидат медицинских наук
В. В. Арзямова**, кандидат медицинских наук
Вирусы — неклеточная форма жизни, которая может воспроизводиться только внутри живых клеток (внутриклеточный паразит). Они вызывают острые и хронические вирусные заболевания. Некоторые из вирусов способны встраивать свою ДНК в хромосомы клетки-хозяина, тем самым вызывая мутации.
Виды хронических вирусных заболеваний
Вирусы способны поражать различные органы и системы человеческого тела. Острые и хронические вирусные заболевания делят на:
- кишечные (ротавирусы);
- респираторные (грипп);
- поражающие ЦНС (энцефалит);
- приводящие к болезням внутренних органов (гепатиты);
- вызывающие болезни кожи и слизистых оболочек (ветряная оспа);
- поражающие сосудистую систему (геморрагические лихорадки);
- нарушающих работу иммунной системы (ВИЧ).
Хроническими вирусными заболеваниями называют патологии, которые часто рецидивируют, вызывая тяжелые поражения центральной нервной системы и внутренних органов, а также подавляют защитные функции иммунной системы.
В зависимости от генетического материала вирусы бывают:
- ДНК-содержащими, состоящими из 1 или 2 спиралей ДНК (аденовирус, герпесвирус, папилломавирус, гепаднавирус);
- РНК-содержащими, которые включают в себя только РНК (ортомиксовирус, флавивирус, ретровирус, полиовирус).
К распространенным острым и хроническим вирусным заболеваниям относятся:
- герпетическая инфекция (поражает все органы и системы, вызывает генитальный герпес, ветряную оспу, герпес губ и т. д.);
- гепатиты (гепатит B, вызывающий цирроз и рак печени);
- ВИЧ (приводит к развитию СПИДа);
- клещевой энцефалит (поражает центральную и периферическую нервную систему);
- краснуха (сопровождается воспалением дыхательных путей, характерной сыпью на коже и интоксикацией);
- ВПЧ (хроническое вирусное заболевание вызывает кожные наросты и может индуцировать онкологические процессы);
- паротит (поражение слюнных и околоушных желез);
- корь (поражает слизистую рта и дыхательных путей, сопровождается сыпью на коже и слизистой);
- инфекционный мононуклеоз (проявляется лимфаденопатией, тонзиллитом, гепатоспленомегалией, лихорадкой);
- грипп (поражение верхних и нижних дыхательных путей с выраженной интоксикацией);
- аденовирусная инфекция (ОРВИ) и т. д.
Стадии развития вирусных заболеваний (острых и хронических)
Жизненный цикл вируса включает в себя такие этапы:
- Адсорбция на клеточной мембране и проникновение в клетку.
- Экспрессия и репликация вирусного генома.
- Сборка вирусов и выход из клетки.
Особенности лечения хронических вирусных заболеваний
Сложность терапии заключается в том, что вирусы являются внутриклеточными паразитами.
Лечение хронических вирусных заболеваний включает в себя:
- этиотропную терапию. Она направлена на уничтожение возбудителей хронических вирусных заболеваний, находящихся внутри клеток, и включает в себя применение препаратов, нарушающих репликацию вируса.
- иммуномодулирующую терапию. Призвана усилить иммунитет организма для борьбы с вирусом.
Хронические вирусные заболевания и иммунитет
Когда вирус проникает внутрь клетки, то функции местного иммунитета выполняют интерфероны и другие цитокины. Вирусные белки в комплексе с антигенами HLA становятся мишенями для несущих соответствующие рецепторы Т-лимфоцитов.
К началу второй недели после заражения активируется гуморальный и клеточный иммунитет. Вырабатываются антитела к вирусу и накапливаются специфичные к нему лимфоциты. Интенсивность иммунного ответа нарастает в течение второй-третьей недели. Выработка антител и накопление лимфоцитов продолжаются еще в течение нескольких месяцев.
В ответ на инфекцию клетки тела также вырабатывают интерфероны α или β. Они подавляют репродукцию вирусов, оказывая воздействие на транскрипцию вирусных геномов.

Внешние факторы не могут ни породить в организме, ни вызвать в нем ничего сверх того, что у него имеется в виде исторически развившихся потенций [8]. Каковы бы ни были внешние условия, они не могут напрямую произвести никаких изменений в организме. Эти изменения возникнут только при наличии соответствующего внутреннего основания. В конечном итоге именно внутренний фактор решает вопрос о возникновении болезни; он же придает ей свои черты в клиническом и морфологическом выражении.
Познание общепатологических механизмов немыслимо без анализа узловых проблем инфекционного процесса. Эволюционное становление воспалительной реакции определялось прежде всего бактериальной инвазией, что убедительно показано еще И.И. Мечниковым. В то же время понять специфические проявления той или иной инфекции, обособленно изучая микро- и макроорганизм, невозможно. Сущность инфекционного процесса открывается лишь в их взаимодействии. Более того, многие важные свойства патогенные микробы вообще не обнаруживают при их росте на искусственных питательных средах [6].
Патогенез инфекционных болезней не исчерпывается непосредственными результатами жизнедеятельности их возбудителей и повреждениями, причиняемыми бактериальными токсинами. Основные симптомы многих инфекционных болезней (лихорадка, кашель, понос и даже нагноение) носят приспособительный характер и отображают не столько повреждение, сколько активную реакцию организма. Так, пирогенные свойства микробных липополисахаридов долгое время представлялись совершенно бесспорными. Между тем выяснилось, что повышение температуры в таких случаях вызывает не сам эндотоксин, а эндогенные пирогены, выделяющиеся из погибающих лейкоцитов. Таким образом, речь идет не о повреждении, а об особом механизме, вступающем в действие под влиянием микробной инвазии и ведущем к температурной реакции, имеющей приспособительное значение. Образование эндогенного пирогена - уникальное свойство фагоцитов, специализирующихся на защите организма [6].
Однако в биологическом взаимодействии паразита с хозяином микроб также занимает свою активную позицию, направленную на выживание вида. Существование в природе многочисленных возбудителей инфекций поддерживается с помощью двух основных механизмов сохранения их видового состава: 1) путем длительной персистенции микробов в организме и 2) путем периодической смены хозяина в процессе бактериовыделения и последующего внедрения в новый организм. По-видимому, у возбудителей с узкой экологической нишей вероятность сохранения вида более надежно обеспечена при их длительном персистировании в организме, чем в процессе беспрерывной смены хозяина. Так, у Mycobacterium tuberculosis сохранение вида в значительной степени определяется их способностью к длительной персистенции, что обусловлено исключительно тесной адаптацией этих бактерий к одному виду хозяина [14]. Основными механизмами персистенции микробов в организме хозяина являются внутриклеточное паразитирование, антигенная мимикрия, образование L-форм, а также механизмы подавления факторов защиты макроорганизма [5, 12, 14]. Они являются биологической основой хронизации инфекционного процесса.
Эпителиальные клетки, подобно фагоцитам мезенхимального происхождения, способны к фагоцитозу. Б.М. Ариэль [2] выдвинул гипотезу, согласно которой при инфекционном процессе в определенных условиях может восстанавливаться фагоцитарная функция эпителия, присущая низко организованным животным и репрессированная в филогенезе. В ходе инфекционного процесса конвергентно сближаются морфологические и функциональные свойства фагоцитов и эпителиальных клеток различного гистогенеза. Эпителий дополняет элиминативную функцию мезенхимных элементов, когда они уже исчерпали свои возможности. Не обладая достаточно эффективными механизмами внутриклеточного разрушения бактерий, эпителиоциты транспортируют их в собственную оболочку, где они, встречаясь с фагоцитами, могут быть уничтожены. Здесь прослеживается один из механизмов отклонения тканевого гомеостаза - нарушение фагоцитарно-элиминативной функции эпителиального пласта. При повреждении (или истощении) этой функции микробы задерживаются, а затем размножаются в цитоплазме эпителиоцитов.
При изучении патогенных факторов микробов целесообразна сравнительная оценка скоростей развития некробиотических и репаративных изменений в тканях. Лишь в том случае, если первая скорость превышает вторую, патогенные факторы микробов приводят к развитию морфологически документируемого повреждения. При инфекционном процессе в первую очередь повреждаются не клетки как таковые, а клеточные популяции, ткани, состоящие из клеток разной дифференцированности и связанные единством происхождения и функции. Основное повреждающее действие на ткани при инфекционном процессе оказывают токсические факторы. Морфологические признаки такого повреждения проявляются в нарушении клеточной дифференцировки и межклеточных контактов, обеспечивающих целостность эпителия как тканевой системы.
Для хронического инфекционного процесса характерно волнообразное течение: фаза обострения при благоприятном течении заболевания сменяется фазой ремиссии и т.д. В фазе ремиссии хронического воспалительного процесса в зоне поражения находят признаки хронического воспаления - макрофагально-лимфоцитарную инфильтрацию (в фазе обострения - нейтрофильную). Что ее поддерживает? Значит, имеет место персистенция причинного фактора [12]. Морфологически в этой фазе наблюдается хроническая (перманентная) дисрегенерация. В чем ее сущность?
Здесь вырисовывается универсальный приспособительный механизм. В фазу ремиссии патогенная инфекция уходит во внутриклеточное персистирование, уклоняясь от иммунной защиты. В ответ на это организм активно включает механизм апоптоза, направленный на элиминацию микробной инфекции. Апоптоз, в свою очередь, вызывает активацию регенераторных процессов. Так поддерживается феномен приспособительного усиления пролиферативной активности ткани в зоне хронического инфекционного процесса (в регенерирующих тканях). В фазе обострения усиление пролиферативных процессов гораздо более выражено в связи с массовой гибелью клеток в зоне воспаления.
Инфекционный процесс во многих случаях начинается не с взаимодействия патогенного микроорганизма с восприимчивым макроорганизмом как таковым, а прежде всего с взаимодействия с микрофлорой хозяина. Микробы-антагонисты на слизистых оболочках осуществляют защитное действие. Так, кишечная микроэкологическая система является частью гомеостатической системы организма. Микроэкология желудочно-кишечного тракта (ЖКТ) включена в систему защиты организма, и при ее нарушении становится источником инфекционного процесса. Основной механизм защиты слизистой ЖКТ - колонизационная резистентность. Пристеночная микрофлора повышает колонизационную резистентность кишечника, конкурируя с патогенными микроорганизмами за взаимодействие с рецепторами эпителиальных клеток слизистой оболочки ЖКТ. Она способствует нормальному течению метаболических процессов в эукариотных клетках [7].
Таким образом, персистенция микробной инфекции в условиях отклонения тканевого гомеостаза барьерных тканей является фундаментальной биологической основой хронизации инфекционного процесса.
Что такое острые респираторные заболевания (ОРЗ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Острые респираторные заболевания (ОРЗ) — группа острых инфекционных заболеваний, при которых возбудители проникают в организм человека через дыхательные пути и вызывают синдром поражения респираторного тракта и общей инфекционной интоксикации. Употребление термина ОРВИ (острое респираторное вирусное заболевание) при отсутствии лабораторно подтверждённой этиологической расшифровки является некорректным.
Этиология
ОРЗ — полиэтиологический комплекс заболеваний, т. е. они могут быть вызваны различными видами возбудителей:
- бактерии (стафилококки, стрептококки, пневмококки, гемофильная палочка, моракселла катаралис и др.);
- вирусы (риновирусы, аденовирусы, респираторно-синцитиальный вирус, реовирусы, коронавирусы, энтеровирусы, герпесвирусы, вирусы парагриппа и гриппа);
- хламидии (х ламидия пневмония , хламидия пситаки, хламидия трахоматис );
- микоплазмы (м икоплазма пневмония ).
Чаще всего возбудителем ОРЗ являются вирусы, поэтому термин ОРВИ используют небезосновательно. В последнее время иногда встречается употребление термина ОРИ (острая респираторная инфекция) [2] [4] .
Эпидемиология
ОРЗ — это преимущественно антропонозы, т. е. болезни, способные поражать только человека . Являются самой многочисленной и частой группой заболеваний у человека (до 80 % всех болезней у детей). Поэтому они представляют серьёзную проблему для здравоохранения различных стран вследствие наносимого ими экономического ущерба.
Источник инфекции — больной человек с выраженными или стёртыми формами заболевания. Восприимчивость всеобщая, иммунитет к некоторым возбудителям (аденовирусы, риновирусы) стойкий, но строго типоспецифичный. Это значит, что заболеть ОРЗ, вызванным одним видом возбудителя, но разными серотипами (их могут быть сотни), можно многократно. Заболеваемость повышается в осенне-зимний период, может принимать вид эпидемических вспышек, довлеет к странам с прохладным климатом. Чаще болеют дети и лица из организованных коллективов (особенно в период адаптации).
Основной механизм передачи — воздушно-капельный (аэрозольный, в меньшей степени воздушно-пылевой путь), но может также играть роль контактно-бытовой механизм (контактный — при поцелуях, бытовой — через загрязнённые руки, предметы или воду) [2] [7] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острых респираторных заболеваний (ОРЗ)
Инкубационный период различен и зависит от вида возбудителя, может варьироваться от нескольких часов до 14 дней (аденовирус).
Для каждого возбудителя ОРЗ имеются свои специфические особенности протекания заболевания, однако все их объединяет наличие синдромов общей инфекционной интоксикации (СОИИ) и поражения дыхательных путей в той или иной степени. СОИИ проявляется общей слабостью, адинамией, быстрой утомляемостью, повышенной температурой тела, потливостью и др.
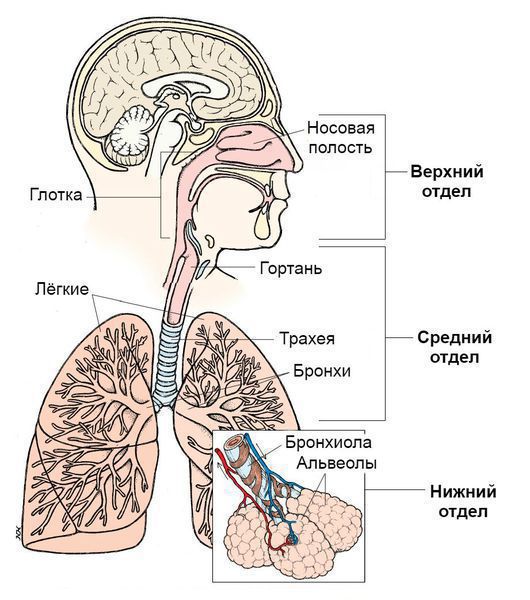
Синдром поражения респираторного тракта (СПРТ) — основной синдром для данных заболеваний, он включает:
- Ринит — воспаление слизистой оболочки носа. Характеризуется заложенностью носа, снижением обоняния, чиханием, выделениями из носа — сначала прозрачными слизистыми, затем слизисто-гнойными (более плотные выделения жёлто-зелёного цвета появляются в результате присоединения вторичной бактериальной флоры). — воспаление слизистой оболочки глотки. Основные симптомы: першение и боли в горле различной интенсивности, сухой кашель — "горловой".
- Ларингит — воспаление слизистых оболочек гортани. Проявляется осиплостью голоса, иногда афонией (отсутствием голоса), кашлем и болью в горле.
- Трахеит — воспаление трахеи. Сопровождается мучительным, преимущественно сухим кашлем, саднением и болями за грудиной.
- Бронхит — воспаление слизистой оболочки бронхов. При этом возникает кашель с наличием мокроты и без, сухие хрипы, редко крупнопузырчатые хрипы при аускультации (выслушивании).
- Бронхиолит — воспаление бронхиол (мелких бронхов). Характеризуется наличием кашля различной интенсивности и хрипов разных калибров.
Дополнительными синдромами могут быть:
- синдром экзантемы (высыпания на кожных покровах);
- тонзиллита (воспаления миндалин);
- лимфаденопатии (ЛАП) — увеличения лимфатических узлов ; ( воспаления слизистой оболочки глаза) ;
- гепатолиенальный синдром (увеличение печени и селезёнки);
- геморрагический синдром ( повышенная кровоточивость) ;
- синдром энтерита (воспаления слизистой оболочки тонкого кишечника) .
Алгоритм по распознаванию ОРЗ различной этиологии:
Наиболее распространенным заболеванием, имеющим тяжёлое течение и высокий риск развития осложнений является грипп. Инкубационный период гриппа длится от нескольких часов до 2-3 дней. В отличие от других острых респираторных заболеваний, при гриппе сначала появляется синдром общей инфекционной интоксикации (высокая температура, озноб, сильная головная боль, слезотечение, боль при движении глазных яблок, ломота в мышцах и суставах). На 2-3-день присоединяются симптомы поражения респираторного тракта: першение в горле, насморк, сухой надсадный кашель.
Типичное ОРЗ начинается с чувства дискомфорта, першения в носу и горле, чихания. В течение непродолжительного периода симптоматика нарастает, першение усиливается, появляется чувство интоксикации, повышается температура тела (обычно не выше 38,5 ℃), появляется насморк, неярко-выраженный сухой кашель. В зависимости от вида возбудителя и свойств микроорганизма могут последовательно появляться все перечисленные синдромы ОРЗ в различных сочетаниях и степени выраженности. Возможно появление осложнений и неотложных состояний [6] [7] .
Патогенез острых респираторных заболеваний (ОРЗ)
- у аденовирусов — гликопротеином (фибриллы);
- у парамиксо- или ортомиксовирусов шипами гемагглютинина;
- у коронавирусов — S-белком соединения и гликолипидами.
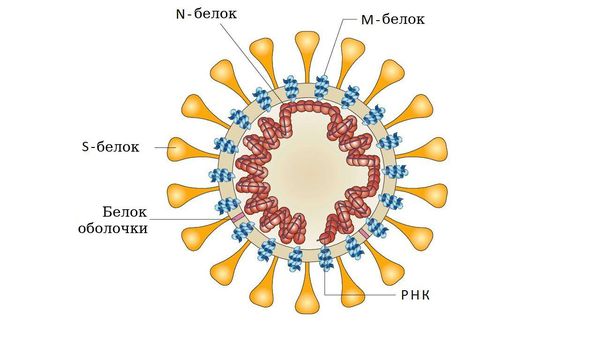
Взаимодействие болезнетворного агента с клеточными рецепторами необходимо не только для прикрепления его к клетке, но и для запуска клеточных процессов, подготавливающих клетку к дальнейшей инвазии. Т. е. наличие соответствующих рецепторов на поверхности клеток — это один из важнейших факторов, определяющих возможность или невозможность возникновения инфекционного процесса. Внедрение возбудителя в клетку хозяина вызывает поток сигналов, активирующих целый ряд процессов, с помощью которых организм пытается от него освободиться, например, ранний защитный воспалительный ответ, а также клеточный и гуморальный иммунный ответ. Повышение метаболизма клеток представляет собой защитный процесс, но с другой стороны в результате накопления свободных радикалов и факторов воспаления запускается патологический процесс:
- нарушается липидный слой клеточных мембран эпителия верхних отделов респираторного тракта и лёгких;
- нарушаются матричные и барьерные свойства внутриклеточных мембран, увеличивается их проницаемость;
- развивается дезорганизация жизнедеятельности клетки вплоть до её гибели.
Второй этап инфицирования характеризуется вирусемией — попаданием вируса в кровь и распространением по всему организму. В совокупности с повышением деятельности защитных механизмов и появлением в крови продуктов распада клеток этот процесс вызывает интоксикационный синдром.
Третий этап характеризуется усилением выраженности реакций иммунной защиты, элиминацию (выведение) микроорганизма и восстановление строения и функции поражённой ткани хозяина [5] [7] .
Классификация и стадии развития острых респираторных заболеваний (ОРЗ)
По вовлечению отдельных частей дыхательной системы:
- Инфекции верхних дыхательных путей. Верхние дыхательные пути начинаются с носа и включают голосовые связки в гортани, придаточные пазухи носа и среднее ухо.
- Инфекции нижних дыхательных путей. Нижние дыхательные пути начинаются с трахеи и бронхов и заканчиваются бронхиолами и альвеолами.
По клинической форме:
- Типичная.
- Атипичная:
- акатаральная (отсутствие признаков поражения дыхательных путей при наличии симптомов общей инфекционной интоксикации);
- стёртая (маловыраженная клиника);
- бессимптомная (полное отсутствие клинической симптоматики).
По течению:
По степени тяжести:
По длительности течения:
- острое (5-10 дней);
- подострое (11-30 дней);
- затяжное (более 30 дней) [8] .
Осложнения острых респираторных заболеваний (ОРЗ)
Если острое респираторное заболевание не пролечить вовремя, могут появиться различные более серьёзные заболевания:
- Связанные с ЛОР-органами: отит, синуситы, бактериальный ринит, ложный круп.
- Связанные с лёгочной тканью: вирусные пневмонии, вирусно-бактериальные и бактериальные пневмонии, абсцесс лёгкого ( ограниченный очаг гнойного воспаления в лёгочной ткани) , эмпиема плевры ( скопление гноя в плевральной полости) . Пневмония проявляется значимым ухудшением общего состояния, выраженным кашлем, усиливающимся на вдохе, при аускультации звуком крепитации ( потрескиванием или похрустыванием) , влажными мелкопузырчатыми хрипами, иногда одышкой и болями в грудной клетке.

- Связанные с поражением нервной системы: судорожный синдром, неврит ( воспаление нерва) , менингит ( воспаление оболочек головного и спинного мозга) , менингоэнцефалит (воспаление оболочек и вещества головного мозга), синдром Гийена—Барре и др. [10]
- Связанные с поражением сердца: миокардит (воспаление сердечной мышцы).
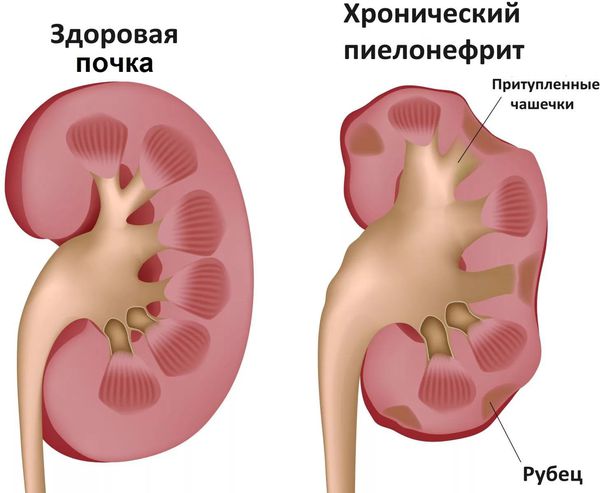
- Связанные с обострением хронических заболеваний: обострение ревматизма, тонзиллита, туберкулёза, пиелонефрита (воспаление почки) и др. [7]
Диагностика острых респираторных заболеваний (ОРЗ)
В широкой рутинной практике лабораторная диагностика ОРЗ (особенно при типичном неосложнённом течении) обычно не проводится. В отдельных случаях могут использоваться:
- Развёрнутый клинический анализ крови. При этом может обнаружиться лейкопения ( снижение количества лейкоцитов) и нормоцитоз ( нормальный размер эритроцитов) , лимфо- и моноцитоз ( увеличение числа лимфоцитов и моноцитов) , при наслоении бактериальных осложнений — нейрофильный лейкоцитоз со сдвигом влево (увеличение количество нейтрофилов и появление их незрелых форм );
- Общеклинический анализ мочи (изменения малоинформативны, указывают на степень интоксикации).
- Биохимические анализы крови. Может выявляться С-реактивный белок (указывает на наличие инфекции). При некоторых системных возбудителях, например аденовирусной инфекции, характерно повышение АЛТ.
- Серологические реакции. Возможна ретроспективная диагностика методами РСК, РА, ИФА, однако она редко используется в практической деятельности. В настоящее время широко применяется ПЦР-диагностика мазков-отпечатков, но её применение ограничено в основном стационарами и научно-исследовательскими группами.
При подозрении на развитие осложнений проводят соответствующие лабораторные и инструментальные исследования (рентген придаточных пазух носа, органов грудной клетки, КТ и др.) [3] [5] .
Лечение острых респираторных заболеваний (ОРЗ)
ОРЗ встречается очень часто и в большинстве случаев протекает в лёгкой и средней степени тяжести, поэтому обычно больные проходят лечение дома. При тяжёлых формах (с риском развития или развившимися осложнениями) пациенты должны проходить терапию в условиях инфекционного стационара до нормализации процесса и появления тенденций к выздоровлению. В домашних условиях лечением ОРЗ занимается терапевт или педиатр (в некоторых случаях инфекционист).
Пища должна быть разнообразной, механически и химически щадящей, богатой витаминами, рекомендуются мясные нежирные бульоны (идеально подходит негустой куриный бульон и т. п.), обильное питьё до — 3 л/сут. (тёплая кипячёная вода, чай, морсы). Хороший эффект оказывает тёплое молоко с мёдом, чай с малиной, отвар брусничных листьев.
Медикаментозная терапия ОРЗ включает в себя этиотропную (т. е. воздействующую на возбудителя заболевания), патогенетическую (дезинтоксикация) и симптоматическую (уменьшение беспокоящих симптомов) терапию.
Этиотропная терапия имеет смысл лишь при назначении в раннем периоде и лишь при ограниченном спектре возбудителей (в основном при гриппе). Использование средств отечественной фарминдустрии ("Арбидол", "Кагоцел", "Изопринозин", "Амиксин", "Полиоксидоний" и т. п.) не обладают никакой доказанной эффективностью и могут иметь эффекта, лишь в качестве плацебо.
В качестве симптоматической терапии могут быть использованы препараты следующих групп:
- жаропонижающие при температуре у взрослых свыше 39,5, у детей — свыше 38,5 ℃ (парацетамол, ибупрофен);
- противовирусные и антибактериальные глазные капли при конъюнктивите;
- сосудосуживающие капли в нос при заложенности носа и насморке (не более 5 дней);
- солесодержащие капли в нос при рините для разжижения слизи;
- противоаллергические препараты при аллергическом компоненте ОРЗ;
- средства противовоспалительного и противомикробного действия местного действия (таблетки, пастилки и др.);
- средства для улучшения образования, разжижения и выделения мокроты (муколитики);
- антибиотики широкого спектра действия (при отсутствии улучшения в течении 4-5 дней, присоединении вторичной бактериальной флоры и развитии осложнений) [2][6] .
Прогноз. Профилактика
Прогноз при ОРЗ — положительный. Больные обычно выздоравливают в течение 5-10 дней без неблагоприятных последствий. Осложнения респираторных заболеваний могут возникнуть при гриппе, другие возбудители менее агрессивны. Также неблагоприятные последствия возможны у пациентов с ослабленным иммунитетом. После выздоровления организмом вырабатывается иммунитет к той инфекции, которой человек переболел .
Ведущую роль в профилактике распространения ОРЗ (исключая грипп) является:

Воспаление – нормальный физиологический процесс, в ходе которого организм пытается устранить причину, вызвавшую повреждение тканей и устранить полученные повреждения. В норме после этого процесс воспаления останавливается, но в некоторых случаях развивается хроническое воспаление.
Хроническое воспаление
В случае хронического воспаления процесс воспаления может начаться даже без явного воздействия внешнего повреждающего фактора и может продолжаться в течение длительного времени. Это может происходить под влиянием некоторых микроорганизмов (вирусов, бактерий, грибов и т.д.) или, например, как следствие ненормальной реакции организма на собственные ткани, что приводит к развитию различных аутоиммунных реакций (болезнь Крона, язвенный колит, атрофический гастрит и т.д.).
Под длительным воздействием воспалительных факторов происходит постоянное повреждение тканей на фоне которого возможно появление злокачественных клеток. Некоторые микроорганизмы-возбудители инфекционных болезней могут повышать риск развития рака. Ниже перечислены наиболее изученные из них.
Вирус папилломы человека (ВПЧ, HPV)
ВПЧ - причина развития практически всех случаев рака шейки матки (РШМ). Кроме того, у носителей данной инфекции значимо повышается риск развития других опухолей наружных половых органов, а также рака головы и шеи. Эта инфекция очень широко распространена в человеческой популяции, так, в США ВПЧ ежегодно поражает около 79 млн. человек. В настоящий момент известно более 150 штаммов этого вируса, при этом только около 15 из них являются онкогенными, т.е. способными приводить к развитию злокачественных новообразований.
В мире РШМ является второй по частоте встречаемости опухолью у женщин. Внедрение повсеместного обследования (скрининга), включающего в себя регулярные осмотры гинекологом со взятием цитологических мазков из шейки матки (цервикального канала), а также определение наличия ДНК ВПЧ в крови позволило резко снизить заболеваемость и смертность от РШМ в развитых странах. На сегодняшний день 9 из 10 случаев смерти от РШМ приходится на бедные регионы и страны.
На сегодняшний день не существует способов лечения ВПЧ, однако в клиническую практику уже внедрены вакцины, которые позволяют резко снизить вероятность развития РШМ, защищая человека от наиболее распространенных штаммов HPV. Очень важно, чтобы вакцинация проводилась до момента первого контакта человека с возбудителем этой инфекции, рекомендуется прививать детей в возрасте от 11 до 12 лет.
Вирусные гепатиты С и В (HCV и HBV)
Хроническая инфекция, вызванная этими возбудителями, может приводить к развитию цирроза и рака печени, кроме этого доказана их связь с развитие некоторых лимфом. В настоящее время широко применяются вакцины против вирусного гепатита B, они позволяют эффективно предотвращать заражение и развитие хронической HBV инфекции, снижая тем самым вероятность развития рака печени.
К сожалению, не существует профилактических вакцин против вируса гепатита С. Это обусловлено высокой мутационной изменчивостью этого вируса, что резко затрудняет разработку и создание таких препаратов. Тем не менее, в настоящее время разработаны весьма эффективные противовирусные лекарственные препараты, которые могут подавить размножение или полностью уничтожить вирус в организме.
Вирус иммунодефицита человека (ВИЧ, HIV)
Этот широко известный вирус вызывает развитие СПИД – синдрома приобретенного иммунодефицита. ВИЧ ослабляет иммунную систему организма, делая её неспособной сопротивляться воздействиям различных микроорганизмов (например тех, что перечислены в этом разделе). Люди, инфицированные ВИЧ, характеризируются повышенным риском развития саркомы Капоши, лимфом, РШМ, печени, легких и других опухолей. Вакцины от ВИЧ не существует, но разработаны специальные препараты для противовирусной терапии, которые позволяют подавить размножение этого вируса и значительно продлить жизнь пациентам.
На фоне подавления иммунитета другого происхождения, например у пациентов, получающих длительное лечение иммуносупрессивными препаратами после трансплантации органов или высокими доза глюкокортикостероидов (например, преднизолон, дексаметазон и т.д.) также повышается риск развития множества опухолей.
Вирусы герпеса
К наиболее онкогенным видам этих вирусов относят вирус Эпштейн-Барр (EBV), который повышает риск развития лимфомы и рака желудка, а также носоглотки. Штамм 8 вируса герпеса ассоциирован с развитием саркомы Капоши.
Бактерии и грибы
Helicobacter pylori (HP) – бактерия, которая может колонизировать слизистую оболочку желудка. На фоне вызванной ей инфекции повышается риск развития язвенной болезни желудка и двенадцатиперстной кишки, а также рака желудка. HP инфекция хорошо поддается лечению антибактериальными препаратами.
Кроме того, некоторые грибки (например, Aspergillus flavus и Aspergillus parasiticus) в процессе своей жизнедеятельности вырабатывают афлатоксины – вредные ещества, которые могут загрязнять сельскохозяйственную продукцию. Распространенность этих грибков велика в жарких и влажных странах, афлатоксины могут попадать в пищу в поле, в процессе сбора урожая и во время её хранения. Употребление в пищу афлатоксинов повышает риск развития рака печени.
Паразиты
К наиболее онкогенным паразитам относят Schistosoma hematobium (возбудитель шистосомоза), который может вызывать рак мочевого пузыря и Opisthorchis viverrini (возбудитель описторхоза), на фоне которого повышается риск развития рака желчевыводящих путей (холингиокарциномы).
Следует помнить, что отсутствие симптомов инфекции не означает отсутствия самой инфекции.
Состоялась встреча группы взаимопомощи Красноярского РО "Здравствуй!"
Прошёл мастер-класс для онкопациентов Кемеровского-Кузбасс РО Ассоциации "Здравствуй" по изготовлению "Воздушного зефира" в преддверии праздника Пасхи
Читайте также:

