Отличие бактерий от микоплазм и риккетсий
Обновлено: 24.04.2024
Об авторе
Добиться успеха можно честным и кропотливым путем, а можно и схитрить. Верно это как в повседневной, так и в биологической жизни. В случае, когда на кону успех репродуктивный (т.е. максимальные численность и распространение), отъявленными жуликами можно назвать паразитов. Их можно встретить на всех уровнях организации живого и в различных царствах. Приемы они могут использовать поведенческие, морфологические, обманывающие восприятие или иммунитет. Есть даже своего рода паразитизм молекулярный, при этом замысел в целом сохраняется: прикинуться кем-то другим или стать незаметным, прокрасться к самому ценному и вероломно его присвоить. Слишком церемониться с хозяином нет нужды — его благополучие не входит в планы паразита, главное — уцелеть самому.
На передовой паразитического фронта находятся самые маленькие клеточные, а значит и живые (omnis cellula e cellula 2 ), организмы. Их размеры менее 1 мкм (вплоть до 100 нм). Есть среди наноорганизмов и внутриклеточные паразиты (например, хламидии, риккетсии, листерии, коксиеллы, микоплазмы, и даже археи, которых в свое время выдворили из царства бактерий в отдельный домен), и честные свободноживущие бактерии, которые, например, обитают в глубинах океана.
Внутриклеточные паразиты — своего рода подрывники, поражающие различные клетки животных (в том числе и человека), включая специализированные (макрофаги) и неспециализированные (фагоциты), эпителиальные и эндотелиальные, а также клетки печени. Как только паразиты пробираются внутрь, им открывается возможность следовать различными путями в цитозоле (основой среде клетки) или изолированных вакуолях. Внеклеточным паразитам приходится иметь дело с гуморальными механизмами иммунитета хозяина и фагоцитозом, обойдя которые, они получают возможность внеклеточного размножения. Внутриклеточные же паразиты стремятся проникнуть главным образом в целевые хозяйские клетки, такие как макрофаги и эпителиальные клетки, где они могут благополучно размножиться. Успешная инфекция требует контакта паразита с определенной клеткой, содержимое которой представляет собой подходящую среду для роста бактерии. Таким образом, их жизнь протекает в пределах клетки, и некоторые из них при необходимости покинуть ее напрямую переходят в другую клетку, добавив к паразитизму еще один порок — домоседство. Однако большинство внутриклеточных паразитов временами могут жить и вне клетки, и именно в этот период у человека могут развиться опасные осложнения — например, сепсис [1].
Скользкий тип
Рассмотрим уникальную в этом отношении микоплазму — M. gallisepticum (рис. 1). А начнем с того, что в ее случае механизмы смены репертуара поверхностных липопротеинов до конца не выяснены. Тем острее интерес!
Рис. 2. Сканирующая электронная микроскопия эритроцитов овцы (а) и курицы (б) после инфекции in vitro штаммом Mycoplasma gallisepticum Rlow [6]. Стрелки указывают на самих микоплазм или следы их внедрения на поверхности эритроцитов
Рис. 3. Схематическое изображение сетей регуляции транскрипции у трех видов Mollicutes: Acholeplasma laidlawii (а), Spiroplasma melliferum (б), Mycoplasma gallisepticum (в). Изогнутая стрелка обозначает промотор; линия с Т-образным концом — репрессию, т.е. подавление активности; широкие стрелки с подписями — соответствующие гены. На гистограммах (г) показано количество транскрипционных факторов у всех трех бактерий
Эти схемы создали сотрудники группы системной биологии Mollicutes (лаборатория протеомного анализа Федерального научно-клинического центра физико-химической медицины), которые разработали новую методику, позволяющую точно идентифицировать координаты сайтов старта транскрипции (transcription start sites, TSSs) при разрешении одного нуклеотида 3 . Метод был применен для точного картирования TSS у трех видов Mollicutes: для свободноживущей бактерии Acholeplasma laidlawii, добывающей пропитание за счет взаимовыгодного (комменсального) симбиоза с растениями и использования разлагающегося субстрата; для паразита домашней пчелы Spiroplasma melliferum и для M. gallisepticum.
Как это работает?
Гены vlhA (значит, и соответствующие им промоторы) разбросаны по рекордно малому (менее 1 млн пар оснований) геному M. gallisepticum. GC-состав — тоже выдающийся, он равен 0,3, т.е. на тугоплавкие пары нуклеотидов G—C (формирующие между собой три водородные связи) приходится менее трети. На объединенные двумя водородными связями пары A—T, как нетрудно посчитать, остается все остальное (0,7). Система регуляции транскрипции предельно упрощена. Из факторов транскрипции — белков, связывающихся в регуляторной части гена и тем самым изменяющих его активность, — остались считанные единицы (см. рис. 3). Несмотря на это, данная микоплазма не просто эффективно меняет свои фазы жизненного цикла (атаковать — осваиваться — размножаться), но делает это чрезвычайно быстро [3]. В чем же ее секрет?
Рис. 4. Схематическое изображение предполагаемого белка HAP (hemagglutinin protease) и место его связывания с последовательностями до и после 12 повторов GAA [7]. Числами указано расстояние (в нуклеотидах) до места начала транскрипции (transcription start site, TSS), буквами — участки расщепления нуклеиновой цепи рестриктазами (H, C и X)
Для чего это нужно?
Подобное положение дел нам удалось описать и для нашего M. gallisepticum. С этой целью мы создали два датасета: в первый вошли промоторы vlhA из 12 различных штаммов M. gallispetium, во второй (для сравнения) — полный набор промоторов генов, не относящихся к семейству vlhA. Первым делом мы взглянули на их нуклеотидную последовательность или, как еще говорят, первичную структуру. Соответствующая визуализация последовательностей представлена на рис. 5 (изображение оригинальное, публикуется впервые). На ней легко заметить необычно длинные консервативные участки, непосредственно прилегающие к треку GAA-повторов с обеих сторон. Их протяженность делает их уникальными для прокариот. А ведь они еще и не имеют гомологов в каких-либо других геномах!
Рис. 5. Выравнивание для всех промоторов семейства vlhA из 12 различных штаммов M. gallisepticum (а) и полного набора прочих генов штамма S6 (б). Первые упорядочены таким образом, что имеющие более короткие GAA-треки расположены выше. Это позволяет легко различать их как желто-красную полосу. Правее них расположены области собственно промотора — ближайшая красно-синяя область (что соответствует обилию аденина и тимина). Создано на основе данных из [3]
Работа выполнена при финансовой поддержке Российского научного фонда (проект № 14-24-00159).
2 Тезис omnis cellula e cellula (‘клетка происходит только от клетки’) ввел Рудольф Вирхов (Rudolf Virchov; 1821–1902) — немецкий ученый, один из основоположников клеточной теории в биологии и клеточной патологии в медицине.
3 Подробнее с методикой и результатами исследований Mollicutes можно ознакомиться на сайте System biology database of Mollicutes (SMDB).
4 Подробнее см.: Орлов М. А. Короткие тандемные повторы // Природа. 2019. № 12. С. 27–33.
Извитые бактерии подразделяют на две основные группы: вибрионы и спирохеты.
У вибрионов и сходных по форме бактерий изогнутость тела не превышает четверти оборота спирали (например, у кампилобактер). Спирохеты имеют изгибы, равные одному или нескольким оборотам спирали (например, возбудитель сифилиса).
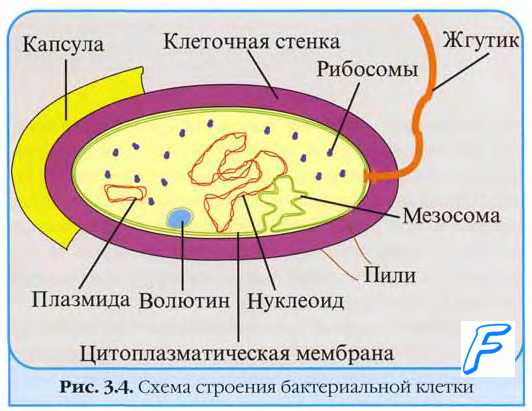
Актиномицеты. Микоплазмы. Хламидии. Риккетсии.
Для некоторых бактерий характерны отклонения от трёх основных форм. Среди коринебактерий часто встречают булавовидные формы, а у некоторых микобактерий, актиномицетов и но-кардий — ветвление клеток.
Актиномицеты — палочковидные грамположительные бактерии, способные к ветвлению. В очагах поражения образуют скопления-друзы, напоминающие отходящие от центра лучи с утолщёнными концами. Именно отсюда произошло их сегодняшнее название [от греч. actis, луч + mykes, гриб]. На питательных средах актиномицеты формируют как субстратный, так и воздушный мицелий, на концах которого могут образовываться споры.
По мере старения культуры мицелий распадается на отдельные палочковидные и кокковидные клетки, морфологически близкие так называемым грамположительным палочкам неправильной формы — микобакте-риям, нокардиям, коринебактериям и др.
Микоплазмы — мелкие бактерии без истинной клеточной стенки. Последнюю заменяет трёхслойная клеточная мембрана, обеспечивающая осмотическую резистентность бактерий. Микоплазмы могут иметь самую разнообразную форму — нитевидную, кокковидную, колбовидную и др.
Хламидии — сферические грамотрицательные бактерии, облигатно паразитирующие в клетках теплокровных организмов. Они значительно меньше, чем обычные шаровидные бактерии.
Риккетсии — мелкие грамотрицательные палочковидные бактерии, облигатно паразитирующие в различных клетках. Морфология риккетсии может существенно меняться в зависимости от условий культивирования. Они могут быть палочковидными, нитевидными или иметь неправильную форму.
L-формы бактерий
Под воздействием некоторых внешних факторов бактерии могут терять клеточную стенку, образуя L-формы (названы в честь Института им. Джозефа Листера, где их впервые выделила Э. Клинебёргер в 1935 г.). Форма подобных клеток может быть весьма разнообразной (нитевидной, шаровидной, палочковидной и т.д.), но практически всегда она отличается от исходной. Подобные превращения могут быть спонтанными или индуцированными (например, под воздействием антибиотиков).
Выделяют стабильные и нестабильные L-формы. Первые не способны к реверсии (то есть обратному восстановлению в исходные формы), а вторые реверсируют после удаления причинного фактора.
Изменённые подобным образом патогенные бактерии способны вызвать персистирующую инфекцию, не реагируя на действие антибиотиков, ингибирующих синтез компонентов клеточной стенки (например, пенициллина). Образование L - форм возможно как in vitro, так и in vivo.
L-формы бактерий образуют многие бактерии. Например, образуются L-формы вибрионов холеры, микобактерий туберкулеза, стрептококков группы Б, менингококков, возбудителя сифилиса и т.д..
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Виды бактерий. Классификация
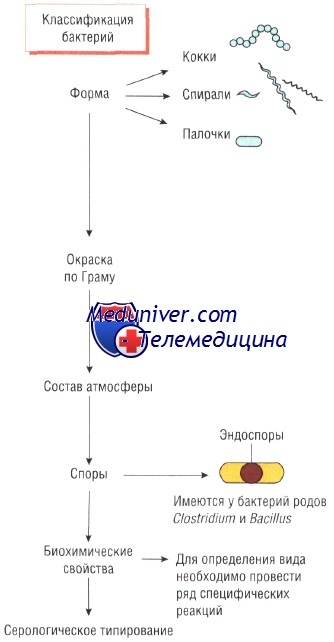
Цель классификации микроорганизмов — определение их патогенности. Например, вероятность развития заболевания при обнаружении в крови Staphylococcus aureus намного выше, чем при наличии Staphylococcus epidermidis. Некоторые бактерии (например, Corynebacterium diphtheriae и Vibrio cholerae) вызывают серьёзные заболевания и обладают способностью к эпидемическому распространению. В основе методов идентификации бактерий лежат их физико-иммунологические или молекулярные свойства.
• Окраска по Граму: чувствительность грамположительных и грамотрицательных бактерий к действию антибиотиков различается. Для идентификации некоторых других микроорганизмов (например, микобактерий) необходимы иные методы окраски.
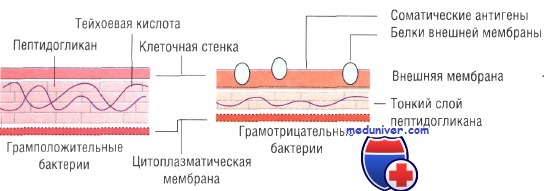
Классификация бактерий по окраске по Граму
• Форма: кокки, палочки или спирали.
• Эндоспоры, их наличие и расположение в бактериальной клетке (терминальные, субтерминальные или центральные).
• Отношение к кислороду: для существования аэробных микроорганизмов необходим кислород, в то время как анаэробные бактерии способны выживать в среде с малым его содержанием или полным отсутствием. Факультативные анаэробы могут жить как в присутствии кислорода, так и без него. Микроаэрофилы быстро размножаются при низком парциальном давлении кислорода, а капнофилы — в среде с высоким содержанием СО2.
• Требовательность: для роста некоторых бактерий необходимы особые условия культивирования.
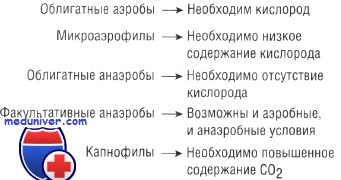
Классификация бактерий по отношению к кислороду
• Эссенциальные ферменты (ферментативная активность): например, недостаток лактозы в среде указывает на присутствие сальмонелл, а уреазный тест помогает определить Helicobacter.
• Серологические реакции возникают при взаимодействии антител с поверхностными структурами бактерий (некоторые виды сальмонелл, Haemophilus, менингококки и др.).
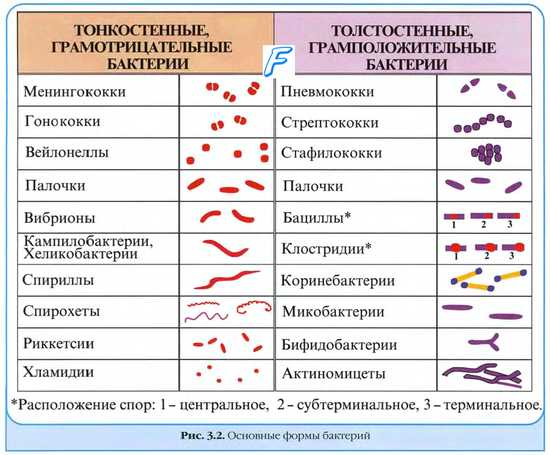
Значимвые в медицине виды бактерий
• Грамположительные кокки:
- стафилококки (каталазоположительные): Staphylococcus aureus и др.;
- стрептококки (каталазоотрицательные): Streptococcus pyogenes, вызывающий ангину, фарингит и ревматическую лихорадку; Streptococcus agalactiae, вызывающий менингит и пневмонию у новорождённых.
• Грамотрицательные кокки: Neisseria meningitidis (возбудитель менингита и септицемии) и N. Gonorrhoeae [возбудитель уретрита (гонореи)].
• Грамотрицательные коккобациллы: возбудители респираторных заболеваний (род Haemophilus и Bordetella), а также зоонозов (рода Brucella и Pasteurella).
• Грамположительные бациллы разделяют на спорообразующие и неспорообразующие бактерии. Спорообразующие бактерии подразделяют на аэробные (род Bacillus, например, Bacillus anthracis, вызывающая сибирскую язву) и анаэробные (Clostridium spp., с ними связаны такие заболевания, как газовая гангрена, псевдомембранозный колит и ботулизм). Неспорообразующие бактерии включают роды Listeria и Corynebacterium.
• Грамотрицательные палочки: факультативные анаэробы семейства энтеробактерий (условно-патогенные представители нормальной микрофлоры человека и животных, а также микроорганизмы, часто встречающиеся в окружающей среде). Наиболее известные представители группы — бактерии родов Salmonella, Shigella, Escherichia, Proteus и Yersinia. В последнее время в качестве возбудителей внутрибольничных инфекций всё чаще выступают антибиотикорезистентные штаммы рода Pseudomonas (сапрофиты, широко распространённые в окружающей среде). При определённых условиях патогенной для человека может стать Legionella, обитающая в водной среде.
• Спиралевидные бактерии:
- мелкие микроорганизмы рода Helicobacter, поражающие желудочно-кишечный тракт человека и вызывающие гастрит, язвенную болезнь желудка и двенадцатиперстной кишки (в некоторых случаях — рак желудка);
- возбудители острой диареи;
- бактерии рода Borrelia, вызывающие эпидемический возвратный тиф (В. duttoni, B. recurrentis); хронические заболевания кожи, суставов и ЦНС; лаймскую болезнь (В. burgdorferi);
- микроорганизмы рода Leptospira, относящиеся к зоонозам, вызывающие острый менингит, сопровождающийся гепатитом и почечной недостаточностью;
- род Treponema (возбудитель сифилиса Т. pallidum).
• Rickettsia, Chlamydia и Mycoplasma. Использование искусственных питательных сред возможно только для выращивания бактерий рода Mycoplasma, в то время как для выделения микроорганизмов родов Rickettsia и Chlamydia необходимо использовать культуру клеток или специальные молекулярные и серологические методы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Цель занятия: знатьморфологию и ультраструктуру риккетсий, хламидий, микоплазм, актиномицет, грибов, простейших; уметьдать описание основным свойствам представителей микромира, использовать микроскопический метод в диагностике инфекционных заболеваний (готовить мазки из исследуемого материала, окрашивать их с помощью различных методов окраски, микроскопировать с масляной иммерсией, описывать морфологические и тинкториальные свойства)
Задание на дом:
I. Вопросы для самоподготовки:
I. Перечислить особенности строения и размножения актиномицет. Перечислить особенности строения, размножения риккетсий. Перечислить особенности строения и размножения хламидий. Перечислить особенности строения, выявления, химический состав микоплазм. Перечислить особенности строения, движения, окраски спирохет. Перечислить особенности строения, размножения грибов, виды мицелия, спор. Перечислить основных представителей патогенных простейших, их морфологические особенности, методы окраски.
II. Актиномицеты
Актиномицеты — это микроорганизмы, занимающие промежуточное положение между бактериями и грибами. Длительное время актиномицеты считали грибами, однако изучение морфологии и биологических свойств позволило отнести их к бактериям семейства Actinomycetaceae отдела Firmicutes. Сходство с грибами определяется способностью к образованию на питательной среде субстратного и воздушного мицелия, на концах которого образуются споры; споры актиномицет являются способом размножения. Однако, в отличие от грибов, клеточная стенка актиномицет не содержит хитина или целлюлозы; они не способны к фотосинтезу, а образуемый ими мицелий достаточно примитивен. Они также резистентны к противогрибковым препаратам. С бактериями актиномицеты объединяет отсутствие четко выраженного ядра, наличие клеточной стенки, а также чувствительность к бактериофагам и антибиотикам.
Актиномицеты — ветвящиеся, нитевидные или палочковидные грамположительные бактерии. Свое название (от греч. actis — луч, mykes— гриб) они получили в связи с образованием в пораженных тканях друз — колоний, состоящие из гранул плотно переплетенных нитей в виде лучей, отходящих от центра и заканчивающихся колбовидными утолщениями. Некислотоустойчивы. Факультативные анаэробы. Актиномицеты могут делиться путем фрагментации мицелия на клетки, похожие на палочковидные и колбовидные бактерии. Споры актиномицетов обычно нетермостойки.
Большинство актиномицет обитают на поверхности слизистых оболочек у млекопитающих; некоторые виды — почвенные сапрофиты. У человека актиномицеты колонизируют слизистые оболочки полости рта и ЖКТ. Способность вызывать специфические поражения не сильно выражена и их рассматривают как условные патогены. Бактерии вызывают актиномикозы — хронические гнойные гранулематозные поражения различных органов.
Подавляющее большинство случаев актиномикозов у людей вызывает А.israelii, в редких случаях А.naeslundii, А.odontolyticus, А.bovis, A.viscosus.
Риккетсии и хламидии— это микроорганизмы, занимающие промежуточное положение между бактериями и вирусами. Как и вирусы, они являются облигатными внутриклеточными паразитами и могут размножаться только в клетке-хозяине. Однако, по своему строению являются мелкими грамотрицательными бактериями.
/. Риккетсии
Риккетсии — мелкие, грамотрицательные полиморфные бактерии (0,3-2,0 мкм), облигатные внутриклеточные паразиты. Капсул и спор не образуют. Жизненный цикл риккетсий включает две стадии — вегетативную (внутриклеточную) и покоящуюся. Вегетативные формы
активно размножаются бинарным делением в цитоплазме, а некоторые — в ядре инфицированных клеток, используя энергетические системы клетки-хозяина, поскольку не способны Спиро синтезировать кофермент НАД и др. метаболиты. Покоящаяся форма обладает повышенной резистентностью с утолщенной клеточной стенкой и уплотненной цитоплазмой.
Обитают в организме членистоногих (вшей, блох, клещей), которые являются их хозяевами или переносчиками. Форма и размер риккетсий могут меняться (клетки неправильной формы, нитевидные, кокковидные, бациллярные) в зависимости от условий роста. В мазках и тканях их окрашивают по Романовскому-Гимзе, по Здродовскому или по Маккиавелло (риккетсии красного цвета, а инфицированные клетки — синего).

Патогенные для человека риккетсии вызывают риккетсиозы; среди них выделяют группы тифов (R.prowazekii, R.typhi) и пятнистых лихорадок (R.ricketsii, R. conorii), Ку-лихорадку (С.burnetii) и др.
2. Хламидии
Хламидии относятся к облигатным внутриклеточным кокковидным грамотрицательным фибрилла (иногда грамвариабельным) бактериям. Они размножаются только в живых клетках. Вне клеток хламидии имеют сферическую форму (0,3 мкм), метаболически неактивны и называются элементарными тельцами. В клеточной стенке элементарных телец имеется главный белок наружной мембраны и белок, содержащий большое количество цистеина. Элементарные тельца попадают в эпителиальную клетку путем эндоцитоза с формированием внутриклеточной вакуоли. Внутри клеток они увеличиваются и превращаются в делящиеся ретикулярные тельца, образуя скопления в вакуолях (включения). Из ретикулярных телец образуются элементарные тельца, которые выходят из клеток путем экзоцитоза или лизиса клетки. Вышедшие из клетки элементарные тельца вступают в новый цикл, инфицируя другие клетки.
Изучают хламидии в живом состоянии с использованием фазово-контрастной микроскопии и окрашивают по методу Романовского-Гимзы (элементарные тельца окрашиваются в розовый, ретикулярные — в сине-голубой цвет), а также в реакции иммуно-флюоресценции (РИФ) и др.
У человека вызывают хламидиозы: С.trachomatis (возбудитель трахомы, урогенитальных инфекций), С.psittaci (орнитоз), С.рпеитоniae (различные формы респираторных инфекций).
3. Микоплазмы
повреждаются, но не погибают. Микоплазмы изучают в нативных препаратах с использованием фазово-контрастной микроскопии, РИФ и др.
У человека микоплазмы вызывают микоплазмозы: М.рпеитоniае (заболевания респираторного тракта), М.hominis, U.urealyticum (инфекции урогенитального тракта).
Об авторах
Вера Александровна Рар — кандидат биологических наук, научный сотрудник лаборатории молекулярной микробиологии Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Автор и соавтор 76 научных работ.
Яна Петровна Иголкина — кандидат биологических наук, младший научный сотрудник лаборатории молекулярной микробиологии Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Автор и соавтор 20 научных работ.
Нина Викторовна Тикунова — доктор биологических наук, зав. лабораторией молекулярной микробиологии ИХБиФМ СО РАН (Новосибирск). Выпускница НГУ (1984).
Валентин Викторович Власов — академик РАН, доктор химических наук, профессор, научный руководитель Института химической биологии и фундаментальной медицины СО РАН (Новосибирск), заведующий кафедрой молекулярной биологии и биотехнологии Новосибирского государственного университета. Лауреат Государственной премии РФ (1999). Автор и соавтор более 500 научных работ и 30 патентов.
В конце XIX в. среди поселенцев в предгорьях Скалистых гор штата Монтана (США) разразилась масштабная вспышка неизвестной болезни, с высокой температурой, геморрагической сыпью и другими тяжелыми симптомами — смертность среди больных достигала 20–30%. В первом десятилетии прошлого века патолог и один из первых американских инфекционистов Говард Риккетс установил, что заражение людей происходит в результате присасывания кровососущих иксодовых клещей рода Dermacentor. В крови больных он обнаружил мелкие бактериоподобные микроорганизмы и экспериментально доказал на морских свинках и обезьянах, что инфекция может передаваться через зараженную кровь.
Самка иксодового клеща Dermacentor andersoni — известного переносчика пятнистой лихорадки Скалистых гор. © CDC, фото J. Gathany
Говард (Хауард) Тейлор Риккетс — американский патолог и микробиолог, первооткрыватель клещевых риккетсиозов. Умер в 1910 г. от сыпного тифа, заразившись при изучении этой болезни во время эпидемии в Мексике
Заболевание назвали пятнистой лихорадкой Скалистых гор, хотя позднее выяснилось, что оно встречается практически на всей территории Северной Америки и части Южной. Сам Риккетс в 1910 г. занялся изучением неизвестного заболевания в Мексике, оказавшегося сыпным тифом, и обнаружил сходство как симптомов, так и возбудителей этой болезни и клещевой лихорадки. При проведении исследований 39-летний профессор заразился сыпным тифом и погиб.
На этом историческом снимке 1953 г. запечатлены технические сотрудники лаборатории вирусов и риккетсий американского Центра по контролю и профилактике заболеваний (CDC), где занимались изучением пятнистой лихорадки Скалистых гор. Как можно увидеть, средства индивидуальной защиты (СИЗ) того времени состояли из обычного лабораторного халата и матерчатого головного убора. © CDC
В России первые случаи клещевого риккетсиоза были отмечены в 1934–1936 гг. на территориях Красноярского края и Дальнего Востока — примерно тогда же, когда там стали фиксироваться весенние вспышки клещевого энцефалита. Это было время активного освоения восточных регионов страны, поэтому эпидемии неизвестных болезней привлекали к себе особое внимание.
Позже научным экспедициям удалось точно установить природу инфекции и выделить ее возбудителя, названного Dermacentor oxenus sibirica (позднее Rickettsia sibirica). Само заболевание было именовано североазиатским клещевым риккетсиозом, или сибирским клещевым тифом (Лобан, 2002).
Эта болезнь привязана к определенным территориям — природным очагам. В нашей стране они встречаются в Сибири и на Дальнем Востоке, а также в соседних странах — Туркмении, Армении, Казахстане и Монголии. При этом роль позвоночных животных как резервуара инфекции, по-видимому, незначительна. На практике у тех же грызунов очень редко выявляются риккетсии — в отличие от возбудителей других болезней, переносимых клещами. Что касается человека, то он, как и в случае других клещевых инфекций, становится лишь случайной жертвой в результате укуса зараженного клеща.
Рука ребенка, покрытая папулезной сыпью, характерной для пятнистой лихорадки Скалистых гор — самого тяжелого и наиболее часто регистрируемого риккетсиоза в США. © CDC
Сыпной тиф — эпидемический и эндемический
К группе сыпного тифа относятся возбудители эпидемического (вшивого) сыпного тифа — Rickettsia prowazekii, и эндемического (блошиного, крысиного) тифа — Rickettsia typhi.
Эпидемический сыпной тиф характеризуется циклическим течением с лихорадкой, сыпью, острым поражением нервной и сердечно-сосудистой систем. Его источник — всегда больной человек, а переносчиком служит платяная или головная вошь. Заражение людей происходит путем втирания в кожу фекалий вшей при расчесах либо через слизистые оболочки глаз и дыхательных путей (Рудаков и др., 2016). Через укусы вшей инфекция не передается, поскольку возбудитель размножается лишь в эпителиальных клетках кишечника насекомых (Лобан и др., 2002).
Эндемический сыпной тиф характеризуется циклическим течением с появлением на коже розеолезно-папулезной сыпи; протекает в основном доброкачественно, летальность незначительная. Резервуарами инфекции являются крысы и домовые мыши, а переносчиками — блохи, три вида вшей и несколько видов гамазовых клещей. Передача человеку происходит фекально-ингаляционно-контактным путем (Лобан и др., 2002). Встречается он на всех континентах, кроме Антарктиды.
Риккетсии — одни из самых мелких бактерий: их длина не превышает 1–2 мкм, что сравнимо с размерами крупных вирусов; к тому же они неспособны расти на питательных средах. Что и неудивительно: эти бактерии являются исключительно внутриклеточными паразитами и могут размножаться только в клетках живых организмов.
Из-за небольших размеров риккетсий их трудно увидеть в тканях с помощью обычных гистологических методов исследования. Чтобы выявить наличие Rickettsia rickettsii в этом образце ткани желточного мешка развивающихся куриных эмбрионов (их используют для культивирования этих бактерий), применили специальный метод окрашивания по Гименесу. Фуксин в водном растворе с фенолом и этанолом окрасил риккетсии в малиновый цвет, а малахитовый зеленый придал контрастность тканям. Фото 1974 г. © CDC
Склонность риккетсий к комфортной и безопасной жизни хорошо согласуется с мнением, что именно эти бактерии эволюционно наиболее близки к вымершим микроорганизмам, которые стали прародителями важнейших внутриклеточных органелл — митохондрий. Эти структуры заняты производством молекул АТФ — универсального источника энергии для клеток. Митохондрии обладают собственным геномом, который передается в череде поколений (в том числе у человека) по материнской линии.
В настоящее время род Rickettsia объединяет более 40 видов, которые делят на несколько групп и подгрупп. Патогенные для человека виды риккетсий входят в две основные группы: сыпного тифа (переносчики — вши и блохи) и клещевых пятнистых лихорадок (переносчики, соответственно, клещи). Что касается остальных групп, то их опасность для человека еще предстоит изучить.
Геномы большинства известных видов риккетсий, представленные одной кольцевой хромосомой, уже расшифрованы. По сравнению со свободноживущими бактериями они небольшие, что в принципе характерно для внутриклеточных паразитов — зачем большой геном, когда и так живешь на всем готовом? Из-за этого у риккетсий редки и геномные перестройки, так как при таком размере любые изменения могут иметь плачевные последствия.
Но даже из этого небольшого числа генов риккетсий часть была позаимствована ими у других организмов. К примеру, в составе генома R. felis имеется более полутора сотен генов, которые попали к ним от других бактерий и даже высших организмов (эукариот).
Утрата некоторых регуляторных генов может менять патогенность бактерии, причем в любую сторону. К примеру, геном одной из самых патогенных риккетсий — R. prowazekii, самый маленький. Но риккетсия может также потерять гены, отвечающие за ее болезнетворность.
В геноме некоторых риккетсий присутствуют еще и плазмиды — свободные генетические элементы, которые могут наследоваться относительно независимо и даже передаваться от одной бактерии к другой при конъюгации (бактериальном аналоге полового процесса). Но об их роли в жизни риккетсий мало что известно.
Ab ovo
Из 36 видов риккетсий, принадлежащих группе клещевой пятнистой лихорадки, только 16 представляют опасность для человека. Передача клещевого риккетсиоза происходит в результате присасывания зараженного клеща. Исключение — вид R. felis, который переносится блохами. У кошек он вызывает лихорадочное состояние, а у человека — вполне типичную для риккетсиозов симптоматику, возможны и неврологические нарушения.
Изображения морфологических структур американского собачьего клеща (Dermacentor variabilis), одного из переносчиков R. rickettsii: детали ротового отверстия, спинного чувствительного волоска, придатков ног. Сканирующая электронная микроскопия. © CDC, фото J. H. Carr
В теле самого клеща риккетсий можно найти практически везде, включая слюнные железы и яичники. Поэтому они могут не только сохраняться в особи в течение всей ее жизни, от личинки до имаго (взрослого), но и, через яйцо, очень эффективно передаваться потомству (Рудаков и др., 2016). И этим риккетсии отличаются от других инфекционных агентов, таких как вирус клещевого энцефалита или боррелии.
Из-за передачи патогена между поколениями зараженность некоторых видов иксодовых клещей может достигать 70–80%! Поэтому для человека представляет опасность присасывание как взрослых клещей, так и личинок и нимф. Личинки особенно часто нападают на детей и могут оставаться незамеченными из-за малого размера, поэтому при заражении поставить диагноз трудно.
Так, в азиатской части РФ в клещах наиболее часто встречаются виды Candidatus R. tarasevichiae, R. raoultii, R. helvetica, R. sibirica и R. heilongjiangensis (два последних представляют наибольшую опасность для человека). При этом, к примеру, виды R. raoultii и R. sibirica явно предпочитают клещей рода Dermacentor (Igolkina et al., 2018a; Mediannikov et al., 2006; Shpynov et al., 2006).
География местообитания клещей также вносит неожиданные коррективы. Так, хотя в таежных клещах чаще всего выявляется Candidatus R. tarasevichiae, на Сахалине более 60% этих клещей инфицировано совсем другой риккетсией — R. helvetica. Такое различие, вероятно, связано с географической изоляцией острова.
Астраханский, сибирский, дальневосточный
Для большинства риккетсиозов характерны одни и те же типичные симптомы: высокая температура и пятнистые высыпания на коже, а также увеличение лимфатических узлов вблизи места укуса. На месте присасывания клеща часто имеется язвочка, покрытая темной коркой и окруженная участком покрасневшей воспаленной кожи. Могут наблюдаться мышечные и головные боли, заторможенность, апатия, нарушения сна, в редких случаях — неврологические нарушения.
Насосавшийся крови лесной клещ (Dermacentor andersoni) на спине мужчины. Обращает внимание необычно сильная местная реакция в виде покраснения кожи и воспаления на месте укуса. © CDC / NIAID
При этом риккетсиозы, вызванные разными возбудителями, могут иметь характерные особенности и отличаться по тяжести заболевания. Один из наиболее тяжелых — пятнистая лихорадка Скалистых гор: даже при своевременном лечении летальность достигает 4%. В Европе широко распространена средиземноморская пятнистая лихорадка с летальностью до 2,5%.
Но хотя и считается, что в азиатской части России есть только один клещевой риккетсиоз, который вызывается R. sibirica, не так давно было установлено, что в Хабаровском крае возбудителем чаще всего является вид R. heilongjiangensis (Mediannikov et al., 2006). Заболевание даже получило свое название: дальневосточный клещевой риккетсиоз.
Различить возбудителей риккетсиозов можно только с помощью молекулярно-генетических методов. Так, было показано, что R. sibirica действительно является основным инфекционным агентом в Новосибирской области и на Алтае (Igolkina et al., 2018b; Granitov et al., 2015), но остальные территории Западной и Восточной Сибири в этом смысле остаются неизученными.
Род Rickettsia относится к семейству Rickettsiaceae, который включает также род Orientia. Бактерия Orientia tsutsugamushi является возбудителем лихорадки Цуцугамуши (японская речная лихорадка), которая протекает по сценарию, типичному для всех риккетсиозов: с лихорадкой, кожными высыпаниями и т. п. Переносится личинками краснотелковых клещей. На фото — бактериальная клетка O. tsutsugamushi, поглощаемая мезотелиальной клеткой брюшины мыши. Просвечивающая электронная микроскопия. Фото 1976 г. © CDC
Так как даже в России летальный исход риккетсиоза не исключен, болезнь необходимо своевременно распознать и лечить. Диагноз сейчас ставят по характерным клиническим проявлениям, а для лечения используют антибиотики тетрациклинового ряда (например, доксициклин). Риккетсии чувствительны и к хлорамфениколам (левомицетину) (Рудаков, 2016). У переболевших вырабатывается стойкий иммунитет, причем ко всем клещевым риккетсиозам независимо от возбудителя. Рецидивов не наблюдается.
Но и здесь не все так гладко.
Нетипичные инфекции
Риккетсию, вызывающую лихорадку Скалистых гор, обнаруживают не только в иксодовых клещах, но, к примеру, и в мягких клещах Ornithodoros kelleyi, паразитирующих на летучих мышах. Однако на сегодня нет данных, что человек может заразиться через укус этого членистоногого. © CDC, фото J. Gathany
О сложности постановки диагноза в нетипичных случаях говорит и тот факт, что у новосибирцев, инфицированных R. slovaca и новыми генетическими вариантами риккетсий, характерных для риккетсиозов симптомов не наблюдалось.
Прирастают числом
Благодаря современным молекулярно-генетическим методам исследователи выявляют не только новые геноварианты и виды риккетсий, но и их присутствие в нехарактерных для них видах клещей и в новых регионах.
Филогенетическое древо риккетсий, основанное на анализе последовательностей ряда генов большинства известных видов риккетсий. По: (Merhej et al., 2014)
Уточняется и база сведений о путях передачи риккетсий в природе. Так, предполагалось, что в этом процессе могут участвовать и клещи, которые никогда не нападают на крупных млекопитающих и человека. К примеру, в Западной Сибири в некоторых местах вместе с таежными клещами обитают норные иксодовые клещи I. trianguliceps и I. apronophorus, которые в течение всего жизненного цикла питаются на мелких млекопитающих. Одновременно на этих же животных могут прокармливаться личинки и нимфы таежных клещей, что открывает возможность обмена патогенными видами риккетсий.
На изображении капилляра мозга мыши, экспериментально зараженной риккетсиозными бактериями Orientia tsutsugamushi, видны свидетельства кровоизлияния и отека. В цитоплазме погибающей клетки сосудистого эндотелия можно увидеть несколько клеток патогенной бактерии. Просвечивающая электронная микроскопия. Фото 1976 г. © CDC
В отличие от клещевого энцефалита и клещевого боррелиоза, риккетсиозы не переходят в хронические формы и не вызывают тяжелых отдаленных последствий для здоровья. Однако все они требуют лечения, а когда болезнь протекает с невыраженной или нехарактерной симптоматикой, поставить правильный диагноз трудно. Такие нетипичные случаи часто связаны с видами риккетсий, ранее не считавшимися патогенными.
Точно диагностировать болезнь в сложных случаях можно лишь с помощью молекулярно-генетических или иммунологических методов, однако в клинической практике нашей страны они, как правило, не применяются. Более того, в РФ на сегодня просто не существует отечественных лицензированных тест-систем для выявления антител риккетсий в сыворотках пациентов.
Литература
1. Лобан К. М., Лобзин Ю. В., Лукин Е. П. Риккетсиозы человека: Руководство для врачей. М.; СПб.: ЭЛБИ, 2002. 473 с.
2. Рудаков Н. В. Риккетсии и риккетсиозы: Руководство для врачей. Омск: Ом. науч. вестн., 2016. 424 с.
3. Granitov V., Shpynov S., Beshlebova O., et al. New evidence on tick-borne rickettsioses in the Altai region of Russia using primary lesions, serum and blood clots of molecular and serological study // Microbes Infect. 2015. V. 17(11–12). P. 862–865.
4. Igolkina Y. P., Rar V. A., Yakimen-ko V. V., et al. Genetic variability of Rickettsia spp. in Ixodes persulcatus / Ixodes trianguliceps sympatric areas from Western Siberia, Russia: Identification of a new Candidatus Rickettsia species // Infect. Genet. Evol. 2015. V. 34. P. 88–93.
5. Igolkina Y., Rar V., Vysochina N., et al. Genetic variability of Rickettsia spp. in Dermacentor and Haemaphysalis ticks from the Russian Far East // Ticks Tick Borne Dis. 2018a. V. 9(6). P. 1594–1603.
6. Igolkina Y., Krasnova E., Rar V., et al. Detection of causative agents of tick-borne rickettsioses in Western Siberia, Russia: identification of Rickettsia raoultii and Rickettsia sibirica DNA in clinical samples // Clin. Microbiol. Infect. 2018b. V. 24(2). P. 199.e9–199.e12.
7. Mediannikov O., Sidelnikov Y., Ivanov L., et al. Far eastern tick-borne rickettsiosis: identification of two new cases and tick vector // Ann. N. Y. Acad. Sci. 2006. V. 1078. P. 80–88.
8. Merhej V., Angelakis E., Socolovschi C. et al., Genotyping, evolution and epidemiological findings of Rickettsia species // Infect. Genet. Evol. 2014. V. 25. P. 122–137.
9. Raoult D., Fournier P. E., Eremeeva M., et al. Naming of Rickettsiae and rickettsial diseases // Ann. N. Y. Acad. Sci. 2005. V. 1063. P. 1–12.
10. Shpynov S., Fournier P. E., Rudakov N., et al. Detection of members of the genera Rickettsia, Anaplasma, and Ehrlichia in ticks collected in the Asiatic part of Russia // Ann. N. Y. Acad. Sci. 2006. V. 1078. P. 378–383.
Читайте также:

