Отличие туберкулоидной от лепроматозного типа лепры
Обновлено: 18.04.2024
В статье отражены современные представления о лепре, представлены современные данные литературы, посвященные вопросам эпидемиологии заболевания, особенностям клинической картины, диагностики, дифференциальной диагностики и лечения дерматоза.
The article summarizes information about the disease leprosy. Data of the literature on epidemiology of the disease, the features of the clinical picture, diagnosis, differential diagnosis and treatment of the dermatosis are presented.
Лепра (проказа, болезнь Хансена) — хроническое инфекционное заболевание из группы микобактериозов, характеризующееся продолжительным инкубационным периодом и рецидивирующим течением. Заболевание носит системный характер и поражает производные эктодермы — кожные покровы, слизистые оболочки и периферическую нервную систему. В настоящее время, несмотря на применение эффективной схемы антибиотикотерапии и устранение угрозы эпидемии лепры, по всему миру продолжают ежегодно выявляться новые случаи заболевания, поэтому перспектива полной ликвидации болезни ставится под сомнение [1–3].
Распространенность лепры в мире стабильно снижается из года в год. Согласно данным ВОЗ, количество новых случаев, каждый год выявляемых во всем мире, уменьшилось с 763 000 в 2001 г. до 249 000 в 2008 г. [1]. В 2013 г. было выявлено 215 656 новых случаев заболевания, в 2014 г. — 213 899, в 2015 г. — 211 973 [2, 3].
Глобальная статистика свидетельствует о том, что 96% (203 600 человек) новых случаев заражения лепрой были выявлены в 22 государствах (таких как Индия, Бразилия, Ангола, Конго, Судан, Эфиопия и др.). На долю других стран приходятся оставшиеся 4% [3].
Одной из шести стран мира с наиболее высокой распространенностью лепры является Бразилия, где ежегодно диагностируется более 30 000 новых случаев заболевания. В 2014 г. распространенность лепры в Бразилии составила 1,27 случая на 10 000 жителей. Уровень распространенности дерматоза по стране неравномерен: помимо эндемичных по лепре регионов существуют и такие, в которых отмечается низкий уровень распространенности лепры [4].
В России эндемичным регионом по лепре является Астраханская область. За последние десятилетия больные лепрой были выявлены и в других субъектах Российской Федерации: в Сибири, на Северном Кавказе и Дальнем Востоке [9, 10]. Однако стоит отметить, что, благодаря внедрению в практику целого комплекса противолепрозных мероприятий, заболеваемость лепрой в России носит устойчивый спорадический характер. В 2015 г. на учете состояло 240 больных, из них в Астраханской области — 135 [10].
Возбудителями лепры являются Mycobacterium leprae (M. leprae) и Mycobacterium lepromatosis (M. lepromatosis). M. leprae была впервые открыта норвежским врачом Герхардом Хансеном в 1873 г. [11]. Данный микроорганизм относится к семейству Mycobacteriaceae и является кислото- и спиртоустойчивой бактерией, которая представляет из себя грамположительную прямую или изогнутую палочку длиной 1–7 мкм и диаметром 0,2–0,5 мкм [12]. M. leprae может длительное время сохранять жизнеспособность при низких температурах и высушивании. Данному микроорганизму свойственен крайне медленный рост, который зачастую не характерен для бактерий (одно деление продолжается приблизительно 12 суток) [12]. Возбудитель заболевания является облигатным внутриклеточным паразитом. M. leprae способна продолжительно персистировать в макрофагах человека, что обеспечивается взаимодействием различных механизмов (антигенная изменчивость и пр.). Именно поэтому пациенты, выписанные из лепрозориев на амбулаторное лечение с персистирующими формами лепры, могут быть источником заражения [9].
В 2008 г. был открыт второй возбудитель лепры — M. lepromatosis, который, в отличие от M. leprae, является некислотоустойчивой бактерией и вызывает преимущественно тяжелый диффузный лепроматозный тип лепры [13, 14].
От других инфекционных заболеваний лепру отличает длительный инкубационный период, который варьирует от 2–3 месяцев до 50 лет (в среднем составляя 4–6 лет) [11].
Общепризнан воздушно-капельный путь передачи инфекционных агентов, однако не исключаются другие пути заражения — через укусы кровососущих насекомых и поврежденные кожные покровы. Лепра является малоконтагиозным заболеванием. Заражение микобактериями лепры происходит в результате длительного тесного общения с больным, не получающим лечения, вследствие сенсибилизации, нарастающей при повторяющихся контактах, снижения сопротивляемости организма (в результате неполноценного питания, тяжелых физических нагрузок, частых простудных заболеваний, алкоголизма и других интоксикаций) и иммуногенетической восприимчивости [11].
На восприимчивость к лепре оказывают влияние различные наборы генов, в том числе системы антигена лейкоцитов человека (HLA). В настоящее время изучаются изменения в генах-кандидатах, участвующих в ответной реакции организма хозяина на инфекционный агент. Исследования геномного сканирования выявили связывающие пики для лепры в областях хромосом 6p21, 17q22, 20p13 и 10p13 [15, 17].
Устойчивость к заражению M. leprae обеспечивается, с одной стороны, низкой вирулентностью M. leprae, с другой — индивидуальными особенностями врожденного иммунитета. Важную роль в поддержании врожденного иммунитета играет целостность эпителия, секрет желез и поверхностный иммуноглобулин A (IgA). Кроме того, уничтожать микобактерии, независимо от активации адаптивного иммунитета, могут NK-клетки, цитотоксические Т-лимфоциты и активированные макрофаги. При заражении регулирование воспалительных цитокинов и хемокинов приводит к пролиферации либо Т-хелперов 1-го типа (Th1), либо Т-хелперов 2-го (Th2) типа, что способствует активации клеточного или гуморального звена иммунитета, что определяет клиническую форму заболевания [16, 17].
Клеточный иммунитет неэффективен в отношении предотвращения развития заболевания у лиц с туберкулоидной формой лепры. Гуморальный иммунитет у лиц с лепроматозной формой заболевания, ответственный за продуцирование IgM против PGL-1 (фенольный гликолипид-1), не обеспечивает защиту и не предотвращает диссеминацию бактерий [17].
Высокий уровень ФНО-α в сыворотке крови у пациентов с туберкулоидной формой лепры свидетельствует об участии данного цитокина в деструкции M. leprae и образовании гранулемы. ФНО-α участвует в иммунной защите посредством активации макрофагов, однако гиперпродукция ФНО-α и его взаимодействие с ИФН-γ способствуют повреждению тканей и формированию узловатой лепрозной эритемы (ENL) [17].
При лепроматозной форме лепры наблюдается повышенный уровень трансформирующего фактора роста бета (ТФР-β), отсутствующего при туберкулоидной форме и проявляющегося в небольшом количестве при пограничной форме лепры. ТФР-β подавляет активацию макрофагов, что ингибирует продуцирование ФНО-α и ИФН-γ, способствуя персистенции инфекции [17].
О механизмах трансмиссии лепры известно, что микобактерии проникают в клетки эндотелия и оседают в Шванновских клетках нервов кожи, к которым имеют тропизм, где в дальнейшем происходит долговременный период их адаптации и размножения. Остается неизвестным, как колонизация Шванновских клеток микобактериями лепры приводит к распространению инфекции в другие ткани [18]. Нейронный тропизм M. leprae обусловлен его связыванием с областью G на мостике молекулы ламинина альфа-2, а альфа-дистрогликан служит рецептором для M. leprae на Шванновских клетках [18].
В работе Masaki и соавт. (2013), в исследовании in vitro и in vivo с использованием мышей, определялось взаимодействие M. leprae со Шванновскими клетками. Исследование показало, что M. leprae изменяют дифференцировку Шванновских клеток до клеток-предшественников [19]. Клеточная перестройка приводит к снижению регуляции Шванновской клеточной линии Sox10 [19]. Таким образом, M. leprae способствуют распространению инфекционного процесса через два механизма: прямая дифференцировка Шванновских клеток в мезенхимальные ткани и образование гранулемаподобных структур, которые выделяют бактерионесущие макрофаги [19]. Исследование расширяет понимание о пластичности зрелых клеток и демонстрирует свойства M. leprae, приводящих к перестройке взрослых клеток в стволовые [18]. Распространение инфекции путем дифференцировки Шванновских клеток возможно при их инфицировании большим количеством M. leprae. Методология, используемая на мышах, у которых нет Т-клеток, упрощает воспалительное микроокружение в преимущественно макрофаги [19]. Данная работа описывает перспективную in vitro модель для объяснения патогенеза M. leprae, но необходимы подробные исследования, прежде чем экстраполировать выводы на течение инфекционного процесса в организме человека [18].
Существует две классификации лепры: мадридская классификация, принятая в 1953 г., а также ее последующая модификация, предложенная Д. С. Ридли и В. Джоплингом в 1973 г. [11].
Согласно мадридской классификации выделяют два полярных типа лепры: туберкулоидный и лепроматозный и два промежуточных типа: недифференцированный и пограничный (диморфный) [11].
В классификации Ридли–Джоплинга выделяют три типа лепры — недифференцированный (I — Indeterminate), туберкулоидный (Tuberculoidtype — TT) и лепроматозный (Lepromatoustype — LL). Лепроматозный и туберкулоидный типы являются полярными. Кроме того, различают субполярные и пограничные группы заболевания. Классификация Ридли–Джоплинга не нашла широкого применения ввиду сложности, поэтому в практической деятельности различают лепроматозный и туберкулоидный тип лепры, а также пограничный тип, который в дальнейшем может трансформироваться в одну из первых двух форм [20].
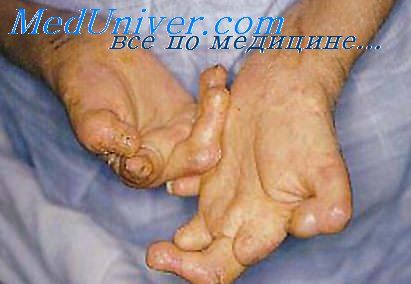
При лепроматозном типе лепры поражается как периферическая, так и центральная нервная система с развитием невротических расстройств, реже — психозов и поражений по типу невритов и полиневритов. В большинстве случаев поражаются лучевые, малоберцовые и большие ушные нервы: они утолщаются и становятся доступными для пальпации. В последующем развиваются двигательные и трофические расстройства, а также нарушения чувствительности. Больным свойственны невралгии, гиперестезии, парестезии, неадекватное или замедленное реагирование на раздражение, аналгезия. На фоне трофических нарушений развивается процесс мутиляции кистей и стоп. Поражение внутренних органов характеризуется неспецифическими изменениями в печени, легких, селезенке и нарушением функции некоторых желез внутренней секреции [11].
При недифференцированной форме лепры специфические высыпания отсутствуют. Для данной формы характерно появление небольшого количества бледных пятен различной величины с нечеткими границами, а также поражение периферической нервной системы по типу полиневрита. Как правило, выявить возбудителя у этой категории лиц удается крайне редко [11].
При развитии обострений лепрозного процесса форма заболевания может меняться. Несмотря на множество клинических проявлений лепры, окончательная постановка диагноза не всегда является простой задачей, так как отсутствуют патогномоничные клинические признаки заболевания [25].
При диагностике лепры учитывают данные эпидемиологического анамнеза (пребывание в эндемичном регионе, контакты с больными лепрой), объективного осмотра (обращают внимание на характер и длительность существования высыпаний, наличие признаков нарушений периферической иннервации).
Общепринятым лабораторным методом диагностики лепры считается бактериоскопическое исследование. Соскобы для исследования берут с очагов поражения на коже и слизистой оболочке носа путем легкого поскабливания. Мазок помещают на предметное стекло и окрашивают по Цилю–Нильсену. Также исследуют пунктат из бедренных или паховых лимфатических узлов. Однако бактериоскопическое исследование имеет очень низкую чувствительность, особенно у больных с промежуточной или туберкулоидной формой поражения [26].
Лепроминовая реакция (проба Митсуды) является показателем способности хозяина поддерживать в своем организме клеточный иммунитет к M. leprae. Проба Митсуды не всегда является достоверной, так как у 10% здоровых по лепре людей может наблюдаться отрицательная реакция. Ограничивают применение лепроминового теста и технические трудности, связанные с получением лепромина и его внутрикожным введением [11].
Наиболее чувствительным методом диагностики, позволяющим определять M. leprae, является полимеразная цепная реакция (ПЦР). ПЦР на данный момент считается наиболее перспективной из прямых диагностических методик и применяется для диагностики любого типа лепры [10, 18]. Преимуществом ПЦР являются неинвазивность и простота получения клинического материала, что предоставляет возможность проведения скрининга большого количества образцов при обследовании пациентов в высокоэндемичных по этому заболеванию регионах. Применение ПЦР позволяет усовершенствовать диагностику лепры и выявлять заболевание на ранней стадии [26].
Используемые в настоящее время традиционные методы диагностики, такие как лепроминовая проба и бактериоскопическое исследование, не всегда позволяют подтвердить диагноз лепры на ранних стадиях заболевания. При этом эффективность лечебных и профилактических мероприятий определяется возможностью ранней диагностики заболевания. В мире постоянно регистрируются новые случаи лепры, поэтому актуальным вопросом остается разработка и внедрение новых, более точных, методов диагностики, которые стали бы доступными для широкого использования и позволили с высокой степенью достоверности диагностировать лепру на ранних стадиях развития заболевания.
Лечение заболевания стандартизовано ВОЗ в 1981 г. [28]. Комбинированная лекарственная терапия включает в себя использование трех основных препаратов: дапсон, рифампицин и клофазимин [28].
Дапсон — бактериостатический препарат, действующий как конкурентный ингибитор ферментов дигидрофолатсинтетазы и дигидрофолатредуктазы, которые являются ключевыми ферментами путей биосинтеза фолатов в микобактериях лепры [28].
Рифампицин — оказывает в отношении M. leprae бактерицидное действие. Является селективным ингибитором ДНК-зависимой РНК-полимеразы и блокирует синтез РНК [29].
Клофазимин — жирорастворимый кристаллический краситель красноватого цвета с бактериостатическим и противовоспалительным свойствами. Механизм антибактериального действия клофазимина изучен недостаточно. Вероятно, он связан с блокировкой матричной функции ДНК, повышением фагоцитарной активности макрофагов и синтеза лизосомальных ферментов [28]. Клофазимин и рифампицин обладают эффективностью в отношении дапсонрезистентных микроорганизмов.
В 1997 г. ВОЗ была установлена продолжительность курса лечения: 6 месяцев для мультибациллярных форм лепры и 12 месяцев для олигобациллярных. Дапсон назначается в дозировке 100 мг для взрослых один раз в день, рифампицин в дозировке 600 мг один раз в месяц, клофазимин в дозировке 300 мг один раз в месяц. Для лечения детей применяются более низкие дозы препаратов [28]. В случае невозможности применения одного или двух препаратов из вышеперечисленных существуют схемы лечения с применением фторхинолонов, которые также показали свою эффективность в отношении M. leprae [30].
Своевременная диагностика лепры, профилактика распространения лепры беженцами и вынужденными переселенцами, особенно из высокоэндемичных государств (Бангладеш, Филиппинские острова, Индия, Ангола, Бразилия, Шри-Ланка и др.), являются серьезной и актуальной проблемой для мирового здравоохранения, одной из приоритетных задач при осуществлении контроля над здоровьем иностранных граждан и лиц без гражданства, въезжающих на территорию страны. В Российской Федерации, в соответствии с существующим порядком, установленным на законодательном уровне, для контроля над распространением заболеваний среди населения, нерезидентам Российской Федерации необходимо пройти медицинское освидетельствование в медицинских организациях. Однако данная процедура освидетельствования осложнена отсутствием комплексной методологической платформы.
Таким образом, несмотря на снижение распространенности лепры, представляется актуальным усиление контроля за обязательным обследованием на лепру прибывающих в страну иностранных граждан, разработка отечественных аналогов лекарственных препаратов и поиск новых схем лечения больных лепрой.
Литература
А. А. Кубанов*, доктор медицинских наук, профессор, член-корреспондент РАН
Т. В. Абрамова**, кандидат медицинских наук
Е. К. Мураховская* , 1 , кандидат медицинских наук
В. А. Ласачко*
* ФГБОУ ДПО РМАНПО МЗ РФ, Москва
** ФГБУ ГНЦДК МЗ РФ, Москва
Клиника лепры. Туберкулоидный тип лепры
Инкубационный период составляет от 3 до 7 лет, иногда 15-20 лет. Болезнь развивается постепенно, незаметно, как бы исподволь. Характерными начальными симптомами служат невриты периферических нервов с анестезией и другими нарушениями их функции, кожные бациллярные инфильтраты и иногда лепрозные реакции.
В соответствии с классификацией Ridley-Jopling (1966), рекомендованной ВОЗ к широкому использованию, различают стабильные полярные туберкулоидныи (Tuberculoid form — ТТ) и лепроматозный (Lepromatous form — LL) типы лепры, нестабильную пограничную (диморфную) лепру (Bordeline s. dimorphous form — ВВ) и переходные погранично-туберкулоидную (Bordeline tuberculoid form —ВТ) и погранично- лепроматозную (Bordeline lepromatous form — BL) формы (рис.45). У больных ВВ и ВТ формами лепры, получающих противолепрозную терапию, могут наблюдаться реактивные состояния (реакции 1 -го типа) без перехода или с переходом в другую классификационную группу по нисходящему (в сторону LL) или по восходящему (в сторону 77) типам, у больных LL формой лепры реактивные состояния (реакции 2 типа) не связаны с лечением и не сопровождаются переходом в другую классификационную категорию.
В соответствии с рекомендациями 7-го экспертного комитета по лепре ВОЗ (июнь 1997 г.) в целях унификации контроля за реализацией GSEL выделяют 3 основные формы лепры в зависимости от распространенности очагов поражений и наличия в них М. leprae: а) пауцибациллярную (безмикробную) лепру с одиночным очагом поражения кожи (Single skin lesion Paucibacillary leprosy- SSL), редко выявляемую (9% от общего числа больных в мире); б) пауцибациллярную лепру (безмикробную) с 2-5 очагами поражения кожи (Paucibacillary leprosy — РВ), превалирующую в настоящее время (52% больных); в) мультибациллярную лепру (с наличием микобактерий в любом очаге) с более чем 5 очагами поражения кожи (Multibacillary leprosy—MB), наблюдаемую у 39% больных (Weekly epidemiological record, № 1. 2002).
Туберкулоидный тип лепры (ТТ) — преобладающая и относительно доброкачественная форма болезни, протекает с преимущественным поражением кожи и периферических нервов, висцеральные расстройства не выражены. В соскобе со слизистой оболочки носа и в очагах поражения кожи М. leprae не обнаруживаются (РВ), лепроминовый тест положительный. Может наблюдаться самопроизвольное излечение больных.
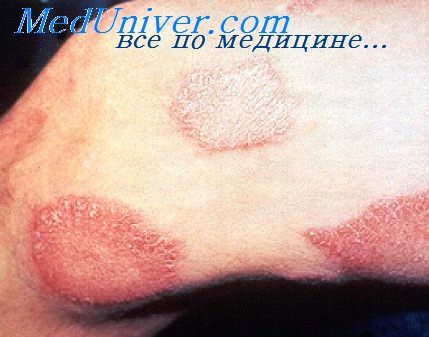
В начальном периоде болезни на коже появляется одиночное (SSL) или возникают единичные (2-5 очагов), асимметрично и повсеместно расположенные четко очерченные светлые или слегка эритематозные пятна, папулы, бляшки или кольцеобразные элементы с западающим бледным центром. Кожные элементы могут быть гипопигментированными (чаще у людей с темной кожей) или приобретать медно-красный (соорегу) оттенок (у светлокожих пациентов), обычно сопровождаются сниженным потои салоотделением, шелушением, утратой пушковых волос, иногда возникает гиперкератоз. В дальнейшем элементы поражения сливаются, образуются группы папул и бляшки с причудливым бордюрным контуром и ограниченные валикообразным приподнятым краем с атрофией и диспигментацией кожи в центре, на лице и конечностях могут отмечаться саркоидные элементы.
Для поражений кожи при туберкулоидной лепре характерна утрата болевой и температурной чувствительности в пределах зоны поражения и тактильной чувствительности в зоне, на 1-1,5 см превышающей очаг поражения (за исключением поражений на лице). Проприоцептивная чувствительность обычно сохранена. В результате нарушения чувствительности очаги поражения часто и незаметно для больного травмируются, подвергаются вторичному инфицированию.
Патогномоничным признаком туберкулоидной лепры является поражение периферических нервов. Считается, что лепра является самой частой причиной периферических невритов в мире.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Инфекции вызванные микобактериями (Mycobacterium tuberculosis, leprae, avium и т.д.): диагностика, лечение, профилактика
Насыщенная липидами клеточная стенка микобактерии обусловливает их кислотоустойчивость. Существует более пятидесяти видов микобактерии, большинство из которых присутствует в окружающей среде и не представляет опасности для человека.
Эпидемиология и патогенез туберкулеза (Mycobacterium tuberculosis)
Основной путь передачи туберкулёза — воздушно-капельный. Лёгкие являются первым органом, поражаемом при туберкулёзе. В месте проникновения возбудителя формируется воспалительный очаг (первичный комплекс), из которого инфекция может распространиться по всему организму (милиарное распространение). Заболевание может неожиданно разрешиться либо перейти в локализованный процесс (например, менингит).
Устойчивость к туберкулёзу обеспечивает Т-клеточное звено иммунитета. При его нарушении болезнь может рецидивировать (предполагаемый риск составляет 10%). Яркую клиническую картину заболевания чаще обнаруживают у пациентов со сниженным иммунитетом (например, у больных с ВИЧ-инфекцией).
Mycobacterium tuberculosis фагоцитируются макрофагами, но не инактивируются фаголизосомами, а размножаются в цитоплазме клеток. Выраженный иммунный ответ приводит к локальному разрушению тканей (образование полостей в лёгких — каверн) и возникновению симптомов, обусловленных цитокин-индуцированной системной воспалительной реакцией (лихорадка, потеря массы тела).
В качестве факторов вирулентности выступает большое количество антигенов, в том числе липоарабиноманнан (стимулятор цитокинов) и супероксиддисмутаза (обеспечивает выживаемость внутри макрофагов).
Клинические признаки туберкулеза
Возбудитель может поражать любой орган: он имитирует как воспалительные заболевания, так и злокачественные новообразования. Симптомы туберкулёза лёгких — хронический кашель, кровохаркание, лихорадка, потеря массы тела, рецидивирующая бактериальная пневмония. При отсутствии лечения болезнь переходит в хроническую форму, характеризующуюся постепенным ухудшением состояния.
При туберкулёзном менингите отмечают повышение температуры, помутнение сознания, при поражении почек — лихорадку, потерю массы тела, а также признаки локальной инфекции, осложнённой фиброзом мочеточников и гидронефрозом. Прогрессирование туберкулёза костей, обычно поражающего пояснично-крестцовый отдел позвоночника, характеризуется признаками вертебрального коллапса и сдавления нервов.
Кроме того, гной из очага инфекции может проникать под оболочку поясничной мышцы, в результате чего возникает паховый абсцесс. Поражение крупных суставов приводит к артриту и разрушению суставной ткани. При абдоминальной инфекции наблюдают брыжеечную лимфаденопатию, хронический перитонит, а также лихорадку, потерю массы тела, асцит, признаки нарушения всасывания в кишечнике. Диссеминированная (милиарная) инфекция может протекать без симптомов поражения лёгких.
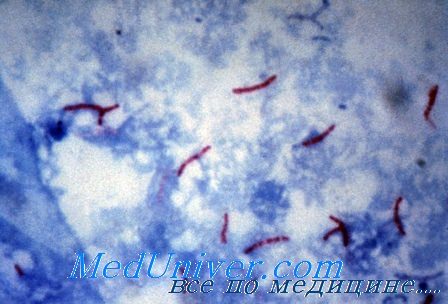
Микобактерии туберкулеза
Лабораторная диагностика туберкулеза (Mycobacterium tuberculosis)
• Культивирование на средах, обогащенных липидами (яичные среды), или с добавлением малахитового зелёного (среда Левенштейна—Йенсена) для подавления роста других бактерий. Препарат окрашивают по методу Циля—Нильсена.
• Определение чувствительности штаммов на скошенной питательной среде Левенштейна—Йенсена.
• Молекулярно-генетические методы (помогает уточнить наличие гена ргоВ, идентифицировать туберкулёзный антигенный комплекс и определить устойчивость к рифампицину).
• Типирование Mycobacterium tuberculosis с помощью анализа полиморфизма длины рестрикционных фрагментов.
• Измерение уровня цитокинов периферической крови, продуцируемых моноцитами (для диагностики остроты процесса).
Лечение и профилактика туберкулеза
Для лечения туберкулёза лёгких применяют этамбутол в комплексе с пиразинамидом (в первые 2 мес) и рифампицин и изониазид (на протяжении 6 мес). При поражении других органов используют такую же схему лечения, основанную на способности лекарственного препарата проникать в различные ткани (например, в спинномозговую жидкость). В последнее время всё чаще выделяют мультирезистентные штаммы возбудителя туберкулёза.
Вероятность их обнаружения зависит от числа случаев неполного излечения, уровня жизни и др. В этом случае для лечения используют препараты второй линии: аминогликозиды, фторхинолоны, этионамид или циклосерин (после обязательного определения чувствительности возбудителя к антибиотикам).
Вакцинация аттенуированными (ослабленными) штаммами (вакцина для профилактики туберкулёза, синоним — вакцина Кальметт—Герена, БЦЖ) позволяет избежать милиарного распространения инфекции, но клинические исследования в некоторых странах не подтвердили её эффективности. Пациентам с высоким риском развития туберкулёза назначают профилактическое лечение рифампицином и изониазидом, а лицам с ВИЧ-инфекцией рекомендован приём рифабутина или кларитромицина в течение длительного времени.
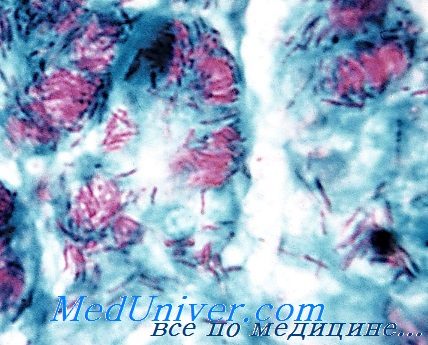
Микобактерии лепры
Инфекция вызванная Mycobacterium leprae - Лепра
Возбудителя лепры (проказы) до настоящего времени не удалось культивировать на искусственных питательных средах.
Mycobacterium leprae вызывает поражение периферических нервов, сопровождаемое нарушением болевой чувствительности. Разрушение и деформация суставов и фаланг пальцев делают пациентов физически недееспособными. Итог заболевания индивидуален и зависит от иммунного ответа. В настоящее время выделяют три типа иммунного ответа при лепре:
• туберкулоидный (превалирует Thl-ответ);
• лепроматозный (преобладает Тh2-ответ);
• пограничный.
При туберкулоидном типе инфекции у пациентов развивается стойкий клеточный иммунитет, возникает большое количество гранулём, трофические поражения нервов. В тканях обнаруживают небольшое количество бактерий. Для лепроматозного типа характерен слабый клеточный иммунитет, отсутствие гранулём и генерализованная инфекция (леонтиаз, депигментация и нарушение чувствительности).
Диагноз основан на результатах микроскопического исследования препаратов поражённой кожи (окраска по Цилю-Нильсену) и биоптатов кожных покровов гистологического исследования. Для лечения применяют рифампицин, дапсон и клофазимин, эффективные на ранних стадиях заболевания, но неспособные препятствовать повреждению нервов и деформации конечностей, при возникновении которых необходимо хирургическое вмешательство.
Микобактерии не вызывающие туберкулез
Различные виды микобактерий могут вызывать локализованные или диссеминированные заболевания у лиц со сниженным иммунитетом. Некоторые из них могут инфицировать имплантируемые ткани.
Mycobacterium avium. В состав комплекса входят Mycobacterium avium, M. intracellular и М. scrofulaceum. Некоторые из них поражают птиц, других животных, являясь санрофитами окружающей среды. Их считают наиболее распространённой причиной микобактериального лимфаденита у детей, остеомиелита у пациентов со сниженным иммунитетом и пневмонии у лиц пожилого возраста. При прогрессирующей ВИЧ-инфекции эти микроорганизмы способны вызывать диссеминированные инфекции и бактериемию.
Возбудители из авиум-внутриклеточного комплекса устойчивы к действию большинства противотуберкулёзных препаратов, поэтому для лечения инфекций, вызванных ими, применяют методы комплексной терапии с использованием рифабутина, кларитромицина и этамбутола. При развитии лимфаденита иногда требуется хирургическое вмешательство.
Mycobacterium kansasi, M. Malmoense, M. Xenopi. Вызывают вялотекущую инфекцию лёгких, похожую на туберкулёз, у пациентов с хроническими заболеваниями лёгких (бронхоэктазией, силикозом, хронической обструктивной болезнью лёгких). Начальную терапию осуществляют с помощью стандартных препаратов после определения чувствительности микроорганизмов к антибиотикам.
Mycobacterium marinum, М. ulcerans. Mycobacterium marinum вызывают хронические гранулематозные инфекции кожи. Возбудитель обитает в реках, запущенных бассейнах и неухоженных садках для рыбы. Заболеванию свойственно возникновение множественных гнойничковых очагов, покрытых твёрдой коркой. Инфекции, вызванные М. ulcerans, распространены в сельскохозяйственных зонах Африки и Австралии. Бактерии обычно поражают нижние конечности, при этом обнаруживают папулёзные очаги, сопровождаемые изъязвлением и глубоким повреждением тканей (включая костную).
Видео диагностика и лечение микобактериоза. Д.м.н., профессор В.Н. Зимина
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гранулемы лепроматозного типа - лепромы. Лепромы туберкулоидного типа
Закономерно возникает поражение периферических нервов, глаз, слизистой оболочки носа с ее разрушением вследствие накопления огромного числа микобактерий (мультибациллярная лепра).
Наряду с поражением кожи вследствие гематогенной диссеминации М. leprae с течением времени лепромы формируются в печени, легких, селезенке, лимфатических узлах, костном мозге, яичках, надпочечниках, костях, мышцах и других тканях. Развивается остеопороз и рассасывание костной ткани преимущественно в области мелких костей кисти и стопы. Характерно развитие нефрита и амилоидоза почек.
Гранулемы туберкулоидного типа формируются в отдельных участках кожи и представлены мощными инфильтратами, разрушающими субэпидермальный слой с эрозией эпидермиса, при этом характерно появление множества эпителиоидных клеток в окружении лимфоцитов, гигантских клеток типа Langhans, небольшого числа плазматических и тучных клеток М. leprae в инфильтрате обычно не обнаруживаются (пауцибациллярная лепра).
Для туберкулоидной лепры характерно развитие эпителиоидной инфильтрации нервных стволов (локтевого, лучевого, тройничного, лицевого, ушного), приводящее к сдавлению и гибели аксонов, и поражение нервных ганглиев. Развиваются параличи, контрактуры, трофические нарушения, остеолиз костей стоп и кисти с мутиляцией конечностей. Висцеральные поражения выражены незначительно.
Гранулемы пограничного типа имеют черты, свойственные обоим описанным выше типам гранулем, и содержат небольшое число М. leprae. В зависимости от динамики иммунологических показателей наблюдается смещение патологических реакций в сторону пауцибациллярного туберкулоидного типа при усилении клеточных реакций, например, при эффективном лечении, или в сторону мультибациллярного лепроматозного типа при угнетении клеточных иммунных реакций, например, при беременности, стрессе, неадекватном лечении.
Инфекционный процесс имеет хронический характер, спонтанное выздоровление наблюдается в некоторых случаях при туберкулоидной лепре, лепроматозная и пограничные формы у нелеченных больных склонны к прогрессированию.
При всех формах лепры возможно развитие лепрозных реакций, характеризующихся резким усилением проявлений болезни. Реакции 1 типа, развивающиеся вследствие активизации клеточных иммунных реакций, характерны для погранично-туберкулоидной и туберкулоидной форм лепры и возникают обычно на фоне терапии.
Реакции погранично-туберкулоидной лепры могут приводить к трансформации формы лепры как в сторону лепроматозной (нисходящий тип), так и в сторону туберкулоидной (восходящий тип) лепры, при туберкулоидной лепре реакции могут приводить к выздоровлению. Реакции 2-го типа, обусловленные активизацией опосредованного иммунными комплексами васкулита, характерны для лепроматозной, погранично-лепроматозной и пограничной форм лепры, развиваются в случаях иммуносупрессивных воздействий и обычно приводят к прогрессированию болезни.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Причина заболевания является инфицирование микобактерией лепры (M. leprae) - грамположительной, кислото- и спиртоустойчивой палочкой длиной 2–7 мкм, диаметром 0, 2–0, 5 мкм, окрашивающейся по методу Циля–Нельсена вкрасный цвет, размножающейся поперечным делением, с длительным циклом генерации.
Источником заражения при лепре чаще всего является больной человек, однако не исключаются и другие источники (лепра буйволов, обезьян, девятипоясных броненосцев). Основным путем передачи инфекции является воздушно-капельный, вместе с тем не исключаются и другие пути заражения (через поврежденные кожные покровы). Микобактерии лепры попадают в клетки эндотелия сосудов и оседают в шванновских клетках кожных нервов (в силу сходства антигенов M. leprae и ткани периферических нервов), где и происходит длительный период их адаптации и размножения. Инфекционный процесс сопровождается клеточной реакцией воспалительно-гранулематозного характера, развивающейся в соединительной ткани ретикулогистиоцитарной системы.
Факторы риска
- Проживание в эндемическом районе
- Близкий родственник, больной проказой
- Алиментарное истощение
- Контакт с животными (инфицированными броненосцами)
Международная классификация болезней 10 пересмотра
- А30. Лепра (болезнь Хансена).
- А30.0. Недифференцированная лепра.
- А30.1. Туберкулоидная лепра.
- А30.2. Пограничная туберкулоидная лепра.
- А30.3. Пограничная лепра.
- А30.4. Пограничная лепроматозная лепра.
- А.30.6. Лепроматозная лепра.
- А.30.9. Лепра неуточненная.
Классификации ВОЗ (1990)
- Многобактериальные формы лепры (МВ - multibacillary leprosy)
- лепроматозный тип лепры (LL)
- субполярная форма (LLs)
- погранично-лепроматозная форма (BL)
- пограничная форма лепры (BB)
- некоторые случаи (при числе очагов свыше пяти) погранично-туберкулоидной лепры (ВТ) .
- туберкулоидный тип (TT),
- субполярная туберкулоидная форма (TTs),
- погранично-туберкулоидная форма (ВТ)
- недифференцированная форма
Туберкулоидный тип лепры
![]()
Отличается более легким по сравнению с лепроматозным типом течением и лучше поддается лечению.Поражаются в основном кожа и периферические нервы, реже —некоторые внутренние органы.
На ранних этапах низкобациллярной туберкулоидной лепры (полярном и субполярном типе) на коже локализуется от 1 до 10 асимметрично расположенных, слегка эритематозных или гипохромных очагов диаметром 3-20 см, четко отграниченных валиком из мелких бугорков. Пятнистые элементы сливаются в бляшки, слегка возвышающиеся над уровнем кожи, с приподнятым краем. В процессе дальнейшего прогрессирования болезни центр бляшек уплощается, становится атрофичным и гипопигментированным. Образуются кольцевидные, сливающиеся друг с другом бордюрные элементы диаметром от 2-3 до 20-30 см и более, иногда захватывающие большую часть туловища. Ширина отграничивающего бляшку бордюра с приподнятым наружным и уплощенным внутренним краем варьирует от нескольких миллиметров до 2-3 см.
Характерные признаки высыпаний при ТТ лепре - раннее снижение тактильной, температурной и болевой чувствительности, выходящее на 0, 5 см за пределы видимых поражений, нарушение потоотделения, а также выпадение пушковых волос. Утолщаются нервные стволы (чаще локтевой и большой ушной), их пальпация умеренно болезненна. Клеточный иммунитет сохранен, внутрикожная реакция на лепромин (реакция Митсуда) положительная. В серозной жидкости из очага поражения микобактерии либо не обнаруживаются, либо их количество менее 1 на 10 полей зрения.М. lерrае выявляются с трудом и только при гистологическом исследовании, а в соскобе кожных поражений и слизистой носа, как правило, отсутствуют. При регрессе всех элементов ТТ лепры на их месте остаются гипопигментные пятна, а в случае более глубокой инфильтрации -атрофия кожи.
Пограничная форма лепры
![]()
Сочетает признаки туберкулоидного и лепроматозного типов лепры.Характеризуется полиморфными высыпаниями: наряду с пятнами находят папулы и бляшки. В пределах очагов поражения снижены болевая чувствительность и потоотделение.В очагах поражения обычно находят множество возбудителей. Может перейти в туберкулоидную или лепроматозную форму.Лепроматозный тип лепры
![]()
Отличается большим разнообразием кожных проявлений, ранним вовлечением в процесс слизистых оболочек и внутренних органов и более поздним - нервной системы, труднее поддается лечению.
На ранних стадиях на коже появляются нерезко очерченные малозаметные гипо- или гипер- пигментированные эритематозные пятна с фиолетовым или вишневым оттенком, характерными признаками которых являются симметричное расположение, небольшие размеры и отсутствие четких контуров.
Лепромы чаще локализуются на лице (надбровные дуги, лоб, крылья носа, подбородок, щеки), мочках ушей, а также на коже кистей, предплечий, голеней, реже - бедер, ягодиц, спины. Они резко отграничены от окружающей кожи, безболезненны. Выпадают брови, ресницы, волосы усов и бороды. Отмечается нарушение потоотделения и секреции сальных желез; сухость, шелушение и истончение кожи.При распаде лепром образуются длительно незаживающие язвы. Периферические лимфатические узлы, чаще пахово-бедренные, увеличены.Во всех высыпаниях выявляется огромное количество M. leprae. Лепроминовая реакция отрицательная
Периферическая нервная система
Слизистые оболочки
Во всех случаях лепроматозной лепры имеются поражения слизистых оболочек носа, а в запущенных случаях поражаются слизистые рта (гортани, спинка языка, красная кайма губ) и глаз (конъюнктивит, эписклерит, кератит), что приводит к полной потере зрения
Ногти
При всех формах лепры обычно бывают изменения ногтей. Они становятся тусклыми, сероватыми, утолщенными, изрезанными продольными бороздками, ломкими, легко крошатся.
Реактивные состояния
При всех разновидностях лепры при изменении иммунологической реактивности организма могут наблюдаться острые или подострые активации процесса (реакции, реактивные фазы, обострения)-внезапное изменение хода болезни.
"Портрет" больного с финальной стадией лепры
![]()
При подозрении на лепру прежде всего уточняется эпидемиологический анамнез (имелись ли контакты с больными лепрой и не проживал ли обследуемый в эндемических по лепре регионах).Больные нередко жалуются на слабость в конечностях, трудность при ходьбе и удержании предметов, заложенность носа и носовые кровотечения, парестезии и боль по ходу нервов, а также общие симптомы — лихорадку, боль в суставах, артриты, миозиты, лимфадениты. Проводится осмотр всего кожного покрова, лучше при дневном рассеянном свете.
Начальные проявления лепры могут быть в виде единичных или немногочисленных эритематозных, гипохромных пятен, мелкопапулезных (лихеноидных) сгруппированных высыпаний, овальных приподнятых инфильтраций, розеолоподобной сыпи, кольцевидных фигурных эритем, мелкоочаговых множественных сливных инфильтратов, напоминающих мраморную синюшность при озноблении, состояния типа акроцианоза, застойных эритем различной этиологии.
Лабораторная диагностика
- Бактериоскопическое исследование.Материалом для бактериоскопии служат соскоб со слизистой оболочки перегородки носа и тканевая жидкость, получаемая при скарификации кожи (с помощью скальпеля или скарификатора) с мочек ушей, надбровных дуг, подбородка, а также нескольких пораженных высыпаниями участков кожи. Материал окрашивается по Цилю-Нильсену. Микобактерии лепры, окрашиваемые в красный цвет на голубом фоне, легко различимы под микроскопом в виде отдельных экземпляров или скоплений.
- Лепроминовая проба (реакция Митсуда).0, 1 мл лепромина (антиген, представляющий собой взвесь убитых автоклавированием микобактерий лепры в физиологическом растворе с добавлением 0, 5% фенола) вводится внутрикожно в область сгибательной поверхности предплечья. Результат реакции учитывается на 21-й день. Лепроминовая проба считается положительной, если на месте введения антигена развивается инфильтрат диаметром 3 мм и более. Реакция положительна у большинства здоровых людей, а также у больных ТТ и отрицательная при лепроматозном типе заболевания. Лепроминовая проба имеет дифференциально-диагностическое и прогностическое значение, а также позволяет следить за динамикой резистентности организма к М. lерrае.
- ДНК диагностика - выявление ДНК М. lерrае полимеразной цепной реакцией
- Гистологическое исследование.Биопсийный материал берется из периферической части подозрительного на лепру элемента. Биоптат должен вместе с дермой захватывать подкожную жировую клетчатку. Количественным показателем, характеризующим бактериальную насыщенность пораженной ткани, является гистологический индекс (ГИ).
- Туберкулоидный тип.Характерно наличие гранулем, состоящих из эпителиоидных и гигантских клеток с дегенерацией и фибриноидным некрозом соединительнотканных волокон. Бациллы Ганзена в препарате либо отсутствуют, либо их единицы.
- Лепроматозный тип. Обнаруживается гранулематозный инфильтрат, массивный в верхней части дермы, а на нижних ее участках располагается очагами вокруг артерий, вен и нервов. Преобладают гистиоциты и развившиеся из них лепрозные клетки - большие пенистые клетки, напоминающие ксантомные. При окраске по Цилю- Нильсену обнаруживаются многочисленные лепрозные палочки, особенно внутри лепрозных клеток, где они располагаются в виде пачки сигар.
Туберкулоидный тип
Лепроматозный тип
Пограничная лепра
-
( нет симптома шнурка при пальпации, центр пигментирован, а не депигментирован, нет расстройства чувствительности и потоотделения) (бордюр состоит из одного ряда узелков, а при лепре он многорядный, нет расстройств чувствительности)
При многобактериальных формах лепры в 1-й день месяца назначется дапсон по 100 мг, рифампицин 600 мг, лампрен300 мг.В последующие дни месяца ежедневно два препарата (дапсон 100 мг, лампрен 50 мг). Длительность курса составляет 1, 5–2 года (до исчезновения М. lерrае в кожных биоптатах).
При малобактериальных формах лепры назначаются в 1-й день месяца рифампицин 600 мг, дапсон 100 мг. В последующие дни месяца ежедневно дапсон по 100 мг. Длительность курса не менее 6 мес.
Читайте также:





