Отравления животных происходят при поедании растения
Обновлено: 24.04.2024
На территории России произрастает несколько сотен ядовитых и вредных для животных растений.
Основными действующими веществами (ядами), обусловливающими токсичность ядовитых растений, являются алкалоиды, гликозиды, сапонины, лактоны, токсальбумины, эфирные масла, смолы, терпены, органические кислоты и др. Все известные в настоящее время ядовитые растения можно разделить на группы по характеру действия ядовитых веществ на те или иные органы и системы животного организма, а также по основным клиническим признакам отравления.
Растения с преимущественным действием на центральную нервную систему: ядовитый вех, конский укроп, белладонна, черная белена, дурман, чистотел, болиголов, собачья петрушка, пикульник, хвощи, опьяняющий плевел, борец, белая чемерица, осенний безвременник, кирказон, марьянники, болотный мытник и др. При отравлениях этими растениями признаки поражения центральной нервной системы обычно бывают хорошо выраженными и имеют ведущее значение в симптомокомплексе заболевания.
Растения, оказывающие судорожное действие и одновременно действующие на сердце, пищеварительный тракт и почки: таврическая полынь, обыкновенная пижма, лютики, болотная калужница, ветреницы, прострелы, прямой ломонос и др.
Растения с преимущественным действием на органы дыхания и пищеварительный тракт: полевая горчица, рапс, сурепка, левкоидный желтушник, гулявник, лесная жеруха, клоповник и др. Отравления такими растениями выражаются в поражении пищеварительного тракта у животных и развитии воспаления желудка и кишечника. У лошадей поражаются также легкие.
Растения с преимущественным действием на желудочно-кишечный тракт: молочай, пролеска, паслен, болотный белокрыльник, почечуйная трава, лекарственный авран, куколь, вороньи ягоды, слабительная крушина, заборный вьюнок, повилика и др. Эти растения оказывают раздражающее действие на слизистую оболочку желудочно-кишечного тракта и вызывают у животных расстройства пищеварения.
Растения с преимущественным действием на сердце: наперстянка, майский ландыш, горицвет, вороний глаз и др.
Растения с преимущественным действием на печень: луговой крестовник, люпины, опушенноплодный гелиотроп. При продолжительном скармливании этих растений у животных развивается цирроз печени.
Растения, вызывающие признаки геморрагического диатеза- донник и действующие на почки и мочевыделительные пути — лекарственный листовень, люпины.
Растения, сенсибилизирующие животных к действию солнечного света: гречиха, клевер, люцерна, зверобой, якорцы, гулявник и др. Эти растения при определенных условиях, особенно на пастбище и под воздействием солнечного света, вызывают у животных поражения кожи.
Клиническая картина отравлений может быть весьма разнообразной и сложной. В зависимости от природы яда отравления могут протекать в молниеносной, острой, подострой и хронической формах. Острые отравления возникают внезапно, проявляются яркими клиническими симптомами. Хронические развиваются постепенно, при более длительном использовании корма, содержащего ядовитые вещества.
Первая и, пожалуй, главная задача, которую приходится решать в случаях массовых заболеваний животных в условиях промышленного содержания — это дифференциация отравления от заболеваний другой этиологии (отравления донником следует отличать от эмкара, сибирской язвы и ряда отравлений, сопровождающихся геморрагическим диатезом).
Диагностика отравлений растениями основывается на получении данных анамнеза, клинических признаков, состава рациона, патологоанатомического вскрытия и химико-токсикологического исследования корма.
Для предупреждения отравлений перед выгоном животных на новые пастбищные участки необходимо обследовать их, при обнаружении мест с наличием большого количества ядовитых растений выпасать животных не разрешается. Многие ядовитые растения прорастают рано весной (ветреница, вороний глаз, пролеска и др.), когда еще недостаточно развит основной травостой. Поэтому, чтобы животные не поедали без разбора всякую траву, в начале пастбищного периода перед выгоном на пастбище их надо подкармливать.
В некоторых случаях пастбищные участки с наличием в травостое ядовитых растений можно использовать для заготовки сена, так как высушивание обезвреживает некоторые ядовитые растения (болиголов, лютики, калужница болотная, мытник, омежник, собачья петрушка и др.). Самая радикальная мера профилактики — уничтожение ядовитых растений на пастбищах и лугах. Это может быть достигнуто путем коренного улучшения лугов и пастбищ: осушения, известкования, перепашки засоренных пастбищ и т. д. Большое значение имеют и такие агротехнические мероприятия, как введение севооборотов с травосеянием, хорошая обработка почвы, создание искусственных пастбищ с многолетними и однолетними травами, тщательная очистка семенного материала и система удобрений.
Лескова О.А. (Чита, учитель химии, Забайкальский Краевой лицей-интернат, канд. биол. наук, доцент, Забайкальский государственный университет)

1. Арбузов С.Я. Пробуждающее и антинаркотическое действие стимуляторов нервной системы – Ленинград: Медгиз. Ленингр. отд-ние, 1960. – 270 с.
4. Голиков С.Н. Неотложная помощь при острых отравлениях (справочник по токсикологии) – М.: Медицина, 1978. – 312 с.
5. Гузеев В.В. Планирование результатов образования и образовательная технология – М.: Народное образование, 2000. – С. 195 – 198.
9. Лесовская М. И. НОУ-ХАУ: Научное общество учащихся – химический арсенал учителя – Красноярск, 2006. – 228 с.
11. Рогозкин В.Д. Радиозащитное действие цианистых соединений (амигдалин) – М.: Медгиз, 1963. – 132 с.
13. Сингур Н.А. Клиническая картина, вопросы терапии и профилактика отравлений ядрами абрикосовых косточек / Вопросы судебно-медицинской экспертизы // Под ред. М. И. Авдеева. – М.: Модгиз, 1954, с. 133–148.
В современном мире очень важным является вопрос о состоянии здоровья. Существует множество факторов отравлений живых организмов. Одним из таких факторов является отравление синильной кислотой и ее производными. К сожалению, встречаются случаи отравления животных и человека цианидами. Цианиды относятся к первому классу опасности и хранятся в особых условиях. Однако отравление этими веществами может произойти по разным причинам. Например, цианид-ион входит в состав витамина В12, цианогенных гликозидов. Так же отравление цианидами может произойти на горно-обогатительном и гальваническом производстве. Синильная кислота и ее производные встречаются в составе косточек абрикосов, вишен, сливы.
Цель: на основе теоретического анализа и экспериментальной работы раскрыть особенности путей поступления и токсического действия синильной кислоты и ее производных.
Задачи:
1) раскрыть характеристики синильной кислоты и ее производных, пути поступления в организм человека и их токсическое действие;
2) провести экспериментальную работу по качественному выявлению производных синильной кислоты в некоторых растительных объектах;
Синильная кислота и ее производные
Синильная (цианистая) кислота – (HCN, цианистый водород, циановодород, нитрил муравьиной кислоты) – неорганическое соединение, представляющее собой бесцветную, очень летучую жидкость, кипящую при 26,7 °С и обладающую характерным запахом горького миндаля [3]. Синильную кислоту в виде водного раствора впервые получил шведский химик Карл Вильгельм Шееле в 1782 году из желтой кровяной соли (K4[Fe(CN)6]). Безводную синильную кислоту получил в 1811 году Жозеф Луи Гей-Люссак, он же и установил ее состав.
Цианид натрия, цианистый натрий, NaCN – натриевая соль синильной кислоты [2]. Бесцветные гигроскопичные кристаллы, хорошо растворимые в воде (32,4% при 10 °C). В водных растворах гидролизуется с образованием синильной кислоты:
NaCN + H2O -HCN + NaOH
Основными сферами применения цианида натрия является цианидная добыча золота (цианидное выщелачивание), а так же цинкование и золочение изделий из металлов.
Цианид калия, цианистый калий — калиевая соль синильной кислоты, химическая формула KCN [15]. Бесцветные кристаллы, по фактуре и размерам напоминающие сахарный песок. Хорошо растворим в воде (41,7% по массе при 25 °C, 55% при 100 °C). Применяется в процессе добычи золота и серебра из руд (цианирование), а также в гальванотехнике цинка, кадмия, меди, серебра и золота, в том числе для ювелирного дела.
Амигдалин. Амигдалин (C20H27NO11) генцибиозид нитрила миндальной кислоты, цианогенный гликозид, содержащийся в косточках многих растений рода Слива, придавая им горький вкус [11]. Впервые выделен из горького миндаля Prunus amygdalus. Содержится в горьком миндале, косточках вишен, слив, персиков, абрикосов.
Линамарин. Линамарин (C10H17NO6) цианогенный гликозид, обнаруженный в листьях и корнях растений (маниока, лимская фасоль, лен).
Пути поступления и механизм токсического действия
В промышленности синильная кислота может выделяться из ее солей (цианидов) при употреблении их в самых разнообразных технических процессах – в гальванотехнике для омеднения, латунирования, золочения и серебрения, в металлургии для извлечения золота и серебра, для флотации руд, закалки стальных изделий и т. д. [8; 14]. В качестве побочного продукта синильная кислота образуется при неполном сгорании органических азотсодержащих веществ (целлюлоида), в небольших количествах содержится в газе доменных печей, в светильном газе, в сточных водах текстильных фабрик, употребляющих красную кровяную соль для протравки и крашения, и, может встречаться в малых количествах во многих других производствах.
В производственных условиях отравления синильной кислотой чаще всего возникают в результате вдыхания газообразного цианистого водорода, а также его солей, находящихся в состоянии аэрозоля [4]. В производственных условиях возможно также попадание синильной кислоты и ее соединений в организм через органы пищеварения. При поступлении в желудок цианиды под влиянием соляной кислоты желудочного сока разлагаются с выделением свободной синильной кислоты, которая быстро всасывается. При наличии больших концентраций цианистого водорода в воздухе возможно проникновение его в организм не только через дыхательные пути и желудочно-кишечный тракт, но и через кожу, что также может вызвать тяжелое отравление. Всасываемости синильной кислоты через кожу способствует высокая температура воздуха производственных помещений и тяжелое физическое напряжение, вызывающие гиперемию кожи и усиление выделения пота. При ферментативном или кислотном гидролизе цианогликозидов синильная кислота может отщепляться и оставаться в свободном состоянии [13]. Такое образование синильной кислоты может дать, например, гликозид амигдалин, гликозид линамарин, гликозид дуррин (образующийся в сорговых растениях), гликозид вицианин (находящийся в некоторых видах вики), гликозид пруляурозин (лавровишня). Для этого необходимо, чтобы под действием сопутствующих гликозидам и находящихся в тех же растениях ферментов (цианогенных гликозидаз) произошло их расщепление.
Гликозид и его расщепляющий фермент находятся в растениях в разобщенном состоянии. Например, амигдалин миндаля отлагается в семядолях, а фермент – в сосудисто-волокнистых пучках. В результате этого возможность их взаимного действия и образования свободной синильной кислоты в нормально развивающемся растении обычно не происходит. Тесное соприкосновение гликозида и фермента наблюдается при хорошем пережевывании растения. В случае лежания свежесобранных растений в кучках или даже при стоянии растений на корню нормальный ход их жизненных процессов нарушается. Процесс расщепления гликозидов происходит с поглощением воды. Поэтому в практических условиях образование синильной кислоты возможно только там, где имеются достаточные условия влажности. Процесс идет интенсивнее при определенной температуре; оптимальной является температура 35-50 °С. [1].
Расщепление гликозидов может быть обусловлено действием не только сопутствующих ферментов, но и пищеварительных ферментов, кислот, бактерий. Таким образом, во всех случаях кормовых отравлений синильной кислотой создаются условия, содействующие расщеплению находящихся в кормовых растениях цианогенных гликозидов. Условием, способствующим наиболее интенсивному проявлению отравления жвачных синильной кислотой, является нарушение руминации. При правильно протекающем процессе руминации часть образующейся синильной кислоты удаляется. Количество синильной кислоты, образующееся в цианогенных растениях, значительно колеблется. Химические исследования дикорастущих и культурных цианогенных растений на содержание синильной кислоты вскрывает определенную зависимость процессов цианогенеза от возраста растений и характера местных экологических условий, в частности почвы.
Наибольшее количество синильной кислоты образуется, например, в сорговых растениях в стадии кущения, при дальнейшем развитии (в стадии трубки и выметывания метелки) содержание ее постепенно падает, но остается еще в количествах, опасных для животных. В зернах находят наименьшие количества синильной кислоты. Цианогенные процессы могут протекать более интенсивно у растений на сухой почве, чем у растений, находящихся на почве умеренно сырой. В последнем случае цианогенные процессы могут совершенно отсутствовать. Примером зависимости цианообразования от условий почвы может служить случай отравления овец колосняком, выросшим на унавоженных старых стоянках овец (тырлах). Условиями, способствующими повышенному образованию в растении цианогенных глюкозидов или даже свободной синильной кислоты, являются: проливные дожди, наступление сильной жары после дождей, холод, засуха, заморозки, вытаптывание, внезапный быстрый рост живых растений, бурное отрастание растения после обрезки или скашивания, поражение растений патогенными грибками и др. При высушивании зараженные растения постепенно теряют синильную кислоту. Считают, что в одних случаях синильная кислота, будучи летучей, при высыхании растений постепенно испаряется; в других – химические процессы, происходящие при высыхании растений, разрушают способность фермента отщеплять синильную кислоту. Некоторые растения и при высушивании сохраняют способность давать значительные количества синильной кислоты. Это относится, прежде всего, к семенам льна, к косточкам миндалей, слив, вишен, персиков, абрикосов и др. В плохо просушенном сене могут создаваться условия, благоприятные для образования и накопления синильной кислоты. Синильная кислота является промежуточным продуктом при синтезе белковых тел из соединений азота, приносимых растению корнями из почвы (азотнокислого калия, азотнокислого натрия, азота клубеньков бобовых растений), и сложных органических соединений (углеводов), образующихся в зеленых частях растений в результате фотосинтеза. Сгорание (окисление) углеводов под влиянием вдыхаемого растениями кислорода является источником энергии, необходимой для правильного течения всех процессов создания белковых тел. Нарушение или выпадение одного или нескольких из указанных условий ведет к нарушению правильного течения этих процессов и соотношений между исходными веществами, промежуточными соединениями и конечными продуктами – белковыми телами. При нарушении внутриклеточных процессов дыхания и окисления углеводов (при увядании растений, задержке роста и др.), когда не все вещества, приносимые из почвы, переводятся в белковые соединения, может накапливаться большое количество промежуточных продуктов, среди них и синильной кислоты. В случае усиленного поступления веществ из почвы (при бурном росте молодых растений, ростков после скашивания, усилении всех процессов под воздействием солнца, особенно после резкой смены погоды, после холодного дождя, при усиленном притоке воды из почвы и пр.) также может происходить накопление большого количества промежуточных соединений, не используемых полностью для синтеза белков. Образование и накопление синильной кислоты, связанные с явлениями фотосинтеза, естественно, в большей мере протекают в зеленых, верхних частях растений. Это обстоятельство имеет огромное практическое значение, так как животные поедают как раз эти части растения, наиболее богатые синильной кислотой [7]. В зависимости от ослабления фотосинтеза образование синильной кислоты в цианогенных растениях ночью уменьшается, но не исчезает совершенно и может происходить в количествах, способных вызвать отравление. Следовательно, использование в корм растений, поврежденных при этих условиях, может вызвать отравление животных синильной кислотой. Отравление животных происходит преимущественно при поедании цианогенных растений в свежем состоянии. Отравления синильной кислотой могут протекать весьма быстро. Часто животные погибают в течение нескольких часов, даже минут.
В организме человека данные вещества блокируют активность ферментов, особенно клеточную цитохромоксидазу, что способствует развитию тканевой гипоксии (кислородному голоданию). Этим и обусловлено токсическое воздействие синильной кислоты на человека. Прежде всего страдает нервная система, особенно центральная. Яд действует на сердечно-сосудистую систему, и на функцию дыхания. Характерные изменения появляются в кровеносном русле. Многие любят раскалывать косточки абрикосов, и есть приятные на вкус ядра. Однако не все знают, какая опасность кроется в них, ведь там содержится синильная кислота.
Основные признаки отравления синильной кислотой следующие [12].
1. Ярко выраженный розовый цвет слизистых и кожи.
2. От пострадавшего исходит запах горького миндаля.
3. Во рту появляется привкус металла, горечь, обильно выделяется слюна, отмечается першение в горле.
4. Пищеварительная система: тошнота, частые позывы на дефекацию, рвота.
5. Сердечно-сосудистая система: частый пульс, боли давящего характера в грудной клетке. В более поздней стадии тахикардия сменяется редким пульсом.
В конце прошлого века было подмечено, что сахар способен обезвреживать цианиды [10]. Однако это явление не подвергалось химической оценке до 1915 г., когда немецкие химики Рупп и Гольце показали, что глюкоза, соединяясь с синильной кислотой и другими цианидами, образует нетоксичное соединение – циангидрин. Некоторые продукты окисления глюкозы, например диоксиацетон, также способны образовывать циангидрины. Особенно активно эта реакция протекает при профилактическом использовании сахаров. Неслучайно, при опасности контакта с цианидами с давних пор рекомендуется держать за щекой кусочек сахара. В этой связи нельзя не вспомнить совершенное в Петрограде в декабре 1916 г убийство Распутина, которого, как известно, вначале пытались отравить цианидом калия, примешанным к кремовым пирожным и портвейну [15]. Однако яд не подействовал, что в последующем с достаточным основанием связали с защитными свойствами сахара, содержавшегося в пирожных и вине.
Эффективность первой помощи при острых отравлениях цианидами зависит от быстроты и четкой последовательности проведения необходимых мероприятий [4]. Для прекращения дальнейшего поступления яда прежде всего следует вынести пострадавшего из зараженной атмосферы и снять с него одежду, которая может быть источником поступления яда в организм. Для освобождения дыхательного фермента (цитохромоксидазы) клеток от молекулы циана и предупреждения дальнейшего поступления этого яда из крови в ткани применяется соответствующая антидотная терапия. В первую очередь используются метгемоглобинообразователи, так как метгемоглобин содержит трехвалентное железо, к которому молекулы циана имеют большое сродство. Циркулирующий в крови метгемоглобин связывает цианистые соединения прежде чем они попадают из крови в ткани, а также способствует извлечению циана из цитохромоксидазы клеток. В результате в крови образуется цианметгемоглобин. В качестве метгемоглобинообразователей применяются вдыхание амилнитрита (по 2-3 капли с кусочка ваты, марли или с носового платка), внутривенное введение свежеприготовленного 1-2% раствора азотистокислого натрия (5-10 мл) или внутривенное вливание хромосмона (50 мл). К сожалению, цианметгемоглобин является нестойким соединением. Он легко распадается, причем циан довольно быстро отщепляется. Поэтому после введения метгемоглобинообразователей рекомендуется примерно через 5 минут вводить внутривенно 20 мл 30% раствора гипосульфита натрия, который обусловливает обезвреживание цианидов путем образования роданидов, выделяющихся из организма главным образом почками. Если в ближайшее время состояние больного не улучшается, необходимо указанные выше антидоты вводить повторно в том же порядке и в той же дозировке.
Определение синильной кислоты и ее производных в растительных объектах (экспериментальная работа)
Исследования проводятся на территории г. Чита (Забайкальский край) в 2016 г. на базе Забайкальского государственного университета и Забайкальского краевого лицея-интерната.
Для качественного определения производных синильной кислоты использовались пробы с бензидиновыми и пикратными бумажками [5]. Перед проведением эксперимента нами были приготовлены бензидиновые и пикратные бумажки (на базе ЗабГУ).
Объектами исследования служили: косточки вишни войлочной (Prunus tomentosa), черемухи уединенной (Padus avium Miller), абрикоса сибирского (Armeniaca sibirica L.(Lam.)). Следует отметить, что нами исследовались отдельно семя и эндокарпий данных растений (рис. 1, 2).

Рис. 1. Подготовка материала к исследованию – абрикос (фото авторов)

Рис. 2. Подготовка материала к исследованию – черемуха (фото авторов)
Измельченную и хорошо растертую в ступке пробу растительного материала, в количестве 10-15 г смочили водой и поместили в коническую колбу на 50 мл (рис. 3).

Рис. 3. Подготовка материала к исследованию (фото авторов)

Рис. 4. Окрашивание пикратных бумажек (фото авторов)
Слегка подкислили 1%-м раствором соляной кислоты (HCl). Колбу плотно закрыли пробкой с прикрепленной к ее нижнему концу полоской реактивной бумаги, с таким расчетом, чтобы конец ее не касался внесенного в сосуд материала. Сосуд оставили стоять при температуре 30-35 °С на ночь в термостат. Согласно литературным данным, в присутствии синильной кислоты бензидиновая бумажка синеет, пикратная бумажка приобретает красновато-оранжевую окраску. По интенсивности окрашивания, особенно пикратной бумажки, можно судить о количестве синильной кислоты, содержащейся в пробе (рис. 4).
Высокий уровень доместикации собак и кошек, высокая доля урбанизации этих животных и низкая осведомленность владельцев о правильном питании своих питомцев часто приводят к возникновению различных патологий желудочно-кишечного тракта, процессов обмена веществ, а также более серьезных системных заболеваний. Определенную долю данных заболеваний составляют алиментарные отравления продуктами питания человека, токсичными для животных. К наиболее распространенным среди них относятся шоколад, изюм, ксилит(заменитель сахара), а также лук и чеснок. Последние два продукта относятся к растениям рода Allium.
Все виды Allium и их производные могут быть токсичными для собак и кошек, но наибольшая инцидентность оправлений наблюдается при поедании животными репчатого лука (Alliumcepa) (Рис.1), чеснока(Alliumsativum) (Рис.2.), лука-порей (Alliumporrum) (рис.3.) и лука скорода (Alliumschoenoprasum) (Рис.4.).
Основными этиологическими факторами поедания животными этих растений являются спонтанное идиопатическое поедание сушеных концентратов (луковиц или листьев), а также искусственное – ятрогенное – чрезмерное введение этих продуктов в рацион животного. При этом добровольное поедание животными сочных частей растений наблюдается довольно редко из-за достаточно непривлекательных органолептических свойств, обусловленных содержанием пахучих эфирных масел и горечей, и наблюдается при поведенческих пищевых извращениях.
Из-за достаточно низкой инцидентности подобных отравлений не у всех практикующих ветеринарных врачей имеется представление о диагностике, патофизиологии и лечении данных заболеваний. Целью данной статьи является попытка обобщить имеющиеся сведения и поделиться с практикующими специалистами нашим опытом диагностики и лечения отравлений, вызванных растениями семейства Allium.




Токсикологические данные
Луковицы и листья растений рода Allium содержат в своем составе азотистые вещества (до 2,5 %), различные сахара (10—11 %) (глюкозу, фруктозу, сахарозу, мальтозу), полисахарид инулин, фитин, флавоноидкверцетин и его глюкозиды, жиры, различные ферменты, со-ли кальция и фосфора, фитонциды, лимонную и яблочную кисло-ты, витамины A A, B1 , B2, PP , C , а также эфирное масло с резким особым запахом.
Основное патогенетическое значение имеют вещества, входящие в состав эфирных масел - дипропил дисульфид (H7C3S2C3H7) и аллил пропил дисуль-фид(H5C3S2C3H7). В последнее время имеются сведения, что натрия-n-пропил тиосульфат, выделенный из вареного лука, ведет к увеличению телец Гейнца в эритроцитах и развитию последующей гемолитической анемии. Так введе-ние собакам 500 ммоль/кг массы тела животного, натрия-n-пропил тиосуль-фата приводит гемолитической анемии, ассоциированной с появлением те-лец Гейнца, особенно при врожденной недостаточности глутатиона.
Механизм действия
Основным токсическим механизмом производных органических соединений серы в растениях рода Allium является внутрисосудистый гемолиз, развивающийся вследствие окислительного повреждения эритроцитов. Данное явление развивается при накоплении в них оксидантов в концентрации, превосходящей компенсаторную возможность антиоксидантной метаболической активности. N-пропил дисульфид и натрия-n-пропил тиосульфат являются крайне ядовитыми для животных сероорганическими соединениями, содержащимися в луке. Воздействие на эритроциты N-пропила дисульфида приводит к значительному снижению активности глюкозо-6-фосфатдегидрогеназы. Глюкозо-6-фосфатдегидрогеназа - первый фермент пентозофосфатного гликолиза. Основная функция фермента заключается в восстановлении НАДФ до НАДФН, необходимого для перехода окисленного глутатиона (GSSG) в восстановленную форму. Восстановленный глутатион (GSH) требуется для связывания активных форм кислорода (перекисей), накапливающихся в эритроците.
При снижении уровня восстановленного глутатиона или активности глюкозо-6-фосфатдегидрогеназы, необходимой для поддержания его в восстановленной форме, под влиянием перекиси водорода происходит окислительное денатурирование гемоглобина и белков мембраны. Денатурированный и преципитированный гемоглобин находится в эритроците в виде включений - телец Гейнца. Эритроцит с включениями быстро удаляется из циркулирующей крови: либо путем внутрисосудистого гемолиза, либо тельца Гейнца с частью мембраны и гемоглобина фагоцитируются клетками ретикулоэндотелиальной системы. В то же время под действием натрия-n-пропил тиосульфата происходит снижение восстановленного глутатиона, появление телец Гейнца и увеличение концентрации метгемоглобина. При этом компенсаторная активность другого внутриклеточного фермента - каталазы, которая катализирует разложение образующегося в процессе биологического окисления пероксид водорода на воду и молекулярный кислород, также является недостаточной.
Аллицин иаджоен (ajoene) – соединения, присутствующие в чесноке, являются мощными фармакологически активными веществами, влияющими на сердечнососудистую систему. В частности, они оказывают вазодилатирующий и гипотензивный эффект. Кроме того, аджоен и другие сероорганические соединения, выделенные из лука и чеснока, оказывают сильный противосвертывающий (антитромбический) эффект. Хотя, по мнению автора, данные эффекты у животных наблюдаются реже и проявляются при поедании достаточно большого количества чеснока, как вариант индивидуальной чувствительности. Указанные эффекты могут усугубить общее течение интоксикации.
Чувствительность и токсичность
Отравление животного происходит при однократном поедании большого количества или длительном поедании малых порций свежих, сочных частей растений (в основном луковиц или листьев), сока этих растений, а также су-шеных концентратов, используемых для приготовления пищи (сушеные, измельченные луковицы чеснока и лука; сушеные, измельченные листья лука и др.).
На практике наиболее частыми являются отравления репчатым луком. Токсические эффекты наблюдаются при поедании 5г/кг репчатого лука у кошек и от 15 до 30г/кг у собак. Собаки с наследственно низким содержанием глутатиона более восприимчивы к окислительному повреждению эритроцитов. Эта особенность характерна для собак японских пород, в частности, акита-ину и сиба-ину. Другие врожденные нарушения, а также нарушения питания, приводящие к дефициту цинка и снижению антиоксидантной защиты (например, глюкоза-6-фосфатдегидрогеназа) эритроцитов, способствуют развитию гемолитической анемии под действием сероорганических соединений лука. Кошки более восприимчивы, чем собаки. По данным зарубежных авторов, отравление кошек может происходить при скармливании детского питания, некоторые производители которого добавляют лук и луковый порошок для усиления вкусовых качеств.
Эритроциты человека являются наиболее устойчивыми относительно других видов животных к воздействию дипропил дисульфида, аллил пропил дисульфида и натрия-n-пропил тиосульфата. Однако имеются сведения о чувствительности некоторых этнических групп к воздействию этих соединений.
Принято считать, что овцы, козы, крысы и мыши являются более устойчивыми к отравлениями луком, чем другие виды домашних животных. Безопасность кормления луком скота зависит от видовой чувствительности. Так, лук может занимать относительно большую долю (20-30%) в рационе МРС без серьезных гематологических изменений. Даже при поедании достаточно большого количества лука этими животными у них наблюдается небольшая анемия, легкая гемоглобинурия и лишь в редких случаях летальный исход. В отличии от МРС, при скармливании лука КРС нужно проявлять осторожность из-за относительной восприимчивости эритроцитов этого вида животных к окислительному повреждению эритроцитов. Ежедневное скармливание лу-каможет привести к развитию кумулятивного эффекта.
Клинические признаки
Клинические признаки заболевания развиваются от 1 до 3-х дней после поедания животным токсической дозы растений рода Allium. Сероорганические соединения оказывают сильное раздражающее действие на слизистые оболочки желудочно-кишечного тракта. Поэтому первые клинические признаки заболевания ассоциированы с расстройствами желудочно-кишечного тракта - рвота, диарея, абдоминальная боль, ухудшение аппетита, депрессия и обезвоживание. Внутрисосудистый гемолиз развивается в течение нескольких дней и приводит к устойчивой гемоглобинемии, гемоглобинурии, билирубинемии с преобладанием фракции несвязанного билирубина, снижение рО2. Это проявляется анемичностью видимых слизистых оболочек, снижению СНК, появлением тахипное, тахикардии, изменением цвета мочи, общим угнетением, депрессией и непереносимостью физических нагрузок.
Описание клинического случая
В марте 2016 года в отделение терапии ИВЦ МВА поступила собака породы карликовый шпиц, 1.3 года, 3.5 кг. В анамнезе помимо прочего владельцами указывалось, что около двух дней назад животное съело около 1/2 стакана резаного репчатого лука. После этого у пациента отмечалась вялость, апатия, резкое снижение аппетита, рвота (около 2-3 р/д), не ассоциированная с приемом пищи или воды, диарея, изменение цвета мочи. Содержимое рвотных масс - желудочный сок с небольшим количеством желчи. Снижения потребления воды не отмечалось.
Объективно при осмотре:
Общее состояние животного удовлетворительное. Т=38,0 С°. Сознание ясное. Положение тела в пространстве естественное. Движения скоординированные. ВСО анемичные (Рис.5), влажные, без видимых признаков патологических изменений. СНК не определяется. Периферические ЛУ не пальпируются. Тургор кожи сохранен. Волос матовый, плохо удерживается в волосяном фолликуле. При осмотре кожи и шерстного покрова патологических изменений не выявлено. Экскурсия грудной клетки симметричная. Дыхание ритмичное, везикулярное на всем поле аускультации. Брюшная стенка мягкая, безболезненная.
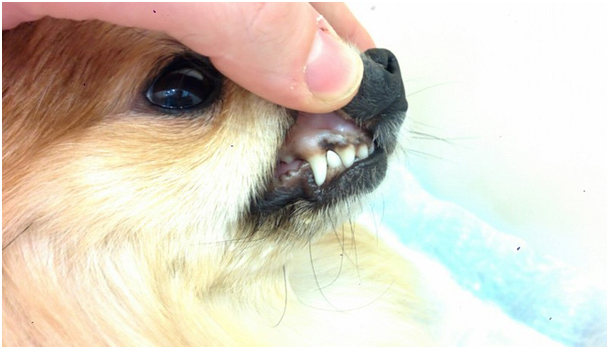
Рис.5. Анемичный вид слизистых
При выполнении гематологического исследования (Рис.6) в день обращения, помимо прочего была выявлена сильная анемия, снижение гемоглобина, повышение скорости оседания эритроцитов и появление большого количества нормобластов. Животное было переведено в отделение реанимации и интенсивной терапии ИВЦ МВА.
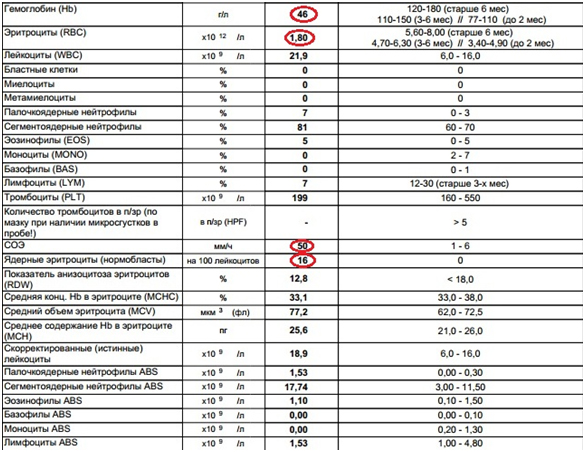
Рис.6. Клинический анализ крови в день обращения.
Сильная анемия требовала немедленной коррекции и проведения гемотрансфузии. С этой целью животному было перелито 50 мл эритроцитарной массы. Перед проведением гемотрансфузии пациенту была проведена катетеризация поверхностной вены предплечья и введено 15 мг Са-глюконата и 14 мг преднизолона. Животное было помещено в бокс для проведения активной оксигенотерапии. После гемотрансфузии выполнена внутривенная инфузия раствора Хартмана в объеме 50мл в течение 60мин. Зная основной патогенетический механизм повреждения эритроцитов, в качестве активного антиоксиданта нами был выбран 5% р-р мексидола. Мексидол обладает выраженными антиоксидантными, антигипоксическими и мембранопротекторными свойствами. Стабилизирует мембранные структуры тромбоцитов и эритроцитов при гемолизе, обладает гиполипидемическим действием, ингибирует перекисное окисление липидов, повышает активность супероксиддисмутазы. 5% раствор мексидола был назначен в дозировке 15мг/кг каждые 12 часов в течение двух дней. В последующие дни дозировка была снижена до 8мг/кг каждые 12 часов.
Промывание желудка и вызывание рвоты актуальны в первые часы после попадания в организм токсического агента, но в данном случае эти мероприятия не были бы эффективны, т.к. с момента отравления прошло более 48 часов. При этом, независимо от времени отравления, применение энтеросорбентов остается актуальным. В первые 48 часов после гемотрансфузии животному назначен преднизолон в дозировке 2.5мг/кг, каждые 12 часов. Для защиты слизистой оболочки желудка было назначено внутривенное введение 1.75мг фамотидина каждые 12 часов, а также орального введения 1.5 мл альмагеля каждые 8 часов. В качестве энтеросорбента животному был назначен энтеросгель по 2 мл внутрь каждые 8 часов, в течение 48часов. Для снижения воспалительной реакции слизистых оболочек ЖКТ животному бы-ло назначено ежедневное выпаивание 20 мл отвара цветков ромашки, с интервалами в 12 часов.
После проведенных мероприятий был осуществлен повторный забор крови для выполнения биохимического анализа и автоматического подсчета форменных элементов крови (Рис.7,8). Отмечено заметное повышение количества эритроцитов и гемоглобина.
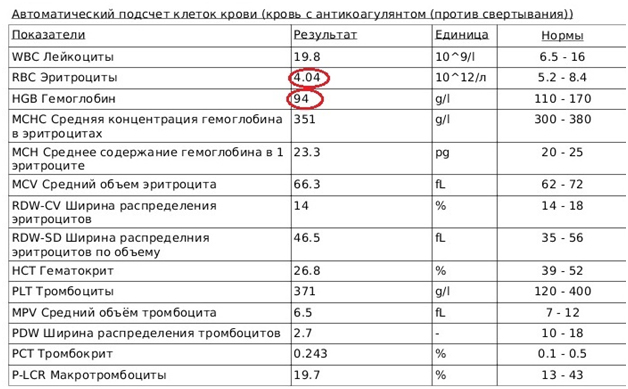
Рис.7. Автоматический подсчет клеток крови после проведенной гемотрансфузии.
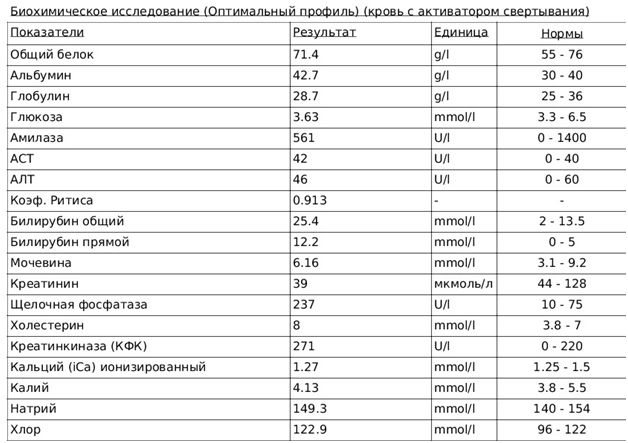
Рис.8. Биохимический анализ крови после проведенной гемотрансфузии.
Для улучшения гемопоэза животному было назначено внутримышечное введение 150 мкг цианокобаламина каждые 24 часа и 0,25 мл гемобаланса 1р/3 дня в течение недели. Продолжена внутривенная инфузия раствора Хартмана в объеме 50 мл, каждые 12 часов в течение 48 часов. В качестве гепатопротектора, для защиты гепатоцитов в условиях повышенного образования билирубина и общего токсического влияния сероорганических соединений, был назначен Гептрал – 17.5 мг, внутривенно, каждые 12часов в течение четырех дней. Через 24 часа выполнен автоматический подсчет форменных элементов крови (Рис.9).
Наблюдается рост количества эритроцитов, хотя и незначительный, и стабильный рост концентрации гемоглобина. Сохраняется стабильный лейкоцитоз. При этом с самого первого дня после обращения у животного наблюдаются все признаки хорошего регенеративного ответа со стороны красного костного мозга.
На момент выписки (3-й день с момента обращения) пациент находился в удовлетворительном состоянии. За все время нахождения животного в отде-лении ОРИ рвота отсутствовала. За все время лечения выраженные признаки диареи наблюдались в первые сутки, в последующее время стул мягкий не-оформленный. ВСО бледно-розового цвета. Признаков дегидратации не отмечено. Перед выпиской, выполнен автоматический подсчет форменных элементов крови (Рис. 10).
Отмечено незначительное снижение концентра-ции гемоглобина, сохранение стабильного количества эритроцитов, сохра-нение стабильного лейкоцитоза. Пациенту назначена вышеуказанная тера-пия на 3дня и животное переведено на амбулаторное лечение. Для стимуля-ции гемопоэза пациенту было однократно введено 700 МЕ эритропоэтина. В качестве лечебной диеты животному назначен корм PurinaEN, на 1 месяц.
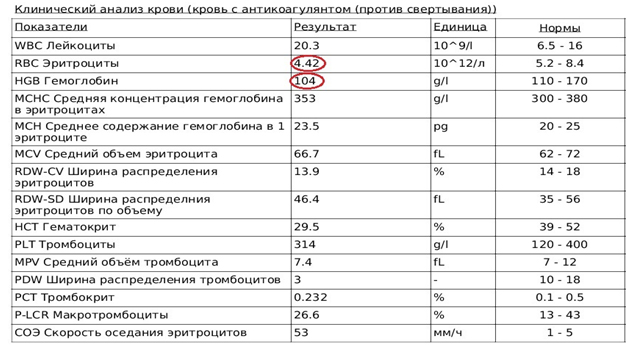
Рис.9. Автоматический подсчет клеток крови. 24 часа после поступления.
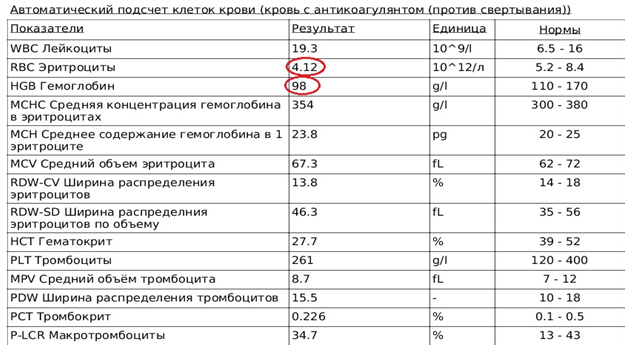
Рис.10. Автоматический подсчет клеток крови на момент выписки.
На назначенный повторный прием владельцы не пришли. Дальнейшее лечение, по желанию владельцев, осуществлялось у другого врача ИВЦ МВА, являющегося постоянным лечащим врачом. Назначенное лечение оставалось неизменным. По данным лечащего врача у животного наблюдается выраженная положительная динамика лечения. Все клинические признаки заболевания, описанные ранее, отсутствуют.
Выводы
Отравления животных растениями рода Allium являются достаточно редкими пищевыми токсикозами собак и кошек. В основном отравления происходят либо при случайном поедании животными пищевых концентратов, либо при намеренном скармливании животным корма содержащего части растений рода Allium, либо при извращении аппетита.
Эритроциты собак и кошек являются очень чувствительными к окислительному повреждению в результате воздействия таких сероорганических соединений как дипропил дисульфид, аллил пропил дисульфид и натрия-n-пропил тиосульфат, содержащихся в растениях рода Allium.
Клинические признаки проявляются в первые трое суток после отравления. Первыми клиническими признаками отравления являются симптомы расстройства ЖКТ. Стойкая гемолитическая анемия развивается минимум через 24 часа после отравления. Специфические антидоты при отравлении растениями рода Allium отсутствуют.
В первые часы после отравления эффективными являются общие методы лечения пищевых отравлений - промывание желудка, провоцирование рвоты. Применений энтеросорбентов является эффективным в любой период лечения. Основное лечение должно быть направлено на стабилизацию гематологических показателей, в частности количества эритроцитов, и фармакологическое балансирование антиаксидантной способности клеток.
При необходимости рекомендовано проведение гемотрансфузии. При эффективной терапии повторное проведение гемотрансфузии, как правило, не требуется. Необходимо контролировать водно-осмотический баланс и при необходимости принять меры к регидратации пациентов. Помимо вышеперечисленного, лечение должно быть направлено на стимуляцию гемопоэза. Постоянно необходимо оценивать степень повреждения почек и гепатоцитов печени. При необходимости следует принять меры по фармакологической протекции этих органов. В большинстве случаев заболевания прогноз лечения положительный.
Отравление ядовитыми растениями — острая или хроническая интоксикация, вызванная ядами, содержащимися в травах, цветах, частях кустов, деревьев. Клиническая симптоматика различается в зависимости от типа растения. Отравление может протекать с преобладанием холинолитического или никотиноподобного синдрома, признаков поражения сердца, почек, печени, кожи, пищеварительного аппарата. Диагностируется на основании токсико-химического анализа крови и мочи, клинической картины и анамнеза. Методы лечения: антидотная терапия, дезинтоксикационные мероприятия, поддержание витальных функций организма.
МКБ-10

Общие сведения
На долю интоксикаций природными ядами приходится около 2-5% от общего количества острых отравлений. Токсичность некоторых растительных ксенобиотиков выше, чем синтетических. Например, смертельная доза цианистого калия составляет 10 мг/кг веса, мускарина, присутствующего в мухоморах — 1,1 мг/кг. Растения могут содержать несколько разновидностей отравляющего вещества: кураре, атропин, никотин, стрихнин, палитокин, рицин, фаллоидин. Наиболее опасные представители флоры — дурман, белена, болиголов, вех, паслен ядовитый, волчье лыко, лютик, чемерица.

Причины
Отравление ядовитыми растениями обычно возникает при пероральном употреблении токсичных трав или тактильном контакте с дерматотропными ядами. Группа риска: дети, люди, использующие рецепты народной медицины, работники фармацевтических предприятий. К возможным причинам относятся:
- Нечаянное употребление ядовитых растений. Чаще страдают жители городов, приезжающие на отдых в загородную зону. Они не обладают необходимыми познаниями и не способны дифференцировать опасные растения (молочай, волчье лыко) от безвредных. Интоксикации также могут развиваться при неграмотном использовании средств нетрадиционной медицины.
- Преднамеренное отравление. Токсичные растения могут использоваться для убийства человека или его нейтрализации. В средние века природные яды активно применялись в ходе дворцовых переворотов. Эксплуатировались вытяжки из аконита, болиголова, цикуты. Сегодня подобные случаи редки, так как разработаны более действенные синтетические поражающие соединения.
- Лечение алкоголизма кукольником. При одновременном использовании со спиртным растение вызывает дисульфирамоподобный эффект. Если терапия проводится тайно, человек может погибнуть, так как не осознает существующей опасности. Причина смерти — эндогенное отравление метаболитами этанола с развитием острой сердечно-сосудистой недостаточности.
- Употребление продуктов с примесью ядовитых трав. Возникает при попытках улучшить вкусовые качества блюда с помощью самостоятельно собранных растений, если человек не обладает достаточными познаниями в сфере гербологии. Количество подобных случаев не превышает 0,5-1% от всех природных экзотоксикозов.
- Кожный контакт с соком растений. Обычно вызывает местные признаки поражения. Наиболее распространены ожоги, спровоцированные соком борщевика. Они проявляются только под влиянием солнечного света. В ночное время растение безопасно. При массивных повреждениях возможна гибель пострадавшего от интоксикации и полиорганной недостаточности.
Патогенез
Патогенез напрямую зависит от вида растения и яда, содержащегося в нем. При отравлениях красавкой и беленой на первый план выходят признаки холинолитического синдрома. Нарушается выделение ацетилхолина и проводимость нервного импульса в синапсах. Никотиноподобное влияние болиголова, хвоща и веха ядовитого приводит к блокированию никотиновых рецепторов организма, что сопровождается ухудшением координации, гиперсаливацией, психическими изменениями.
Сердечные гликозиды, содержащиеся в наперстянке, горицвете, ландыше, приводят к нарушениям коронарного ритма. Происходит ингибирование действия некоторых ферментов на мембраны кардиомиоцитов, в них накапливаются ионы натрия, снижается количество внутриклеточного калия. Гелиотроп и крестовник обладают гепатотоксическим влиянием. Они провоцируют нарушение функции печени, развитие диффузных изменений паренхимы. Комплексным действием на ЦНС и сердце обладает аконит, на сердце и ЖКТ — чемерица.
Классификация
Отравление ядовитыми растениями подразделяют по причинам (бытовые, суицидальные, криминальные), по степени тяжести (легкие, средние, тяжелые и крайне тяжелые), по токсичности самого растения (высокотоксичные, среднетоксичные, слаботоксичные). Нужно учитывать, что отравляющая способность трав изменяется в зависимости от времени года и того, какая именно ее часть была употреблена в пищу. Наиболее распространенной является классификация по способности флоры поражать ту или иную систему организма:
Симптомы отравлений
Отравление нейротоксичными растениями
Клиническая картина интоксикации растительными ядами варьирует в широких пределах. Употребление нейротоксичных субстанций приводит к возникновению делирия, психомоторного возбуждения, галлюцинаций, головной боли. Позднее развивается угнетение сознания, сопор, кома. Помимо непосредственных признаков поражения ЦНС, у пациента обнаруживается рвота, тошнота, осиплость голоса, тахикардия, сухость слизистых оболочек. Длительность латентного периода зависит от дозы токсиканта и пути его поступления, может составлять от 10 минут до 10-15 часов.
Отравление кардиотоксичными растениями
Основные симптомы при приеме кардиотропных растений: аритмия, тахикардия, желудочковая экстрасистолия. Пациенты жалуются на ощущение перебоев в работе сердца, чувство сдавления в груди. Кроме того, может возникать абдоминалгия, рвота, мелькание мушек перед глазами. Если отравление ядовитыми растениями имеет хронический характер, развиваются невриты, маниакально-депрессивный психоз. Существует риск полной атриовентрикулярной блокады, остановки сердца.
Отравление гепатотоксичными растениями
Гепатотоксическое влияние трав приводит к появлению желтухи, атаксии, сосудистых звездочек на коже. Определяются явления диспепсии. Живот вздут, отхождение газов нарушено. Кал приобретает светло-серый оттенок, что свидетельствует об ухудшении оттока желчи. Токсический гепатит, развивающийся как результат отравления, нередко сочетается с поражением почек. У пострадавшего снижается количество суточной мочи, нарастают показатели мочевины и креатинина.
Поражение дерматотропными растениями
Попадание сока обжигающих растений на кожу сопровождается возникновением эритемы, пузырей, наполненных серозным содержимым. Возможны системные и местные аллергические реакции. При небольшом размере поражения угроза жизни отсутствует. Массивные травмы проявляются симптоматикой полиорганной недостаточности и интоксикации. Отравления ядами смешанного действия провоцируют картину, которая включает симптомы экзотоксикоза, относящиеся к разным группам.
Осложнения
Распространенным осложнением поражений нейротоксическими ядами считается нарушение работы дыхательных структур головного мозга и паралич респираторных мышц. Развивается у 10-15% пострадавших, при отсутствии медицинской помощи оканчивается летально. Кардиотропные яды приводят к блокаде проводимости I-II степени у 45% больных, III степени – у 3-5%. Поражение печени сопровождается формированием ДВС-синдрома, внутренних кровотечений, полиорганной недостаточности.
Химические ожоги, спровоцированные растительным соком, могут инфицироваться. При этом существует риск сепсиса, инфекционно-токсического шока. Отравляющие вещества, выделяющиеся в кровь при распаде некротизированных тканей, способны нарушить работу систем выделения. Подобная патология встречается у 6-8% больных. Отравление ядовитыми растениями смешанного действия нередко является причиной острой дыхательной и сердечно-сосудистой недостаточности, коматозного состояния. У пациентов, длительно пребывающих на ИВЛ, развиваются пневмонии.
Диагностика
- Физикальное обследование. При нарушении дыхания определяются хрипы, брадипноэ, диффузный цианоз. Может возникать неадекватное поведение, ослабление координации. Кожа бледная или синеватого оттенка, зрачки сужены при интоксикациях атропиноподобными веществами. Присутствует изменение зрения.
- Функциональные методы. На ЭКГ деформированные внеочередные комплексы QRS, волны фибрилляции F, выпадение части желудочковых сигналов, сокращение интервала R-R. АД выше или ниже нормы, характерна тахикардия.
- Лучевые исследования. На УЗИ живота — увеличение размеров печени, диффузные изменения печеночной и почечной паренхимы. На рентгенограмме больных, длительно находящихся на искусственной дыхательной поддержке, могут определяться признаки отека легких.
- Лабораторные анализы. Проводятся качественные пробы, позволяющие определить наличие токсиканта в крови или моче. Показан биохимический анализ, который обнаруживает рост активности ферментов печени. Почечная патология сопровождается увеличением количества креатинина, мочевины. Возможно снижение концентрации факторов свертывания крови.
Лечение отравлений ядовитыми растениями
Доврачебная помощь
При появлении симптомов интоксикации травами следует вызвать медиков и оказать пострадавшему первую помощь. Если яд был употреблен внутрь, необходимо произвести беззондовое промывание желудка: дать выпить 400-500 мл воды, вызвать рвоту. Процедуру повторить 3-5 раз. После контакта с кожными ядами пораженный участок необходимо промыть большим количеством чистой воды, прикрыть тканью, чтобы предотвратить попадание на него прямых солнечных лучей.
Первая медицинская помощь
Отравление ядовитыми растениями требует немедленного введения антидотов. При интоксикации беленой, дурманом вводят прозерин; наперстянкой, ландышем — лидокаин и другие антиаритмические препараты. Требуется зондовое промывание желудка с последующим введением кишечных адсорбентов. Отравляющие вещества, всосавшиеся в кровоток, нейтрализуют с помощью тиосульфата натрия, унитиола. При тяжелой патологии показана симптоматическая коррекция, инфузионная терапия.
Реанимационное пособие
В ОРИТ помещают пострадавших с тяжелой и крайне тяжелой степенью поражения. Здесь проводится круглосуточный аппаратный мониторинг состояния, массивный форсированный диурез (до 10 литров за сутки), строгий контроль водного баланса. При необходимости осуществляется респираторная поддержка с помощью аппарата ИВЛ. Полная блокада внутрисердечной проводимости требует установки внешнего кардиостимулятора. Для поддержания гемодинамики вливается дофамин, норадреналин. При остановке сердца проводятся мероприятия, направленные на восстановление жизнедеятельности.
Лечение в условиях стационара
Во время стационарного лечения пациент продолжает получать адсорбенты и антидоты. Используются способы активной детоксикации (гемосорбция или гемодиализ), форсированный диурез, солевые слабительные или кишечный лаваж. С целью купирования судорог применяют антиконвульсанты, психомоторное возбуждение устраняют нейролептическими средствами. Показано профилактическое введение антибиотиков. Это особенно актуально в отношении пациентов, длительно сохраняющих лежачее положение.
Прогноз и профилактика
Прогноз в большинстве случаев благоприятный. Отравление ядовитыми растениями в 90% наблюдений проходит без последствий. Гибель пострадавшего возможна при тяжелых интоксикациях и отсутствии специализированной помощи. Отсроченные осложнения возникают редко. Подобное происходит, если имела место полиорганная недостаточность, токсический гепатит.
Профилактика заключается в отказе от употребления незнакомых растений внутрь, исключении самолечения с помощью средств народной медицины, содержащих опасные травы, внимательном изучении информации о собираемых растениях.
3. Руководство по скорой медицинской помощи/ Багненко С.Ф., Мирошниченко А.Г., Верткин А.Л., Хубутия М.Ш. — 2007.
Читайте также:

