Паразиты относятся к патогенам
Обновлено: 24.04.2024
В статье представлены современные данные о ларвальных гельминтозах у детей, самым распространенным и трудно диагностируемым из которых является токсокароз, имеющий тяжелое хроническое течение с выраженным иммуносупрессивным эффектом и полиорганными пораже
The article represents the modern data on larva migrans in children, toxocariasis being the most widespread and difficultly diagnosed among them, with severe clinical course, pronounced immunosuppressing effect and multiple affections of organs. Pathogenesis, therapy and prevention of the disease are discussed.
Распространенность гельминтозов среди жителей различных континентов Земли огромна: на каждого жителя Африки приходится более двух видов гельминтов, в Азии и Латинской Америке более одного вида, в Европе поражен каждый третий житель. В России практически каждый человек в течение жизни переносит паразитарное заболевание, причем чаще страдают дети [1]. По величине ущерба, наносимого здоровью людей, гельминтозы занимают 4-е место после диареи, туберкулеза и ишемической болезни сердца. Ежегодно в мире от гельминтозов погибают 135 тыс. человек, причем число это неуклонно растет [2].
- санитарно-гигиенические — высокий уровень контаминации окружающей среды яйцами гельминтов в результате сброса необезвреженных сточных вод и стоков животноводческих комплексов; недостаточные гигиенические навыки населения, привычка удобрять почву экскрементами;
- миграционными — усилением миграции населения и завозом паразитарных болезней из эндемических стран, вторжением городского населения в сельскую местность (работа на садовых участках, дачах, личных фермах), рост числа бродячих животных;
- информационными — малая информированность населения, а порой и врачей о гельминтозах и путях их заражения, профилактика гельминтозов ограничена лишь лечением вновь выявленных случаев заболевания;
- этническими — особенности питания населения, а именно употребление сырой или слабообработанной продукции;
- экономическими — обеднение населения, удорожание лекарственных препаратов;
- экологическими — снижение общей иммунной реактивности.
В настоящее время известно около 270 видов гельминтов, паразитирующих в организме человека, из которых 30 широко распространены на территории России. Гельминты, паразитирующие у человека, относятся к типу плоских червей, среди которых различают два класса: Cestoidea — ленточные черви и Trematoda — сосальщики, и типу круглых червей (класс Nematoda — собственно круглые черви). В зависимости от места паразитирования в организме человека, гельминты подразделяются на просветные, к которым относится большинство патогенных для человека гельминтов, и тканевые. В тканях в свою очередь могут обитать как взрослые особи, так и личинки.
Гельминтозы, при которых основным патогеном являются личинки, мигрирующие или покоящиеся, называют личиночными или ларвальными [3]. Особенностью ларвальных гельминтозов является то, что человек в данной ситуации является промежуточным или случайным хозяином, а жизненный цикл паразита не завершается, личинка не превращается в половозрелую особь и не может дать потомство [4]. Следовательно, такой вид паразитирования является биологическим тупиком. К числу таких гельминтозов относят многие филяриозы, трихинеллез, гнатостомоз, капилляриоз, спарганоз, эхинококкозы, токсокароз и др.
В отсутствие этиологического диагноза, который поставить удается не всегда, этот вид гельминтозов обозначают обобщенным термином Larva migrans, под которым понимают симптомокомплекс, обусловленный паразитированием личинок гельминтов, для которых человек не является естественным хозяином [5–7]. В зависимости от пути проникновения и места паразитирования условно выделяют перкутанные, или кожные, и висцеральные формы. Возбудителями кожной формы являются шистосомы, анкилостомы, некоторые виды филярий. При этом личинки гельминтов проникают в неповрежденную кожу при контакте с водой или почвой, паразитируют в эпидермисе, дерме или гиподерме, а после самопроизвольной гибели личинки, через 1–6 месяцев, наступает полное выздоровление [8]. Это условно доброкачественные гельминтозы. Висцеральная форма, возбудителями которой являются эхинококки, токсокары, цистицерки и др., возникает при проглатывании человеком яиц гельминтов с водой, продуктами питания, частичками почвы и протекает зачастую тяжело, длительно, порой годами и, как правило, не заканчивается спонтанным выздоровлением. Прогноз у данной группы гельминтозов серьезный, вплоть до летального исхода [9].
Наиболее тяжело протекают ларвальные (личиночные) гельминтозы вследствие множественного поражения печени, легких, сердца, почек, головного мозга, органа зрения и др. (токсокароз, однокамерный эхинококкоз, цистицеркоз) или агрессивного роста и метастазов зародышей или яиц паразита (многокамерный эхинококкоз, парагонимоз). Кроме этого, обладая значительной антигенной чужеродностью, мигрирующие личинки вызывают тяжелую общую и местную аллергическую реакцию, вплоть до формирования в тканях эозинофильных гранулем, оказывают механическое и токсическое повреждение [10].
Для гельминтозов характерен широкий диапазон клинических симптомов: от слабовыраженных до генерализованных реакций с множественными поражениями. Именно такая неспецифичность, малоинформативность стандартных методик гельминтологического исследования на яйца глистов, в совокупности с традиционным отсутствием настороженности у городских практических врачей, побудили нас еще раз обратить внимание на эту проблему. Часто правильный диагноз скрывается за самыми разнообразными масками и распознается поздно (рис. 1).
.jpg)
Токсокароз является самым распространенным из ларвальных гельминтозов у детей, пораженность токсокарозом в странах умеренного пояса составляет от 2% до 37%, достигая 92,8% в тропических странах [11–14]. Токсокароз — это зоогельминтоз, имеющий тяжелое хроническое течение с выраженным иммуносупрессирующим эффектом и полиорганными поражениями. Возбудителем токсокароза является нематода из рода Toksokara. Наиболее известны Toksokara catis, паразитирующая в организме кошек, и Toksokara canis, паразитирующая в организме собак, волков, лисиц, песцов и других представителей семейства псовых [15, 16]. Самка Toksokara canis имеет длину 9–18 см, самец — 5–10 см. Взрослые паразиты локализуются в желудке и тонкой кишке окончательных хозяев. Средняя продолжительность жизни половозрелых особей составляет 4–6 мес, и каждая самка Toksokara canis откладывает более 200 тыс. яиц в сутки. Яйца выделяются незрелыми и через 5–8 дней инкубации в почве становятся инвазионными, сохраняя жизнеспособность и инвазивность до 10 лет. Кроме этого, широкому распространению токсокароза среди животных способствует совершенный механизм передачи возбудителя, при котором сочетаются прямой (заражение яйцами из окружающей среды), внутриутробный (заражение плода личинками через плаценту), трансмаммарный (передача личинок с молоком) пути передачи и заражение через резервуарных (паратенических) хозяев.
Основной источник опасности для человека — это домашние и бродячие собаки разного возраста. В настоящее время в Москве численность собак превышает 1 млн особей, которые ежедневно оставляют на ее территории около 270 тонн экскрементов, содержащих более 40 тысяч яиц токсокар в каждом грамме! Поэтому каждая вторая проба почвы детских площадок, скверов, парков и территорий вокруг жилых домов содержит яйца этих паразитов [17–20]. У детей заражению может способствовать геофагия, именно поэтому токсокарозом чаще болеют дети дошкольного возраста. Прямой контакт с собакой также может привести к заражению через шерсть, загрязненную почвой, содержащей зрелые яйца токсокар. Ребенок может заражаться круглогодично через загрязненные яйцами почву, продукты питания, воду, руки. Установлена роль тараканов в распространении токсокароза: они поедают значительное количество яиц токсокар и до 25% их выделяют в жизнеспособном состоянии в окружающую среду [21]. Группу риска составляют люди, по роду деятельности контактирующие с животными и почвой.
Человек служит паратеническим (резервуарным) хозяином, являясь для паразита биологическим тупиком, так как токсокары паразитируют у него только в личиночной стадии, не выделяясь в окружающую среду. После проглатывания человеком зрелых яиц, в проксимальном отделе тонкого кишечника из них выходят личинки, которые через слизистую оболочку проникают в кровоток, затем заносятся в печень и правую половину сердца. Попав в легочную артерию, личинки продолжают миграцию и переходят из капилляров в легочную вену, достигают левой половины сердца и затем разносятся кровью по разным органам и тканям. Мигрируя, они достигают места, где диаметр сосуда меньше размера самой личинки, и покидают кровяное русло. Личинки токсокар могут оседать абсолютно во всех органах и тканях, сохраняя жизнеспособность в течение длительного времени, периодически активизируясь и возобновляя миграцию. С течением времени часть личинок инкапсулируется и постепенно разрушается внутри капсулы.
Токсокароз имеет длительное, рецидивирующее течение [22]. Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека [23, 24]. В зависимости от преимущественной локализации личинок выделяют висцеральную и глазную формы токсокароза.
Висцеральный токсокароз встречается чаще как у детей, так и у взрослых и возникает в результате заражения большим числом личинок [25]. Клинические проявления острого токсокароза разнообразны (рис. 2).
Для больных токсокарозом наиболее характерна субфебрильная, реже — фебрильная лихорадка с пиком во второй половине дня, сопровождающаяся недомоганием и ознобом. Как правило, одновременно с лихорадкой выявляется синдром поражения легких, варьирующий в широких пределах: от катаральных явлений до тяжелых астмоидных состояний. Могут наблюдаться рецидивирующие бронхиты, бронхопневмонии вплоть до летального исхода. При рентгенологическом исследовании в этот период выявляются множественные или единичные эозинофильные инфильтраты, так называемый синдром Леффлера. Наряду с синдромом поражения легких часто отмечается увеличение размеров печени, а иногда и селезенки, сопровождающееся болями в животе, тошнотой, рвотой и диарей. Практически у всех больных выявляется лимфаденопатия. В отдельных случаях токсокароз сопровождается развитием аллергического миокардита, панкреатита, поражением почек [26]. Поражение кожи при токсокарозе встречается реже и отличается полиморфностью высыпаний: от эритем до пятнисто-папулезных и уртикарных элементов. Все чаще стали выявлять и поражение центральной нервной системы, которое может протекать в виде эписиндрома, гиперактивности, аффективной неустойчивости, трудностей в учебе. В тяжелых случаях регистрируется менингоэнцефалит, парезы, параличи, нарушения психики. Увязать такие явления непосредственно с токсокарозом весьма проблематично, однако в одном из сероэпидемиологических исследований, проведенном в 1984 г., показана связь затруднений при чтении, невозможности сосредоточиться и низкого уровня интеллекта с заболеванием дошкольников токсокарозом.
Золотым стандартом диагностики любого гельминтоза является паразитологический метод. Однако прижизненный паразитологический диагноз токсокароза практически невозможен, поскольку обнаружить мигрирующие личинки трудно, а идентифицировать их по гистологическим срезам весьма непросто [29].
Клиническо-анамнестическая диагностика токсокароза также затруднительна ввиду полиморфизма и неопределенности клинических проявлений. В повседневной клинической практике своевременная постановка диагноза и назначение специфической терапии — скорее исключение, чем правило. Для облегчения задачи в 1978 г. был предложен диагностический алгоритм (табл.).
При сочетании симптомов и признаков на сумму более 12 баллов целесообразно назначение иммунологической диагностики. В диагностике глазного токсокароза может помочь офтальмологическое обследование с обнаружением личинки в области диска зрительного нерва или в макулярной части.
Диагностика токсокароза на сегодняшний день основывается на лабораторных методах исследования [30]. Одним из постоянных проявлений висцеральной формы токсокароза является лейкоцитоз и стойкая длительная эозинофилия до 30–90%. Наблюдается также умеренная анемия, гиперпротеинемия, гипергаммаглобулинемия, высокий уровень IgE. При поражении печени отмечаются нарушения ее функции.
Наиболее информативными в диагностике токсокароза являются иммунологические методы, а именно определение титра специфических IgG-антител к Toksokara canis методом иммуноферментного анализа (ИФА), обладающим высокой чувствительностью и достаточной специфичностью при висцеральной локализации гельминта — 93,7% и 89,3% соответственно [31]. Установлена корреляция между клиническими проявлениями, тяжестью процесса и титpами антител. Титp специфических антител 1:800 и выше с большой степенью вероятности свидетельствует о заболевании, а титpы 1:200–1:400 — о носительстве токсокаp при висцеральном токсокаpозе и патологическом процессе пpи токсокаpозе глаза. За лицами с низкими титрами противотоксокарозных антител устанавливается диспансерное наблюдение и пpи появлении клинических признаков болезни рекомендуется проведение специфической терапии. Однако необходимо помнить, что не всегда имеется прямая корреляция между титром антител и тяжестью заболевания, так как токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного. Кроме того, возможны и ложные результаты исследования: ложноположительные могут наблюдаться у больных эхинококкозами, описторхозом (в острой фазе заболевания), миграционной фазой аскаридоза; ложноотрицательные — при токсокарозе глаз, первичном иммунодефиците, длительном течении гельминтоза.
До настоящего времени нет единой схемы специфической терапии токсокароза, базирующейся на научных данных. Обычно применяют противонематодозные препараты, действующие на личиночную стадию гельминтов — альбендазол и мебендазол; ивермектин и диэтилкарбамазин [32]. Все препараты активны в отношении мигрирующих личинок и недостаточно активны в отношении тканевых форм, находящихся в гранулемах. Самым часто используемым является мебендазол, назначаемый в дозе 200–300 мг/сут в 2–3 приема, внутрь, в течение 10–14 дней. Повторный курс проводят через 2 недели. Диэтилкарбамазин назначают в дозе 3–4 мг/кг/сут в 2 приема, внутрь, в течение 21 дня. Однако наиболее широким спектром действия обладает альбендазол, эффективный в отношении большинства кишечных нематодозов и ларвальных цестодозов. Механизм действия альбендазола связан с избирательным подавлением полимеризации бета-тубулина, что ведет к деструкции цитоплазматических микроканальцев клеток кишечного тракта гельминтов. Назначается альбендазол в дозе 10 мг/кг/сут в два приема, внутрь, после еды в течение 10–14 дней. Необходимость повторного курса устанавливается после клинико-лабораторного обследования больного. Побочные явления, возникающие при применении вышеуказанных препаратов, могут быть связаны не только с токсическим действием антигельминтных препаратов, но и с реакцией организма на массовую гибель личинок токсокар. Поэтому в процессе лечения целесообразно назначать антигистаминные препараты, а в ряде случаев и кортикостероиды.
При глазном токсокарозе гранулемы удаляют микрохирургическими методами, для разрушения личинок в средах глаза применяют лазерокоагуляцию [33]. При бессимптомном течении с низкими титрами специфических антител лечение не проводится, а за больными устанавливается динамическое наблюдение.
Критериями эффективности лечения считают постепенное снижение и ликвидацию клинических проявлений токсокароза, уменьшение уровня эозинофилов и специфических антител. Вместе с тем исследования показывают, что в результате лечения процесс снижения уровня специфических антител идет медленно и не охватывает всех пациентов. Клинический эффект от лечения опережает гематологический и иммунологический. При рецидивах симптоматики, сохранении стойкой эозинофилии или повышении титра специфических антител проводят повторные курсы, иногда до 4–5.
Диспансерное наблюдение за переболевшими проводит врач-инфекционист или педиатр на протяжении не менее 6 месяцев. Больные подлежат осмотру 1 раз в 2 месяца и снимаются с учета после 2-кратного отрицательного результата на антитела методом ИФА с интервалом в 3–4 месяца. Прогноз в большинстве случаев благоприятный.
Основную роль в контроле заболеваемости токсокарозом играет традиционная профилактика, которая включает в себя соблюдение правил личной гигиены, обязательное обучение детей санитарным навыкам, своевременную дегельминтизацию собак, оборудование мест выгула собак, повышение культурного уровня владельцев собак [34].
Литература
А. С. Боткина 1 , кандидат медицинских наук
М. И. Дубровская, доктор медицинских наук, профессор
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Типы патогенных микроорганизмов. Токсины
В норме организм человека населён различными бактериями и простейшими, которые не вызывают инфекционных заболеваний. Инфекционный процесс возникает при поражении патогенной микрофлорой тканей и слизистых оболочек организма хозяина. Патоген — агент, способный вызвать инфекционный процесс.
Представителей нормальной микрофлоры считают условно-патогенными (комменсалами). Патогенность — способность микроорганизма вызывать заболевание макроорганизма. Вирулентность — степень патогенности (способность вызвать тяжёлое течение заболевания).
Например, основной фактор, определяющий патогенность Streptococcus pneumoniae, — капсула, без которой этот микроорганизм не может вызвать инфекцию. В роли возбудителей могут выступать простейшие и некоторые многоклеточные организмы. Они также могут быть патогенными и условно-патогенными.
Типы патогенных микроорганизмов
Облигатные патогены практически всегда вызывают заболевание (например, Treponema pallidum, ВИЧ). Условно-патогенные микроорганизмы вызывают заболевание только при определённых условиях.
Например, Bacteroides fragilis (комменсал) — представитель нормальной микрофлоры кишечника, но при попадании в брюшную полость (особенно вместе с Е. coli) он может стать причиной абсцесса; Staphylococcus aureus является комменсалом бактериальной флоры передних отделов носовых проходов, он может быть причиной заболевания только при попадании на раневую поверхность.
Другие микроорганизмы считают оппортунистическими патогенами. Они обычно поражают людей со слабой иммунной системой. Например, Pneumocystis jiroveci может быть причиной пневмонии только у пациентов со сниженным Т-клеточным иммунитетом.
Токсины патогенных микроорганизмов
Эндотоксины — стимуляторы выработки ИЛ-1 и ФНО-а макрофагами, вызывающие развитие лихорадки и шока.
Экзотоксины — вещества белковой структуры, оказывающие местное или системное повреждающее воздействие на макроорганизм. Большинство из них состоит из нескольких субъединиц, одна из которых способствует прикреплению или проникновению в клетки-мишени, а вторая обусловливает физиологический эффект.
Классический пример — холерный токсин, В-субъединица которого связывается с эпителиальными клетками, а А-субъединица активирует аденилатциклазу и усиливает отток ионов натрия и хлора из клетки, способствуя возникновению диареи.
Некоторые экзотоксины выступают в роли суперантигенов, вызывая неспецифическую активацию Т-клеток, усиливая выработку медиаторов воспаления — цитокинов, что приводит к развитию ярко выраженных физиологических эффектов (лихорадки, шока, желудочно-кишечных расстройств, сыпи).
Некоторые экзотоксины влияют на синтез белка (например, дифтерийный токсин и синегнойный экзотоксин А), в то время как другие нарушают нервно-мышечную передачу (столбнячный и ботулиновый токсины).
В большинстве случаев антитела к токсинам нейтрализуют их эффекты и обладают протективным действием.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
• Хотя на теле человека или в его организме обитает много микробов, лишь небольшая их часть представляет собой патогенные бактерии
• Патогенные бактерии способны заселять ткани организма хозяина, а также размножаться и существовать в них
• Многие патогенные микроорганизмы продуцируют токсины, которые усугубляют поражение клеток организма хозяина
Организм животных содержит достаточное количество питательных веществ и обеспечивает поддержание относительно стабильных значений pH, осмотического давления и температуры. Это создает оптимальную среду для роста разнообразных прокариот. Тесные биологические взаимоотношения, существующие между двумя различными организмами, например между микробами и клетками хозяина, называются симбиотическими. В зависимости от степени выгоды или вреда, симбиоз между хозяином и микробом может быть взаимным, комменсальным паразитическим или патогенным. Эндосимбиоз рассматривался в предыдущем разделе.
Абсолютное большинство прокариот, находящихся в симбиотических отношениях с другими клетками, являются комменсальными резидентами, которые или слабо влияют на организм хозяина, или вообще не оказывают на него никакого влияния. Некоторые комменсальные обитатели оказываются полезными, и в некоторых случаях выполняют нужные функции в организме хозяина. Например, штаммы Е. coli, содержащиеся в желудочно-кишечном тракте, помогают пищеварению.
Микробы, растущие в организме, и не приносящие ему пользы называются паразиты. Некоторые из таких паразитических взаимоотношений оказываются вредными для организма хозяина. Микробы, которые причиняют вред организму хозяина, называются патогенными, и их способность заселять организм и вызывать заболевания является результатом многих факторов как со стороны организма хозяина, так и со стороны микроорганизмов. Патогенные микроорганизмы подразделяются на оппортунистические и первичные. Оппортунистические бактерии вызывают инфекции только при поражениях организма, например при тяжелых ожогах, СПИДе, и у некоторых раковых больных.
Первичные патогены вызывают заболевание нормального, здорового организма, и иногда их размножение полностью зависит от самого организма хозяина. Независимо от типа патогена, вызывающего инфекцию, микроб должен проникнуть в организм хозяина, заселить его, избежать атаки со стороны иммунной системы, и начать размножаться. Наряду с этим, первичные патогены должны подготовиться к передаче инфекции к другому хозяину.
До того как патоген вызовет повреждения в организме хозяина, он должен получить доступ к его тканям и начать размножаться. Места первичной инфекции обычно представляют собой открытые участки, например на коже или участки слизистой дыхательного, мочеполового и кишечного эпителия. На поверхности микробных клеток экспрессируются несколько разных молекул, которые связываются с рецепторами, присутствующими в тканях хозяина. Эти адгезивные молекулы представляют собой полисахариды или белки. Например, Streptococcus mutans посредством своей полисахаридной капсулы адсорбируется на поверхности зубной эмали и вызывает кариес.
Для прикрепления к клеткам тканей хозяина, многие микробы используют такие поверхностные белковые структуры, как пили. Наличие таких адгезивных органелл часто обеспечивает патогену вирулентность, и при их отсутствии микроорганизмы оказываются неспособными вызвать инфекцию; они обычно уничтожаются и выводятся из организма.
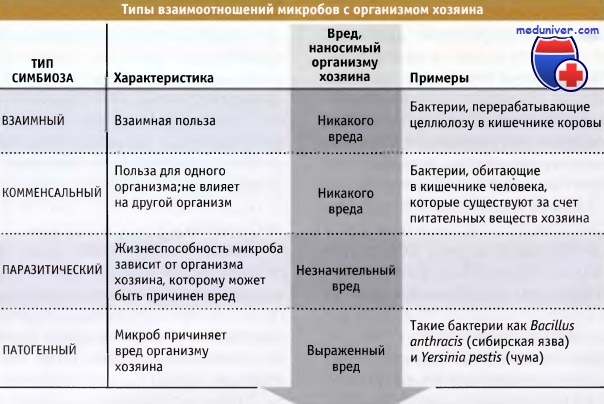
Существует несколько типов симбиотических взаимоотношений.
В зависимости от этого, симбиоз может оказаться полезным или вредным для организма хозяина.
Прикрепление микробов к тканям представляет собой тканеспецифичный процесс и зависит также от вида бактерий. Специфичность по отношению к определенным тканям обычно называют тропностыо. Например, микроб, вызывающий гоноррею, Neisseria gonorrhoeae, прочно прикрепляется к эпителию мочеполовой системы и почти не связывается с эпителиальными клетками другой локализации. К числу примеров иллюстрирующих специфичность связывания, в зависимости от вида бактерий, относится связывание с клетками почечного эпителия штамма Е. coli, вызывающего пиелонефрит. Эти штаммы обладают одной из трех разновидностей Р-ворсинок, каждая из которых специфична в отношении почечного эпителия человека, собаки или крысы.
Некоторые бактериальные патогены заселяют эпителий, вызывая инфекцию. Такая инвазия дает микробам доступ к питательным продуктам, которые поддерживают их размножение. Попадание через эпителий в кровеносные сосуды позволяет бактериям расти не только в местах первоначального заселения, но и в более отдаленных. Системные инфекции часто являются результатом проявления активности патогена, получившего доступ в кровь или лимфатическую систему, при инвазии эпителиального слоя.
Поскольку первоначальный очаг заражения редко бывает достаточно обширным, патоген должен размножиться в организме, чтобы вызвать ощутимые последствия. Ткани организма хозяина являются подходящим местом для роста бактерий. Однако в тканях существует недостаток некоторых необходимых питательных компонентов, и патогенные микроорганизмы должны быть способны более эффективно использовать имеющиеся ресурсы и в то же время противостоять атакам со стороны иммунной системы хозяина. Преимуществом обладают бактерии, способные использовать сложные источники питания, например гликоген. Патогены могут конкурировать с клетками организма хозяина за микроэлементы, например за железо.
В клетках животных есть два белка, трансферрин и лактоферрин, которые связывают и переносят железо. Таким образом в тканях организма хозяина находится очень мало свободной формы железа. Для обхода этой системы у патогенных бактерий существуют эффективные комплексы, хелатирующие железо, которые называются сидерофоры. Они помогают им накапливать железо из окружающей среды.
Патогенные бактерии продуцируют множество вирулентных факторов, которые помогают им инфицировать организм хозяина и поддерживать патологический процесс. К числу грамположительных патогенов относятся Streptococci, Staphylococci и Pneumococci, которые продуцируют ферменты, расщепляющие полисахариды клетки хозяина, что дает возможность инфекции распространяться по тканям. Clostridium является продуцентом коллагеназы, которая деполимеризует коллагеновые структуры, скрепляющие ткани хозяина, в результате чего микроб распространяется по организму. Streptococcus pyogenes распространяется по тканям благодаря действию стрептокиназы, которую продуцирует этот микроорганизм. Стрептокиназа ослабляет фибриновые структуры клеток и тканей хозяина, препятствующие распространению патогена.
Наоборот, некоторые патогены способны локализоваться (образовывать защитную оболочку вокруг своей клетки) за счет продуцирования ферментов, обеспечивающих образование фибринового сгустка. К числу хорошо известных ферментов такого типа относится коагулаза, продуцируемая Staphylococcus aureus. Микроорганизмы, продуцирующие коагулазу, покрываются фибриновой оболочкой, и считается, что она предохраняет микроб от действия защитных систем организма хозяина.
Наряду с попаданием бактерий и их размножением поражение организма хозяина усиливается под действием бактериальных токсинов. Выделяемые токсины называются экзотоксинами, и они способны повреждать ткани, расположенные далеко от места первичной инфекции. По механизму действия экзотоксины можно подразделить на три группы. Цитолитические экзотоксины, например гемолизин, действуют на цитоплазматические мембраны клеток организма хозяина и вызывают их лизис. Штаммы бактерий, обладающие гемолитическим действием, легко идентифицируются при выращивании на агаре, содержащем кровь. При выделении гемолизина происходит лизис эритроцитов, что приводит к образованию белых участков на фоне красного агара. Представителем второй группы экзотоксинов является токсин, продуцируемый Corynebacterium diphtheriae, который вызывает заболевание дифтерией.
Когда Corynebacterium попадает в среду с низким содержанием железа (что свидетельствует о попадании бактерии в организм хозяина), она начинает секретировать дифтерийный токсин, который попадает в клетки организма хозяина и вызывает остановку трансляции. К третьей группе относятся нейротоксины, включая ботулинический токсин, продуцируемый Clostridiun botulinum. Для человека это наиболее токсичный из известных токсинов. Ботулинический токсин блокирует высвобождение ацетилхолина из нервных клеток, что приводит к необратимому расслаблению мышц и к параличам.
Каждый патогенный микроорганизм использует свои детерминанты вирулентности, вызывающие то или иное инфекционное заболевание. Для микроорганизмов, продуцирующих сильные токсины, начальная степень инвазии и темпы размножения микробов не играют критической роли. Например, Clostridium tetani не относится к инвазивным микроорганизмам, поскольку продуцирует мощный токсин. Инфекция С. tetani часто приводит к смертельному исходу. В то же время Streptococcus pneumoniae не продуцирует токсин однако из-за высоких темпов размножения микроорганизма в легочной ткани инфекции оказываются смертельными. Большие количества бактерий в ткани легких ослабляют иммунную систему организма и вызывают пневмонию. Исследование механизмов вирулентности прокариот обеспечивает разработку новых терапевтических средств для борьбы с инфекционными заболеваниями.
Динамика взаимоотношений организма хозяина с патогенными микробами представляет собой бурно развивающуюся область исследований.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Паразитарные заболевания человека – это отдельная группа болезней, все они провоцируются паразитирующими одноклеточными и одноклеточными организмами. Самыми распространёнными паразитами являются черви (гельминты), за ними следуют членистоногие (насекомые и клещи). Паразитарные болезни называют инвазионными болезнями или просто инвазиями.
Паразиты могут быть временными и постоянными. Их жизненный цикл очень сложен, в ряде случаев для формирования полноценной особи паразиту требуется сменить троих хозяев.
Инвазионные болезни весьма опасны для здоровья человека. Паразиты способны причинять организму хозяина механические повреждения, отравлять его продуктами своей жизнедеятельности, провоцировать развитие аллергических реакций, питаться кровью человека, оказывать негативное влияние на течение других заболеваний.
Паразитарные заболевания имеют широкое распространение. По данным ВОЗ, каждый четвёртый житель Земли является носителем того или иного паразита. Кишечные гельминты относят к наиболее опасным болезням, считается, что они занимают 4 место по нанесению ущерба здоровью человека в сравнении с другими патологиями. Обгоняют паразитарные болезни по распространенности только туберкулёз, ишемическая болезнь сердца и диарея. Одна из особенностей паразитарных болезней заключается в том, что в организме человека (если лечение отсутствует) и вызывать повторное заражение.
Различают следующие виды гельминтов:
-Трематодозы, гельминтозы, провоцируемые сосальщиками: лёгочный сосальщик, печёночный сосальщик, кошачья двуустка, шистосомы, клонорх.
-Нематодозы – инвазии крупными червями. Источников заражения является человек. среди всех видов гельминтов нематодозы распространены шире всего. Они вызываются аскаридами, острицами, власоглавами, токсокарами и трихинеллами.
- Цестодозы – инвазии ленточными червями, среди которых бычий цепень (солитёр или цепень невооружённый) свиной цепень (цепень вооружённый), карликовый цепень, широкий лентец, эхинококк и альвеококк.
Кроме гельминтов, возбудителями паразитарных болезнея являются:
- протозойные или простейшие организмы, среди которых лямблии, малярийные плазмодии, токсоплазмы, трихомонады и пр.
- эктопаразиты, среди которых вши (лобковая, головная и платяная), клопы и клещи.
- прочие паразиты: личинки москитов, личинки мух, песчаные блохи.
Симптомы паразитарных болезней зачастую бывают смазаны. Они могут вовсе отсутствовать на протяжении многих лет, а могут проявляться остро.
Основными признаками паразитарной инвазии являются:
- Аллергические реакции по типу крапивницы;
- повышение температуры тела;
- Лимфаденит – воспаление лимфатических узлов. Одновременно возникают головные боли, ухудшается аппетит, недомогание;
- Артралгии и миалгии. Боли в мышцах и суставах чаще всего являются следствием иммунологических реакций. Мышцы и суставы могут болеть потому, что в них находятся личинки паразитов, либо по причине общей воспалительной реакции организма;
- Лёгочный синдром часто возникает и проявляется в изнурительном кашле, одышке, боли в груди;
- Отёки – частый синдром. Они могут затрагивать конечности и лицо, но могут распространяться на всё тело;
- Абдоминальный синдром – запоры или понос, метеоризм, тошнота, рвота, боли в животе;
- Астеноневротические расстройства- проблемы со сном, раздражительность, судороги, головные боли, головокружение;
- Кожные заболевания – псориаз, себорея, дерматит, ухудшается состояние волос;
- Нарушения со стороны мочеполовой и выделительной систем;
- Частые простудные заболевания.
Лечение паразитарных заболеваний сводится к приёму антипаразитарных препаратов, которые подбирать должен врач.
Профилактика паразитарных заболеваний сводится к соблюдению следующих рекомендаций:
- Соблюдение правил личной гигиены. Это касается мытья рук перед приёмом пищи, после каждого посещения туалета, общественных мест и после контакта с животными;
- Все продукты питания должны проходить соответствующую обработку;
- мясо и рыба должны быть обработаны термически;
- Воду следует кипятить;
-домашним животным необходимо проводить профилактические антипаразитарные курсы;
- в помещении должна проводиться регулярная влажная уборка;
- Во время работы с землёй руки должны быть в перчатках.
Это основные меры профилактики паразитарных заболевания, которые позволят максимально оградить себя и близких от возможной инвазии.

Существует огромное количество разнообразных паразитов, которые могут существовать во внутренних органах человека или населять его кожу и волосы. В том числе такими паразитами могут быть и гельминты.
Гельми́нты - общее название червей-паразитов, обитающих в организме человека, других животных или растений.
Согласно статистическим данным Всемирной организации здравоохранения, в мире более 4,5 млрд. человек заражены различными паразитами, многие из которых являются гельминтами.
В официальной отчетной статистике Российской Федерации отмечается рост заболеваемости основными гельминтозами на некоторых территориях субъектов Российской Федерации, в частности: эхинококкоз, описторхоз. В ряде территорий остаются на высоком уровне показатели заболеваемости энтеробиозом и аскаридозом.
Способов попадания в организм человека гельминтов довольно много, однако, одним из наиболее часто встречающихся путей заражения является заражение через пищевые продукты. Плохо промытые овощи, фрукты или зелень, недостаточно прожаренное или сваренное мясо, рыба, птица, неправильно обработанные продукты питания, могут привести к заражению гельминтами.
Заразиться можно и в случае неправильного хранения готового продукта, например, хранение сладкой выпечки без защитной упаковки может привести к заражению гельминтами, яйца которых могут попасть в готовой продукт с помощью мух или других насекомых.
Давайте же попробуем разобраться, какие гельминты, передающиеся с пищей и встречаются наиболее часто в нашей стране, и как свести к минимуму риск заражения ими.
Сосальщики (кошачий, печеночный, ланцетовидный и др. )
У человека могут паразитировать более 40 видов сосальщиков, при этом локализация гельминтов в организме может быть самой различной – печень, легкие, кровеносные сосуды.
Печеночный сосальщик является возбудителем возбудитель фасциолеза и поражает печень и желчный пузырь.
На территории Российской федерации встречается в Тюменской, Иркутской, Калининградской, Кировской областях, в республике Саха.
Человек заражается при употреблении овощных огородных культур, для полива которых использовалась вода из открытых водоемов.
У больных появляются общие симптомы интоксикации – слабость, снижение аппетита, тошнота, головные боли. Могут возникнуть аллергические реакции в виде кожного зуда или крапивницы, астматические приступы.
Увеличение размеров паразита может привести к нарушению поступления желчи в двенадцатиперстную кишку и возникновению признаков механической желтухи. У больных появляются боли в правом подреберье. Далее может наблюдаться желтушность кожных покровов и наблюдается обесцвечивание кала.
Возбудители описторхоза является кошачий сосальщик.
Заболевание характеризуется преимущественным поражением печени и поджелудочной железы. В России основные очаги гельминтоза это Обь-Иртышский бассейн, а также бассейны рек Волги и Камы.
Заражение человека происходит при употреблении сырой, недостаточно термически обработанной или просоленной рыбы.
Клинические проявления описторхоза характеризуются значительным разнообразием. Это зависит от индивидуальных особенностей организма, а также от интенсивности и продолжительности заражения. Количество паразитирующих червей может колебаться в большом диапазоне: от единичных паразитов до нескольких десятков, и даже сотен. Повторное употребление зараженной рыбы приводит к нарастанию заражения и усугубления протекания клинических проявлений. Клинически заболевание может сопровождаться повышением температуры у больных, появлением крапивницы, кожного зуда, болями в мышцах и суставах. У больных могут быть боли в правом подреберье, чувство тяжести в желудке, тошнота.
Основным возбудителем парагонимоза у человека является легочный сосальщик.
Легочный сосальщик на территории РФ обитает в Приморском и Хабаровском краях, Амурской области.
Возбудитель заболевания попадает в кишечник человека при употреблении в пищу ракообразных, обитающих в местностях, где имеется очаг заболевания, и совершает миграцию по организму: проникают через стенку кишечника в брюшную полость, а затем через диафрагму попадают в плевральную полость, далее – в ткань легких. Личинки сосальщика могут также проникнуть в другие органы и ткани. Особенно опасна локализация паразита в головном мозге. Внелегочная локализация паразита бывает у трети зараженных людей и часто является причиной летального исхода.
На ранней стадии заболевания, когда легочный сосальщик только мигрирует по организму, болезнь протекает практически бессимптомно. Иногда возможны небольшие аллергические реакции, кожный зуд, реже — боль в животе, желтуха. Как только паразит достигает места конечной локализации, у больных появляются ярко выраженные симптомы поражения легких: постоянный кашель с обильной мокротой, сильные боли в области грудной клетки. Во время болезни могут возникнуть различные осложнения, например, пневмоторакс – попадание воздуха в плевральную полость. Очень часто у больных развиваются пневмония или плеврит (воспаление в плевральной полости).
Ленточные черви
Ленточные черви (цестоды) – группа паразитических червей, имеющих лентовидную форму и состоящих из различного количества анатомически изолированных члеников – проглоттид. Размеры червей варьируют от нескольких миллиметров до 10-15 метров и более. На переднем конце червя располагается головка, которая является органом фиксации паразита к слизистой кишечника человека. Фиксируется гельминт к стенке кишечника с помощью разных приспособлений – округлых или щелевидных присосок, крючьев.
Возбудителем дифиллоботриоза является лентец широкий, который обитает в кишечнике человека.
Очаги заболевания географически связаны с пресноводными водоемами и сосредоточены в бассейнах восточных и северных рек – Обь, Иртыш, Лена, Енисей, Амур, Свирь, Печора, Нева, Волжско - Камский бассейн.
Лентец широкий – достигают в длину 12-15 метров и более, а число члеников – нескольких тысяч.
Заражение человека происходит при употреблении недостаточно термически обработанной, свежемороженой, слабопросоленной, плохо провяленной и прокопченной рыбы, сырого рыбного фарша, а также при употреблении свежепосоленной икры рыб. Клиническая картина обусловлена механическим воздействием гельминта на слизистую кишечника и поглощением им питательных веществ. Больные дифиллоботриозом жалуются на боли и урчание в животе, тошноту, рвоту. Часто имеет место расстройство стула. При одновременном паразитировании нескольких червей может возникнуть кишечная непроходимость.
Лентец адсорбирует на своей поверхности витамин В12, а это приводит к нарушению образования эритроцитов в организме больных и возникновению анемии. У больных отмечается бледность кожных покровов, слабость, недомогание.
Возбудителем тениаринхоза является бычий цепень, который локализуется тонком кишечнике человека и может достигать в длину 10 метров.
Заболевание регистрируется во многих областях России, особенно часто встречается в Дагестане.
Люди заражаются тениаринхозом при употреблении в пищу зараженного мяса крупного рогатого скота (слабо прожаренного или проваренного, строганины, фарша).
Тениаринхоз часто протекает бессимптомно и обнаруживается случайно, когда больной видит в своих фекалиях членики паразита, либо обнаруживает их в постели или на одежде. При расспросе больной может жаловаться на то, что в последнее время ощущает слабость, повышенную утомляемость, нарушение сна, кожный зуд урчания в животе, боли в правой подвздошной области, позывы к рвоте, нарушение стула.
Как осложнение тениаринхоза у больных может возникнуть приступ острого аппендицита или кишечная непроходимость.
Возбудителем тениоза является свиной цепень, который локализуется в тонком кишечнике человека и может достигать в длину 3 метров.
На территории РФ случаи тениоза регистрируются в тех местностях, где развито свиноводство. Это южные регионы страны, граничащие с Украиной и Белоруссией.
Свиной цепень может локализоваться в различных органах и тканях.
Относительно благоприятно протекает цистицеркоз с локализацией в подкожной клетчатке или скелетных мышцах.
При цистицеркозе глаз пациенты жалуются на искажение формы предметов, слезотечение, постепенное понижение остроты зрения.
Цистицеркоз головного мозга протекает тяжело и часто заканчивается смертельным исходом для заболевшего человека.
Возбудителем эхинококкоза – является эхинококк, который локализацией в печени и легких и может достигать в длину 5-6 метров.
На территории России наиболее часто эхинококкоз регистрируется в Якутии, Бурятии, Новосибирской, Томской и Омской областях, в Закавказье.
Для человека заражение эхинококком возможно при употребление немытых огородных культур, овощей или фруктов, на которых могли оказаться яйца паразита.
Клинические проявления заболевания зависят от размеров, количества и локализации пузырей эхинококка в организме больного. При локализации эхинококка в печени больные жалуются на тяжесть и боль в правом подреберье, а также желтушности кожных покровов в результате нарушения оттока желчи. Большие кисты, сдавливающие воротную вену, приводят к нарушению оттока венозной крови от кишечника и появлению асцита - накоплению жидкости в брюшной полости.
При локализации в легких больных беспокоят сухой кашель и боли при дыхании.
Возбудителем альвеококкоза является альвеококк, который поражает печень с возможными последующими метастазами в различные другие органы. Размер альвеококка не превышает 5 мм.
Очаги заболевания на территории России встречаются на Дальнем Востоке, в Челябинской, Пермской, Самарской и Ростовской областях. Заболевание характеризуется длительным и тяжелым течением и высоким процентом смертности.
Человек заражается при употреблении в пищу немытых дикорастущих трав и лесных ягод, а также при употреблении продуктов, мытье которых осуществляюсь в открытом водоеме.
На ранней стадии заболевания больных беспокоит слабость, недомогание, головная боль, кожный зуд. В дальнейшем могут появиться жалобы на чувство тяжести в правом подреберье; рвота, понос, вздутие живота, особенно после употребления жирной пищи.
Состояние больного значительно ухудшается при попадании альвеококка в другие органы. Наиболее опасны метастазы в головной мозг, почки, легкие. На фоне угнетения иммунной системы больного, очень часто происходит нагноение пузырей, возникают абсцессы во внутренних органах, что еще в большей степени отягощает состояние больного и могут быть причиной летального исхода.
Круглые черви (нематоды)
Круглые черви — один из самых многочисленных типов червей. Заболевания, вызываемые круглыми червями, называются нематодозами.
Тело нематод имеет веретеновидную или нитевидную форму, на концах сужается, в поперечном сечении округлое, размеры круглы червей могут быть различные, но чаще не превышает 0,5 метра.
Возбудителем аскаридоза является аскарида, паразитирующая в тонком кишечнике человека. Размер зрелых червей может достигать 40 см.
Основной и единственно возможный механизм заражения человека аскаридозом – фекально-оральный. Немытые овощи или фрукты, вода, предметы обихода, грязные руки – основные факторы передачи. А если вспомнить механических переносчиков яиц – насекомых, то перечень продуктов, на которых могут оказаться яйца аскарид, будет чрезвычайно большим.
Клинические проявления аскаридоза зависят от количества паразитов в тонком кишечнике. Чаще всего в кишечнике человека обитает одна особь – тогда заболевание протекает чаще всего бессимптомно.
При наличии нескольких особей в организме у больных возникают признаки интоксикации организма продуктами жизнедеятельности червей. Больные жалуются на головокружение, головную боль, нарушение сна. Появляется чувство тяжести в животе, неустойчивый стул. При паразитировании большого количества аскарид могут появиться симптомы непроходимости кишечника.
Возбудителем энтеробиоза является острицы, которые локализуются в кишечнике, и могут достигать размера до 1 см.
Единственный путь заражение острицами – фекально-оральный. Немытые овощи и фрукты, бытовые предметы, грязные руки – основные факторы передачи. Насекомые тоже могут быть разносчиками яиц остриц на продукты питания.
При паразитировании небольшого количества паразитов возможно бессимптомное течение заболевания, в то время как при наличии большого числа паразитов, наблюдается зуд в области ануса, у больных возможны боли в животе, тошнота, расстройство стула.
При миграции самки остриц могут проникнуть в половые органы с последующим возникновение воспалительного процесса в них.
Возбудителем трихинеллеза является трихинелла, которая локализуется в тонком кишечнике и скелетной мускулатуре хозяина.
Трихинелла – одна из самых маленьких нематод. Размеры паразитов едва достигают 4 мм. Взрослые трихинеллы паразитируют в тонком кишечнике, а в личиночной стадии в поперечно-полосатой мускулатуре, исключение составляет сердечная мышца.
Человек заражается, употребляя зараженных животных - кабанов, свиней, медведей, тюленей. Для заражения достаточно употребить 30-50 г трихинеллезного мяса. Чаще всего человек заражается при употреблении мяса, сала, окорока, бекона, грудинки, а также колбас, изготовленных из туш зараженных животных.
Несколько позже появляется выраженный отек век или всего лица, иногда возникают отеки конечностей. К этим симптомам добавляются боли в мышцах – икроножных, жевательных, поясничных. Постепенно боли в мышцах усиливаются, распространяются на новые группы мышц. Движения больного становятся все более ограниченными, иногда до полного обездвиживания.
Интоксикация организма больного продуктами жизнедеятельности паразита приводит к поражению сердца, легких, головного мозга и могут быть причиной смерти больного.
Профилактика гельминтозов
Чтобы не допустить заражения гельминтами, нужно соблюдать несколько правил, а именно:
Читайте также:

