Паразиты в мышцах диких животных
Обновлено: 24.04.2024
Кожная мигрирующая личинка. Диагностика и лечение
б) Распространенность (эпидемиология):
• Распространенное заболевание у путешественников, вернувшихся из тропических стран.
• Точная заболеваемость в США неизвестна, поскольку учета данного заболевания не ведется. В обзоре Центра контроля заболеваемости приводятся сведения о том, что 35-52% собак в приютах для животных заражены глистами, способными вызвать заболевание у человека. Кожная мигрирующая личинка - вторая по распространенности глистная инфекция.
• В нашей стране инфекция встречается преимущественно во Флориде и на побережье Мексиканского залива.
• Дети болеют чаще, чем взрослые.
в) Этиология (причины), патогенез (патология):
• Вызывается присутствующими у собак и кошек кровососущими нематодами (кривоголовками), например, Ancylostorna braziliense, Ancylostoma caniurri.
• Яйца глистов передаются с экскрементами собак и кошек.
• Личинки выводятся во влажном теплом песке/почве.
• В стадии инфицирования личинки проникают в кожу.
Кожная мигрирующая личинка Серпигинозный ход кожной мигрирующей личинки на голени. Сама личинка находится в 2-3 см от видимого хода
г) Клиника. Диагноз кожных мигрирующих личинок устанавливается на основании анамнеза и клинической картины.
• Приподнятые над поверхностью серпигинозные или линейные красновато-коричневые ходы длиной 1-5 см.
• Симптомы продолжаются в течение нескольких недель или месяцев.
д) Типичная локализация на теле. Нижние конечности, в частности стопы (73%), ягодицы (13-18%) и живот (16%)
е) Анализы при заболевании. Не показаны. В редких случаях при анализе крови выявляется эозинофилия или повышение уровня иммуноглобулина Е.
ж) Дифференциальная диагностика кожных мигрирующих личинок. В случаях инфицирования кожной мигрирующей личинкой нередко ошибочно предполагают следующие заболевания:
• Кожные грибковые инфекции. Очаги представляют собой характерно шелушащиеся бляшки и кольцевидные пятна с разрешением в центре. Если серпигинозный ход кожной мигрирующей личинки имеет кольцевидную форму, часто неверно предполагается дерматофития.
• Контактный дерматит. Отличие заключается в расположении очагов, наличии везикул и отсутствии классических серпигинозных ходов.
• Мигрирующая эритема при болезни Лайма. Очаги обычно представляют собой кольцевидные пятна или бляшки, но не имеют серпигинозной формы и не приподняты над поверхностью кожи.
• Фитофотодерматит. В острой фазе фитофотодерматит проявляется отеком и везикулами, позднее возникают очаги поствоспалительной гиперпигментации. Такие очаги могут возникать после посещения пляжа, однако их причиной является не инфицированный личинками песок, а приготовление напитков с соком лайма.
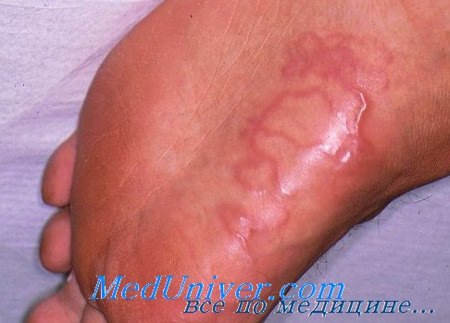
Кожная мигрирующая личинка
з) Лечение заражений кожными мигрирующими личинками:
• Тиабендазол перорально - единственный препарат, утвержденный Федеральным агентством по контролю лекарств, для лечения больных с кожной мигрирующей личинкой.
Из таблеток по 500 мг можно приготовить местный крем (15%) на водорастворимой основе. Испытаний эффективности системной и местной лекарственных форм было немного, и проводились они в еще 1960 гг.
Крем является хорошим выбором для детей, которые не могут проглотить таблетку.
- Рекомендуемая доза для перорального приема -25 мг/кг каждые 12 часов в течение 2-5 дней (доза не должна превышать 3 г в день). Крем наносится местно 2-3 раза в день в течение пяти дней на личиночные ходы с захватом 2-3 см кожи над очагами.
- Эффективность составляет 75-89% при системной терапии и 96-98% при местном лечении.
- Системная терапия переносится несколько хуже; побочные реакции включают тошноту (49%), рвоту (16%) и головную боль (7%). Побочных эффектов для местных препаратов не отмечено.
• Ивермектин (стромектол) (не утвержден Федеральным агентством по контролю лекарств для этого применения).
- Рекомендуется однократная доза, составляющая 0,2 мг/кг (12-24 мг).
- Эффективность при однократной дозе составляет 100%.
- В серии из шести испытаний побочных эффектов не отмечено.
- Многие специалисты считают это средство препаратом выбора.
• Албендазол успешно назначается более 25 лет, но также не утвержден Федеральным агентством по контролю лекарств для этого применения.
- Рекомендуемая доза составляет 400-800 мг в день в течение 3-5 дней.
- Эффективность превышает 92%.
- Ежедневно в течение трех дней и более применяется доза 800 мг, побочные эффекты со стороны желудочно-кишечного тракта могут отмечаться у 27% пациентов.
• Криотерапия неэффективна и даже вредна, ее необходимо избегать.
• Антигистаминные препараты могут облегчить зуд.
• При присоединении вторичной инфекции необходимо назначить антибиотики.
и) Консультирование врачом пациента:
• На пляжах, куда допущены животные, рекомендуется носить обувь.
• Детские песочницы необходимо закрывать от животных.
• Для владельцев домашних животных: не допускайте животных на пляжи, при необходимости лечите их от глистов и надлежащим образом убирайте экскременты.
к) Наблюдение пациента врачом. Наблюдение необходимо при персистируютцих очагах.
л) Список использованной литературы:
1. Usatine RP. A rash on the feet and buttocks. West J Med. 1999;170 (6):334-335.
2. Caumes E.Treatment of cutaneous larva migrans. Clin Infect Dis. 2000;30:811-814.
3. Center for Disease Control, cdc.gov/ncidod/dpd/ parasites/ascaris/prevention.pdf Accessed June 5, 2020.
4. Hotez P, Brooker S, Bethony J, et al. Hookworm Infection. N Engl J Med. 2004;351 (8):799-807.
5. Le E, Hsu S. A serpiginous eruption on the buttocks. Am Earn Physician. 2000;62(11):2493—2494.
6. Jelinek T, Maiwald H, Nothdurft H, LoscherT. Cutaneous larva migrans in travelers: Synopsis of histories, symptoms and treating 98 patients. Clin Infect Dis. 1994:19:1062-1066.
7. Caumes E, Carriere J, Datry A, et al. A randomized trial of ivermectin versusalbendazoleforthetreatmentof cutaneous larva migrans. / Trap Med Hyg. 1993;49(5):641-644.
Что такое тениоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Тениоз (Taeniosis) — паразитарное заболевание человека, вызываемое половозрелой стадией ленточного гельминта (свиного цепня), который проникает в организм человека при употреблении плохо приготовленного мяса, паразитирует в тонком кишечнике и вызывает расстройства пищеварения. В некоторых случаях может осложняться цистицеркозом — паразитированием в тканях организма личинок свиного цепня, что приводит к серьёзным последствиям и даже смерти.
Возбудитель
- домен — эукариоты;
- царство — животные;
- тип — плоские черви;
- класс — ленточные черви;
- отряд — циклофиллиды;
- семейство — тенииды;
- род — Taenia;
- вид — свиной цепень (Taenia solium).
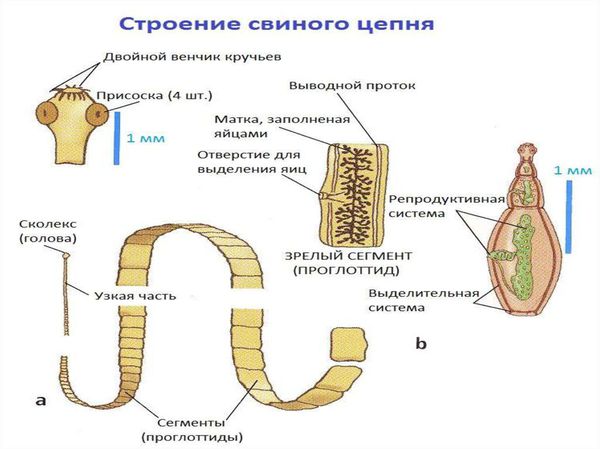
Свиной цепень (устаревшее название "cолитёр") — это плоский (ленточный) паразитический червь, длина которого в кишечнике человека достигает 3 метров, а по данным Ц ентра по контролю и профилактике заболеваний США (CDC) его длина может достигать 7 метров. Как правило, паразитирует только 1 червь. Паразит имеет головку, шейку и тело. Тело червя (стробила) состоит из члеников (п роглоттидов), их число может достигать 1000 . Головка (сколекс) размерами до 2 мм в диаметре имеет хоботок и 4 мышечные присоски (органы прикрепления), расположенные крестообразно. На хоботке есть крючья в количестве от 22 до 32, из-за этого есть второе название паразита — вооружённый цепень.
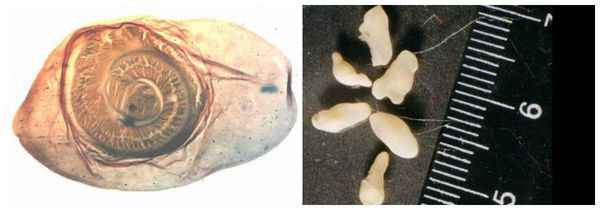
Яйца паразита попадают с калом человека в окружающую среду. Животные (свиньи, собаки, кошки и даже человек при несоблюдении гигиены) поедают яйца, зародыши проходят через кишечную стенку и разносятся кровью по всему организму, после чего оседают в тканях (в основном в соединительной ткани между мышцами). Через пару месяцев яйца превращаются в финны (цистицерки), которые живут до 5 лет, после чего они погибают и обызвествляются (накапливают минеральные вещества, соли кальция). Цистицерки имеют вид полупрозрачных беловатых пузырьков диаметром до 1,5 см, внутри видна мелкая сформированная головка.
Для полноценного развития свиного цепня необходима смена хозяев за его жизнь. Человек является окончательным хозяином. В его кишечнике паразитирует взрослый гельминт, который развивается за 2 месяца из финны (личинки червя в тканях), съеденной с мясом. Паразит прикрепляется к стенке тонкого кишечника и растёт, поглощая пищу и постепенно наращивая членики (от шейки), которые по мере созревания отрываются и выходят в окружающую среду при дефекации. Паразит может жить в кишечнике десятки лет.
Человек может стать и промежуточным хозяином (при поедании яиц). В этом случае для паразита наступит "экологический тупик" — он не сможет развиться до половозрелой стадии и продолжить свой род, потому что мясо человека с финнами никто не ест.
Яйца выживают в окружающей среде в течение нескольких месяцев в зависимости от условий. Высыхание могут выдерживать в течение 10 месяцев, способны зимовать под снегом, в воде живут до 4 месяцев. При кипячении погибают практически мгновенно, при 65 °С сохраняют жизнеспособность в течение 3 минут, при 20-25 °С под воздействием прямых солнечных лучей сохраняются до 2 дней, если они закрыты травой — до полутора месяцев. Раствор хлорной извести 10-20 % убивает яйца за 5-6 часов. Цистицерки в мясе погибают при его замораживании при температуре -12 °С и поддержании в толще мяса температуры не ниже -10 °С в течение 10 дней [1] [2] [9] [10] .
Эпидемиология
Тениоз является одним из древнейших известных заболеваний. Первые упоминания встречаются ещё в 16 веке до нашей эры (Древний Египет), имеются записи Аристотеля и Гиппократа (финноз свиней). В настоящее время ВОЗ относит тениоз и цистицеркоз к группе забытых ("пренебрегаемых") болезней, т. е. тех, о которых мало говорят и обращают внимание развитые страны.
Распространение повсеместное, но наиболее поражены отдельные регионы: Индия, Африка, Южная Америка, Азия, Северный Китай, Восточная Европа, Белоруссия, Украина. Это регионы, где уровень дохода низкий или ниже среднего, где люди едят много плохо приготовленной свинины и недостаточно соблюдается гигиена. Здесь цистицеркоз является причиной эпилепсии в 30 % случаев, а в некоторых областях, где свиньи и люди живут вместе — до 70 %, по данным ВОЗ [3] . В РФ в среднем выявляется до 500 случаев в год [11] . Есть тенденция к повышенной заболеваемости сельских жителей и работников свиноводческих хозяйств.
Механизм передачи фекально-оральный, путь заражения пищевой. Источник инфекции и окончательный хозяин — заражённый человек, выделяющий с фекалиями яйца гельминта. Промежуточные хозяева — иногда человек, но чаще животные, которые поедают корм, загрязнённый фекалиями человека: свиньи (отсюда происходит название вида), кабаны, обезьяны, собаки, кошки.
Факторы передачи:
- При тениозе — недостаточно термически обработанное мясо свиней или диких кабанов. Наиболее опасно мясо, не прошедшее ветеринарный контроль. В этом случае человек заражается, поедая финны, т. е. зародыши червя, с инфицированным мясом.

- При цистицеркозе — загрязнённые яйцами пища и объекты внешней среды при несоблюдении людьми правил гигиены. Фактором передачи также может быть аутоинвазия, когда у человека с паразитом в кишечнике из-за нарушения перистальтики ЖКТ яйца из кишечника попадают в желудок. Т. е. яйца свиного цепня заразны и опасны для человека сразу, как только покидают организм с каловыми массами. Поэтому риск заражения цистицеркозом есть для любого человека, особенно если пренебрегать правилами гигиены и правилами обработки пищевых продуктов (тщательное мытьё) [1][3][5][7][11] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тениоза
Множество случаев заражения и болезни проходит бессимптомно или малосимптомно. Жалобы таких больных обычно незначительны и связаны в основном с расстройствами пищеварения. Примерно через 1-1,5 месяца от момента заражения (а может и раньше) может наблюдаться лёгкое недомогание, головокружение, слабость, нарушения сна, умеренные головные боли, раздражительность, сниженный или повышенный аппетит, тошнота, дискомфорт и несильные боли в разных отделах живота. Развиваются запоры, чередующиеся с диареей, возможен анальный зуд, больной может умеренно худеть.
Характерной особенностью является периодическое (раз в несколько месяцев) выделение с калом оторвавшихся члеников паразита начиная с 2-3 месяцев паразитирования и так десятки лет. Их хорошо видно невооружённым глазом. Могут быть симптомы гипохромной анемии (недостатка железа): бледность кожи и слизистых, быстрая утомляемость при физической нагрузке, шум в ушах, обмороки, чувство мурашек по коже. Развивается гиповитаминоз В1 (тёмно-красный сухой язык со сглаженными сосочками). В результате отравления организма продуктами жизнедеятельности паразита, а также из-за расстройства пищеварения повышается склонность к необъяснимым высыпаниям токсико-аллергического характера на коже.

Тениоз у беременных
У беременных заболевание может протекать более тяжело, что обусловлено характерными физиологическими процессами в организме женщины этого периода. Наиболее часто наблюдаются расстройства пищеварения (запоры, диарея), тошнота, рвота, снижение гемоглобина, зуд кожи, перианальный зуд. Может быть плохой набор веса у плода. Вследствие более частого нарушения желудочно-кишечной перистальтики (моторики) повышается риск заброса яиц паразита в желудок и развития цистицеркоза [1] [4] [6] [10] .
Патогенез тениоза
Во время паразитирования свиной цепень повреждает слизистую при помощи крючьев и присосок, что вызывает расстройство пищеварения и нарушает моторику кишечника. Кроме того, гельминт потребляет много важных для человека питательных веществ, микроэлементов и отравляет организм продуктами своей жизнедеятельности, что приводит к токсико-аллергическому отравлению.
При заглатывании яиц паразита извне или при рефлюксной болезни, когда нарушается моторика кишечника и яйца из кишки попадают в желудок, развивается цистицеркоз. В различных органах и тканях развиваются соединительнотканные капсулы, содержащие зародыш — цистицерк. Вокруг наблюдаются воспалительные изменения в виде аллергической реакции и дистрофически-атрофические изменения из-за механического давления на окружающую ткань.
При локализации в головном мозге вокруг капсулы наблюдается воспаление мелких сосудов и инфильтрация окружающей ткани плазматическими клетками, что вызывает расстройство движения спинномозговой жидкости (ликвора), отёк мозговой ткани, развитие менингита и энцефалита. При паразитировании в оболочках мозга у его основания возможно развитие рацемозной (ветвистой) формы цистицеркоза до 25 см в длину.
С течением времени (до 5 лет) цистицерк претерпевает дегенеративные изменения — происходит его набухание и разложение (расплавление), что сопровождается усилением токсического и местного воспалительного воздействия. Исходом гибели личиночной формы паразита является кальцификация и местное рубцевание. Специфичных симптомов при этом процессе нет, после полной гибели цистицерков болезнь заканчивается, если, они не находятся в жизненно важных органах [1] [5] [6] [9] .
Классификация и стадии развития тениоза
По Международной классификации болезней 10-го пересмотра (МКБ 10):
- Тениоз:
- B68.0 Инвазия, вызванная Taenia solium.
- B68.9 Тениоз неуточнённый (при подозрении на болезнь, но отсутствии лабораторного подтверждения).
- Цистицеркоз:
- B69.0 Цистицеркоз центральной нервной системы (судороги, эпилепсия, необъяснимая рвота).
- B69.1 Цистицеркоз глаза (нарушения зрения, слепота).
- B69.8 Цистицеркоз других локализаций.
- B69.9 Цистицеркоз неуточнённый [1][2] .
Осложнения тениоза
Острый аппендицит. В правой половине живота снизу постепенно нарастают боли, появляется тошнота, характерен субфебрилитет (температура тела от 37,1 до 38,0 °С). В анализе крови наблюдается нейтрофильный лейкоцитоз со сдвигом влево — повышенный уровень нейтрофилов с преобладанием незрелых форм, которые не могут в полной мере осуществлять защитную функцию.
Панкреатит ( воспаление поджелудочной железы) . Характеризуется тошнотой, рвотой, опоясывающими болями в животе.
Кишечная непроходимость. Симптомы — с хваткообразные боли в животе без связи с приёмом пищи, запоры, метеоризм, вздутый живот, учащение пульса, рвота, бледность кожи.
Холангит ( воспаление жёлчных протоков) . Субфебрильная или фебрильная лихорадка, выраженные боли в правом подреберье, озноб, повышенная потливость, тошнота и рвота, желтуха и кожный зуд.
Гипохромная анемия. Бледность кожи и слизистых оболочек, повышенная утомляемость, чувство мурашек и покалывания, головокружения, шум в ушах, обмороки.
Цистицеркоз. Может быть осложнением тениоза, а может быть отдельным заболеванием. В основном симптоматика проявляется при поражении центральной нервной системы (ЦНС) — головного и спинного мозга и глаз. В зависимости от локализации возникают головные боли различной интенсивности, рвота, эпилептические припадки, нарушения речи, расстройства личности, бред и галлюцинации, деменция. При поражении глаз могут наблюдаться воспалительно-дистрофические процессы в различных отделах глаз — рецидивирующие конъюнктивиты, увеиты, отслоение сетчатки, атрофия глазного яблока, что может привести к слепоте. При поражении сердца могут возникать нарушения ритма. При поражении мышц и подкожной клетчатки иногда может наблюдаться некоторая болезненность при ощупывании и приподнятость этого участка в виде подкожного плотного опухолевидного бугорка [1] [5] [5] [8] .
Диагностика тениоза
Тениоз или цистицеркоз может быть заподозрен на основании следующих признаков:
- эпиданамнез — проживание на территории развитого свиноводства, употребление плохо приготовленной свинины, низкий социально-экономический уровень страны или региона;
- расстройства пищеварения;
- астено-невротические проявления — слабость, повышенная утомляемость, эмоциональная нестабильность, раздражительность, повышенная потливость;
- выход с калом неподвижных члеников паразита;
- развитие неврологической симптоматики (эпилепсия), патологии органов зрения.
Дифференциальная диагностика
Основывается на данных анамнеза, типичном виде члеников паразита и их микроскопическом исследовании.
Лабораторная диагностика
Клинический анализ крови — изменений может не быть, иногда наблюдаются гипохромная анемия, умеренное повышение эозинофилов, повышение скорости оседания эритроцитов (СОЭ), редко выявляется небольшое повышение лейкоцитов за счёт сегментоядерных клеток (наиболее большой группы иммунных клеток).
Общий анализ мочи — как правило, без отклонений.
Биохимический анализ крови — возможны отклонения при развитии осложнений:
- При холангитах — повышение маркеров нарушения выработки или оттока желчи: АСТ, ГГТ, ЩФ, общего билирубина.
- При панкреатитах — повышение амилазы.
- При поражении сердца — повышение ЛГД и КФК-МВ.
Серологические специфические исследования:
- Иммуноферментный анализ (ИФА) антител IgG — в основном применяются с целью диагностики внекишечного поражения — цистицеркоза, результаты могут быть ложноположительными;
- Иммунный блоттинг — более точный метод лабораторного исследования сыворотки крови на присутствие антител , который применяют для подтверждения результатов ИФА. Этот метод позволяет снизить число ложных результатов, но в РФ он недоступен.
ПЦР кала — выявление антигенов свиного цепня. Это достаточно чувствительный метод, однако может дать ложноотрицательный результат ввиду ограниченного количества материала в кале.
Копроовоскопия — микроскопическое изучение кала с целью обнаружения яиц и зрелых члеников паразита. По яйцам невозможно установить точный диагноз, т. к. они очень похожи на яйца других представителей этого рода, проводится не менее трёх раз в разные дни. Для определения вида паразита необходимо исследование члеников.
Инструментальная диагностика
Компьютерная (КТ) и магнитно-резонансная томография (МРТ), ультразвуковое исследование (УЗИ), прямая офтальмоскопия — применяются для выявления цистицеркоза. КТ лучше выявляет кальцификаты цистицерков (особенно небольшие). МРТ больше подходит для обнаружения цистицерков в некоторых трудновизуализируемых местах мозга, также МРТ указывает на местные окружающие изменения (отёк) и возможную гибель паразита.
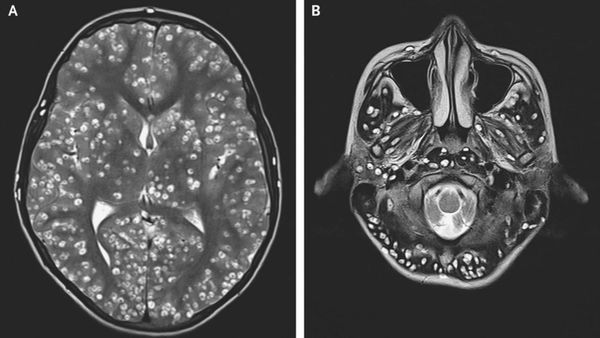
Исследования спинномозговой жидкости при поражении цистицерками ЦНС (лимфоцитарный плеоцитоз, увеличение уровня эозинофилов, белка).
Биопсия — морфологическое исследование биоптатов при оперативном вмешательстве [1] [3] [6] [10] .
Лечение тениоза
Госпитализации подлежат больные с тяжёлыми сопутствующими заболеваниями, а также больные с цистицеркозом ЦНС и глаз. Остальные больные могут лечиться амбулаторно.
В качестве этиотропной терапии (направленной на уничтожение возбудителя) применяется Празиквантел и Никлозамид. Есть данные об эффективности Альбеназола, но они ограничены. Продолжительность лечения — 3 дня.
При лечении цистицеркоза выбор способа уничтожения паразита зависит от его локализации и количества. При локализации под кожей и в тканях (кроме ЦНС и глаз) лечение, как правило, не проводят, так как риск последствий от приёма препарата выше пользы от лечения. Однако, если наличие паразита ведёт к каким-то физическим и эстетическим недостаткам, лечение назначается.
При локализации цистицерков в ЦНС и глазах лечение проводят только в условиях неврологического стационара, применяются Празиквантел и Альбендазол в сочетании с глюкокортикостероидами (т. к. есть риск местного воспаления и повреждения нервной системы и глаз).
В качестве мер патогенетической и симптоматической терапии при тениозе могут назначаться средства нормализации моторики кишечника (прокинетики) и микрофлоры кишечника (пре- и пробиотики).
При цистицеркозе головного мозга применяют противосудорожные препараты.
Возможно хирургическое лечение (удаление цистицерков при поражении головного и спинного мозга).
Контроль излеченности тениоза:
- визуальный — осмотры кала (о выздоровлении говорит отсутствие периодического отделения члеников червя);
- 4 отрицательных анализа кала на яйца гельминтов с интервалом в 1 месяц [2][4][5][8] .
Прогноз. Профилактика
При изолированном тениозе прогноз благоприятный. При развитии осложнений, особенно цистицеркозе ЦНС и глаз, прогноз серьёзный: возможно развитие тяжёлых стойких поражений (эпилепсия, слепота) и летальный исход.
Паразитарные воспалительные миопатии. Миопатия при цистицеркозе.
Течение заболевания, прогноз и лечение паразитарных миопатий
1. Токсоплазмоз — это протозойная инфекция, вызванная Toxoplasma gondii. Заражение происходит при употреблении в цищу зараженного паразитами мяса или при контакте с фекалиями больных кошек. Также возможен трансплацентарный или трансфузионный путь передачи возбудителя. Наиболее часто токсоплазмоз встречается у больных СПИДом. Миопатия — это только один из симптомов системной инфекции. Течение заболевания подострое, прогрессирующее и клинически неотличимое от других видов воспалительных миопатии. Иногда наблюдаются лихорадка, миалгии, лимфаденопатия и боли в шее.
Уровень креатинкиназы в крови может быть повышен. На ЭМГ обнаруживаются изменения, характерные для полиомиозита. Диагноз токсоплазмоза подтверждается методами серологической диагностики. Тахизоиды в мышечной ткани могут быть выявлены при биопсии.

Точная диагностика токсоплазменного миозита важна, т. к. лечение значительно отличается от лечения других видов миозита. Препаратами выбора являются пириметамин и сульфадиазин или трисульфапиридины. Пириметамин — антагонист фолиевой кислоты, поэтому ее назначают дополнительно для уменьшения риска подавления функции костного мозга.
2. Цистицеркоз. Заражение цистицеркозом происходит при употреблении в пищу свинины, подвергшейся недостаточной термической обработке, или при использовании загрязненной фекалиями воды и пищи. Заболевание вызывается личиночной формой ленточного червя Taenia solium. Заболевание может развиться спустя много лет после первичного инфицирования. Возбудитель внедряется в мягкие ткани, чаще всего в скелетные мышцы, ЦНС и глаза. Пораженная мышца увеличена в размерах, в ней прощупываются болезненные узелки.
Часто отмечается эозинофилия. Для подтверждения диагноза проводится исследование кала на яйца и взрослые формы паразита, серологическое исследование цереброспинальной жидкости (ЦСЖ) и сыворотки крови для выявления специфического антигена. Однако для подтверждения инфекционной этиологии миопатии необходима биопсия мышцы с макро- и микроскопическим выявлением инкапсулированной личиночной формы, а также специфического антигена. Псевдогипертрофия мышц обусловлена множественными паразитарными включениями. Часто наблюдается кальцификация цист в мышцах.
Для борьбы со взрослыми формами паразита применяется никлозамид и антибиотик парамомицин. Празиквантел (билтрицид), используемый для лечения цистицеркоза ЦНС, неэффективен. Преднизолон назначается наряду с основными препаратами для подавления воспалительной реакции. Иногда цисты удаляют хирургическим путем. 3. Трихинеллез вызван нематодой Trichinella spiralis. Личиночные формы паразита инфильтрируют многие ткани, но наиболее часто — мышечную. Инкубационный период составляет 2—12 дней после употребления в пищу свинины, не прошедшей адекватную термическую обработку и зараженной инкапсулированными личинками.
Продромальный период часто характеризуется болью в животе, диареей, за чем следуют лихорадка, миалгии и слабость проксимальных мышечных групп. Слабость может распространяться на экстраокулярные мышцы, межреберные мышцы и диафрагму. Может также наблюдаться периорбитальный отек и птоз. Миалгии достигают пика своей выраженности на третьей неделе болезни. Иногда отмечается поражение сердечной мышцы. На ЭМГ обнаруживаются признаки, характерные для острой миопатии. У 60% больных в крови отмечается выраженная эозинофилия. Антитела к Trichinella spiralis определяются примерно через 3 недели после инфицирования. Диагноз подтверждается обнаружением личинки при биопсии мышц.
Препаратом выбора для лечения взрослой и личиночных форм паразита является альбендазол. Его назначают по 400 мг 3 раза в сутки в течение двух недель. Препарат противопоказан детям и беременным женщинам. Больным с выраженной слабостью рекомендован преднизолон в дозе 1,0—1,5 мг/кг/сут. Прогноз плохой у больных с выраженным миозитом сердечной мышцы, с энцефалитом и иммунодефицитом.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Tрихинеллёз (лат. trichinellosis) — гельминтоз, вызываемый паразитирующими в организме человека нематодами рода Trichinella. Характеризуется острым течением, лихорадкой, болями в мышцах, отёками, высокой эозинофилией и различными аллергическими проявлениями.
Классификация
Этиология и патогенез
ЭТИОЛОГИЯ
Возбудители трихинеллёза — круглые черви семейства Trichinellidae, включающего два вида — Trichinellа spiralis c тремя вариететами (T. s. spiralis, T. s. nativa, T. s. nelsoni) и Trichinella pseudospiralis. В патологии населения России наибольшее значение имеют T. s. spiralis и T. s. nativa. Trichinella s. spiralis распространена повсеместно, паразитирует у домашних свиней, патогенна для человека. Trichinellа s. nativa встречается в северном полушарии, паразитирует у диких млекопитающих, чрезвычайно устойчива к холоду, патогенна для человека. Trichinella s. nelsoni обитает в Экваториальной Африке, паразитирует у диких млекопитающих, малопатогенна для человека. Trichinella pseudospiralis распространена повсеместно, паразитирует у птиц и диких млекопитающих. Патогенность для человека не доказана. Трихинеллы — мелкие нематоды с цилиндрическим бесцветным телом, покрытым прозрачной кутикулой кольчатой структуры. Длина неоплодотворённой самки 1,5–1,8 мм, оплодотворённой — до 4,4 мм, половозрелого самца — около 1,2–2 мм, диаметр гельминтов менее 0,5 мм. В отличие от других нематод трихинеллы — живородящие гельминты. Их личинки, юные трихинеллы, имеют палочковидную форму, длину до 0,1 мм; через 18–20 дней развития личинка удлиняется до 0,7–1,0 мм. Один и тот же организм теплокровного животного для трихинелл служит сначала дефинитивным (кишечные трихинеллы), а затем промежуточным (инкапсулированные в мышцах личинки) хозяином. В организм нового хозяина паразит попадает с мясом животных, в котором содержатся живые инкапсулированные личинки. Под действием желудочного сока капсула растворяется, личинки в тонкой кишке через час активно внедряются в слизистую оболочку. На 4–7-е сутки самки начинают производить живых личинок. Каждая самка в течение репродуктивного периода, длящегося 10–30 дней, рождает от 200 до 2000 личинок. Из кишечника личинки током крови разносятся по всему организму. Дальнейшее развитие паразита возможно только в поперечнополосатых мышцах. На третьей неделе после заражения личинки становятся инвазионными и принимают типичную спиралевидную форму. К началу второго месяца после заражения вокруг них в мышцах формируется фиброзная капсула, которая через 6 мес начинает обызвествляться. В капсулах личинки сохраняют жизнеспособность 5–10 лет и более. В мышцах человека капсулы личинок трихинелл размером 0,3–0,6 мм всегда имеют лимоновидную форму. Личинки трихинелл, находящиеся в мышцах животных, устойчивы к высоким и низким температурам. Нагревание мяса, содержащего инкапсулированные личинки трихинелл, в микроволновой печи до 81 °С не обеспечивает их инактивации. При варке куска мяса толщиной около 10 см личинки погибают только через 2–2,5 ч. Личинки устойчивы к таким видам кулинарной обработки, как соление, копчение, замораживание. Наибольшую опасность представляют термически не обработанные мясные продукты: строганина, сало (шпик) и т.д.
ПАТОГЕНЕЗ
В основе патогенеза трихинеллёза лежит сенсибилизация организма к антигенам гельминта, проявляющаяся в разной степени в кишечной, миграционной и мышечной стадиях инвазии. К концу первой недели после заражения преимущественно в тонкой кишке обнаруживают самок трихинелл, погружённых в слизистую оболочку, вокруг которых развивается местная катаральногеморрагическая воспалительная реакция. При тяжёлой инвазии наблюдаются язвенно-некротические повреждения слизистой оболочки кишечника. Взpослые особи гельминта выделяют иммуносупpессивные вещества, подавляющие буpную воспалительную pеакцию, что способствует мигpации личинок. В тощей кишке активизиpуется система кининов, других гоpмонов, вызывающих функциональные pасстpойства, болевой синдpом. Метаболиты мигрирующих личинок, продукты, освобождающиеся после их гибели, — это антигены, обладающие сенсибилизирующим, ферментативным и токсическим свойствами. Вследствие этого развиваются выраженные аллергические реакции с поражением кровеносных сосудов, коагуляционными нарушениями, тканевым отёком, повышением секреторной активности слизистых оболочек. На второй неделе личинок обнаруживают не только в скелетных мышцах, но и в миокарде, лёгких, почках, головном мозге. В паренхиматозных органах личинки погибают. Развивающиеся иммунопатологические реакции ведут к тяжёлым поражениям: миокардиту, менингоэнцефалиту, пневмонии. Воспалительные процессы со временем стихают, но через 5–6 нед могут сменяться дистрофическими, последствия которых исчезают только через 6–12 мес. Из скелетных мышц чаще всего поражаются группы с обильным кровоснабжением (межрёберные, жевательные, глазодвигательные мышцы, диафрагма, мышцы шеи, языка, верхних и нижних конечностей). У больных с тяжёлой формой болезни находят 50–100 и более личинок трихинелл в 1 г мышечной массы. К концу третьей недели личинки приобретают спиралевидную форму, вокруг них наблюдается интенсивная клеточная инфильтрация, на месте которой затем формируется фиброзная капсула. Процесс образования капсулы нарушается при чрезмерной антигенной нагрузке (при массивной инвазии), а также под воздействием веществ с иммунодепрессивными свойствами (глюкокортикоиды и др.). В паренхиматозных органах встречаются узелковые инфильтраты. В миокарде личинки трихинелл обусловливают появление множественных воспалительных очагов в интерстициальной ткани, но настоящие капсулы в сердечной мышце не формируются. При интенсивной инвазии в миокарде развиваются очагово-диффузная воспалительная реакция и дистрофические изменения; возможны образование гранулём и развитие васкулитов с поражением артериол и капилляров мозга и мозговых оболочек. Для трихинеллёза характерен стойкий нестерильный иммунитет, который обусловлен наличием инкапсулированных личинок возбудителя в мышцах заражённых людей. Высокое содержание специфических антител в сыворотке крови отмечается с конца второй недели и достигает максимума на 4–7-й неделе. Комплекс реакций в энтеpальной стадии предупреждает проникновение в кровоток значительной части личинок, что ограничивает их распространение в организме.
Эпидемиология
Клиническая картина
Cимптомы, течение
Инкубационный период при трихинеллёзе в среднем длится 10–25 дней, но может составлять от 5–8 дней до 6 нед. При заражении в синантропных очагах (после употребления инфицированного мяса домашних свиней) наблюдается обратная зависимость между продолжительностью инкубационного периода и тяжестью течения болезни: чем короче инкубационный период, тем тяжелее клиническое течение, и наоборот. При заражении в природных очагах такой закономерности обычно не отмечают. В зависимости от характера клинического течения различают следующие формы трихинеллёза: бессимптомную, абортивную, лёгкую, средней степени тяжести и тяжёлую. Первые симптомы в виде тошноты, рвоты, жидкого стула, болей в животе у некоторых больных появляются в ближайшие дни после употребления заражённого мяса и могут длиться от нескольких дней до 6 нед. При бессимптомной форме единственным проявлением может быть эозинофилия крови. Для абортивной формы характерны кратковременные (длительностью 1–2 дня) клинические проявления. Основные симптомы трихинеллёза — лихорадка, боли в мышцах, миастения, отёки, гиперэозинофилия крови. Лихорадка ремиттирующего, постоянного или неправильного типа. В зависимости от степени инвазии повышенная температура тела у больных сохраняется от нескольких дней до 2 нед и дольше. У некоторых больных субфебрильная температура сохраняется несколько месяцев. Отёчный синдром появляется и нарастает довольно быстро — в течение 1–5 дней. При лёгкой и среднетяжёлой формах болезни отёки сохраняются
Диагностика
Во время вспышек и групповых заболеваний при наличии типичных симптомов у больных постановка диагноза трихинеллёза не вызывает трудностей. Необходимо установить общий источник заражения и, по возможности, провести исследование остатков пищи (мяса или мясных продуктов) на наличие личинок трихинелл. Трудности возникают при диагностике спорадических случаев. В подобных ситуациях большое значение имеет эпидемиологический анамнез. Паразитологические методы лабораторной диагностики регламентирует МУК 4.2735-99. При отсутствии данных об источнике заражения иногда прибегают к биопсии мышц (дельтовидной или икроножной у лежачих больных или длинной мышцы спины у ходячих больных): кусочек мышечной ткани массой 1 г исследуют под микроскопом при малом увеличении на наличие личинок трихинелл. Серологические методы диагностики можно использовать только на 3-й неделе болезни, так как в первые 2 нед преобладают реакции местного иммунитета (кишечная фаза инвазии), и концентрация специфических антител в крови низкая. Используют ИФА с антигеном T. spiralis и РНГА. Сроки появления диагностических титров антител зависят от интенсивности инвазии и вида возбудителя: у больных трихинеллёзом, которые заразились при употреблении мяса свиньи, сильно инвазированного трихинеллами, антитела выявляются на 15–20-е сутки после заражения; если интенсивность инвазии меньше, сроки выявления антител удлиняются. При заражении мясом диких животных (T. s. nativa) начальные сроки выявления антител могут составлять до 1,5 мес. Титры специфических антител могут нарастать в течение 2–4 мес после заражения, заметно снижаясь через 4–5 мес, однако могут оставаться на диагностическом уровне до 1,5 года, а при интенсивном заражении — до 2–5 лет. Для ранней серологической диагностики трихинеллёза желательна одновременная постановка двух серологических реакций: ИФА и РНГА. Чувствительность в этих случаях достигает 90–100% и специфичность — 70–80%. У лиц, употреблявших заражённое трихинеллами мясо, проводят серологическое обследование через 2–3 нед после превентивного лечения. Диагностические показатели серологических реакций — подтверждение того, что эти лица переболели трихинеллёзом. У всех больных трихинеллёзом, наряду с клиническими анализами крови и мочи, проводят биохимический анализ крови, ЭКГ, рентгенологическое исследование лёгких, определяют уровень электролитов в плазме крови.
Дифференциальный диагноз
Дифференциальную диагностику проводят с острыми кишечными инфекциями, брюшным тифом и паратифом, ОРЗ, сыпным тифом, корью, лептоспирозом, иерсиниозом, отёком Квинке. При нарастании эозинофилии в крови трихинеллёз дифференцируют от острой фазы других гельминтозов (описторхоз, фасциолёз, стронгилоидоз, токсокароз), эозинофильного лейкоза, узелкового периартериита, дерматомиозита.
Лечение
Противопаразитарная терапия направлена на уничтожение кишечных трихинелл, пресечение продукции личинок, нарушение процесса инкапсуляции и рост гибели мышечных трихинелл. Для этих целей применяют албендазол и мебендазол. Албендазол назначают внутрь после еды по 400 мг два раза в сутки больным с массой тела 60 кг и более или по 15 мг/кг в сутки в два приёма больным с массой тела менее 60 кг. Длительность лечения 14 дней. Мебендазол назначают внутрь через 20–30 мин после еды в дозе 10 мг/кг в сутки в 3 приёма. Длительность курса лечения 14 дней. При лёгком течении болезни эти же препараты назначают курсом длительностью до 7 дней. Превентивное противопаразитарное лечение лиц, употреблявших в пищу инвазированные мясные продукты, проводят албендазолом в тех же дозах в течение 5–7 дней. Наиболее эффективна этиотропная терапия в инкубационном периоде, когда можно предотвратить клинические проявления, или в первые дни болезни, когда трихинеллы ещё находятся в кишечнике. Во время мышечной стадии заболевания и инкапсуляции эффективность этиотропной терапии значительно ниже, и её применение в этот период может даже способствовать обострению болезни. Больным назначают антигистаминные препараты, ингибиторы простагландинов, НПВС. При тяжёлой инвазии с неврологическими расстройствами, миокардитом, ИТШ, лёгочной недостаточностью используют глюкокортикоиды: обычно преднизолон в суточной дозе 20–60 (по показаниям до 80) мг внутрь в течение 5–7 дней. В связи с тем что глюкокортикоиды могут удлинять период и количество ларвопродукции в кишечнике, рекомендуют назначать противопаразитарные препараты (албендазол или мебендазол) в течение всего периода применения глюкокортикоидов и нескольких дней после их отмены. Опасность представляют также возможные язвенные поражения кишечника в сочетании с нарушениями в системе гемостаза. У таких больных резко возрастает риск ульцерогенного действия глюкокортикоидов, особенно при одновременном назначении НПВС (индометацин, диклофенак и т.п.). В этих случаях для профилактики язвенных поражений в ЖКТ рекомендуют применять ингибиторы протонного насоса (омепразол и др.). Больным трихинеллёзом тяжёлого течения с генерализованными отёками (вследствие ускоренного катаболизма белка и гипопротеинемии) рекомендуют инфузионную терапию с введением дезинтоксикационных средств и препаратов для парентерального белкового питания.
Прогноз
Прогноз благоприятный при лёгкой и среднетяжёлой форме инвазии. Возможно кратковременное возобновление некоторых клинических проявлений: миалгии, умеренных отёков, эозинофилии в анализах крови. При тяжёлой форме с осложнениями прогноз серьёзный: при поздней диагностике и запоздалом противопаразитарном лечении возможен летальный исход; при злокачественном течении он может наступить уже в первые дни болезни.
Госпитализация
Лечение больных среднетяжёлой и тяжёлой формой трихинеллёза проводят в условиях инфекционного стационара или ЛПУ общетерапевтического профиля. Лечение в значительной степени индивидуально и включает специфическую (этиотропную) и патогенетическую терапию.
Профилактика
Меры профилактики паразитарных болезней на территории Российской Федерации регламентирует Санитарные правила и нормы 3.2.1333-03. Основу профилактики трихинеллёза составляют обеспечение ветеринарно-санитарного надзора и санитарно-просветительная работа. Для предупреждения заболевания людей наибольшее значение имеют обязательная ветеринарная экспертиза используемого в пищу мяса, которое допускается к pеализации только после тpихинеллоскопии. Исследованию подлежат также и туши диких животных, добытых на охоте. Большое значение имеет информирование населения через средства массовой информации о гельминтозе и путях его распространения, а также распространение зоотехнических знаний сpеди лиц, содеpжащих свиней в личном хозяйстве. По каждому случаю заболевания трихинеллёзом проводят экстренное эпидемиологическое расследование с целью выявить источник инвазии и предотвратить её распространение. Всем лицам, заведомо употреблявшим в пищу мясные продукты, инвазированные трихинеллами, проводят превентивное лечение.
Кости и мышцы при паразитарной инфекции - лучевая диагностика
а) Визуализация:
• Характеризуется вторичной кальцификацией мягких тканей вследствие кальцификации погибших гельминтов
• Цистицеркоз (свиной цепень):
о Множественные мелкие линейные/овоидные очаги кальцификации расположенные вдоль длинной оси брюшка мышцы
о Проглоченные гельминты проникают в тонкий кишечник и перемещаются в подкожную жировую клетчатку и мышцы
о Характерные очаги инфекции: легкие, головной мозг, глаза, печень
о ↑ заболеваемости на западе Америки, особенно среди латиноамериканцев
• Дракункулез (ришта):
о Кальцифицированные женские особи гельминтов: линейные, могут быть закрученные или фрагментированные; чаще в нижних конечностях
о Употребление зараженной воды
о Другие проявления: стерильные абсцессы, асептический артрит
(Слева) Фронтальная КТ: множественные овальные внутримышечные кальцификаты, характерные для цистицеркоза. Следует отметить, что на сегодняшний день эта паразитарная инфекция чаще встречается на западе США, особенно у латиноамериканцев.
(Справа) Рентгенография в ПЗ проекции: множественные овоидные, имеющие форму риса, кальцификаты, ориентированные вдоль длинной оси мышечных волокон бедра. Классическая картина цистицеркоза. (Слева) Рентгенография в ПЗ проекции: процесс остеолизиса, поражающий проксимальную часть бедренной кости, неровный наружный край кортикального вещества кости. Визуализируется образование мягких тканей с периферической минерализацией.
(Справа) Аксиальный КТ-срез с КУ, этот же пациент: визуализируется мягкая ткань внутри костного мозга с внутрикостной деструкцией. Образование мягких тканей - многодольчатая кистозная структура. Отмечается минерализация стенки кисты. Находки типичны для эхинококкоза костей и мягких тканей.
• Эхинококкоз (гидатидная болезнь):
о Кальцификация по типу яичной скорлупы по периферии кисты
о Паразит попадает с пищей; человек-промежуточный хозяин
о Наиболее часто поражаются: легкие, печень
о Костно-мышечные очаги: позвоночник, кости таза, конечности
о Классическое проявление: множественные кисты (комплексы по типу виноградной грозди) с дочерними кистами
о Очаги могут быть мягкотканными или костными с распадом ± увеличение кости
о МРТ Т1 ВИ: жидкость имеет различную интенсивность сигнала от низкой до высокой; зависит от содержания белка
о MPT С+: усиление кисты по периферии и в перегородках
б) Дифференциальная диагностика:
• Линейная кальцификация мягких тканей: сосудистая, дерматомиозит
• Очаговая кальцификация мягких тканей: флеболиты, гранулемы
Читайте также:

