Паразиты водоросли у человека
Обновлено: 25.04.2024
Какие бывают
Гельминты разделяют на 3 основных группы:
- сосальщики (трематоды),
- ленточные
- круглые (нематоды).
География гельминтозов крайне разнообразна и имеет еще и территориальную привязку.
Сосальщики
Риск заразиться фасциоллезом (печеночный сосальщик) возрастает при употреблении в пищу:
- недостаточно обработанных водяных растений (водорослей и др.),
- печени скота
- и воды из открытых водоемов.
Ленточные черви
Источники бычьего и свиного цепня – очевидны.
Эхинококкоз возникает при употреблении немытых огородных культур, овощей и фруктов, а альвеолококкоз – дикорастущих ягод и трав, или воды из открытых водоемов.
Круглые черви
Аскаридоз и энтеробиоз – распространены повсеместно, а источником заражения могут стать:
А заражение трихинеллезом возможно только при употреблении в пищу мяса кабанов, свиней, медведей и тюленей, чаще в форме сала, бекона, грудинки и колбас.
Какие могут быть симптомы
Заселяя кишечник, гельминты потребляют питательные вещества, витамины и минералы, что неизбежно приводит к:
Эхино- и альвеококки, а также различного рода сосальщики чаще всего поражают печень, провоцируя:
- тошноту,
- диарею,
- вздутие
- и тяжесть в правом подреберье (особенно после приема жирной пищи),
- а в тяжелых случаях – пожелтение кожи и слизистых (признаки гепатита и холецистита).
Альвеококк – нередко проникает и в легкие, сопровождаясь частыми бронхолегочными заболеваниями, изнуряющим кашлем и приступами одышки, подобными бронхиальной астме.
Как выявить
Диагностика гельминтозов сегодня представляет серьезную мировую проблему. Отсутствие каких бы то ни было специфических признаков практически не позволяет предположить инвазию на ранней стадии, а частота стертой симптоматики – еще больше усугубляет ситуацию.
Обоснования для полноценного обследования на паразитов в отечественных клинических рекомендациях представлены крайне скудно. И наличие гельминтов нередко становится случайной находкой во время УЗИ или КТ по поводу другого заболевания.
1.Традиционный анализ кала на яйца глист
Данное исследование обладает достаточно низкой информативностью и чувствительностью, ввиду особенностей жизненного цикла паразитов и методики проведения; и все более теряет актуальность в современной медицине.
Метод позволяет выявлять даже минимальное количество яиц паразитов в материале, что выгодно отличает его от традиционной формы анализа.
Однако стоит отметить, что для выявления энтеробиоза анализ все же не подходит. А для большей информативности, тест рекомендуется сдавать трижды, с интервалом в 3-5 дней.
3.Кровь на антитела к паразитам
Отследить сложный цикл роста и размножения паразитов нередко не удается даже самыми современными методами диагностики кала. Тогда как иммунитет, в большинстве случаев, все же реагирует на инвазию возбудителя.
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
Нематоды, или собственно круглые черви (Nematoda), – тип первичноротых первичнополостных билатерально симметричных линяющих животных.
Распространение. Нематоды – один из самых широко распространенных типов животных, которые смогли освоить самые разные среды обитания – начиная от интерстициали (пространства между песчинками) и моховых сообществ и заканчивая арктическими льдами (как, например, Theristis melnikovi и Cryonema crissum, найденные в толще многолетнего льда в центральной части Северного Ледовитого океана). Особый интерес для исследователей представляют паразитические нематоды, в том числе ввиду большого разнообразия их хозяев.
План строения. Тонкое веретеновидное тело, сужающееся к концам, круглое в поперечном сечении. На переднем конце располагается рот, а на заднем порошица (анус). Снаружи тело покрыто многослойной эластичной кутикулой – неклеточным образованием, выделяемым гиподермой. Гиподерма, или эпидермис, располагается под кутикулой. Мускулатура представлена слоем продольных косо исчерченных мышечных волокон. Первичная полость тела (схизоцель), лишенная собственной эпителиальной выстилки, заполнена жидкостью.
Пищеварительная система. Ротовое отверстие на переднем конце тела окружено выступами – губами (обычно тремя) и ведет в мускулистую эктодермальная глотку с трехгранным просветом. Глотка ведет в энтодермальную среднюю кишку из одного слоя цилиндрических эпителиальных клеток. Далее идет короткая эктодермальная задняя кишка, открывающаяся анальным отверстием.
Кровеносная и дыхательная системы. Эти системы отсутствуют. Дыхание происходит через кожу. Возможен также анаэробный метаболизм (анаэробное расщепление гликогена до масляной и валериановой кислот у паразитов).
Нервная система. Нервная система стволовая лестничного типа. Представлена нервным кольцом и шестью продольными стволами. Два нервных ствола, проходящие по брюшной и спинной линии, более мощные, соединены полукольцевыми нервными перемычками (комиссурами).
Органы чувств. Имеются папиллы и щетинки – органы осязания, расположенные вокруг рта. У некоторых морских представителей обнаружены примитивные глаза – пигментные пятна. Органы химического чувства, амфиды, обычно имеют форму кармана, спирали или щели. Они располагаются по бокам головного конца и особенно хорошо развиты у самцов, так как помогают в поиске самок.
Размножение и развитие. Нематоды – раздельнополые животные. Внутренние половые органы парные, имеют трубчатое строение. Размножение только половое. Половой диморфизм выражен: самки крупнее, у самцов задний конец тела загнут. Оплодотворение внутреннее, встречается живорождение. Нематоды в развитии проходят четыре личиночные стадии, разделенные линьками, которые сопровождаются сбрасыванием кутикулы. Третья стадия у некоторых видов (в том числе у знаменитой Caenorhabditis elegans) при неблагоприятных условиях видоизменяется в так называемую дауер-стадию – покоящуюся личинку.
Паразитизм. В настоящее время из более чем 24000 описанных видов нематод около половины относятся к паразитическим. Они могут поражать почти все ткани и органы: соединительные ткани, мышцы, кровеносные и лимфатические сосуды, гонады, органы чувств, а также полость тела и т. д. Среди них встречаются как экто-, так и эндопаразиты растений, позвоночных и беспозвоночных животных, в том числе других нематод, и даже простейших.
Далее следуют описания наиболее значимых с точки зрения медицинской паразитологии представителей круглых червей.
Человеческая аскарида (Ascaris lumbricoides)
Внешний вид. Заостренное на концах тело розовато-белого цвета. Размеры: самцы – 15-25 см, самки – 20-40 см (рис. 1). Тело покрыто десятислойной гибкой кутикулой, защищающей от механического воздействия и пищеварительных ферментов хозяина.
Рис. 1. Человеческая аскарида: самка, самец, яйцо
Распространение. Вид космополитичен – распространен повсеместно, но в разных странах разный процент зараженных. В Японии, например, более 90% населения заражено аскаридой из-за использования человеческих экскрементов в качестве удобрений. В зонах с жарким сухим климатом аскарида встречается реже.
Жизненный цикл. Развитие протекает без смены хозяев (рис. 2). Взрослые черви паразитируют в тонком кишечнике, вызывая аскаридоз. Человека обычно поражают несколько десятков аскарид (рекорд – 900 штук). Срок жизни в кишечнике – около одного года. Аскариды раздельнополы, как и другие нематоды. Половозрелая самка откладывает в сутки около 200 тысяч яиц овальной формы, которые с испражнениями попадают во внешнюю среду. Аскариды относятся к геогельминтам – для них обязательно развитие личиночной стадии в почве. При попадании в благоприятные условия (во влажную почву при температуре около 25 °C и при достаточном доступе кислорода) в яйце развивается личинка. Срок развития варьируется от 16 дней до нескольких месяцев и зависит от температуры воздуха. Такие яйца, содержащие личинку, можно считать инвазионными.
Рис. 2. Жизненный цикл человеческой аскариды
Клиническая картина аскаридоза. На миграционной стадии аскаридоза наблюдается кашель (помогает личинкам попасть в глотку), боль в груди, аллергические реакции, повышенная температура.
На кишечной стадии происходит повреждение слизистой оболочки кишечника и отравление организма ядовитыми продуктами обмена веществ. Симптомы: тошнота, рвота, нарушения стула, снижение аппетита.
Долговременные эффекты заражения: общее снижение работоспособности, нарушения сна. При заползании червей в желчные протоки и дыхательные пути – летальный исход. Также личинки аскариды могут попадать в головной мозг (например, из нижней полой вены в верхнюю, далее по плечеголовной), вызывая менингоэнцефалит, сопровождающийся мигренями.
Профилактика. Мытье рук перед едой и приготовлением пищи. Мытье овощей и фруктов. Яйца также разносятся мухами, так что борьба с этими двукрылыми посредством, например, липучек тоже способствует профилактике аскаридоза.
Интересный факт. Есть исследования, показывающие положительное влияние заражения аскаридами на облегчение симптомов аутоиммунных заболеваний и повышения плодовитости у женщин. Ученые связывают это с воздействием паразитов на иммунную систему посредством влияния на уровень T-клеток в организме, но на данный момент механизм слишком малоизучен, чтобы делать достоверные выводы.
Острица (Enterobius vermicularis)
Жизненный цикл. Острицы паразитируют в нижней части тонкого кишечника и толстом кишечнике (рис. 4), вызывая энтеробиоз. Срок жизни – 1-2 месяца. Передним концом острицы прикрепляются к стенке кишки. Половозрелая самка из толстого кишечника выползает через задний проход и откладывает на кожу возле анального отверстия от 5 до 15 тысяч яиц, после чего погибает.
Выползание самок сопровождается зудом. При расчесывании кожи яйца переносятся на руки и не только. Также в переносе яиц участвуют мухи. Заражение происходит при заглатывании. Из попавших в кишечник яиц выводятся личинки.Рис. 4. Жизненный цикл острицы
Симптомы: боли в животе, снижение аппетита, головные боли, аллергические проявления, перианальный зуд (приводит к нарушениям сна, повышает раздражительность).
Трихинелла (Trichinella spiralis)
Описание. Мелкая нематода длиной 2-4 мм (рис. 5). Паразитирует в слизистой оболочке тонкого кишечника. Распространена в Евразии и Северной Америке.
Рис. 5. Трихинелла
Жизненный цикл. Для развития трихинеллы необходима смена хозяев. Обычно это дикие животные (лисы, волки, медведи, кабаны), а также люди и скот. Самки закрепляются передним концом тела в кишечный эпителий и рождают 1-2 тысячи личинок. Свойственно яйцеживорождение: вылупление личинок из яиц происходит в половых путях самки. Личинки по кровеносным и лимфатическим сосудам разносятся по всему телу и оседают в поперечно-полосатых мышцах. На этой стадии у них есть стилет, они разрушают с его помощью мышечную ткань, вызывая формирование хозяином капсулы, в которой, свернувшись спиралью, пребывают в дальнейшем. Через несколько месяцев капсула пропитывается известью. Такая мышечная трихина может существовать несколько лет и выжить даже после гибели хозяина и разложения его трупа.
Попав в желудок нового хозяина (после поедания им трупа предыдущего) личинки освобождаются от капсулы (рис. 6.), проникают в слизистую оболочку и в течение пары дней, претерпев четыре линьки, превращаются во взрослых червей.
Рис. 6. Развитие трихинеллы в организме человека
Клиническая картина трихинеллеза. Повышение температуры, одутловатость лица, боли в мышцах, аллергические реакции.
Профилактика. Трихинеллез передается пищевым путем, через зараженное мясо. Поэтому для профилактики заболевания мясо должно пройти ветеринарную экспертизу и быть правильно приготовлено – проварено в течение 2-3 часов. Такие методы приготовления, как копчение и соление, трихинелл не уничтожают.
Власоглав (Trichocephalus trichurus)
Внешний вид. Червь беловатого цвета, длиной около 4 см (рис. 7). Передний конец утончен, напоминает волос (отсюда и название).
Распространение. Предпочитают страны с влажным и теплым климатом.
Жизненный цикл. Жизненный цикл власоглава показан на рис. 8. Червь паразитирует в начальном отделе толстой кишки, только на человеке. Вызывает трихоцефалез. Длительность жизни в человеке – несколько лет. Тонким концом проникает в толщу слизистой оболочки стенки кишки. Питается тканевой жидкостью и кровью.
Самка откладывает 1-3 тысячи яиц, которые с фекалиями попадают во внешнюю среду. Как и аскарида, власоглав относится с геогельминтам: для того чтобы яйца стали инвазивными, им необходимо пребывание в почве при определенной влажности и температуре (25-30 °C) в течение месяца. После этого происходит заражение при проглатывании яиц, в кишечнике хозяина из них выходят личинки, проникают в кишечные ворсинки и растут в них около недели. Затем, разрушив ворсинки, они выходят в просвет кишечника, достигают толстой кишки, закрепляются там и за месяц достигают половозрелости.
Рис. 8. Жизненный цикл власоглава
Клиническая картина трихоцефалеза. Червь повреждает слизистую оболочку толстой кишки и вызывает отравление хозяина продуктами жизнедеятельности. Власоглав – гематофаг, поэтому может привести к малокровию. Трихоцефалез сопровождается болями в животе, головными болями и головокружениями. Из-за того что власоглав прикрепляется к стенке кишечника, его извлечение из организма хозяина труднее, чем извлечение других паразитов.
Ришта (Dracunculus medinensis)
Внешний вид. Тонкая беловатая нематода (рис. 9), самки 30-120 см в длину, самцы не более 4 см. На хвосте имеется маленький шип.
Рис. 9. Ришта: слева – взрослая самка, справа – личинка в циклопе (по Павловскому)
Распространение: тропические страны Азии и Африки.
Жизненный цикл. Заражение происходит при употреблении некипячёной воды с веслоногими рачками (рис. 10). Рачки в желудке под действием соляной кислоты погибают, а вот личинки ришты выживают и через лимфатическую систему разносятся по организму. Далее они проникают в полость тела, там линяют и достигают половой зрелости. После спаривания самец погибает, а самка перемещается в подкожную клетчатку, где образуется гнойный нарыв, сопровождающийся жжением и болью. Для облегчения боли лучше всего подходит прохладная вода.
Рис. 10. Жизненный цикл ришты
Дракункулёз. Инкубационный период продолжается до девяти месяцев и завершается к моменту достижения самкой половой зрелости. А у человека, уже заболевшего дракункулёзом, в это время начинают образовываться гнойные нарывы. Единственное спасение от боли — водоем. Облегчение моментальное, но во время контакта с водой пузыри разрываются, и ришта выбрасывает личинок в воду. Рачки их поглощают, и жизненный цикл начинается снова.
При лечении дракункулёза нередко делают надрез на месте волдыря и понемногу вытягивают червя, наматывая его на палочку. Это занимает дни, а иногда и недели (вытягивать червя приходится медленно и аккуратно, чтобы он не порвался). Высказывались предположения, что вид ришты, намотанной на палочку, стал своеобразным прототипом символа медицины – посоха Асклепия, обвитого змеей (рис. 11).
Рис. 11. Ришта, извлекаемая из ноги человека, страдающего дракункулёзом
Нитчатка (филиярия) Банкрофта, или Банкрофтов струнец (Wuchereria bancrofti)
Внешний вид. Белая нитевидная нематода, самки длиной 10 см, самцы – 4 см (рис. 12).
Рис. 12. Филярия Банкрофта
Распространение. Тропики, субтропики Азии, Африки, Центральной и Южной Америки.
Жизненный цикл. Взрослые особи обычно встречаются в лимфатических железах и сосудах, затрудняя отток лимфы и вызывая постоянный отек. Самки производят личинок – ночных микрофиллярий, которые по ночам появляются в периферической крови, а днем уходят в глубь тела (в легочные сосуды и почки). Это связано с тем, что промежуточным хозяином являются комары, которые сосут кровь обычно в вечерне-ночное время. Личинки попадают в желудок комара, затем в полость тела, где подрастают, после чего скапливаются возле хоботка, из которого передаются человеку при сосании крови. Нитчатки Банкрофта вызывают элефентиаз, или элефантиазис, или слоновую болезнь. Стоит отметить, что это заболевание также могут вызывать другие нематоды.
Клиническая картина и лечение элефантиаза. Происходит увеличение какой-либо части тела (рис. 13) за счет гиперплазии (болезненного разрастания) кожи и подкожной клетчатки, которая вызвана воспалительным утолщением стенок лимфатических сосудов и застоем лимфы, происходящим из-за закупоривания лимфатических сосудов взрослыми особями нитчатки Банкрофта. Кожа на больной части тела покрывается язвами.
Лечение элефантиаза направлено на улучшение оттока жидкости. Эффективно применение противогельминтных препаратов, таких как авермектин. На поздних стадиях может потребоваться хирургическое вмешательство.
Рис. 13. Больной, страдающий элефантиазом (по Брунту)
Список литературы
Генис Д. Е. Медицинская паразитология. 5-е изд. 2017.
Заяц Р. Г. ЕГЭ. Биология в таблицах, схемах и рисунках. 6-е изд. Ростов н/Д: Феникс, 2013.
Чесунов А. В. Биология морских нематод. М.: T-во научных изданий КМК, 2006.
Дирофиляриоз — один из гельминтозов, ранее считавшихся исключительно зооспецифическим и до недавнего времени бытовало мнение, что этому заболеванию подвержены исключительно животные. В первую очередь — собаки. Но в последние годы все чаще стали регистрироваться случаи заражения людей.
Дирофиляриоз: симптомы, подкожный и внутренний дирофиляриоз у человека, лечение и профилактика
Дирофиляриоз — один из гельминтозов, ранее считавшихся исключительно зооспецифическим и до недавнего времени бытовало мнение, что этому заболеванию подвержены исключительно животные. В первую очередь — собаки. Но в последние годы все чаще стали регистрироваться случаи заражения людей.
Дирофиляриоз (Dirofilariasis) — относится к ларвальным гельминтозам. То есть, при этом заболевании паразитирует не взрослая особь нематоды, а ее личинка, не достигшая половой зрелости. Разносчиками заразы являются комары, поэтому наиболее часто этот гельминт встречается в теплом климате: от Австралии, Южной Америки и Африки до Юга России и Средней Азии. На протяжении последних лет наибольшее количество заболевших дирофиляриозом регистрировалось в Иране и Греции. Но в последние годы все чаще регистрируют эту болезнь и в умеренном климате.
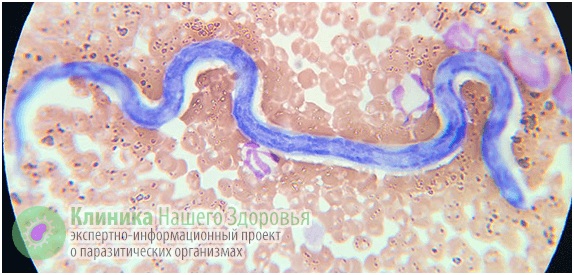
Так, на территории Российской Федерации на протяжении нескольких лет выявляют по 35-40 случаев дирофиляриоза ежегодно. Причем география заражения весьма обширна — от теплого Ростова, умеренных климатических зон Тулы и Рязани, до морозной Сибири. На самом же деле уровень заболеваемости может быть значительно выше. Поскольку этот вид гельминтоза долго считался присущим только животным, то медики его не изучали, и на сегодняшний день о нем мало знают и не сразу могут поставить верный диагноз.
Причины возникновения дирофиляриоза
Как происходит заражение дирофиляриозом?
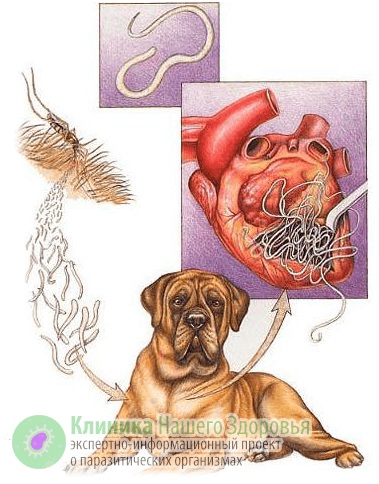
Механизм заражения у людей — трансгемный, то есть инфицирование происходит через кровь. Передается болезнь, зачастую, через укусы комаров. Реже, через укусы блох, слепней и других видов кровососущих насекомых. А источником заразы, как это ни прискорбно, выступают наши домашние животные. В первую очередь собаки, изредка кошки. По данным ветслужбы до 30% собак, живущих в городах, страдают от упомянутой инвазии. В сельской местности этот показатель еще выше. В организме животного взрослые дирофилярии паразитируют в сердце, легких, бронхах и крупных кровеносных сосудах. Самки выделяют в кровь тысячи личинок-микрофилярий, которые имеют микроскопический размер — до 0,3 мм в длину. Именно поэтому они с кровотоком и лимфотоком разносятся по всему организму.
Микрофилярии так микроскопичны, что с кровью и лимфой попадают не только во все органы и ткани человека или животного, но даже преодолевают плацетнарный барьер и внутриутробно инфицируют плод. С кровью животного микрофилярия попадает к промежуточному хозяину — комару. Насекомое, в свою очередь, кусает инвазированное животное, личинки попадают в его брюшную полость, но часть из них остается в хоботке комара. Когда насекомое кусает следующую жертву — часть паразитов из хоботка попадает в кровоток следующего хозяина. Так дифиляриоз передается от животного к животному и к человеку.
У людей тотальная восприимчивость к дирофилриозу – то есть, если человека кусает инфицированный комар, то он заразится со 100% вероятностью. Но в наибольшей зоне риска заражения дирофиляриозом находятся некоторые категории людей, среди которых:
- заводчики собак и кошек;
- люди, проживающие у открытых водоемов;
- те, кто часто бывает на природе — охотники, туристы, огородники, рыбаки.
Этапы развития дирофиляриий
Когда комар (реже другое кровососущее насекомое) заглатывает личинку нематоды с кровью, та около суток остается у него в кишечнике. Затем микрофилярии мигрируют в обратном направлении — к хоботку комара, где дозревают до инвазивной стадии. В этот период, комар, кусает жертву и заражает ее дирофиляриозом.
У нового хозяина около трех месяцев личинки остаются в месте комариного укуса: в коже или в подкожной клетчатке. Именно тут микрофилярии линяет и уже более жизнеспособными попадают в кровоток и разносятся по организму. Паразитировать микрофилярия может около трех лет.
До половозрелости дирофилярия развивается только в организме животных. Человеческий организм для нее тупиковый вариант, так как большинство личинок все же гибнут в крови людей. Это значит, что человек не может быть источник заражения.
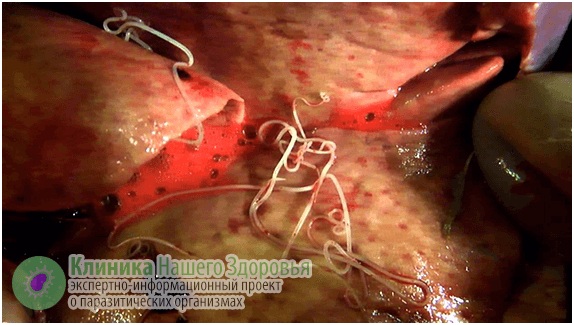
Воздействие дирофилярий на человека
Главная опасность дирофиляриоза — первичные реакции на месте внедрения микрофилярии. Может возникнуть сильная аллергическая реакция. Кроме того, кожа воспаляется, образуются уплотнения (шишки) довольно большого диаметра. Внутри этих уплотнений находится серозная жидкость и/или гной, внутри этого содержимого и обитает какое-то время дирофилярия. Часто паразит погибает, тогда уплотнение постепенно может само рассосаться. Но чаще все же требуется хирургическое вмешательство.
Виды дирофиляриоза
Инвазионное заболевание вызывает червь-паразит. Личинки нитевидной нематоды, вызывающие болезнь, бывают нескольких разновидностей, и поэтому заражение ими приводит к разным формам заболевания.
Dirofilaria repens и Dirofilaria immitis — основные виды, поражающие собак и реже кошек. Именно эти разновидности гельминта являются самыми распространенными среди заболевших людей, ведь в подавляющем большинстве случаев дирофиляриоз у человека появляется при укусе комара-переносчика, контактировавшего до этого с данными животными.
- Dirofilaria repens вызывает подкожную разновидность дирофиляриоза.
- Dirofilaria immitis — висцеральную.
В России и странах ближнего зарубежья встречается в основном подкожный дифиляриоз. Висцеральный дирофиляриоз распространен в жарких странах Азии, Японии, Индии, США, Африке, Канаде, Вьетнаме, Австралии, на юге Европы.
Симптомы и места распространения дирофиляриоза
Скрытая форма дирофиляриоза у человека длится от 1 до 12 месяцев. Основным симптомом является появление под кожей или слизистой, болезненного уплотнения, с покраснением и зудом на месте внедрения. При этом гельминт под кожей может перемещаться (со скоростью до 15 мм в сутки), что может быть заметно для человека, как по ощущениям, так и визуально. Часто, заметив на теле уплотнение похожее на опухоль, пациенты обращаются к хирургу, а тот решает, что это липома, опухоль, фиброма, атерома и т.п., а затем уже в ходе операции обнаруживает гельминта.
У дирофилярий есть любимые места на теле человека — это органы зрения, ноги и руки, шея, лицо, грудь, мошонка. Могут появиться такие симптомы, как слабость, пассивность, тошнота, нервозность, бессонница, повышенная температура, боли в голове и в области поражения паразитом. В 50 % случаев обычно поражаются органы зрения. Человек жалуется на ощущение чего-то ползающего в глазу, у него наблюдается покраснение век и глаз, блефароспазм. При перемещении гельминта возникает боль, слезотечение и зуд. Иногда через конъюнктиву виден сам гельминт.
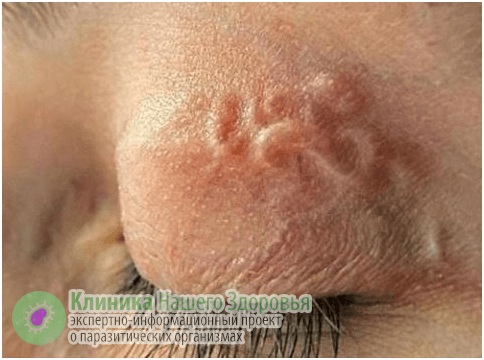
При нахождении дирофилярии в глазу вокруг нее образуется гранулема, что вызывает развитие экзофтальма и диплопии. Поражение глаз приводит к ослаблению зрения. Человек способен увидеть мигрирующего паразита. Наблюдения показали, что его перемещения усиливается под воздействием тепла.
Дифиляриоз обычно носит хронический характер, с рецидивами, характеризующимися периодами вспышек и затихания заболевания. Если вовремя не заняться лечением, вероятны воспаления тканей, и возникновение абсцесса.
Симптомы внутреннего дирофиляриоза
При этой разновидности паразитом поражаются легкие. Личинка живет в левом желудочке сердца и легочных артериях, образуя при этом фиброзную капсулу. Обычно болезнь протекает бессимптомно, реже вызывает боль в груди, кашель и кашель с кровью.
Заболевание часто выявляется случайно, например, при рентгене грудной клетки (видны узелки размером 1-2 см) или при оперировании легких.
Диагностика дирофиляриоза у человека
Диагностика заболевания представляет определенную сложность, так как её симптоматика схожа со многими другими заболеваниями, поэтому врачами часто ставится ложный диагноз и своевременное лечение затягивается. Основными жалобами пациентов являются появление мигрирующих подкожных узлов, ощущения перемещения паразита.
Диагноз дирофиляриоза можно подтвердить, сдав следующие анализы:
- анализ крови;
- после удаления паразита хирургом, проводится его макроскопическое исследование;
- проведение исследования на наличие серологической реакции, позволяющей обнаружить антиген паразита;
- аппаратная диагностика (УЗИ узлов, рентгеновские исследования, эхокардиография и электрокардиография).
Кроме того, перед постановкой диагноза специалист проводит анализ условий проживания больного, времени года, его деятельности. Факторами риска являются наличие домашних и бездомных собак и кошек, комаров, выезд в лес, на рыбалку, на дачу или в сад.
Риск заболевания дирофиляриозом особенно увеличивается в период высокой активности комаров. В связи с чем важны профилактические меры, производимые санитарными службами по ликвидации насекомых на территории водоемов. Известно, что заболевание носит сезонный характер, поэтому основное количество заболевших фиксируется весной и летом. Пики заболеваемости приходятся на периоды июнь-июль и октябрь-ноябрь.
Диагностика дирофиляриоза у животных
Для профилактики заболевания домашним животным необходимо регулярно давать противоглистные препараты. Признаками заболевания паразитами служат различные высыпания, уплотнения, ранки, опухоли на коже.
Больше всего при поражении страдает сердечно-сосудистая система животного. Поведение его становится пассивным, теряется аппетит, отмечается температура, кашель. Собака может прихрамывать и страдать от судорог.
Лечение дирофиляриоза
Форма болезни диктует методы лечения. Обычно у человека паразитирует одна неполовозрелая особь. Основной метод избавления от паразита — хирургический. Чтобы исключить перемещение паразита применяют дитразин. Редко применяется терапия медикаментами с использованием ивермектина или диэтилкарбамазина. Дополнительно при лечении используются успокаивающие и антигистаминные лекарства, нестероидные противовоспалительные средства, глюкокортикостероиды.
При глазном дирофиляриозе основным методом лечения будет удаление гельминта с помощью операции и последующие назначение дезинфицирующих и противовоспалительных препаратов для глаз, иногда также прописываются капли дексаметазона для уменьшения воспаления. Обязательно назначаются антигистаминные средства.
Профилактика дирофиляриоза
В России 4-30% (в зависимости от географии их проживания) домашних и уличных собак являются хозяевами-переносчиками микрофилярий. Самый большой процент зараженных животных в Греции и Иране- 25-60%.
Профилактика заболевания включает в себя истребление комаров и ограничение контакта с ними животных и человека, своевременное выявление дирофилярий животных и их лечение, борьба с бродячими животными, противоглистная профилактика у домашних питомцев.
Так как очагами дирофиляриоза являются водоемы около жилых районов, очевидна эффективность мер, применяемых санитарными органами по борьбе с кровососущими насекомыми. К тому же необходима борьба с комарами в подвалах жилых домов, ведь здесь эти паразиты могут с комфортом обитать весь год. Из подвалов жилых домов комары и другие насекомые попадают по вентиляционной системе в квартиры.
В лесу и около водоемов необходимо использовать репелленты и защищать участки тела с помощью одежды. Животным кроме репеллентов могут быть одеты специальные ошейники. По возможности старайтесь отказаться от прогулок в вечернее и ночное время суток.
Человек сам в ответе за собственное здоровье, а также за здоровье своих детей, родных и близких, поэтому отправляясь в отпуск в теплые страны, будьте бдительны! Легче предотвратить болезнь, соблюдая профилактические меры, чем лечить ее последствия!
Как происходит заражение?
До попадания в организм человека, гельминты и простейшие проходят цикл развития в других средах или живых организмах.
- В почве при определённых условиях температуры и влажности сохраняются яйца и личинки аскарид, стронгилоид, анкилостом Человек заражается при попадании зараженной почвы через грязные руки, воду, непромытые фрукты и овощи, непосредственно с землёй.
- В живых организмах проходят циклы развития следующие гельминты: описторхи (кошачья двуустка), клонорхи, трихинеллы, токсокары, эхинококки, свиной и бычий цепень. До достижения зрелости, чтобы паразитировать в человеке, возможна смена одного или двух промежуточных хозяев. Это моллюски, ракообразные, рыба, насекомые. Употребление термически недостаточно обработанной рыбы и мяса, сырой воды приводит к заражению.
Ещё один путь заражения - при непосредственном контакте людей через рукопожатия, общие предметы гигиены и быта или путем самозаражения. Речь идёт о контагиозных гельминтах: энтеробиоз, стронгилоидоз, цистицеркоз, лямблиоз.
Как можно заподозрить паразитарное заболевание?
Проявления могут быть разнообразными, течение от легкого до тяжёлого. Редко возникают типичные признаки, выдающие конкретного возбудителя. Зачастую признаков нет, или они маскируются под другие заболевания, или исчезают по мере окончания одного цикла развития паразита и начала другого. Например, личинки аскарид сначала попадают в лёгкие человека, где дозревают и мигрируют в кишечник. Ребёнка может беспокоить недолгий кашель (похоже на простуду), не настораживающий родителя.
Тем не менее, обычно выделяют острую и хроническую фазы течения паразитарного заболевания.
Острые проявления возникают вследствие общего воздействия на организм:
- Влияния токсинов – повышение температуры до 37 – 37,5 градусов, слабость, головные боли, снижение настроения и работоспособности, нарушения сна;
- Аллергических реакций – кожный зуд, крапивница, бронхоспазм, одышка, реже отёк Квинке;
- Активации иммунной системы– боли в мышцах и суставах; увеличение лимфоузлов, печени и селезенки
- Механического воздействия – если посмотреть под микроскопом, у каждого гельминта можно увидеть приспособления для закрепления в организме, травмирующие слизистую: зубья, крючья, присоски. В результате возникают боли в животе, частый стул, диспепсия.
Хроническая фаза характеризуется поражением определённых органов и систем. Чаще всего страдает кишечник, длительное механическое воздействие приводит к его воспалению, нарушениям всасывания и переваривания пищи. Развивается анемия, недостаток витаминов и микроэлементов, а у маленьких детей отмечается задержка роста и набора веса. Могут поражаться желчный пузырь и желчевыводящие пути (лямблиоз); сердечно-сосудистая система, лёгкие, нервная система (чаще трихинеллез); лёгкие и печень (эхинококкоз) и так далее. При длительном течении подавляется иммунитет и присоединяются вторичные инфекции.
Если Вы обнаружили любой из перечисленных признаков, сдайте клинический анализ крови с лейкоцитарной формулой. Повышение эозинофилов до 7-10% и более станет ещё одним подозрительным критерием.
Как выявить паразитарное заболевание?
-
, предпочтительнее обогащающий метод – PARASEP Определяет яйца всех видов гельминтов и простейших, обитающих в кишечнике
Следует обратить внимание на следующие моменты:
На что нужно обратить внимание?
- Наличие проявлений и одновременное обнаружение IgG могут свидетельствовать о хронической фазе гельминтоза
- В сомнительных случаях рекомендовано повторное исследование IgG через 2 недели. Нарастание уровня антител в 2 раза и более говорит об активности гельминта
- При трихинеллезе, эхинококкозе, цистицеркозе определение антител – единственный возможный метод лабораторной диагностики, поскольку человек – промежуточный хозяин для данных гельминтов.
Читайте также:

