Патогенез интоксикации при воспалении
Обновлено: 26.04.2024
2.КЛАССИФИКАЦИЯ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
2.1. ПРИЧИНЫ И МЕХАНИЗМЫ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Эндогенная И может быть вызвана токсическими продуктами, образующимися в организме при различных заболеваниях (аллергических болезнях, ожоговой болезни) и экстремальных состояниях. К эндогенной И. относится отравление продуктами жизнедеятельности бактерий, находящихся в организме. В ряде случаев И. становится ведущим патогенетическим фактором, определяющим развитие клинической картины (уремия, токсикоинфекции, тиреотоксикоз, токсическая дифтерия, токсическая диспепсия и др).
В механизмах как эндогенной, так и экзогенной И. имеется много общего, т. к. в том и другом случае повреждающим фактором является токсический агент. Кроме того, И, вызванная экзогенным фактором, может реализоваться эндогенным путем; например, отравление антихолинэстеразными ядами типа физостигмина или фосфакола в основном сводится к аутоинтоксикации ацетилхолином, который накапливается в синаптических образованиях вследствие прекращения его ферментативного гидролиза.
К числу веществ, накапливающихся в организме при различных заболеваниях и вызывающих эндогенную И., относятся химические соединения различной природы: продукты превращения аминокислот (фенол, крезол, индол, скатол, путресцин, кадаверин), жиров (γ-оксимасляная кислота, ацетоуксусная кислота и ацетон). Имеют значение также активные белки, аденилнуклеотиды, гистамин, серотонин, кинины и другие физиологически активные вещества, выделяющиеся в значительных количествах при повреждении клеток и тканей. При инфекционных заболеваниях происходит накопление бактериальных токсинов и других продуктов жизнедеятельности микробов, а также продуктов распада тканей.
Основной причиной И в условиях трансплантации является реакция трансплантат против хозяина. При возникновении И в различных экстремальных состояниях, например, при ожоговой болезни, травме, патогенетическое значение имеет подавление детоксицирующей способности ретикулоэндотелиальной системы, в связи с чем в организме происходит накопление эндотоксина Е. coli. вызывающего расстройства микроциркуляции. Имеет место также стимулирование неферментативного перекисного окисления липидов клеточных мембран, в результате чего в организме накапливаются токсичные продукты, что вызывает изменение проницаемости этих мембран. При лучевом поражении, кроме того, происходит накопление липидных и хиноноподобных токсинов, повреждающее действие которых на клетки приводит к накоплению в организме гистамина и других физиологически активных продуктов белкового распада. Снижение содержания в тканях естественного ингибитора цепных окислительных реакций токоферола имеет значение для развития И при авитаминозе Е и новообразованиях.
2.2. ИСТОЧНИКИ ЭНДОТОКСИНЕМИИ
- продукты нормального обмена веществ в высоких концентрациях (лактат, пируват, мочевая кислота, мочевина, креатинин, билирубина глюкуронид и др.);
- вещества, избыточно образующиеся при извращенном метаболизме (кетоны, альдегиды, спирты, карбоновые кислоты, аммиак и др.);
- продукты распада клеток и тканей из очагов тканевой деструкции и/или из ЖКТ при нарушении барьерных функций мембран (липазы, лизосомальные ферменты, катионные белки, миоглобин, индол, скатол, фенол и др.);
-компоненты и эффекторы регуляторных систем организма в патологических концентрациях: активированные ферменты (лизосомальные, протеолитические, продукты активации калликреинкининового каскада, системы свертывания крови и фибринолиза);
- медиаторы воспаления, биогенные амины, цитокины, простагландины, лейкотриены, белки острой фазы и другие биологически активные вещества;
- активные соединения, образующиеся при перекисном окислении липидов;
- микробные токсины (экзо- и эндотоксины) и другие факторы патогенности микроорганизмов (патогенных, условно-патогенных, непатогенных);
- иммуночужеродные продукты клеточного распада, антигены и иммунные комплексы-агрессоры.
2.3. ПУТИ ЭЛИМИНАЦИИ ЭНДОГЕННЫХ ТОКСИНОВ
- газообразные вещества – выделяются через легкие;
- гидрофильные низко- и среднемолекулярные вещества – удаляются почками, через кожу, ЖКТ в виде растворов;
- гидрофобные низко- и среднемолекулярные вещества – транспортируются белками и/или клетками крови в печень и легкие, где и биотрансформируются при участии монооксигеназной системы или
претерпевают изменения в реакциях связывания с последующим удалением через почки, кожу, ЖКТ;
- гидрофобные низко- и среднемолекулярные вещества – связываются с белками плазмы крови, приобретают свойства гаптенов и поглощаются клетками иммунной системы;
- высокомолекулярные соединения – транспортируются по лимфатическим сосудам, элиминируются моноцитарно-макрофагальной системой (до 80% макрофагов организма находится в печени).
2.4. СТАДИИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Острый эндотоксикоз протекает как каскадный процесс. Развитие и прогрессирование его связано с несоответствием между образованием (поступлением и т.д.) токсических субстанций, в том числе образующихся в результате последующей токсической аутоагрессии, и способностью органов, входящих в функциональную систему детоксикации (легкие, печень, почки, ЖКТ, кожа, система иммунологического надзора), их трансформировать, нейтрализовать и элиминировать. Существенное значение могут иметь нарушения соотношений между веществами антагонистами в гуморальных регуляторных системах (ферменты-антиферменты, оксиданты-антиоксиданты, цитокины-антицитокины и т.д.).
Исходя из взаимоотношений эндогенной интоксикации и возможностей функциональной системы детоксикации (ФСД) можно выделить 4 стадии развития эндотоксикоза: компенсации, напряжения, субкомпенсации и декомпенсации.
3. ПАТОГЕНЕЗ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Механизм И в основном заключается в повреждающем действии эндогенного или экзогенного токсического агента на те или иные клеточные структуры и нарушении метаболических процессов в организме. При некоторых видах И повреждение клеток может иметь характер некроза (напр., при воздействии четыреххлористого углерода на печень), однако, в большинстве случаев происходят обратимые изменения на различных уровнях организма от субклеточного до системного, которые приводят к сдвигам гомеостаза в связи с нарушением метаболизма. Так, в основе мембранотоксического действия афлатоксинов, некоторых бактериальных токсинов, сапонинов лежит нарушение структуры фосфолипидов и образование промежуточных продуктов гидролиза. В механизмах И имеет значение не только непосредственное действие токсических веществ на определенные функции, но и нейрогуморальные и рефлекторные влияния, а также вовлечение в патологический процесс серотонина, кининов и других физиологически активных веществ, выделяющихся в значительных количествах при повреждении клеток и тканей.
В механизмах И имеют значение не только непосредственное действие токсических веществ на определенные функции, но и нейрогуморальные и рефлекторные влияния, а также вовлечение в патологический процесс различных органов и систем. При хронических И некоторыми химическими соединениями, алкилирующими фосфатные группы нуклеиновых кислот (нитрозоэтилмочевина, этилметан-сульфонат и др.), может проявиться их мутагенное действие; при И некоторыми циклическими углеводородами (3,4-бензпирен и др.) – канцерогенное действие.
Развитию И противостоят детоксицирующие системы организма, обеспечивающие химическое превращение токсичных веществ в менее токсичные или растворимые вещества, поддающиеся выведению из организма (окисление, гидролиз, метилирование, восстановление и образование парных соединений и другие процессы). Эти процессы происходят с участием ферментных систем организма, обеспечивающих обезвреживание и метаболические превращения ядовитых веществ. Яды, поступающие в кровь, через воротную вену попадают в печень, являющуюся мощным детоксицирующим барьером, и частично в ней нейтрализуются. И развивается при поступлении в организм токсичных веществ в количестве, превышающем возможности детоксицирующих систем или при их неполноценности.
4. КЛИНИКА ЭНДОГЕНОЙ ИНТОКСИКАЦИИ
5. КЛИНИЧЕСКОЕ ОБСЛЕДОВАНИЕ ПАЦИЕНТОВ С СИНДРОМОМ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ. УРОВНИ ДИАГНОСТИКИ
Диагностика ЭИ разработана главным образом на биохимическом уровне.
В том случае, если состояние не является критическим, для его диагностики целесообразно использовать тот же принцип, что и заложенный в основу распознавания дистресса, т.к., по-видимому, эндогенная интоксикация во многом пересекается с реакцией общего адаптационного синдрома. Мы предлагаем оценивать такие признаки дистресса, главным образом субъективные, которые составляют основу ряда вопросников для диагностики дистресса (табл. 1).
Несмотря на схожесть патогенеза, синдрома эндогенной интоксикации при каждой нозологической форме имеет определенные специфические признаки (Ю. С. Гольд-фарб, 1988; Б. И. Шулутко, 1993; Э. А. Туликова, 1994). Перитонит условно можно назвать классической моделью СЭИ, поэтому его целесообразно рассмотреть в качестве базовой модели данного состояния.
Патогенез. Выделяют три компонента, участвующих в формировании СЭИ при перитоните:
1. Микробиологический.
2. Биохимический.
3. Иммунологический.
В течении СЭИ выделяют три (разы (В. К. Гостищев и соавт., 1992):
I фаза — фаза интоксикации. В формировании СЭИ участвуют болезнетворные микробы и их токсины, биоактивные вещества, синтезируемые в организме в норме, но в данном случае их синтез выходит из-под контроля и вещества начинают накапливаться.
II фаза — диспротеинемия. Для нее характерны активные деструктивные процессы в тканях; усиливается распад белков, снижается их синтез, нарушаются процессы дезаминирования. С момента начала деструкции в крови повышается уровень некротических тел, СМ, которые и вызывают токсический эффект. В начале II фазы присоединяются аутоаллергические процессы.
III фаза — накопление промежуточных метаболитов. В крови и лимфе накапливаются этанол, аммиак, ацетон и др. Микробный фактор может ускорить переход одной фазы в другую. Тяжесть, время развития и обратимость СЭИ прямо связаны с тем, какие микробы вызвали заболевание: ранее имевшаяся микрофлора или новые.
Клинически в течении синдрома эндогенной интоксикации различают три степени тяжести (В. К. Гостищев и соавт., 1992). Основные критерии клинических данных степеней тяжести эндогенной интоксикации представлены в табл. 28.
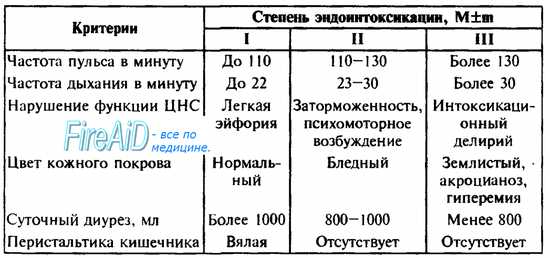
Таблица 28. Степени эндогенной интоксикации при перитоните (В. К. Гостищев и соавт., 1992).
Наиболее характерным признаком появления синдрома эндогенной интоксикации при перитоните является нарушение сознания в виде энцефалопатии (см. тему НЕОТЛОЖНЫЕ СОСТОЯНИЯ В ПСИХИАТРИИ). Больной становится заторможенным и безразличным к окружающему. Вначале данное состояние чередуется с периодами легкой эйфории, в это время больные говорливы, не могут сосредоточиться на одной мысли. При нарастании интоксикации заторможенность также нарастает, иногда наоборот, возникает психомоторное возбуждение, переходящее в интоксикационный делирий, после чего возможно наступление комы (см. тему ОБМОРОК, КОЛЛАПС, КОМА). Для определения снижения (угнетения) уровня сознания можно использовать шкалу Глазго.
Другим характерным признаком синдрома эндогенной интоксикации является сокращение почасового диуреза, обусловленное поражением почечных канальцев по типу острого нефроза и потери жидкости (рвота, понос, выход жидкости во внеклеточное пространство). Вследствие этого происходит дополнительное отравление организма невыведенными продуктами белкового обмена. Каждой степени СЭИ соответствует определенный суточный диурез (см. табл. 28). Критическим является почасовой диурез в объеме 40 мл/час и менее. При тяжелой степени интоксикации с переходом олигурии в анурию возможно формирование ОПН (см. тему ОСТРАЯ ПОЧЕЧНАЯ И ПЕЧЕНОЧНАЯ НЕДОСТАТОЧНОСТИ).
Появление желтушности кожных покровов и склер является прогностически неблагоприятным признаком, так как это свидетельствует о развитии острой печеночной недостаточности и снижении детоксикационных возможностей организма (см. тему ОСТРАЯ ПОЧЕЧНАЯ И ПЕЧЕНОЧНАЯ НЕДОСТАТОЧНОСТИ).
Гемодинамические изменения при СЭИ, как впрочем и все другие, не являются специфическими. Причиной учащения пульса, снижения АД могут быть шок, реакция на боль, кровопотерю, предшествующая сердечная недостаточность. Следует помнить, что снижение давления ниже 90 мм рт. ст. характерно для шока II степени (см. тему ШОКОВЫЕ СОСТОЯНИЯ).
Основные биохимические показатели синдрома эндогенной интоксикации на фоне перитонита представлены в табл. 29.
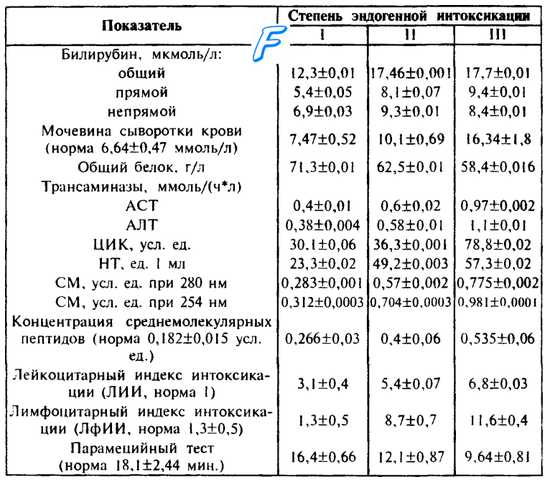
Таблица 29. Биохимические показатели крови при эндогенной интоксикации различной степени, М±т (В. К. Гостищев и соавт., 1992).
Примечание. 1. ЦИК — циркулирующие имунные комплексы; НТ некротические тела; СМ — средние молекулы.
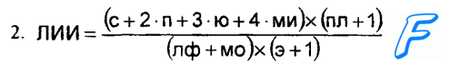
ми миелоциты;
с сегментоядерные лейкоциты;
ю метамиелоциты;
п палочкоядерные лейкоциты;
пл плазменные клетки;
лф лимфоциты;
МО моноциты;
э эозинофилы.
Этиология синдрома эндогенной интоксикации. СЭИ встречается при гнойно-воспалительных заболеваниях (перитонит, холецистит, панкреатит и др.), тяжелых травмах (краш-синдром), некоторых заболеваниях (сахарный диабет, тиреотоксический зоб), различных отравлениях и др.
Патогенез синдрома эндогенной интоксикации. Что может объединять данные нозологические формы, весьма далекие по этиологии? На определенном этапе заболевания, при стечении неблагоприятных факторов, это будет: 1. Токсемия, 2. Тканевая гипоксия и 3. Угнетение функции собственных детоксицируюших и защитных систем организма.
Основным звеном данного патологического каскада является токсемия (В. А. Остапенко, 1994).

Токсемия
Токсемию вызывает избыточное накопление в организме эндотоксинов. С. А. Симбирцев и Н. А. Беляков (1994) классифицируют эндотоксины по следующим группам:
• продукты естественного обмена в высоких концентрациях;
• активированные ферменты, способные повреждать ткани;
• медиаторы воспаления и другие биологически активные вещества (БАВ);
• класс среднемолекулярных веществ различной природы;
• перекисные продукты;
• неоднородные по составу ингредиенты нежизнеспособных тканей;
• агрессивные компоненты комплемента;
• бактериальные токсины (экзо- и эндотоксины).
Эндотоксины вызывают деструкцию белков и липидов клеток, блокируют синтетические и окислительные процессы. Особо следует акцентировать внимание на биологически активных веществах (БАВ) и средних молекулах (СМ).
Существуют четкие корреляции между концентрацией в крови и тканях продуктов калликреин-кининового каскада, биогенных аминов и степенью структурных поражений при многих острых процессах. Во всех случаях увеличение активности медиаторов воспаления сочетается с усилением тяжести поражений органов и систем (С. А. Симбирцев, Н. А. Беляков, 1994).
Эндотоксины оказывают прямое и опосредованное воздействие на структуру клеток, сами клетки, системы и органы (дистантное действие).
По действию на уровне клеточных структур эндотоксины можно классифицировать следующим образом (С. А. Симбирцев, Н. А. Беляков (1994):
• обладающие цитолитическим эффектом;
• активаторы лизосомальных ферментов;
• блокаторы митохондриальной энергетики;
• инициаторы свободнорадикальных процессов;
• ингибиторы рибосомального синтеза;
• способные к воздействию на различные клеточные образования.
Дистантное действие эндотоксинов выражается поражением системы микроциркуляции, которое наблюдается как в виде изолированных вне- и внутрисосудистых расстройств, так и комбинированных изменений. К внесосудистым изменениям относят нарушение регуляции тонуса периферических сосудов, среди внутрисосудистых изменений основное место отводят нарушениям реологического состояния крови, нарушениям транскапиллярного и трансмембранного обмена.
На уровне межорганных и межсистемных влияний (дистантное повреждение) действие эндотоксинов преломляется следующим образом (С. А. Симбирцев, Н. А. Беляков (1994):
• активаторы комплемента и белых клеток крови;
• активаторы калликреин-кининовой системы;
• активаторы коагуляции и фибринолизиса;
• вещества, изменяющие тонус гладкой мускулатуры;
• индукторы агрегации;
• воздействующие на проницаемость сосудистой стенки.
Это разделение на группы носит элемент условности, поскольку нет четкой границы между особенностями действия эндотоксинов, когда одни и те же вещества запускают каскадные реакции и повреждающий эффект тканевых структур осуществляется синерги-ческим влиянием с одномоментным включением защитных механизмов.
Заключение. Развитие процесса интоксикации можно представить как поступление эндотоксинов из мест образования (очаги воспаления, иммунная система, печень как источник синтеза патологических белков) в кровоток. Через кровь они попадают в органы фиксации и биотрансформации (печень, иммунная система, легкие), органы выделения патологических субстанций (печень, почки, ЖКТ, легкие, кожа), а также в органы и ткани депонирования патологических субстанций (жировая, нервная, костная ткань, органы эндокринной системы, лимфоидная ткань). При различных патологических состояниях, когда количество естественных продуктов жизнедеятельности организма, появившихся в больших количествах в биологических средах, а также заведомо агрессивные компоненты превышают возможности их биотрансформации, развивается СЭИ (К. Я. Гуревич, А. Л. Костюченко, 1994).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Синдром эндогенной интоксикации. Клиника синдрома эндогенной интоксикации.
В настоящее время одной из наиболее сложных проблем интенсивной терапии является синдром эндогенной интоксикации (СЭИ), сопровождающий значительное количество патологических состояний (шок, перитонит, панкреатит и др.), которые по мере своего развития могут приводить к летальному исходу.
Прогрессирование эндотоксикоза обусловлено накоплением в крови различных по происхождению, химической структуре и биологическому воздействию веществ, именуемых эндотоксинами. Эндотоксины способствуют развитию острой почечно-печеночной недостаточности, сердечно-сосудистой недостаточности, острого респираторного дистресс-синдрома, приводя в конечном итоге к появлению крайне тяжелого состояния - синдрома мультиорганной дисфункции.
Эндогенная интоксикация - клинический синдром, возникающий при различных по этиологии патологических состояниях, обусловленных накоплением в тканях и биологических жидкостях организма продуктов нарушенного обмена веществ, метаболитов, деструктивных клеточных и тканевых структур, разрушенных белковых молекул, pi сопровождающийся функциональными и морфологическими поражениями органов и систем организма.
Выделяют три основных звена, которые определяют тяжесть состояния больных и выраженность клинической симптоматики: токсемия, нарушение микроциркуляции, угнетение функций собственных детоксицирующих и защитных систем организма.
Основным звеном патогенеза синдрома эндогенной интоксикации является токсемия. К сожалению, четкая дифференциация токсических веществ эндогенного происхождения практически невозможна. Однако в каждом конкретном случае можно выделить "первичные" и "вторичные" эндотоксины. Так, при ожогах, синдроме длительного раздавливания, облитерирующих сосудистых заболеваниях "первичными" являются продукты белковой деградации, "вторичными" - продукты естественного метаболизма, накопление которых в организме является следствием угнетения функций естественной детоксикации и экскреции.
Эндотоксемия, нарушая тонус периферических сосудов, реологию крови, кинетические и механические свойства форменных элементов крови, приводит к тканевой гипоксии, которая является одним из важных звеньев патогенеза СЭИ, течение которого усугубляется снижением функции органов естественной детоксикации и экскреции. Токсины блокируют места связывания молекул альбумина, что ведет к снижению эффективности проводимого медикаментозного лечения, поскольку этот белок является транспортным агентом для многих фармакологических препаратов.
Клиника синдрома эндогенной интоксикации.
Сопоставление экспериментальных и клинических исследований позволило выявить следующие стадии развития синдрома эндогенной интоксикации.
I стадия синдрома эндогенной интоксикации. Реактивно-токсическая возникает в ответ на формирование первичного деструктивного очага или травматического повреждения. Лабораторными признаками этой стадии являются повышение в крови уровней молекул средней массы (МСМ), продуктов перекисного окисления липидов (ДК и МДА), возрастание ЛИИ.
II стадия синдрома эндогенной интоксикации - стадия выраженной токсемии развивается после прорыва гастогематического барьера, когда в циркулирующую кровь попадают эндотоксины, образовавшиеся в первичном очаге интоксикации, с последующим распространением и накоплением в организме. В зависимости от состояния организма, его резистентности и исходного уровня детоксицирующих и иммунных систем выделяют компенсированную и декомпенсированную стадии выраженной токсемии.
III стадия синдрома эндогенной интоксикации - мультиорганной дисфункции (СМОД) наблюдается при дальнейшем прогрессировашш патологического процесса как следствие тяжелого повреждения эндотоксинами различных органов и систем с развитием их функциональной декомпенсацш!. Клинически эта стадия Проявляется нарушением сознания, гипоксией, выраженной сердечной Недостаточностью, олигурией, паралитической непроходимостью кишечника. В крови определяется высокая концентрация креатинина, мочевины, билирубина.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Студент медицинского факультета УЛГУ. Интересы: современные медицинские технологии, открытия в области медицины, перспективы развития медицины в России и за рубежом.
- Запись опубликована: 27.06.2019
- Reading time: 2 минут чтения
Интоксикация — это отравление организма, вызванное воздействием какого-либо вещества.
Стадии отравления
В зависимости от тяжести интоксикации принято выделять три стадии течения патологического процесса.
- Первая стадия (легкая степень). Симптоматика в этом случае ограничивается изменением дыхания: оно становится частым и неритмичным. Характерно появление преходящих хрипов при дыхании. Наблюдается появление немотивированной эйфории, апатии и их чередование. Такие изменения психоэмоционального фона провоцируются отёком головного мозга. Для этой стадии характерны сердечно-сосудистые нарушения в виде тахикардии и/или незначительная артериальная гипотензия.
- Вторая стадия. Такое состояние характеризуется головными болями, ознобом, мышечными спазмами и судорогами. Больной жалуется на бессонницу на фоне слабости и усталости, снижение аппетита вплоть до его отсутствия, тошноту.
- Третья стадия. Это тяжёлая лихорадка, способная привести к летальному исходу. Человека беспокоят мышечные боли, озноб, выраженная тахикардия и снижение артериального давления. Галлюцинации и бредовые состояния на этой стадии не редкость. При отсутствии адекватной терапии возможна кома.
Клиническая картина острой интоксикации
Характерная черта этого расстройства — появляется оно сразу, незамедлительно. В этом случае важно оказать помощь на ранней стадии.
Возникновение острой интоксикации связано с проникновением в организм большого количества веществ, обладающих токсическим действием, употреблением пищи или воды ненадлежащего качества или выраженной передозировкой лекарственных препаратов. Характер течения и степень тяжести интоксикации определяется разновидностью токсического вещества, попавшего в организм.
Проявления острой интоксикации
Наиболее характерные проявления острой интоксикации:
- выраженная резкая боль в области желудка;
- неудержимая рвота;
- остро появившийся жидкий стул.
Рвота и понос в этой ситуации — реакция организма на отравление, с помощью которой он старается очиститься от токсического вещества. Поэтому первое время после появления такой симптоматики нет смысла стараться ее заблокировать.
Особенности клинической картины в зависимости от происхождения интоксикации могут варьироваться. Это помогает при диагностике, когда необходимо отличить экзогенную интоксикацию от эндогенной.
Экзогенная интоксикация
Токсические вещества, вызывающие расстройства, могут проникать в организм различными способами: через пищеварительный тракт, слизистые оболочки, кожный покров, через дыхательные пути.
Заподозрить экзогенную интоксикацию помогут следующие симптомы:
- Выраженная гипертермия.
- Лихорадочное состояние.
- Острая реакция со стороны пищеварительного тракта: рвота, диарея, выраженная изжога. При отравлении растворами, имеющими щелочную или кислую реакцию, в рвоте могут присутствовать сгустки крови.
- Судорожные сокращения мышц конечностей.
- Ухудшение картины рефлексов.
В случае трансдермального проникновения яда в организм или попадания его через слизистую оболочку, в большинстве случаев наблюдается местная реакция в виде выраженных аллергических проявлений: покраснений, очагов высыпаний, напоминающих ожоги.
Важным признаком экзогенной интоксикации синдрома является острое кислородное голодание всех тканей организма. Оно обусловлено способностью токсинов блокировать возможность эритроцитов переносить кислород. Гипоксия приводит к расстройству всех систем жизнеобеспечения организма человека:
- снижается частота пульса;
- развивается распространённый отёчный синдром, наиболее опасны отёк лёгких и головного мозга.
Эндогенная интоксикация
Интоксикационный синдром эндогенного происхождения — не самостоятельное заболевание. Он сопровождает многие заболевания и является частью их патогенеза.
Эндотоксинами или аутоядами называются вещества, которые вырабатываются внутри организма в результате распада молекул или клеточных структур. Обладая токсическими свойствами, эти вещества вызывают развитие недостаточности работы жизненно важных органов: почек, печени, сердца.
Проявления эндогенной интоксикации:
- головная боль;
- нарушение сна;
- исчезновение аппетита.
Такой симптомокомплекс часто наблюдается при интоксикационном синдроме, сопровождающем инфекционно-воспалительные заболевания.
В случае более выраженной степени интоксикации добавляются следующие симптомы:
- снижение суточного объёма мочи;
- головокружение;
- ощущение прогрессирующей накопившейся хронической усталости;
- нарушение ритма работы сердца;
- галлюцинации — признак тяжёлого интоксикационного синдрома, который сопровождается лихорадкой, в частности, этот симптом характерен для ожоговых травм при поражении большой площади тела с глубиной ожогов 3–4 степени.
В некоторых случаях к указанной симптоматике общего характера добавляются специфические признаки, которые могут помочь при диагностике. Например, желтушное окрашивание склер и кожных покровов при поражении печени билирубином.
Медицинская помощь при отравлении с разными типами интоксикации
Остановить прогрессирование патологических изменений при интоксикации независимо от её характера можно, если прекратить воздействие отравляющего вещества на организм и максимально быстро провести комплекс мероприятий по выведению его из организма больного. В зависимости от механизма отравления для этого применяются следующие методы:
- промывание желудка;
- приём сорбентов;
- форсированный диурез;
- гемодиализ.
В некоторых случаях эти методы дополняют друг друга.
Одновременно необходимо принимать меры по восстановлению жизненно важных функций организма больного. Особенно это важно при тяжёлой степени отравления. Нарушение водно-электролитного баланса и обезвоживание, возникшие в результате рвоты и диареи, корректируется при помощи обильного питья и/или инфузионной терапии.
При этом существует опасность усугубления отёка головного мозга и лёгких, поэтому за больным необходимо постоянное наблюдение с целью своевременной коррекции нарушений.
На фоне адекватной инфузионной терапии сердечно-сосудистые нарушения могут начать регрессировать самостоятельно. В противном случае приходится брать под контроль давление и удерживать его с помощью соответствующих медикаментов.
При лечении интоксикации на любой стадии может понадобиться и симптоматическая терапия:
Читайте также:

