Патогенез желтухи при малярии
Обновлено: 22.04.2024
Тяжесть течения P.falciparum-малярии. Клинические особенности P.falciparum-малярии
С первых дней болезни на фоне лихорадки (обычно ремиттирующего, субконтинуального или неправильного типов) больные отмечают сильную головную боль, головокружение, разлитые миалгии и артралгии, резкую слабость При высокой температуре тела наблюдаются тошнота, повторная рвота, артериальная гипотензия, тахикардия и тахипноэ Характерным признаком болезни являются боли в мезогастрии, учащение стула, при этом, в отличие от острых кишечных инфекций, каловые массы обычно не имеют патологических примесей.
У ряда больных в начальный период болезни наблюдаются кашель, признаки бронхоспазма, аллергическая экзантема.
Увеличение печени и селезенки выявляется позднее, чем при других видах инфекции, — на 7-10-й день болезни, что затрудняет раннюю диагностику. Анемия развивается рано и быстро прогрессирует, сопровождаясь желтушностью южных покровов.
Частыми проявлениями Р. falciparum-малярии являются олигурия, альбуминурия, микрогематурия и цилиндрурия, которые обычно купируются этиотропными средствами. У многих больных определяется клинико-биохимический комплекс симптомов острого гепатита.
В случае несвоевременной диагностики и неадекватной терапии у неиммунных лиц в течение первых 5-7 дней болезни часто развиваются шок, малярийная кома, острая почечная недостаточность, острый массивный гемолиз, гемоглобинурия, геморрагический синдром и другие тяжелые осложнения.
Коматозная Р. falciparum-малярия характеризуется стадийным развитием клинической картины. Вначале больные отмечают интенсивную и усиливающуюся головную боль, головокружение, повторную рвоту. Наблюдаются вялость, выраженная психическая истощаемость и сонливость больного (стадия сомноленции). Спустя несколько часов может развиться сопорозная стадия, в которой сознание больных может быть спутанным, возникают судороги, отмечаются оживление рефлексов и появление патологических рефлексов, явления менингизма.
При отсутствии терапии развивается глубокая кома с арефлексией, артериальной гипотензией, прогрессирующей одышкой, парезом сфинктеров Прогноз в таких случаях часто неблагоприятный, но адекватная терапия в период сомноленции и сопора может обеспечить выздоровление большей части больных.
Острая почечная недостаточность при Р. falciparum-малярия обычно развивается в конце 1-й или в начале 2-й недели болезни и характеризуется прогрессирующей олигурией и анурией, азотемией, гиперкалиемией. В моче обнаруживаются высокое содержание белка, эритроциты, лейкоциты, гиалиновые и зернистые цилиндры. Острая почечная недостаточность часто сочетается с другими видами осложнений. Своевременная этиотропная терапия обеспечивает хороший купирующий эффект.
Тяжелым осложнением P. falciparum-малярии является гемоглобинурия, возникающая как в результате острого внутрисосудистого гемолиза вследствие массивной инвазии, так и (наиболее часто) в результате использования хинина, примахина, сульфаниламидных препаратов у лиц с дефицитом Г-6-ФДГ. В зависимости от степени гемолиза у больных остро повышается температура тела, возникают боли в поясничной области, олиго- и анурия с отделением скудной мочи почти черного цвета (за счет оксигемоглобина в свежей моче) или цвета красного вина (за счет метгемоглобина в постоявшей моче).
При отстаивании моча разделяется на два слоя: верхний — прозрачный, темно-вишневого цвета и нижний — мутный, с большим количеством детрита. Отмечается быстрое развитие и прогрессирование желтухи и анемии. В дальнейшем может развиться острая почечная недостаточность с неблагоприятным прогнозом. Как правило, гемоглобинурия развивается при массивной паразитемии, однако ввиду первоочередного разрушения инвазированных эритроцитов в препаратах толстой капли и мазках крови паразиты могут обнаруживаться с трудом, что усложняет распознавание болезни и может приводить к диагностическим ошибкам.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
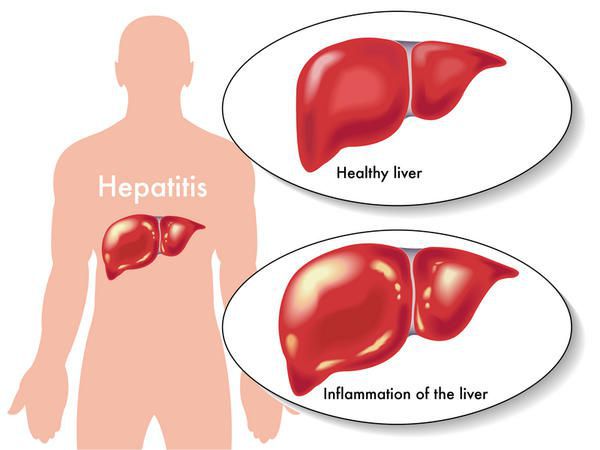
Этиология
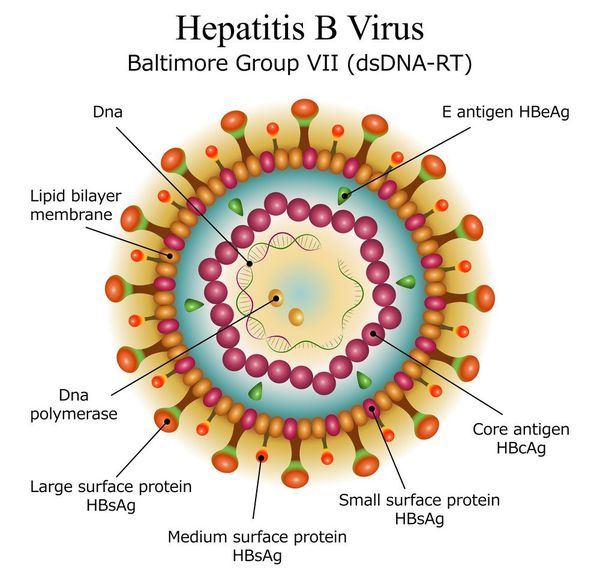
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
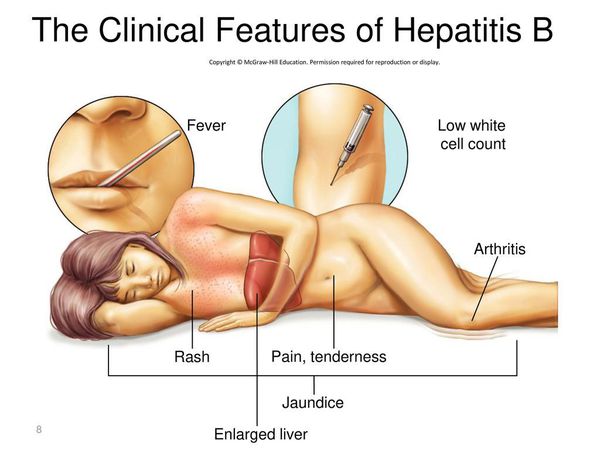
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
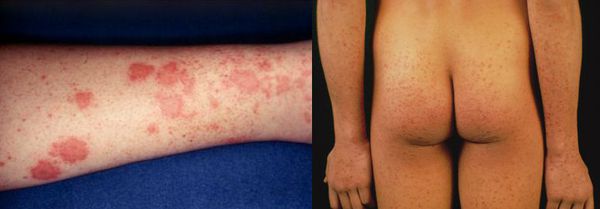
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
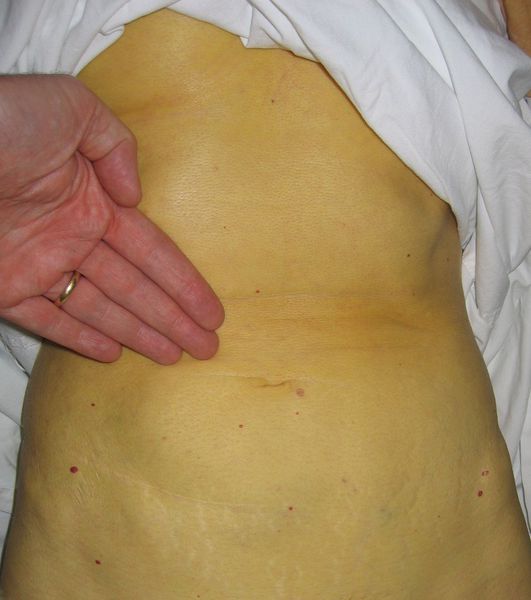
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
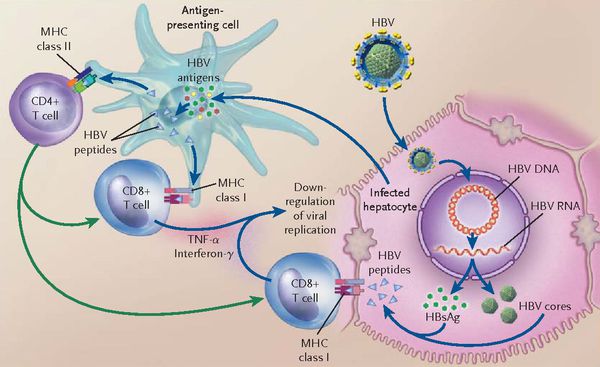
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Что такое синдром Жильбера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Синдром Жильбера — это генетический пигментный гепатоз с аутосомно-доминантным типом наследования, протекающий с повышением уровня неконъюгированного (свободного) билирубина, чаще проявляющееся в период полового созревания и характеризующийся доброкачественным течением [1] .
Краткое содержание статьи — в видео:
Синонимы названия болезни: простая семейная холемия, конституциональная или идиопатическая неконъюгированная гипербилирубинемия, негемолитическая семейная желтуха.
По распространённости данное заболевание встречается не менее, чем у 5 % населения, в соотношении мужчин и женщин — 4:1. Впервые заболевание описал французский терапевт Августин Жильбер в 1901 году.
Чаще синдром Жильбера проявляется в период полового созревания и характеризуется доброкачественным течением. Основным проявлением этого синдрома является желтуха.
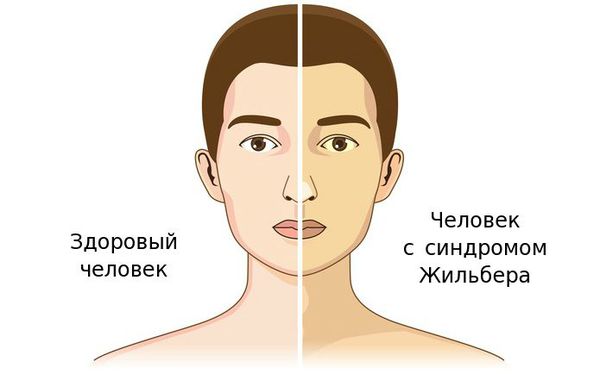
К провоцирующим факторам проявления синдрома можно отнести:
- голодание или переедание;
- жирную пищу;
- некоторые лекарственные средства;
- алкоголь;
- инфекции (грипп, ОРЗ, вирусный гепатит);
- физические и психические перегрузки;
- травмы и оперативные вмешательства.
Причина заболевания — генетический дефект фермента УДФГТ1*1, который возникает в результате его мутации. В связи с этим дефектом функциональная активность данного фермента снижается, а внутриклеточный транспорт билирубина в клетках печени к месту соединения свободного (несвязанного) билирубина с глюкуроновой кислотой нарушается. Это и приводит к увеличению свободного билирубина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Жильбера
Некоторые специалисты трактуют синдром Жильбера не как болезнь, а как физиологическую особенность организма.
До периода полового созревания данный синдром может протекать бессимптомно. Позже (после 11 лет) возникает характерная триада признаков:
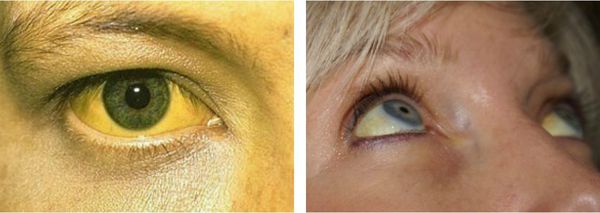
- желтуха различной степени выраженности;
- ксантелазмы век (жёлтые папулы);
- периодичность появления симптомов [1] .
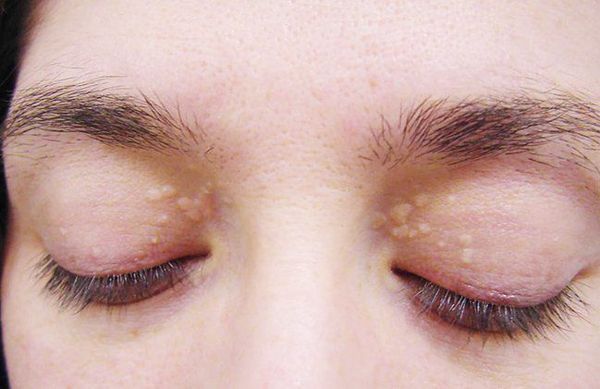
Желтуха чаще всего проявляется иктеричностью (желтушностью) склер, матовой желтушностью кожных покровов (особенно лица), иногда частичным поражением стоп, ладоней, подмышечных впадин и носогубного треугольника.
Заболевание нередко сочетается с генерализованной дисплазией (неправильным развитием) соединительной ткани.
Усиление желтухи может наблюдаться после перенесения инфекций, эмоциональной и физической нагрузки, приёма ряда лекарственных препаратов (в частности, антибиотиков), голодания и рвоты.
Клиническими проявлениями заболевания общего характера могут быть:
- слабость;
- недомогание;
- подавленность;
- плохой сон;
- снижение концентрации внимания.
В отношении ЖКТ синдром Жильбера проявляется снижением аппетита, изменением привкуса во рту (горечь, металлический привкус), реже возникает отрыжка, тяжесть в области правого подреберья, иногда наблюдается боль ноющего характера и плохая переносимость лекарственных препаратов.
При ухудшении течения синдрома Жильбера и существенном повышении токсичной (свободной) фракции билирубина может появляться скрытый гемолиз, усиливая при этом гипербилирубинемию и добавляя в клиническую картину системный зуд.
Патогенез синдрома Жильбера
В норме свободный билирубин появляется в крови преимущественно (в 80-85 % случаев) при разрушении эритроцитов, в частности комплекса ГЕМ, входящего в структуру гемоглобина. Это происходит в клетках макрофагической системы, особенно активно в селезёнке и купферовских клетках печени. Остальная часть билирубина образуется из разрушения других гемсодержащих белков (к примеру, цитохрома P-450).
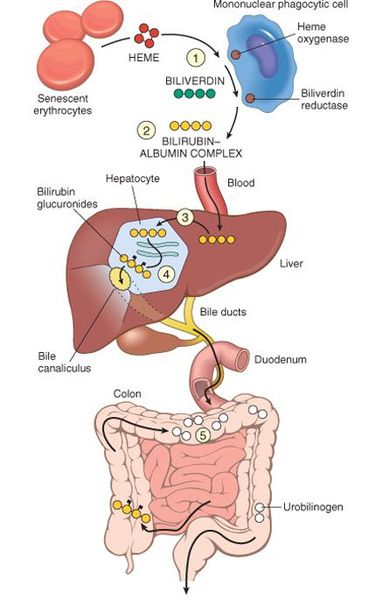
У взрослого человека в сутки образуется приблизительно от 200 мг до 350 мг свободного билирубина. Такой билирубин слаборастворим в воде, но при этом хорошо растворяется в жирах, поэтому он может взаимодействовать с фосфолипидами ("жирами") клеточных мембран, особенно головного мозга, чем можно объяснить его высокую токсичность, в частности токсичное влияние на нервную систему.
Первично после разрушения комплекса ГЕМ в плазме билирубин появляется в неконъюгированной (свободной или несвязанной) форме и транспортируется с кровью при помощи белков альбуминов. Свободный билирубин не может проникнуть через почечный барьер за счёт сцепления с белком альбумином, поэтому сохраняется в крови.
В печени несвязанный билирубин переходит на поверхность гепатоцитов. С целью снижения токсичности и выведения в клетках печени свободного билирубина при помощи фермента УДФГТ1*1 он связывается с глюкуроновой кислотой и превращается в конъюгированный (прямой или связанный) билирубин. Конъюгированный билирубин хорошо растворим в воде, он является менее токсичным для организма и в дальнейшем легко выводится через кишечник с желчью.
При синдроме Жильбера связывание свободного билирубина с глюкуроновой кислотой снижается до 30% от нормы, тогда как концентрация прямого билирубина в желчи увеличивается.
В основе синдрома Жильбера лежит генетический дефект — наличие на промонторном участке A(TA)6TAA гена, кодирующего фермент УДФГТ1*1, дополнительного динуклеотида ТА. Это становится причиной образования дефектного участка А(ТА)7ТАА. Удлинение промонторной последовательности нарушает связывание фактора транскрипции IID, в связи с чем уменьшается количество и качество синтезируемого фермента УДФГТ1, который участвует в процессе связывания свободного билирубина с глюкуроновой кислотой, преобразуя токсичный свободный билирубин в нетоксичный связанный.
Вторым механизмом развития синдрома Жильбера является нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой, которая доставляет свободный билирубин к микросомам клеток печени.
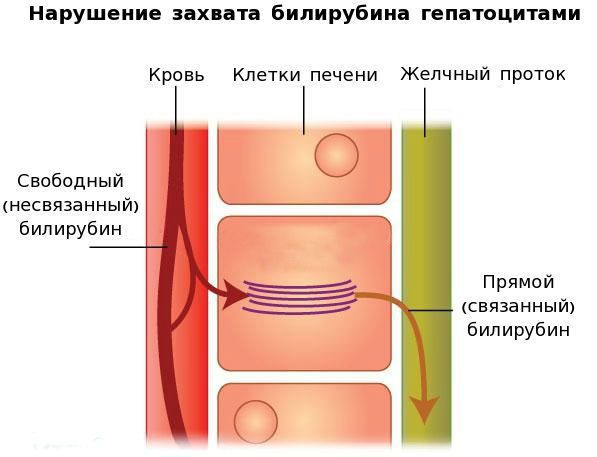
В конечном итоге вышеперечисленные патологические процессы приводят к увеличению содержания свободного (несвязанного) билирубина в плазме, что обуславливает клинические проявления заболевания [6] .
Классификация и стадии развития синдрома Жильбера
Общепринятой классификации синдрома Жильбера не существует, однако условно можно разделить генотипы синдрома по полиморфизму.
Малярия (от лат. mala aria - плохой воздух) - острое или хроническое рецидивирующее инфекционное заболевание, имеющее различные клинические формы в зависимости от срока созревания возбудителя; характеризуется лихорадочными пароксизмами, гипохромной анемией, увеличением селезенки и печени.
Этиология и патогенез
Заболевание вызывается несколькими видами простейших рода Plasmodium (впервые плазмодий малярии был обнаружен в эритроцитах А. Лавераном в 1880 г.). Попав в кровь при укусе комара, плазмодии проделывают сложный цикл развития, паразитируют в эритроцитах человека, размножаясь бесполым путем, который называют шизогонией. Шизонты паразита накапливают в цитоплазме частицы темно-бурого пигмента - гемоме-ланина. При гемолизе паразиты и гемомеланин высвобождаются из эритроцита, причем пигмент фагоцитируется клетками макрофагальной системы, а шизонты вновь внедряются в эритроциты. В связи с этим развиваются надпеченочная (гемолитическая) анемия, гемомеланоз и гемосидероз элементов ретикуло-эндотелиальной системы, завершающийся склерозом. В периоды гемолитических кризов появляются острые сосудистые расстройства (стаз, диапедезные кровоизлияния). В связи с персистирую-щей антигенемией при малярии в крови появляются токсические иммунные комплексы. С их воздействием связано поражение микроциркуля-торного русла (повышение проницаемости, геморрагии), а также развитие гломерулонефрита.
Патологическая анатомия
В связи с существованием нескольких видов малярийного плазмодия, различающихся по срокам их созревания, выделяют трехдневную, четырехдневную и тропическую формы малярии. При трехдневной малярии, наиболее частой, в связи с разрушением эритроцитов развивается анемия, тяжесть которой усугубляется свойством плазмодиев трехдневной малярии поселяться в молодых эритроцитах - ретикулоцитах. Высвобождающиеся при распаде эритроцитов продукты, особенно гемомеланин, захватываются клетками макрофагальной системы, что приводит к увеличению селезенки и печени, гиперплазии костного мозга. Органы, загруженные пигментом, приобретают темно-серую, а иногда черную окраску. Селезенка увеличивается особенно быстро, вначале в результате полнокровия, а затем - гиперплазии клеток, фагоцитирующих пигмент. Пульпа ее становится темной, почти черной. В острой стадии малярии селезенка мягкая, полнокровная, в хронической - плотная вследствие развивающегося склероза; масса ее достигает 3-5 кг
Симптомы
При хронической малярии отмечаются огрубение стромы печени и разрастание в ней соединительной ткани. Костный мозг плоских и трубчатых костей имеет темно-серую окраску, отмечается гиперплазия его клеток и отложение в них пигмента. Встречаются участки аплазии костного мозга. Гемомеланоз органов гистиоцитарно-макрофагальной системы сочетается с их гемосидерозом. Развивается надпеченочная (гемолитическая) желтуха. Патологическая анатомия четырехдневной малярии подобна таковой при трехдневной малярии. При тропической малярии изменения, с одной стороны, имеют много общего с описанными при трехдневной форме, с другой - отличаются некоторыми особенностями. Они объясняются тем, что эритроциты, содержащие дозревающие шизонты тропической малярии, скапливаются в терминальных участках кровяного русла, что ведет к развитию паразитарных стазов. В местах скопления дозревающих шизонтов в период деления их на мерозоиты происходит фагоцитоз неитрофилами и макрофагами как зараженных эритроцитов и незрелых шизонтов, так и продуктов распада и пигмента, появляющихся после деления плазмодиев. С паразитарными стазами связаны опасные для жизни изменения головного мозга, которые определяют развитие малярийной комы. Кора и другие участки серого вещества головного мозга имеют в таких случаях темную коричнево-серую (дымчатую) окраску. В белом веществе встречаются многочисленные точечные кровоизлияния, которые окружают сосуды, заполненные агглютинированными эритроцитами с паразитами в цитоплазме или гиалиновыми тромбами. Вокруг таких сосудов, помимо кровоизлияний, появляются очаги некроза мозговой ткани. На границе некроза и кровоизлияния через 2 сут от начала комы находят реактивное разрастание клеток глии, что ведет к формированию своеобразных узелков - так называемых гранулем Дюрка.
Прогноз
Осложнением острой малярии может быть гломерулонефрит, хронической - истощение, амилоидоз.
Смерть наблюдается обычно при тропической малярии, осложненной комой.
Стадии малярийного приступа. Печень при малярии
Малярии свойственна смена периодов лихорадочных приступов и межприступного латента, когда исчезает лихорадка и смягчаются другие признаки болезни. При тропической малярии в межприступ-ном периоде ряд клинических проявлений может быть более выражен, чем при других формах малярии.
Наиболее характерным клиническим признаком малярии является лихорадка. Иногда периоду высокой лихорадки предшествуют недомогание, чувство слабости, разбитости, головные боли, нарушение аппетита и др. Лихорадочные приступы возникают после инкубационного периода в 8—10 дней при тропической, 10—14 дней при трехдневной (с короткой инкубацией) и 20—25 дней при четырехдневной малярии. В первые дни лихорадка может носить неправильный, ремиттирующий, иногда даже (при тропической малярии) постоянный характер. Эта так называемая начальная (инициальная) лихорадка наблюдается только при свежем первожизненном заболевании малярией. Через несколько дней устанавливается правильное чередование лихорадочных приступов и периодов нормальной температуры.
В малярийном приступе различают три стадии: периоды озноба, жара к пота. Выраженность озноба и пота у больного связана с быстротой подъема и снижения температуры. При мягком течении болезни, а также при тяжелой малярии с лихорадкой неправильного, постоянного или послабляющего типа озноби пот могут быть мало выражены, а иногда и совсем отсутствовать.
Малярийные приступы, как правило, возникают в первой половине суток, максимум температуры обычно приходится на утренние часы. Эта особенность служит дифференциально-диагностическим признаком малярийной лихорадки. Однако нужно помнить, что для трехдневной малярии, вызываемой P. ovale, характерны вечерние н ночные приступы, С началом снижения температуры и появлением сильного пота состояние больного постепенно улучшается, больной успокаивается и засыпает. Продолжительность приступа обычно не превышает 8— 12 часов. Иногда, особенно при переводе правильного типа лихорадки в ежедневный, приступы могут длиться больше суток.
При правильном чередовании малярийных приступов (при трехдневной малярии через день и четырехдневной через 2 дня) в дни, свободные от приступов, состояние больного может быть удовлетворительным, возвращается аппетит, работоспособность. Однако по мере нарастания количества приступов и в дни апирексии состояние больного может оставаться тяжелым. Более тяжелое течение наблюдается при ежедневных лихорадочных приступах, что часто имеет место при тропической малярии.
Вторым характерным признаком малярии является увеличение к болезненность печени и селезенки. Увеличение печени обычно определяется раньше; селезенка в свежих случаях малярии отчетливо увеличивается только после перенесения нескольких приступов малярии. Вместе с тем увеличение селезенки остается более длительно, чем увеличение печени. Последнее связано с тем, что печень увеличивается главным образом за счет повышенного кровенаполнения и в меньшей степени за счет прироста ретикуло-эндотелиальной ткани. Увеличение селезенки обусловлено не только гиперемией, но и гиперплазией.
Во время малярийного приступа печень и селезенка становятся особенно болезненными. Это связано с повышенным кровенаподнением и растяжением капсулы органов. Размеры печени й селезенки с каждым приступом увеличиваются. При затянувшемся лихорадочном периоде переполнение селезенки кровью и растяжение ее капсулы могут привести к разрыву селезенки. При правильном лечении размеры обоих органов быстро уменьшаются, причем печень сокращается быстрее селезенки.
Диффузное поражение печени при малярии встречается редко; исключительно редко возникает острая или подострая атрофия печени. Частота хронических поражении печени у населения эндемичных по малярии колониальных или развивающихся стран связана прежде всего с постоянным белковым голоданием, гельминтозами, гепатотропными вирусными инфекциями и др.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

