Патогенное действие гельминтов на организм человека
Обновлено: 23.04.2024
В статье представлены современные данные о ларвальных гельминтозах у детей, самым распространенным и трудно диагностируемым из которых является токсокароз, имеющий тяжелое хроническое течение с выраженным иммуносупрессивным эффектом и полиорганными пораже
The article represents the modern data on larva migrans in children, toxocariasis being the most widespread and difficultly diagnosed among them, with severe clinical course, pronounced immunosuppressing effect and multiple affections of organs. Pathogenesis, therapy and prevention of the disease are discussed.
Распространенность гельминтозов среди жителей различных континентов Земли огромна: на каждого жителя Африки приходится более двух видов гельминтов, в Азии и Латинской Америке более одного вида, в Европе поражен каждый третий житель. В России практически каждый человек в течение жизни переносит паразитарное заболевание, причем чаще страдают дети [1]. По величине ущерба, наносимого здоровью людей, гельминтозы занимают 4-е место после диареи, туберкулеза и ишемической болезни сердца. Ежегодно в мире от гельминтозов погибают 135 тыс. человек, причем число это неуклонно растет [2].
- санитарно-гигиенические — высокий уровень контаминации окружающей среды яйцами гельминтов в результате сброса необезвреженных сточных вод и стоков животноводческих комплексов; недостаточные гигиенические навыки населения, привычка удобрять почву экскрементами;
- миграционными — усилением миграции населения и завозом паразитарных болезней из эндемических стран, вторжением городского населения в сельскую местность (работа на садовых участках, дачах, личных фермах), рост числа бродячих животных;
- информационными — малая информированность населения, а порой и врачей о гельминтозах и путях их заражения, профилактика гельминтозов ограничена лишь лечением вновь выявленных случаев заболевания;
- этническими — особенности питания населения, а именно употребление сырой или слабообработанной продукции;
- экономическими — обеднение населения, удорожание лекарственных препаратов;
- экологическими — снижение общей иммунной реактивности.
В настоящее время известно около 270 видов гельминтов, паразитирующих в организме человека, из которых 30 широко распространены на территории России. Гельминты, паразитирующие у человека, относятся к типу плоских червей, среди которых различают два класса: Cestoidea — ленточные черви и Trematoda — сосальщики, и типу круглых червей (класс Nematoda — собственно круглые черви). В зависимости от места паразитирования в организме человека, гельминты подразделяются на просветные, к которым относится большинство патогенных для человека гельминтов, и тканевые. В тканях в свою очередь могут обитать как взрослые особи, так и личинки.
Гельминтозы, при которых основным патогеном являются личинки, мигрирующие или покоящиеся, называют личиночными или ларвальными [3]. Особенностью ларвальных гельминтозов является то, что человек в данной ситуации является промежуточным или случайным хозяином, а жизненный цикл паразита не завершается, личинка не превращается в половозрелую особь и не может дать потомство [4]. Следовательно, такой вид паразитирования является биологическим тупиком. К числу таких гельминтозов относят многие филяриозы, трихинеллез, гнатостомоз, капилляриоз, спарганоз, эхинококкозы, токсокароз и др.
В отсутствие этиологического диагноза, который поставить удается не всегда, этот вид гельминтозов обозначают обобщенным термином Larva migrans, под которым понимают симптомокомплекс, обусловленный паразитированием личинок гельминтов, для которых человек не является естественным хозяином [5–7]. В зависимости от пути проникновения и места паразитирования условно выделяют перкутанные, или кожные, и висцеральные формы. Возбудителями кожной формы являются шистосомы, анкилостомы, некоторые виды филярий. При этом личинки гельминтов проникают в неповрежденную кожу при контакте с водой или почвой, паразитируют в эпидермисе, дерме или гиподерме, а после самопроизвольной гибели личинки, через 1–6 месяцев, наступает полное выздоровление [8]. Это условно доброкачественные гельминтозы. Висцеральная форма, возбудителями которой являются эхинококки, токсокары, цистицерки и др., возникает при проглатывании человеком яиц гельминтов с водой, продуктами питания, частичками почвы и протекает зачастую тяжело, длительно, порой годами и, как правило, не заканчивается спонтанным выздоровлением. Прогноз у данной группы гельминтозов серьезный, вплоть до летального исхода [9].
Наиболее тяжело протекают ларвальные (личиночные) гельминтозы вследствие множественного поражения печени, легких, сердца, почек, головного мозга, органа зрения и др. (токсокароз, однокамерный эхинококкоз, цистицеркоз) или агрессивного роста и метастазов зародышей или яиц паразита (многокамерный эхинококкоз, парагонимоз). Кроме этого, обладая значительной антигенной чужеродностью, мигрирующие личинки вызывают тяжелую общую и местную аллергическую реакцию, вплоть до формирования в тканях эозинофильных гранулем, оказывают механическое и токсическое повреждение [10].
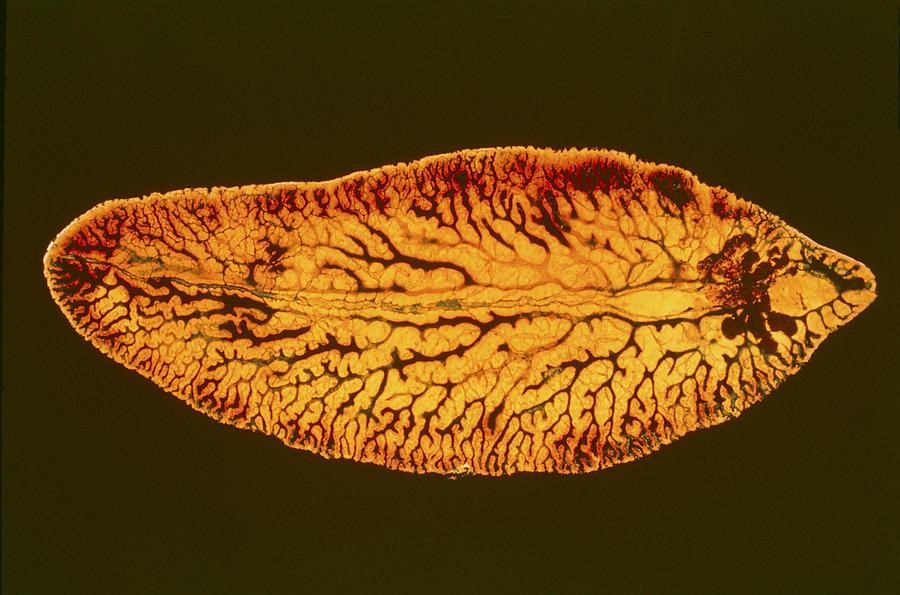
Для гельминтозов характерен широкий диапазон клинических симптомов: от слабовыраженных до генерализованных реакций с множественными поражениями. Именно такая неспецифичность, малоинформативность стандартных методик гельминтологического исследования на яйца глистов, в совокупности с традиционным отсутствием настороженности у городских практических врачей, побудили нас еще раз обратить внимание на эту проблему. Часто правильный диагноз скрывается за самыми разнообразными масками и распознается поздно (рис. 1).
.jpg)
Токсокароз является самым распространенным из ларвальных гельминтозов у детей, пораженность токсокарозом в странах умеренного пояса составляет от 2% до 37%, достигая 92,8% в тропических странах [11–14]. Токсокароз — это зоогельминтоз, имеющий тяжелое хроническое течение с выраженным иммуносупрессирующим эффектом и полиорганными поражениями. Возбудителем токсокароза является нематода из рода Toksokara. Наиболее известны Toksokara catis, паразитирующая в организме кошек, и Toksokara canis, паразитирующая в организме собак, волков, лисиц, песцов и других представителей семейства псовых [15, 16]. Самка Toksokara canis имеет длину 9–18 см, самец — 5–10 см. Взрослые паразиты локализуются в желудке и тонкой кишке окончательных хозяев. Средняя продолжительность жизни половозрелых особей составляет 4–6 мес, и каждая самка Toksokara canis откладывает более 200 тыс. яиц в сутки. Яйца выделяются незрелыми и через 5–8 дней инкубации в почве становятся инвазионными, сохраняя жизнеспособность и инвазивность до 10 лет. Кроме этого, широкому распространению токсокароза среди животных способствует совершенный механизм передачи возбудителя, при котором сочетаются прямой (заражение яйцами из окружающей среды), внутриутробный (заражение плода личинками через плаценту), трансмаммарный (передача личинок с молоком) пути передачи и заражение через резервуарных (паратенических) хозяев.
Основной источник опасности для человека — это домашние и бродячие собаки разного возраста. В настоящее время в Москве численность собак превышает 1 млн особей, которые ежедневно оставляют на ее территории около 270 тонн экскрементов, содержащих более 40 тысяч яиц токсокар в каждом грамме! Поэтому каждая вторая проба почвы детских площадок, скверов, парков и территорий вокруг жилых домов содержит яйца этих паразитов [17–20]. У детей заражению может способствовать геофагия, именно поэтому токсокарозом чаще болеют дети дошкольного возраста. Прямой контакт с собакой также может привести к заражению через шерсть, загрязненную почвой, содержащей зрелые яйца токсокар. Ребенок может заражаться круглогодично через загрязненные яйцами почву, продукты питания, воду, руки. Установлена роль тараканов в распространении токсокароза: они поедают значительное количество яиц токсокар и до 25% их выделяют в жизнеспособном состоянии в окружающую среду [21]. Группу риска составляют люди, по роду деятельности контактирующие с животными и почвой.
Человек служит паратеническим (резервуарным) хозяином, являясь для паразита биологическим тупиком, так как токсокары паразитируют у него только в личиночной стадии, не выделяясь в окружающую среду. После проглатывания человеком зрелых яиц, в проксимальном отделе тонкого кишечника из них выходят личинки, которые через слизистую оболочку проникают в кровоток, затем заносятся в печень и правую половину сердца. Попав в легочную артерию, личинки продолжают миграцию и переходят из капилляров в легочную вену, достигают левой половины сердца и затем разносятся кровью по разным органам и тканям. Мигрируя, они достигают места, где диаметр сосуда меньше размера самой личинки, и покидают кровяное русло. Личинки токсокар могут оседать абсолютно во всех органах и тканях, сохраняя жизнеспособность в течение длительного времени, периодически активизируясь и возобновляя миграцию. С течением времени часть личинок инкапсулируется и постепенно разрушается внутри капсулы.
Токсокароз имеет длительное, рецидивирующее течение [22]. Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека [23, 24]. В зависимости от преимущественной локализации личинок выделяют висцеральную и глазную формы токсокароза.
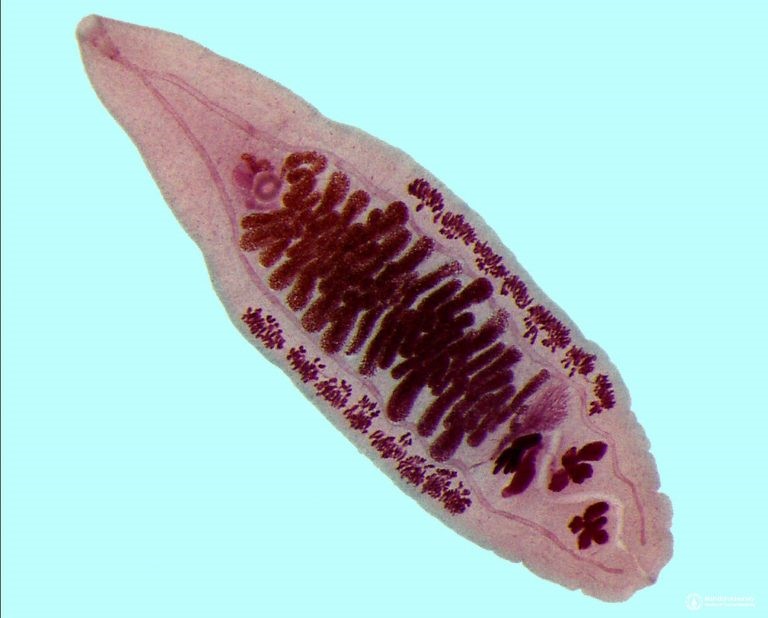
Висцеральный токсокароз встречается чаще как у детей, так и у взрослых и возникает в результате заражения большим числом личинок [25]. Клинические проявления острого токсокароза разнообразны (рис. 2).
Для больных токсокарозом наиболее характерна субфебрильная, реже — фебрильная лихорадка с пиком во второй половине дня, сопровождающаяся недомоганием и ознобом. Как правило, одновременно с лихорадкой выявляется синдром поражения легких, варьирующий в широких пределах: от катаральных явлений до тяжелых астмоидных состояний. Могут наблюдаться рецидивирующие бронхиты, бронхопневмонии вплоть до летального исхода. При рентгенологическом исследовании в этот период выявляются множественные или единичные эозинофильные инфильтраты, так называемый синдром Леффлера. Наряду с синдромом поражения легких часто отмечается увеличение размеров печени, а иногда и селезенки, сопровождающееся болями в животе, тошнотой, рвотой и диарей. Практически у всех больных выявляется лимфаденопатия. В отдельных случаях токсокароз сопровождается развитием аллергического миокардита, панкреатита, поражением почек [26]. Поражение кожи при токсокарозе встречается реже и отличается полиморфностью высыпаний: от эритем до пятнисто-папулезных и уртикарных элементов. Все чаще стали выявлять и поражение центральной нервной системы, которое может протекать в виде эписиндрома, гиперактивности, аффективной неустойчивости, трудностей в учебе. В тяжелых случаях регистрируется менингоэнцефалит, парезы, параличи, нарушения психики. Увязать такие явления непосредственно с токсокарозом весьма проблематично, однако в одном из сероэпидемиологических исследований, проведенном в 1984 г., показана связь затруднений при чтении, невозможности сосредоточиться и низкого уровня интеллекта с заболеванием дошкольников токсокарозом.
Золотым стандартом диагностики любого гельминтоза является паразитологический метод. Однако прижизненный паразитологический диагноз токсокароза практически невозможен, поскольку обнаружить мигрирующие личинки трудно, а идентифицировать их по гистологическим срезам весьма непросто [29].
Клиническо-анамнестическая диагностика токсокароза также затруднительна ввиду полиморфизма и неопределенности клинических проявлений. В повседневной клинической практике своевременная постановка диагноза и назначение специфической терапии — скорее исключение, чем правило. Для облегчения задачи в 1978 г. был предложен диагностический алгоритм (табл.).
При сочетании симптомов и признаков на сумму более 12 баллов целесообразно назначение иммунологической диагностики. В диагностике глазного токсокароза может помочь офтальмологическое обследование с обнаружением личинки в области диска зрительного нерва или в макулярной части.
Диагностика токсокароза на сегодняшний день основывается на лабораторных методах исследования [30]. Одним из постоянных проявлений висцеральной формы токсокароза является лейкоцитоз и стойкая длительная эозинофилия до 30–90%. Наблюдается также умеренная анемия, гиперпротеинемия, гипергаммаглобулинемия, высокий уровень IgE. При поражении печени отмечаются нарушения ее функции.
Наиболее информативными в диагностике токсокароза являются иммунологические методы, а именно определение титра специфических IgG-антител к Toksokara canis методом иммуноферментного анализа (ИФА), обладающим высокой чувствительностью и достаточной специфичностью при висцеральной локализации гельминта — 93,7% и 89,3% соответственно [31]. Установлена корреляция между клиническими проявлениями, тяжестью процесса и титpами антител. Титp специфических антител 1:800 и выше с большой степенью вероятности свидетельствует о заболевании, а титpы 1:200–1:400 — о носительстве токсокаp при висцеральном токсокаpозе и патологическом процессе пpи токсокаpозе глаза. За лицами с низкими титрами противотоксокарозных антител устанавливается диспансерное наблюдение и пpи появлении клинических признаков болезни рекомендуется проведение специфической терапии. Однако необходимо помнить, что не всегда имеется прямая корреляция между титром антител и тяжестью заболевания, так как токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного. Кроме того, возможны и ложные результаты исследования: ложноположительные могут наблюдаться у больных эхинококкозами, описторхозом (в острой фазе заболевания), миграционной фазой аскаридоза; ложноотрицательные — при токсокарозе глаз, первичном иммунодефиците, длительном течении гельминтоза.
До настоящего времени нет единой схемы специфической терапии токсокароза, базирующейся на научных данных. Обычно применяют противонематодозные препараты, действующие на личиночную стадию гельминтов — альбендазол и мебендазол; ивермектин и диэтилкарбамазин [32]. Все препараты активны в отношении мигрирующих личинок и недостаточно активны в отношении тканевых форм, находящихся в гранулемах. Самым часто используемым является мебендазол, назначаемый в дозе 200–300 мг/сут в 2–3 приема, внутрь, в течение 10–14 дней. Повторный курс проводят через 2 недели. Диэтилкарбамазин назначают в дозе 3–4 мг/кг/сут в 2 приема, внутрь, в течение 21 дня. Однако наиболее широким спектром действия обладает альбендазол, эффективный в отношении большинства кишечных нематодозов и ларвальных цестодозов. Механизм действия альбендазола связан с избирательным подавлением полимеризации бета-тубулина, что ведет к деструкции цитоплазматических микроканальцев клеток кишечного тракта гельминтов. Назначается альбендазол в дозе 10 мг/кг/сут в два приема, внутрь, после еды в течение 10–14 дней. Необходимость повторного курса устанавливается после клинико-лабораторного обследования больного. Побочные явления, возникающие при применении вышеуказанных препаратов, могут быть связаны не только с токсическим действием антигельминтных препаратов, но и с реакцией организма на массовую гибель личинок токсокар. Поэтому в процессе лечения целесообразно назначать антигистаминные препараты, а в ряде случаев и кортикостероиды.
При глазном токсокарозе гранулемы удаляют микрохирургическими методами, для разрушения личинок в средах глаза применяют лазерокоагуляцию [33]. При бессимптомном течении с низкими титрами специфических антител лечение не проводится, а за больными устанавливается динамическое наблюдение.
Критериями эффективности лечения считают постепенное снижение и ликвидацию клинических проявлений токсокароза, уменьшение уровня эозинофилов и специфических антител. Вместе с тем исследования показывают, что в результате лечения процесс снижения уровня специфических антител идет медленно и не охватывает всех пациентов. Клинический эффект от лечения опережает гематологический и иммунологический. При рецидивах симптоматики, сохранении стойкой эозинофилии или повышении титра специфических антител проводят повторные курсы, иногда до 4–5.
Диспансерное наблюдение за переболевшими проводит врач-инфекционист или педиатр на протяжении не менее 6 месяцев. Больные подлежат осмотру 1 раз в 2 месяца и снимаются с учета после 2-кратного отрицательного результата на антитела методом ИФА с интервалом в 3–4 месяца. Прогноз в большинстве случаев благоприятный.
Основную роль в контроле заболеваемости токсокарозом играет традиционная профилактика, которая включает в себя соблюдение правил личной гигиены, обязательное обучение детей санитарным навыкам, своевременную дегельминтизацию собак, оборудование мест выгула собак, повышение культурного уровня владельцев собак [34].
Литература
А. С. Боткина 1 , кандидат медицинских наук
М. И. Дубровская, доктор медицинских наук, профессор
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гельминтоз (глистная инвазия): причины появления, симптомы, диагностика и способы лечения.
Определение
Гельминтозы - болезни человека, животных и растений, вызываемые паразитическими червями (гельминтами).
Причины появления гельминтозов
В настоящее время в России встречается более 70 видов из известных 250 гельминтов, паразитирующих в организме человека. Наиболее распространены круглые черви (аскариды, острицы, трихинеллы, власоглав), ленточные черви (свиной, бычий и карликовый цепни, широкий лентец, эхинококки), сосальщики (печеночная и кошачья двуустки).
Заражение гельминтами чаще всего происходит после попадания в организм их яиц и/или личинок. В зависимости от механизма заражения и путей передачи гельминтозы подразделяются на: геогельминтозы, биогельминтозы и контактные гельминтозы. Геогельминты развиваются без промежуточных хозяев, биогельминты - с последовательной сменой одного-двух-трех хозяев, контактные гельминты передаются контактным путем.
Свиной цепень, бычий цепень, эхинококк и другие виды червей развиваются с последовательной сменой одного-двух-трех хозяев. Промежуточными хозяевами могут быть рыбы, моллюски, ракообразные, насекомые. Человек заражается этими гельминтами, употребляя в пищу продукты, не прошедшие полноценную термическую обработку:
- мясо говядины, инфицированную финнами (личинками) бычьего цепня;
- свинину, пораженную финнами свиного цепня;
- малосоленую и сырую рыбу с личинками описторхиса или широкого лентеца;
- сырую воду или обработанные этой водой овощи, фрукты.
Контактным путем - то есть при личном контакте здорового человека с зараженным, при пользовании общей посудой, предметами туалета, бельем, при вдыхании пыли в помещении, где находится зараженный человек - передаются энтеробиоз (возбудитель – острица) и гименолепидоз (возбудитель – карликовый цепень). В случае энтеробиоза часто случается самозаражение.
Гельминты определенного вида паразитируют в определенных органах, вызывая различные гельминтозы:
- в толстой кишке - свиной, бычий, карликовый цепни, нематоды (анкилостомы, аскариды, стронгилоиды), острицы, власоглав. Из просвета кишки личинки свиного цепня могут попадать в кровоток и распространяться по организму, оседая в жировой клетчатке, сосудах мышц, камерах глаза, мозге;
- в печени и желчных путях - трематоды (описторхис, клонорхис, фасциола). В печени первично располагаются эхинококковые кисты, а после их разрыва дочерние пузыри можно обнаружить в брыжейке, листках брюшины, селезенке и других органах;
- в органах дыхания - эхинококки, альвеококки, легочные сосальщики, вызывающие парагонимоз;
- в нервной системе - шистосомозы, парагонимоз, эхинококкоз и альвеококкоз;
- в органах зрения - онкоцеркоз, лоаоз, осложненные формы тениоза;
- в органах кровообращения - некатороз, шистосомозы, дифиллоботриоз;
- в лимфатической системе - филяриатозы, трихинеллез;
- в коже и подкожной клетчатке - анкилостомидоз, онкоцеркоз, лоаоз, личиночная стадия шистосомозов;
- в костной системе - эхинококкоз;
- в скелетной мускулатуре - трихинеллез, цистицеркоз мышечной ткани.
Срок жизни гельминтов в организме окончательного хозяина может быть различным, зависит от вида паразита и колеблется от нескольких недель (острицы) до нескольких лет (цепни) и десятилетий (фасциолы).
Классификация заболевания
У человека паразитируют черви двух видов:
- Nemathelminthes – круглые черви, класс Nematoda;
- Plathelminthes – плоские черви, которые включают в себя классы
- Cestoidea – ленточных червей,
- Trematoda – класс сосальщиков.
- биогельминтозы;
- геогельминтозы;
- контактные гельминтозы.
На организм человека гельминты оказывают различное воздействие:
- антигенное воздействие, когда развиваются местные и общие аллергические реакции;
- токсическое действие (продукты жизнедеятельности гельминтов вызывают недомогание, слабость, диспепсические явления);
- травмирующее действие (при фиксации паразитов к стенке кишечника происходит нарушение кровоснабжения с некрозом и последующей атрофией слизистой оболочки; могут нарушаться процессы всасывания; механическое сдавление тканей гельминтами);
- вторичное воспаление в результате проникновение бактерий вслед за мигрирующими личинками гельминтов;
- нарушение обменных процессов;
- в результате поглощения крови некоторыми гельминтами возникает анемия;
- нервно-рефлекторное влияние - раздражение гельминтами нервных окончаний провоцирует бронхоспазм, дисфункцию кишечника и т.д.;
- психогенное действие, проявляющееся невротическими состояниями, нарушением сна;
- иммуносупрессивное действие.
Для гельминтозов характерна стадийность развития. Каждая стадия характеризуется своими клиническими симптомами.
Жалобы пациентов в острой стадии:
- повышение температуры от нескольких дней до двух месяцев (субфебрильная или выше 38ºС, сопровождающаяся ознобом, резкой слабостью и потливостью);
- зудящие рецидивирующие высыпания на коже;
- локальные или генерализованные отеки;
- увеличение регионарных лимфатических узлов;
- боли в мышцах и суставах;
- кашель, приступы удушья, боль в грудной клетке, длительные катаральные явления, бронхит, трахеит, симптомы, симулирующие пневмонию, астматический синдром, кровохарканье;
- боль в животе, тошнота, рвота, расстройства стула.
Для кишечных гельминтозов характерны следующие синдромы:
- диспепсический (дискомфорт в животе, чувство переполнения после еды, раннее насыщение, вздутие живота, тошнота);
- болевой;
- астеноневротический (чувство сильной усталости, повышенная нервная возбудимость и раздражительность).
Кишечные цестодозы (тениаринхоз, дифиллоботриоз, гименолепидоз, тениоз и другие) протекают бессимптомно или с малым количеством симптомов (с явлениями диспепсии, болевым синдромом, анемией).
Трематодозы печени (фасциолез, описторхоз, клонорхоз) вызывают:
- хронический панкреатит;
- гепатит;
- холецистохолангит;
- неврологические нарушения.
Мочеполовой шистомоз проявляется появлением в самом конце мочеиспускания крови, частыми позывами к мочеиспусканию, болью во время мочеиспускания.
Альвеококкоз, цистицеркоз, эхинококкоз могут длительное время протекать бессимптомно. На позднем этапе нагноение или разрыв кист, содержащих паразитов, приводит к анафилактическому шоку, перитониту, плевриту и другим тяжелейшим последствиям.
Для заболеваний, обусловленных паразитированием мигрирующих личинок зоогельминтов, когда человек не является естественным хозяином, различают кожную и висцеральную формы. Кожная форма обусловлена проникновением под кожу человека некоторых гельминтов животных: шистосоматид водоплавающих птиц (трематоды), анкилостоматид собак и кошек, стронгилид (нематоды). При контакте человека с почвой или водой личинки гельминтов проникают в кожу. Возникает чувство жжения, покалывания или зуда в месте внедрения гельминта. Может наблюдаться кратковременная лихорадка, признаки общего недомогания. Через 1-2 недели (реже 5-6 недель) наступает выздоровление.
Висцеральная форма развивается в результате заглатывания яиц гельминтов с водой и пищевыми продуктами. В начале заболевания может быть недомогание, аллергическая экзантема (кожная сыпь). В кишечнике человека из яиц гельминтов выходят личинки, которые проникают через кишечную стенку в кровь, достигают внутренних органов, где растут и достигают 5-10 см в диаметре, сдавливают ткани и нарушают функцию органов. При расположении личинок цепней (цистицерки, ценура) в оболочках и веществе головного мозга наблюдается головная боль, признаки церебральной гипертензии, парезы и параличи, эпилептиформные судороги. Личинки также могут располагаться в спинном мозге, глазном яблоке, серозных оболочках, межмышечной соединительной ткани и др.
Исходом гельминтозов может быть полное выздоровление с ликвидацией гельминтов или развитие необратимых изменений в организме хозяина.
Диагностика гельминтоза
Диагноз гельминтоза устанавливается на основании совокупности жалоб, полученных от пациента сведений о течении болезни, данных лабораторных и инструментальных методов обследования.В острой фазе гельминтозов имеется реакция крови на присутствие гельминта в организме, поэтому рекомендованы следующие исследования:
-
клинический анализ крови: общий анализ, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов);
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Для цитирования: Бронштейн А.М., Малышев Н.А. Гельминтозы органов пищеварения: кишечные нематодозы, трематодозы печени и ларвальные цестодозы (эхинококкозы). РМЖ. 2004;4:208.ММА имени И.М. Сеченова
Клиническая инфекционная больница № 1, Москва
Г ельминтозы широко распространены среди населения земного шара. Наиболее часто встречаются гельминтозы органов пищеварения, которыми, по оценкам Всемирной Организации Здравоохранения инфицирована четвертая часть населения Земли.Патогенное воздействие гельминтов на организм человека связано не только с патологией тех органов, где они локализуются (табл. 1,2), но и с общим воздействием на организм человека. При гельминтозах отмечается уменьшение выработки инсулин–подобного фактора роста (IGF–1) и увеличение фактора некроза опухоли- a (TNT- a ), а также уменьшение синтеза коллагена, что способствует снижению аппетита, уменьшению процессов всасывания в кишечнике, задержке роста и отставанию в умственном и физическом развитии. Существенное значение имеет также хроническая постоянная микрокровопотеря, в частности, из кишечника при анкилостомидозах и через желчные протоки при трематодозах печени, при которых также происходит и потеря с желчью аминокислот [3,6,7].
Новые данные, полученные группой авторов, показали, что кишечные гельминты способствуют высвобождению Th2 цитокинов, которые подавляют цитокины Th1, в связи с чем лица, инвазированные гельминтозами, более подвержены инфицированию, в частности, заболеванию туберкулезом после инфицирования M. tuberculosis. В связи с широким распространением штаммов M. tuberculosis, резистентных к антибиотикам, эти наблюдения подтверждают необходимость более активных мероприятий по борьбе с гельминтозами, распространенными в регионах, где среди населения высокий уровень пораженности туберкулезом. [2].
В наибольшей степени патогенное влияние гельминтозов отражается на беременных и детях из бедных слоев населения с неполноценным питанием. Инвазии ведут к снижению трудовой деятельности в старших возрастах и в целом наносят существенный медико–социальный и экономический ущерб.
Для Российской Федерации в этом отношении наиболее неблагополучными являются эндемичные по гельминтозам регионы Сибири и Дальнего Востока, где среди коренных народностей отмечается высокий уровень пораженности гельминтозами органов пищеварения (описторхоз, дифиллоботриоз, клонорхоз, метагонимоз, нанофиетоз, эхинококкозы) и туберкулезом на фоне широкого распространения алкоголизма и алкогольной патологии. Под действием комплекса экстремальных климато–метеорологических условий этих регионов патогенное влияние вышеуказанных факторов существенно усиливается.
Клинические проявления паразитозов характеризуются, как правило, неспецифичностью клинической симптоматики, хроническим течением с относительно медленным нарушением функции различных органов и систем за счет кумулятивного эффекта, часто латентным течением с субклиническими проявлениями болезни. Указанные особенности маскируют их негативный эффект и создают впечатление слабой патогенности по сравнению с другими заболеваниями. Наиболее часто паразиты обитают в органах пищеварения (табл.1,2) и имитируют заболевания этих органов. Поэтому наблюдаемые в клинической практике расстройства со стороны желудочно–кишечного тракта могут являться в ряде случаев замаскированными формами паразитарных болезней.
Клинические проявления паразитарных болезней органов пищеварения в начальных стадиях болезни обычно проявляются неспецифической неврологической симптоматикой – повышенная слабость, утомляемость, раздражительность, плохой сон. В дальнейшем, по мере увеличения длительности болезни развиваются симптомы, свидетельствующие о заболеваниях органов пищеварения: снижение аппетита, тошнота, боли в животе, неустойчивый стул.
Стоимость разработки новых лекарственных средств за последние десятилетия значительно возросла, и фармацевтические фирмы не относят работы по созданию новых антигельминтиков к числу приоритетных, поскольку в центре их внимания находятся другие заболевания. Ситуация с разработкой новых препаратов усугубляется тем, что паразитарные заболевания распространены в странах с низким социально–экономическим уровнем развития. В связи с этим фармацевтические фирмы не имеют достаточных экономических стимулов в исследованиях и производстве новых противопаразитарных препаратов.
Тем не менее за последние годы в результате синтеза новых препаратов роль химиотерапии в борьбе с некоторыми паразитарными заболеваниями значительно возросла и появилась реальная возможность в снижении заболеваемости путем проведения массовых химиотерапевтических мероприятий. Появившиеся за последние годы антигельминтики получены либо путем модификации известных соединений с антигельминтной активностью, либо в результате изучения новых классов химических соединений. В таблице 3 представлены наиболее широко используемые в настоящее время антигельминтики, спектр их действия и эффективность в отношении основных гельминтозов органов пишеварения.
Использование современных препаратов позволяет успешно лечить наиболее распространенные кишечные гельминтозы. Однако следует иметь в виду, что ни один из самых современных препаратов не может гарантировать 100% излечение после применения одного курса. Эффективность одного курса лечения обычно не превышает 90%, а полное излечение, как правило, достигается при повторных курсах.
В связи с наличием множества факторов, влияющих на эффективность лечения (высокая частота реинвазий, наличие географических штаммов, резистентных к стандартным схемам химиотерапии и др.), стандартные схемы (табл. 4) в ряде случаев требуют изменений с учетом опыта, накопленного в конкретном регионе.
Результаты многочисленных исследований, проведенных в различных регионах мира, свидетельствуют, что препаратом выбора для лечения большинства кишечных нематодозов является албендазол (Немозол) [4], а для лечения трематодозов – празиквантел [1].
Трематодозы печени. Существенную медико–социальную значимость для многих регионов мира составляют трематоды печени, относящиеся к семейству Opisthorchiidae (Opisthorchis felineus, Opisthorchis viverrini, Clonorchis sinensis), заражение которыми происходит при употреблении в пищу инвазированной рыбы (табл. 2). Ориентировочно трематодозами печени поражены около 17 млн. человек, а риску заражения подвержены 350 млн. жителей 13 стран [3]. Для населения России негативный эффект описторхоза усугубляется его преимущественным распространением в северных, в том числе приполярных районах, зонах нового промышленного освоения и проживания народностей Севера, где отмечается запаздывание социально–гигиенических мероприятий, относительно низкий уровень инфраструктуры здравоохранения, высокая детская смертность, распространены другие инфекционные заболевания, алкоголизм [1].
Особый аспект составляют паразитарно–онкологические ассоциации трематодозов печени с канцерогенезом. Например, в России наибольшая частота холангиокарциномы отмечается в интенсивных очагах описторхоза в Обь–Иртышском регионе. Развитие холангиокарциномы при трематодозах печени – многофакторный процесс, в котором паразиты играют роль стимуляторов злокачественного роста [5].
Основным патологическим процессом являются хронический пролиферативный холангит и каналикулит поджелудочной железы, сопровождающийся различной степенью фиброза этих органов. В ряде случаев течение болезни может быть тяжелым – с обструкцией желчных протоков, развитием желтухи, рецидивирующего холангита, абсцессов печени, острого панкреатита и желчного перитонита.
Лечение описторхоза и клонорхоза должно быть комплексным и наряду со специфическими препаратами включать патогенетическое лечение. В острой стадии при тяжелом течении проводится десенсибилизирующая и дезинтоксикационная терапия. Клиника хронической стадии обусловлена главным образом поражением органов дуоденохоледохопанкреатической зоны, и поэтому проводится комплексная терапия в соответствии с общими принципами лечения больных гастроэнтерологического профиля [1,3]. В настоящее время единственным средством для специфической терапии описторхоза и клонорхоза является празиквантел (табл. 3,4).
Эхинококкозы. Возбудителями эхинококкозов у человека являются гельминты семейства Taeniidae: Echinococcus granulosus и E. multilocularis. Инвазия E. granulosus вызывает у человека гидатидозный эхинококкоз, а инвазия E. multilocularis – альвеолярный эхинококкоз (альвеококкоз).
Гидатидозный эхинококкоз широко распространен во всем мире, особенно в странах Южной Америки, Средиземноморских странах, включая страны Европы, в ряде стран Азии и Северной Африки. В России и сопредельных государствах эхинококкоз регистрируется повсеместно.
Длительное время болезнь может протекать бессимптомно. Клинические проявления определяются локализацией, множественностью и размерами кист, а также возможными осложнениями в виде нагноения, разрывов, желтухи и др. Локализация эхинококковых кист возможна в любых органах, при этом нередко сочетание кист в различных органах у одного больного. Наиболее часто наблюдаются эхинококкоз печени. При сдавлении кистой крупных сосудов портальной системы и желчных протоков возможно развитие портальной гипертензии и механической желтухи. Одним из тяжелых осложнений является нагноение кисты и ее инфицирование. При распространении процесса на ткани печени может развиться гнойный холангит и абсцесс печени. Существенную опасность представляет разрыв кисты. Клиническая картина при перфорации кист определяется тем, в каком направлении и в какой орган произошел разрыв кисты. В этих случаях возможно развитие анафилактического шока, гнойного перитонита и плеврита, гнойного холангита, тампонады сердца. Разрывы кист ведут к диссеминации возбудителя и развитию вторичного множественного эхинококкоза.
Альвеококкоз, вызываемый E. multilocularis, регистрируется преимущественно в альпийских районах некоторых стран Европы. В России альвеококкоз встречается чаще в Якутии, Магаданской и Камчатской областях, а также в Красноярском крае, Новосибирской, Омской и Томской областях, в Поволжье, Хабаровском крае.
Особенностью E. multilocularis является инфильтративный рост и способность метастазировать. Наиболее часто первичные поражения отмечаются в правой доле печени, реже в левой. Альвеококкоз печени длительно, иногда многие годы протекает бессимптомно. Это обусловлено медленным ростом паразита. Клинические симптомы неспецифичны и определяются главным образом объемом и локализацией поражения. Наиболее частым осложнением альвеококкоза является механическая желтуха и портальная гипертензия. Вследствие способности к инфильтративному росту возможно прорастание альвеококка в близлежащие органы – диафрагму, почки, легкие, забрюшинное пространство и образование полостей распада в толще паразитарной опухоли. Также может отмечаться метастазирование в любые органы (чаще в легкие).
Лечение эхинококкозов проводится путем хирургического вмешательства и химиотерапии. В последние годы при гидатидозном эхинококкозе печени в случаях соответствующей локализации и относительно небольших размерах кист начали успешно применять дренирование эхинококковых кист путем чрескожной аспирации и обработки полости гипертоническим раствором с последующей химиотерапией.
Показания к консервативной терапии эхинококкозов: множественные поражения печени, легких и других органов, оперативное удаление которых сопряжено с высоким риском для жизни больного или технически невозможно, а также в качестве противорецидивного лечения, особенно показанного при разрыве эхинококковых кист.
Схемы химиотерапии эхинококкозов окончательно не разработаны. В настоящее время химиотерапия эхинококкозов проводится албендазолом. Используют различные схемы лечения албендазолом (Немозол): от 10 до 20 мг на 1 кг массы тела в сутки. Длительность одного непрерывного цикла лечения колеблется от 21 дней до нескольких лет; число циклов от 1 до 20 и более; интервалы между циклами от 21 до 28 дней или непрерывно в течение нескольких лет.
Эффективность лечения албендазолом гидатидозного эхинококкоза печени и легких колеблется от 41 до 72%; рецидивы отмечаются в среднем у 25%. Изменения в эхинококковых кистах (уменьшение размеров, кальцификация и др.) – относительно медленный процесс, и оценка эффективности лечения обычно возможна не ранее, чем через 6 мес.–1 год после завершения курса албендазола.
В процессе химиотерапии могут возникнуть осложнения, связанные со снижением жизнедеятельности и гибелью паразита: нагноение кист, спонтанные разрывы, возникновение полостей распада альвеолярного эхинококкоза с последующим абсцедированием. В связи с высокими дозами албендазола, используемыми для химиотерапии эхинококкозов, и длительностью курса лечения могут развиться осложнения, связанные с гепатотоксическим действием препарата – лейкопения и агранулоцитоз, токсический гепатит, лихорадка, алопеция и др., в ряде случаев ведущие к летальному исходу. Частота возникновения гепатоцеллюлярной токсичности при применения албендазола в дозе 10 мг/кг, по данным ряда авторов, достигает 15%.
Консервативное и хирургическое лечение эхинококкозов дополняет друг друга и требует индивидуального подхода. В частности, некоторым больным с хорошей эффективностью консервативной терапии может потребоваться хирургическое лечение осложнений, а другим – необходима консервативная терапия после успешного оперативного лечения.
Заключение. Всемирная Организация Здравоохранения сообщила о первых данных, свидетельствующих о возможности развития резистентности у кишечных нематод к антигельминтикам, в частности, при некаторозе к мебендазолу и при анкилостомозе – к пирантелу. Поэтому стратегия и тактика химиотерапии должны быть направлены на то, чтобы предотвратить развитие химиорезистентности. Должны назначаться наиболее эффективные антигельминтики и таким образом, чтобы риск развития химиорезистентности был минимальным. При назначении недостаточно эффективных препаратов в популяции гельминтов происходит отбор особей, имеющих резистентность к определенным препаратам или к группе препаратов сходной химической структуры. Идеальный антигельминтик должен быть высокоэффективным, хорошо переноситься больными и иметь низкую стоимость. Его антигельминтный спектр должен включать наиболее распространенные гельминтозы человека. В настоящее время этим требованиям соответствует и стал препаратом выбора для лечения гельминтозов органов пищеварения (кишечных нематодозов, трематодозов печени и ларвальных цестодозов) албендазол (Немозол), обладающий широким спектром действия и наиболее высокой эффективностью по сравнению с другими антигельминтиками, а также возможностью лечения большинства кишечных нематодозов путем назначения одной дозы.
1. Бронштейн А.М., Лучшев В.И. Трематодозы печени: описторхоз, клонорхоз. Русский мед. журнал 1998; 3(63): 140–148
2. Beyers A, Helden P., Beyers N. Cross–regulation of Th1 and Th2 responses. The Wellcome Trust Rev 1999; 48–52.
3. Control of foodborne trematode infections. WHO Techn Rep Ser,1995, N 849.
4. Horton J. Albendazole: a review of anthelmintic efficacy and safety in humans. Parasitology 2000; 121 Suppl: S 113 – 132
5. Schistosomes, liver flukes and Helicobacter pylori. Lyon, International Agency for Research on Cancer, 1994 (IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, Vol. 61).
6. Stephensen L.S. Optimising the benefits of anthelmintic treatment in children. Paediatr Drugs 2001; 3: 495 – 508.
7. Stephensen L.S., Holland C.V., Cooper E.S. The public health significance of Trichuris trichiura. Parasitology 2000; 121 Suppl: S 73 – 95
Контактный адрес:
Александр Маркович Бронштейн
127015, Москва, ул. Писцовая 10, ГКБ № 24
Тел/факс (095) 285–2669
![Гельминты: чем опасны черви-паразиты для человека?]()
Согласно данным ВОЗ, ежегодно каждый второй человек на планете заражается гельминтами. Многие думают, что паразитические черви не наносят особого вреда здоровью. Однако не все так просто: гельминты способны поражать важные внутренние органы: сердце, легкие, головной мозг.
Гельминты — кто они?
Гельми́нты — паразитические черви, которые в качестве хозяина могут выбирать организм человека, животного, растения. Всего существует три класса гельминтов:
- ленточные черви. Данный класс насчитывает около 3,5 тыс. видов гельминтов. Длина паразитических червей варьируется от нескольких мм до 10-15 метров;
- сосальщики. Паразиты получили такое названия за счет наличия у них присосок, при помощи которых они получают питательные вещества. Человеческий организм может поражать около 4 десятков видов сосальщиков. Как правило, длина червей не превышает 5 см;
- круглые черви. Этот класс гельминтов насчитывает более 24 тыс. видов. Круглые черви имеют веретенообразную форму. Обычно их длина составляет не более 0,5 метра.
Заразиться гельминтами можно различными путями. Однако чаще всего паразитарная инвазия происходит по следующим причинам:
- Несоблюдение гигиены рук.
- Немытые овощи, фрукты; недожаренные или недоваренные мясо, рыба — употребление таких продуктов увеличивает риск паразитарной инвазии многократно.
- Хранение продуктов вне холодильника открытыми. Насекомые способны переносить яйца гельминтов на продукты, которые хранятся без упаковки.
- Контакт с домашними животными.
Основные симптомы наличия паразитов в организме:
- тошнота, рвота, диарея;
- снижение веса;
- аллергические высыпания;
- вздутие живота;
- зуд в заднем проходе;
- скрип зубами во сне.
Более подробно о признаках наличия паразитов в организме читайте в нашей статье.
Какие гельминты чаще всего встречаются в России? Рассмотрим самые распространенные виды паразитарных червей и заболевания, которые они вызывают.
Ленточные черви
Тело ленточного червя состоит из членников, общее число которых колеблется от 3 до 5000. Главный элемент фиксации гельминта — головка, дополнительные — присоски, крючья.
Наиболее часто ленточные черви становятся причиной следующих заболеваний:
Дифиллоботриоз
Возбудитель заболевания — лентец широкий, который поражает кишечник человека. Развитие яиц червя происходит в пресных водоемах. Схема попадания лентеца в человеческий организм выглядит следующим образом:
- Яйца червя заглатывают рачки, которые обитают в водоеме.
- Зараженных рачков поедают рыбы.
- Человек заражается паразитом, употребляя рыбу, прошедшую недостаточную тепловую обработку.
Симптоматика заболевания развивается через 1,5 месяца после заражения. Основной признак патологии — наличие в кале белесых фрагментов гельминта.
Прикрепляясь к слизистой кишечника, лентец поглощает в большом количестве витамин В12. По этой причине у людей с дифиллоботриозом часто развивается анемия. Кроме этого, лентец может вызывать увеличение печени, селезенки, непроходимость кишечника.
Тениаринхоз
Возбудитель заболевания — бычий цепень, который преимущественно обитает в тонкой кишке человека. За свой цикл развития гельминт сменяет двух хозяев: промежуточным является крупный рогатый скот, основным — человек. Бычий цепень может в течение 20 лет обитать в организме, размножаясь и нанося вред здоровью. Болезнь распространена во многих регионах РФ, однако чаще всего встречается в районах Северного Кавказа.
Как правило, люди заболевают тениаринхозом после употребления недожаренной или недоваренной говядины.
Болезнь часто протекает без выраженных симптомов и выявляется случайно, когда человек видит в своем кале элементы гельминта. У некоторых людей, кроме основных признаков заражения гельминтами, может возникать болевой синдром в правой части передней брюшной стенки.
Взрослые гельминты способны проникать в аппендикс, проток поджелудочной железы, желчевыводящие пути, провоцируя в них острые воспалительные процессы. При множественной паразитарной инвазии может развиться непроходимость кишечника.
![ggg-3.jpg]()
Тениоз
Возбудитель заболевания — свиной цепень, который первоначально поражает тонкую кишку человека. В РФ наибольший рост заболеваемости среди населения наблюдается в районах, где распространено свиноводство. Это регионы, которые граничат с Украиной и Республикой Беларусь. Инфицирование человека происходит в результате потребления сырой или приготовленной ненадлежащим образом свинины.
Паразит может проникать в различные органы и ткани, вызывая болевой синдром в животе, спине, конечностях. Наиболее благоприятно патология протекает при локализации червя в подкожно-жировой клетчатке и скелетной мышечной ткани. При проникновении в глазные мышцы гельминты вызывают снижение остроты зрения, слезотечение, светобоязнь. Поражение свиным цепнем головного мозга может закончиться летальным исходом.
Сосальщики
Сосальщики имеют листовидную форму и отличаются высокой способностью к размножению в различные периоды жизненного цикла. Размножение червей возможно не только половым путем с оплодотворением, но и без него. Кроме присосок, черви имеют множество крючков и шипов, за счет которых они надежно прикрепляются к слизистым оболочкам органов.
![ggg-4.jpg]()
Распространенные патологии, вызываемые сосальщиками:
- фасциолез;
- описторхоз;
- парагонимоз.
Фасциолез
Фасциолез возникает при поражении печени или желчного пузыря печеночным сосальщиком. В основном заражение происходит при употреблении овощей, для полива которых использовали воду из открытых водоемов.
Кроме стандартных признаков заражения паразитами, у человека могут возникать астматические приступы, которые сопровождаются затрудненным дыханием, покраснением лица, расширением зрачков, тахикардией. Если взрослая особь вызвала непроходимость желчевыводящих протоков, то развивается механическая желтуха. Признаки патологии:
- схваткообразные боли в правом подреберье;
- пожелтение кожных покровов;
- лихорадка;
- бесцветные фекалии.
Описторхоз
Возбудитель болезни — кошачий сосальщик. Название паразита обусловлено тем, что кроме человека он часто поражает кошек и других млекопитающих, которые употребляют рыбу.
![ggg-5.jpg]()
Как правило, кошачий сосальщик поражает печень и поджелудочную железу, вызывая в органах воспалительные процессы. Симптоматика разнообразна и зависит от количества паразитов. У больного могут наблюдаться:
- симптомы интоксикации;
- лихорадка,
- крапивница;
- зуд кожи;
- боли в мышцах, суставах, правом подреберье.
В отдельных случаях гельминты вызывают увеличение лимфатических узлов, развитие желтухи. Хроническая форма патологии нередко приводит к гепатиту, циррозу печени.
Парагонимоз
Виновник заболевания — легочный сосальщик, который проникает в организм человека с зараженными ракообразными. В России очаги парагонимоза — реки Дальнего Востока.
Сначала паразит проникает в кишечник человека, далее — в брюшную полость. Конечная точка его путешествия — ткань легких. Кроме этого, червь способен проникать в головной мозг и поражать центральную нервную систему.
![ggg-6.jpg]()
Специфические признаки паразитарной инвазии легких:
- болевой синдром в грудной клетке;
- кашель с мокротой, в которой могут присутствовать гной и кровь;
- лихорадка.
В отдельных случаях гельминты вызывают нарушение вентиляционной функции легких и газообмена при дыхании.
Круглые черви
Благодаря своему строению, круглые черви (нематоды) способны выживать даже в экстремальных условиях. Их тело покрыто трехслойным кожно-мускульным мешком, который надежно защищает паразитов от внешних воздействий.
![ggg-7.jpg]()
Распространенные заболевания, вызываемые нематодами:
- аскаридоз;
- энтеробиоз;
- трихинеллез.
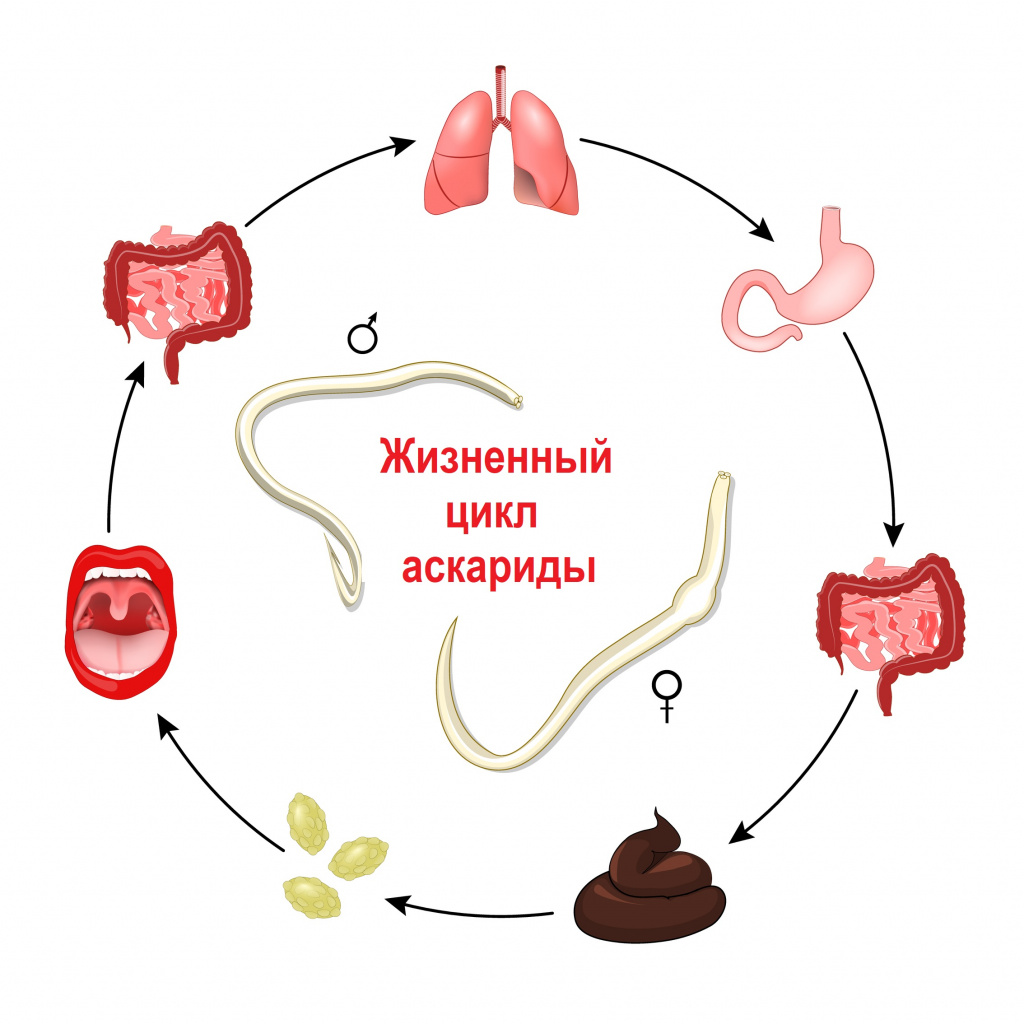
Аскаридоз
Развитие заболевания провоцирует аскарида, которая первоначально закрепляется в тонком кишечнике. Средняя длина взрослых особей составляет 40 см. Личинки паразита могут попасть в пищеварительную систему человека с немытыми овощами и фруктами, зараженной водой. Также нередко причиной аскаридоза становятся плохо вымытые перед едой руки.
Во время проникновения личинок в организм у человека могут наблюдаться субфебрильная температура, аллергические высыпания, кашель с выделением прозрачной мокроты. Признаки кишечной стадии аскаридоза (диарея, болевой синдром в животе) наблюдаются только при наличии нескольких паразитов. Как правило, обитание в кишечнике одного червя, протекает бессимптомно.
Осложнения при многочисленной паразитарной инвазии:
- закупорка желчного протока;
- гнойные воспалительные процессы в желчном пузыре, печени;
- воспаление аппендикса;
- кишечная непроходимость.
Энтеробиоз
Провокаторами заболевания являются острицы — небольшие черви длиной до 1 см. Гельминты проникают в пищеварительную систему человека также, как и аскариды.
![ggg-8.jpg]()
В настоящее время энтеробиоз является самой распространенной паразитарной патологией в мире. В основном заболевание диагностируется у детей в возрасте до 10 лет.
Симптоматика, как и в предыдущих случаях, развивается только при многочисленной паразитарной инвазии. У детей часто наблюдаются диарея, наличие в кале слизи, затрудненное и болезненное пищеварение, зуд в области ануса, тошнота. При тяжелом течении болезни могут возникать судороги конечностей. Кроме этого, острицы способны проникать в половые органы, вызывая в них острые воспаления.
Трихинеллез
Данное заболевание провоцирует трихинелла — один из самых маленьких паразитарных червей. Длина паразита редко превышает 4 мм. В личиночной стадии черви могут поражать скелетные мышцы. Исключением является миокард — мышечная ткань сердца. Взрослые особи паразитируют в тонкой кишке.
Как правило, заражение человека происходит при употреблении полусырой свинины. При этом для развития болезни достаточно употребить всего 30 г мяса, пораженного паразитами.
Патология проявляется стандартными симптомами паразитарной инвазии. В запущенной стадии могут возникнуть отечность век, лица, рук и ног, болевой синдром в пояснице, жевательных мышцах. Возможные осложнения — полное или частичная потеря подвижности, паралич дыхательных путей.
Как избежать заражения гельминтами?
Чтобы снизить риск заражения паразитическими червями, важно соблюдать следующие правила:
Читайте также: