Переносчиком возбудителей американского трипаносомоза является
Обновлено: 26.04.2024
Болезнь Шагаса, известная также как американский трипаносомоз, представляет потенциальную угрозу для жизни. Ее возбудителем является простейший паразит Trypanosoma cruzi (T. cruzi). Болезнь распространена, главным образом, в эндемичных районах 21 латиноамериканской страны 1 , где она передается людям, в основном, через фекалии клопов-триатоминов, известных под разными названиями в зависимости от географической области, в том числе и как "целующие клопы".
По оценкам, во всем мире инфицировано от 7 до 8 миллионов человек, преимущественно в Латинской Америке, где болезнь Шагаса является эндемической. В одной лишь Колумбии ежегодные расходы на медицинскую помощь всем пациентам с этой болезнью оцениваются примерно в 267 миллионов долларов США. Распыление инсектицидов для борьбы с переносчиками болезни обходилось бы ежегодно примерно в 5 миллионов долларов США.
Болезнь Шагаса названа именем Карлуса Рибейру Жустиниану Шагаса, бразильского врача, открывшего эту болезнь в 1909 году.
Распространение
Болезнь Шагаса распространена, в основном, в Латинской Америке. Однако в течение последних десятилетий она все больше обнаруживается в Соединенных Штатах Америки, Канаде, многих европейских странах и некоторых странах Западной части Тихого океана. Главным образом, это вызвано передвижением людей между Латинской Америкой и остальным миром. Реже инфицирование происходит в результате переливания крови, вертикальной передачи (от инфицированной матери ребенку) или пересадки органов.
Признаки и симптомы
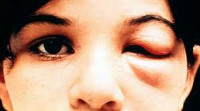
Болезнь Шагаса протекает в двух стадиях. Первая, острая, стадия длится около двух месяцев после инфицирования. В течение острой стадии в крови циркулирует большое количество паразитов. В большинстве случаев симптомы болезни отсутствуют или протекают в легкой форме, но они могут включать лихорадку, головную боль, увеличение лимфатических узлов, бледность, мышечную боль, затрудненное дыхание, отеки и боли в области живота и груди. Менее чем у 50% людей, укушенных клопом-триатомином, характерными первыми видимыми признаками могут быть поражения кожи или багровый отек век одного глаза.
На протяжении второй стадии паразиты концентрируются, в основном, в сердце или мускулатуре пищеварительного тракта. До 30% пациентов страдает от нарушений сердечной деятельности и до 10% – от изменений в органах пищеварения (характерна гипертрофия пищевода или толстой кишки), нервной системе или целом ряде органов. В последующие годы инфекция может приводить к внезапной смерти или сердечной недостаточности, вызываемой прогрессивным разрушением сердечной мышцы.
Передача инфекции
В Латинской Америке паразиты T. Cruzi передаются, главным образом, через инфицированные фекалии кровососущих клопов-триатоминов. Как правило, эти клопы живут в трещинах плохо построенных домов в сельских или пригородных районах. В дневное время они прячутся, а по ночам становятся активными и питаются кровью людей. Обычно они кусают в открытые участки кожи, такие как лицо. Рядом с укусом клоп испражняется. Паразиты проникают в организм человека, когда он инстинктивно втирает фекалии клопа в место укуса, глаза, рот или какую-либо трещину кожи.
T. cruzi может также передаваться:
- через пищевые продукты, загрязненные T. cruzi, например, в результате контакта с фекалиями клопа-триатомина;
- при переливании крови, полученной у инфицированных доноров;
- от инфицированной матери новорожденному ребенку во время беременности или родов;
- при трансплантации органов, взятых у инфицированных доноров;
- во время лабораторных инцидентов.
Лечение
Для того чтобы убить паразита, болезнь Шагаса необходимо лечить бензнидазолом, а также нифуртимоксом. Эффективность лечения обоими препаратами составляет почти 100% в случае, если лечение начато вскоре после инфицирования при наступлении острой стадии. Однако чем более длительное время человек инфицирован, тем менее эффективными становятся эти препараты. Лечение назначается людям с реактивированной инфекцией (например, в результате подавления иммунитета), детям грудного возраста с врожденной инфекцией и пациентам в начальной хронической стадии. Инфицированным взрослым людям, особенно тем, у кого нет симптомов заболевания, также необходимо предлагать лечение. Необходимо применять взвешенный подход, оценивая потенциальные преимущества медикаментозного лечения для предотвращения или отсрочивания развития болезни Шагаса, с одной стороны, и длительность лечения (до 2 месяцев) и возможные побочные реакции (наблюдаемые у 40% пациентов, получающих лечение), с другой стороны.
Бензнидазол и нифуртимокс не должны принимать беременные женщины и люди с почечной или печеночной недостаточностью. Нифуртимокс также противопоказан людям с неврологическими или психиатрическими расстройствами.
Кроме того, может требоваться специальное лечение нарушений сердечной деятельности и пищеварения.
Борьба и профилактика
Вакцины против болезни Шагаса нет. Самым эффективным способом профилактики болезни Шагаса в Латинской Америке является борьба с переносчиками заболевания. Для предотвращения инфицирования в результате переливания крови или пересадки органов необходима проверка крови.
Изначально (более 9000 лет назад) T. cruzi поражал только диких животных. Большой резервуар паразитов T. cruzi среди диких животных Америки означает, что ликвидировать этого паразита нельзя. Вместо этого, целями борьбы являются ликвидация передачи инфекции и обеспечение доступа инфицированных и больных людей к медицинской помощи.
T. cruzi может инфицировать несколько видов клопов-триатоминов, большинство из которых распространено в Америке. В зависимости от географической области ВОЗ рекомендует следующие подходы в области профилактики и борьбы:
- распыление инсектицидов в домах и окружающих районах;
- улучшение домов для предотвращения их заражения переносчиками болезни;
- принятие индивидуальных профилактических мер, таких как использование прикроватных сеток;
- соблюдение надлежащей гигиены при приготовлении транспортировке, хранении и потреблении пищи;
- скрининг доноров крови;
- тестирование доноров и реципиентов органов, тканей и клеток;
- скрининг новорожденных и детей других возрастных групп, рожденных инфицированными матерями, для обеспечения диагностирования и лечения на ранних стадиях.
Деятельность ВОЗ
С 1990-х гг. достигнуты значительные успехи в борьбе с паразитами и переносчиками болезни в Латинской Америке, а именно на территории Южного конуса, Центральной Америки, стран Андского пакта и стран Амазонских межправительственных инициатив с участием Секретариата Панамериканской организации здравоохранения – Технического секретаря ПАОЗ. Эти многонациональные инициативы привели к значительному уменьшению масштабов передачи инфекции домашними переносчиками. Кроме того, во всей Латинской Америке был существенно снижен риск передачи инфекции при переливании крови. Эти достижения стали возможными благодаря твердой приверженности эндемичных государств-членов и их надежным организациям в области научных исследований и борьбы с переносчиками инфекции при поддержке со стороны многих международных партнеров.
В то же время необходимо решать ряд дополнительных проблем, таких как:
- устойчивость, поддержание и укрепление успехов, достигнутых в борьбе с заболеванием;
- возникновение болезни Шагаса в районах, считавшихся ранее свободными от этой болезни, таких как бассейн Амазонки;
- повторное возникновение болезни в районах, где проводилась борьба с переносчиками, таких как район Чако в Аргентине и Боливии;
- распространение болезни, главным образом, в результате возрастающих масштабов передвижения населения между Латинской Америкой и остальным миром;
- обеспечение доступа миллионов инфицированных людей к диагностике и лечению.
Для достижения цели по ликвидации передачи болезни Шагаса и обеспечению медицинской помощи для инфицированных / больных пациентов как в эндемичных, так и в неэндемичных странах ВОЗ стремится расширить создание сетей на глобальном уровне и усилить региональный и национальный потенциал, уделяя основное внимание таким мерам, как:
- усиление систем эпиднадзора и информационных систем в мире;
- предотвращение передачи инфекции при переливании крови и пересадке органов в эндемичных и неэндемичных странах;
- содействие разработке диагностических тестов для скрининга и диагностирования инфекции;
- расширение вторичной профилактики передачи врожденной инфекции и ведения случаев врожденной и неврожденной инфекции;
- содействие достижению консенсуса в отношении надлежащего ведения случаев заболевания.
1 Аргентина, Белиз, Боливия (Многонациональное Государство), Бразилия, Венесуэла (Боливарианская Республика), Гайана, Гватемала, Гондурас, Колумбия, Коста-Рика, Мексика, Никарагуа, Панама, Парагвай, Перу, Сальвадор, Суринам, Уругвай, Французская Гайана, Чили и Эквадор.
Болезнь Шагаса, известная также как американский трипаносомоз, — потенциально опасное для жизни заболевание, вызываемое простейшим паразитом Trypanosoma cruzi.
Болезнь Шагаса названа именем бразильского врача и ученого Карлуса Рибейру Жустиниану Шагаса, который открыл эту болезнь в 1909 г. В мае 2019 г. по решению семьдесят второй сессии Всемирной ассамблеи здравоохранения был учрежден Всемирный день борьбы с болезнью Шагаса, отмечаемый 14 апреля (в этот день в 1909 г. Карлус Шагас диагностировал первый случай этой болезни у человека — двухлетней девочки по имени Беренис.
Распространение
Ранее распространение болезни Шагаса ограничивалось исключительно сельскими районами континентальной части Региона стран Америки — преимущественно Латинской Америки (за исключением островов Карибского бассейна). Однако в настоящее время, главным образом в результате роста мобильности населения за последние десятилетия, большинство лиц с данной инвазией проживают в городских районах (урбанизация заболевания), в результате чего она все чаще встречается в Соединенных Штатах Америки, Канаде, многих европейских странах, а также в некоторых странах Африки, Восточного Средиземноморья и Западной части Тихого океана.
Передача заболевания
T. cruzi может также передаваться:
- при потреблении пищевых продуктов, загрязненных T. cruzi, например в результате их соприкосновения с продуктами жизнедеятельности триатомовых клопов или сумчатых (такая передача, как правило, вызывает вспышки с одновременным заражением целых групп людей и более высокой заболеваемостью и смертностью);
- от инфицированной матери новорожденному ребенку во время беременности или родов;
- при переливании крови или препаратов крови, полученных у инфицированных доноров;
- при трансплантации некоторых органов, взятых у инфицированных доноров;
- в случае лабораторных инцидентов.
Признаки и симптомы
Болезнь Шагаса протекает в двух стадиях. Первая — острая — стадия длится около двух месяцев после заражения. В острой стадии в крови циркулирует большое количество паразитов, однако в большинстве случаев симптомы болезни отсутствуют или протекают в легкой форме и являются неспецифическими. Менее чем у 50% людей, укушенных триатомовым клопом, характерными первыми видимыми признаками могут быть поражения кожи или багровый отек век на одном глазу. Кроме того, они могут включать лихорадку, головную боль, увеличение лимфатических узлов, бледность, мышечную боль, затрудненное дыхание, отеки и боль в области живота и груди.
На протяжении второй стадии паразиты концентрируются в основном в сердце или мускулатуре пищеварительного тракта. Спустя одно–три десятилетия до 30% пациентов начинают страдать нарушениями сердечной деятельности, а до 10% пациентов — желудочно-кишечными (обычно в виде гипертрофии пищевода или толстой кишки), неврологическими или комбинированными расстройствами. В последующие годы у таких пациентов инвазия может приводить к поражению сердечной мышцы и нервной системы с последующей сердечной аритмией или прогрессирующей сердечной недостаточностью и внезапной смертью.
Лечение
Болезнь Шагаса можно лечить бензнидазолом, а также нифуртимоксом, что позволяет уничтожить паразита. Если лечение обоими препаратами начато вскоре после инфицирования в начале острой стадии, его эффективность составляет почти 100%, в том числе в случаях врожденной инвазии. Однако, чем дольше сохраняется инвазия, тем менее эффективными становятся эти препараты, а в более пожилом возрасте чаще развиваются побочные реакции. Лечение показано также пациентам с реактивированной инфекцией (например, в результате подавления иммунитета) и пациентам в начальной хронической стадии, в том числе девочкам и женщинам детородного возраста (до или после беременности) для профилактики врожденной передачи инвазии.
Лечение следует предлагать взрослым пациентам с инвазией, особенно при отсутствии симптомов, поскольку лечение противопаразитарными препаратами может также предотвращать или сдерживать прогрессирование заболевания. В остальных случаях следует сбалансированно учитывать потенциальные преимущества лекарственного лечения для предотвращения или задержки развития болезни Шагаса и длительность лучения (до двух месяцев), а также возможные побочные реакции (которыми страдают до 40% взрослых пациентов, получающих лечение). Бензнидазол и нифуртимокс не должны принимать беременные женщины или пациенты с почечной или печеночной недостаточностью. Нифуртимокс также противопоказан людям с неврологическими или психиатрическими расстройствами. Дополнительно пациенту может потребоваться специфическое лечение нарушений сердечной деятельности, желудочно-кишечных или неврологических расстройств.
Борьба и профилактика
Изначально (более 9 000 лет назад) T. сruzi поражал только диких животных. Позднее эта инвазия распространилась на домашних животных и людей. Ликвидировать ее не представляется возможным в связи с наличием большого резервуара паразитов T. cruzi среди диких животных в странах Америки. Таким образом, целями борьбы являются элиминация передачи заболевания и своевременное оказание медицинской помощи лицам с инвазией.
Против болезни Шагаса не существует профилактической вакцины. T. cruzi может инфицировать несколько видов триатомовых клопов, большинство из которых встречаются в странах Америки. Самым эффективным способом профилактики болезни Шагаса в Латинской Америке является борьба с переносчиками. Во всех странах для предотвращения инвазий в результате переливания крови или пересадки органов, а также для более эффективной диагностики и оказания помощи затронутым группам населения необходимо проводить скрининг крови.
В зависимости от географического района ВОЗ рекомендует следующие методы профилактики заболевания и борьбы с ним:
- опрыскивание жилых помещений и придомовой территории инсектицидами остаточного действия;
- ремонт домов и поддержание чистоты в быту для предотвращения инфестации переносчиками болезни;
- принятие индивидуальных профилактических мер, таких как использование прикроватных сеток, соблюдение надлежащих мер гигиены при приготовлении, транспортировке, хранении и употреблении пищи;
- организация информационных, просветительских и разъяснительных мероприятий по вопросам принятия профилактических мер и методов эпиднадзора с учетом потребностей различных субъектов и различных сценариев;
- скрининг доноров крови;
- тестирование доноров и реципиентов органов, тканей и клеток;
- обеспечение доступа к диагностике и лечению лиц, которым по медицинским основаниям показано или рекомендовано проведение противопаразитарного лечения, особенно детей и женщин детородного возраста до наступления беременности; и
- скрининг новорожденных и детей более старшего возраста, рожденных инфицированными матерями, которые не получали противопаразитарного лечения, для обеспечения своевременной диагностики и лечения.
Согласно расчетам, расходы на оказание медицинской помощи пациентам с сердечной, желудочно-кишечной, неврологической или комбинированной формой заболевания более чем на 80% превышают стоимость мероприятий по опрыскиванию инсектицидами остаточного действия для борьбы с переносчиками и профилактики инфицирования.
Деятельность ВОЗ
С 1990-х гг. в рамках сотрудничества с Секретариатом Панамериканской организации здравоохранения достигнуты значительные успехи в борьбе с паразитами и переносчиками болезни в Латинской Америке, а именно на территории Южного конуса, Центральной Америки, стран Андского пакта и стран Амазонских межправительственных инициатив. Эти международные инициативы позволили существенно уменьшить масштабы передачи инвазии и повысить доступность средств диагностики и противопаразитарного лечения.
Кроме того, в континентальных странах Латинской Америки благодаря обеспечению всеобщего скрининга всеми банками крови существенно снижен риск передачи инвазии при переливании крови. Всеобщий скрининг крови введен также в банках крови Соединенных Штатов Америки и большинства стран Европы и Западной части Тихого океана, где регистрируются случаи заболевания.
Эти достижения стали возможны благодаря решительным усилиям государств-членов, затронутых болезнью, а также благодаря наращиванию потенциала их организаций в области научных исследований и борьбы с этой болезнью при поддержке со стороны многих международных партнеров.
В 2005 г. Всемирная организация здравоохранения включила болезнь Шагаса в число забытых тропических болезней. Это способствовало более широкому признанию заболевания как проблемы общественного здравоохранения на международной арене и позволило противодействовать дезинформации, укреплять социальный запрос и политический курс на решение проблем, связанных с болезнью Шагаса, и устранять пробелы в научных исследованиях и разработках в области ее профилактики, выявления и комплексного оказания помощи, в том числе для выработки средств диагностики и лечения, информирования о лекарственных препаратах, методов решения социальных вопросов, информационных, просветительских и коммуникационных инструментов.
В принятой в 2020 г. дорожной карте по забытым тропическим болезням на 2021–2030 гг. предусматривается пять целей в области борьбы с болезнью Шагаса:
- верификация ликвидации передачи болезни переносчиками в жилых помещениях;
- верификация ликвидации гемотрансфузионной передачи болезни;
- верификация ликвидации передачи болезни при пересадке органов;
- элиминация врожденной болезни Шагаса;
- повышение уровня охвата противопаразитарным лечением целевых категорий населения до 75%.
В то же время будет необходимо решить ряд дополнительных проблем. К ним относятся:
- трудности в сохранении и закреплении успехов, достигнутых в области профилактики и контроля инфекции, особенно в контексте санитарно-эпидемиологических и социально-экономических последствий пандемии COVID-19;
- появление болезни Шагаса в районах, ранее считавшихся свободными от нее, например в бассейне Амазонки;
- продолжение циркуляции болезни в регионах, где принимаются меры по контролю инфекции, например в регионе Чако в Аргентине или на территории Многонационального Государства Боливия;
- распространение болезни, преимущественно обусловленное растущим перемещением населения между Латинской Америкой и остальным миром;
- наличие контингента лиц с инвазией, проживающих в странах/районах, где учреждения здравоохранения имеют мало информации и опыта в отношении этой болезни;
- предупреждение последствий низкой осведомленности или нехватки знаний, стигматизация и/или дискриминация в связи с болезнью Шагаса;
- низкий уровень регистрации случаев болезни, слабый мониторинг и эпиднадзор и низкий уровень верификации успехов, достигнутых в области борьбы с заболеванием; и
- недостаточная доступность услуг по диагностике и лечению для миллионов лиц с инвазией.
Для достижения цели по элиминации передачи болезни Шагаса и предоставлению медицинской помощи инфицированным и больным людям как в эндемичных, так и в неэндемичных районах ВОЗ намерена расширять сетевое взаимодействие на глобальном уровне и усиливать региональный и национальный потенциал, уделяя основное внимание таким мерам, как:
1 Аргентина, Белиз, Боливия (Многонациональное Государство), Бразилия, Чили, Колумбия, Коста-Рика, Эквадор, Сальвадор, Французская Гайана, Гватемала, Гайана, Гондурас, Мексика, Никарагуа, Панама, Парагвай, Перу, Суринам, Уругвай и Венесуэла (Боливарианская Республика).
Африканский трипаносомоз человека, также известный как сонная болезнь, относится к трансмиссивным паразитарным заболеваниям. Его возбудителям являются паразитирующие простейшие, принадлежащие к роду трипаносом. Они передаются человеку при укусе мухи цеце (род Glossina), инфицированной от людей или животных, выступающих в роли хозяев этих патогенных для человека паразитов.
Муха цеце обитает только в Африке к югу от Сахары, и передавать болезнь могут лишь некоторые ее виды. По неизвестным на сегодняшний день причинам во многих районах ареала обитания мухи цеце случаи сонной болезни не отмечаются. Наиболее подвержены укусам мухи цеце и, следовательно, данной болезни жители эндемичных сельских районов, занимающиеся сельским хозяйством, рыболовством, животноводством и охотой. Случаи болезни могут отмечаться как на территории отдельных деревень, так и в целом регионе. В пределах отдельно взятого инфицированного района интенсивность распространения болезни может сильно варьироваться от одного сельского поселения к другому.
Формы африканского трипаносомоза человека
Африканский трипаносомоз человека имеет две формы в зависимости от вида возбудителя:
Существует еще одна форма трипаносомоза, которая встречается преимущественно в Латинской Америке. Она известна как американский трипаносомоз, или болезнь Шагаса. Возбудитель болезни Шагаса относится к другому подроду Trypanosoma, передается другими переносчиками и вызывает заболевание, клинические проявления которого отличаются от африканского трипаносомоза человека.
Трипаносомоз животных
Другие виды и подвиды паразитов рода Trypanosoma являются патогенными для животных и вызывают трипаносомоз у некоторых видов диких и домашних животных. Трипаносомоз крупного рогатого скота называют нагана. Трипаносомоз домашних животных, особенно крупного рогатого скота, серьезно подрывает экономическое развитие инфицированных сельских районов.
Животные могут быть носителями патогенных для человека паразитов, особенно T.b. rhodesiense, причем домашние и дикие животные являются важным резервуаром последнего. Животные могут быть также инфицированы T.b. gambiense и, вероятно, могут также выступать в качестве его резервуара, хотя и в меньшей степени. Тем не менее реальная роль животного резервуара в эпидемиологии гамбийской формы болезни до сих пор недостаточно изучена.
Крупные эпидемии
За последнее столетие в Африке произошло несколько эпидемий:
- эпидемия 1896-1906 гг., преимущественно затронувшая Уганду и бассейн реки Конго;
- эпидемия 1920 г., затронувшая ряд африканских стран; и
- последняя по времени эпидемия, начавшаяся в 1970 г. и продолжавшаяся до конца 1990-х гг.
В 1920 г. борьба с эпидемией велась силами передвижных бригад, которые выполняли скрининг миллионов людей, проживающих в районах высокого риска. К середине 1960-х гг. распространение болезни было взято под контроль, и на всем континенте регистрировалось менее 5 000 случаев заболевания. После такого успеха эпиднадзор был ослаблен, в связи с чем болезнь вернулась, и к 1970 г. в нескольких регионах ее вспышки разрослись до эпидемии. В 1990-е гг. и в начале XXI века благодаря усилиям ВОЗ, осуществлению национальных программ по борьбе с болезнью, двустороннему сотрудничеству и деятельности неправительственных организаций (НПО) тенденция к росту заболеваемости была остановлена.
Поскольку число новых случаев заболевания африканским трипаносомозом человека за период с 2000 по 2012 г. значительно сократилось в результате международных координированных усилий, в Дорожной карте ВОЗ по борьбе с забытыми тропическими болезнями была поставлена цель по его элиминации как проблемы общественного здравоохранения к 2020 г. и ликвидации передачи инфекции (сведение числа случаев к нулю) к 2030 г.
Бремя болезни
Сонная болезнь угрожает здоровью миллионов людей в 36 странах Африки к югу от Сахары. Многие из них проживают в отдаленных районах с ограниченным доступом к необходимой медицинской помощи, что затрудняет эпиднадзор и, следовательно, диагностику и лечение больных. Кроме того, важными факторами, способствующими передаче инфекции, являются перемещение населения, вооруженные конфликты и нищета.
Текущий ареал распространения заболевания
Показатели распространенности болезни варьируются между странами, а также между районами на территории отдельно взятой страны.
Механизм передачи и симптомы
Болезнь передается главным образом при укусе инфицированной мухи цеце, однако известны и другие механизмы передачи инфекции:
- передача инфекции от матери ребенку: трипаносомы могут проходить через плаценту и инфицировать плод;
- возможна механическая передача через других кровососущих насекомых, однако эпидемиологическая значимость этого пути передачи инфекции неизвестна;
- известны случаи случайного инфицирования персонала лабораторий в результате травмы зараженной иглой;
- есть сведения о передаче паразита половым путем.
На первой стадии инфекции трипаносомы размножаются в подкожных тканях, крови и лимфе. Эта стадия известна как гемолимфатическая фаза болезни, для которой характерны приступы лихорадки, головная боль, увеличение лимфоузлов, боль в суставах и зуд.
На второй стадии паразиты проходят гематоэнцефалический барьер и инфицируют центральную нервную систему. Эта стадия известна как неврологическая, или менингоэнцефалитическая. В целом на этой стадии появляются наиболее очевидные признаки и симптомы болезни: изменение поведения, спутанность сознания, сенсорные расстройства и нарушение координации движений. Важным клиническим признаком на этой стадии является нарушение цикла сна, которое и дало название этой болезни. Без лечения сонная болезнь считается смертельной, хотя известны случаи здорового носительства инфекции.
Ведение болезни: постановка диагноза
Ведение болезни осуществляется в три этапа:
- Скрининг на предмет выявления вероятной инфекции. Он включает серологическое исследование (возможно только в отношении T.b. gambiense) и проверку на наличие клинических признаков, в частности увеличения шейных лимфатических узлов.
- Поиск паразита в биологических жидкостях.
- Определение стадии болезни. Для этого выполняется клиническое обследование пациента и в некоторых случаях исследование спинномозговой жидкости, полученной путем люмбальной пункции.
Во избежание необходимости применения сложных и тяжелых методов лечения диагностика должна выполняться как можно раньше до развития неврологической стадии заболевания.
Ввиду длительного и бессимптомного течения первой стадии сонной болезни, вызванной T. b. gambiense, рекомендуется организация тщательного и активного скрининга групп риска с целью выявления пациентов на ранней стадии заболевания и ограничения дальнейшего распространения инфекции посредством их лечения, после которого они перестают выступать в качестве резервуара. Всесторонний скрининг населения требует серьезных финансовых вложений в кадровые и материальные ресурсы. В Африке, особенно в отдаленных районах с наибольшей распространенностью заболевания, этих ресурсов часто не хватает. В результате часть инфицированных умирает еще до постановки диагноза и получения лечения.
Лечение
Тип лечения зависит от формы и стадии заболевания. Раннее выявление болезни повышает шансы на успешное излечение. Ввиду того что паразит может сохранять жизнеспособность в течение длительного времени и вызывать рецидивы через много месяцев после окончания терапии, для оценки результатов лечения пациенты должны оставаться под наблюдением в течение периода продолжительностью до 24 месяцев, в рамках которого следует проводить клиническое обследование пациентов и выполнять лабораторные исследования физиологических жидкостей, в том числе в некоторых случаях спинномозговой жидкости, полученной путем люмбальной пункции.
Для успешного лечения болезни на второй стадии необходимо применение лекарственных препаратов, способных преодолевать гематоэнцефалический барьер и нейтрализовать паразита в центральной нервной системе.
Препараты для лечения болезни на первой стадии:
- Пентамидин: впервые получен в 1940 г., используется для лечения сонной болезни, вызванной T.b. gambiense, на первой стадии. Несмотря на наличие серьезных побочных эффектов, препарат в целом хорошо переносится.
- Сурамин: впервые получен в 1920 г., используется для лечения болезни, вызванной T.b. rhodesiense, на первой стадии. Препарат имеет ряд нежелательных побочных эффектов, включая нефротоксическое действие и аллергические реакции.
Препараты для лечения болезни на второй стадии:
Препараты для лечения заболевания на обеих стадиях:
Фексинидазол – пероральный препарат для лечения гамбийской формы африканского трипаносомоза человека. В 2019 г. препарат был включен в Перечень основных лекарственных средств ВОЗ и рекомендован в руководстве ВОЗ по лечению африканского трипаносомоза человека. Препарат показан в качестве терапии первой линии на первой и нетяжелой второй стадии заболевания. Он принимается в течение 10 дней через 30 минут после приема твердой пищи под наблюдением квалифицированного медицинского персонала. В настоящее время проводятся клинические испытания этого препарата для лечения родезийской формы трипаносомоза.
Частно-государственные партнерства
В 2000 и 2001 гг. ВОЗ учредила частно-государственное партнерство с компаниями Aventis Pharma (в настоящее время Sanofi) и Bayer HealthCare, в результате чего была создана программа по эпиднадзору и борьбе с данным заболеванием под руководством ВОЗ, в рамках которой эндемичным странам предоставляется поддержка в осуществлении противоэпидемических мероприятий и бесплатно поставляются лекарственные препараты.
Партнерство неоднократно продлевалось в 2006, 2011, 2016 и 2021 г. Успехи в сокращении числа случаев сонной болезни и появление реальной перспективы ее элиминации побудили ряд других партнеров из частного сектора поддержать инициативу ВОЗ по элиминации болезни как проблемы общественного здравоохранения и обеспечению ликвидации передачи инфекции к 2030 г.
Деятельность ВОЗ
ВОЗ оказывает содействие и техническую поддержку национальным программам по борьбе с сонной болезнью.
Для содействия разработке новых и недорогостоящих средств диагностики ВОЗ в 2009 г. создала банк образцов биоматериалов, которыми могут пользоваться исследователи. В банке, размещенном в Институте Пастера в Париже, хранятся образцы крови, сыворотки, спинномозговой жидкости, слюны и мочи, взятые у пациентов, инфицированных обеими формами болезни, а также образцы, взятые у неинфицированных людей из эндемичных районов.
В 2014 г. в целях активизации и поддержки усилий по элиминации болезни по инициативе ВОЗ была создана координационная сеть по африканскому трипаносомозу человека. В число партнеров этой сети вошли национальные программы по борьбе с сонной болезнью, организации, занимающиеся созданием новых лекарственных и диагностических средств, международные и неправительственные организации, а также организации-доноры.
Переносчики — это живые организмы, способные передавать патогенные микроорганизмы от человека к человеку или от животных людям. Многие из этих переносчиков являются кровососущими насекомыми, в организм которых попадают болезнетворные микроорганизмы во время питания кровью зараженного хозяина (человека или животного) и которые затем, после репликации патогена, переносят эти микроорганизмы новому хозяину. Зачастую после однократного попадания патогена в организм переносчик становится заразным на протяжении всего жизненного цикла и передает болезнетворные микроорганизмы при каждом укусе/во время каждого акта питания.
Трансмиссивные болезни
Трансмиссивные болезни — это заболевания человека, возбудителями которых являются паразиты, вирусы и бактерии, и передаваемые переносчиками. Ежегодно во всем мире более 700 000 человек заболевают такими болезнями как малярия, лихорадка денге, шистосомоз, африканский трипаносомоз человека, лейшманиоз, болезнь Шагаса, желтая лихорадка, японский энцефалит и онхоцеркоз.
В тропических и субтропических районах бремя этих болезней особенно велико, и от них особенно сильно страдает беднейшее население. С 2014 г. в ряде стран мира многие люди пострадали или погибли в связи с крупными вспышками денге, малярии, чикунгуньи, желтой лихорадки и болезни, вызванной вирусом Зика, а системы здравоохранения испытали колоссальную нагрузку. Другие заболевания, такие как чикунгунья, лейшманиоз и лимфатический филяриоз, оставляют после себя стойкие последствия, обрекают людей на страдания на протяжении всей жизни, приводят к инвалидности и, порой, к стигматизации.
Перечень трансмиссивных болезней, в разбивке по переносчику
Ниже представлен неполный перечень трансмиссивных болезней, который упорядочен по переносчику. Кроме того, в перечне указан тип патогенного микроорганизма, вызывающего болезнь у человека.
Переносчик
Вызываемое заболевание
Тип патогенного микроорганизма
Комары
Лихорадка долины Рифт
Лихорадка Западного Нила
Водные брюхоногие моллюски
Мошки
Онхоцеркоз (речная слепота)
Блохи
Чума (передается от крыс людям)
Вши
Эпидемический возвратный тиф, переносимый вшами
Москиты
Москитная лихорадка (флеботомная лихорадка)
Клещи
Геморрагическая лихорадка Крым-Конго
Возвратный тиф (вызывается боррелиями)
Риккетсиальные заболевания (сыпной тиф и квинслендская лихорадка)
Триатомовые клопы
Болезнь Шагаса (американский трипаносомоз)
Мухи це-це
Сонная болезнь (африканский трипаносомоз)
Деятельность ВОЗ
Секретариат ВОЗ предоставляет стратегические, нормативные и технические рекомендации странам и партнерам по развитию, касающиеся усиления борьбы с переносчиками болезней как фундаментальной, основанной на ГМПБИ стратегии профилактики болезней и реагирования на вспышки. В частности, в связи с проблемой трансмиссивных болезней ВОЗ принимает следующие меры:
- предоставление основанных на доказательных данных рекомендаций по борьбе с переносчиками и защите людей от заражения;
- оказание технической поддержки странам с целью обеспечить возможность эффективного ведения случаев заболеваний и реагирования на вспышки;
- оказание странам поддержки в совершенствовании системы регистрации случаев и определении точных характеристик бремени болезни;
- помощь в проведении профессиональной подготовки (укрепление потенциала) по вопросам клинического ведения пациентов, диагностики и борьбы с переносчиками совместно с некоторыми сотрудничающими центрами; и
- содействие в разработке и оценке новых методов, технологий и подходов, касающихся трансмиссивных заболеваний, включая технологии и средства борьбы с переносчиками и ведения трансмиссивных заболеваний.
Первоочередное значение в деле снижения бремени трансмиссивных болезней имеют поведенческие изменения. ВОЗ сотрудничает с партнерскими организациями по линии просветительской работы и повышения информированности населения в отношении мер индивидуальной и коллективной защиты от комаров, клещей, клопов, мух и других переносчиков инфекций.
Важнейшим фактором в борьбе с болезнями и их ликвидацией является доступ к воде и средствам санитарии. ВОЗ проводит совместную работу со многими государственными секторами, направленную на совершенствование систем аккумулирования воды и водоотведения, тем самым содействуя осуществлению контроля за заболеваниями на уровне общин.
Болезнь Шагаса – трансмиссивная протозойная инфекция, возбудителем которой является патогенная Trypanosoma cruzi, а переносчиком триатомовые клопы. Острая форма болезни Шагаса проявляется лихорадкой, головной и мышечной болью, отеками, сыпью, лимфаденитом, гепатоспленомегалией, кардиомегалией и миокардитом, менингоэнцефалитом; хроническая - сердечной недостаточностью, мегаэзофагусом, мегаколоном. Диагноз болезни Шагаса основан на данных анамнеза, клинической картины, микроскопического, культурального и серологического исследований. В лечении болезни Шагаса применяются антипаразитарные препараты, симптоматические средства, при осложнениях - оперативное вмешательство.
МКБ-10
Общие сведения
Болезнь Шагаса (американский трипаносомоз) – протозооз, вызываемый внутриклеточным простейшим паразитом рода Трипаносома (T. cruzi), приводящий к воспалительно-дегенеративным изменениям со стороны сердца, нервной системы, ЖКТ. Болезнь Шагаса относится к природно-очаговым заболеваниям, широко распространена практически во всех странах Американского континента: эндемичными по трипаносомозу районами являются Центральная и Южная Америка. В сельской местности большинство населения заражается трипаносомозом еще в детском возрасте, часто инвазия протекает бессимптомно. Среди зараженных болезнью Шагаса преобладают лица мужского пола.

Причины болезни Шагаса
Возбудителем болезни Шагаса является жгутиковое простейшее Trypanosoma cruzi, сложный цикл развития которого включает смену хозяев - позвоночных животных и человека, а специфическим переносчиком служат кровососущие клопы подсемейства Triatominae (триатомовые). T. cruzi имеет веретенообразную форму, жгутик и ундулирующую мембрану. Паразит проходит несколько фаз жизненного цикла: амастигота, обитающая в тканевых клетках человека; эпимастигота, растущая в кишечнике переносчиков; и трипомастигота, находящаяся в крови животных и человека. Основным хозяином T. cruzi служит человек, дополнительными - броненосцы, муравьеды, обезьяны и домашние животные (собаки, кошки, свиньи). Инвазионной стадией для переносчиков и хозяев являются трипомастиготные формы.
Заражение клопов происходит в процессе питания кровью человека или животных, содержащей трипомастиготы. В организм человека возбудитель болезни Шагаса заносится вместе с инфицированными фекалиями клопов при расчесывании ранок после их укусов на коже и слизистых губ, носа, конъюнктивы. Характерной особенностью T. cruzi является способность к внутриклеточному паразитизму в макрофагах кожи и слизистых оболочек, в клетках миокарда, эндотелия лимфатических узлов, селезенки, печени, легких, нейроглии. После разрыва пораженных клеток, переполненных размножившимися амастиготами, происходит заражение новых клеток. Паразитирование трипаносом приводит к воспалительно-дистрофическому и дегенеративному поражению внутренних органов. Наиболее распространенный способ заражения болезнью Шагаса – трансмиссивный, возможна передача алиментарным, половым, трансплацентарным, гемотрансфузионным путем и при трансплантации органов. Для T. cruzi характерна персистенция в организме хозяина в течение всей жизни.
Симптомы болезни Шагаса
Инкубационный период заболевания продолжается 1-3 недели. Затем в месте проникновения трипаносом может развиться местная воспалительная реакция (шагома) в виде эритематозного узла с припухлостью и покраснением либо одностороннего багрового отека века (симптом Роминьи) с конъюнктивитом, сопровождающиеся увеличением регионарных лимфоузлов. Болезнь Шагаса проходит в 2 стадии: острую (первые 2 месяца) с циркуляцией большого количества паразитов в крови и хроническую - с концентрацией трипаносом во внутренних органах.
В острую стадию болезни Шигаса в большинстве случаев симптомы отсутствуют, у части больных проявляются в легкой форме. У детей до 5 лет развивается наиболее тяжелая форма с системными проявлениями и летальностью до 10-14%. Среди общих симптомов болезни Шагаса может отмечаться недомогание, постоянная или ремитирующая лихорадка (до 39-40°С), головная и мышечная боль, отеки на ногах, одутловатость лица, мелкая макулезная сыпь. Характерен шейный, паховый и подмышечный лимфаденит, гепатоспленомегалия. Могут возникать вторичные шагомы – плотные узлы в подкожной клетчатке. Отмечается преимущественное поражение сердца, ЦНС и периферических ганглиев, органов ретикулоэндотелиальной системы. Развивается острое воспаление и расширение всех камер сердца (кардиомегалия), диффузный миокардит, нарушение сердечной деятельности. У некоторых больных (особенно, у детей раннего возраста) может возникнуть острый специфический менингоэнцефалит, кровоизлияние в мозговые оболочки. Врожденная болезнь Шагаса может приводить к спонтанному аборту или преждевременным родам; у новорожденных сопровождается тяжелой анемией, гепатоспленомегалией, желтухой, судорогами, нередко - летальным исходом.
При хронической форме болезни Шагаса симптомы могут долго отсутствовать, пока не произойдут необратимые повреждения внутренних органов. Чаще всего развивается кардиомиопатия, выражающаяся сердечной недостаточностью, аритмией, тромбоэмболией. Со стороны ЖКТ характерны патологическое расширение пищевода (мегаэзофагус), проявляющееся дисфагией, болью при глотании, и расширение толстой кишки (мегаколон), сопровождающееся кишечной непроходимостью, скоплением каловых камней. Возникают вегетативные нарушения и периферическая нейропатия. С течением времени болезнь Шагаса может приводить к внезапной смерти вследствие прогрессирующего разрушения сердечной мышцы.
Диагностика болезни Шагаса
Диагностика болезни Шагаса включает тщательный сбор анамнеза (с учетом места рождения больного, поездок в эндемичные по заболеванию районы), анализ данных клинической картины и лабораторных исследований (микроскопического и культурального методов, серологических анализов и ПЦР).
В качестве исследуемого материала используется кровь, спинномозговая жидкость, пунктаты из первичных мест поражения, лимфоузлов, селезенки, костного мозга. В острую стадию болезни Шагаса (первые 6-12 недель) паразитов можно обнаружить при микроскопии толстой капли крови или фиксированных окрашенных препаратов. Бактериологический посев крови больного помогает выявить чистую культуру T. cruzi. При болезни Шагаса применяется ксенодиагностика, включающая исследование содержимого кишечника неинвазированного триатомового клопа после насыщения его кровью больного. Возможно проведение биологической пробы с введением крови пациента морским свинкам или белым мышам и последующим изучением образцов тканей.
При хронической болезни Шагаса более эффективна серодиагностика: реакция связывания комплемента, реакция непрямой флюоресценции, реакция непрямой гемагглютинации, ИФА. Наличие специфических IgM говорит об острой стадии болезни Шагаса, при хронической имеются только IgG . Некоторые инфекции, например, малярия, сифилис, лейшманиоз могут давать ложноположительные результаты на трипаносомоз, поэтому рекомендуется применять не менее двух независимых методов серодиагностики. Необходима дифференциальная диагностика патогенных трипаносом от непатогенных видов, способных находится в организме человека, не вызывая развитие заболевания.
Лечение и прогноз болезни Шагаса
На сегодняшний день лечение болезни Шагаса малоэффективно; терапия позволяет снизить летальность среди больных, но не дает уверенности в полной эрадикации внутриклеточных форм T. cruzi. В лечении болезни Шагаса применяются два антипаразитарных препарата: нифуртимокс и бензнидазол, прием которых более эффективен в острую стадию заболевания. В хронической стадии инфекции лечение направлено на облегчение симптомов развившихся осложнений болезни Шагаса. При сердечной недостаточности и аритмии, для профилактики тромбоэмболических состояний назначаются ингибиторы АПФ, сердечные гликозиды, антиаритмические средства, антикоагулянты, в тяжелых случаях показаны аортокоронарное шунтирование, имплантация кардиостимулятора, трансплантация сердца. Лечение менингоэнцефалита – симптоматическое; при поражении ЖКТ могут использоваться кортикостероиды; при мегаколоне возможно хирургическое вмешательство: наложение колостомы, резекция толстой кишки.
Прогноз болезни Шагаса зависит от стадии заболевания, остроты развития и обратимости воспалительно-дегенеративных поражений внутренних органов, возраста больного. Пациенты с поздней стадией болезни Шагаса часто умирают от острой сердечной недостаточности, инфаркта, инсульта, дети раннего возраста - от стремительно развившегося острого менингоэнцефалита. Профилактика болезни Шагаса включает инсектицидную обработку жилья человека, птичников, свинарников – основных мест обитания клопов - переносчиков паразитов, благоустройство жилища; отбор и обследование на трипаносомоз потенциальных доноров крови и органов, санитарное просвещение населения.
Читайте также:

